CH3-C:::CH + HOH CH3- C(OH) = CH2 CH3-CO-CH3 propanoon e atsetoon Reageerimine vesinikhalogeniididega R-CH == CH2 + H+Cl- R-CHCl- CH3 CH3-CH = CH2 + HCl CH3-CH(Cl)-CH3 tekib 2-kloropropaan Redoksomadused Võrreldes küllastunud ühenditega on nad mõnevõrra rohkem oksüdeerunud, kuid siiski eeskätt redutseerijad. Nad põlevad C3H6 + 9/2O2 = 3CO2 + 3H2O. Etüüniga (atsetüleeniga ) keevitatakse- Ilma lisaõhuta on leek tahmav, sest vesinikusisaldus on väike C2H2 + 3/2O2 = 2CO2 + H2O Alkeene võib oksüdeerida aldehüüdideks ja hapeteks. Alküüne hapeteks Eteenist saab etanaali C2H4 + 1/2O2 = CH3CHO Hüdreerimine on ühtlasi redutseerimine, selles reaktsioonis on küllastumata ühendid oksüdeerijad C2H4 + H2 C2H6 Kuna küllastumata ühendid on kallimad, siis alkeene praktiliselt ei hüdreerita Pigem vastupidi, alkaanide dehüdreerimisel toodetakse alkeene. Proov kaaliumpermanganaadiga
Tunnuslõpp -aan -een -üün -ool -hape Üldvalem CnH2n +2 CnH2n CnH2n-2 R-OH R-COOH Side üksikside kaksikside kolmikside üksikside üksikside Põhiesindaja CH4 -metaan C2H2 -eteen C2H2 - etüün C2H2OH -etanool CH3COOH -metaanhape CH4 metaan - - CH3OH metanool HCOOH etaanhape C2H6 etaan C2H4 eteen C2H2 metüün C2H5OH - etanool CH3COOH
Alkoksiidioon on väga nõrga happe anioon. Alkohol on on hape. Alkoholaat on alkoholi sool. Metanool- Ch3Oh puupiiritus. Etanool C2H5OH piiritus. Puskari õli on destillatsioonijääk etanooli eraldamisel käärimissegust. See koosneb kahest pentanooli isomeerist. Etandiool HOCH2CH2OH-etüleenglükool- diool. Antifriis-mootori jahutussegu. Glütserool- HOCH2CHOHCH2OH-looduslik. Alkaanid- CH4-metaan C2H6-etaan C3h8-propaan Alkeenid- C2H4-eteen C3H6-propeen Alküünid- C2H2-etüün C3H4-propeen Alkoholid- ch3oh-metanool c2h5oh- etanool c3h7oh- propanool Karboksüülhapped- hcooh-metaanhape ch3cooh-etaanhape C2h5cooh-propaanhape Sahhariidid- c6h12o6-glükoos c6h12o6-fruktoos c12h22o11-sahharoos (c6h10o5)n-tärklis tselluloos Aineid, mille molekulis tetraeedrilise süsiniku aatomi juures asuv vesinik on asendatud hüdroksüülrühmaga oh, nimetatakse alkoholideks. Hüdroksüülrühma olemasolust alkoholi molekulis tuleneb asendiisomeeria. Alkoholi
1 1.GAASKEEVITUS JA GAASLÕIKAMINE Gaaskeevitus on keemilisel reaktsioonil põhinevate sulakeevitusprotsesside üldnimetus, kus energiaallikana kasuatakse hapniku ja põlevgaasi segu põlemise soojus. Rahvusvaheliselt nimetatakse neid keevitusprotsesse hapnik-põlevgaasikeevituseks, kus liidetavate detailide servad sulatatakse kokku kõrgtemperatuuril gaasileegiga, kasutades vajadusel lisametalli. Enamlevinud on hapnik-atsetüleenkeevitus, kus põlevgaasina kasutatakse atsetüleeni (C2H2). Põlevgaasina võib veel kasutada vesiniku, loodusliku gaasi, propaani või butaani. 1.1. Gaaskeevituse ja gaaslõikamise ajalugu. Esimesed gaaskeevituse ja lõikamise katsed olid juba 20 sajandi algusel. Gaaskeevituse ja lõikamise gaaside segude põlemise abil protsesside uurimisele alguse, andis Prantsuse teadlane Henri Louis Le Chatelier. 1895 aastal ta teatas Prantsuse Teaduste Akadeemiale, et ta sai suure temperatuuri leek (üle 3000o C), põletamisel atsetüleeni ja hapniku.
Keemia - Alküünid Alküünid on küllastumata süsivesinikud, mille üldvalemiks on CnH2n-2 ja kus süsinike vahel esineb kovalentne kolmikside. Kuna süsinike vaheline kaugus alküüni molekulis on väiksem kui alkeenis, on kolmikside võrreldes kaksiksidemega keemiliselt püsivam. Iseloomulikud on liitumisreaktsioonid, mis toimuvad kahes astmes. Tähtsaimaks ühendiks on etüün e. atsetüleen (C2H2; värvusetu, küüslaugu lõhna ja narkootilise toimega vees lahustuv gaas), mida saadakse laboratoorselt ja tööstuslikult kaltsiumkarbiidist vee toimel. Gaaskeevituses tuntud aine, kus atsetüleeni balloonides on see gaas rõhu all lahustatud orgaanilises vedelikus, millega on immutatud balloonis sisalduv poorne materjal. Etüüni segu hapnikuga on väga plahvatusohtlik ning võib olla purustava jõuga. Põleb tugeva tahmava leegiga
t. reageerib vesinikuga C2H4 + H2 = C2H6 4) oksüdeerub 5) polümeerub · Saamine 1) nafta krakkimisel 2) kivisöe gaasistamisel 3) põlevkivi kuumutamisel · Kasutamine: eteeni kasutatakse piirituse sünteetilise kautsuki, mootorikütuse, plastmasside, lahustite, mürkkemikaalide ja külmakindlate vedelike tootmisel. Alküünid · Alküünid on küllastumata · Homoloogiline rida süsivesinikud, mille 1) - molekulis esineb süsiniku 2) C2H2 - etüün aatomite vahel lisaks 3) C3H4 - propüün üksiksidemetele ka üks kovalentne kolmikside. 4) C4H6 - butüün · Üldvalem CnH2n-2 5) C5H8 - pentüün · Nimetuse lõpp -üün 6) C6H10 - heksüün 7) C7H12 - heptüün 8) C8H14 - oktüün 9) C9H16 - nonüün 10) C10H18 - deküün Etüün
Atsetüleen Atsetüleen on alküün, mis koosneb kahest vesiniku aatomist ja kahest süsiniku aatomist kolmiksidemega seotuna. Kolmiksideme tõttu kuulub see küllastumata süsivesinike hulka. Atsetüleen on alküünide tähtsaim esindaja. Keemiline nimetus: atsetüleen; süstemaatiline nimetus: etüün Keemiline valem: C2H2 Molaarmass: 26,0373 g/mol Keemistemperatuur: -80,8 °C; sulamistemperatuur: -84 °C. Lahustub vees. Etüün on värvitu, omapärase lõhnaga ning narkootilise toimega gaas. Selle tihedus on 1,09670 kg/m3. Kolmiksideme olemasolu tõttu on etüünile eriti iseloomulikud liitumisreaktsioonid. Ajalugu Atsetüleeni avastas 1836. aastal Edmund Davy. Uuesti avastati see 1860. aastal prantsuse
SÜSIVESINIKUD.- sisaldavad ainult H ja C aatomeid. Küllastunud süsivesinikud. C vahel on ainult üksiksidemed Alkaanid. Üldvalem: CnH2n+2 Metaan CH4 Vees mittelahustuvad gaasid. Etaan C2H6 Lõhnata, maitseta. Kas. Küttegaasina jm. Propaan C3H8 Butaan C4H10 C5 C15 Vees mittelahustuvad, veest kergemad, bensiini lõhnaga vedelikud. Nendest koosnebki bensiin ja petrooleum. Bensiin-hea lahusti. Alkaani nimetusel on lõpp- aan Alkaani nimetused on alusteks kõigi teiste ainete nimetuste moodustamisel. Süsivesinike täielikul põlemisel tekib CO2 ja H2O CH4+O2 - CO2+H2O SÜSIVESINIK + O2 CO2 +H2O Süsivesinikud reageerivad halogeenidega ja moodustavad ühendeid (üks või mitu vesinikku asendub halogeeniga) N: freoonid Küllastunud süsivesinikud C vahel on kaksiksidemed alkeenid CnH2n (lõpp - een) Eteen ehk etüleen....
4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptaan C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22 kaksikside alkeen 12. eteen C2H4 13. propeen C3H6 14. buteen C4H8 15. penteen C5H10 16. hekseen C6H12 17. hepteen C7H14 18. okteen C8H16 19. noneen C9H18 20. dekeen C10H20 kolmikside alküün 32. etüün C2H2 33. propüün C3H4 34. butüün C4H6 35. pentüün C5H8 36. heksüün C6H10 37. heptüün C7H12 38. oktüün C8H14 39. nonüün C9H16 40. deküün C10H18 oh - alkohol 21. metanool CH2OH 22. etanool C2H5OH 23. propanool C3H7OH 24. butanool C4H9OH 25. pentanool C5H11OH 26. heksanool C6H13OH 27. heptanool C7H15OH 28. oktanool C8H17OH 29. nonanool C9H19OH 30
Isopreen on madala keemistemperatuuriga (34,067 °C) värvitu vänge lõhnaga vedelik, mis polümeriseerub kergesti. Isopreeni keemiline valem on C5H8 ehk 2=(3) =2. Tööstuslikult saadakse isopreeni nafta termilise krakkimise produktidest. Etüün ehk atsetüleen Atsetüleen on lihtsaim alküün,mis koosneb kahest vesiniku aatomist ja kahest süsiniku aatomist kolmiksidemega seotuna. Keemiline valem on C2H2. Atsetüleeni kasutatakse keemilises sünteesis ja tööstuses, näiteks põlevgaasina metallide keevitamisel ja lõikamisel. Sulamistemperatuur on -84 °C. Keemistemperatuur on -80,8 °C. Propüün
Küllastumata süsivesinikud. II poolaasta tasemetöö kordamiseks Küllastumata süsivesinik- süsiniku aatomite vahel võib esineda kaksik- või kolmiksidet. Alkeen- süsiku aatomite vahel kaksiksidemed een, Eteen C2h4. Alküün- süsiniku aatomite vahel kolmiksidemed üün, Etüün C2H2. Hüdrogeenimine- vesiniku molekuli liitmine keemilise reaktsiooni käigus. Hüdraatimine- keemiline liitumisreaktsioon veega. Nitreerimine- nitrorühma (NO2) viimine orgaanilise ühendi koostisse. Benseeni füs omadused- värvusetu, veest kergem, iseloomuliku lõhnaga vedelik, vees ei lahustu, lahustub bensiinis ja etanoolis. Karbonüülühendid- sisaldavad karbonüülrühma ehk süsinikku, mis on kaksiksidemega seotud hapniku külge
Küllastumata ühendid on orgaanilised ained kus C aatomite vahel esineb kovalentne kaksikside või kolmikside. Pii side moodustub hübridiseerimata p orbitaalide kattumisel Alkeenid on küllastumata süsivesinikud mis sisaldavad kaksiksidet. (nomenklatuuris -een lõpp) Üldvalem CnH2n eteen Alkeenidel esineb isomeeria: 1) Kaksiksideme asukoha muutusest H3C H2C HC = CH2 -> H3C HC = CH - H3C 2) Süsivesinikahela lagunemisel H3C H2C HC = CH CH3 -> 3) Tsükliliste struktuuride ühendite tekkest Keemilised omadused eteeni näitel: C2H4 -> H2C = CH2 1) Põlemine C2H4 + 3O2 -> 2CO2 + 2H2O 2) Astuvad liitumisreaktsioon a) Br2 -> H2C = CH2 + Br2 -> CH2 BrCH2 Br b) HCl -> H2C = CH2 + HCl -> CH3CH2Cl c) H2O -> H2C ...
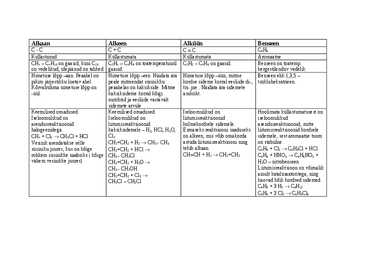
Alkaan Alkeen Alküün Benseen C-C C=C CC C6H6 Küllastunud Küllastumata Küllastumata Aromaatne CH4 C4H10 on gaasid, kuni C10 C2H4 C4H8 on toatemperatuuril C2H2 C4H6 on gaasid. Benseen on toatemp. on vedelikud, ülejäänud on tahked gaasid. kergestilenduv vedelik Nimetuse lõpp aan. Peaahel on Nimetuse lõpp een. Näidata ära Nimetuse lõpp üün, mitme Benseen ehk 1,3,5 pikim järjestikku loetav ahel. peale mitmendat süsinikku kordse sideme korral eesliide di-, tsükloheksatrieen. Kõrvalrühma nimetuse lõpp on peaahelas on kaksikside
10) Dekaan C10H22 Alkeenid Cn+H2n ; -een 2) Eteen C2H4 3) Propeen C3H6 CH2=CH-CH3 4) Buteen C4H8 CH3-CH=CH-CH3 5) Penteen C5H10 CH3-CH=CH-CH2-CH3 6) Hekseen C6H12 CH3-CH=CH-CH2-CH3 7) Hepteen C7H14 CH3-CH2-CH2-CH=CH-CH2-CH3 8) Okteen C8H16 CH3-CH2-CH2-CH=CH-CH2-CH2-CH3 9)Noneen C9H18 CH3-CH2-CH2-CH=CH-CH2-CH2-CH2-CH3 10) Dekeen C10H20 CH3-CH2-CH2-CH2-CH2-CH=CH-CH2-CH2-CH3 Alküün CnH2n-2 ; -üül ; 1 kolmikside. 2) Etüün C2H2 H-C(kolmikside)C-H 3) Propüün C3H4 H-C-C(KOLMIKSIDE)C-H 4) Butüün C4H6 5)Pentüül C5H8 6)Heksüün C6H10 7)Heptüün C7H12 8)Oktüün C8H14 9)Nonüün C9H16 10)Deküün C10H18
Milliseid süsivesinikke nim. küllastumata süsivesinikeks? Küllastumata süsivesinikeks nimetatakse orgaanilisi ühendeid, kus süsinike aatomite vahel on kordsed ehk kovalentsed kaksik- või kolmiksidemed. Nimeta eteeni ja etüüni füüsikalisi omadusi. Eteen! Molekulvalem: C2H4 lihtsaim alkeen värvusetu nõrk meeldiv lõhn narkootilise toimega gaas saadakse nafta töötlemisel Etüün Molekulvalem: C2H2 lihtsaim alküün ,värvusetu,meeldiva lõhnaga ,narkootiliste omadustega gaas toodetakse metaanist kõrgtemperatuurilise pürolüüsi teel Mis on hüdraatimine, nitreerimine, hüdrogeenimine? Hüdraatimine - on liitumisreaktsioon veega (H2O) Nitreerimine on nitrorühma (NO2) viimine orgaanilise ühendi koostisse temasse lämmastikoksiidide või nitreerimisseguga toimides. Hüdrogeenimine on vesiniku molekuli liitmine keemilise reaktsiooni käigus Nimeta benseeni füüsikalisi omadusi.
Alkaanid on küllastunud ühendid, alkeenid ja alküünid küllastumata ühendid. Süsinike arv Alkaani Alkeeni Alküüni ahelas nimetus nimetus nimetus CnH2n+2 CnH2n CnH2n-n 1 Metaan - - CH4 2 Etaan Eteen Etüün C2H6 C2H4 C2H2 3 Propaan Propeen Propüün C3H8 C3H6 C3H4 4 Butaan Buteen Butüün C4H10 C4H8 C4H6 5 Pentaan Penteen Pentüün C6H12 C5H10 C5H8 6 Heksaan Hekseen Heksüün
Söögisooda(NaHCO3+HCl) ja pesusooda (Na2CO3*10H2O) NaHCO3+HCl>NaCl+H2O+CO2 (uus sool+H2O+CO2 tekivad alati) Metaan CH4 (soogaas) Füüsikalised omadused: värvitu,lõhnatu,vees lahustumatu,õhust 2x kergem,toatemperatuuril gaas,keemistemp.-161kraadi , plahvatusohtlik, kergelt narkootilise toimega Keemilised omadused: *põleb CH4+2O2>CO2+2H2O täieliku põlemise saadused on süsiniku ja vesiniku ühenditel CO2 ja H2O *laguneb kuumutamisel CH4>C+2H2 (tahm) 2CH4>C2H2+3H2 Kasutamine: küttegaasina, lahustite tootmiseks (kloroform)
· Alkaan süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega. Mõnikord nimetatakse alkaane ka parafiinideks. (metaan, CH4) · Alkeen küllastumata süsivesinikud, mille molekulides on vähemalt üks kaksikside süsiniku aatomite vahel. Alkeene nimetatakse mõnikord ka olefiinideks. (eteen, C2H4) · Alküün küllastumata süsivesinikud, mille molekulides esineb kovalentne kolmikside. (etüün, C2H2) · Detergendid sünteetilised keemilised ühendid (pindaktiivsed ained), mida kasutatakse pesemis- ja puhastustoime parandajatena. Detergendi ja seebi erinevus seisneb selles, et detergendis puuduvad leeliselised aktiivsed ained. · Dihapped looduses üsna levinud. Lihtsaim neist etaandihape ehk oblikhape HOOCCOOH. On mürgine aine mida leidub spinatis, hapuoblikas, rabarbris mitte küll ohtlikes kogustes. · Esterdumine estrite tekkereaktsioon.
sulamis ja keemisto Vedelad alkaanid on head hüdrofoobsed lahustid, lahustavad ainult hüdrofoobseid aineid Vedelate ja gaasiliste alkaanide aurud on elusorganismidele ohtlikud ning narkootilise toimega Alkaanide keemilised omadused Põlevad CH4 + 2O2 CO2 + 2H2O Reageerimine halogeenidega (7A rühm, asendusreaktsioon) CH3CH3 + Cl2 CH3CH2Cl + HCl Etaan kloroetaan Termiline lagunemine CH4 1000.C C + 2H2 tahm CH4 1500.C C2H2 + 3H2 etüün Konversioon veeauruga 1:1 CH4 + H2O CO + 3H2 1:2 CH4 + 2H2O CO2 + 4H2 Oksüdeerumine alkoholiks 2CH3CH3 + O2 CH3CH2OH
süsivesinikest – üle 500. Peamised süsivesinikud – alkaanid, tsükloalkaanid, areenid, alkeenid ja tsükloalkeenid. Hapnikuhendid: alkohol, eetrid jt. Kütuse detonatsioon. Kütuse ülikiire plahvatuslik põlemine. Bensiinimargid. Bensiinimargid: 95, 98. Lisandid: varem lisati bensiinile oktaaniarvu tõstmiseks antidetonaatoreid, mis hoiavad kütesegu põlemiskiiruse parajates piirides. Tuntuim ja odavaim nendest on tetraetüülplii [Pb (C2H2)4]. R Bensiinilisandid. Lisandid: varem lisati bensiinile oktaaniarvu tõstmiseks antidetonaatoreid, mis hoiavad kütesegu põlemiskiiruse parajates piirides. Tuntuim ja odavaim nendest on tetraetüülplii [Pb (C2H2)4]. Raske värvitu vedelik. Vähesel hulgal lisatult tõstab see oktaani arvu, aga saastab keskkonda mürgiste pliiühenditega, mis kogunevad organismis ja kahjustavad meid ajaga. Teine võimalus oktaaniarvu tõstmiseks on
metanaali CH4 + O2 = HCHO + H2O , millest saab liime, plastmasse... Metaani pürolüüs Kuumutamisel laguneb metaani molekul radikaalideks ( radikaal = osake, millel on paardumata elektrone, väga reaktsioonivõimeline) Jahtumisel radikaalid rekombineeruvad.(taasühinevad) . . . . CH4 H3C + H ja hiljem 2H3C H3C CH3 2H H2 jne. Põhilised pürolüüsi saadused on: tahm ( C- kummitõõstusele) ; etüün e atsetüleen ( C2H2 kasutatakse keevitamiseks ja mitmete ainete sünteesimiseks) ja vesinik ( ammoniaagi sünteesiks) Metaani halogeenimine Vesiniku aatomeid saab asendada halogeenide aatomitega. Jood praktiliselt ei reageeri metaaniga ja fluori toimel ta kipub lihtsalt põlema ( CH4 + 2F2 C + 4HF) Seega jäävad kloor ja broom.Reaktsioon kulgeb ahelreaktsioonina. I etapp ahela teke . sellel etapil tekivad aktiivsed osakesed, antud juhul radikaalid .
Iseseisev töö Juhendaja Juhendaja Nimi Pärnu 2009 Gaasikeevitus kuulub sulakeevituse rühma. Võrreldes kaarkeevitusega on gaasikeevitusel väiksem keevituskiirus ja suurem kuumutuspiirkond. Gaasikeevitusel kasutatakse järgnevaid põlevgaase: atsetüleen, propaan, looduslik gaas, vesinik, bensiin ja petrooleumi aurud. Atsetüleen. (C2H2) Atsetüleen on põhiline põlevgaas mida kasutatakse gaasikeevituse ja lõikamise juures. Tema leegi temperatuur võib ulatuda kuni 3150 oC-ni. Atsetüleen on värvitu ja terava küüslaugu lõhnaga gaas. Ta on plahvatusohtlik 0,15 -0,20 MPa rõhu all plahvatab sädemest või leegist ning samuti kiirel kuumutamisel temperatuurini, mis ületab 200 oC. Kõige plahvatusohtlikumad on atsetüleeni ja õhu segud, mis sisaldavad 2,4 83% atsetüleeni.
mõõtmetele Maa omast oluliselt suurem. Raskusjõud Saturni pilvepiiril ületab Maa oma vaid 1,2 korda. Saturni läbimõõt on 120 536 km, see on Maa läbimõõdust 9,4 ja mahust 774 korda suurem. Samas on Saturn vaid 95 korda Maast raskem, sest koosneb peamiselt kergetest gaasidest: vesinik (87-90 mahu-%) ja heelium (10-13 mahu-%). Väiksemates kogustes esineb ka ammoniaaki (NH3), metaani (CH4), etaani (C2H6), vett (H2O), etüüni (C2H2) atsetüleen (C2H2) ja fosfiini(PH3). Jälgi on leitud ka keerulisematest ainetest. Keemiline koostis on Saturnil umbkaudu sama mis Jupiteril. Saturni siseelu Väga vähe on teada hiidplaneetide siseelu kohta. Tänu "Voyageritele" on olemas hea ülevaade gigantide kaaslastest ja rõngastest, kuid planeetidest saadi andmeid vaid pilvkatte ülemise piiri kohta. Aga sedagi on rohkem, kui sajandialguse astronoom unistada julges. Saturni fantastiliselt
C4H8 -- BUTEEN C5H10 --- PENTEEN C6H12 -- HEKSEEN C7H14 -- HEPTEEN C8H16 -- OKTEEN C9H18 -- NONEEN C10H20 -- DETSEEN 7. Mis on cis- isomeeria? Too näide ( 104 105 + konsp) Cis-isomeeria aatomiterühmad paiknevad ühel pool kaksiksidet cis-but-2- een 8. Mis on trans isomeeria? Too näide 104 105 +konsp) Trans-isomeeria aatomiterühmad paiknevad teine teisel pool kaksiksidet trans-but-2-een 9. ALKÜÜN ALKÜÜNI NIMETUS C2H2 -- ETÜÜN C3H4 -- PROPÜÜN C4H6 -- BUTÜÜN C5H8 -- PENTÜÜN C6H10 - HEKSÜÜN C7H12 -- HEPTÜÜN C8H14 -- OKTÜÜN C9H16 -- NONÜÜN C10H18 -- DETSÜÜN
R-CH == CH2 + H+Cl- à R-CHCl- CH3 CH3-CH = CH2 + HCl à CH3-CH(Cl)-CH3 tekib 2-kloropropaan 11. klassi Orgaanika konspekt Jaan Usin 13 Redoksomadused Võrreldes küllastunud ühenditega on nad mõnevõrra rohkem oksüdeerunud, kuid siiski eeskätt redutseerijad. Nad põlevad C3H6 + 9/2O2 = 3CO2 + 3H2O. Etüüniga (atsetüleeniga ) keevitatakse-Ilma lisaõhuta on leek tahmav, sest vesinikusisaldus on väike C2H2 + 3/2O2 = 2CO2 + H2O Alkeene võib oksüdeerida aldehüüdideks ja hapeteks. Alküüne hapeteks Näiteks eteenist saab etanaali C2H4 + 1/2O2 = CH3CHO Hüdrogeenimine on ühtlasi redutseerimine, selles reaktsioonis on küllastumata ühendid oksüdeerijad C2H4 + H2 à C2H6 Kuna küllastumata ühendid on kallimad, siis alkeene praktiliselt ei hüdrogeenita Pigem vastupidi, alkaanide dehüdrogeenimisel toodetakse alkeene. Proov kaaliumpermanganaadiga
1. Eteen ehk etüleen CH2 = CH2 Molekulvalem: C2H4 lihtsaim alkeen värvusetu nõrk meeldiv lõhn narkootilise toimega gaas saadakse nafta töötlemisel tööstuslikult kõige rohkem toodetav orgaaniline aine sellest valmistatakse polüeteeni ja etanooli Eteeni hüdrogeenimine: CH2 = CH2 + H2 > CH3 CH3 2. Etüün ehk atsetüleen CH = CH Molekulvalem: C2H2 lihtsaim alküün värvusetu meeldiva lõhnaga narkootiliste omadustega gaas toodetakse metaanist kõrgtemperatuurilise pürolüüsi teel keemiatööstuses on väga oluline lähteaine paljude saaduste valmistamisel hapnikuga segatuna tekib põlemisel väga kõrge temperatuuriga leek, mida kasutatakse gaaskeevituseks. Etüüni segu õhu või hapnikuga on väga plahvatusohtlik Selle avastas 1836
o Põlemine Täielik a. 2 C4H10 + 13 O2 8 CO2 + 10 H2O Mittetäielik a. 2 C4H10 + 9 O2 8 CO + 10 H2O o Pürolüüs alkaanide lagunemine või isomeerumine kõrgemal temperatuuril, mille tulemusena moodustuvad hargnenud ahelaga ühendid CH4 t0 C + H2 2CH4 t0 C2H2 + 3H2 o Asendusreaktsioonid halogeenidega Nn radikaalmehhanism Astmeliselt Saaduseks halogeenühend ja vesinikhalogeenid a. CH3CH3 + Cl2 CH2ClCH3 + HCl b. CH2ClCH3 + Cl2 CH2ClCH2Cl + HCl Halogeenühendid Orgaanilised ühendid, milles süsiniku aatom on seotud halogeeni aatomi või aatomitega Halogeenderivaat
aldehüüdid levinud, arvatavasti aldehüüdrühma suure keemilise aktiivsuse tõttu. Enamik suhkruid on siiski aldehüüdide derivaadid. Kuid glükoosi vesilahuses eksisteerib üksnes väike osa glükoosist aldehüüdi kujul. Lineaar Alkeeni sed alka Alküünid d anid nimetus valem nimetus valem nimetus Valem Metaan CH4 Etaan C2H6 Eteen C2H4 Etüün C2H2 Propaan C3H8 Propeen C3H6 Propüün C3H4 Butaan C4H10 Buteen C4H8 Butüün C4H6 Pentaan C5H12 Penteen C5H10 Pentüün C5H8 Heksaan C6H14 Hekseen C6H12 Heksüün C6H10 Heptaan C7H16 Hepteen C7H14 Heptüün C7H12 Oktaan C8H18 Okteen C8H16 Oktüün C8H14 Nonaan C9H20 Noneen C9H18 Nonüün C9H16 Dekaan C10H22 Dekeen C10H20 Deküün C10H18
6. Keevituspõleti 7. Keevitustraat 8. Gaasidüüs 9. Keevitatav metall 10. Leek 2. Atsetüleen ja teised põlevgaasid Atsetüleen on metallide gaaskeevitamisel ja lõikamisel põhiline põlevgaas. Tema leegi temperatuur ulatub tehniliselt puhtas hapnikus põlemisel 3150ºC-ni. Kasutusala: kõik gaasileektöötlemise liigid. Atsetüleen (C2H2) on süsiniku ja vesiniku keemiline ühend. Normaaltemperatuuril ja rõhul on tehniline atsetüleen värvitu, terava küüslaugulõhnaga gaas. Atsetüleeni kestev sissehingamine põhjustab iiveldust, peapööritust ning isegi mürgistust. Atsetüleeni plahvatamisel tõusevad rõhk ja temperatuur väga järsku, mis võib esile kutsuda suuri purustusi ning raskeid õnnetusi. Atsetüleeni segud vahekordades õhuga 2,3...84% ja hapnikuga 2,3...93% võivad
ALKÜÜNIDE HOMOLOOGILINE RIDA JA NIMETUSTE ANDMINE Küllastumata süsivesinike homoloogilised read algavad süsiniku aatomite arvust kaks, sest mitmikside saab tekkida ainult kahe süsiniku aatomi vahel. Teades alküünide homoloogilise rea üldvalemit, saame kirjutada selle alusel kõikide vastavate alküünide valemid. ALKÜÜN ALKÜÜNI NIMETUS C2H2 ETÜÜN C3H4 PROPÜÜN C4H6 BUTÜÜN C5H8 PENTÜÜN C6H10 HEKSÜÜN C7H12 HEPTÜÜN C8H14 OKTÜÜN C9H16 NONÜÜN
Kõrgtemperatuuril gaasileek (atsetüleen + hapnik) toimib samuti kaitsva kihina. Lisamaterjalide valik (elektrood, kaitsegaas, põlevgaas, lisametall) Gaaskeevitus on sulakeevitusviis, kus vajaminev kuumus metalli sulatamiseks saadakse põlevgaasi ja hapniku segust süüdatud leegist. Põlevgaasiks võib olla atsetüleen, propaan või butaan. Kõige laialdasemalt kasutatakse hapniku (O2) ja atsetüleeni (C2H2) segu, mis annab sulatustemperatuuriks kuni 3200°C. Enamikel juhtudel kasutatakse gaaskeevitusel lisametalli traadi kujul. Gaaskeevituse eeliseks on see, et see sobib peaaegu kõikide laiemalt kasutatavate metallide keevitamiseks. Negatiivse poolena võib välja tuua asjaolu, et gaaskeevitusel toimub väga suur soojuse ülekan- dumine keevitatavale detailile, mis omakorda tekitab ulatuslikke deformatsioone. Gaaskeevituse
(Vt joonis 4). Gaaskeevitus oli varemalt väga laialdaselt kasutatav keevitusviis, kuid seoses uute keevitustehnoloogiate kasutuselevõtuga on gaaskeevituse osatähtsus langenud. Gaaskeevitus on sulakeevitusviis, kus vajaminev kuumus metalli sulatamiseks saadakse põlevgaasi ja hapniku segust süüdatud leegist. Põlevgaasiks võib olla atsetüleen, propaan või butaan. Kõige laialdasemalt kasutatakse hapniku (O2) ja atsetüleeni (C2H2) segu, mis annab sulatustemperatuuriks kuni 3200°C. Enamikel juhtudel kasutatakse gaaskeevitusel lisametalli traadi kujul. Gaaskeevituse eeliseks on see, et see sobib peaaegu kõikide laiemalt kasutatavate metallide keevitamiseks. Negatiivse poolena võib välja tuua asjaolu, et gaaskeevitusel toimub väga suur soojuse ülekandumine keevitatavale detailile, mis omakorda tekitab ulatuslikke deformatsioone. Gaaskeevituse protsess on ka suhteliselt aeglane, võrreldes elekterkeevitustega.
sideme kordsus kahe aatomi vaheliste kovalentsete sidemete arv. Molekuli kuju - on määratud - sidemete suunaga molekulis. hübridisatsioon ühe ja sama aatomi eri tüüpi orbitaalide ühtlustumine -sidemete moodustamisel, molekulis moodustavad sidemeid hübriidsed (segatüüpi) orbitaalid. hübridisatsioon molekuli kuju näited sp BeCl2, CO2, C2H2 lineaarne sp2 BF3, C2H4, SO2, CO32- tasapinnaline kolmnurk 3 sp CH4, NH3, NH4+, SO42- tetraeeder delokaliseeritud (kovalentne) -side -side, mis ühendab enam kui kahte aatomit.
Kõik karbonaadid reageerivad hapetega, kusjuures eraldub CO2. Seda reaktsiooni kasutatakse karbonaatide määramiseks. Kuumutamisel karbonaadid(välja arvatud leelismetallide karbonaadid) lagunevad: CaCO3CaO+CO2 Karbiidid Need on metallide( ja mõningatre mittemetallide, näiteks räni) ühendid süsinikuga: 1) soolataolised karbiidid, milles aatomite vahel on iooniline side(caC2, Al4C3). Veega reageerimisel eraldub süsivesinik. CaC2+2H2OCa(OH)2+C2H2(etüün) Al4C3+12H2O4Al(OH3)3+3CH4 (metaan) 2) Kovalentsed sidemetega karbiidid(SiC, B4C) on suure kõvadusega, rasksulavad ja keemiliselt inertsed, 3) Intermetallilised karbiidid, kus süsiniku aatomid on metallide kristallstruktuuri tühimikes. Need on suure kõvades ja kõrge sulamisetemperatuuriga ained(HfC, W2C) Söe adsorptsioon Puidu söestamisel ja saadud puidusöest veeauru läbijuhtimisel tekkinud aktiivsöe omadust
sideme kordsus – kahe aatomi vaheliste kovalentsete sidemete arv. Molekuli kuju - on määratud σ- sidemete suunaga molekulis. hübridisatsioon – ühe ja sama aatomi eri tüüpi orbitaalide ühtlustumine σ-sidemete moodustamisel, molekulis moodustavad sidemeid hübriidsed (segatüüpi) orbitaalid. hübridisatsioon molekuli kuju näited sp BeCl2, CO2, C2H2 lineaarne sp2 BF3, C2H4, SO2, CO32- tasapinnaline kolmnurk 3 sp CH4, NH3, NH4+, SO42- tetraeeder delokaliseeritud (kovalentne) π-side – π-side, mis ühendab enam kui kahte aatomit.
Alkeenid ja alküünid Kaksiksidemega süsivesikuid nimetatakse alkeenideks ning kolmiksidemega süsivesikuid alküünideks. Kõige lihtsam alkaan on eteen ning kõige lihtsam etüün. C2H4 eteen C2H2 etüün Tähtsamad vinüülpolümeerid a) Polüetüleen (PE) Mis on polüetüleen? Polüetüleen on poolkristallilise struktuuriga kõige levinum plast, mida on erinevaid liike: HDPE, (PE-HD)- kõrgtihe polüetüleen, LLDPE, (PE-LLD)- lineaarne madaltihe polüetüleen ja LDPE, (PE-LD)- madaltihe polüetüleen. on madala hinna ja mitmekülgsete omadustega (sitke, tugev, veniv, keemiliselt inertne). See sulab vahemikus 100C-140C. Kus seda kasutakse
Referaadi viimane peatükk annab ülevaate ohutusnõuetest ning tähtsamate kaitsevahendite kasutamisest. 3 1. Gaaskeevitus Gaaskeevitus kuulub sulakeevituse rühma. See on lihtne protsess, mis ei nõua keerukaid seadmeid ega elektrienergiaallikat. Antud liitmistehnoloogia aktiveerimise energia allikaks on põlevgaasid. Kõige kõrgema põlemistemperatuuriga on atsetüleenileek (tavaliselt kasutatakse atsetüleeni-hapniku segusid - C2H2 + O2). Enamasti kasutatakse gaaskeevituse puhul lisametallina traati. Gaaskeevituse eeliseks on, et see sobib peaaegu kõikide laiemalt kasutatavate metallide keevitamiseks. Negatiivse poolena võib välja tuua asjaolu, et gaaskeevitusel toimub väga suur soojuse ülekandumine keevitatavale detailile, mis omakorda tekitab ulatuslikke deformatsioone. Gaaskeevitust rakendatakse soovituslikult kuni 6 mm paksusest lehtmetallist toodete valmistamisel ja parandamisel
kaarleegi poolt eralduvat soojusenergiat. Keevituskaare abil sulatatakse liidetavate detailide servad. Enamasti kasutatakse lisametalli sulava elektroodi näol. MIG Keevitus - Traatkeevitus inertgaasi keskkonnas MAG keevitus - Traatkeevitus aktiivgaasi keskkonnas TIG keevitus - Keevitus sulamatu elektroodiga inertgaasi keskkonnas Gaasikeevituse gaasid ja nende otstarve. Põlevgaasiks võib olla atsetüleen, propaan või butaan. Kõige laialdasemalt kasutatakse hapniku (O2) ja atsetüleeni (C2H2) segu, mis annab sulatustemperatuuriks kuni 3200°C. Hapnik on temperatuuri reguleermiseks. Varraselektrood - Keevituskaare, mille temperatuur on 5000…6000 °C, toimel elektroodivarras ja selle kate ning põhimetall sulavad. Tekib keevisvann, kuhu siirduvad elektroodimetalli tilgad ja katte sulamisel tekkinud räbu tilgad, mis moodustavad keevisvanni pinnal sularäbu kihi. Elektroodivarda ots sulab kattest kiiremini,
vedelas, kui ka tahkes olekus. Metaani keemistemperatuur on -161,4 C ja sulamistemperatuur -182,6 C. Saturni läbimõõt on 120 536 km, Maa läbimõõt on aga 12 756 km, seega on Saturni läbimõõt Maa omast umbes 10 ja maht 774 korda suurem. Samas on Saturn vaid 95 korda Maast raskem, sest koosneb peamiselt kergetest gaasidest: vesinik (87-90 mahu-%) ja heelium (10-13 mahu-%). Väiksemates kogustes esineb ka ammoniaaki (NH3), metaani (CH4), etaani (C2H6), vett (H2O), etüüni (C2H2) ja fosfiini(PH3). Jälgi on leitud ka keerulisematest ainetest. Kuna Saturn on võrreldes Maaga suhteliselt hõre, pole seal ka raskusjõud vaatamata planeedi hiiglaslikele mõõtmetele Maa omast oluliselt suurem. Saturni keskmine tihedus on ainult 0,7 vee tihedust (1g/cm3), see on Maa keskmisest kaheksa korda hõredam. Raskusjõud Saturnil ületab maise vaid 1,2 korda. Nagu teistelgi hiidplaneetidel, Jupiteril, Uraanil ja Neptuunil, ei ole
1. Hapnikuballoon 2. Atsetüleeniballoon 3. Kaitseklapp 4. Hapnikuvoolik 5. Atsetüleenivoolik 5 6. Keevituspõleti 7. Keevitustraat 8. Gaasidüüs 9. Keevitatav metall 10. Leek Keevitusgaasid Atsetüleen ja teised põlevgaasid Atsetüleen on metallide gaaskeevitamisel ja lõikamisel põhiline põlevgaas. Tema leegi temperatuur ulatub tehniliselt puhtas hapnikus põlemisel 3150ºC-ni. Kasutusala: kõik gaasileektöötlemise liigid. Atsetüleen (C2H2) on süsiniku ja vesiniku keemiline ühend. Normaaltemperatuuril ja rõhul on tehniline atsetüleen värvitu, terava küüslaugulõhnaga gaas. Atsetüleeni kestev sissehingamine põhjustab iiveldust, peapööritust ning isegi mürgistust. Atsetüleeni plahvatamisel tõusevad rõhk ja temperatuur väga järsku, mis võib esile kutsuda suuri purustusi ning raskeid õnnetusi. Atsetüleeni segud vahekordades õhuga 2,3...84% ja hapnikuga 2,3..
-> m=1 -> s= + 1/2 (8) -> m=1 -> s= - 1/2 (17) -> m=2 -> s= +1/2 (9) -> m=2 -> s= -1/2 (18) Kokku 18 elementi. 9. H2O Sp3, nurkjas 8 C2H6 Sp3, kaks tetraeedrit koos C2H4 Sp2, kaks kolmnurka koos C2H2 Sp, lineaarne CO Sp, lineaarne 9 CO2 Sp2, lineaarne NH3 Sp3, trigonaalne püramidaalne 10. Kovalentsed sidemed tekivad: a) Kui aatomite väliste elektronkihtide paardumata elektronid moodustavad molekulis ühised elektronpaarid.
: CH2=CH-CH=CH2 3) Liitumine halogeenidega C2H5OH→ CH2=CH2+H2O Elektrofiilne liitumine, tekivad halogeeniühendid 1,3- butadieen CaC2+H2O→Ca(OH)2+C2H2 CH2=CH2 + Cl2 → CH2Cl-CH2Cl (but-1,3-dieen) Eteeni kasut piirituse, sünteetilise 4) Liitumine vesinikhalogeenidega Elektrofiilne liitumine, tekivad halogeeniühendid
Koostas: Reppy 21.11.2012 5. Gaaskeevituse protsess Gaaskeevitamine on keemilisel reaktsioonil põhinevate sulakeevitusprotsesside üldnimetus, kus energiaallikana kasutatakse hapniku ja põlevgaasi segu põlemissoojust. Reeglina on sel juhul tegu käsikeevitusega. Enimlevinud on hapnik-atsetüleenkeevitus, kus põlevgaasina kasutatakse atsetüleeni (C2H2). Atsetüleenileegi temperatuur ulatub kuni 3100 °C. Veel kasutatakse vesinikku ja looduslikku gaasi, nende puhul on gaasileegi temperatuur märgatavalt madalam. Gaaskeevitamisel juhitakse hapnik ja põlevgaas balloonidest läbi gaasireduktorite ja keevitusvoolikute põletisse, kus nad segunevad ja tekitavad gaasileegi. Tänapäeval kasutatakse universaalseid keevitus-lõikepõleteid, millega on võimalik nii gaaskeevitada kui
Atsetüleen. Atsetüleen on metallide gaaskeevitamisel ja -lõikamisel põhiline põlevgaas. Teda saadakse kaltsiumkarbiidist, millel terav küüslaugulõhn ja ta imab väga hästi vett. Saadakse teda koksi ja kustutamata lubja sulatamisel elektriahjudes temperatuuril 1900...2300° C reaktsiooniga CaO+3C=CaC2 +CO. Uuesti veega reageerides saadakse temast atsetüleen ja kustutatud lubi sellise võrrandiga CaC2 +2H2O=C2H2 +CA(OH)2 . Ühest kilogrammist võib saada 235...285 dm 3-rit atsetüleeni. Kõrge energiasisalduse tõttu kasutatakse atsetüleeni põlevgaasina, kus leegi temperatuur ulatub põlemisel tehniliselt puhtas hapnikus kuni 3200° C-ni. Seega on atsetüleen süsiniku ja vesiniku keemiline ühend. Normaaltemperatuuril ja -rõhul on tehniline atsetüleen värvitu, terava küüslaugulõhnaga gaas. Lõhna põhjustavad gaasis sisalduvad
Saturn on hiiglaslik gaasikera. Tema atmosfäär koosneb peamiselt vesinikust, kuid sisaldab hulganisti ka teist kerget gaasi heeliumi. Seetõttu on Saturn oma suuruse kohta kerge, s.t väikese tihedusega, hõre. /1, lk 30/ 3 Keemiline koostis: levinuim element on vesinik (mahu järgi 87-90%), ülejäänud (10-13%) heelium, lisanditest ammoniaak (NH 3), metaan (CH4), etaan (C2H6), vesi, atsetüleen (C2H2) ja fosfiin (PH3). Lisandid moodustavad paksu ja mitmevärvilise pilvekihi. Pilvkate jaguneb vöönditeks. Vööndid kulgevad ekvaatoriga paralleelselt. /2, lk 250/ Esimeste teleskoopidega ei olnud võimalik Saturni rõngaid selgesti näha. Esimesena nägi neid Galileo Galilei 17. sajandi alguses. Algus paistis talle, et seal on reas kolm planeeti. Seejärel et Saturnil on kaks suurt kuud. /1, lk 31/ Saturni rõngad koosnevad sadadest väikestest rõngastest
.. Metaani pürolüüs Kuumutamisel laguneb metaani molekul radikaalideks ( radikaal = osake, millel on paardumata elektrone, väga reaktsioonivõimeline) Jahtumisel radikaalid rekombineeruvad.(taasühinevad) . . . . CH4 à H3C + H ja hiljem 2H3C à H3C CH3 2H à H2 jne. Põhilised pürolüüsi saadused on: tahm ( C- kummitõõstusele) ; etüün e atsetüleen ( C2H2 kasutatakse keevitamiseks ja mitmete ainete sünteesimiseks) ja vesinik ( ammoniaagi sünteesiks) Metaani halogeenimine Vesiniku aatomeid saab asendada halogeenide aatomitega. Jood praktiliselt ei reageeri metaaniga ja fluori toimel ta kipub lihtsalt põlema ( CH4 + 2F2 à C + 4HF) Seega jäävad kloor ja broom. 2 Reaktsioon kulgeb ahelreaktsioonina. I etapp ahela teke . sellel etapil tekivad aktiivsed osakesed, antud juhul radikaalid .
Mürgisus, toksilisus- suures koguses tekitab alkoholimürgituse ja valkude kalgenemist. 9. Vees lahustuvus, milles lahustub kui vees ei lahustu? lahustub igas vahekorras vee ja enamiku orgaaniliste lahustitega. 10. Olek toatemperatuuril Vedel 11. Värvus, elektrijuhtivus, tihedus Läbipaistev, ei juhi elektrit, 0.789 Mg/m3 12. Kasutamine Kõrist alla, lahustina, parfümeerias, värvitööstuses jne. 1. Nimetus(keemiline ja triviaalne)- etüün või atsetüleen 2. Summaarne valem C2H2 3. CAS nr - 74-86-2 4. Struktuurvalem (graafiline, klassikaline jne) - 5. Sulamistemp. -84 °C 6. Keemistemp. -80,8 °C 7. LD 50 1100 mg/kg 8. Mürgisus, toksilisus sissehingamisel võib põhjustada peapööritust või lämbumist. Nahale sattudes põletab 9. Vees lahustuvus, milles lahustub kui vees ei lahustu? 0.106 g/100 mL 10. Olek toatemperatuuril gaas 11. Värvus, elektrijuhtivus, tihedus värvitu, ei juhi elektrit, 1,09670 kg/m3 12
sidet. CnH2n Alkeenid Alküünid C aatomite vahel 1 kaksikside. C aatomite vahel 1 kolmikside. N=1 C=? Ei ole olemas C= ? ei ole olemas N=2 H C = C H H C =C H H H HC=CH CH2=CH2 CH=CH C2H4 eteen C2H2 etüün N=3 H H H-C=C-C H H-C=C-C H H H H H CH2=CH-CH3 CH=C-CH3 C3H6 propeen C3H4 propüün N=4 HH H H H-C=C-C-C H H-C=C-C-C H H H HH HH CH2=CH-CH2-CH3 C4H8
17 Kaltsiumkarbiidi pannakse plastpudelisse, millele valatakse vesi peale ja seejärel keerataksel kork hästi kõvasti peale. Pudel visatakse võimalikult kaugele ja vajaduse korral liigutakse ise veel pudelist kaugemale [13]. Katsevahenditeks on vesi mida saab näiteks kodust kraanist, plastpudel mida müüakse tavalistes poodides, aga kaltsiumkarbiid ei ole kätte saadav tavakodanikule. CaC2 + H2O Ca(OH)2 C2H2 [13] Kaltsiumkarbiid on vees hästi lahustuv aine. Kaltsium on ise väga aktiivne metall, mis tõrjub kahest vee molekulist ühe vesiniku aatomi välja ning tekib kaltsiumhüdroksiid [Ca(OH)2]. Vabad vesiniku aatomid reageerivad süsiniku aatomitega ning tekib gaasi etüleeni (C2H2). Kaltsiumhüdroksiid on lahusena söövitav, lahuse sattumisel nahale pesta koheselt rohke veega. Plahvatuse ohutuskaugus on vähemalt 15 meetrit. Nahale sattunud
Siinpool tooks näite, kuidas valmistatakse olmekeemia tooteid. Pürolüüs Pürolüüs on orgaaniliste ainete lagunemine kõrgel temperatuuril, mida rakendatakse nafta, maagaasi, kivisöe, põlevkivi ja puidu töötlemisel. Sõltuvalt temperatuurist võib metaanist saada kas väga puhast tahma ja vesinikku või siis etüüni ja vesinikku: tº tº CH4®C + 2H2 2CH4®C2H2 + 3H2 Puidu, turba, kivisöe ja põlevkivi kuivdestillatsiooni ehk kuumutamist ilma õhu juurdepääsuta nimetatakse utmiseks. Viimast vaadeldakse kui pürolüüsi erisaadust. Kõrvuti koksiga (söega), mida vajab metallurgia, tekib utmisel veel mitmeid gaasilisi ja vedelaid saadusi. Viimased leiavad rakendust nii keemiatööstuses kui ka olmekeemia toodete valmistamiseks. Atsetoon ehk propanoon ( CH3-CO-CH3 ) on väga hea lahusti. Atsetoon on üks põhiline