OKSIIDID JA NENDE SAAMINE. VESI JA LAHUSED Raudvara 8. klassile OKSIIDID Oksiidid on ained, mis koosnevad hapnikust oksüdatsiooniastmega II ja mõnest muust keemilisest elemendist. Metallioksiid Mittemetallioksiid Nimetuse andmisel kasutatakse metallilise Nimetuste andmisel kasutatakse eesliiteid: elemendi oksüdatsiooniastet. Kui elemendil on oksüdatsiooniaste kindel (IA, 2 di; 3 tri; 4 tetra; 5 penta; IIA ja Al, tavaliselt ka Zn (OA II); Ag (OA I), 6 heksa; 7 hepta; 8 okta; 9 nona; siis seda nimetusse ei pane. 10 - deka I -II VII -II Na2O naatriumoksiid Cl2O7 dikloorheptaoksiid II -II IV -II CaO kaltsiumoksiid SO2 vääveldioksiid III -II ...
oksiid- hapniku ja mingi teise keemilise elemendi ühend CaO-kaltsiumoksiid, CO- süsinikoksiid alus. oksiid- alusele vastav oksiid, reageerides happega annab soola ja vee Li2O- liitiumoksiid; CrO- kroomoksiid happ. oksiid- hapnikhappele vastav oksiid, reageerides alustega annab soola ja vee SO2- vääveldioksiid, CO2, süsinikdioksiid amfoteerne oksiid- oksiid, millel on nii aluselise kui happelise oks. omadused Al2O3- alumiiniumoksiid, ZnO, tsinkoksiid neutraalne oksiid- oksiid, mis ei reageeri ei happe, ei alusega ega veega. N2O- dilämmastikoksiid; CO- süsinikoksiid aluselised oksiidid: 1) aliseline oksiid + vesi = leelis 2) aluseline oksiid + hape = sool + H2O 3) aluseline oksiid + happeline oksiid= sool happelised oksiidid: 1) happeline oks. + vesi = hape 2) alus + hap. oks= sool + H2O 3) alusel. + hap. oks= sool Aluselise oksiidi kindlaks tegemine: võtta katseklaasi veidi CaO pulbrit ja lisada dest. vett. Loksutada! Jätta seisma CaO+ ...
KEEMIA OKSIIDID JA HAPPED 01.03.2012 OKSIIDID Tähtsamad ühendid: SiO2 ränidioksiid NO2 lämmastikdioksiid SO2 vääveldioksiid H2O vesi Fe2O3 raud(III)oksiid CO2 süsinikdioksiid CO süsinikoksiid CaO kaltsiumoksiid Valemi koostamine Valemi koostamiseks kasutan alati elementide oksüdatsiooniastet. Tean alati o.a's A-rühma metallid I-III, Vesinik H +I, Hapnik O II O.a näitab rühmanumber 1) elemendi sümboli kohale panen kirja elementide laengud ühendis 2) Kui võimalik, siis taandan o.a jagades arvuga, millega mõlemad o.a'd jaguvad 3) Molekulvalemite alaindeksid saame kui võtame taandatud o.a risti, ilma märgita ja kirjutame väikese numbrina sümboli alla. Vt. vihikust näiteid NIMETAMINE Metalli oksiidid A-rühma metalli oksiidid I-IIIA metalli nimetus + oksiid Nt: Li2O liitiumoksiid Al2O3 alumiiniumoksiid B-rühma metalli oksiidid / IV-VA metalli nimi (metalli o.a rooma number sulgudesse) + oksiid. Nt: Ag2O hõbe(I)oksii...
Metallide keemilised omadused ja saamise viisid Katse 1: oksiidi saamine 2Mg + O2 tº 2MgO Pannes kõrgel temperatuuril magneesiumi (hall) reageerima hapnikuga, on saaduseks valge magneesiumoksiid. Tegemist on redoksreaktsiooniga, kus redutseerijaks on magneesium, saades laenguks II ning oksüdeerijaks hapnik, saades laengu II. Katse 2: soola saamine Fe + S FeS + Q (soojus) Pannes raua (hall) reageerima väävliga (kollane), tekib sool raud(II)oksiid ning eraldub soojus. Seega on reaktsioon eksotermiline. Tegemist on redoksreaktsiooniga, kus redutseerijaks on raud, saades laenguks II ning oksüdeerijaks väävel, saades laenguks II. Katse 3: soola ja happe vaheline reaktsioon FeS + H2SO4 FeSO4 + H2S Pannes omavahel reageerima raud(II)sulfiidi (sool) ning väävelhappe (hape), on reaktsiooni tulemuseks uus sool ning nõrgem hape, ehk raud(II)sulfaat ning lenduv divesiniksulfiid, mille lendumist tunneme eelkõ...
Oksiidid Oksiidid on ained mis koosnevad kahest elemendist, millest üks on hapnik (oksüdatsiooniastmes -2). Oksiidide saamine Lihtainete vaheline reaktsioon Paljusid oksiide võib saada lihtaine reageerimisel hapnikuga. Näide: C + O2 =CO2 Hüdroksiidide ja karbonaatide lagundamine kuumutamisel Paljusid oksiide on võimalik saada neile vastavate hüdroksiidide või ka mõnede soolade(eelküige karbonaatide) lagundamisel kõrgel temperatuuril. Näide: Cu(OH)2 = CuO + H2O CaCO3= CaO + CO2 Liigitus Oksiide liigitatakse aluselisteks, happelisteks, amfoteerseteks ja neutraalseteks. Aluselised oksiidid Aluselisteks oksiidideks nimetatakse oksiide, mis reageerivad hapetega. Aktiivsete metallide(leelis-ja leelismuldmetallide) oksiidid on tugevalt aluselised. Nendele vastavad hüdroksiidid on vees hästilahstuvad tugevad alused ehk leelised. Vähemaktiivsete metallide oksiidid on nõrgalt aluselise. Nõrgalt aluselistele oksiididele vastavad hüd...
ANORGAANILISED AINED OKSIIDID - Ühendid, mis koosnevad kahest elemendist, millest üks on hapnik Oksiide saadakse: Lihtainete vaheline reaktsioon 2Mg + O2 -> 2MgO CH4 + 2O2->CO2 + 2H2O Hüdroksiidide ja karbonaatide kuumutamisel MgCO3 --to> MgO + Co2 OKSIIDIDE LIIGITUS - Oksiide saab liigitada aluselisteks, happelisteks ja amfoteerseteks ning neutraalseteks oksiidideks (happelisust, ega aluselisust üldse ei avaldu) ALUSELINE OKSIID - Oksiid, mis reageerib hapega NB! Kõik aluselised oksiidid on mittemolekulaarsed. Tugevalt aluselised oksiidid reageerivad aktiivselt veega, nõrgalt aluselised oksiidid veega ei reageeri. HAPPELINE OKSIID - Oksiid, mis reageerib alusega Suurem osa tuntumaid happelisi oksiide on molekulaarsed, kuid nende seas on ka mittemolekulaarseid aineid(nt SiO2 ja CrO3). Happeline oksiid + alus = sool + vesi SO2 + 2NaOH -> Na2SO3 + H2O Happeline oksiid + ves...
HAPPELISED JA ALUSELISED OKSIIDID. OKSIIDIDE SAAMINE Eesmärgid · Liigitan oksiide aluselisteks ja happelisteks. · Tean, et happelistest oksiididest. reageerivad veega ainult aktiivsete metallide oksiidid. · Kirjutan ja tasakaalustan reaktsioonivõrrandid oksiidi reageerimisel veega. · Nimetan oksiidide saamisvõimalusi (2). Metallioksiid ja mittemetallioksiid Leia järgmisest loetelust metallioksiidid ja mittemetallioksiidid: CaO, SiO2, Na2O, Cr2O3, N2O3, B2O3, CrO3, Fe2O3, BaO, MnO2, CO, Cl2O7, Al2O3, CuO, H2O. Oksiidide liigitamine · Oksiidid liigitatakse nende keelimiste omaduste alusel. · Enamik oksiide on kas aluselised või happelised. · TV lk 17 E (1) Aluselised oksiidid ...on aluseliste omadustega, nad reageerivad hapetega. Enamus metallioksiide on aluseliste omadustega. Aktiivsete metallide (I ja IIA rühm) oksiidid on tugevalt aluselised. Vähemaktiiv...
Aineklasside vahelised reaktsioonid Aluselise ja 1. alus + hape sool + NaOH + HCl NaCl + H2O happelise aine vesi 2 Fe(OH)3 + 3 H2SO4 Fe2(SO4)3 + 6 H2O reaktsioon: tekib 2. aluseline oksiid + hape CaO + 2HCl CaCl2 + H2O alati sool. sool + vesi Na2O + H2SO4 Na2SO4 + H2O (Happelise oksiidi 3. happeline oksiid + alus Ca(OH)2 + CO2 CaCO3 + H2O reageerimisel tekib sool + vesi 2 NaOH + SO3 Na2SO4 + H2O oksiidile vastava happe 4. happeline oksiid + CaO + CO2 CaCO3 sool!) aluseline oksiid sool 6 Na2O + P4O10 4 Na3PO4 Oksiidi 5. aluseline oksiid + vesi Na2O + H2O 2 NaOH reageerimine alus CaO + H2O Ca(OH)2 veega. Reageerivad vaid IA ja IIA al CuO + H2O ei toimu ...
Keemia tunnikontroll 29.01 Alused Mõisted: Alus, hüdrooksiid, leelis, neutralisatsioon Saamine (3 viisi), Reeglid, võrrandid, keemilised omadused Alus – Aine mis annab lahusesse hüdroksiidioone(üaine mis seob vesinikioone ehk prootoneid) Hüdroksiid- Anorgaaniline ühend mille koostisse kuuluvad hüdroksiidioonid OH või hüdroksiidrühmad Leelis – Vees hästilahustuv tugev alus (ehk hüdroksiid) Neutralisatsioon – Aluse ja happe vaheline reaktsioon, milles tekivad sool ja vesi Aluste saamine – Leelise saamine metalli reageerimisel veega (Veega reageerivad ainult aktiivsed metallid. Se on redoksreaktsioon, mille käigus eraludb vesinik). 2Na + 2H2O 2NaOH + H2 (lendub) Leelise saamine tugevalt aluselise oksiidi reageerimisel veega. Siis saadakse leelis kui vesi reageerib metalliga, mis asub IA-s või IIA metallidega, mis on Ca,Sr,Ba BaO + H2O Ba(OH)2 Aluse(hüdroksiidi)kau...
Hape on aine, mis annab vesilahusesse vesinikioone. Omadused: hapumaitse, reageerimine alustega, indikaatorite isel. Värvus hapete lahustes, reageerimine metallidega, reageerimine aluseliste oksiididega. Hapete liigitamine. * Hapnikuta hape hape, mis eisisalda hapnikku, nt HCl, HBr, HI, H2S. * Hapnikhape hape, mille koostisse kuulub ühe elemendina hapnik, nt H2SO4, H2SO3, HNO3, HNO2, H3PO4, H2CO3. * Üheprootonihape hape, mille molekul annab lahusesse ainult ühe vesinikiooni. Nt HCl, HBr, HI, HNO 3, HNO2, CH3COOH. * Mitmeprootonihape hape, mille molekul annab lahusesse kaks või enam vesinikiooni, nt H2SO4, H2SO3, H2CO3, H3PO4, H4SiO4.* Tugevad happed on tugevalt happeliste omadustgea. HCl, HBr, HI, HNO3, H2SO4. * Nõrgad happed on oluliselt nõrgemate happeliste omadustega nt. H2CO3, H2S, H3PO4, HNO2, CH3COOH( äädikhape). Kontsentreeritud tugeva happe lahjendamiseks tuleb teda valada peene joana vette ! Karboksüülhapete e orgaanili...
Tabasalu Ühisgümnaasium Sahhariidid referaat Koostaja: Aiki Sats Juhendaja: Evelin Maalmeister Tabasalu, 2013 Sisukord 1 Glükoos 1.1 Saamine 1.2 Tootmine 1.3 Kasutamine 1.4 Keemilised omadused 1.5 Fakte elus 2 Fruktoos 2.1 Saamine 2.2 Tootmine 2.3 Kasutamine 2.4 Keemilised omadused 3 Sahharoos 3.1 Saamine 3.2 Tootmine 3.3 Kasutamine 3.4 Keemilised omadused 3.5 Fakte elus 4 Kasutatud kirjandus 5 Lisa Glükoos (C6H12O6) 1.1 Saamine Glükoosi leidub puu- ja juurviljades, marjades, õites, mees. Rikkalikult leidub teda viinamarjades, millest tuleneb tema rahvapärane nimetus viinamarj...
Siirdemetallide ühendid Keijo Västrik TTG 10.c 1. Fe2O3 - Raud (III) oksiid Nimetused igapäevaelus - rooste Nimetused tööstuses - hematiit, rooste (hüdratiseeritud raua oksiid), punane raua oksiid, sünteetiline magnemiit Leidumine looduses - on maakmineraal hematiit, leidub inimese veres Omadused - ferromagnetiline (magneetub välise magnetvälja toimel ehk loob oma sisese magnetvälja), tumepunase värvusega, kergesti hapete poolt mõjutatav Kasutamine - rauatööstuses (raua, terase ja erinevate sulamite valmistamiseks), metalliliste ehete ja läätsete poleerimine, kasutatakse pigmendina (ka kosmeetikas) Tähtsus - on üks kolmest põhilisest raua koostisesse kuuluvast oksiidist Saamine 1) Raud(III) oksiid on raua oksüdeerumise saadusek...
Alumiinium ja raud Koostaja nimi: Tööülesanne: Täita alumiiniumi näidet järgides raua kohta slaidid nr 3, 4, 6, 7, 15 ja 17. Slaididele nr 4 ja 17 kanda alla märkustesse ka selgitavad tekstid võõrsõnade ja materjalide nimetuste selgitamiseks. Valmis töö salvestada nimega Raud(perek nimi).ppt (NB! Arvestatakse hindamisel!) Saata õpetajale meilile: [email protected] Aatomi ehitus Al Fe 3. periood, IIA 4 periood, VIIIB alarühm alarühm Al:+13|2)8)3) Fe:+26]2)8)14)2) A = 27 A = 55 Z = 13, N = 14 Z = 26, N = 30 Ioonid Al+3 Ioonid Fe² ja Fe³ OA III OA II Või III (oksüdatsiooniaste) Leidumine Al Fe Metallidest levinuim Aktiivne, esineb ainult Hõbevalge keskmise ühenditena ...
vKeemia praktiline töö Oksiidid 1. Oksiidide saamine. Olid antud NiSO4 lahus ning P, Zn ja Fe tahkel kujul. 1) Esiteks oli vaja tsink(II)oksiidi. Selleks puistasime piirituslambi leegi kohal tahket tsinki, mis seal põles. Et saada enam vähem puhast tsink(II)oksiidi kordasime eelmainitud katset mitu korda. 2Zn+ O2 2ZnO 2) Fe2O3 valmistamiseks toimisime samamoodi nagu ZnO valmistamisel. Puistasime kulbiga rauapuru piirituslambi leeki ja tekkis raud(III)oksiid. 4Fe + 3O2 2Fe2O3 3) Et valmistada nikkel(II)oksiidi valasime lahusesse kokku NiSO4 ja KOH. Tekkisid sool ja alus. NiSO4 + 2KOH Ni(OH)2 + K2SO4 Et nikkel(II)hüdroksiidist saada nikkel(II)oksiidi on vaja lahust kuumutada. Nikkel(II)oksiid lagunes kuumutamisel n...
Oksiid - on aine, mis koosneb kahest elemendist, millest üks on hapnik. 1) aluselised oks. - reageerib happelise oksiidi ja hapetega, veega tugevalt aluseline. 2) happelised oks. - reageerib alustega, aluselise oksiidiga ja veega. 3) amforteersed oks. - reageerib hapete ja alustega. saamine : *lihtainete vaheline reaktsioon * hüdroksiidide ja soolade lagundamine kuumutamisel Alus - on aine, mis annab vesilahusesse hüdroksiidioone. OM.- *sööbiv toime, *reageerimine hapetega, *reageerimine happeliste oksiididega. Hüdroksiid - on mitte- molaarne kristalne aine. Leelis - vees lahustuv tugev alus. Sool - kristalsed ained, mis koosnevad aluse katioonidest ja happe anioonidest. 1) lihtsoolad Na2CO3 2) vesiniksoolad NaHCO3 3) hüdr.soolad MgClOH OM. - * reageerib leelistega, *hapetega, *metallidega, *sooladega saamine: metall+mittemet.=sool alus+hape=sool+vesi oksiid+hape=sool+vesi aluseline oks.+happeline oks.=sool sool+leelis=alus+sool sool+...
Aineklassid ja nendevahelised seosed Aineklassid Lihtained: · Metallid (Na, Zn, Fe, Cu...) · Mittemetallid (C, Si, B, O2, H2, N2, F2, Cl2...) Liitained · Oksiidid (koosnevad kahest elemendist, millest üks on hapnik o.a-ga II; Na2O, CO, Cl2O3...) o Keemiliste omaduste järgi Aluselised oksiidid peamiselt metallioksiidid (eriti madalamas o.a-s); reageerivad hapetega; Na2O, CaO, BaO Happelised oksiidid peamiselt mittemetallioksiidid; reageerivad alustega; SiO2, SO3, CO2 Amfoteersed võivad reageerida nii hapete kui alustega; Al2O3, ZnO Neutraalsed ei astu tavaliselt keemilisse reaktsiooni; NO, N2O, CO · Happed (koosnevad ühest või mitmest vesinikust ja happe(jääk)anioonist; HCl, H2SO3, H3PO4...) o Vesiniku aatomite arvu järgi: Ü...
Aineklassid ja nendevahelised seosed Aineklassid Lihtained: Metallid (Na, Zn, Fe, Cu...) Mittemetallid (C, Si, B, O2, H2, N2, F2, Cl2...) Liitained Oksiidid (koosnevad kahest elemendist, millest üks on hapnik o.a-ga –II; Na2O, CO, Cl2O3...) o Keemiliste omaduste järgi Aluselised oksiidid – peamiselt metallioksiidid (eriti madalamas o.a-s); reageerivad hapetega; Na2O, CaO, BaO Happelised oksiidid – peamiselt mittemetallioksiidid; reageerivad alustega; SiO2, SO3, CO2 Amfoteersed – võivad reageerida nii hapete kui alustega; Al2O3, ZnO Neutraalsed – ei astu tavaliselt keemilisse reaktsiooni; NO, N2O, CO Happed (koosnevad ühest või mitmest vesinikust ja happe(jääk)anioonist; HCl, H2SO3, H3PO4...) o Vesiniku aatomite arvu järgi: ...
Liitium Üldine/aatomi ehitus Lühend: Li Elektronskeem: + 3| 2)1) Aatominumber: 3 Elektronide arv: 3 Aatommass: 6,941 Prootonite arv: 3 Kuuluvus: leelismetallid Neutronide arv: 4 Füüsikalised omadused Liitium see hõbevalge/hallika värvusega suhteliselt pehme leelismetall on kõige väiksema tihedusega metall üldse. Tema tihedus on 0,535 g/cm³, mis teeb liitiumist ka kõige väiksema tihedusega normaaltingimusel tahke aine. Olles erakordselt kerge metall on ta viis korda kergem kui alumiinium ning kaks korda kergem kui vesi. Sellepärast on liitium võimeline ujuma isegi petrooleumis. Tema sulamistemperatuur on 180,54 °C ning keemistemperatuur 1342 °C. Agregaatolek tavatingimustel on tahke. Võrreldes teiste leelismetallidega on liitium väiksema tihedusega ning kõrgema s...
Kordamisküsimused 1.Selgita mõisted. Redutseerija-loovutab elektrone. Oksüdeerija-redoksreaktsiooni käigus liidab endaga elektrone. Oksüdeerumine-aine loovutab elektrone ehk oksüdeerub. Redutseerimine-elektronide liitmisprotsess Korrosioon-metallide hävimine ümbritseva keskkonna toimel. Aluminotermia-oksiidist vaba metalli saamine alumiiniumi- ja oksiidipulbri segu süütamise teel. Akumulaator-aku, energia salvestamise seade Karbotermia-kõrgel temperatuuril metalli redutseerimine maagist süsiniku või süsinikoksiidi abil. Särdamine-metalliühendi üleviimine oksiidiks kuumutamisel õhuhapniku juuresolekul Keemiline vooluallikas-elektrokeemilises reaktsioonis vabanev energia muundub vahetult elektrienergiaks. Maagi rikastamine-maak vabastatakse kõrvalainetest kasutades füüsikaliste omaduste erinevust. 2.Võrrelge keemilise ja elektrokeemilise korrosiooni toimumise tingimusi. Keemiline- kuiva...
1) Skandiumi üldiseloomuomadused Skandium on element järjekorranumbri ning tuumalaenguga 21 ja massiarvuga 44,956. Omadustelt on skandium siirdemetall. See on raske ja hõbedase välimusega. See ei ole ilmastikule vastupidav ja lahustub aeglaselt kõigis lahjendatud hapetes. Sellel on 4 elektronkihti ja 2 elektroni väliskihil. Skandiumi oksüdatsiooniaste on +3. Skandium avastati 1879 aastal. Kristalli struktuur - kuusnurkne Ühendid ... on amfoteersed Skandium (III) kloriid, ScCl3On valge iooniline ühend mis õhu käes vedeldub ja ning lahustub vees hästi. 2Sc(s) + 6HCl(l) 2ScCl3 (s) + 3H2 (g) Skandium (III) fluoriid, SCF3On iooniline ühend, mis lahustub vees halvasti. Sc2O3 + NH4HF2 2ScF3 + 6NH4F + 3H2 Skandium (III) oksiid, Sc2O3 on kõrge sulamistemperatuuriga nõrgalt happeline valge tahke aine, mida kasutatakse kõrge temperatuuriga süsteemides, elektroonilises keraamikas ja klaasi koostises (kui abistaja materjal). Sc2O3 + 6 HCl 2 ...
Oksiidid Oksiidid koosnevad kahest elemendist, millest üks on hapnik. OKSIIDIDE LEIDMINE Otsusta, millised valemid kuuluvad oksiididele SO3, HNO3, CaC2, Cl2O7, BaO, CaCO3, NaOH, O2, H2O, CH4, Al2O3, MgSO4, P4O10, NH3 OKSIIDIDE SAAMINE I Metalli või mittemetalli reag. hapnikuga ◦ lihtainete põletamisel õhus või hapnikus liitainete põlemisel C + O2 CO2 CH4 + 2O2 CO2 + 2H2O 2Mg + O2 2MgO OKSIIDIDE SAAMINE II Hapnikku sisaldavat soolade, hapete ja aluste lagundamisel CaCO3 CaO + CO2 H2SO3 H2O + SO2 2Fe(OH)3 Fe2O3 + 3H2O Oksiidide liigitus koostiselementide järgi: OKSIIDI D Metallioksiidid : Mittemetallioksiid id: Na2O, CaO, CuO, Fe2O3 CO2...
Pärnu Ühisgümnaasium Hapnik Kaspar Rätsep 2011 1. Hapniku saamisvõimalused 1.1. Tööstuses saadakse hapnikku põhiliselt õhust vedela õhu fraktsioneerival destilleerimisel (kasutades hapniku ja lämmastiku keemistemperatuuride erinevust). 1.2. Eriti puhast hapnikku saadakse vee elektrolüüsil. 1.3. Vähepüsivate hapnikku sisaldavate ainete lagundamist (nt KMnO4, H2O2) Hapniku saamine H2O2 katalüütilisel lagundamisel H2O22H2O + O2 Gaaside valmistamise seadmesse valatakse 3 cm3 vesinikperoksiidi H2O2. Seejärel puistatakse ülemise mahuti kaudu seadmesse väikene kogus katalüsaatorit mangaan(IV)oksiidi MnO2, misjärel ava kohe kummikorgiga suletakse. Eralduvat hapnikku kogutakse kaaslase abiga läbi vee (st eelnevalt veega täidetud katseklaasi, mis on asetatud kõrge servaga klaasalusele). Gaas surub katseklaasist vee välja. 2. Hapniku kindlakstegemi...
AINF.KLASSIDE VAHELISF.D REAKTSIOONID Aluselise ja l. alus hape sool NaOH HCI NaCl + HIC) happelise aine vesi 2 3 H2S04 6 E-120 reaktsioon: tekib 2. aluseline oksiid + hape Mgo + 2HCl MgC12 + alati sool. sool vesi Na20 + H2SOå* Na2S04 + 1-120 3. happcline oksiid + alus —i COZ CaC03 + H20 (Happelise oksiidi sool 4 vesi reageerimisel tekib 2 NaOH + — Nazso, + HIC) oksiidile happe 4. happelinc Okiid aluseline cao + c02 — CaC03 oksiid 6 Nazo moo — 4 Nan, Oksiidi 5. aluseline oksiid + vesi Na20 + H20 2 NaOH reageerimine alus reageerivad vaid ja al CaO ...
Hapniku leidumine lihtainena - õhukoostis - vesi - mulle pindmised kihid Leidumine liitainete koostises - vesi - liiv - rasvad ja valgud - suhkur - puit - kivimid - soolad ja happed Füüsikalised omadused - gaasiline - värvitu - maitsetu - lõhnatu - vees lahustub - õhust raskem - vajalik kõigile elusorganismidele elutegevuseks Hapniku saamine - tööstus õhu fraktsioneerival destillatsioonil ja vee elektrolüüsil - laboris vee elektrolüüsil ja hapniku sisaldava ainete kuumutamisel Hapniku kogumine - õhuga täidetud anumasse - läbi vee Hapniku tõestamine - kui anumas on hapnikku, siis hõõguv puutikk süttib heleda leegiga põlema . Hapniku keemilised omadused - hapnik reageerib erinevate lihtainetega 1. metallide reageerimine hapnikuga ( põlemine ) 2. mittemetallide reageerimine hapnikuga ( põlemine ) - liitainetega reageerimine hapnikuga Hapniku kasutamine - põlemisel - hingamisel - keemiliste ainete saamisel - lõhkamistöödel Eran...
Hüdroksiidid e. alused Hüdroksiidid koosnevad metallioonist Me+.... ja hüdroksiidiooni(de)st OH- Hüdroksiidide nimetused ja valemid Nimetused · Püsiva o.-a.-ga metalli puhul: Al(OH)3 alumiiniumhüdroksiid · Muutuva o.-a.-ga metalli puhul: Cu(OH)2 vask(II)hüdroksiid Valemis hüdroksiidioonide arvu määrab metalliooni laeng: Fe+3(OH-1)3 Kirjuta järgmiste aluste nimetused: · Fe(OH)3 · Zn(OH)2 · KOH · Fe(OH)2 · Ca(OH)2 · Cr(OH)3 · LiOH Kontrolli aluste nimetusi · Fe(OH)3raud(III)hüdroksiid · Zn(OH)2 tsinkhüdroksiid · KOH kaaliumhüdroksiid · Cu(OH)2 vask(II)hüdroksiid · Ca(OH)2 kaltsiumhüdroksiid · Cr(OH)3 kroom(III)hüdroksiid · LiOH liitiumhüdroksiid Koosta järgmiste aluste valemid: · naatriumhüdroksiid · magneesiumhüdroksiid · vask(II)hüdroksiid · alumiiniumhüdroksiid · baariumhüdroksiid · kaaliumhüdroksiid · mangaan(II)hüdroksiid · liitiumhüdroksiid Kontrolli aluste valemeid · naatr...
1. Kõik happed annavad lahusesse vesinikioone. 2. Hapete omadused on tingitud vesinikioonide esinemisest lahuses. Om.-d: hapu maitse, muudavad indikaatorite värvust, reag. aluste ja aluseliste oksiididega, reag. metallidega. 3. Indikaatori muudavad happed punaseks. 4. Happed liigitatakse: 1)hapnikusisalduse järgi- *hapnikuta hape (n. HCl), * Hapnikhape (n.H2SO4) 2)vesinikioonide e prootonite arvu järgi-*üheprootonihape, *Mitmeprootonihape 3)tugevuse järgi- tugevad happed, nõrgad happed 5.Üheprootonihape- hape, mille molekul annab lahusesse ainult ühe vesinikiooni. (n. HCl, HNO3) 6.Mitmeprootonihape- hape, mille molekul annab lahusesse kaks või enam vesinikiooni. (n. H2SO4) 7. Vesinikiooni nim. ka prootoniks, sest ta koosnebki vaid ühest prootonist. 8. Sattumisel kätele või riietele- pesta veega, loputada söögisooda lahusega ja uuesti veega. ...
Riidaja Põhikool Referaat teemal Sn Koostaja: Tauno Johanson Juhendaja: Märt Tomp Riidaja 2009 Tina Mis see on? Tina on keemiline element, mille ladina keelne nimi on stannum ning sümbol on Sn.. Tina on hõbevalge, pehme, hästi taotav ja venitatav madala sulamistemperatuuriga metall. Ta on teistest metallidest kergesti ära tuntav seetõttu, et ta krigiseb painutamisel. Tina Mendelejevi tabelis Mendelejevi tabelis asub tina 50. kohal, seega on tema tuumalaeng 50 ja aatomituuma ümber tiirleb 50 elektroni. Tina peamised oksüdatsiooni astmed on II ja IV, sulamistempereatuur on 232°C ja keemistemperatuur on 2687°C ning tihedus on 7,29g/cm3, mis tähendab, et tina on 7,29 korda veest raskem. Molaarmassiks on 118,69 g/mol. Saamine Puhta ainena tina looduses ei esine, tähtsaim tinamaak on kassiteriit ehk ti...
OKSIIDID Oksiid-ühend, mis koosneb kahest elemendist, millest üks on hapnik. Nimetused: · Püsiva o.a astmega metallide korral nimetusse metalli o.a d ei märgita. Need on A rühma metallid v.a Sn ja Pb. · Muutuva o.a metallide korral märgitakse o.a väärtus oksiidi nimetusse · Mitemetallide korral antakse nimetused eeliidete abil. Saamine: 1. Lihtainete põlemisel 2Ca + O2 2CaO (Leek värvub punaseks) 2Cu + O2 2CuO ( Leek sinakasroheline) S + O2 SO2 ( Väävel põleb kahvatu sinise leegiga) 4P + 5O2 P4O10 ( Toss+leek) 2. Aluste lagunemisel ( Ei lagune I A metallil hüdroksiid v.a LiOH) Cu(OH)2 CuO + H2O 3. Hapete lagunemisel H2CO3 CO2 + H2O 4. Soolade lagunemisel CaCO3 CaO + CO2 5. Liitainete põlemise CH4 + 2O2 CO2 + 2H2O Liigitus: · Aluselised oks...
Oksiidid Oksiidid koosnevad kahest elemendist, millest üks on hapnik. Oksiidide liigitus koostiselementide järgi: · Metallioksiidid Na2O, CaO, CuO, Fe2O3 · Mittemetallioksiidid CO2, CO, SiO2, P4O10 Nimetuste andmine oksiididele: · Metallioksiidide nimetamine: a) Püsiva oksüdatsiooniastme korral metalli nimi+oksiid K2O kaaliumoksiid, Al2O3 alumiiniumoksiid b) Muutuva oksüdatsiooniastme puhul metalli nimi(oksüdatsiooniaste)+oksiid FeO raud(II)oksiid Cu2O vask(I)oksiid Fe2O3 raud(III)oksiid CuO vask(II)oksiid Mittemetallioksiidide nimetused: · Indeksite(sümboli taga all) nimetamisel kasutatakse eesliiteid: 1 (mono) 6 heksa 2 di 7 hepta 3 tri 8 okta 4 tetra 9 nona 5 penta 10 deka N2 O5 dilämmastikpentaoksiid NO2 lämmastikdioksiid Anna nimetus oksiididele: · CaO P2O5 · Al2O3 N 2O · CuO ...
Tartu Kivilinna Gümnaasium Liitium Koostas: Juhendaja: Tartu 2009 Sissejuhatus Liitium on keemiline element järjenumbriga 3. Liitium tuletati kreekakeelsest sõnast lithos, Mis tähendab kivi. Looduses on liitiumi suhteliselt palju, ta moodustab 0,02% maakoore aatomite üldhulgast. Suuremad liitiumiühendite leiukohad asuvad Kanadas, U.S.A.-s, Kagu-Aafrikas, Kasahstanis ja Kesk-Aasias. Liitium on hõbevalge ja erakordselt kerge metall, mis sulab temperaturril 180°C. Ta on kõrge väiksema tihedusega metall ja üldse kõige väiksema tihedusega normaaltingimusel tahke lihtaine: tema tihedus on 0,535g/cm³. Liitium on esikohal metallide hulgas kerguse poolest. Ta on viis korda kergem kui alumiinium ja kaks korda kergem kui vesi. Seepärast ujub liitium mitte ainult veepinnal vaid isegi petrooleumis. Liitium on leelismetall. Keemili...
Vesinik Koostas: Brenda · Avastaja, avastamisaeg, koht: Henry Cavendish, 1766, London, Suurbritannia · Aatomnumber: 1 · Aatommass: 1,00794 · Klassifikatsioon: selemendid · Maa massist moodustab vesinik umbes umbes 0,12%. Aatomi ehitus · Elektronvalem: 1s1 · Elektronskeem: +1|1) · Elektronite arv: 1 · Neutronite arv: 0 · Prootonite arv: 1 · Oksüdatsiooniast(m)e(d) ühendites: -I, 0, I · Kristalli struktuur: heksagonaalne · Põhiliselt liidab ühe elektroni, väga harva loovutab. · Deetrium raske vesinik, aatommass 2 (1 prooton + 1 neutron) · Triitium - Üliraske vesinik, aatommass 3 (1 prooton + 2 neutronit) Vesiniku isotoopidest · Tal on kaks stabiilset isotoopi massiarvudega 1 ja 2. · Erinevalt muudest elementidest on keemilised ja füüsikalised erinevused vesiniku isotoopide vahel suhteliselt suured. Seetõttu on neil erinimetused ja mitteametlikud, ent laialdas...
"Keemia alused" 3. kontrolltöö Küsimused, mis on toodud kaldkirjas, ei tule kontrolltöösse, kuid võivad esineda eksamiküsimustes. Tudeng peab teadma erinevate rühmade elementide peamiste ühendite nimetusi, oskama kirjutama ühendile vastavat keemilist valemit või vastupidi. Tudeng peab oskama kirjutama erinevate rühmade elementide peamiste ühendite tekkereaktsioone ning neid tasakaalustama. 1. Tähtsamad perioodilised seosed aatomite omadustes. Selgitage, kuidas muutuvad aatomiraadius, ionisatsioonienergia, elektronafiinsus, elektronegatiivsus ja polariseeritavus perioodilisustabelis. Aatomiraadiused vähenevad perioodis vasakult paremale ja rühmas kasvavad ülevalt alla. Aatomi raadius väheneb perioodilisuse tabelis vasakult paremale ja suureneb ülevalt alla. Igas uues perioodis lisanduvad uued elektronid järjest välimistele elektronkihtidele, mis asuvad aina kaugemal tuumast ja seetõttu suureneb raadius üleva...
Tallinna Arte Gümnaasium Liitium Koostaja : Maris Lallo 2010 Sisukord 1.Üldinfo 2.Omadused 3.Ajalugu 4.Liitiumi aspektid ja ravi 5.Liitiumi kasutamine 6.Liitiumi omadused 7.Kasutatud kirjandus Liitium Li metall Liitium Aatomnumber: 3 Aatommass: 6,947 Klassifikatsioon: leelismetallid, s- elemendid Aatomi ehitus: · Elektronvalem: 1s2 2s1 · Elektronskeem: +3|2)1) · Elektronite arv: 3...
ANORGAANILISTE AINETE KLASSID konspekt ja tööleht OKSIIDID on liitained, mis koosnevad kahest elemendist, millest üks on hapnik(oa II ). Näit: H2O CO2 Fe2O3 CaO. HÜDROKSIIDID (ALUSED) on liitained, koosnevad metalliiooonidest ja hüdroksiidioonidest OH-. Näit: NaOH Ca(OH)2 HAPPED on liitained, mis koosnevad vesinikioonidest ja happeanioonidest. Näit: HCl H2SO4 H3PO4 SOOLAD on liitained, mis koosnevad metalliioonidest ja happeanioonidest. Näit: NaCl CaF2 Al2(SO4)3 Aine valemis asuvad esimesel kohal positiivsed koostisosad (H + Na+ Al3+ jne ) ja teisel kohal negatiivsed koostisosad ( O 2- OH- SO42- Cl- jne ) Kirjuta iga valemi taha aine klassiline kuuluvus (O Hü Ha S ): Na2SO4 KBr N2O5 P4O10 H3PO4 Ca3(PO4)2 Ca(OH)2 CaO HCl CaCl 2 H2SO4 SO3 MgSO3 Mg(OH)2 MgO FeO . OKSIIDID Oksiidid on looduses ühed kõige enam levinumad ühendid. Oksiidid on iseloomulikud ühendid, kuna nende omadused on heas koos...
Õpimapp Keemias 2011 Sisukord Skeem: Anorgaaniliste ainete põhiklassid.......................................3 Skeem: Aineklasside vahelise seosed.............................................5 Aineklasside tähtsamad keemilised omadused...............................8 Kõikide aineklasside saamisviis.....................................................10 2 Anorgaaniliste ainete põhiklassid (skeem) Alused on ained, mis annavad lahusesse hüdroksiidioone OH-. Tüüpilised alused on hüdroksiidid. Hüdroksiidid koosnevad metalliioonidest ja hüdroksiidioonidest (OH-). Happed on ained, mis annavad lahusesse vesinikioone (H+). Happed koosnevad vesinikioonidest ja happeanioonidest (happejäägist). Happeaniooni laeng võrdub vesiniku aatomite arvuga happe molekulis. Hapete liigitamine vesiniku aatomite arvu järgi: 1. Üheprootonilised happed (n...
Aatomnumber: 19 Aatommass: 39,098 Klassifikatsioon: leelismetallid, s-elemendid Aatomi ehitus: · Elektronvalem: 1s2 2s2p6 3s2p6 4s1 · Elektronskeem: +19|2)8)8)1) · Elektronite arv: 19 · Neutronite arv: 20 · Prootonite arv: 19 · Oksüdatsiooniast(m)e(d) ühendites: 0, I · Kristalli struktuur: ruumikeskne kuubiline Füüsikalised omadused: · Aatommass: 39,098 · Sulamistemperatuur: 63,25 °C · Keemistemperatuur: 759,9 °C · Tihedus: 0,862 g/cm3 · Värvus: hõbevalge · Agregaatolek toatemperatuuril: tahke · Kõvadus Mohsi järgi: 0,4 · Isotoobid: Nukliid Levimus (%) Mass Poolestusaeg 39 K 93,22 38,9637 - 40 K 0,118 39,974 1,28 · 109 aastat 41 K 6,77 40,9618 ...
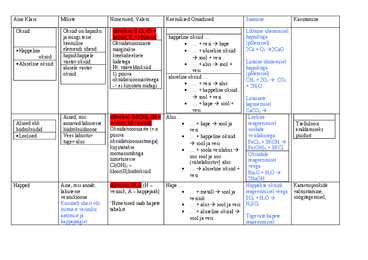
Aine Klass Mõiste Nimetused, Valem Keemilised Omadused Saamine Kasutamine Oksiid Oksiid on hapniku üldvalem: E2On (O = Lihtaine ühenemisel ja mingi teise hapnik, E = element) happeline oksiid ... hapnikuga keemilise Oksüdatsiooniaste · ... + vesi hape (põlemisel) · Happeline elemendi ühend märgitakse · ... + aluseline oksiid 2Ca + O2 2CaO oksiid hapnikhappele kreekakeelsete sool + vesi · Aluseline oksiid vastav oksiid liidetega Liitaine ühinemisel · ... + alus sool ...
1. LEELISMULMETALLIDE LDISED OMADUSED ( VRRANDID, REAG.HAPNIKUGA, HALOGEENIDEGAM VEEGA, LAHJENDATUD HAPETEGA). Ca, Sr, Ba ja Ra- leelismuldmetallid, nimetus tuleneb sellest,et nende metallide oksiidid mood. vees leeliseid, nii nagu leelsimetallid. Keemilise aktiivsuse tttu leiduvad rhma elemendidlooduses ainult henditena. Metallid on hbevalge vi hallikasvalge vrvusega. Vrreldes leelismetallidega on neil suurem tihedus, kvadus ja krgem sulamis- ja keemistemp., mille heks phjuseks on asjaolu, et nende aatomite vliselektronkihil on kaks korda rohkem valentselektrone kui vastavatel leelismetallidel. Lihtainena on IIA rhma metallid keem.aktiivsed, kuid vhemakt. kui leelismetallid. - Reag.hapnikuga: krgemal temp'l sttivad metallid heleda leegiga plema ja mood. vastava oksiidi. 2Mg + O2 tekib 2Mg - Reag. halogeenidega: hinevad energiliselt mood. vastavaid halogeniide: Ca + Cl2 tekib CaCl2 (kaltsiumkloriid) Sr + Br2 tekib SrBr2 (strontsiumbro...
referaat Tseesium Sisukord Elemendist üldiselt. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . lk 3 Ajalugu . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .lk 3 Omadused . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .lk 4 Leidumine looduses . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . lk 4 Kasutamine . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . lk 4 Andmed . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .lk 5 Lihtaine saamine . . . . . . . . . . . . . . ...
LÄMMASTIK JA FOSFOR ÜLDISELOOMUSTUS · VA rühma tuntuimad ja tähtsamad elemendid on LÄMMASTIK ja FOSFOR · Rühmas ülevalt alla elementide aatomiraadiused kasvavad, mittemetallilisus tugevasti väheneb. · Selles rühmas on elementide aatomite väliskihis 5 elektoni (puudu 3 elektroni) · Maksimaalne oksüdatsiooniaste V ja madalaim oksüdatsiooniaste III. LIHTAINED · LÄMMASTIK koosneb kaheaatomilistest molekulidest. · LÄMMASTIKUL allotroope ei esine. · Tavatingimustes esineb värvusetuna ja on lõhnatu. · Vees peaaegu ei lahustugi. · Keemistemperatuur -196 kraadi. · FOSFORi põhiline allotroop on kihilise ehitusega punane fosfor. · Valge fosfor tugevalt mürgine tetraeedrilistest molekulidest koosnev fosfor on ebapüsiv ja keemiliselt aktiivsem. Kuumutamisel ühtlaselt inertses keskkonnas läheb see üle PUNASEKS FOSFORIKS. · Vees ei lahustu. · MÕLEMAD on väheaktiivsed ained. ...
LÄMMASTIK JA FOSFOR ÜLDISELOOMUSTUS • VA rühma tuntumad ja tähtsamad elemendid LÄMMASTIK ja FOSFOR • Rühmas ülevalt alla elementide aatomiraadiused kasvavad, mittemetallilisus tugevasti väheneb. • Selles rühmas on elementide aatomite väliskihis 5 elektoni (puudu 3 elektroni) • Maksimaalne oksüdatsiooniaste V ja madalaim oksüdatsiooniaste –III. LIHTAINED • LÄMMASTIK koosneb kaheaatomilistest molekulidest. • LÄMMASTIKUL allotroope ei esine. • Tavatingimustes esineb värvusetuna ja on lõhnatu. • Vees peaaegu et ei lahustugi. • Keemistemperatuur -196 kraadi. • FOSFORi põhiline allotroop on kihilise ehitusea punane fosfor. • Valge fosfor – tugevalt mürgine tetraeedrilistest molekulidest koosnev fosfor on ebapüsiv ja keemiliselt aktiivsem. Kuumutamisel ühtlaselt inertses keskkonnas läheb see üle PUNASEKS FOSFORIKS. • Vees ei lahustu. • MÕLEMAD on väheaktiivsed ained. ...
Rubiidium Ettekanne Kristina Hertmann 10K Juhendaja : Anna Perova Üldiseloomustus Aatominumber: 37 Aatomimass: 85,4678 Klassifikatsioon: Leelismetallid, s-elemendid Aatomi ehitus: · Elektronvalem: 1s2 2s2p6 3s2p6d10 4s2p6 5s1 · Elektronskeem: +37|2)8)18)8)1) · Elektronite arv: 37 · Neutronite arv: 48 · Prootonite arv: 37 · Oksüdatsiooniast(m)e(d) ühendites: 0, I · Kristalli struktuur: ruumikeskne kuubiline Avastamine: R.W. Bunsen & G.R. Kirchoff, 1861, Heidelberg, Saksamaa Avastati see mineraal lepidokrokiidist, kasutades spektroskoopi. Nimi rubiidium tuleneb ladina keelsest sõnast "ruber", mis tähendab sügavpunast. Sellist nime põhjustasid rubiidiumi erepunased spektroskoopilised jooned. Leidumine looduses Rubiidiumi (Rb) puudust looduses ei ole. Teda leidub rohkem kui kulda, hõbedat või tina jne. Rubiidium kuulub kohekümne kolme kõige ...
Kordamisküsimused (õpik lk 150 176) 1) Selgita mõisteid: korrosioon: metalli hävimine (oksüdeerumine) keskkonna toimel keemiline korrosioon: toimub kuivades gaasides ja vedelikes, mis ei juhi elektrivoolu (nt raua ühinemine hapnikuga ilma niiskuse juurdepääsuta) elektrokeemiline korrosioon: on seotud galvaaniaelementide tekkimisega, toimub kui kaks erinevat metalli on kontaktis elektrolüüdi lahusega (juhib elektrit) maak:kivim või mineraal, mis on mingi lihtaine saamisel tooraineks metallurgia: metallide ja sulamite tootmine metallimaakidest särdamine: mitteoksiidsete maakide kuumutamine õhu juuresolekul, et saada oksiidne maak (metallide tootmisel maagist, pärast seda viiakse läbi redutseerimine) redutserimine: metalli saamine maagis sisalduva metalliühendi redutseerimisel (aluminotermia, karbotermia) maagi rikastamine: maak vabastatakse lisanditest, kasuta...
Lämmastik 1. Mittemet. Ja nende ühendite omaduste võrdlev iseloomustus. 2. mittemet. Ja nende ühendite kasutamise valdkonnad 3. Mittemet. Ja nende ühendid looduses sealhulgas elusorganismides 4. Süsiniku, hapniku, lämmastiku ja väävli ringkäik looduses. LÄMMASTIK N (ld.k. nitrogenium- salpeetri tekitaja) Leidumine Lämmastik esineb looduses nii lihtainena kui ka ühendites. Lihtainena koosneb lämmastik kaheaatomilistest molekulidest N2. Lihtainena leidub lämmastikku kõige rohkem atmosfääris, kus õhu koostises on teda 78,1 mahuprotsenti. Ühendite koostises leidub lämmastikku erinevates mineraalides, eelkõige nitraatides ehk salpeetrites (NaNO3 tsiili salpeeter, KNO3 india salpeeter). Joonis NaNO3 Lämmastikku leidub ka valkudes ja nukleiinhapetes, olles seega kogu eluslooduse väga tähtis koostiselement. Lisaks esineb lämmastikku veel neutraalsete ja ioniseeritud aatomitena ning ühenditena Päikese ja teiste planeetide a...
METALLIDE SAAMINE. Üle 80% kõikidest elementidest on metallid. Mõned neist, näiteks kuld ja plaatina esinevad looduses ehedana, enamik metalle on looduses aga ühenditena. Looduslikud mineraalse tooraine mitmesuguseid liike, mis kõlbavad vabade metallide saamiseks tööstuslikus mastaabis, nimetatakse maakideks. Metallide saamiseks maakidest on mitu meetodit. Tähtsama neist on : 1) Metallide oksiidide redutseerimine söe või süsinikoksiidi abil. Raua tootmine oksiididest põhineb näiteks süsinikoksiidiga redutseerimise reaktsioonil. Fe2 O 3+3 CO=2 Fe+3 Co2 2) Metallide oksiidide redutseerimine aktiivsemate metallidega. Seda meetodit nimetatakse metallotermiaks. Tänapäeval kasutatakse metallotermiat peamiselt raskesti sulavate metallide saamisel. Näiteks tekib kroom (III) oksiidi ja alumiiniumi segu kuumutamisel: Cr 2 O 3 +2 Al= Al 2 O 3 +2 Cr Alumiiniumiga redutseerimise prot...
Gümnaasium referaat Koostaja: Juhendaja: Tartu 2009 Sissejuhatus Elemendist üldiselt Tina on keemiliste elementide perioodilisussüsteemi IV rühma element, selle sümbol on Sn(lad. k. stannum)ja järjenumber on 50 .Looduslik tina koosneb kümnest stabiilsest isotoobist, mille massiarvud on 112, 114-120, 122 ja 124. Tal on kõigist elementidest kõige rohkem stabiilseid isotoope. Tina on õhu käes väga aeglaselt tumenev hõbevalge, pehme, plastne ja venitatav madala sulamistemperatuuriga metall. See on püsiv õhuhapniku ja vee suhtes, sest kattub kaitsva oksiidikihiga. Ta on teiste metallide seast kergesti äratuntav seetõttu, et tina krigiseb painutamisel. Looduses on see väheesinev element, teda leidub maakoores pealmiselt kassiteriide ehk tinakivi (SnO2) kujul, millest teda saadakse redutseerimisel söega. Tina esineb kolme kristallmo...
Happed – koosnevad vesinikioonidest ja happeanioonidest. Annavad lahusesse vesinikioone (H2 SO3). vesinikioon happeanioon Alused – koosnevad metalliioonidest (metall) ja hüdroksiidioonidest (OH -). Annavad lahusesse hüdroksiidioone. Näiteks: KOH (kaaliumhüdroksiid), Fe(OH) 2 (raud(II)hüdroksiid), Ca(OH)2 (kaltsiumhüdroksiid). Oksiidid – koosnevad kahest elemendist, millest üks on hapnik (SO 2, Al2O3). Liigitatakse aluselised (metall + hapnik), happelised (mittemetall + hapnik), neutraalsed ja amfoteersed oksiidid. Hapniku oksüdatsiooniaste on oksiidides –II. Soolad – koosnevad metallioonist (näiteks – Na+, Fe2+, Cu2+, Al3+ jne.) ja happeanioonist (näiteks: SO4 2-, Cl- jne.). Näiteks: NaCl, FeSO 4, K2CO3. Anioon Happeaniooni OH- -hüdroksiid metall-OH (NaOH) - Cl- -kloriid HCl (vesinikkloriidhape) metall-Cl näit. KCl (kaaliumkloriid) F- -flouriid HF (vesinikflouriidhape) metall-F näit. NaF (naatriumflouriid) Br- -bromiid HBr (vesinikb...
Mittemetalliliste elementide aatomiehituse iseärasused Mõõtmed on suhteliselt väiksemad, kui metallilistel elementidel ning neil on väliskihil rohkem elektrone, kui metallilistel elementidel. Elementidemittemetallilised omadused on seotud aatomite võimega liita elektrone. Fluor saab elektrone ainult liita. Metallid käituvad oksüdeerijana reageerimisel metallidega ja endast vähem aktiivsete mittemetallidega. Mittemetallid käituvad redutseerijana reageerimisel endast aktiivsemate mittemetallidega. Max. o.-a on vastavuses rühma numbriga. Min. o.-a. on vastavuses n-8. Vahepealne o.-a. on püsivast o.-a. 2 võrra väiksem. Püsivad o.-a. H(I); B(III); C, Si(IV); N(-III); P,As(V); O, S(-II); Se, Te(VI); F, Cl, Br, I(-I). Poolmetallid on metalliliste ja mittemetalliliste omadustega elemendid. Neil on läige, haprad, raskesti töödeldavad, elektrijuhtivuselt vahepealsed(pooljuhid) Mittemetallide ühised füüsikalised omadused · Kõik on väga erineva...
OKSIIDID Metallioksiidid: nimetus à metalli nimi (vajadusel oksüdatsiooniaste)oksiid Mittemetallioksiidid : tavaliselt on molekulaarse ehitusega ja nimetus reagee Metallioksiidid on ioonilised ained ja molekule pole moodustatakse eesliidete abil (mono, di ,tri, tetra, penta, heksa, hepta, okta, rimine Näiteks CaO kaltsiumoksiid Fe2O3 raud(III)oksiid e. diraudtrioksiid nona ,deka) CO2 süsinikdioksiid N2O dilämmastikoksiidP4O10 tetrafosfordekoksiid reageerimi ne SOOLATEKITAJAD OKSIIDID ...
Millega tegeleb keemia Keemia teadus, mis uurib aineid ja ainetega toimuvaid muundumisi. Puhas aine koosneb ühte liiki aineosakestest (molekulid, aatomid või ioonid). Kindel koostis ja kindlad omadused. Nt, keedusool(NaCl), suhkur( C12 H 22 O11 ), kuld(Au), vask(Cu). Ainete segu koosneb mitme aine osakestest. Kindel koostis puudub. Omadused sõltuvad koostisest. nt, õhk, looduslik vesi, muld, pronks. Ainete füüsikalised omadused: Värvus, lõhn, maitse iseloomulikud omadused, mille järgi saab aineid kergesti eristada. Agregaatolek aine võib tavatingimustel olaa tahke(kindel kuju), vedel(voolav, võtab anuma kuju) või gaasiline(levib kogu ruumi ulatuses). Tihedus näitab, kui suur on kindla ruumalaga ainekoguse mass Tähis (roo). Valem =m/V. Mõõtühikud: kg/m 3 ; g/cm 3 ; kg/dm 3 . Tugevus aine vastupidavus painutamisele, venitamisele või survele. Kõvadus aine vastupidavus kriimustamisele või lõikamisele. Sulamis- ja keemistempe...