elementide aatomeid (fosfor, väävel, raud...). Põhielementide valentsid ja valentsolekud. C valents 4, valentsolekuid 3; N valents 3, valentsolekuid 3; O valents 2, valentsolekuid 2; H valents 1, valentsolekuid 1. Süsiniku o.a ja selle arvutamine. Süsiniku o.a väärtused ulatuvad -4 kuni +4. iga vesinik annab -1 juurde, iga süsinik annab 0 juurde ja hapnik ja kõik muu annab +1 juurde Keskmise arvutamine.NT: C5H12 H12=12 , et saada C ka - 12 tuleb 12/5=-2.4 Mis on süsivesinikud? Keemilised ained, mis koosnevad ainult süsinikust ja vesinikust. Mis on isomeeria? Ühendid, millel on sarnane summaarne valem kuid erinev struktuur. Mis on alkaanid?(Alkaanide üldvalemiks on CnH2n+2 ning nimetuse lõpuks –aan.) Alkaanid on küllastunud süsivesinikud, kus süsiniku aatomi vahel on kovalentsed üksiksidemed
ka keemikutele olulisemad · Nomenklatuur aine struktuuri ja nimetust siduvate reeglite kogu Alkaan Nimi Alküülrühm Alküülrühma nimet. CH4 Metaan CH3 Metüül C2H6 Etaan C2H5 Etüül C3H8 Propaan C3H7 Propüül C4H10 Butaan C4H9 Butüül C5H12 Pentaan C5H11 Pentüül C6H14 Heksaan C6H13 Heksüül C7H16 Heptaan C7H15 Heptüül C8H18 Oktaan C8H17 Oktüül C9H20 Nonaan C9H19 Nonüül C10H22 Dekaan C10H21 Deküül · Alkaani tunnuseks on liide aan · Sõnatüvi kirjeldab süsinikahela pikkust
Keemia kontrolltöö 4 )ALKAANID: 1)Aatomite olek molekulis(lk 25, E ): 1) metaan- CH4 C(süsinik)- neli sidet 2) etaan- C2H6 N(lämmastik)-kolm sidet 3) propaan- C3H8 O(hapnik)- kaks sidet 4) butaan- C4H10 H(vesinik)-üks side 5) pentaan- C5H12 6) heksaan- C6 H14 7) heptaan- C7 H16 8) oktaan- C8 H18 9) nonaan- C9 H20 10) dekaan- C10H22 2)Teooria( õp lk 96-111): Alkoholid( üldvalemiga ROH ) Alkoholid-alkaanidest tuletatud ühendid · molekulis üks või enam vesinikuaatomit on asendatud hüdroksüülrühmaga (- OH-rühmaga) · veesõbralikud, lahustuvad vees paremini kui alkaanid · ei muuda vesilahuse keskkonda · mõned alkoholid on mürgised · alkoholid ei ole alused Metanool (CH3OH) e. puupiiritus
· Reaktsioonivõime tõtstmiseks tuleb kasutada katalüsaatorit või kuumutada. · Alkaanid ei reageeri toatemperatuuril isegi konsentreeritud hapetega ja leelistega. a) Täielik põlemine ehk kiire oksüdatsioon CH4 + 2O2 CO2 + 2H20 b) Mittetäielik põlemine ehk aeglane oksüdatsioon C5H12 + 5O2 2CO2 + 6H2O + C (tahm) c) Oksüdeerumine alkoholis 2C2H6 + O2 2C2H5OH d) Pürolüüs (krakkimine) Aine lagundamine kõrge temperatuuri või katalüsaatorite toimel, mille käigus pikad alkaanide ahelad lagundatakse lühemateks. C8H18 temp./katal. C5H12 + C3H6 3.Alkaanide füüsikalised omadused.
SÜSIVESINIKUD On orgaanilisedühendid mis koosnevad süsinikust ja vesinikust Alkaanides on 1-4 liiget gaasid ja alates 5. on vedelikud. ALKAANID 1) Metaan CH4 2) Etaan C2H6 3) Propaan C3H8 4) Butaan C4H10 5) Pentaan C5H12 6) Heksaan C6H14 7) Heptaan C7H16 8) Oktaan C8H18 9) Nonaan - C9H20 10) Dekaan C10H2 ALKOHOOLID Alkohoolide nimetus on tuletatud süsivesinikest, millest üks või mitu on hüdroksiid. Alkohoolide nimed pannakse lähtudes alkaanide reast C-de(süsinike) arvu järgi. CnH2 + 2 = AAN lõpuga 1) CH4 metaan ---- CH3OH = metanool ehk puupiiritus 2) C2H6 etaan ---- C2H5OH = etanool ehk viin (vodka)
(ALKAANID) (ASENDUSRÜHM) CH4 Metaan CH3-metüül C2H6 Etaan C2H5- etüül C3H6 Propaan C3H7 -Propüül C4H10 Butaan C4H9 -butüül C5H12- Pentaan JNE.... C6H14- Heksaan C7H16- heptaan C8H18 -oktaan C9H20 - nonaan C10H22- dekaan Valents- näitab mitut kovalantet sidet võib antud aatom moodustada. Orgaanilises ühendites on süsiniku valem alati 4 ORAAGILISED ÜHENDID- a)atsüklilised b) tsüklilised Isomeeria on nähtus, kus ainetel on ühesugune element koostis ja molekulmass aga erinev struktuur ja omadused Molekulvalem- summaarvalem nõitab aine koostist, kui palju ja milliste elementide aatomid
o NÄIDE C4H10 + 2Cl2 C4H8Cl2 + 2HCl (diklorobutaan) C arv saaduses ei muutu H indeksi saadusesse saad, kui lahutad algaine vesiniku indeksist halogeeni kordaja – (H)10- 2(Cl 2) = saaduses C4H8Cl2 Saadusesse C4H8Cl2 läheb algne halogeen koos oma indeksiga, ignoreeri antud hetkel talle antud kordajat o NÄIDE 2, 3 C5H12 + (1)F2 C5H11F + HF (flouropentaan) C9H20 + Br2 C9H19Br + HBr (bromononaan) Oktadekaan 8 + 10 C18H(2*18+2)=38
Valem Nimetus Valem Nimetus Valem Nimetus 1 Mono CH4 metaan CH3- metüül- - - 2 Di C2H6 etaan C2H5- etüül- - - 3 Tri C3H8 propaan C3H7- propüül- C3H6 tsüklopropaan 4 Tetra C4H10 butaan C4H9- butüül- C4H8 tsüklobutaan 5 Penta C5H12 pentaan C5H11- pentüül- C5H10 tsüklopentaan 6 Heksa C6H14 heksaan C6H13- heksüül- C6H12 tsükloheksaan 7 Hepta C7H16 heptaan C7H15- heptüül- C7H14 tsükloheptaan 8 Okta C8H18 oktaan C8H17- oktüül- C8H16 tsüklooktaan 9 Nona C9H20 nonaan C9H19- nonüül- C9H18 tsüklononaan
üksik side alkaan Homoloogiline rida: 1. metaan CH4 2. etaan C2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptaan C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22 kaksikside alkeen 12. eteen C2H4 13. propeen C3H6 14. buteen C4H8 15. penteen C5H10 16. hekseen C6H12 17. hepteen C7H14 18. okteen C8H16 19. noneen C9H18 20. dekeen C10H20 kolmikside alküün 32. etüün C2H2 33. propüün C3H4 34. butüün C4H6 35
Alkaanideks nimetatakse orgaanilisi aineid, mis koosnevad C ja H'st, ning kus C aatomite vahel on üksikside ehk sigmaside. Üldvalem CnH2n+2 (n on jrk nr) Orgaanilistele ainetele pannakse nimed alkaanide homoloogilise rea alusel. 1. metaan CH4 2. etaan C2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptann C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22 Radikaalid on molekulid või aatomid, mille elektronkihis asub paardumata elektron. 2-metüül propaan Alkaanide keemilised omadused: 1) Põlemine CH4 + 2O2 -> CO2 + 2H2O
Hal on negatiivne osalaeng, sest elektronpilv on suurem Elektrofiil- tühja orbitaaliga osake Elektrofiilsustsenter- elektrofiili koostisesse kuuluv tühja või osaliselt tühja orbitaalida aatom Nukleofiil- vaba elektronpaariga osake Nukleofiilide suhteline tugevus Nõrgad nukleofiilid *Happeanionid ROOO *Halogeeniidiioonid Hal *Vesi H2O *Alkoholid ROH Tugevad nukleofiilid *Hüdroksiidid OH *Alkoksiidiioon OR *Tsüaniidioon CN *Amiinid R-NH2 CH4-metaan C2H6-etaan C3H8-propaan C4H10-butaan C5H12-pentaan C6H14-heksaan C7H16-heptaan C8H18-oktaan C9H20-nonaan C10H22-dekaan
Nimetus Valem Metaan CH4 Etaan C2H6 Propaan C3H8 Butaan C4H10 Pentaan C5H12 Heksaan C6H14 Heptaan C7H16 Oktaan C8H18 Nonaan C9H20 Dekaan C10H22 Undekaan C11H24 Dodekaan C12 H26 Tridekaan C13H28 Tetradekaan C14H30 Pentadekaan C15H32 Reaktsioonivõrrandis Mittemetallioksiidid + Vesi = Hape Sool + Hape = Uus hapse + Uus sool SiO2 (liiv) veega ei reageeri Tekkiv hape peab olema algsest nõrgem Metallioksiidid + Vesi = Alus Sool + Sool = Sool + Sool
Väga mürgine. · Etanool (CH3CH2OH) e. piiritus väga palju kasutatakse lahustites ja orgaanilistes sünteesides. Samuti kasutatakse etanooli ka alkoholitööstuses alkohoolsete jookide valmistamiseks. · Etaandiool (HOCH2CH2OH) kõrge keemistemperatuur, hea lahutuvus ja madal külmumistemperatuur. Kasutatakse antifriiside (automootorite jahutussegud) koostises. Alkaan Nimetus CH4 metaan C2H6 etaan C3H8 propaan C4H10 butaan C5H12 pentaan C6H14 heksaan C7H16 heptaan C8H18 oktaan C9H20 nonaan C10H22 dekaan
arv nimetus nimetus 1 CH4 metaan CH3 metüül 2 C2H6 etaan C2H5 ehk CH2CH3 etüül 3 C3H8 propaa C3H7 ehk CH2CH2CH3 propüül n 4 C4H10 butaan C4H9 ehk CH2CH2CH2CH3 butüül 5 C5H12 pentaan ... ... 6 C6H14 heksaan ... ... 7 C7H16 heptaan ... ... 8 C8H18 oktaan ... ... 9 C9H20 nonaan ... ... 10 C10H22 dekaan ... ...
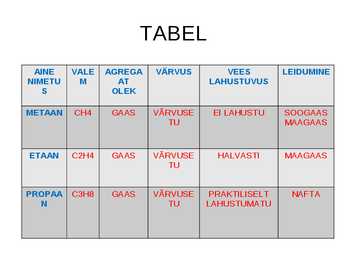
TU PROPAA C3H8 GAAS VÄRVUSE PRAKTILISELT NAFTA N TU LAHUSTUMATU ALKAANIDE ÜLDVALEM CnH2n+2 C-aatomite arv Nimetus Valem Olek 1 METAAN CH4 G 2 ETAAN C2H6 A 3 PROPAAN C3H8 A 4 BUTAAN C4H10 S 5 PENTAAN C5H12 6 HEKSAAN C6H14 7 HEPTAAN C7H16 VEDELIK 8 OKTAAN C8H18 9 NONAAN C9H20 10 DEKAAN C10H22 · Alkaanid-lõppsilp-aan Alkeenid-lõpp-een · Keemiliselt on aktiivsemad alkeenid · Metaani esineb:maa,-soo,-kaevandusgaasis · Metaan on kasvuhoooneefekti tekitav gaas · Biogaas-orgaaniliste jäätmete kääritamisel hermeetiliselt saadakse biogaas · Parafiinid-sisaldavad tahkeid alkaane
etaanhape- pole mürgine 2) Milleks kasutatakse etaandiooli ja glütserooli *etaandiool- jahutusvedelikes *glütserool- kosmeetikas 3) Too kaks näidet igapäevaelust leiduvatest karboksüülhapetest *sidrunhape (sidrunites) *oblikhape (rabarberis) 4) Alkaanid *metaan- CH4 *etaan- C2H6 *propaan- C3H8 *butaan- C4H10 Juergen Guido *pentaan- C5H12 *heksaan- C6H14 *heptaan- C7H16 *oktaan- C8H18 *nonaan- C9H20 *dekaan- C10H22 5) Süsiniku oksüdatsiooniastme arvutamine ühendis *C-H =-1 *C-C =0 *C-O =+1 *C=O =+2 6) Alkoholide ja karboksüülhapete valemite äratundmine CH3OH- metanool C2H5OH- etanool C3H7OH- propanool C4H9OH- butanool C5H11OH- pentanool C6H13OH- heksanool C7H15OH- heptanool C8H17OH- oktanool C9H19OH- nonanool C10H21OH- dekanool
7C Struktuuriteooria · Igal ühendil on kindel koostis ja temale omane ehitus · Ühendi omadused sõltuvad molekuli koostisest ja aatomite paigutusest e. Ehitusest · Aatomite paigutuse muutmine muudab järslult ainete omadusi Süsivesinikud C x+ Hy Alkaanid Alkeenid Alküünid Alkaanid 1) Metaan CH4 2) Etaan C2H6 3) Propaan C3H8 4) Butaan C4H10 5) Pentaan C5H12 6) Heksaan C6H14 7) Heptaan C7H16 8) Aktaan C8H18 9) Nonaan C9H20 10) Dekaan C10H22 Alkeenid Cn+H2n ; -een 2) Eteen C2H4 3) Propeen C3H6 CH2=CH-CH3 4) Buteen C4H8 CH3-CH=CH-CH3 5) Penteen C5H10 CH3-CH=CH-CH2-CH3 6) Hekseen C6H12 CH3-CH=CH-CH2-CH3 7) Hepteen C7H14 CH3-CH2-CH2-CH=CH-CH2-CH3 8) Okteen C8H16 CH3-CH2-CH2-CH=CH-CH2-CH2-CH3 9)Noneen C9H18 CH3-CH2-CH2-CH=CH-CH2-CH2-CH2-CH3
butaanhape C4H10 prutaan C4H8 buteen C4H6 butüün C4H9OH butanool C3H7COOH petaanhape C5H12 pentaan C5H10 penteen C5H8 pentüün C5H11OH pentanool C4H9COOH heksaanhape jne jne jne jne Jne 1. Süsiniku aatomite arv igas rühmas suureneb ülevalt alla liikudes 1 võrra ja vesiniku aaotomite arv kahe võrra. 2
Nt Metaani molekuli C-H side katkemine reaktsioonis, moodustub metüülradikaal ja vedinikradikaal ALKAAN NIMETUS ALKÜÜLRÜHM -NIMETUS CH4 Metaan CH3 Metüül- C2H6 Etaan C2H5 Etüül- C3H8 Propaan C3H7 Propüül- C4H10 Butaan C4H9 Butüül- C5H12 Pentaan C5H11 Pentüül- C6H14 Heksaan C6H13 Heksüül- C7H16 Heptaan C7H15 Heptüül- C8H18 Oktaan C8H17 Oktüül- C9H20 Nonaan C9H19 Nonüül- C10H22 dekaan C10H21 Deküül- 1
Keemia Süsivesinikud 1) Milliseid aineid nimetatakse süsivesinikeks? Süsivesinikud on liitained, mille molekul koosneb süsinikust ja vesinikust. 2) Millised ained on alkaanid, nende üldvalem + nimetused Alkaanid on küllastunud süsivesinikud, mille molekulis süsiniku aatomite vahel on ühekordne kovalentne side. Üldvalem: CnH2n+2 Nimetused: CH4 metaan C2H6 etaan C3H8 propaan C4H10 butaan C5H12 pentaan C6H14 heksaan C7H16 heptaan C8H18 oktaan C9H20 nonaan C10H22 dekaan 3) Millised ained on alkeenid, nende üldvalem + nimetused Alkeenid on küllastamata süsivesinikud, mille molekulis süsiniku aatomite vahel on üks kaksikseos. Üldvalem: CnH2n Nimetused tuletatakse vastavast alkaanist, kus lõpp aan asendatakse een'iga. 4) Millised ained on alküünid, nende üldvalem + nimetused
......................................................................................... 11 Kasutatud materjalid...........................................................................................................................12 3 Sissejuhatus Penteen kuulub alkeenide perekonda, valemiks on C5H12,Penteeni omadused on samad, mis tema perekonnal ehk alkeenidel. Alkeenideks küllastumata süsivesinikke, kus süsiniku aatomite vahel esineb üks kovalentne kaksikside. Alkeenid on küllastumata süsivesinikud, mille üldvalemiks on CnH2n. Alkeenide nimetuse tunnuseks on lõpuliide een. Küllastunud ainetel on süsinikahelas kõik ühekordsed sidemed ja iseloomulikud on asendumisreaktsioonid. Küllastumata ühenditel on süsinike vahel
Füüsikalised omadused:alkaanid on mittepolaarsed ühendid,ei lahustu vees.C 1-C4on toatemp gaasiline C5-C10 on toatemp vedelikud ...on toatemp tahked e. parafiinid.Vedelad alkaanid on head lahustid rasvadele,nad on lõhnatud,värvitud.Gaasilised alkaanid on narkootilised ained. Keemilised omadused:CH4+2O2--CO2+2H2O ; C5H12+8O2--5CO2+6H2O ; C4H10+6,5O2-- 4CO2+5H2O pikema ahelaga alkaane saab lõhkuda väiksemaks kasutades katalüsaatori ja temp toimel. Seda nim krakkimiseks.kasutatakse naftast suurema hulga bensiini saamiseks. CH3-CH2--CH2-CH2-CH3--- ; reageerimine halogeenidega.asendusreaktsioon CH 4+Cl2-- CH3Cl+HCl ; ta onradikaalne ahelreaktsioon(radikal:üksiku vab elektroniga aktiivne osa) TAHKE KÜTUS: looduslik-kivisüsi,põlevkivi jm. tehis-turbabrikett,koks
Nimetus CH4 (keemist. metaan C6H14(keemist. heksaan -161) 69) C2H6(keemistemp etaan C7H16(keemist. heptaan -89) 98) C3H8(keemistemp propaan C8H18(keemist. oktaan -42) 126) C4H10(keemist- butaan C9H20(keemist. nonaan 0,5) 151) C5H12(keemist. pentaan C10H22(keemist.1 dekaan 36) 74) Radikaal – osake, millel on üks paardumata elektron. Alkaanide tüüpilised reaktsioonid on pürolüüs ja oksüdeerumine. Elektrofiil on tühja orbitaali ja positiivse laengu osake. Nukleofiil on vaba elektronpaariga osake ja kannab negatiivset laengut. Alkaanide füüsikalised omadused: Homoloogilises reas C aatomite
Graafikute koostamine ja järelduste tegemine (Nt lineaarne sõltuvus) 6. Individuaalne ja keskmine o.a. 7. Kütteväärtuse hindamine, põlemisvõrrandid. Alkaanide põlemine hapniku reageerimine ainega, mille tulemusel eraldub soojus ja valgus. Kuidas hinnata aine kütteväärtust? On vaja leida selle aine o.a. muutus, kasutades keskmisi o.a.-id. 2,5 C5H12 -> IVCO2 2 2/7 C7H16 Mida negatiivsem on C o.a., seda suurem on kütteväärtus. Kõige suurem kütteväärtus on metaanil (C o.a. on IV). 8. Radikaal vaba elektroniga osake, millel on suur energia. (Radikaalil on paardumata elektron!) Tekkevõimalused: Alkaan reageerib hapnikuga/ klooriga/ broomiga.
ahelatega ühenditeks Fraktsioneeriv destillatsioon - on destillatsioonimeetod kasutades destillatsioonikolonni, milles toimub korduv aurustumine ja kondensatsioon. Alkaanide nimetused/valemid (graafilised, tasapinnalised, lihtsustatud) Tähtsamad alkaanid: CH4 metaan CH3 metüül C2H6 etaan CH3CH2 etüül C3H8 propaan CH3CH2CH2 propüül C4H10 butaan CH3CH2CH2CH2 butüül C5H12 pentaan C6H14 heksaan C7H16 heptaan C8H18 oktaan C9H20 nonaan C10H22 dekaan Isomeerid (Koostamine, füüsikaliste omaduste tuletamine ja põhjendamine) Isomeeride struktuur on erinev, siis erinevad on ka nende omadused ehk omadused sõltuvad aine struktuurist. Füüsikalised omadused: 1. Sulamistemperatuur 2. Keemistemperatuur 3. Tihedus Põlemisreaktsioonid Põlemisel ained oksüdeeruvad hapniku toimel ehk tekivad OKSIIDID Lihtained
Need ühendid on hüdrofoobsed, neist koosnevad materjalid põlevad hõlpsalt ning annavad asendusreaktsioone. Põhiliseks leidumisallikaks on nafta. Täielik põlemine: CH4 + 1,5O2 CO2 + 2H2O Mittetäielik põlemine: 2CH4 + 3O2 CO2 + 4H2O + C Halogeenidega (VIIA): CH4 + Br2 CH3Br + HBr Vesinikhalogeenidega: CH4 + HBr CH3Br + H2 Oksüdeeerumine: 2CH4 + O2 2CH3OH Homoloogiline rida: 1. metaan CH4 2. etaan C2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptaan C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22
Valem Tihedus m3/kg Kütteväärtus Koostis % kJ/m3 Metaan CH4 0,716 35820 97,1 Etaan C2H6 1,342 63750 0,3 Propaan C3H8 1,967 91260 0,1 Butaan C4H10 2,593 118650 - Pentaan C5H12 3,218 146080 - Lämmastik N2 1,251 2,4 Süsinikdioksiid CO2 1,97 0,1 = 100 Ülesanne 1 Alumine kütteväärtus Põlemiseks teoreetiliselt vajalik õhuhulk Kolmeaatomilise gaaside teoreetilie maht Veeauru teoreetiline maht Võtan dq=10 Lämmastiku teoreetiline maht
8. Mis on DDT? Miks teda vaja on? Vastus: DDT on diklorodifenüültrikloroetaan. Kasutatkse putukatõrjena. 9. Milline on DDT kahjulik toime inimesele? Vastus: Jah, nad kahjustavad selgroogsete kesknärvisüsteemi ja eriti maksa. On ilmenud ka DDT mutageenne ( päriliku struktuuri muutusi esile kutsuv) ja kantsereogeenne(vähkitekitav) toime. Alkaanid: CH4- Metaan C2H6- Etaan C3H8- Propaan C4H10-Butaan C5H12- Pentaan C6H14- Heksaan C7H16- Heptaan C8H18-Oktaan C9H20-Nonaan C10H22-Dekaan
koos rühma nimetusega eesliiteid di-, tri-, tetra- jne. Summaarne valem Nimetus Tuletatud alküülrühm CH4 Metaan CH3 metüül C2H6 Etaan C2H5 etüül C3H8 Propaan C3H7 propüül C4H10 Butaan C4H9 butüül C5H12 Pentaan C5H11 pentüül C6H14 Heksaan C6H13 heksüül C7H16 Heptaan C7H15 heptüül C8H18 Oktaan C8H17 oktüül C9H20 Nonaan C9H19 nonüül C10H22 Dekaan C10H21 deküül
mitmiksidemeid) Alifaatne ( ka atsükliline) molekulis pole tsükleid Alkaanid jagunevad normaal(ahelaga) alkaanideks sirgeks pole teda ilus kutsuda , sest nurk on ikkagi ~1100 ja hargneva ahelaga alkaanideks Nimetused Normaalahelaga alkaane nimetatakse Metaan CH4 Pentaan C5H12 Nonaan C9H20 Etaan C2H6 Heksaan C6H14 Dekaan C10H22 Propaan C3H8 Heptaan C7H16 Undekaan C11H24 Butaan C4H10 Oktaan C8H18 Dodekaan C12H26 jne Hargneva ahela korral loetakse pikim ahel peaahelaks ja muud ahelad kõrvalahelateks Peaahel määrab nime lõpu
Iga side vesinikuga alandab süsiniku oksüdatsiooniastet ühe ühiku võrra, iga side hapniku, lämastiku või mõne muu elektronegatiivsema aatomiga tõstab seda ühe ühiku võrra Orgaaniliste ühendite omadused 1Sisaldavad süsinikku ja vesinikku C arvsõna Alkaani valem arv 1 Meta CH4 2 Eta C2H6 3 Propa C3H8 4 Buta C4H10 5 Penta C5H12 6 Heksa C6H14 7 Hepta C7H16 8 Okta C8H18 9 Nona C9H20 10 deka C10H22 2Üldiselt küllaltki suure molaarmassiga 3Aatomite vahel on kovalentne side (side, mis tekib ühise elektronpaari moodustumise tõttu) 4Vesilahused ei juhi elektrit 5Keemilised reaktsioonid kulgevad üldiselt aeglaselt 6Lagunevad juba 400 0C juures 7Põlevad (saadustena on alati CO2 ja H2O) alkaanide füüs. omadused
negatiivset laengut (:NH3, H2:O:, CH3COO, Cl). *Elektrofiiliks nimetatakse osakest, mis omab tühja orbitaali või positiivset laengut (Na+, K+, Li+,H+). V = n * Vm n = m/M m= n x M n= V/Vm = m/V M molaarmass Vm molaarruumala (22,4) m mass n moolide arv tihedus mol/mol; m/M; V/Vm (gaas); V/M (vedelik) 1. metaan CH4 2. etaan C2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptaan C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22
Kuid glükoosi vesilahuses eksisteerib üksnes väike osa glükoosist aldehüüdi kujul. Lineaar Alkeeni sed alka Alküünid d anid nimetus valem nimetus valem nimetus Valem Metaan CH4 Etaan C2H6 Eteen C2H4 Etüün C2H2 Propaan C3H8 Propeen C3H6 Propüün C3H4 Butaan C4H10 Buteen C4H8 Butüün C4H6 Pentaan C5H12 Penteen C5H10 Pentüün C5H8 Heksaan C6H14 Hekseen C6H12 Heksüün C6H10 Heptaan C7H16 Hepteen C7H14 Heptüün C7H12 Oktaan C8H18 Okteen C8H16 Oktüün C8H14 Nonaan C9H20 Noneen C9H18 Nonüün C9H16 Dekaan C10H22 Dekeen C10H20 Deküün C10H18 Karboksüülhapped on orgaanilises keemias happed, mis sisaldavad karboksüülrühma (COOH). CH3CH3 (etaan) -> CH3COOH (etaanhape). Palju on kasutusel ka triviaalnimetusi, eriti biokeemias.
Need jaotatakse omakorda a)hargnemata ahelaga ehk normaalalkaanid ja b)hargnenud ahelaga . 2) tsüklilised alkaanid ehk tsükloalkaanid , üldvalemiga C nH2n. Nomenklatuur on aine struktuuri ja aine nimetust siduvate reeglite kogu. 1. Hargnemata ahelaga atsükliliste alkaanide valemid ja nimetused ( C nH2n+2 -aan ) 1) CH4 metaan 2) C2H6 etaan CH3-CH3 3) C3H8 propaan CH3-CH2-CH3 4) C4H10 butaan CH3-CH2-CH2-CH3 5) C5H12 pentaan 6) C6H14 heksaan 7) C7H14 heptaan 8) C8H18 oktaan 9) C9H20 nonaan 10) C10H22 dekaan 2. Tsükloalkaanide valemid ja nimetused (C nH2n) tsüklopropaan tsüklobutaan tsüklopentaan tsükloheksaan ∆ □ ⌂ (graafilised kujutised) 3. Hargnenud ahelaga alkaanide nimetamine valemi järgi 1) asendusrühm ehk alküülrühm, tähis -R, üldvalem Cn H2n+1
5. Orgaaniliste ainete põlemise saadused. Orgaaniline aine + O2 CO2 + H2O + energia (täielik põlemine) Orgaaniline aine + O2 (vähese hapniku korral) CO (vingugaas) + H2O + natuke energiat REEGEL! Suurema kütteväärtusega põlevad need kütused, mille koostises oleva süsiniku o-a on väikseim. 6. Alkaanide koostis. Alkaanid koosnevad C ja H aatomitest ning süsiniku aatomite vahel on ainult üksiksidemed. CH4 metaan C5H12 pentaan C9H20 nonaan C2H6 etaan C6H14 heksaan C10H22 dekaan C3H8 propaan C7H16 heptaan C4H10 butaan C8H18 oktaan 7. Alkaanide leidumine looduses. Metaan- maagaasi koostises. Propaan vedelgaasi koostises. 8
(IUPAC Ineternational Union of Pure and Applied Chemistry). Alkaani tunnusteks on järelliide aan (metaan, etaan, propaan, butaan, pentaan jne...). Sõnatüvi (met-, et-, prop-, but-, pent-) kirjeldab süsinikahela pikkust. Alkaan Nimetus Sõnatüvi CH4 metaan met- C2H6 etaan et- C3H8 propaan prop- C4H10 butaan but- C5H12 pentaan pent- C6H14 heksaan heks- C7H16 heptaan hept- C8H18 oktaan okt- C9H20 nonaan non- C10H22 dekaan dek- C11H24 undekaan undek- C12H26 dodekaan dodek- C13H28 tridekaan tridek- C14H30 tetradekaan tetradek-
LINE Propaan C3H8 Propeen C3H6 Propüün C3H4 RIDA CH3 CH2 CH3 CH3 =CH CH3 CH C CH3 Keemia 2012 Keemia 2012 Butaan C4H10 Buteen C4H8 Butüün C4H6 CH3 CH2 CH2 CH3 CH2 = CH CH2 CH3 CH C CH2 CH3 Pentaan C5H12 Penteen C5H10 Pentüün C5H8 CH3 CH2 CH2 CH2 CH3 Heksaan C6H14 Hekseen C6H12 Heksüün C6H10 CH3 CH2 CH2 CH2 CH2 CH3 Heptaan C7H16 Hepteen C7H14 Heptüün C7H12 CH3 CH2 CH2 CH2 CH2 CH2 CH3
7 Krakkimine Krakkimisel kasutatakse lähtematerjalidena naftafraktsioone, mille keemispind on üle 200 kraadi. Krakkimise teel saavutatakse bensiini saagise ligi kolmekordne tõus, kusjuures krakkbensiin on isegi väärtuslikum kui tavaline naftabensiin. Termiline krakkimine annab paljude süsivesinike segu. Krakkimist püütakse läbi viia nii, et tekiks vähem alkeene, kuna nad polümeeruvad kütuse säilitamisel vaigutaoliseks aineks. C10H22 termiline krakkimine-> C5H12 + C5H10 CnH2n+2 alkaan CnH2nalkeen Katalüütiline krakkimine võimaldab termilise lagunemise protsesse suunata soovitavate reaktsioonide suunas. C10H22 katalüütiline krakkimine-> CH4 + C9H18
Krakkimisel kasutatakse lähtematerjalidena naftafraktsioone, mille keemispind on üle 200 kraadi. Krakkimise teel saavutatakse bensiini saagise ligi kolmekordne tõus, kusjuures krakkbensiin on isegi väärtuslikum kui tavaline naftabensiin. Termiline krakkimine annab paljude süsivesinike segu. Krakkimist püütakse läbi viia nii, et tekiks vähem alkeene, kuna nad polümeeruvad kütuse säilitamisel vaigutaoliseks aineks. C10H22 termiline krakkimine-> C5H12 + C5H10 CnH2n+2 alkaan CnH2nalkeen Katalüütiline krakkimine võimaldab termilise lagunemise protsesse suunata soovitavate reaktsioonide suunas. C10H22 katalüütiline krakkimine-> CH4 + C9H18 Kasutus Naftat kasutatakse peamiselt kütuse ja ligi 10% ka keemiatööstuse toorainena. Vedelkütus ja nafta kerged fraktsioonid on naftakeemiatööstuse tooraine. Parafiine kasutatakse paberitööstuses ja meditsiinis. Raskeid destillaatidest valmistatakse
vesiniku aatom) nimetus tuletatakse süsivesiniku nimetuse lõpu aan asendamisel lõpuga üül (alkaan alküül, etaan etüül, pentaan pentüül). Alkaan (CnH2n+2) Vastav alküülradikaal (CnH2n+1) CH4 metaan CH3 metüül C2H6 etaan C2H5 etüül C3H8 propaan C3H7 propüül C4H10 butaan C4H9 butüül C5H12 pentaan C5H11 pentüül C6H14 heksaan C6H13 heksüül C7H16 heptaan C7H15 heptüül C8H18 oktaan C8H17 oktüül C9H20 nonaan C9H19 nonüül C10H22 dekaan C10H21 detsüül · Hargnenud ahelaga alkaane nimetatakse ahela järgi, milles süsiniku aatomite arv on suurim (peaahela järgi). · Kõrvalahelate nimetamiseks nummerdatakse peaahel alates sellest otsast, kus kõrvalahela
H H Isomeeria · Isomeeria on nähtus, kus ainetel on ühesugune elementkoostis ja molekulmass, kuid erinev struktuur (ehitus) ning seetõttu ka erinevad omadused. Alkaanid · Alkaanid on küllastunud süsivesinikud, mille molekulis on süsiniku aatomite vahel üks 3) C3H8 - propaan ühekordne kovalentne side. 4) C4H10 - butaan · Üldvalem CnH2n+2 5) C5H12 - pentaan · Nimetuse lõpp -aan · Homoloogiline rida 6) C6H14 - heksaan 1) CH4 - metaan 7) C7H16 - heptaan 2) C2H6 - etaan 8) C8H18 - oktaan 9) C9H20 - nonaan 10) C10H22 - dekaan · Füüsikalised omadused: esimesed 4 liiget on gaasid, liikmed 5-16 on vedelikud ja ülejäänud alkaanid tahked. Kõik alkaanid
Kütteväärtus- näitab, kui palju soojusenergiat annab kindle kogus küttust täielikul põlemisel. Kütusena võib kasutada igasuguseid aineid või materjale, mille koostises on mõni madalama o-a elemendi aatom. Kütteväärtus on seda kõrgem, mida madalam on elemendi o-a ehk mida rohkem on ta vesiniku ühenditega seotud. Kõige enam kasutame süsiniku kütuseid, sest see on odav ja kättesaadav. 1. Gaasiline kütus (põlevad täielikult) CH4, C2H6, C3H8, C4H10 2. Vedelkütused (nafta) C5H12, C9H20 Kütteväärtus on väiksem, koos maagaasiga põletamisel ei teki mingeid jääke. 3. Tahked kütused (põlemine on mittetäielik, tuhk) Kütteväärtus on kõige väiksem. Põlemine- kiiresti kulgev oksüdatsioon, milles eraldub palju soojust ja ka valgust. Leek tekib ainult siis, kui põlevad gaasid ja aurud. Kütteväärtuse puhul on tähtis see, kui palju on kütuse koostises mittepõlevaid lisandeid. Toit- on elusorganismidele nii kütuseks kui ka ehitusmaterjaliks.
Alkaan Nimi Alküülrühm Alküülrühma nimet. CH4 Metaan CH3 Metüül C2H6 Etaan C2H5 Etüül C3H8 Propaan C3H7 Propüül C4H10 Butaan C4H9 Butüül C5H12 Pentaan C5H11 Pentüül C6H14 Heksaan C6H13 Heksüül C7H16 Heptaan C7H15 Heptüül C8H18 Oktaan C8H17 Oktüül C9H20 Nonaan C9H19 Nonüül C10H22 Dekaan C10H21 Deküül 81. Alkaani tunnuseks on liide aan 82
Üh. nimetus Molekuli valem Struktuurivalem Olek 25 oC Keemistemperatuur oC juures Metaan CH4 CH4 gaas - 161, 5 Etaan C2H6 CH3CH3 gaas - 88, 0 Propaan C3H8 CH3CH2CH3 gaas - 42, 2 Butaan C4H10 CH3CH2CH2CH3 gaas - 0, 5 Pentaan C5H12 CH3CH2CH2CH2CH3 vedelik 36, 0 Heksaan C6H14 CH3CH2CH2CH2CH2CH3 vedelik 69, 0 Alkaanide füüsikalised omadused muutuvad homolooglises reas pidevalt ja seaduspäraselt. Alates pentaanist kuni pentadekaanini on alkaanid vedelad ja alates heksadekaanist C 16 tahked ühendid. Hargnenud ahelaga ühenditel on madalam keemistemperatuur kui sama süsiniku aatomite arvuga hargnemata ahelaga ühenditel.
* Alkaanide üldvalem: CnH2*n+2 * Alkaanide homoloogiline (ühetaoline) rida iga järgnev valem suureneb ühe süsiniku ja kahe vesiniku võrra. * Alkaane saab toornaftast. * Kuni neljandani on alkaanid gaasilised, viies kuni viieteistkümnes on vedelad ning kuueteistkümnendast edasi on nad tahked ehk parafiinid. * Erinevad alkaanid: -) CH4 metaan (maagaas) -) C2H6 etaan (maagaasi lisandiks) -) C3H8 propaan (balloonigaas) -) C4H10 butaan (baloonigaasil lisandiks) -) C5H12 pentaan -) C6H14 heksaan -) C7H16 heptaan -) C8H18 oktaan -) C9H20 nonaan -) C10H22 dekaan * Need nimetused kehtivad ainult hargnemata ahelaga alkaanide puhul. Hargnenud ahelaga alkaanide nimetamine: 1) Leitakse kõige pikem süsinikahel (ei pea olema sirgelt, peaasi, et süsinikud oleks omavahel seotud), mida nimetatakse peaahelaks ehk tüviühendiks. 2) Süsinikud, mis jäävad peaahelast välja moodustavad asendusrühmad ehk kõrvalahelad.
Tüüpilisemateks oksüdeerijateks loetakse kaaliumpermanganaadi (KMnO4) lahust või broomivett. Tõestamisreaktsioon: 3C2H4 + 2KMnO4 -> 2KMnO4+ 4H2O -> 2MnO2 + 2KOH + OH-CH2-CH2-OH Benseeni ja tsüklohekseeni reageerimise võrdlus broomivee ja kaaliumpermanganaadi lahusega.Benseen viimastega ei reageeri, mistõttu nendele iseloomulik värvus säilub. a) Täielik põlemine C5H8 + 7O2 ->5CO2 + 4H2O b) Mittetäielik põlemine C5H12 + 3O2 ->5Co + 6H2O Eteen põleb etaaniga võrreldes palju heledama leegiga, kuna ta sisaldab protsentuaalselt rohkem süsinikku. Süsiniku osakesed ei jõua leegis kiiresti ära põleda, mille tagajärjel hööguvad söeosakesed muudavadki leegi valgustavamaks. 8 2) Liitumisreaktsioonid (elektrofiilsed liitumisreaktsioonid) a) Liitumisreaktsioonid vesinikuga (hüdrogeenimine)
ladinakeelsetest numbritest. C-aatomite arv Valem Alkaan Alküülasendaja Alküülasendaja valem 1 CH4 metaan metüül -CH3 2 C2 H6 etaan etüül -C2H5 3 C3H8 propaan propüül -C3H7 4 C4H10 butaan butüül -C4H9 5 C5H12 pentaan pentüül -C5H11 6 C6H14 heksaan heksüül -C6H13 7 C7H16 heptaan heptüül -C7H15 8 C8H18 oktaan oktüül -C8H17 9 C9H20 nonaan nonüül -C9H19 10 C10H22 dekaan deküül -C10H21
Valents näitab, mitu kovaletset sidet võib antud aatom moodustada. Kui element on ühekordse sama elemendiga on tegemist kovalente üksisksidemega. Kahe elektronpaari abil tekib kovalentne kasksiksida, kolme elektronpaariga kolmikside Nende põhimõtete abil saab kirjutada struktuur valemeid. 1. Metaan CH4 2. Etaan C2H6 3. Propaan C3H8 4. Butaan C4H10 5. Pentaan C5H12 6. Heksaan C6H14 7. Heptaan C7H16 8. Oktaan C8H18 9. Nonaan C9H20 10. Dekaan C10H22 Molekul valem: näitab millistest aatomitest koosneb valem Klassikaline struktuur valem Lihtsustatud struktuur valem, ühe reapeal Kriipsu otsad ja murde kohad on süsiniku aatomid. Ning kriips on side.Lihtsustatud, klassikaline ja kraafiline kujund oktaani kohta. C8H18
1,08 103 kg 97. 3,40,4 6,40,15 171. C10H8 211. 5,8% 98. 3,1,4 3,4,6 133. 1,01 1014 molekuli 172. C2H5Br 212. CF4 99. 1,12 2,2,3 134. 896 dm3 173. C2H2 213. 35,7% 100. 40 mol 135. 6,02 1018 aatomit 174. C8H8 214. 44,8 dm3 101. 5 mol CO2 , 10 mol SO2 136. 24,8 g 175. C5H12 215. 7,29% 102. 900 mol H2 , 600 mol O2 137. 98 cm3 176. C3H8 216. 57,2 g 103. 500 mol 138. 3 dm3 SO2 , 7 dm3 SO3 177. C3H6 217. 88,9% Cu , 11,1% Fe 104. 1,24 mol H2SO4 , 139. 18,5% NaOH , 178. C3H8 218. 47 dm3 3,2 mol H2O 18,5% KOH 179. C4H8Br2 219. 0,05 mol 105. 0,154 mol 140
Süsinik on võimeline moodustama üksteisega vahetult seotud aatomitest väga pikki ja püsivaid ahelaid. Isobutaani molekulis on süsinikahel hargnenud. Kinnine ring e. tsükkel. Süsivesinikke, mis sisaldavad ainult C-C- ja C-H-üksiksidemeid, nimetatakse alkaanideks. Alkaanid on süsivesinikud, milles süsinikuaatomite vahel on ühekordne side. Alkaane nimetatakse süsinikuaatomite arvu järgi. CH4 - metaan C2H6 - etaan C3H8 - propaan C4H10 - butaan C5H12 - pentaan C6H14 - heksaan C7H16 - heptaan C8H18 - oktaan C9H20 - nonaan C10H22 dekaan Mis on polümeer? Alkaani, mille süsinikahelas on mitu tuhat või mitukümmend tuhat süsiniku aatomit, nimetatakse polüetüleeniks. Polüeteen koosneb tuhandetest CH2-lülidest, mis on üksteise külge seotud täpselt samuti nagu butaanis või parafiinides. Polümeerideks nimetatakse aineid, mille suured molekulid koosnevad väga paljudest enamasti ühesugustest üksteisega seotud väikeste