Keemia: oksiidid, alused, soolad, happed. 1. Oksiidid Koostis: koosnevad kahest elemendist, üks on hapnik. AlO3; CaO Nimetused: a. metallioksiidide puhul märgitakse esikohale metalli nimi, tesele kohale oksiid, vahele metalli o-a, kui o-a on muutuv. Fe2O3 raud(III)oksiid b. mittemetallide puhul kasutatakse eesliiteid. CO2 süsinikdioksiid, P2O5 difosfor- pentaoksiid. Saamine: 1.lihtainete ühinemine hapnikuga: C + O2 => CO2 2. liitainete põlemine: CH4 + 202 => CO2 + 2H2O 3. liitainete lagunemine: CaCO3 => CaO + CO2 Oksiidide liigid: · Sooleatekitajad (reageerivad hapete ja leelistega, annavad soolad) · Mittesoolatekitajad (inertsed, ei reageeri hapete ja leelistega) NO, CO Soolatekitajad jagunevad: 1. aluselised 2. happelised 3. amforteersed 1. Aluselised oksiidid: Metallioksiidid, kui metalli o-a on 1,2,3, näiteks CuO. Keemilised omadused: 1. Mõned neist moodustavad veega aluse (...
HAPPELISED JA ALUSELISED OKSIIDID. OKSIIDIDE SAAMINE Eesmärgid · Liigitan oksiide aluselisteks ja happelisteks. · Tean, et happelistest oksiididest. reageerivad veega ainult aktiivsete metallide oksiidid. · Kirjutan ja tasakaalustan reaktsioonivõrrandid oksiidi reageerimisel veega. · Nimetan oksiidide saamisvõimalusi (2). Metallioksiid ja mittemetallioksiid Leia järgmisest loetelust metallioksiidid ja mittemetallioksiidid: CaO, SiO2, Na2O, Cr2O3, N2O3, B2O3, CrO3, Fe2O3, BaO, MnO2, CO, Cl2O7, Al2O3, CuO, H2O. Oksiidide liigitamine · Oksiidid liigitatakse nende keelimiste omaduste alusel. · Enamik oksiide on kas aluselised või happelised. · TV lk 17 E (1) Aluselised oksiidid ...on aluseliste omadustega, nad reageerivad hapetega. Enamus metallioksiide on aluseliste omadustega. Aktiivsete metallide (I ja IIA rühm) oksiidid on tugevalt aluselised. Vähemaktiiv...
Oksiidid Oksiidid koosnevad kahest elemendist, millest üks on hapnik. Oksiidide liigitus koostiselementide järgi: · Metallioksiidid Na2O, CaO, CuO, Fe2O3 · Mittemetallioksiidid CO2, CO, SiO2, P4O10 Nimetuste andmine oksiididele: · Metallioksiidide nimetamine: a) Püsiva oksüdatsiooniastme korral metalli nimi+oksiid K2O kaaliumoksiid, Al2O3 alumiiniumoksiid b) Muutuva oksüdatsiooniastme puhul metalli nimi(oksüdatsiooniaste)+oksiid FeO raud(II)oksiid Cu2O vask(I)oksiid Fe2O3 raud(III)oksiid CuO vask(II)oksiid Mittemetallioksiidide nimetused: · Indeksite(sümboli taga all) nimetamisel kasutatakse eesliiteid: 1 (mono) 6 heksa 2 di 7 hepta 3 tri 8 okta 4 tetra 9 nona 5 penta 10 deka N2 O5 dilämmastikpentaoksiid NO2 lämmastikdioksiid Anna nimetus oksiididele: · CaO P2O5 · Al2O3 N 2O · CuO ...
Oksiidid Liigitus keemiliste omaduste järgi: 1. ALUSELISED OKSIIDID: a) REAGEERIMINE VEEGA - tugevalt aluselised on leelis- ja leelismuldmetallide (IA ja IIA rühm) oksiidid. Reageerivad väga aktiivselt veega ning saadusena tekib leelis (tugevalt aluseline hüdroksiid). Li2O, K2O, BaO, Na2O, CaO CaO + H2O → Ca(OH)2 - nõrgalt aluselised oksiidid on vähemaktiivsete metallide oksiidid. Ei reageeri veega. CrO, Fe2O3, FeO, NiO, CuO, ZnO b) REAGEERIMINE HAPETEGA - aluseline oksiid + hape= sool+vesi Tugevalt aluseliste oksiidide korral toimub reaktsioon väga energiliselt. Nõrgalt aluselise oksiidide korral vajalik kuumutamine. BaO + 2HCl →BaCl2 + H2O 2. HAPPELISED OKSIIDID a) REAGEERIMINE VEEGA - enamik reageerib veega, moodustades vastava happe. SO2, NO2, CO2, P4O10, SO3 Veega ei reageeri SiO2 (liiv...
OKSIIDID (R 68-75) Tööleht 1. OKSIIDID on ained, mis koosnevad kahest elemendist, millest üks on hapnik oksüdatsiooniastmega II. 2. Oksiidide liigitamine: 3. ALUSELISED OKSIIDID e tavaliselt metallioksiidid on oksiidid, mis reageerivad hapetega. · Aluselised oksiidid jagunevad: 1. tugevalt aluselised oksiidid, mis reageerivad veega ja tekib alus 2. nõrgalt aluselised oksiidid, mis ei reageeri veega 4. HAPPELISED OKSIIDID e tavaliselt mittemetallioksiidid on oksiidid, mis reageerivad alustega · Happelised oksiidid jagunevad: 1. Happelised oksiidid, mis reageerivad veega ja tekib hape 2. Happelised oksiidid, mis ei reageeri veega, aga millele vastab mingi hape 5. AMFOTEERSED OKSIIDID on väheaktiivsed oksiidid, mis võivad reageerida nii hapete kui alustega, ei reageeri aga veega. 6. NE...
Keemia oksiid koosneb kahest elemendist, millest üks on hapnik Aluselised oksiidid on aluseliste omadustega, reageerivad hapetega Happelised oksiidid- on happeliste omadustega, reageerivad alustega Tugeval aluseliste oksiidide - reageerimisel veega tekivad tugevad alused ehk leelised. Enamiku happeliste oksiidide reageerimisel veega tekib vastav hape. Veega ei reageeri nõrgalt aluselised ning ka mõned happelised oksiidid nt SiO2 Oksiidide põhilised saamisvõimalused : 1. vastavate lihtainete reageerimine hapnikuga, 2. suhteliselt ebapüsivate hapnikku sisaldavate ühendite lagunemine Aluselised oksiidid on metall oksiidid(ainult I ja II A rühma metallid reageerivad veega) ja happelised oksiid on mittemetal oksiid. SO2 ja CO2 saamise võimalused: Põlemine,hingamine Hape aine, mis annab lahusesse vesinikioone Hape molekulid jagunevad lahuses vesinikioonideks ja happe anioonideks Ha...
Oksiidid Oksiidid on ained mis koosnevad kahest elemendist, millest üks on hapnik (oksüdatsiooniastmes -2). Oksiidide saamine Lihtainete vaheline reaktsioon Paljusid oksiide võib saada lihtaine reageerimisel hapnikuga. Näide: C + O2 =CO2 Hüdroksiidide ja karbonaatide lagundamine kuumutamisel Paljusid oksiide on võimalik saada neile vastavate hüdroksiidide või ka mõnede soolade(eelküige karbonaatide) lagundamisel kõrgel temperatuuril. Näide: Cu(OH)2 = CuO + H2O CaCO3= CaO + CO2 Liigitus Oksiide liigitatakse aluselisteks, happelisteks, amfoteerseteks ja neutraalseteks. Aluselised oksiidid Aluselisteks oksiidideks nimetatakse oksiide, mis reageerivad hapetega. Aktiivsete metallide(leelis-ja leelismuldmetallide) oksiidid on tugevalt aluselised. Nendele vastavad hüdroksiidid on vees hästilahstuvad tugevad alused ehk leelised. Vähemaktiivsete metallide oksiidid on nõrgalt aluselise. Nõrgalt aluselistele oksiididele vastavad hüd...
OKSIIDID OKSIIDI mõiste: Liitained, mis koosnevad kahest elemendist millest üks on hapnik. CO2 OKSIIDID TEKIVAD: Mittemetall + hapnik= mittemetallioksiid. C + O2 = CO2 Metall + hapnik = metallioksiid 2Ca + O2 = 2CaO OKSIIDE LIIGITATAKSE Happelised oksiidid. Aluselised oksiidid. Enamasti mittemetalli Enamasti oksiidid. metallioksiidid. SO2, SO3, CO2 Al2O3,CuO,CaO HAPPELISTE OKSIIDIDE KEEMILISED OMADUSED happeline oksiid + vesi = hape CO2 + H2O = H2CO3 happeline oksiid + alus = sool + vesi CO2 + 2NaOH = Na2CO3 + H2O happeline oksiid + aluseline oksiid= sool CO2 + CaO = CaCO3 ALUSELISTE OKSIIDIDE KEEMILISED OMADUSED aluseline oksiid + vesi= alus CaO + H2O = Ca(OH)2 aluseline oksiid + hape = sool + vesi CaO + 2HCl = CaCl2 + H2O aluseline oks...
OKSIIDID - TK 1. A. Tõmba joon alla aluseliste oksiidide valemitele. BaO, NO, CO2, SnO, Cl2O7, Na20, MgO, B2O3 B. Vali allajoonitutest üks ning koosta ja tasakaalusta võrrand selle oksiidi reageerimisest veega. BaO + H2O = Ba(OH)2 2. Kirjuta ühe toatemperatuuril tahke oksiidi valem ja nimetus. Fe3O2 = raud(III)oksiid 3. Kirjuta järgnevate oksiidide nimetused. Li2O = liitiumoksiid BeO = berülliumoksiid FeO = raud(II)oksiid N2O5 = dilämmastikpentaoksiid Cr2O3 = kroom(III)oksiid SO3 = vääveltrioksiid 4. Tõmba joon alla oksiididele, mille reageerimisel veega tekib söövitav lahus. K2O, CuO, SO2, CaO, Al2O3, SiO2, N2O5, Li2O, P4O10, H2O, Ag2O 5. Kirjuta järgmiste oksiidide valemid. Alumiiniumoksiid Al2O3 dilämmastikoksiid N2O kroom(VI)oksiid CrO3 raud(II)oksiid FeO 6. Nimeta üks metallioksiid ja üks mittemetallioksiid ning kirjuta, kus neid kasutatakse. ...
Oksiidide keemilised omadused · Aluselised oksiidid reageerivad hapetega = sool ja vesi. · Aluselised oksiidid reageerivad veega = leelis. Veega reageerivad ainult aktiivsete metallide oksiidid (IA rühma ja IIA rühma metallid alates Ca) · Aluselised oksiidid reageerivad happeliste oksiididega = sool. · Happelised oksiidid reageerivad veega = oksiidile vastav hape. Veega ei reageeri SiO2. · Happelised oksiidid reageerivad alustega = sool ja vesi. · Happelised oksiidid reageerivad aluseliste oksiididega = sool. Hapete keemilised omadused · Reageerivad metallidega = sool ja vesinik Reag. < h2 · Reageerivad alustega = sool ja vesi · Reageerivad aluseliste oksiididega = sool ja vesi · Reageerivad sooladega = uus sool ja uus hape Reaktsioon toimub siis, kui tekib nõrgem hape või sade Kui tekib H2CO3, siis tekkemomendil laguneb ta veeks ja süsinikdioksiidiks · Lagunemine kuumutamisel = happeline o...
Õpimapp Keemias 2011 Sisukord Skeem: Anorgaaniliste ainete põhiklassid.......................................3 Skeem: Aineklasside vahelise seosed.............................................5 Aineklasside tähtsamad keemilised omadused...............................8 Kõikide aineklasside saamisviis.....................................................10 2 Anorgaaniliste ainete põhiklassid (skeem) Alused on ained, mis annavad lahusesse hüdroksiidioone OH-. Tüüpilised alused on hüdroksiidid. Hüdroksiidid koosnevad metalliioonidest ja hüdroksiidioonidest (OH-). Happed on ained, mis annavad lahusesse vesinikioone (H+). Happed koosnevad vesinikioonidest ja happeanioonidest (happejäägist). Happeaniooni laeng võrdub vesiniku aatomite arvuga happe molekulis. Hapete liigitamine vesiniku aatomite arvu järgi: 1. Üheprootonilised happed (n...
AINETE PÕHIKLASSID JA NENDE VAHELISE SEOSED . Oksiidid. *Oksiid-aine, mis koosneb kahest elemendist, millest üks on hapnik(o/a-II). -aluselised oksiidid (metall + hapnik) reageerivad hapetega. Tugevalt aluseliste oksiidide reageerimisel veega tekivad leelised ehk lahustuvad alused(tugevad alused). Nt. NaOH -happelised oksiidid(mittemetall + hapnik) reageerivad alustega. Happeliste oksiidide reageerimisel veega tekib enamasti hape. Nt. H2SO4. -amfoteersed oksiidid (Al2O3;Cr2O3;Fe2O3;ZnO) reageerivad nii aluste kui hapetega alustega reageerimisel tekivad kompleksühendid. Nt Na[Al(OH)4]. Amfoteersed oksiidid veega ei reageeri. -Neutraalsed oksiidid(CO;NO;N2O) on mittemetallioksiidid, mis veega reageerides hapet ei anna. Oksiidide peamised saamisvõimalused a) Vastavate lihtainete reageerimine hapnikuga = C + O2 = CO2 b) Suhteliselt ebapüsivate hapnikku sisaldavate ühendite lagundamine(kuumutamine). Alus=Oks...
1 ANORGAANILISTE AINETE PÕHIKLASSID Keemilised ained jaotatakse: lihtained (koosnevad ühe elemendi aatomitest) -metallid näiteks: vask - Cu, alumiinium - Al -mittemetallid näiteks: hapnik - O2, grafiit - C liitained (koosnevad mitme elemendi aatomitest) Olulisemad anorgaaniliste liitainete klassid on: -oksiidid näiteks: CO2, CaO, H2O -happed näiteks: HCl, H2SO4 -alused näiteks: NaOH, Ca(OH)2 -soolad näiteks: NaCl, K2SO4 OKSIIDID Oksiidid on liitained, mis koosnevad kahest elemendist, millest üks on hapnik (O). Oksiidid võivad tekkida: 1. Liht- või liitainete reageerimisel hapnikuga (oksüdeerumisel). Kiiret oksüdeerumist nimetatakse põlemiseks. C + O2 CO2 (põlemine) S + O2 SO2 (põlemine) 4Fe + 3O2 2Fe2O3 (aeglane oksüdeerumine, roostetamine) 2. Hapnikku sisaldavate ainete lagunemisel. CaCO3 CaO + CO2 (...
ANORGAANILISTE AINETE KLASSID konspekt ja tööleht OKSIIDID on liitained, mis koosnevad kahest elemendist, millest üks on hapnik(oa II ). Näit: H2O CO2 Fe2O3 CaO. HÜDROKSIIDID (ALUSED) on liitained, koosnevad metalliiooonidest ja hüdroksiidioonidest OH-. Näit: NaOH Ca(OH)2 HAPPED on liitained, mis koosnevad vesinikioonidest ja happeanioonidest. Näit: HCl H2SO4 H3PO4 SOOLAD on liitained, mis koosnevad metalliioonidest ja happeanioonidest. Näit: NaCl CaF2 Al2(SO4)3 Aine valemis asuvad esimesel kohal positiivsed koostisosad (H + Na+ Al3+ jne ) ja teisel kohal negatiivsed koostisosad ( O 2- OH- SO42- Cl- jne ) Kirjuta iga valemi taha aine klassiline kuuluvus (O Hü Ha S ): Na2SO4 KBr N2O5 P4O10 H3PO4 Ca3(PO4)2 Ca(OH)2 CaO HCl CaCl 2 H2SO4 SO3 MgSO3 Mg(OH)2 MgO FeO . OKSIIDID Oksiidid on looduses ühed kõige enam levinumad ühendid. Oksiidid on iseloomulikud ühendid, kuna nende omadused on heas koos...
Anorgaaniliste ainete keemilised omadused OKSIIDID Aluseliste oksiidide keemilised omadused Aluseline oksiid ehk metallioksiid 1) Reageerimine veega Saadus on leelis (tugev alus) + - Li2O + H2O > 2LiOH 2+ - CaO + H2O > Ca(OH)2 Veega reageerivad ainult I ja II A rühma, alates kaltsiumist, nende metallide oksiidid. 2) Reageerimine happega Saadused on sool ja vesi. + - + - Na2O + 2HCl > 2NaCl + H2O III -II + -2 3+ 2- Fe2O3 + 3H2SO4 > Fe2(SO4)3 + 3H2O 2+ - BaO + 2HI > BaI2 + H2O 3) Reageerimine happelise oksiidiga Saaduseks on sool. + 2- K2O + CO2 > K2CO3 Happeliste oksiidide keemilised omadused 1) Reageerimine veega Saaduseks on hape. + 2- CO2 + H2O > H2CO3 + 3- P4O10 + 6H2O > 4H3PO4 SiO2 + H2O Ei toimu, sest SiO2 on liiv. 2) Reageerimine alustega Saadused on s...
Oksiidid. · Oksiidid on liitained, mis koosnevad kahest elemendist, millest üks on hapnik. · Oksiidid on elemendi ühendid hapnikuga. · Oksiide liigitatakse: 1. happelised S03 3. amfoteersed Al203 2. aluselised K20 4. inertsed (neutraalsed) CO · Oksiididele nimetuste andmine: 1. IA, IIA ja IIIA rühma metalli oksiididele nimetuse annan järgmiselt: Nimetan metalli ja lisan sõna oksiid K20 - kaaliumoksiid 2. Mittemetallioksiidide nimetused annan eesliidetega: mono-, di-, tri-, tetra-, penta-, heksa-, hepta-, okta-, nona-, deka- N205- dilämmastikpentaoksiid 3. B-alarühma ja IVA, VA rühma metallioksiididele nimetuse andmisel kasutan oksüdatsiooniastet V -II Mn205 - mangaan(V)oksiid · Happelised oksiidid. Happelised oksiidid on...
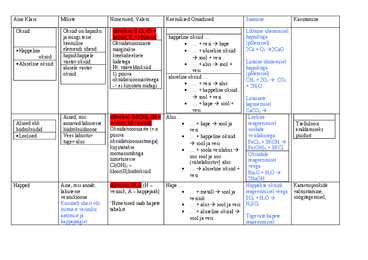
Aine Klass Mõiste Nimetused, Valem Keemilised Omadused Saamine Kasutamine Oksiid Oksiid on hapniku üldvalem: E2On (O = Lihtaine ühenemisel ja mingi teise hapnik, E = element) happeline oksiid ... hapnikuga keemilise Oksüdatsiooniaste · ... + vesi hape (põlemisel) · Happeline elemendi ühend märgitakse · ... + aluseline oksiid 2Ca + O2 2CaO oksiid hapnikhappele kreekakeelsete sool + vesi · Aluseline oksiid vastav oksiid liidetega Liitaine ühinemisel · ... + alus sool ...
Anorgaania. Oksiidid on ühendid, mis koosnevad kahest elemendist, millest üks on hapnik. Oksiide saadakse põletamisel * Mg + O2 - 2MgO * ja lihtainete *metall ja mittemetall* omavahelisel reaktsioonil *4Fe +3O2 2Fe3O3* Oksiide liigitatakse happelisteks oksiidideks, aluselisteks oksiidideks, anforteerseteks oksiidideks ja neutraalseteks oksiidideks. Happelised oksiidid siia kuuluvad enamasti mittemetalli oksiidid ja kõrge o.-a. Metalli oksiidid. *CO2; NO2; P4O10; CrO3; Mn2O7* Aluselised oksiidid siia kuuluvad enamasti metalli oksiidid. *Na2O;FeO* Amfoteersed oksiidid siia kuuluvad Al2O3; ZnO; Fe2O3; Gr2O3 Neutraalsed oksiidid siia kuuluvad mittemetallid *CO; NO; N20* Oksiidide keemilised omadused. 1. Happelised oksiidid reageerivad veega *CO2 + H2O H2CO3* 2. Happelised oksiidid reageerivad aluseliste oksiididega *CO2 + Na2O Na2CO3* 3. Happelised oksiidid reageerivad alustega *N2O...
Anorgaanilised ühendid Oksiid – hapnikuühend mingi elemendiga Aluseline Amfoteerne Happeline Neutraalne oksiid oksiid oksiid oksiid metallioksiid sellel võivad Mittemetalliok happelised ja avalduda nii siid aluselised omadused aluselised kui puuduvad happelised omadused reageerib Reageerib reageerib Ei reageeri millegagi hapetega; tugevate hapete ja alustega tugevalt leelistega aluselised reageerivad veega Li2O, CrO, Al2O3, Cr2O3, Fe2O3, SO2, SiO2 CO, NO, N2O Na2O, FeO, ZnO NO2, CaO, NiO CO2, BaO ...
OKSIIDID Oksiid aine, mis koosneb kahest elemendist, millest üks on hapnik. Aluseline oksiid aluseliste omadustega, reageerib hapetega. Happeline oksiid happeliste omadustega, reageerib alustega. Oksiidide saamine: *Põlemise teel: C+O2 CO2 2Ca+O2 2CaO *Kuumutamise teel: 2Cu+O2 2CuO HAPPED Hape aine, mis annab vesilahusesse vesinikioone. Liigitamine: Hapnikusis Prootonite Tugevuse järgi alduse järgi arvu järgi Hapnikhappe Hapnikut Üheprootonilis Mitmeprootonilis Tugevad Nõrgad d a ed happed ed happed happed happed happed Sisaldavad Ei Sisaldab ainult Sisaldab mitut Vesinikkloriid Süsihape ühe sisalda ühte vesinikiooni. , , elemendina hapnikku vesinikiooni. vesinikbromii fosforhap hapnikku. . ...
OKSIID koosneb kahest elemendist, millest üks on hapnik (o.-a. II) ehk siis Lihtaine + hapnik = oksiid Aluseline oksiid on aluseliste omadustega, reageerib hapetega (enamus metallioksiide on aluselised. Aktiivse metalli oksiid + vesi = hüdroksiid ehk leelis ehk tugev alus) Happeline oksiid - on happeliste omadustega, reageerib alustega (enamus mittemetallioksiide on happelised) Enamik happelisi oksiide + vesi = vastav hape HAPE aine, mis annab vesilahusesse vesinikioone (happeid liigitatakse 1. hapnikusisalduse järgi (hapnikhapped ja hapnikuta happed), 2. prootonite arvu järgi, 3. tugevuse järgi (nõrgad ja tugevad). Hapnikhape saadakse: happeline oksiid + vesi ALUS ehk hüdroksiid aine, mis annab vesilahusesse hüdroksiidioone. (aluseid liigitatakse: 1. leelised (vees hästi lahustuvad tugevad alused), 2. nõrgad alused , mis enamasti vees ei lahustu) Leelis (IA ja IIA rühma metallide hüdroksiid) = tugevalt aluseline oksii...
Happed – koosnevad vesinikioonidest ja happeanioonidest. Annavad lahusesse vesinikioone (H2 SO3). vesinikioon happeanioon Alused – koosnevad metalliioonidest (metall) ja hüdroksiidioonidest (OH -). Annavad lahusesse hüdroksiidioone. Näiteks: KOH (kaaliumhüdroksiid), Fe(OH) 2 (raud(II)hüdroksiid), Ca(OH)2 (kaltsiumhüdroksiid). Oksiidid – koosnevad kahest elemendist, millest üks on hapnik (SO 2, Al2O3). Liigitatakse aluselised (metall + hapnik), happelised (mittemetall + hapnik), neutraalsed ja amfoteersed oksiidid. Hapniku oksüdatsiooniaste on oksiidides –II. Soolad – koosnevad metallioonist (näiteks – Na+, Fe2+, Cu2+, Al3+ jne.) ja happeanioonist (näiteks: SO4 2-, Cl- jne.). Näiteks: NaCl, FeSO 4, K2CO3. Anioon Happeaniooni OH- -hüdroksiid metall-OH (NaOH) - Cl- -kloriid HCl (vesinikkloriidhape) metall-Cl näit. KCl (kaaliumkloriid) F- -flouriid HF (vesinikflouriidhape) metall-F näit. NaF (naatriumflouriid) Br- -bromiid HBr (vesinikb...
REAKTSIOONIVÕRRANDID (LOTE I) Ainete valemite koostamisel arvesta laenguid ühendis (risti alla indeksiteks). Võrrandi tasakaalustamiseks loe aatomeid ja pane teisele poole reaktsiooninoolt kordajad, kuni mõlemale poole saab võrdne arv aatomeid. Kordaja korrutab indekseid! 1. Element + hapnik = oksiid Põlemisreaktsioon C+O2->CO2 süsiniku põlemine 4Fe+3O2->2Fe2O3 raua roostetamine Harjuta ( oksiidi valemi koostamiseks kasuta aatomi väliskihi elektronide arvu, vaadates tabelist A-rühma nr- sellest tulenes elemendi aatomi oksüdatsiooniaste ühendis) S+O2-> P+O2-> 2. Orgaanilised ained oksüdeeruvad (põlemine, hingamine) süsihappegaasiks ja veeks CH4+ 2O2->CO2+2H2O metaani ehk maagaasi põlemine C6H12O6+6O2->6CO2+6H2O hingamine, glükoosi oksüdatsioon rakkudes Harjuta C3H8+O2-> 3. Happelised oksiidid (mittemetallide oksiidid) reageerivad veega ja tekib hape. SO2, SO3 ja ...
REAKTSIOONIVÕRRANDID (LOTE I) Ainete valemite koostamisel arvesta laenguid ühendis (risti alla indeksiteks). Võrrandi tasakaalustamiseks loe aatomeid ja pane teisele poole reaktsiooninoolt kordajad, kuni mõlemale poole saab võrdne arv aatomeid. Kordaja korrutab indekseid! 1. Element + hapnik = oksiid Põlemisreaktsioon C+O2->CO2 süsiniku põlemine 4Fe+3O2->2Fe2O3 raua roostetamine Harjuta ( oksiidi valemi koostamiseks kasuta aatomi väliskihi elektronide arvu, vaadates tabelist A-rühma nr- sellest tulenes elemendi aatomi oksüdatsiooniaste ühendis) S+O2-> P+O2-> 2. Orgaanilised ained oksüdeeruvad (põlemine, hingamine) süsihappegaasiks ja veeks CH4+ 2O2->CO2+2H2O metaani ehk maagaasi põlemine C6H12O6+6O2->6CO2+6H2O hingamine, glükoosi oksüdatsioon rakkudes Harjuta C3H8+O2-> 3. Happelised oksiidid (mittemetallide oksiidid) reageerivad veega ja tekib hape. SO2, SO3 ja ...
Keemia kordamisküsimused KT:Happed ja alused 1.Tuleb pähe õppida hapate tabel. Kolm esimest tulpa. Happe valem Happe nimetus Aniooni valem HF vesinikfluoriidhape F- HCl vesinikkloriidhape Cl- HBr vesinikbromiidhape Br- HI vesinikjodiidhape I- H2S divesiniksulfiidhape S2- H2SO4 väävelhape SO42- H2SO3 väävlishape SO32- HNO3 lämmastikhape NO3- HNO2 lämmastikushape NO2- H3PO4 fosforhape PO43- H2CO3 ...
Õppeasutus Eriala Nimi ja Perekonnanimi Orgaanilised happed Referaat keemias Aineõpetaja Koht Aasta SISUKORD SISSEJUHATUS..............................................................................3 KARBOKSÜÜLHAPPED........................................................................................4 KARBOKSÜÜLHAPETE KEEMILISED OMADUSED..........................................................4 KARBOKSÜÜLHAPETE FÜÜSILISED OMADUSED......................................4 ASENDAMATA KARBOKSÜÜLHAPPED..........................................................5 METAANHAPE EHK SIPELGHAPE...................................................................5 ETAANHAPE EHK ÄÄDIKHAPE.......................................................................5 RASVHAPPED........................................................................................................5 ASENDATUD K...
Väävel : Füüsikalised omadused : tahke, rabe, kergestisüttiv. Looduses esineb puhtana ning o N2+3H22NH3 ühenditena. o Reageerib kuumutamisel hapnikuga Keemilised omadused : o N2+022NO (äike) o Väävel on halb elektri-ja soojusjuht, vees ei lahustu Kasutamine: külmutusvedelikuna, ammoniaagi lähteainena, tulekustutites toitegaasina Väävli kasutamine :Väävelhappe tootmiseks lähtainena; Kummi hulkaniseerimiseks Lämmastiku ühendid : (kautsukist kummi valmistamiseks); Taimekaitsevahendina Ammoniaak NH3 ;Lõhkeainete tootmisel ...
Keemia Perioodilisustabel ja aatom Lahter- Perioodi rühmad- eemiliste elementide perioodilisussüsteem on süsteem, mis jaotab keemilised elemendid nende tuumalaengute järgi rühmadesse ja perioodidesse. Järjekorra number: Keemilise elemendi aatomnumber ehk järjenumber ehk laenguarv on prootonite arv selle elemendi aatomi tuumas. A-rühma numbrist: Kui aktiivne metall on. Perioodi Number: Mitmendas perioodis asub element, Elemendid: 1.Raud : Fe, 2,Vask: Cu, 3,Jood: I, 4,Broom: Br , 5,Tina: Sn , 6,Plii:Pb 7,hõbe: Ag 8, Broom: Br 9, kuld : Au, 10,Elavhõbe : Hg, 11, tsink: Zn, 12,mangaan : Mn, 13 Kroom Cr 14, Baarium: Ba 15,magneesium : Mg 16,naatrium : Na 17,kaalium : K 18,koobalt : Co 19,titann: Ti 20,alumiinum : Al 21,nikkel : Ni 22, Gallium : Ga 23,Iriidium: Ir 24,Plaatina: pt 25,Rubiidium: Rb 26,plii: Pb 27, Indium : In 28,frantsium : Fr 29,Raadium : Ra 30,Vsimut : Bi 31,Tellur : Te 32, flueo : F ...
KT 7 1. Karboksüülhapped on orgaanilises keemias nõrgad happed, mis sisaldavad karboksüülrühma (COOH). Rasvhapped on looduslike rasvade koostises olevad monohapped, milles on üle kümne paarisarv süsiniku aatomi. Rasvhapped võivad olla küllastunud või küllastumata. Asendatud karboksüülhapped e. hüdroksühapped on puuviljades ja teistes looduslikes allikates esinevad orgaanilised karboksüülhapped. Aminohapped e. aminokarboksüülhapped on keemilised ühendid, mis sisaldavad funktsionaalsete rühmadena nii aminorühmi kui ka karboksüülrühmi. Aminohapped on karboksüülhapped, mille alküülradikaalis on üks või mitu vesiniku aatomit asendunud aminorühmaga. Kodeeritavad aminohapped on eluks vajalikud 20 aminohapet, millest loodus on ehitanud valgud. Asendamatud aminohapped on aminohapped, mida inimese organism ise kas üldse ei tooda või toodab vähesel määral, nii e...
Oksiidid Happed Alused Soolad Nimetused 1) Mittemetallioksiidide nimetustes tähistatakse Hapete nimetused peavad olema peas. Vesiniksoolade nimetustes lisatakse happeaniooni nimetuse ette elementide aatomite arvud kreeka keelest "vesinik", mille ees on mitme vesiniku aatomi korral aatomite tuletatud eesliidetega (Cl2O- diklooroksiid). arvu näitav liide. 2) Kui metallil on muutuv o.a, siis märgitakse see CaHPO4- kaltsiumvesinikfosfaa...
Laboratoorse töö protokoll Anorgaaniliste ainete põhiklassid Tallinna 32. Keskkool 10B klass Koostasid: Getterly Monika Stiina Mari-Liis 18.oktoober 2012 Tallinn Katse 1. Happe reageerimine soolaga Katsevahendid: Katseklaas, tahke sooda ( Na CO ), pird, tikud, vesinikkloriidhape (HCl) või äädikhape (CH COOH). Katse kirjeldus: Paneme katseklaasi hernesuuruse koguse soodat ja lisame paar kuupsentimeetrit hapet. Kohe algab katseklaasis tormiline reaktsioon ja eraldub gaas. Tõestame põleva pirruga, kas era...
Kordamine. KEEMILINE ELEMENT- ühesuguste tuumalaengutega aatomite liik. ALLOTROOPIA- nähtus, kus 1 keemiline element võib esineda mitme lihtainena. O2-dihapnik, O3- trihapnik(ehk osoon) ISOTOOP- ühesuguste tuumalaenguga, erineva massiarvuga osakesed. 1. AINE KLASSID: a. Lihtained- (400),koosnevad ühe elemendi aatomitest.: · mittemetallid(19)- S, P, O2, Cl2 jne · poolmetallid e. metallid(15)- Ge, As, Sb, Te, At jne · metallid (90); Al, Au, jne b. Liitained- koosnevad mitme elemendi aatomitest: 1. Oksiidid- on ained, mis koosnevad kahest elemendist, millest üks on hapnik (oksüdatsiooniaste -II). Oksiid on hapnik (o.-a. II) ja mingi teise keemilise elemendi ühend. a. Aluselised oksiidid oksiidid, mis reageerivad hapetega, moodustades soola ja vee. Aluseliste oksiidide hulka kuulub...
OKSIIDID Metallioksiidid: nimetus à metalli nimi (vajadusel oksüdatsiooniaste)oksiid Mittemetallioksiidid : tavaliselt on molekulaarse ehitusega ja nimetus reagee Metallioksiidid on ioonilised ained ja molekule pole moodustatakse eesliidete abil (mono, di ,tri, tetra, penta, heksa, hepta, okta, rimine Näiteks CaO kaltsiumoksiid Fe2O3 raud(III)oksiid e. diraudtrioksiid nona ,deka) CO2 süsinikdioksiid N2O dilämmastikoksiidP4O10 tetrafosfordekoksiid reageerimi ne SOOLATEKITAJAD OKSIIDID ...
Halogeenid Leidumine : looduses leidub ühenditena merevees ja mineraalidena:CaF2 sulapagu , NaCl naatriumkloriid e. Keedusool , KCl. Nad on bioelemendid :F kuulub hambaemaili ja luude koostisesse, inimorganismis NaCl on u. 200 g ja Ioonidena on veres , maomahlas, sapis jt. Broomiühendeid on ajus, joodiühendeid on kilpnäärmes ja lihastes. Füüsikalised omadused: F2 on helekollane väga mürgine gaas, terava lõhnaga. Cl2 on kollakasroheline mürgine gaas, terava lõhnaga, lahustub vees ja seda nimetatakse kloorveeks. (s.o.tugev oksüdeeria). Br2 on punakaspruunivärvusega väga mürgine vedelik, kergesti aurustub, vees lahustub vähe, paremini orgaanilistes lahustites (benseenis , eetris, alkohoolis). I2 on metalse läikega mustjasvioletse värvusega kristalne aine. Vees lahustub halvasti, hästi benseenis, piirituses, eetris jt. Kuumutamisel sublimeerub s.t. tahke aine muutub gaasiks , gaasiline jood ...
Mettallide kasutamine igapäeva elus ! Mettallidest on valmistatud paljud meile vajalikud tarbeesemed, noad, kahvlid, tööriistad, ukselukud, lennukid, autod, arvutid, laevad, tööstusseadmed, jalgratattad, masinad, raudteed, raadiomastide, elektrijuhtmed ([hõbe], vask) ning torustikud ja mitmel pool mujal. Erivevaid asju valmistatakse väga erinevatest mettallidest ning mettallisulamitest. Mettallide omadused on: tavatingimustes tahked ained, (erand elavhõbe), hallika värvitooniga (varieerub hõbevalgest terashallini), peegeldavad hästi valgust, metalne läige, käega katsumisel külmad, head soojus- ja elektri juhid, hästi sepistatavad, plastilised, tugevad. Elemendi metallilised omadused avalduvad seda tugevamini, mida kergemini tema aatomid loovutavad väliskihi elektrone. Raud tähtsaim ja odavaim metall. Eestis toodeti rauda vanasti soorauamaagist. Rauda leidub ka elusorganismides, vere punalibledes hemoglobiini koostises. ...
Lämmastik, lämmastikuühendid Created by Janus +I N2O +II NO & N2O2 +IV NO2 & N2O4 +V (max) N2O5 -III (min) NH3 ammoniaak 0 N2 lämmastik dilämmastikoksiid lämmastikoksiid lämmastikdioksiid dilämmastikpentoksiid Naerugaas H Elektronide arv on … püsiv radikaal Dimeer ...
ANORGAANILISTE AINEKLASSIDE KEEMILISED OMADUSED Reaktsioonivõrrandite koostamisel peab meeles pidama järgmiseid üldpõhimõtteid: 1) Nii lähteainetele kui ka saadustele tuleb märkida peale laengud ja oksiididele oksüdatsiooniastmed. Lihtaine oksüdatsiooniaste on null! 2) Lähteainetes vesiniku ja metallide all olevad indeksid saadustesse kaasa ei viida. (Ioonide kuju tuleb järele vaadata lahustuvustabelist). 3) Kui aine on toatemperatuuril gaasilises olekus, siis tuleb selle aine valemi taha märkida nool üles. Kui aine on toatemperatuuril tahkes olekus või vees mittelahustuv või veest raskem, siis tuleb märkida selle aine valemi taha nool alla. 4) Kõik toimuvad reaktsioonivõrrandid tuleb tasakaalustada. 5) Kui reaktsiooni ei toimu, siis tuleb sõnadega märkida põhjendus, miks antud reaktsioon ei toimu. Aluseliste oksiidide keemilised omadused 1) aluseline oksiid + hape sool + vesi II -II + - 2+ - III -II + 2- 3+ 2- CuO + 2HCl CuCl2 + H2O Al...
VIA RÜHMA ELEMENDID. HAPNIK JA VÄÄVEL Üldiseloomustus: · Hapnik ja väävel kuuluvad perioodilisustabeli VIA rühma elementide ehk kalkogeenide hulka · Enamik VIA rühma elemente on üsna tugevate mittemetalliliste omadustega, kuid jäävad elektronegatiivsuselt siiski alla samas perioodis asuvale halogeenile · Rühmas ülevalt alla elementide aatomiraadius kasvab, mistõttu nende elektronegatiivsus väheneb ja mittemetallilised omadused nõrgenevad · VIA rühma elementide aatomite väliskihis asub 6 elektroni · Väliskihi täielikust täitumisest on puudu 2 elektroni, järelikult saavad nad moodustada ühendeid o.a-s -II kuni VI · Negatiivses o.a-s ühendeid moodustavad nad metalliliste ja endast vähemaktiivsete mittemetalliliste elementidega · Väävli ja hapniku sarnasus avaldubki kõige selgemini o.a-s -II ühendite korral · Väävli aatomite raadius on suurem kui hapniku aatomitel, seetõttu loovutavad nad elektro...
1 Aatomi ehitus ja perioodilisussüsteem. 1.1 Aatomi ehitus. Aatom on keemilise elemendi väikseim osake. Keemiline element on kindla tuumalaenguga aatomite liik. Aatom koosneb aatomituumast ja elektronkattest. Aatomituuma koostisse kuuluvad prootonid ja neutronid. Elektronkate koosneb elektronkihtidest, millel liiguvad elektronid. Esimesele kihile mahub kuni 2 elektroni, teisele kihile kuni 8 elektroni, kolmandale kihile kuni 18 elektroni ja neljandale kihile kuni 32 elektroni. Väliskihil pole kunagi üle 8 elektroni ja eelviimasel kihil üle 18 elektroni. Isotoobid on elemendi teisendid, mille tuumas on erinev arv neutrone. Osake Laeng (elementaarlaengutes) Mass (aatommassiühikutes) Prooton (p) +1 1 Neutron (n) 0 1 Elektron (e ) -1 0,0005 (~0) Seega on aatomi mass koondunud suhteliselt väiksesse tuuma. Elektronkatte raadius ületab tuuma raadiust ~100 000 korda. 1.2 Aatomi ehituse seosed perioo...
Aatom koosneb aatomituumast ja elektronkattest, tuum prootonitest ja neutronitest, elektronkate elektronidest. Elektronide maksimumarv kihil = 2* n-ruudus Orbitaalid s,p ja d Massiarv = prootonite arv + neutronite arv. Elektronegatiivsus - Tõmbevõime keemilises sidemes. Metallid loovutavad elektrone Mittemetallid seovad elektrone. Muidu suureneb elektronegatiivsus paremalt vasakule ja ülevalt alla, aga B-rühmas alt üles. Ioon Laenguga aatom või aatomirühm Katioon positiivne. Anioon negatiivne. Oksüdatsiooniaste(o.a.) iooni laengu suurus. A-rühma metallidel on püsiv o.a. Maksimaalne o.a. On oksiidi valemis ja minimaalne on mittemetalli vesinikühendis. Molekul koosneb aatomitest Molekulaarsed ained koosnevad molekulidest. Mittemolekulaarsed ioonidest või aatomitest. Keemilise sideme tekkel eraldub energiat, eksotermiline. Sideme lõhkumisel neeldub energiat, endotermiline protsess. Mittepolaarne kovalentne side esineb ühe...
Kordamisküsimused: VÄÄVEL 1.Väävli leidumine looduses, allotroopia (allotroobi nimi, aatomite kuju ja paiknemine, omadused erinevatel temperatuuridel Leidumine: Ehedalt võib väävlit leida maapinna lähedal vulkaanilistes piirkondades. Tuntumatest väävliühenditest leidub looduses kõige enam sulfiide (FeS2 püriit, PbS- galeniit , HgS kinaver jt) ja sulfaate ( CaSO4*2H2O kips jt) Väävel kuulub elemendina ka kivisöe, põlevkivi, nafta ja teiste fosiilsete kütuste koostisse. Väävel on tähtis element ka eluslooduses. Ta on mitme aminohappe ja valkude koostises. Keskmisest enam on väävlit juustes, karvades, küüntes, sarvedes ja sulgedes. Allotroopia-1)rombiline väävel- 2.Väävli füüsikalised omadused, väävli oksüdatsiooniastmed, oksüdatsiooniastmete arvutamine. Väävel on kollane, rabe, elektrit mittejuhtiv kristalne aine tihedusega 2,07 g/cm³. Vees kristalne väävel ei lahustu, vähesel määral lahustub...
Anorgaaniline keemia 1. Aine ehitus Aatom on keemilise elemendi väikseim osake. Keemiline element on kindla tuumalaenguga aatomite liik. Aatom koosneb aatomituumast ja elektronkattest. Aatomituuma koostisse kuuluvad prootonid ja neutronid. Elektronkate koosneb elektronkihtidest, millel liiguvad elektronid. Esimesele kihile mahub kuni 2 elektroni, teisele kihile kuni 8 elektroni, kolmandale kihlie kuni 18 elektroni ja neljandale kihile kuni 32 elektroni. Väliskihil pole kunagi üle 8 ja eelviimasel kihil üle 18 elektroni. Anorgaaniliste ühendite hulka kuuluvad vesi, soolad, happed ja alused. 2. Aatomi ehituse seos perioodilisustabeliga Elementide omadused on perioodilises sõltuvuses aatomite tuumalaengust (s.t. kui reastada elemendid tuumalaengu kasvu järjekorras, siis kordub kindla arvu elementide järel sarnaste o...
"Keemia alused" 3. kontrolltöö Küsimused, mis on toodud kaldkirjas, ei tule kontrolltöösse, kuid võivad esineda eksamiküsimustes. Tudeng peab teadma erinevate rühmade elementide peamiste ühendite nimetusi, oskama kirjutama ühendile vastavat keemilist valemit või vastupidi. Tudeng peab oskama kirjutama erinevate rühmade elementide peamiste ühendite tekkereaktsioone ning neid tasakaalustama. 1. Tähtsamad perioodilised seosed aatomite omadustes. Selgitage, kuidas muutuvad aatomiraadius, ionisatsioonienergia, elektronafiinsus, elektronegatiivsus ja polariseeritavus perioodilisustabelis. Aatomiraadiused vähenevad perioodis vasakult paremale ja rühmas kasvavad ülevalt alla. Aatomi raadius väheneb perioodilisuse tabelis vasakult paremale ja suureneb ülevalt alla. Igas uues perioodis lisanduvad uued elektronid järjest välimistele elektronkihtidele, mis asuvad aina kaugemal tuumast ja seetõttu suureneb raadius üleva...
Keemia kordamisküsimused 9.klassile 1.Aineklassid ja nendevahelised seosed OKSIIDID-koosnevad kahest elemendist, millest üks on hapnik (O). Oksiidide liigitus:1) Aluselised oksiidid-metalli oksiidid: # tugevalt aluselised, ( leelis ja leelismuld metallid IA ja IIA alates Ca metallide oksiidid) # nõrgalt aluselised oksiidid- vähem aktiivsete metallide oksiidid. 2) Happelised oksiidid-mitte metallide oksiidid. Keemilised omadused: happeline oksiid + vesi = vastavhape ! Veega ei reageeri SiO N: dilämmastikpentaoksiid + vesi happeline oksiid + alus = sool +vesi HAPPED-ained, mis annavad lahusesse vesinikioone. Hapete liigitus erinevate tunnuste järgi:1) Hapniku sisalduse järgi: # hapniku mittesisaldavad happed N: # hapnikhapped N: 2) Prootonite arvu järgi: # üheprootonilised happed N: # mitmeprootonilised happed N: 3) Tugevuse järgi: # tugevad happed- kõik happemolekulid jagunevad lahuses ioonideks N: ...
Keemia kordamisküsimused 9.klassile põhikool 1.Aineklassid ja nendevahelised seosed OKSIIDID-koosnevad kahest elemendist, millest üks on hapnik (O). Oksiidide liigitus:1) Aluselised oksiidid-metalli oksiidid: # tugevalt aluselised, ( leelis ja leelismuld metallid IA ja IIA alates Ca metallide oksiidid) # nõrgalt aluselised oksiidid- vähem aktiivsete metallide oksiidid. 2) Happelised oksiidid-mitte metallide oksiidid. Keemilised omadused: happeline oksiid + vesi = vastavhape ! Veega ei reageeri SiO N: dilämmastikpentaoksiid + vesi happeline oksiid + alus = sool +vesi HAPPED-ained, mis annavad lahusesse vesinikioone. Hapete liigitus erinevate tunnuste järgi:1) Hapniku sisalduse järgi: # hapniku mittesisaldavad happed N: # hapnikhapped N: 2) Prootonite arvu järgi: # üheprootonilised happed N: # mitmeprootonilised happed N: 3) Tugevuse järgi: # tugevad happed- kõik happemolekulid jagunevad lahuses ioonideks N: ...
KEEMIA KT o Karboksüülhappe (KH) struktuur KH funktsionaalrühm on karboksüülrühm. Karboksüülrühmas on kaks hapniku aatomit. Mõlemal on nukleofiilne (-) tsenter, kuid nende omavaheline vastastikmõju nihutab elektronid suuresti karbonüülsele hapnikule ning seetõttu on see tsenter nukleofiilsem ja aluselisem. Vt. elektrofiilide ja nukleofiilide paiknemist õpik lk 19 o KH keemilised omadused Kõige tähtsam keemiline omadus on happelisus. Kuigi nad on nõrgemad happed kui tuntumad mineraalhapped, nagu soolhape, lämmastikhape, väävelhape, ent nad on siiski tugevamad süsihappest ning palju tugevamad happed kui alkoholid. Nende tugevuse põhjuseks on karboksülaatiooni stabiliseerimine laengu delokalisatsiooni teel. Karboksülaatioon on nõrk nukleofiil. KHte üldisteks omadusteks: reageerimine metallide, aluste, aluseliste oksiidide ja nõrgemate hapete sooladega. Vt. happe tugevuse kasv õpik lk 21 o KH füüsikalised omadused Füüsikalise...
KORDAMISKÜSIMUSED: ( karboksüülhapped, amiidid, estrid). 1. Selgitada mõisted: karboksüülhape, ester, amiid, happe halogeniid, hüdroksühape, küllastunud hape, küllastumata hape, aminohape, halogeenhape, dihape, rasvhape, happe asendusderivaat, happe funktsionaalderivaat, laengu delokalisatsioon, hüdrolüüs, happeline katalüüs, leeliseline katalüüs. 2. Miks karboksüülhappel on happelised omadused? Kirjutada dissotsiatsioonivõrrand ja selgitada. R-COOH = R-COO- + H+ Karboksüülhappel on happelised omadused, sest tal on võime dissotseeruda ja anda lahusesse vesinikkatioone. 3. Võrrelda alkoholi ja karboksüülhappe happelisust. Põhjendada erinevust. Karboksüülhapped on miljardeid kordi happelisemad kui alkoholid, sest alkoholi happeline dissotsiatsioon on tugevalt vasakule nihutatud, kuid karboksüülhappe happeline dissotsiatsioon on tasakaalus. R-COOH + H2O R-COO- + H3O+ R-OH + H2O RO- + H3O+ 4. Võrrelda süsihappe ja etaanh...
Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O2, Si, H2) (HCl) (KOH) (Na2SO4) Happelised oksiidid Aluselised oksiidid (SO2, CO2, NO2, SO) (Na2O, CaO, MgO) Happed koosnevad vesinikioonidest ja happeanioonidest. Annavad lahusesse vesinikioone (H2 SO3). vesinikioon happeanioon Alused koosnevad metalliioonidest (metall) ja hüdroksiidioonidest (OH-). Annavad lahusesse hüdroksiidioone. Näiteks: KOH (kaaliumhüdroksiid), Fe(OH)2 (raud(II)hüdroksiid), Ca(OH)2 (kaltsiumhüdroksiid). Oksiidid koosnevad kahest elemendist, millest üks on hapnik (SO2, Al2O3). Liigitatakse aluselised (metall + hapnik), happelised (mittemetall + hapnik), neutraalsed ja amfote...
Anorgaanilised ained Lihtained Liitained Metallid Mittemetallid Happed Alused Oksiidid Soolad (Na, Cu, Au) (O2, Si, H2) (HCl) (KOH) (Na2SO4) Happelised oksiidid Aluselised oksiidid (SO2, CO2, NO2, SO) (Na2O, CaO, MgO) Happed koosnevad vesinikioonidest ja happeanioonidest. Annavad lahusesse vesinikioone (H2 SO3). vesinikioon happeanioon Alused koosnevad metalliioonidest (metall) ja hüdroksiidioonidest (OH-). Annavad lahusesse hüdroksiidioone. Näiteks: KOH (kaaliumhüdroksiid), Fe(OH)2 (raud(II)hüdroksiid), Ca(OH)2 (kaltsiumhüdroksiid). Oksiidid koosnevad kahest elemendist, millest üks on hapnik (SO2, Al2O3). Liigitatakse aluselised (metall + hapnik), happelised (mittemetall + hapnik), neutraalsed ja amfote...
ARVESTUSED Õppeaines: Keemia Klass: 11 Õpilane: Keila 2005 I Arvestus ALKAANID Alkaanid ehk parafiinid on kõik küllastunud süsivesinikud ja alifaatsed ühendid. Alkaanid on mittepolaarsed molekulid. Üldiselt on nad inaktiivsed, kuid põlevad õhus, moodustades süsinikdioksiidi, ja reageerivad halogeenidega. Neid kõiki v.a metaani, saadakse naftast. Mõnede alkaanide füüsikalisi omadusi: Üh. nimetus Molekuli valem Struktuurivalem Olek 25 oC Keemistemperatuur oC juures Metaan CH4 CH4 gaas - 161, 5 Etaan C2H6 CH3CH3 gaas - 88, 0 Propaan C3H8 CH3CH2CH3 gaas - 42, 2 Butaan C4H10 CH3CH2CH2CH3 gaas - 0, 5 Pentaan C5H12 CH3CH2CH2CH2CH3 ...