Ande Andekas Keemia - Alkeenid Alkeenid on küllastumata süsivesinikud, mille üldvalemiks on CnH2n. Küllastunud ainetel on süsinikahelas kõik ühekordsed sidemed ja iseloomulikud on asendumisreaktsioonid. Küllastumata ühenditel on süsinike vahel vähemalt üks kordne side ja iseloomulikud on liitumisreaktsioonid ning nad on keemiliselt aktiivsemad. Alkeenide molekulis on süsinukuahelas üks kaksikside. Küllastumatus tähendab, et süsiniku valentsid ei ole kaetud täielikult vesinikega
kaksiksidemega keemiliselt püsivam. Iseloomulikud on liitumisreaktsioonid, mis toimuvad kahes astmes. Reaktsioonitüübi erinevus: Kolmiksidemega ühendite omapäraseks reaktsiooniks on asendusreaktsioon metallidega, mille tulemusel moodustuvad atsetüliidid.Füüsikalised omadused: Keemistemp. Molekulmassiga suureneb. Sulasmistemp. Süsinikarvu kasvuga alkeenidel kahanevad ja alküünidel kasvavad. Alkeenid ja alküünid on hüdrofoobsed,ei lahkustu vees.nende homoloogilises reas muutuvad analoogiliselt nagu ka alkaanidel. Rea kolm esimest liiget eteen, propeen ja buteen on toatemperatuuril gaasid. Alates penteenist on vedelikud ja süsinku arvust 18 (C18H36) tahked ained. Keemilised omadused:kolmikside on kaksiksidemega võrreldes veidi püsivam ning alküünidele iseloomulikud reaktsioonid kulgevad aeglasemalt võrreldes alkeenidega. Hüdrogeenimine: CH≡CH + H2 → CH2=CH2 → CH3–CH3
Alkeenid Kirke Kübarsepp, Helin Raudnagel, Liis Teder, Doris Tihu, Kristiina Valdman 31. 10.2011 Alkeenid Alkeenideks nimetatakse küllastumata süsivesinikke, kus süsiniku aatomite vahel esineb üks kovalentne kaksikside. Alkeenide nimetuse tunnuseks on lõpuliide EEN, mis viitabki kaksiksideme olemasolule süsivesiniku molekulis. Alkeenide üldvalem on CnH2n ALKEENIDE HOMOLOOGILINE RIDA ALKEEN ALKEENI NIMETUS C2H4 ETEEN C3H6 PROPEEN C4H8 BUTEEN C5H10 PENTEEN C6H12 HEKSEEN C7H14 HEPTEEN C8H16 OKTEEN C9H18 NONEEN
vinl (krval side) alkaanidl esinevad ka isomeerid, vivad olla ka tskloalkaanid.Alkeenide isomeerid: trans vi cis ja nad on omavahel isomeerid. Alkaanide saamine: 1)laboratoorsel teel- alkoholide dehdraatimine(vee ra vtmise teel) nt. CH3CH2OH->H2O+CH2=CH2 2)tstuslikul teel- alkaanide dehdrogeenimiselt CH3CH2CH3->H2+CH2=CH-CH3 Alkaanide fsikalised omadused: 1)homoloogilises reas 3 esimest liiget gaasid,jrgmised vedelikud ning alates 18-dast ssinikust on alkeenid tahked. 2)keemistemp-d suurenevad molekulmassi kasvuga.sulamistemp. vheneb molekulmassi kasvuga. 3)on hdrofoobsed ained-seetttu ei lahustu vees.4)alkeenid on lhnavad ained.5)sulamis-ja keemistemp. on alkeenidel tavaliselt madalamad, kui neile vastavatel alkaanidel. Alkaanide keemilised omadused:1)alkeenidel on iseloomulikud liitumisreaktsioonid. plemine e. oksdeerumine /alkeenil on tahvav leek alkaanil mitte/ CH2=CH2+2CO2+2H2O 2) reageerimine halogeenidega CH3CH=CHCH3+Cl2-
Kõrgemate süsivesinike lagunemine Alkoholide retutseerimine vesinikuga Aldehüüdi katalüütiline redutseerimine Keemilised omadused: Täielik oksüdatsioon Oksüdatsioon alkoholi tekkega Oksüdatsioon adlehüüdi tekkega Täielik lagunemine Dehüdrogeenimine Dehüdrogeenimine (tsükli teke) Asendusreaktsioon halogeeniga (järkudes) Kõrgemate alkaanide lagunemine madalamateks Isomerisatsioon Alkeenid Tekkeviisid: Alkaanide hüdrogeenimine Tsükloalkaanide detsükliseerimine Alküünide hüdrogeenimine Alkadieenide hüdrogeenimine Alkoholide dehüdraatimine Kõrgemate süsivesinike lagunemine Keemilised omadused: Täielik põlemine Mittetäielik põlemine Täielik lagunemine Lagunemine madalamateks süsivesinikeks Hüdrogeenimine Ühinemine vesinikhalogeniidiga Ühinemine halogeeniga Hüdraatimine Tsükliseerimine Isomerisatsioon Polümerisatsioon
H2O Alkeene võib oksüdeerida aldehüüdideks ja hapeteks. Alküüne hapeteks Eteenist saab etanaali C2H4 + 1/2O2 = CH3CHO Hüdreerimine on ühtlasi redutseerimine, selles reaktsioonis on küllastumata ühendid oksüdeerijad C2H4 + H2 C2H6 Kuna küllastumata ühendid on kallimad, siis alkeene praktiliselt ei hüdreerita Pigem vastupidi, alkaanide dehüdreerimisel toodetakse alkeene. Proov kaaliumpermanganaadiga KMnO4 Õrnroosa lahuse toimel oksüdeeruvad alkeenid dioolideks, kuna värvus seejuures kaob (valastumine) saab ka seda reaktsiooni kasutada küllastumata ühendite tõestamiseks. Võrrand on keeruline. R-CH=CH2 R -CH(OH)-CH2OH Tähtsamad esindajad Eteen H2C == CH2 Saadakse Etaani dehüdreerimisel C2H6 H2 +C2H4 või C2H6 + 1/2O2 = C2H4 + H2O Samuti eraldatakse teda nafta krakkgaasidest Keemilised omadused Redoksomadused Põleb: C2H4 + 3O2 = 2CO2 + 2H2O teda saab oksüdeerida vastavaks aldehüüdiks (etanaal)
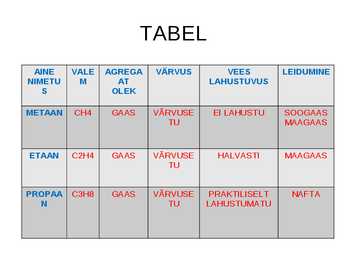
1 METAAN CH4 G 2 ETAAN C2H6 A 3 PROPAAN C3H8 A 4 BUTAAN C4H10 S 5 PENTAAN C5H12 6 HEKSAAN C6H14 7 HEPTAAN C7H16 VEDELIK 8 OKTAAN C8H18 9 NONAAN C9H20 10 DEKAAN C10H22 · Alkaanid-lõppsilp-aan Alkeenid-lõpp-een · Keemiliselt on aktiivsemad alkeenid · Metaani esineb:maa,-soo,-kaevandusgaasis · Metaan on kasvuhoooneefekti tekitav gaas · Biogaas-orgaaniliste jäätmete kääritamisel hermeetiliselt saadakse biogaas · Parafiinid-sisaldavad tahkeid alkaane · Parafiin-kasutatakse määrdeainete ja õlide ning küünakde välmistamisel · Eteen-saadakse nafta krakkimisel või põlevkivi utmisel ETEEN · Eteen-saadakse nafta krakkimisel või põlevkivi utmisel · Eteeni kasutatakse: lahustid,etanool,etanaal
4. Alkaanide nomenklatuur - reeglistik nimetuste andmiseks. Alkaanide süstemaatilised nimetused struktuuri järgi ning struktuurvalemi joonistamine nimetuse järgi. 5. Alkaanide keemilised omadused –asendusreaktsioonid halogeenidega, reageerimine hapnikuga e. põlemine (saaduseks CO 2 ja H2O) 6. Alkeenide mõiste - küllastumata süsivesinikud, mille molekulides on vähemalt üks kaksikside süsiniku aatomite vahel 7. Tuntumad alkeenid: Eteen – taimede kasvuhormoon, polümeerid, äädikhape, etanool Propeen-polüpropeen,atsetoon, orgaaniliste ainete süntees 8. 2-metüül-buta-1,3-dieen e. Isopreen - kummitööstus struktuur ja olulisus eluslooduses 9. Alkeenide keemilised omadused : liitumisreaktsioonid halogeenide ning vesinikhalogeniididega, reageerimine veega – hüdraatumisreaktsioon (saaduseks alkohol), reageerimine vesinikuga – hüdrogeenimisreaktsioon (saaduseks alkaan), polümerisatsioon
sel põhjusel -side on ka nõrgem side võrreldes -sidemega. Seda plahvatus ohtlik ja narkootilise toimega gaas.Etüüni saamise tõestab -sidet sisaldavate ühendite (näiteks alkeenide, alküünide) võimaluseks ja eriti laboris on tema tootmine kõrgem keemiline aktiivsus võrreldes -sidememeid sisaldavate kaltsiumkarbiidist.Kaltsiumkarbiidi saadakse elektriahjus alkaanidega. 3.Miks on alkeenid alküünidest keemiliselt kustutamata lubja kuumutamisel koksiga.Kui kaltsiumkarbiidile aktiivsemad? Kuna alküünides sisalduv kolmikside sisaldab - lisada vett,siis hakkabki mullikestena eralduma etüüni.Hapnikus sidemeid, mis on oluliselt nõrgemad kui üksiksidemetes olevad põleb etüün helesinise leegiga.Väga suure plahvatus ohtlikuse tõttu
Sissehingamisel tekitab narkoosi. Mis on hüdraatimine, nitreerimine, hüdrogeenimine?- Hüdraatimine alkeeni liitmine veega Hüdrogeenimine alkeeni liitmine vesinikuga Nitreerimine - kui benseeni molekuli üks vesiniku aatom asendatakse nitrorühmaga. Nimeta benseeni füüsikalisi omadusi. Värvitu, veest kergem. Iseloomuliku lõhnaga vedelik, ei lahustu vees. Toatemperatuuril aurustub, aurud on väga mürgised. Iselahustiks rasvadele ja valkudele. Mis on alkeenid ja alküünid? Seleta mõisted ja too iga rühma kohta üks näide. Alkeenid ühendid mis sisaldavad süsivesinike vahel kaksiksidet. Nt: -C=C- / CH2=CH2 Alküünid ühendid mis sisaldavad süsivesinike vahel kolmiksidet. Nt: -C=C- / CH=CH Mille poolest erinevad aromaatsed süsivesinikud teistest küllastumata süsivesinikest? Aromaatsed süsivesinikud kujutatakse alati kinnise ehk tsüklilise süsinikuahelana. Ehk Graafiliselt. Mis on aromaatsed süsivesinikud ehk areenid? Defineeri.
Alkoholid H H H H H-C-H H-C-OH H-C-C-OH H H H H metaan metanool etanool Alkoholid sisaldavad O ja H ühendit! Ei tohi sisaldada kaksiksidet. Alkaan Radikaal Alkohol R-OH CnH2n+2 CnH2n+1 CnH2n+1OH n= 1 Ch4 Ch3 Ch3OH n=2 C2H6 C2H5 C2H5OH n=3 C3H8 C3H7 C3H7OH jne Radikaali iseloomustab poolik side (võib tekkida pürolüüsi käigus), seal on 1 vesiniku võrra vähem kui alkaanis. Kui aga radikaalile lisada OH saab alkoholi. Alkaanide oksüdeerumisel on võimalik saada vastavaid alkohole. Alkoholid ise oksüdeeruvad ise ka edasi. Pohmelli põhjus on alkoholi oksüdatsiooniproduktid, mis ladestuvad organismi. 2 süsinikuga aldehüüdi mürgistus ongi pohm. Pohm lõppeb .... Alkohol i...
Alkeenid on küllastumata süsivesinikud, mille molekulides on vähemalt üks kaksikside süsiniku aatomite vahel. Alküünid on küllastumata süsivesinikud, mille molekulides esineb kovalentne kolmikside. Alküünide tähtsamaks esindajaks on etüün ehk atsetüleen HCCH. küllastunud ühend (e. alkaan) - C aatomite vahel on ainult ühekordsed sidemed, kõik vabad sidemed on küllastunud H-ga küllastumata ühend - süsivesinik, mis sisaldab kordseid sidemeid. Kaksikside on keemiline side, kus on ühinenud kaks elektronpaari.Kaksikside kuulub kovalentsete sidemete hulka. Kolmikside on keemiline side, kus on ühinenud kolm elektronpaari.Kolmikside kuulub kovalentsete sidemete hulka. Alküülimine on alküülrühmaga asenduse teostamine. Fenoolid (ka hüdroksüareenid) on aromaatsed ühendid, milles üks või mitu benseenituuma kuuluvat süsinikuaatomit on seotud hüdroksüülrühmaga. Hüdraatimine on keemiline liitumisreaktsioon veega. Dehüdrogeenimine on vesiniku eraldumine...
Küllastumata ühendid on orgaanilised ained kus C aatomite vahel esineb kovalentne kaksikside või kolmikside. Pii side moodustub hübridiseerimata p orbitaalide kattumisel Alkeenid on küllastumata süsivesinikud mis sisaldavad kaksiksidet. (nomenklatuuris -een lõpp) Üldvalem CnH2n eteen Alkeenidel esineb isomeeria: 1) Kaksiksideme asukoha muutusest H3C H2C HC = CH2 -> H3C HC = CH - H3C 2) Süsivesinikahela lagunemisel H3C H2C HC = CH CH3 -> 3) Tsükliliste struktuuride ühendite tekkest Keemilised omadused eteeni näitel: C2H4 -> H2C = CH2 1) Põlemine C2H4 + 3O2 -> 2CO2 + 2H2O 2) Astuvad liitumisreaktsioon a) Br2 -> H2C = CH2 + Br2 -> CH2 BrCH2 Br b) HCl -> H2C = CH2 + HCl -> CH3CH2Cl c) H2O -> H2C ...
Aine süstemaatiline/ Struktuurvalem Füüsikalised ja füsioloogilised Kasutamine ja rahvapärane omadused esinemine nimetus Suurem osa eteenist saadakse etaani Taimede kasvuhormoonina dehüdrogeenimisel. Värvuseta, kiirendab ta aed- ja puuviljade CH2=CH2 nõrgalt meeldiva lõhnaga, veidi valmimist. Üle poole eteenist uimastava toimega gaas. Õhuga kasutatakse ära polümeeride Eteen/etüleen ligikaudu üheraskune. Vees vähesel tööstuses, ülejäänu läheb määral lahustuv. äädikhappe, etanooli ja halogeenühendit...
Süsinikevahelise kaksiksidemega ühendeid nimetatakse alkeenideks. Süsinikevahelise kolmiksidemega ühendeid nimetatakse alküünideks. Süsivesinikke liike on kolm: alkaanid, alkeenid, alküünid. Alkaanid on küllastunud ühendid, alkeenid ja alküünid küllastumata ühendid. Süsinike arv Alkaani Alkeeni Alküüni ahelas nimetus nimetus nimetus CnH2n+2 CnH2n CnH2n-n 1 Metaan - - CH4 2 Etaan Eteen Etüün C2H6 C2H4 C2H2
NIMETUS STRUKTUURVALEM FÜÜSIKALISED KEEMILISED KASUTAMINE RAHVAPÄRANE OMADUSED OMADUSED NIMETUS (kui on) eteen ehk ● värvusetu ● vees ● Sellest etüleen ● narkootilise lahustamatu valmistatakse polü toimega eteeni ja etanooli ● nõrga lõhnaga ● Kasutatakse ● maitsetu plastide tootmisel ...
Alkeenid ja alküünid Kaksiksidemega süsivesikuid nimetatakse alkeenideks ning kolmiksidemega süsivesikuid alküünideks. Kõige lihtsam alkaan on eteen ning kõige lihtsam etüün. C2H4 eteen C2H2 etüün Tähtsamad vinüülpolümeerid a) Polüetüleen (PE) Mis on polüetüleen? Polüetüleen on poolkristallilise struktuuriga kõige levinum plast, mida on erinevaid liike: HDPE, (PE-HD)- kõrgtihe polüetüleen, LLDPE, (PE-LLD)- lineaarne madaltihe polüetüleen ja LDPE, (PE-LD)- madaltihe polüetüleen. on madala hinna ja mitmekülgsete omadustega (sitke, tugev, veniv, keemiliselt inertne). See sulab vahemikus 100C-140C. Kus seda kasutakse? Peamiselt kasutatakse polüetüleeni veel ja rasval põhineva toidu ning jookide pakendamisel madalatel temperatuuridel, kaasa arvatud miinuskraadides. Polüetüleeni kasutatakse palju toidu (pagaritoodete, puuviljade) pakendamisel. Kõrgtihedast polüetüleenist (HDPE) saadakse termovormimisel või p...
ALKEENID JA ALKÜÜNID Propeen Propeen on värvuseta ja vees lahustumatu gaas ning ta kuulub alkeenide aineklassi. Keemistemperatuur on -47,6 C Sulamistemperatuur on -185,2 C Keemiline valem on C3H6 Eteen Eteen on normaaltingimusel värvitu gaas. See on lihtsaim alkeen. Molekulvalem on C2H4 Sulamistemperatuur -169.1 °C Keemistemperatuur -103.7 °C Buta-1,3-dieen Isopreen ehk 2-metüülbuta-1,3dieen Isopreen ehk 2-metüül-1,3-butadieen on orgaaniline ühend. Isopreen on madala keemistemperatuuriga (34,067 °C) värvitu vänge lõhnaga vedelik, mis polümeriseerub kergesti. Isopreeni keemiline valem on C5H8 ehk 2=(3) =2. Tööstuslikult saadakse isopreeni nafta termilise krakkimise produktidest. Etüün ehk atsetüleen Atsetüleen on lihtsaim alküün,mis koosneb kahest vesiniku aatomist ja kahest süsiniku aatomist kolmiksidemega seo...
Täiteained: vajalikud polümeeri kulu vähendamiseks ning materjali omaduste kujundamiseks (nt. peenestatud kvarts, kaoliin, klaaskiud, tekstiilmaterjalid) Stabilisaatorid lisatakse, et suurendada valgus ja kuumuskindlust, kaitsta oksüdeerumise eest. Plastifikaatorid suurendavad plastmassi painduvust. Enamus lisanditest on mürgised. ! Polüalkeenid Alkeenid ja asendatud alkeenid polümeeruvad liitumispolümerisatsioonil. Ahelreaktsioonides osalevad aktiivsed osakesed on kas ioonid või radikaalid, sõltuvalt tehnoloogiast. Radikaalilise või ioonilise polümerisatsiooni teel valmistatakse mitmesuguseid polüalkeene e. polüalküleene e. polüolefiine. Polüalkeenid Monomeer Polümeer Omadused Rakendused
Alkaanid on süsivesinikud, milles on üksiksidemed(CnH2n+2). Alkeenid on kaksiksidemega küllastumata süsivesinikud(CnH2n). Alküünid on kolmiksidemega ühendid(CnH2n-2). Isomeerid on ained, millel on ühesugune molekulvalem, kuid erinev struktuur ja omadused. Monomeer on üksiklüli, millest tekib polümeer. Polümeerisatsioon on polümeeri teke monomeeridest. Fünktsionaalne rühm on aatom või aatomite rühm, mis määrab aine omadused. Radikaal on vaba elektroniga osakesed; reaktsiooni võimelised. Nukleofiil on vaba või osaliselt vaba elektronpaariga negatiivselt laetud osake. Elektrofiil on tühja või osaliselt täitmata orbitaaliga positiivselt laetud osake.
· Alküünid süsivesinikud, mille molekulis esineb kolmiksidemeid. · Areenid ehk aromaatsed ühendid orgaanilised ühendid, mis sisaldavad aromaatsed tuuma. · Fenoolid hüdroksü või polühüdroksüareenid. · Hüdrogeenimine vesiniku liitumine. · Hüdraatimine vee liitumine. 2. Alkeenide, alküünide ja areenide nomenklatuur. 3. Alkeenide, alküünide ja areenide füüsikalised omadused. · Alkeenid, alküünid on meeldiva lõhnaga, värvusetud gaasid. · Areenid on vedelikud või kristalsed ained. Ei lahustu vees, küll aga süsivesinikes, eetris ja teistes mittepolaarsetes lahustites. Benseen lahustab hästi vaikusid, rasvu ja teisi vähepolaarseid aineid. 4. Alkeenide, alküünide ja areenide esindajaid. · Eteen e. etüleen CH2=CH2 on värvusetu, nõrga meeldiva lõhnaga. Narkootilise toimega gaas,
Suurem osa toodetud eteenist läheb polüeteeni valmistamiseks, kuid eteenist saadakse ka etanooli. Etüün e. Atsetüleen CHCH on meeldiva lõhnaga narkootiliste omadustega värvusetu gaas. Teda toodetakse metaanist kõrgtemperatuurilise pürolüüsi teel. Etüün on keemiatööstuses väga oluline lähteaine paljude saaduste valmistamisel. Etüüni segu õhu või hapnikuga on väga plahvatusohtlik. Terpeenid- lahtise süsinikahelaga või tsüklilised looduslikud alkeenid. Neid leidub väga erinevates organismides, eriti taimedes. Paljud terpeenid on meeldiva lõhnaga: limoneen(sidruni koor), karoteen(porgandi värvaine) Amiin- ammoniaagi (NH3) derivaat, kus vesiniku aatomi asemel on orgaaniline rühm või rühmad. Amiine leidub looduses, enamikel amiinidel on ebameeldiv lõhn. Hüdraatimine-veega liitumine (CH2=CH2+H2O->CH3-CH2-OH tekib alkohol) (alkaanide puhul) (CHCH+H2O->CH3CHO) (alküünide puhul) Hüdrogeenimine-vesinikuga liitumine
KT nr 3 mõisted. Mittepolaarse kordse sidemega ühendid Alkeenid – süsivesikud, mille molekulis esineb kaksiksidemeid Alküünid – süsivesikud, mille molekulis esineb kolmiksidemeid Kaksikside - Kolmikside -side- -sidemele lisanduv suhteliselt nõrgem side 2ik- või kolmiksideme korral küllastunud süsivesinik - alkaanid küllastumata süsivesinik – süsivesinik, mis sisaldab kordseid ühendeid hüdraatimine – vee liitmine hüdrogeenimine – vesiniku liitmine dehüdraatimine dehüdrogeenimine alküülimine aromaatne ühend aromaatne struktuur (tsükkel) – benseeni molekuli struktuur areenid – aromaatsete ühendite üldnimetus heterotsüklilised ühendid – tsükliline ühend, mille tsüklit moodustavad peale süsinike ka teiste elementide aatomid fenoolid - hüdroksüareenid fenolaat – fenooli kui happe sool delokalisatsioon – elektronide või laengute jaotumine aatomite vahel
Aineklass, Funkt- Ees- või Näited Füüsika-lised Leidumine, Keemilised omadused sio- üldvalem, järelliited omadused saamine, naalne mõiste nimetuses kasutamine rühm -aan CH4 metaan C1-C4 gaasid Maagaas(CH4) 1.)Põlemine(täielik oksüdeerumine) Alkaanid C2H6 etaan C5-C16 vedel. Nafta(vedelate CH4+2O2CO2+2H2O CnH2n+2 alkaanide segu C3H8 propaan C17-...tahked 2.)Pürolüüs(kuumutamine õhu juurdepääsuta) Küllastunud Parafiin(tahke-te süsivesinkud, C4H10 buta...
üksik side alkaan Homoloogiline rida: 1. metaan CH4 2. etaan C2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptaan C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22 kaksikside alkeen 12. eteen C2H4 13. propeen C3H6 14. buteen C4H8 15. penteen C5H10 16. hekseen C6H12 17. hepteen C7H14 18. okteen C8H16 19. noneen C9H18 20. dekeen C10H20 kolmikside alküün 32. etüün C2H2 33. propüün C3H4 34. butüün C4H6 35. pentüün C5H8 36. heksüün C6H10 37. heptüün C7H12 38. oktüün C8H14 39. nonüün C9H16 40. deküün C10H18 oh - alkohol 21. metanool CH2OH 22. etanool C2H5OH 23. propanool C3H7OH 24. butanool C4H9OH 25. pentanool C5H11OH ...
Alkaanid üksiksidemed +hal2Hhal+halalkaan -aan +O2CO2+H2O +H2alkaan +hal2dihalogeenalkaan Ainult C-H +Hhalhalogeenalkaan Alkeenid kaksikside +H2Oalkohol -een (OH/hal liitub sinna, kus on rohkem C-C sidemeid) +O2CO2+H2O Ainult C-H +H2alkeen
Orgaaniline keemia 1. Orgaanilise keemia olemus · Orgaaniline keemia tegeleb orgaaniliste ainetega o Elusorganismidest pärinevate ainete keemia · Kõik orgaanilised ained sisaldavad süsinikku · Orgaanilised ained koosnevad peamiselt süsiniku ja vesiniku aatomitest. Nende molekulid võivad sisaldada ka hapnikku, lämmastiku ja halogeenide aatomeid: C, H, O, N, Hal 2. Süsiniku erilisus · C võime moodustaa pikki ahelaid · Seotud C ühendis teise kihi S ja P elektronid võrdsed o o Väga püsiv 8 elektronist koosnev konfiguratsioon 3. Süsinik · Sp3 tetraeedriline süsinik o Nurk on 1090 o 4 üksiksidet, kõik on sigmasidemed · Sp tasandiline ehk planaarne süsinik 2 o Nurk on 1200 o Üks kaksik side ja kolm üksiksidet ...
Alkeenid -Küllastumata CH'd, mol 1 kaksikside ja teised üksiksidemed. (1sigma ja 1 side) CnH2n CH2=CH-CH2-CH3 but-1-een Need on kaks 2 buteeni isomeeri( ained, millel on CH3-CH=CH-CH3 but-2-een ühesugune koostis, aga erinev ehitus.) 3. isomeer on tsüklobutaan Omadused: Eteen on värvusetu, vees lahustumatu, nark. toimega gaas. *Looduses esineb vähe, saadakse nafta töötl. *Lihtsaim ja keem.töö. toorainena enim kasutatav alkeen (CH). 1. Põleb - CO2 + H2O (redutseerija) 2. Liitumisreakts. -side katkeb ja liitumise tulemusena tekkib vastav küllast. ühend. a) Liitumine H2-ga CH2=CH2 - CH3-CH3 b) liitumine HG-dega CH2=CH2 + Br2 - CH2Br-CH2Br (1,2 di-bromoetaan) c) H HG-dega CH2=CH2 + HCl - CH2Cl -CH3 d) H2O-ga (OH rühm) CH2=CH2 + H2O - CH3 -CH2(OH) 3. Polümeriseerub(ühe sama või erinevate ainete palju X liitumine, mille tulemusena tek-pmeer) ! n- näitab lülide arv...
Orgaaniline keemia on süsiniku ühendite keemia. Orgaaniliste ainete omadused: sageli suure molekulmassiga, kuumutamisel lagunevad, reaktsioonid sageli aeglased, ainete omadused sõltuvad aatomite järjestusest molekulis. Orgaanilised ained jaotatakse: 1)Mitte tsükliline Ahel on sirge ch3 ch2 ch2 ch3 Ahel on hargnenud ch 3 ch / ch3 ch3 2) tsükliline ch 2 ruuduna Valents näitab mitu keemilist sidet võib antud aatomil olla. Süsinik on nelja valentne. Hapnik on kolmevalentne Lämmastik on kolmevalentne Vesinik on ühevalentne Lihtsustatud struktuur valem: ch3 ch2 ch2 ch3 Molekul valem C4H10 Alkaanid on orgaanilised ained, kus süsinik aatomite vahel on üksiksidemed. Alkaanidel on nimetuses lõppliide aan. 1 meta 2 eta 3 propa 4 buta 5 penta Alkaanide esindajad Metaan CH4 - Soogaas, maagaas, kaevandusgaas Kasutatakse majapidamis gaasina Nafta on süsivesinike segu. Naftast toodetakse: bensiini, petrooliumi, kütteõli, diislit ...
Süsinikievahelise kaksiksidemega ühendeid nimetatakse alkeenideks. Süsinikevahelise kolmiksidemega ühendeid nimetatakse alküünideks. Alkaanid on küllastunud ühendid, alkeenid ja alküünid on küllastumata ühendid. Kaksikside koosneb -sidemest + -side sidemest ning selliselt seotud süsiniku aatomid on tasandilised. Kaksikside käitub nagu nukleofiilne tsenter. Seda ründavad elektrofiilid. Küllastumata ühendite reaktsioonid algavadki elektrofiili ühinemisega, millele järgneb nukleofiilseosakese ühinemine. Küllastumata ühenditega liituvad halogeenid, vesinikhalogeenid, vesi (hapekatalüütiliselt), vesinik (katalüsaatori abil)
Küllastumata ühendid -ühendid, mis sisaldavad süsiniku aatomite vahel kaksik- või kolmiksidet. ALKAANID ALKEENID ALKÜÜNID Alkaanid on niisugused süsiniku ja vesiniku Alkeenid on küllastumata süsivesinikud, mille Alküünid on süsivesinikud, mille molekulis ühendid, mille molekulides süsiniku aatomid molekulides on vähemalt üks kaksikside süsiniku esineb kolmiksidemeid. Nad on on omavahel seotud kovalentse aatomite vahel. Alkeene nimetatakse mõnikord ka reaktsioonivõimelisemad kui alkeenid ja üksiksidemega. olefiinideks. alkaanid, sest side katkeb kergesti.
ISESEISEV TÖÖ TEEMAL SÜSIVESINIKUD Koostas: Tenno Sirgi Tallinna Täiskasvanute Gümnaasium Klass: 11K1 1. Millistest keemilistest elementidest koosnevad süsivesinikud? C ja H 2. Kuidas jaotatakse keemilise sideme kordusest lähtuvalt süsivesinikud? Küllastunud või küllastumata süsivesinikud 3. Kuidas nimetatakse kinnise e. tsüklilise ahelaga süsivesinike klasse? Alkaanid, alkeenid, alküünid 4. Märkige alkaanide, alkeenide, alküünide üldvalemid ja kolm esimest liiget homoloogilistes ridades (valem, nimetus) 5. Alkaanid on keemiliselt püsivad. Kirjutage 3 võrrandit omal vabal valikul 1. Põlemine 2. Pürolüüs 3. Asendusreaktsioon 6. Alkeenid on võrreldes alkaanidega reaktsioonivõimelisemad. Kirjutage liitumisreaktsioonid: 1. Eteen+ vesinik (hüdrogeenimine) 2. Eteen+kloor (halogeenimine) 3
Looduslikkütus:kivisüsi,põlevkivi;nafta;maagaas.Tehis kütus:turbabrikett,koks;bensiin,kütteõli;generaatorigaas. Kütuse iseloomustamisel on tähtsaim tema kütteväärtus. See näitab, kui palju energiat saadakse kütuse ühiku põletamisel. Kütteväärtust alandavad mittepõlevad lisandid. Mida enam vesinikke süsiniku aatomi kohta, seda enam annab süsinikku oksüdeerida ja seda rohkem energiat kütus kannab.Separeerimisel eraldatakse toornaftas sisalduvad gaasilised süsivesinikud ja alles jäänud vesi. Stabiliseerimisel eraldub naftagaas. Keemis temperatuuri järgi jaotatakse nafta fraktsioonideks: Gaasid c1-c4 <0; Petrooleeter c5-c7 30-100; Bensiin c5-c10 40-210; Petrooleum c10-c18 150-320; Diislikütus c12-c20 200-350; Gaasiõli c14-c22 230-360; Solaarõli c20-c30 300-400; Bituumen. Krakkimisel jagunevad pikkade ahelatega molekulid kõrge rõhu ja temperatuuri või katalüsaatorite toimel väiksemateks. Termilise krakkimise põhisaadused on sirge ahelaga alk...
Eteenist saadakse ka etanooli ja vastupidi. Etüün ehk atsetüleen- CH(kolm joont)CH on hea lõhnaga ja narkootiliste omadustega värvusetu gaas. Teda toodetakse metaanist kõrgtemperatuurilise pürolüüsi teel. Etüün on väga oluline keemiatööstuses lähteainete paljude saaduste valmistamisel. Etüüni sega õhu või hapnikuga on väga plahvatusohtlik. Kasutatakse keevitamisel kui segatakse hapnikuga. Terpeenid-on lahtise süsinikahelaga või tsüklilised looduslikud alkeenid, neid leidub väga erinevates organismides, eriti taimedes. Enamus tarpeene on hea ja meeldiva lõhnaga. Limoneen (sidrunikoores), Pineen(okaspuuvaigus ja sellest destileeritud tärpentinis. Karoteen(porgandi värviaine) Kokkuvõte: Süsinikevahelist kaksiksidet sisaldavad ühendid on alkeenid, kolmiksidemega ühendid aga alküünid. Kaksikside käitub nagu nukleofiilne tsenter. Seda ründavad elektrofiilid
Aineid, mille molekulis tetraeedrilise süsiniku aatomi juures asuv vesinik on asendatud hüdroksüülrühmaga oh, nimetatakse alkoholideks. Hüdroksüülrühma olemasolust alkoholi molekulis tuleneb asendiisomeeria. Alkoholi molekulis on hapniku aatomil nukleofiilsustsenter, hapnikuga seotud süsiniku ja vesiniku aatomitel aga elektrofiilsustsentrid. Side süsinik-hapnik on palju püsivam kui side vesinik hapnik. Alkoksiidioon on väga nõrga happe anioon. Alkohol on on hape. Alkoholaat on alkoholi sool. Metanool- Ch3Oh puupiiritus. Etanool C2H5OH piiritus. Puskari õli on destillatsioonijääk etanooli eraldamisel käärimissegust. See koosneb kahest pentanooli isomeerist. Etandiool HOCH2CH2OH-etüleenglükool- diool. Antifriis-mootori jahutussegu. Glütserool- HOCH2CHOHCH2OH-looduslik. Alkaanid- CH4-metaan C2H6-etaan C3h8-propaan Alkeenid- C2H4-eteen C3H6-propeen Alküünid- C2H2-etüün C3H4-propeen Alkoholid- ch3oh-metanool c2h5oh- etanool c3h7oh- propan...
ALKÜÜNID Küllastumata süsivesinikud, kus süsinike vahel esineb kovalentne kolmikside. Nimetuse lõpp üün Üldvalem CnH2n2 Füüsikalised omadused sarnased alkeenidele. Füüsikalised omadused Homoloogilise rea 3 esimest liiget on gaasid(C 2C4), järgmised vedelikud(C5C17), alates 18ndast süsinikust on alkeenid tahked Süsiniku arvu kasvuga suureneb keemistemperatuur ja väheneb sulamistemperatuur. Sama süsinikuarvuga alkeenidel on võrreldes alkaanidega madalamad sulamis ja keemisto Hüdrofoobsed ained ja seetõttu ei lahustu vees Alkeenid on lõhnavad ühendid, narkootilise toimega Keemilised omadused Hüdrogeenimine CH#CH + H2 CH2=CH2 Halogeenimine CH#CCH3 + Br2 CHBr=CBrCH3 prop1üün reag. Broomiga
.............................................................12 3 Sissejuhatus Penteen kuulub alkeenide perekonda, valemiks on C5H12,Penteeni omadused on samad, mis tema perekonnal ehk alkeenidel. Alkeenideks küllastumata süsivesinikke, kus süsiniku aatomite vahel esineb üks kovalentne kaksikside. Alkeenid on küllastumata süsivesinikud, mille üldvalemiks on CnH2n. Alkeenide nimetuse tunnuseks on lõpuliide een. Küllastunud ainetel on süsinikahelas kõik ühekordsed sidemed ja iseloomulikud on asendumisreaktsioonid. Küllastumata ühenditel on süsinike vahel vähemalt üks kordne side ja iseloomulikud on liitumisreaktsioonid ning nad on keemiliselt aktiivsemad. Alkeenide molekulis on süsinukuahelas üks kaksikside. Küllastumatus tähendab, et
toodetakse metaanist kõrgtemperatuurilise pürolüüsi teel keemiatööstuses on väga oluline lähteaine paljude saaduste valmistamisel hapnikuga segatuna tekib põlemisel väga kõrge temperatuuriga leek, mida kasutatakse gaaskeevituseks. Etüüni segu õhu või hapnikuga on väga plahvatusohtlik Selle avastas 1836. a Edmund Davy 3. Terpeenid lahtise süsinikahelaga või tsüklilised looduslikud alkeenid neid leidub väga erinevates organismides, eriti taimedes paljud terpeenid on meeldiva lõhnaga Molekulis sisaldub 2 või enam isopreeni molekulist tulenevat lüli Üldvalem: (C H ) 5 8 n
tühja orbitaaliga aatom Markovnikovireegel: ühinemisreaktsioonil liitub elektrofiilne · Aine lahustuvus vees sõltub: hüdrofoobse C-ahela pikkusest osake kordse sideme selle C-ga, millega on seotud rohkem H-si. -OH ja NH2 rühmade arvust nukleofiilne osake selle C-ga, mille juures rohkem C-C sidemeid. · Isomeeria: - struktuuriisomeeria: molekulid koosn. samadest aatomitest, kuid · Alkeenid: nad on omavah erinevalt seotud - saadakse alkaanide dehüdrogeenimisel - C-C side nõrk - geomeetriline: aatomid paiknevad erinevalt kordsesideme suhtes - omased elektrofiilsed liitumisreaktsioonid või siis tsükloalkaanis - halogeenimine: CH2=CH2 + Cl2 = CH2Cl-CH2-Cl
Orgaaniline keemia Põhimõisted · Valents Mitu keemilist sidet elelemendid moodustavad (NB! AATOMI EHITUS!) · Süsiniku valents on 4 []1s[]2s[]2p[][] · Vesinikul on 1 · Hapnikul on 2 · Lämmastikul on 3 Valemite tüübid · Molekulvalem näitab molekuli elemendilise koostise · Struktuurvalem näitab molekuli ehituse e. Aatomite paigutuse · Lihtustatud struktuurvalem Näitab süsiniku aatomite paigutuse · Graafiline struktuur Näitab süsiniku aatomite vahelisi sidemeid ja nende asendeid Ainete koostis: C2H6O 78,4 C -23.7C Struktuuriteooria · Igal ühendil on kindel koostis ja temale omane ehitus · Ühendi omadused sõltuvad molekuli koostisest ja aatomite paigutusest e. Ehitusest · Aatomite paigutuse muutmine muudab järslult ainete omadusi Süsivesinikud C x+ Hy Alkaa...
Küllastumata ühendid on orgaanilised ained, mis sisaldavad kordset sidet. Võivad olla süsivesinikud, küllastumata alkoholid jne. Liigitus: Alkeenid een lõpuga. Alküünid üün lõpuga. Kui aines on nii kaksik-, kui ka kolmikside siis nimetuses tuleb kõigepealt kaksiksideme tunnus ja seejärel kolmiksideme tunnus. Küllastumata ühendid on omega3 rasvhapped (alkeenid) Kui nimetuses on ees di, tri.. siis ei ole üüni/eeni ees heks vaid heksA. Küllastumata ühendite isomeerid: Alkeenidel eristatakse Cis- ja transisomeere. Cisisomeeridel on asendusrühmad ühelpool tasapinda
2) Millised ained on alkaanid, nende üldvalem + nimetused Alkaanid on küllastunud süsivesinikud, mille molekulis süsiniku aatomite vahel on ühekordne kovalentne side. Üldvalem: CnH2n+2 Nimetused: CH4 metaan C2H6 etaan C3H8 propaan C4H10 butaan C5H12 pentaan C6H14 heksaan C7H16 heptaan C8H18 oktaan C9H20 nonaan C10H22 dekaan 3) Millised ained on alkeenid, nende üldvalem + nimetused Alkeenid on küllastamata süsivesinikud, mille molekulis süsiniku aatomite vahel on üks kaksikseos. Üldvalem: CnH2n Nimetused tuletatakse vastavast alkaanist, kus lõpp aan asendatakse een'iga. 4) Millised ained on alküünid, nende üldvalem + nimetused Alküüniod on küllastamata süsivesinikud, mille molekulis süsiniku aatomite vahel on üks kolmikseos. Üldvalem: CnH2n2 Nimetused tuletatakse vastavast alkaanist, kus lõpp aan asendatakse üün'iga
Mis on hüdraatimine, nitreerimine, hüdrogeenimine? Hüdraatimine - on liitumisreaktsioon veega (H2O) Nitreerimine on nitrorühma (NO2) viimine orgaanilise ühendi koostisse temasse lämmastikoksiidide või nitreerimisseguga toimides. Hüdrogeenimine on vesiniku molekuli liitmine keemilise reaktsiooni käigus Nimeta benseeni füüsikalisi omadusi. värvitu, iseloomuliku lõhnaga (mürgine!), vees lahustamatu, on ise hea lahusti lahustab hästi rasvu ja muid hüdrofoobseid aineid. Mis on alkeenid ja alküünid? Seleta mõisted ja too iga rühma kohta üks näide. Alkeenid süsinikevahelise kaksiksidemega ühendid Alküünid süsinikevahelise kolmiksidemega ühendid Mille poolest erinevad aromaatsed süsivesinikud teistest küllastumata süsivesinikest? Aromaatne ühend orgaaniline ühend, mille molekulis sisaldub aromaatne tsükkel. küllastumata ühend - süsivesinik, mis sisaldab kordseid sidemeid. Mis on aromaatsed süsivesinikud ehk areenid? Defineeri.
pehmenevad ja veelduvad ning jahtumisel tahkestuvad ( korduvalt ) - lahustuvad mingis iseloomulikus lahustis - jõu mõjul voolavad - kasutustemperatuur on madalam pehmenemistemperatuurist. · Termoreaktiivsed e. reaktoplastid ( thermosets)- võrestikstruktuuriga polümeerid- ristseotakse peamiselt kuumutamisel pöördumatult- ei pehmene ega sula kuumutamisel- lahustites ainult punduvad- jäigad ja mittevoolavad - taluvad pikaajalisi koormusi ja kõrgemat temperatuuri. Polüalkeenid Alkeenid ja asendatud alkeenid polümeeruvad liitumispolümerisatsioonil. Ahelreaktsioonides osalevad aktiivsed osakesed on kas ioonid või radikaalid, sõltuvalt tehnoloogiast. Radikaalilise või ioonilise polümerisatsiooni teel valmistatakse mitmesuguseid polüalkeene e. polüalküleene e. polüolefiine. Polüestrid On polümeersed ained, mida saadakse dikarboksüülhapetest ja mitmehüdroksüülsetest alkoholidest polükondensatsiooni teel. Tuntuim neist on lavsaan
· Liitumispolümeer saadakse siis kui kaks alkeeni polümeeruvad, liitudes kaksiksidemete arvel. · Polükondensatsioon on polümeeride saamine ühest või mitmest monomeerist, mis sisaldavad erinevaid funktsionaalseid rühmi . Funktsionaalrühmade reageerimisel eraldub näiteks vesi või alkohol. · Plastmass on aine mis koosneb polümeeri ühendist, stabilisaatoritest, plastifikaatoritest, värvainetest jpt lisaainetest. · Miks võivad alkeenid polümeriseeruda? Alkeenid on küllastumata ühendid. Alkeenidel on süsiniku aatomite vahel kaksikside, mis polümeriseerumisel katkeb. SAHHARIIDID · Sahhariidid ehk süsivesikud on biomolekulid, mis koosnevad süsiniku, vesiniku ja hapniku aatomitest. Sahhariidide hulka kuuluvad suhkur, tärklis, tselluloos jt. Sisaldavad hüdroksüül- ja karboksüül rühma. Liigitatakse Monosahhariidideks, Oligohhariidideks ja Polüsahhariidideks.
..........................................................................11 Eetrid.................................................................................................................................... 11 Amiinid.................................................................................................................................12 Alkeenid ja alküünid................................................................................................................13 Alkeenid................................................................................................................................13 Alküünid...............................................................................................................................13 Alkeenide ja alküünide isomeeria....................................................................................... 13 Keemilised omadused................................................................................
KÜLLASTUMATA ÜHENDID Küllastumata ühendid on ühendid, kus süsiniku aatomite vahel esineb kahekordne side ehk kaksikside või kolmekordne side ehk kolmikside. Esimesed neist kaanavad nime alkeenid (nimetuse lõpp een), teised nime alküünid (nimetuse lõpp üün). Nimetused antakse lähtuvalt süsiniku aatomite arvust, kordse sideme asukoht määratakse ära selle süsiniku järgi, mille järel ta asub. CH2=CHCH2CH3 1-buteen ehk but-1-een CH3CH=CHCH3 2-buteen ehk but-2-een CHCCH2CH3 1-butüün ehk but-1-üün CH3CCCH3 2-butüün ehk but-2-üün CH2=CHCH=CH2 1,3-butadieen ehk but-1,3-dieen KÜLLASTUMATA ÜHENDITE KEEMILISED OMADUSED
reaktsiooni mehhanismi analüüs; nukleofiilne asendusreaktsioon; halogeenühenditega seotud keskkonnaprobleemid; alkoholide struktuur ja omadused; funktsionaalrühm; struktuuri- ja asendiisomeeria; alkohol kui hape; vesinikside; eetrite määratlemine; alküülamiinide struktuur ja omadused; amiin kui alus. 8. MITTEPOLAARSE KORDSE SIDEMEGA SÜSINIKÜHENDID (ALKEENID, ALKÜÜNID, AREENID): küllastumatuse mõiste; alkeenid ja alküünid; kaksiksideme nukleofiilsus; elektrofiilne liitumine kaksiksidemele; areenid; aromaatsus; areenide asendusreaktsioonid; fenoolid, nende erinevus alkoholidest; delokalisatsioon; aromaatsete ühendite keskkonnaohtlikkus. 9. KARBONÜÜLÜHENDID JA KARBOKSÜÜLÜHENDID: aldehüüdide ja ketoonide struktuur; polaarne kaksikside, selle reaktsioonid; aldehüüdide redoksomadused; sahhariidide mõiste ja liigitus, bioloogiline tähtsus;
Aineklass Funktsionaalne rühm Nimetus(lõppliide) Alkaanid Üksiksidemed - -aan Halogeenühendid - - Alkoholid -OH -ool Amiinid -NH2 -amiin Alkeenid Kaksikside = -een Alküünid Kolmikside -üün Areenid Aromaatine side Benseen(tolueen) Aldehüüdid -CHO -aal Ketoonid O -oon -C- Karboksüülhapped -COOH -hape Estrid -COO- (-üül) aat Amiid O Amiid // -C NH2 Eetrid -O- -eeter
selle süsiniku aatomiga kaksiksidemes, mille juures on rohkem vesinike aatomeid. Selle tulemusena tekivad kaks radikaali (positiivse osalaenguga alküülradikaal ja negatiivse laenguga vaba elektronpaariga halogeenioon). Moodustunud radikaalid ühinevad omavahel ja saaduseks on süsivesiniku halogeeniühend. Liitumisreaktsioon halogeenidega: CH2=CH-CH2-CH=CH2 + Br2-> CH2Br - CHBr-CH2-CH=CH2 c) Liitumisreaktsioonid vesinikhalogeenidega Alkeeni liitumisel vesinikhalogeenidega annavad alkeenid samuti halogeeniühendeid ning reaktsiooniprotsess kulgeb etapiviisiliselt analoogselt nagu eelmiselgi. Vesinikhalogeniid on vesilahuses iooniline, mistõttu kaksiksidet saab rünnata ainult elektrofiiliks olev vesinikioon ehk prooton. Elektrofiilne liitumine toob süsivesiniku molekulisse elektrofiilsuse (positiivse osalaengu). Seejärel liitub negatiivse laenguga 9