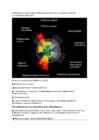
Rõngad Jupiteril on ähmaseid rõngaid nagu Saturnil, kuid palju väiksemad Erinevalt Saturnist, on Jupiteri rõngad tumedad Arvatavasti koosnevad nad väga väikestest kivise materjali teradest Osakesed Jupiteri rõngastes ei püsi seal kaua.Seetõttu, kui rõngastel on jäävad tunnused, peavad nad saama pidevalt uut gaasilist ainet Väikesed kaaslased Metis ja Adrastea, mis tiirlevad rõngaste sees, on ilmsed gaasilise aine allikate kandidaadid Kokkupõrge 1994 aastal põrkas Comet Shoemaker-Levy 9 kokku Jupiteriga Kokkupõrke tagajärjel tekkisid Jupiteri ümber kilomeetrite kõrgused "gaasimullid" ja planeedi atmosfääris võis näha hiiglaslikke auke Kuigi kokkupõrge on möödas, pole Jupiter ikka veel rahunenud Kuna tükid tabasid Jupiteri üksteise järel, kukkusid nad planeedi pöörlemise tõttu erinevatesse kohtadesse Jupiteri lõunapoolkeral
9. Milles seisneb sisehõõre? Sisehõõre on keskkonnas (vedelikus ja gaasis) liikuvale kehale mõjuv takistusjõud. 10. Kuidas muutub temperatuuri tõusul gaaside sisehõõre? Sisehõõre on gaasides seda suurem, mida kõrgem on gaasi temperatuur. 11. Millega tegeleb aerodünaamika? Aerodünaamika on teadusharu, mis tegeleb kehade liikumisega gaasides. 12. Millised on vedeliku põhiomadused? Vedel olek on midagi tahke ja gaasilise vahepealset. Vedelike kokkusurutavus on lähedane tahkete ainete kokkusurutavusele. Üheks põhiomaduseks on tema omadus voolata. Vedelikus on tihe molekulide paiknemine. Vesi võtab erinevate anumate kuju. Vedeliku kokkusurumiseks on vaja väga suurt rõhku. Vedelikus ei saa molekulid ilma põrkumata läbida oluliselt suuremat vahemaad, kui molekuli enda läbimõõt. 13. Mida nimetatakse vedelkristallideks?
Süsinikdiokssidi molaarmassi määramine Töö ülesanne ja eesmärk Töö eesmärgiks oli gaaside saamine laboratooriumis. Leida tuli seosed gaasiliste ainete mahu, temperatuuri ja rõhu vahel. Leida tuli ka gaasilise aine molaarmassi, kasutades kolme erinevat meetodit, nendeks olid molaarmassi leidmine kasutades gaasi suhtelise tiheduse võrrandit, moolide arvu ja Clapeyroni võrrandit. Sissejuhatus Gaasi suhteline tihedus: m1 M 1 D= = m2 M 2 Gaasi absoluutne tihedus: g mol dm3 /¿ ¿ Vm¿
· Happe tugevuse järgi Tugevad happedon tugevalt happeliste omadustega. Tuntumatest hapetest kuuluvad tugevate hapete hulka vesinikloriidhape, väävelhape ja lämmastikhape. Nõrgad happed on oluliselt nõrgemate happliste omadustega.Enamik tuntud hapetest on nõrgad happed. Nt süsihape, divesinikulfiidhape, fosforhape, ränihape, äädikhape e. etaanhape. ' Hapete saamisvõimalusi · Happe saamine gaasilise vesinikühendi lahustamisel vees · Happe saamine happelise oksiidi reageerimisel veega nt. P4O10 + 6H2O = 4H3PO4 · Happe kaudne saamine soola ja tugeva happe vahelises reaktsioonis. Nt: Na2SiO3 + H2SO4 = Na2SO4 + H2SiO3 Alused Alus on aine, mis annab vesilahuses hüdroksiidioone.Väheaktiivsete metallide hüdroksiidid lahustuvad vees halvasti. Enamik hüdroksiide laguneb kuumutamisel vastava metalli oksiidiks ja veeks.
Süsiniku oksüdatsiooniaste on IV . 10. Metaani omadused . Metaan on : 1) Värvusetu , 2) Lõhnatu , 3) maitsetu . Vees lahustub võrdlemisi vähe . Õhust on tublisti kergem. Põleb hästi . 11. Metaani leidumine looduses. Metaan on maagaasi põhiline koostisosa . Metaani leidub Ka mitmesugustes gaasides , mis tekivad orgaaniliste ainete lagunemisel ilma õhu juurdepääsuta (soogaas ) . Kasutatakse gaasilise kütusena . 12. Metaani põlemise võrrand CH4+202CO2+2H2O 13. Nimeta süsiniku oksiide , nende valemid. Süsiniku oksiide on kaks : CO ja CO2 . 14. Süsinikoksiidi omadused, kahjulikkus. Süsinikoksiid CO on 1) Värvusetu 2) Lõhnatu 3) Vees vähe lahustuv 4) Väga mürgine gaas Kuulub küttegaaside koostisse, CO nimetatakse ka vingukaasiks , kuna tekib süsinikuühendite põlemisel
kivisool NaCl jaKCl. Kasutus: · Tekstiili- ja paberitööstuses kasutatakse kloori peamiselt pleegitajana, keemiatööstuses rakendatakse teda orgaaniliste ühendite (värvained, ravimid, mürkkemikaalid jm.), vesinikkloriidhappe (soolhape) ja kloriidide tootmisel. · Veepuhastusjaamades klooritakse joogivett, et hävitada pisikuid. · Kloori on kasutatud ka sõjagaasina. · Naatriumkloriid e keedusool (NaCl) · Vesinikkloriidhape ehk soolhape (HCl) on gaasilise vesinikkloriidi lahus. Soolhapet kasutatakse laialdaselt tööstuses. Vesinikkloriidhapet kasutatakse metallipinna puhastamiseks jootmis- ja tinatamistöödel, keemiatööstuses kloriidide saamiseks, orgaaniliste ühendite tootmisel jm. Ka inimese maomahl sisaldab 0,5% HCl, mis võtab osa toiduainete seedimisprotsessist. Vesinikkloriidhape on kõikide metallikloriidide lähtehape. Vesinikkloriidhappe(HCl) ehk soolhappe saamine: · Laboritingimustes saadakse soolhapet kontsentreeritud
ρo=29/22,4= 1,29 g/dm3; veeauru tihedus ρo=18/22,4= 0,80 g/dm3 Ideaalgaaside seadused (Boyle`i, Charles`i, Daltoni[ülal]) Boyle`i seadus- konstantsel temperatuuril on kindla koguse gaasi maht (V) pöördvõrdelises sõltuvuses rõhuga (P). PV= const. P1/P2=V2/V1 Charles`i seadus- konstantsel rõhul on kindla koguse gaasi maht võrdelises sõltuvuses temperatuuriga V/T=conts. V1/T1=V2/T2. Sealt selgub universaalne gaasikonstant: ühe mooli gaasilise aine korral PV/T=R (konstant) PV=nRT ehk PV=[m/M]RT Avogadro seadus- kõikide gaaside võrdsed ruumalad sisaldavad ühesugusel temperatuuril ja rõhul võrdsel arvul molekule (-väärisgaaside korral aatomeid). Kui normaaltingimustel on 1,0 mooli gaasi maht ehk molaarruumala Vm=22,4dm3/mol, siis standardtingimustel Vm=22,7 dm3/mol. Molaarmass (M, g/mol) on ühe mooli aine molekulide (aatomite, ühe mooli ioonide) mass grammides. Ideaalgaaside seadused.
ja vabastatakse CO2 st, seejärel jahutatakse astmeliselt põhikomponentide eraldamiseks, kuni saadakse küllalt puhas He. Omadused : Kõige inertsem tuntud ainetest. Ei moodusta keemilisi ühendeid ega klatraate. Molekulidevahelised vastasmõjud on heeliumis väiksemad kui üheski teises aines. He aatom (ühtlasi molekul) on molekulaarsete st struktuuridest lihtsaim. Vähe kerge gaas, veskinikust vaid 1,98 korda suurema tihedusega (õhust 7 korda kergem). Sellest tuleneb gaasilise He suur difusioonivõim e (tungib kiiresti läbi väikeste avade, omab head jahutusvõimet, läbib kergesti õhukesi kilesid). He läbib ka paljusid metalle (läbimatud on raud ja plaatinametall id), polümeere, klaasi (tugevasti sõltuvalt klaasiliigist) jt materjale. Parim gaasiline elektrijuht; soojusjuhtivuselt 2.kohal (vesiniku järel). Erakordselt vähelahustuv vees jt polaarsetes, sh bioloogilistes vedelikes. Sellel põhineb He kasutamine tuukrite
3. HAPPE TUGEVUSE JÄRGI TUGEVAD HAPPED - tugevalt happeliste omadustega. Tuntumad on vesinikkloriidhape(HCl), väävelhape(H2SO4) ja lämmastikhape(HNO3) NEED HAPPED ON SÖÖVITAVA TOIMEGA! NÕRGAD HAPPED - oluliselt nõrgemate happeliste omadustega. Tuntumad on süsihape(H2CO3), divesiniksulfiidhape(H2S), fosforhape(H3PO4) jpt. Kontsentreeritud tugeva happe lahjendamiseks tuleb teda valada peene joana vettel. Anorgaanilised happed - mineraalhapped Hapete saamine: Gaasilise vesinikühendi lahustamisel vees HCl(gaas) ---+h2O--> HCL(lahus Vesinikkloriid(gaas) --> vesinikkloriidhape Happelise oksiidi reageerimisel veega P4O10(t) + 6H2O(v) --> 4H3PO4(l) Happe kaudne saamine soola ja tugeva happe vahelises reaktsioonis Neid hapnikhappeid, millele vastav happeline oksiid veega ei reageeri(nt SiO2), saadakse kaudselt. NaSiO3(l) + H2SO4(l) ---> Na2SO4(l) + H2SiO3(t) (nool alla)
teistele (P2, T2), sealhulgas ka normaal- või standardtingimustele PVT 0 V 0 0 PT , 1.6 kus V0 on gaasi maht normaal- või standardtingimustel, P0 normaal- või standardtingimustele vastav rõhk (sõltuvalt valitud ühikutest), T0 normaal- ja standardtingimustele vastav temperatuur kelvinites (mõlemal juhul 273 K), P ja T aga rõhk ja temperatuur, mille juures maht V on antud või mõõdetud. Ühe mooli gaasilise aine korral PV const R T , 1.7 R – universaalne gaasikonstant n mooli gaasi kohta kehtib seos PV nRT ehk 1.8 m PV RT M Clapeyroni võrrand 1.9 Valemeid 1.8 ja 1.9 kasutatakse gaasi mahu leidmiseks temperatuuril T ja rõhul P, kui on teada gaasi moolide arv või mass. Järgmiste ühikute korral – rõhk P [Pa]; mass m [g]; moolide arv n [mol]; maht V [m3];
Seda seost kasutatakse gaaside mahu viimiseks ühtedelt tingimustelt (rõhk P 1, te-ur T2) teistele (P2, T2), sealhulgas ka normaal- või standartingimustele PVT 0 V0 = , P 0T kus V0- gaasi maht normaal-või standaarttingimustel P0- normaal- või standardtingimustele vastav rõhk (sõltuvalt valitud ühikutest) T0- normaal- või standardtingimustele vastav te-ur kelvinites P ja T- rõhk ja te-ur, mille juures maht V on antud või oli mõõdetud Ühe mooli gaasilise aine korral PV = const = R T n mooli gasi kohta kehtib seos PV = nRT ehk m PV = RT Clapeyroni võrrand M R- universaalne gaasikonstant Neid valemaid kasuatakse gaasi mahu leidmiseks temperatuuril T ja rõhul P, kui on teada gaasi moolide arv või mass. Gaasilise konstandi R arvuline väärtus sõltub valitud ühikutest ja omab järgmisi väärtusi: 760mmHg 22413,8 cm 3 mol mmHg cm 3 R= = 62400
praktiliselt lahustumatu · Keemilised omadused: kuna on suhteliselt aktiivne mittemetall, siis võib reageerida paljude metallide ja mittemetallidega; oksüdeerijana käitub metallide ja endast vähemaktiivsete mittemetallide suhtes, saadustena tekivad sulfiidid; redutseerijana käitub väävel aktiivsemate mittemetallide jt tugevate oksüdeerujate suhtes, moodustades positiivse oksüdatsiooniastmega (IV või VI) ühendid; väävel põleb õhtus, moodustades gaasilise vääveldioksiidi (SO2); väga tugevad üksüdeerujad (nt kuum kontsentreeritud lämmastikhape) võivad oksüdeerida väävli väävelhappeks · Keemilised omadused: S + H2 = H2S; S + Fe = FeS; S + konts. HNO3 = H2SO4; S + O2 = SO2 · Vääveldioksiid: iseloomuliku terava lõhnaga, värvuseta, veidi mürgine, õhust raskem gaas, vees lahustuv · Vääveltrioksiid: kergesti lenduv vedelik, värvuseta, lõhnatu, õhust raskem
muutuva kuju ja heledusega, väiksematest detailidest on kuulsaim nn. Suur Punane Laik, mille avastas 1666. a. Cassini.SATURN Erilised on nn Saturni rõngad. Need kujutavad endast kivipuru või härmatisetaolise pealispinnaga jäätükke. Iseloomustage asteroide, komeete ja meteoore ( mõiste, millest koosnevad) Asteroidid on väikeplaneedid, mis tiirlevad Marsi ja Jupiteri vahel.Kujutavad endast kivikamakaid.Komeedid on udused tahke tuuma (tolm + tahked gaasid CO 2 NH3 CH4) ja pika gaasilise sabaga taevakehad. Komeet kujutab endast mõne kilomeetrise läbimõõduga tuuma (kivistunud moodustis või ka tahke gaas). Aeg-ajalt satuvad meie Päikesesüsteemi suvalise trajektooriga taevakehad. Selliseid väikekehasid, mis liiguvad kosmoses vabalt ringi nimetatakse meteoorideks. Nad koosnevad kas rauast, kivist või raudkivist. 2011 PTG Leili Jaagant
säilitada osakeste keskmine kiirus. o Miks ei muutu sulamisel süsteemi temperatuur? Kristallstruktuuri mõjust vabanenud osakestele tuleb anda kineetilist energiat, et säilitada osakeste keskmine kiirus. o Milleks kulub aurustumissoojus? Molekulide omavahelise vastastikmõju ületamiseks (lahtirebimisel); Vedeliku pindpinevuse ületamiseks (pinnani jõudmisel); Paisumistööks, mis on määratud aine vedela ja gaasilise faasi tiheduste vahega ning osakestevaheliste tõmbejõudude sõltuvusega kaugusest gaasilises faasis. o Kui suur on keskmine relatiivne niiskus kõrbes, talvel keskküttega korteris, Eestis, vihmasel päeval? Kõrbes 20-30%; Talvel.... 20-30%; Eestis 60-70%; Vihmasel päeval 100%; o Kas relatiivne niiskus võib olla suurem kui 100%? Kui jah, siis kus?- Udus ja pilvedes.
oleme harjunud/nendega kohanenud Kõikide aineringete ühised jooned Süsteemsus Igal etapil ja protsessil oma kindel koht Elusorganismidel on oma osa Elemendid on kord ühe, kord teise ühendi koostises Läbivad kõiki sfääre Erinevate ainete ja elementide ringed põimuvad omavahel Globaalsed ja lokaalsed aineringed Globaalsed toimivad globaalsel tasandil, hõlmavad atmosfääri ja ökosüsteemi vahelisi protsesse (nt gaasilise komponendiga ringed N, O, H2O). Sellised ringed liidavad ühte kõik maailma organismid ja moodustavad hiiglasliku ökosüsteemi Maa biosfääri. Lokaalsed toimivad ökosüsteemisiseselt, hõlmavad elemente, mis on vähem liikuvad (nt P, Ca, K, Mg). Elemente saadakse kivimite murenemise teel. Biogeokeemiliste aineringete häirimine Eriti problemaatiline just lämmastiku (N) ja fosfori (P) ringe häiringud Põhjus: tööstuslikud ja põllumajanduslikud protsessid
Tootmine on suhteliselt lihtne ja (soojusvahetite abil) reaktsioonisfäärist eemaldada. Püriidi 1)absorptsioon vask-ammoniakaalses lahuses odav. Ammooniumnitraati toodetakse ettekuumutatud põletus on tüüpiline heterogeenne protsess tahke ja 2)pesemine vedela lämmastikuga gaasilise ammoniaagi segunemisel samuti ettekuumutatud gaasilise aine vahel, mille intensiivistamiseks püriiti 3)katalüütiline hüdreerimine (väikestel CO lahja peenestatakse. Temperatuuri tõstmist üle 900°C piirab jääksisaldustel) lämmastikhappega (joonis 9). Segunemine toimub täidise osakeste paakumine ja sulamine. Varem kasutati püriidi 5. Ammoniaagi süntees
Ideaalse gaasi olekuvõõrand p*V=m/M*R*T, kus m on gaasi mass, M gaasi molaarmass, R=8.31 J/mol*K universaalne gaasikonstant. Võrrand tähendab seda, et gaasikoguse rõhu ja ruumala korrutis on võrdeline selle absoluutse temperatuuriga. Gaasi rõhu sõltuvus massipunktide liikumise keskmisest kineetilisest energiast: p=2/3nEkin Ekin=3/2kT . Ideaalse gaasi siseenergia (U) on ideaalse gaasi massipunktide kineetiliste energiate summa: U=Ekin,i=NEkin=N3/2kT. 2Analüüsige isotermilist protsessi gaasilise süsteemi puhul. Kirjutage isotermi võrrand lähtudes gaasi olekuvõrrandist ja kujutage seda koordinaatides p ja V. Isotermiline protsess, kui gaasi temperatuur ei muutu (Boyle'i - Mariotte'i seadus pV=cont:; kahe oleku võrdlemisel saame p1V1=p2V2 ( NB! - rõhu ja ruumala suhet kujutab hüperbool ehk pöördvõrdelisus) . pV=m/M'R*T Kirjutage energia jäävuse seaduse avaldis makroskoopilise keha (termodünaamilise süsteemi) jaoks jne
püriidimaagis 35-50%-ni ningja raua sisaldus 30-40%-ni. Et toota püriidist SO2, tuleb püriiti põletada.4FeS2 + 11O2 8SO2 + 2Fe2O3Tööstuses põletatakse püriiti tavaliselt temperatuuril 700-900 °C. Kuna reaktsioon on tugevalt eksotermiline, siis vabaneb palju soojust, mida osaliselt kasutatakse ära protsessis, osa aga tuleb jahutamise teel (soojusvahetite abil) reaktsioonisfäärist eemaldada. Püriidi põletus on tüüpiline heterogeenne protsess tahke ja gaasilise aine vahel, mille intensiivistamiseks püriiti peenestatakse. Temperatuuri tõstmist üle 900°C piirab osakeste paakumine ja sulamine. Varem kasutati püriidi põletamiseks riiulahjusid, nüüd tolmpõletuse ja keevkihi ahjusid. Saadud ahjugaas sisaldab 8-12% SO2, peale selle lämmastikku, hapnikku, veeauru jt. Põletusjääk (särdam) sisaldab olenevaltpõletusprotsessi intensiivsusest (ahju konstruktsioonist) 1-3% väävlit. Väävli põletamine Tunduvalt lihtsam,
sulamistemperatuur), siis kolme faasi tasakaal on võimalik vaid ühel kindlal rõhul ja temperatuuril. Sellist rõhu ja temperatuuri väärtust nimetatakse antud aine kolmikpunkti rõhuks ja temperatuuriks. Kolmikpunktis on võimalik aine kolme faasi tasakaal juhul, kui selline süsteem on soojuslikult isoleeritud. Vee kolmikpunkt asub rõhul 6mm Hg ja 0,01 kraadi. Kolmikpunkt ei pea olema sugugi vaid gaasilise, tahke ja vedela faasi jaoks. Ta võib olemas olla ka näiteks kolme tahke faasi või ühe vedela ja kahe tahke faasi jaoks. Oluline on, et ühel kindlal rõhul ja temperatuuriväärtusel ei saa tasakaalus olla rohkem kui kolm faasi. Seetõttu ei ole võimalik ,,nelikpunktide" jne. olemasolu. Toodud väite tõestus jääb aga väljaspoole meie käsitlust. Häädemeeste Keskkool Referaat
eraldamiseks, kuni saadakse küllalt puhas He. Omadused He on: · Kõige inertsem tuntud ainetest. Ei moodusta keemilisi ühendeid ega klatraate. Molekulidevahelised vastasmõjud on heeliumis väiksemad kui üheski teises aines. He aatom (ühtlasi molekul) on molekulaarsetest struktuuridest lihtsaim. · Vähe kerge gaas, veskinikust vaid 1,98 korda suurema tihedusega (õhust 7 korda kergem). Sellest tuleneb gaasilise He suur difusioonivõime (tungib kiiresti läbi väikeste avade, omab head jahutusvõimet, läbib kergesti õhukesi kilesid). He läbib ka paljusid metalle (läbimatud on raud ja plaatinametallid), polümeere, klaasi (tugevasti sõltuvalt klaasiliigist) jt materjale. · Parim gaasiline elektrijuht; soojusjuhtivuselt 2.kohal (vesiniku järel). · Erakordselt vähelahustuv vees jt polaarsetes, sh bioloogilistes vedelikes.
Vastused: 1.Saadi kokkuleppe teel,aluseks võeti veerand meridiaan mille pandi nimi 1m. 2.pikkus- üks meeter (1m), mass- üks kilogramm(1kg), aeg üks sekund (1s) 3. 1)põhiühikutest suuremad ja väiksemad ühikud saadakse selle ühiku korrutamisel või jagamisel kümmnega, sajaga, tuhandega jnt. 2)Kordsete ühikute moodustamisel kasutatakse kindla tähendusega eesliiteid. 3)Põhiühikutest moodustatakse uusi ühikuid korrutamis või jagamistehte abil.Selliseid ühikuid nimetatakse tuletatud ühikuteks. 4.Mõõtmistulemuste vahemikku, milles tõeline väärtus asub, nimetatakse mõõtemääramatuseks 5.Hodomeeter on mõõdetaval pinnal lveerev ratas.Mõõdetakse tee pikkust. 6.Kraadiglaas.Näitab inimese keha temperatuuri. 7.Pindala ühik tuletatakse m2 pikkus korrutada iseendaga. 8.Põhiühik on 1m2 ja S 9.Otse mõõtmine on mõõteühikuga võrdlemine aga kaudsel mõõtmisel arvutatakse suurust teistet mõõdetud suuruste kaudu. 10.Ruumala abil väljendatakse ruumi suurust, mill...
rõhk 101 325 Pa (1,0 atm; 760 mm Hg) Viimasel ajal soovitatakse kasutada nn standardtingimusi: temperatuur 273,15K (0C) rõhk 100 000 Pa (0,987 atm; 750 mm Hg) Avogadro seadus: Normaaltingimustel: Standardtingimustel: Põhilised ideaalgaaside seadused: Boyle'i seadus: Charles'i seadus: Kaks eelmist kombineerides saab: Ühe mooli gaasilise aine korral: 2 R- universaalne gaasi konstant; R=8,314 J/mol·K Clapeyroni võrrand: Difusioon on aine osakeste soojusliikumisest tingitud protsess, mis viib konsentratsioonide ühtlustumisele süsteemis. Gaasi suhteline tihedus on ühe gaasi massi suhe teise gaasi massi samadel tingimustel. Õhu keskmine molaarmass on 28,96 29,0 g/mol.
Magistraaltorustik on varustatud harutorudega, mille otstes on kraanid. Kraanide otsa kinnitatakse joatorudega tuletõrjevoolikud. Veepihustussüsteemi kasutatakse nii tulekahju kustutamisel kui ka ruumide, konstruktsioonide ja inimeste kaitsmisel tuleohtlike temperatuuride mõju eest. Sisselülitamine toimub tuletõrjepumba sisselülitamisega ja vastavate kraanide avamisega Süsihappegaas -(CO2-) kustutussüsteemid on ette nähtud tulekahju mahtkustutamiseks suletud laevaruumides gaasilise CO2-ga. Gaasiline CO2 on õhust raskem, mittetoksiline (kuid lämmatav), lasti- ning laevaruumide konstruktsiooni ning sisustust mittekahjustav aine. Süsteemid koosnevad mahutitest veeldatud süsihappegaasi hoidmiseks ja jaotustorustikest selle juhtimiseks kustutavatesse ruumidesse koos vastava juht-, kaitse- ja kontroll- mõõtearmatuuri ning hoiatus- ja signalisatsiooniseadmetega. Vedel CO2 juhitakse kustutavasse ruumi ülalt düüside kaudu. Düüsidest väljuv CO2 aurustub, jahutades
FAASI MUUTUSED Enamus aineid saavad esineda vedelal, gaasilisel või tahkel kujul. Üleminek ühest faasist teise on faasi muutus, sõltub temperatuurist ja rõhust. -tasakaalus ei saa olla rohkem kui 3 faasi, nelikpunkti pole olemas; -olekudiagrammid koostatakse katse andmete põhjal; -võimaldab öelda, millises olekus antud tingimustel aine on; Kolmikpunkt- tahke, vedel ja gaasiline olek esinevad koos; Kriitiline punkt- kaob erinevus vedela ja gaasilise faasi vahel; Olekudiagrammil üleminek tahke ja vedela faasi vahel sulamiskõver · Järsult tõusev · Vee puhul p-telje suunas kaldu kõrgemal rõhul jää sulamine madalamal temp. (1500 at, -14.1° C) · Enamasti p-teljest eemal (dP/dT>0) · Sulamiskõver on lõputu (aurustumiskõveral lõpuks kriitiline punkt) Olekudiagrammil üleminek vedela ja gaasilise faasi vahel aurustumiskõver · Lõpeb kriitilise punktiga
Toimub faasisiire, milles tahkis muutub vedelikuks. Kui vedelik kuumutada piisavalt kõrge temperatuurini, tekivad kogu vedelikus aurumullid (keemine) ja vedelik muutub gaasiks (aurustumine). 8.13.Aine oleku diagram Iga aine olekudiagrammil on vedeliku ja aurufaasi tasakaalu kõveral (keemiskõveral) olemas kriitiline punkt, millest kõrgemal algab ülekriitiline piirkond. Kriitilisest punktist edasi on vedelik ja selle aur eraldamatud ning on kadunud erinevus vedela ja gaasilise oleku vahel. Kriitilisest punktist kõrgematel rõhkudel ja temperatuuridel muudab temperatuuri ja rõhu muutus ainult fluidumi tihedust, kuid ei põhjusta ülekriitilise fluidumi üleminekut vedelasse või gaasilisse faasi. Ainete segude puhul on olukord sageli väga komplitseeritud kriitiliste punktide ja ülekriitiliste piirkondade määramisel, kuid see ei mõjuta kõige olulisemat – gaasilise ja vedela oleku eristamatust. Kriitilise punkti parameetrid on iga aine jaoks ainulaadsed.
Päikesesüstee m. Päikesesüsteemi sünd algas ligikaudu 5.miljardit aastat tagasi tähtedevahelises ruumis kogunenud gaasipilvest , mille mass oli umbes 2 päikese massi ja läbimõõt umbes 4va. Peale vesiniku ja heeliumi oli pilves ka 1-2protsenti raskemaid elemente. Raskusjõud tõmbas pilve järjest kokku , kuni aine tihedus ja temp. muutus pilve südamikus nii suureks , et kergemad aatomi tuumad , peamiselt vesiniku omad , hakkasid ühinema raskemateks ja algas "aeglane" tuumapõlemine . Kokku tõmbudes hakkas pilv pöörlema ja muutus lapikuks , moodustades protoplanetaarse pilve.Selles tekkisid omakorda keerilised tihenemistsentrid, millest moodustuvad pöörlevad protoplaneedid ja nendest suuremate ümber omakorda väiksemad ainetetiheneised, millest hiljem moodustusid planeetide kuud. Nii tekkisid : Merkuur , Maa, Veenus , Marss . Hiid planeedid Jupiter , Saturn , Uraan ja Neptuun on oma proto...
L korrutise ning Avogadro arvu NA suhtega. Siirdesoojus on aurustumissoojus, mis on vajalik ühikulise massiga vedeliku aurustamiseks teatud temperatuuril. Teatued temperatuuril tähendab seda, et mida kõrgem on vedeliku temperatuur, seda väiksem on aurustumissoojus, seda vähem tuleb juurde anda energiat. Valemid: Q=ml L= Q:m Vedeliku aurustamiseks vajalik soojushulk on arvuliselt võrdne vedeliku massi m ja aurustumissoojuse L korrutisega. Kondenseerumiseks nim gaasilise faasi muutumist vedelaks faasiks ehk osakeste tagasitulekut vedelikku. a) mitteküllastunud aur(uga) on tegemist vedeliku aurumisel vabalt pinnalt, mis tähendab, et teatud aja jooksul vedelikust lahkub rohkem osakesi, kui sama aja jooksul vedelikku naaseb. b) küllastunud aur ( umine) tekib suletud ruumis, kus algul on vedeliku kohal mitteküllastunud aur, kuid aurumise jätkumisel vedelikust osakeste lahkumisega vedeliku
mida aktiivsem on aine, seda kiiremini kulgeb reaktsioon 4.Kuidas mõjutab reaktsiooni kiirust reageerivate ainete kontsentratsioon? Mida näitab kontsentratsioon? mida suurem on lähteaine kontsentratsioon, seda kiiremini kulgeb reaktsioon ja osakesed põrkuvad. Aine kontsentratsioon väljendab aine hulka ruumala ühikus. tähis on c ja põhiühik mol/dm3 5.Kuidas mõjutab rõhk gaasiliste ainete reaktsioonikiirust? kiireneb, kuna kui tõsta rõhku, suureneb gaasilise aine hulk ruumala ühikus st. et kasvab aine kontsentratsioon. 6.Kuidas mõjutab reageerivate ainete kokkupuute pinna suurus reaktsiooni kiirust? Miks? mida peenestatum on tahke lähteaine, seda suurem on ainete vaheline kokkupuute pind st. reaktsioon on kiirem 7.Kuidas mõjutab segamine reaktsiooni kiirust? kiireneb, kuna segamisel reageerivad ained kiiremini ja ühtlasemalt 8.Kuidas mõjutab temperatuuri tõstmine reaktsiooni kiirust? Miks? Kiireneb, kuna kõrgemal temperatuuril on osakeste
Orgaanilise keemia praktikum Keemia instituut Töö pealkiri: Infrapunaspektroskoopia Teostaja:Marietta Lõo Kursus: Keemia III Töö algus Töö lõpp: Juhendaja: 25.09.2007 25.09.2007 Uno Mäeorg Kasutatud kirjandus: 1) Juhend 2) Internet Kasutatavad ained: 1) Tahke KBr 2) metaan 3) isoamüülalohol 4) bensiil 5) kloroform-CHCl3 Kasutatavad töövahendid: 1) ahhaatuhmer 2) uhmrinui 3) spaatel 4) pressivorm 5) automaatpipett 6) vatt 7) KBr plaadid 8) gaasiküvett 9) spektofotomeeter 11) kummikindad 12) vaakumpump Töö eesmärk: Määrata ära uuritavate ainete puhtus Meetodi olemus 1)Infrapunane spektroskoopia on analüüsimeetod, mis lubab (osaliselt) identifitseerida või tõestada ainete struktuuri (eeskätt iseloomulike neeldumismaksimumidega funktsionaalrühmad). 2)...
õhu pall kui ma puhun selle täis ja pigistan seda muudab se kuju aga kui ma lõpetan surve õhupallile siis ta võtab omale kuju tagasi ja näiteks paber jälle on plastne kui ma kortsutan kokku jääb ta selliseks nagu milliseks ma ta pigistasin. 6.Rõhk Rõhk on kahele pinnale näiteks anuma seintele vedceliku ja kaasi poolt valtatav mõju on rõhk. Rõhuks nimetatakse suurust mida pinnale mõjuva ja pinna osa suuruse suhtes.Kõihe lihtsam näide näitseks rõhu kohta on see, et ma võ´tan gaasilise joogi pudeli loksutan seda tekitases rõhu sinna pudelisse ja kõigelihtsam näha seda rõhku eraldumas on see kui ma võtan selle pudeli ja keeran sellel pudelil korgi maha. 7.Soojus Soojus on ühelt süsteemilt teisele energia ülekandmise mikroskoopiline moodus. Siin kandub üle ainult siseenergia ning see jääb ka uues süsteemis mikroosakeste korpäratu liikumise energiaks. Üksnäide veel miks pannakse soojus radikad akna alla. Selle pärast ,et aknast tuleb
Kuidas ja milleks seda kasutati? Millega büretti ja pipetti loputatakse? Pipett on klaastoru, mille ühes otsas on kummist pall (kokkupigistamiseks). Kasutatakse nii, et pigistatakse kummist ots kokku, klaasist otsa toru suunatakse vedelikku. Kummi pigistamisel kõrvaltähistatud noolest imes pipett vedelikku enda sisse. Vajalik mahu mõõtmiseks. Loputatakse eelnevalt sama ainega, mille mahtu hakatakse mõõtma. 15. Arvutada molaarne kontsentratsioon lahusele, mis saadakse 250 ml gaasilise vesinikkloriidi juhtimisel 1,0 liitrisse vette normaaltingimustel. V(lahusti)= 1 l= 100 ml V(HCl)= 250 ml CM=? V(lahus)=250+100= 350 ml M(HCl)= 1+35,5 g/mol Vm=22,4 dm3/mol n=V/Vm= 250/22,4=11,16 mol Vastus:11,16 mol.
Kodused ülesanded: 1. Õhu relatiivne niiskus 20 oC juures on 90%. Kui palju tekib õhu jahtumisel 5 oC-ni kondensaati? Lahendus: Andmed tabelist: P küllastatud veeaur = 17,54mmHg (20 oC juures) P küllastatud veeaur = 6,54mmHg (5 oC juures) Pvee aur 20oC juures= 17,54mmHg*0,90 = 15,8mmHg. Veeauru osarõhu suhe üldrõhku on võrdne veeauru mahuga 100 mahuühikus õhus: Vveeaur 20oC juures = (PH2O*100)/Püld = (15,8mmHg*100)/760mmHg = 2,08% Teiste sõnadega 20 oC juures, 100L õhus on 2,08L veeauru või 20,8L veeauru 1m3 (1000L) õhu kohta. Arvutame vee auru ruumala normaaltingimustel: Kus P0=760mmHg, V0=?, T0=273K. P1=760mmHg, V1=20,8L/1m3, T1=(20+273)=293K V0=(760mmHg*20,8L/1m3*273K)/(760mmHg*293K) = 19,38L/1m3 n(vee aur) = V/Vm = 19,38L/22,4L/mol = 0,865mol/1m3 m(vee aur) = n*M = 0,865mol*18g/mol = 15,6g/1m3 (20 oC juures) P vee aur 5oC juures= 6,54mmHg Püld = 760mmHg ...
tekkiv sade (mis sade tekkis?) loksutamisel lahustub ja värvus enam ei muutu. Millise värvuse annab lahusele tekkiv kompleksioon [Cu(NH3)4]2+ ? Cu2+ + 4NH3 H2O = [Cu(NH3)4]2+ + 4H2O CuSO4 + 4NH3 H2O = Cu(OH)2 + 4NH3 H2O = [Cu(NH3)4]SO4 + 4H2O Alguses tekkis valge sade Cu(OH)2 Cu(NH3)4 tõttu tekib tumesinine lahus. Katse 7 Võtta ühte katseklaasi tükk metallilist tsinki ja teise vaske. Lisada katseklaasidesse lahjendatud vesinikkloriidhapet. Jälgida gaasilise vesiniku eraldumist metalli pinnal mullikestena. Kas reaktsioon toimub mõlemas katseklaasis? Põhjendada, lähtudes metallide pingereast. Zn + 2HCl = ZnCl2 + H2 Zn on oksüdeerija ja H on reutseerija Cu + HCl Cu soolhappega ei reageeri, kuna Cu on H2 pingereas tagapool. Katse 8 Kuiva katseklaasi panna tükk vaske ja lisada ~1 ml kontsentreeritud lämmastikhapet. Millised muutused toimuvad? Mis on eralduv pruunikas gaas (mürgine!)?
Aastal 1900 avastasid Marie ja Pierre Curie, et õhk, mis on kokkupuutes raadiumiga, muutub radioaktiivseks. Ernest Rutherfordi ja Frederick Soddy uurimine kinnitas, et raadiumist eraldub õhku mingi gaas, mis pimedas helendub ja nimetasid selle nitooniks. Andre Louis Debierne täheldas, et aktiiniumi lagunemisel eraldub gaas, mille ta nimetas aktiooniks. Ka tooriumist eraldub gaas, millele anti nimetuseks emanatsioon. Tegelikult selgus, et tegemist on kõikidel juhtudel ühe ja sama gaasilise ainega, mida nimetatakse radooniks. Erinevus on vaid selles , et tegemist on radooni erinevate isotoopidega (aatomi tuumas on prootonite arv võrdne, neutronite arv erinev). Erinevate radooni isotoopide avastamise tõttu peetakse avastaja au vääriliseks järgmisi teadlasi: E.Rutherford, F.Soddy, E.Dorn, A.L. Debierne, W.Ramsay. Kõik 6 avastatud gaasi on keemiliselt väga passiivsed, seepärast anti neile inergaaside nimetus ja paigutati perioodilisussüsteemi nullrühma [LISA 5] [2, lk 92]
0 PV T 0 V = 0 1.6 PT kus V0 on gaasi maht normaal- või standardtingimustel, P0 normaal- või standardtingimustele vastav rõhk (sõltuvalt valitud ühikutest), T0 normaal- ja standardtingimustele vastav temperatuur kelvinites (mõlemal juhul 273 K), P ja T aga rõhk ja temperatuur, mille juures maht V on antud või mõõdetud. Ühe mooli gaasilise aine korral PV T = const = R 1.7 R – universaalne gaasikonstant n mooli gaasi kohta kehtib seos PV =n R T ehk 1.8 m PV = RT M Clapeyroni võrrand 1.9 Valemeid 1.8 ja 1.9 kasutatakse gaasi mahu leidmiseks temperatuuril T ja rõhul P, kui on teada gaasi moolide arv või mass.
· Keemistemperatuur: 184,35 °C · Tihedus: 4,93 g/cm3 · Värvus joodi värvus on kas metalse läikega must (tumehall) või violetne. Metalse läikega must on jood puhtal kujul kristallilisena; gaasilises olekus on jood violetne. Joodi nimetus tuleb Kreeka keelest (ids sinililla) joodi auru värvusest. · Kõvadus puhtal kujul on jood väga kõva kristalne aine. · Tahkus jood on puhtal kujul tahke aine kuid võib esineda nii gaasilise kui ka vedelana. Keemilised omadused: · Oksiidi tüüp: tugevhappeline · Ühendid: Fluoriidid: IF, IF3, IF5, IF7 Kloriidid: ICl, [ICl3]2 Bromiidid: IBr Oksiidid: I2O4, I2O5, I4O9 · Kuumutamisel tekivad toksilised aurud. Aine on tugev oksüdeerija ja reageerib süttivate ja redutseerivate ainetega . Reageerib ägedalt leelismetallidega, fosffhori,
CuSO 4 + 4NH3 * H2O = [Cu(NH3)4]SO4 + 4H2O Cu2+ + 4NH3 * H2O = [Cu(NH3)4]2+ + 4H2O Esialgselt tekkinud sade on kustutatud lubi (Cu(OH)2), mis andis lahusele valge sademe. Loksutamisel muutus lahus tumesiniseks. Selle värvuse andis kompleksühend [Cu(NH 3)4]2+. REDOKSREAKTSIOONID METALLID, METALLIDE PINGERIDA KATSE 7 Võtta ühte katseklaasi tükk metallilist tsinki ja teise vaske. Lisada katseklaasidesse lahjendatud vesinikkloriidhapet. Jälgida gaasilise vesiniku eraldumist metalli pinnal mullikestena. Zn + 2HCl = ZnCl 2 + H 2 Cu + HCl = reaktsiooni ei toimu Reaktsioon toimus ainult ühes katseklaasis. Esimeses reaktsioonis eraldus gaasiline H 2, teises katseklaasis reaktsiooni ei toimunud, kuna Cu on metallide pingereas vesinikust taga pool ehk vähem aktiivsem kui vesinik. KATSE 7 Kuiva katseklaasi panna tükk vaske ja lisada ~ 1 ml kontsentreeritud lämmastikhapet.
Kuul puuduvad nii atmosfäär kui ka magnetväli. Asteroidid on Maa tüüpi planeetide sarnased, kuid neist tunduvalt väiksemad taevakehad. Nad tiirlevad enamuses Marsi ja Jupiteri orbiitide vahel, kusjuures nende orbiidid on tihti väljavenitatud. Asteroidide läbimõõt ulatub mõnest kilomeetrist kümnete kilomeetriteni. Paljud asteroidid on korrapäratu kujuga. Oletatakse, et tegemist on kunagi eksisteerinud planeetide kildudega. Komeedid on udused tahke tuuma ja pika gaasilise sabaga taevakehad (nn. ,,sabatähed"). Tuum koosneb tolmust ja tahketest gaasidest (CO2, NH3, CH4). Saba moodustub Päikese läheduses aurustumise tõttu. Komeetide mass on alla miljondiku Maa massist, nad ei põhjusta häireid planeetide liikumises, kuid planeedid nende liikumist mõjutavad. Üldiselt eemalduvad Komeedid Päikesest sadade tuhandete aü kaugusele. Meteoorkehad tekivad komeetide lagunemisel. Nende suurus on herneterast piljardikuulini. Nende tihedus on 0,9 g/cm3
Keemiline elementkindla tuumalaenguga aatomite liik ioonlanguga aineosake Molekulaine väiksem osake, mis koosneb aatomitest tuumalaengprootonite arvu poolt määratud suurus elektronkateaatomituuma ümbritsev elektronkogum elektronide väliskihtaatomtuumast kõige kaugemal paikneb elektronkiht aatommassaatomi mass, mis on väljendatud aatomi massi ühikutest moolaine hulga ühik molaarmass 1 mooli aine mass gaasi molaarruumalaühe mooli mistahes gaasilise aine ruumala ( 22,4 ) avokaadoarvühes moolis sisaldava osakeste arv lihtainekoosneb ühe ja sama keemilise elemendi aatomitest liitainekoosneb mitme keemilise elemendi aatomitest metalllihtaine, mille aatomite väliskihil on tavaliselt 12 elektroni, mille nad kergesti loovutavad mittemetalllihtaine, mille aatomite väliskihil on 4 elektroni või rohkem indekselemendi all paremal olev arv, näitab aatomite arvu molekulis
Füüsikaline absorptsioon puhastusprotsessis seisneb heitgaasi kontakteerumises mitmesuguste vesilahustega, mille tulemusena heitgaasi üks või mitu lisandit neelduvad lahuses. Tingituna aine difusioonitakistustest nii gaasi kui vedelikupoolsel küljel toimub tavaline füüsikaline absorptsioon aeglaselt. Seda püütakse kiirendada rõhu või kineetilise energia abil. Absorptsioon on tuntud keemilise tehnoloogia protsess, mis põhineb ainete tasakaalulisel jaotusel gaasilise ja vedela keskkonna vahel. Levinuimaks absorbendiks on vesi. 4. Gaasiliste lisandite eemaldamine adsorptsiooniga Adsorptsioon on ülekandenähtus, kus aine siirdub gaasilisest faasist tahkesse faasi. Gaaside adsorptsioon põhineb mõnede eriti poorsete ja suure eripinnaga tahkete kehade omadusel valikuliselt kontsentreerida oma pinnal üksikuid gaasisegu komponente. Adsorptsioon on üldiselt pöörduv protsess st neeldunud gaasilist komponenti võib tavaliselt eraldada tahkest ainest
Millise värvuse annab lahusele tekkiv kompleksioon [Cu(NH3)4]2+ ? Cu2+ + 4NH3 H2O = [Cu(NH3)4]2+ + 4H2O CuSO4 + 4NH3 H2O = Cu(OH)2 + 4NH3 H2O = [Cu(NH3)4]SO4 + 4H2O Esimeses katseklaasis tekkis piimjas valge sade Cu(OH)2 Hüdraati lisades ja loksutades tekib tumelilla värvus [Cu(NH3)4]2+ tõttu. Redoksreaktsioonid: Katse 7. Võtta ühte katseklaasi tükk metallilist tsinki ja teise vaske. Lisada katseklaasidesse lahjendatud vesinikkloriidhapet. Jälgida gaasilise vesiniku eraldumist metalli pinnal mullikestena. Kas reaktsioon toimub mõlemas katseklaasis? Põhjendada, lähtudes metallide pingereast. Zn + 2HCl = ZnCl2 + H2 oksüdeerija H redutseerija Zn Cu + HCl = reaktsiooni ei toimu, kuna Cu on vesikikust passiivsem (pingerea põhjal). Esimeses reaktsioonis eraldus H2. Katse 8. Kuiva katseklaasi panna tükk vaske ja lisada ~1 ml kontsentreeritud lämmastikhapet. Millised muutused toimuvad
piires. Molekulidevaheline vastastikmõju suureneb või väheneb, see sõltub, kas keha soojendatakse või jahutatakse. Kui soojendatakse, siis molekulidevahelised jõud nõrgenevad, kuid energia suureneb. Milleks kulub aurustumissoojus? a)Molekulide omavahelise vastastikmõju ületamiseks (lahtirebimisel) b) Vedeliku pindpinevuse ületamiseks (pinnani jõudmisel) c) Paisumistööks, mis on määratud aine vedela ning gaasilise faasi tiheduste vahega ning osakestevaheliste tõmbejõudude sõltuvusega kaugusest gaasilises faasis. Kriitiline temperatuur- Temperatuuri väärtus, millest kõrgemal ei ole võimalik antud gaasi veeldumine rõhu mõjul. Nt H2O puhul tkr= 373° C Küllastunud aur- Aur antud temperatuuril, kus vedeliku aurumine ja kondensatsioon on tasakaalus. Keemine- Aurumise eriliik, mis leiab aset olukorras, kus antud aine auru rõhk on küllastunud.
= const = Kombineerides saab = = Seda seost kasutatakse gaaside mahu viimiseks ühtedelt tingimustelt (rõhk P1, temperatuur T1) teistele (P2, T2), sealhulgas ka normaal- või standardtingimustele V = Ühe mooli gaasilise aine korral = const = R R universaalne gaasikonstant n mooli gaasi kohta kehtib seos PV= nRT ehk PV = R T Clapeyroni võrrand Daltoni seadus. Keemiliselt inaktiivsete gaaside segu üldrõhk võrdub segu moodustavate gaaside osarõhkude summaga. Osarõhk on rõhk, mida avaldaks gaas, kui teisi gaase segus poleks. Püld = p + p + ... = pi
Kompaktluminofoorlampe on saadaval ka koos väliskestaga, mis varjab gaasiga täidetud torusid ja muudab need veelgi sarnasemaks hõõglampidega. CFL-lampide tööiga on sõltuvalt lambi tüübist ja kasutamisest 6 00015 000 tundi. Hõõglampide tööiga on ainult ligikaudu 1 000 tundi. Kompaktluminofoorlampe tuntakse nende tõhususe ja pika tööea tõttu säästulampide nime all. 3.Leek. Leek (ladina flamma ) on nähtav (valgust kiirgav), gaasiline osa tulest. Leek on gaasilise või gaasi eraldava aine intensiivse põlemise ala, milles harilikult ilmnevad valgusnähtused. Leegi loomus ja kuju sõltuvad suurel määral nii põlevast ainest kui ka põlemise tingimustest. leek koosneb kolmest osast. 1) siseosa, 2) keskosa, 3) välisosa. Madala temperatuuriga ja mittehelendav siseosa sisaldab põlevaine termilisel lagunemisel tekkinud (kuid veel mitte süttinud) gaasilisi süsivesinike. Keskosas algab süsivesinike põlemine, aga
Millise värvuse annab lahusele tekkiv kompleksioon [Cu(NH3)4]2+ ? Cu2+ + 4NH3 * H2O = [Cu(NH3)4]2+ + 4H2O CuSO4 + 4NH3 * H2O = Cu(OH)2 + 4NH3 * H2O = [Cu(NH3)4]SO4 + 4H2O Esimeses katseklaasis tekkis piimjas valge sade Cu(OH)2 Tesise katseklaasi tekkis tumesinine värvus tänu komplektsioonile [Cu(NH3)4]2+ Redoksreaktsioonid: Katse 7. Võtta ühte katseklaasi tükk metallilist tsinki ja teise vaske. Lisada katseklaasidesse lahjendatud vesinikkloriidhapet. Jälgida gaasilise vesiniku eraldumist metalli pinnal mullikestena. Kas reaktsioon toimub mõlemas katseklaasis? Põhjendada, lähtudes metallide pingereast. Zn + 2HCl = ZnCl2 + H2 Cu + HCl = reaktsiooni ei toimu Esimeses reaktsioonis eraldus H2. Teist reaktsiooni ei toimu kuna Cu on vähem aktiivsem kui H (pingerida) Katse 8. Kuiva katseklaasi panna tükk vaske ja lisada ~1 ml kontsentreeritud lämmastikhapet. Millised muutused toimuvad? Mis on eralduv pruunikas gaas (mürgine!)?
elusorganismide ainevahetusprotsessides omastatavasse vormi – keemiliste ühendite energiaks. Fotosünteesil moodustunud orgaanilised ühendid on energia- ja süsinikuallikaks kõigile neile organismidele, kes ise valgusenergiat püüdma ja siduma ei ole võimelised. Fotosüntees on ainus looduslik protsess, mille käigus moodustub molekulaarne hapnik. CO2 sidumine ja O2 eraldumine fotosünteesil on määrava tähtsusega atmosfääri gaasilise koostise stabiilsuse tagamisel. Hingamine 6.1. Mõiste, summaarne võrrand ja põhiülesanded. Hingamine on protsess, mille käigus vabastatakse orgaaniliste ainete keemiliste sidemete energia nende ainete oksüdeerimise teel, ning selle energia arvel sünteesitakse ATP. See on redoksreaktsioon, milles elektronide doonoriteks on orgaanilised ained ja elektronide lõppaktseptoriks on hapnik. Hapnik redutseerub H2O-ks, ja
NH3 H2O, kuni esialgselt tekkiv sade (mis sade tekkis?) loksutamisel lahustub ja värvus enam ei muutu. Millise värvuse annab lahusele tekkiv kompleksioon [Cu(NH3)4]2+ ? CuSO4 + 4NH3*H2O [Cu(NH3)4]SO4+ 4H2O annab lahusele tumesinise värvuse, tekib sade. Cu2+ + 4NH3*H2O [Cu(NH3)4]2+ + 4H2O Redoksreaktsioonid 5. Metallid, metallide pingerida Katse 7. Võtta ühte katseklaasi tükk metallilist tsinki ja teise vaske. Lisada katseklaasidesse lahjendatud vesinikkloriidhapet. Jälgida gaasilise vesiniku eraldumist metalli pinnal mullikestena. Kas reaktsioon toimub mõlemas katseklaasis? Põhjendada, lähtudes metallide pingereast. Zn + 2HCl ZnCl2+H2(gaas) Zn2++Cl- ZnCl2 reaktsioon toimub, sest Zn asub vesinikust vasakul. Reaktsiooni käigus eraldub H2. Cu + HCl reaktsiooni ei toimu, sest Cu asub metallide pingereas vesinikust vasakul(väheaktiivne metall). Katse 8. Katse viia läbi ja katseklaasid hoida ning tühjendada pärast
topistuse. organisatsioon ja kaltsifikatsioon- hüüve asendub tihesidekoega rekanalisatsioon- organiseerunud trombis moodustuvad sekundaarsed verevoolu kanalid. Patoloogia, kui tromb arteris- Kohalik verevarustuse vähenemine e. isheemia, mis võib viia infarkti tekkele. Patoloogia, kui tromb veenis- Venoosne hüpereemia ja tsüanootiline e. paisinfarkt. Emboolia veresoone topistumine mujalt saabunud tahke, vedela või gaasilise materjali ehk emboliga. Trombembol- enamasti lähtub alajäseme veenilaiendite tromboosist, kõige ohtlikum kopsuarteris- äkksurm Rasvembol- pikkade toruluude murdude korral ,maksa, pankrease vigastuse korral Õhkembol – operatsioonide komplikatsioonina, vereülekannetel Gaasembol – tuukrihaiguse korral; Septiline embol – nakkushaiguste ja sepsise korral; Rakkembol – kasvajate korral metastaasid või irdunud koetükikesrd aterosklerootiliste naastude piirkonnast;
Ühik g/mol. Kasutatakse keemiaalastes arvutustes. Mr ja M arvväärtused on ühe ja sama ainepuhul samad, vahe seisneb vaid ühikus. M(H2SO4)=98 g/mol MOOL aine hulga ühik, milles sisaldub Avogadro arv (NA=6,02 × 1023) loendatavat osakest, mis on sama palju kui aatomeid 12 grammis süsiniku isotoobis massiarvuga 12. aine hulk aine kogus Aine kogust mõõdetakse massi- või ruumalaühikutes, aine hulka aga moolides. MOLAARRUUMALA Vm - ühe mooli gaasilise aine ruumala. Kõikide gaaside molaarruumalad on normaaltingimustel (0°C=273 K ja rühk 101 325 Pa) Vm=22,4 dm3/mol = 22,4 l/mol GAY-LUSSACI SEADUS reageerivate ja reaktsioonil tekkivate gaaside ruumalad suhtuvad üksteisesse nagu lihtsad täisarvud. 2H2 + O2 = 2H2O 2 : 1 : 2 (ruumalade vahekord) AVAGADRO SEADUS kõikide gaaside võrdsed ruumalad sisaldavad võrdsel tempeartuuril ja võrdsel rõhul võrdse arvu gaasi molekule.
Et vesinik on tuleohtlik, hakati kasutama vesiniku asemel heeliumit, kuigi heeliumi tõstejõud on veidike väiksem 1,11 kg kui vesinikul. Vesinikku kasutatakse: · ilmajaamades - aerostaatides ja sondides; · vanasti kasutati suurtes õhulaevades ehk aerostaatides dirizaablites ja tsepeliinides, kuulsamad olid "Hindeburg" ja "Graft Zeppelin" · margariini tootmisel taimne rasv ehk õli muudetakse gaasilise vesiniku abil tahkeks rasvaks margariiniks, selle tuelmusel küllastatakse vesinike aatomite poolt taimses rasvas süsinike aatomite vahelised kaksiksidemed üksiksidemeteks · kütusena paljudes riikides on loodud autosid ja busse, mis sõidavad vesiniku põlemisreaktsiooni energial (vaata "Äripäev" 10.04.2003 lk 23); lennuk "Canberra" läks veerandi võrra kergemaks ja kolmandiku võrra odavamaks, kui ta läks üle