VÄÄVEL VÄÄVEL · Sümbol S · Mittemetall · Asub perioodilisus tabelis paremal üleval · VI A rühmas e.kalkogeenid AATOMI OMADUSED · Väliskihil 6 elektroni · Võib siduda kuni kaks elektroni, saades miinimum oks.astmeks II · Võib loovutada 6 elektroni, saades maksimum oks.astmeks VI · Elektronskeem: +16I 2)8)6) FÜÜSIKALISED OMADUSED · Kaks allotroopi- rombiline ja monokliine väävel · Värvuselt kollane · Kristalne · Vees halvasti lahustuv · Halb elektri- ja soojusjuht · Rabe · Sulamistemperatuur +110-120 C (sõltub väävli puhtusest) KEEMILISED OMADUSED · Väävel on aktiivne metall · Reageerib metallidega, aluseliste oksiididega alustega ja sooladega · Enamiku mettalidega reageerib alles kuumutamisel · Mettalidega reageerides käitub väävel oksüdeerijana ning tekivad sulfiidid N: Ca + S= Ca S Fe + S= FeS · · TÄHTSAMAD ÜHENDID · Sulfiidid (püriit) · Sulfaadid (kips) · Gaasilised ühendid (div...
Väävel Kätlin Viilukas Sisukord Omadused Allotroobid Sulfiidid Sulfaadid Kasutusalad Väävel looduses Happevihmad Lõpp Omadused Mittemetall Elektrit mitte juhtiv Keemiline valem S8 4 stabiilset isotoopi Palju allotroopseid vorme Madala sulamistemperatuuriga Kollane (rohekas punakas), rabe, Lahustub mitmetes orgaanilistes ainetes Keemiliselt aktiivne metall Allotroobid Rombiline väävel (a) Peenepulpriline väävliõis S8 rombikujulistest molekulidest. Monokliinne väävel (b) Peenete nõeljate kristallidega allotroop, mis on saadud sulatatud väävli aeglasel jahutamisel. Plastiline väävel (c,d) Mustjaspruun plastiliini taoline aine, mida saadakse väävlimassi kiirel jahutamisel. Sulfiidid Keemilised ained, mis koosnevad kahest elemendist, millest üks on väävel. Mittemetallisulfiidides on kovalentne side. Me...
Ühendid Ühendites võib vask omada kahte metallikatiooni: vähem stabiilne Cu+ ja rohkem stabiilne Cu2+, mis muudab soola siniseks või rohekassiniseks. Tähtsaim vasesool on vasksulfaat vesi (1/5), mida tavaliselt nimetatakse vaskvitrioliks CuSO4 x 5H2O. See on sinise värvusega kristallaine, mida kasutatakse puidu immutamiseks ja taimekaitsevahendite valmistamiseks. Suure tähtsusega on mitmesugused vasesulamid. Vase ja tina sulam - pronks kujunes umbes viis tuhat aastat tagasi peamiseks tööriista-, relva- ja ehtemetalliks, pannes niiviisi aluse pronksiajale. Mõned pronksliigid olid väliselt äravahetamiseni sarnased kullaga ning neid hinnati eriti kõrgelt. Juba muistsest ajast on vask olnud tornikella metall. Kellapronksis on keskmiselt 20 % tina. Teistsuguse koostisega on relvapronks, mis pidi olema kõva elastne ja kulumiskindel. Relvapronksis oli umbes 10 % tina. Vase sulam tsingiga valgevask ehk messing on heade mehaaniliste om...
Rakvere Ametikool Tõnu Kaine AL12 Mittemetallid ( Väävel ) Referaat Juhendaja : Piia Kirs Rakvere 2012 Omadused Väävlil on 4 stabiilset isotoopi, massiarvudega 32, 33, 34 ja 36. Väävel on mittemetall. Tal on rohkelt allotroopseid vorme. Tavatingimustes on stabiilne rombiline väävel. See on kollane, rabe, elektrit mittejuhtiv kristalne aine tihedusega 1,96 g/cm³. Vees kristalne väävel ei lahustu, vähesel määral lahustub orgaanilistes lahustites nagu benseen ja etanool. Lisaks halvale elektrijuhtivusele on väävel ka halb soojusjuht. Väävli hõõrumisel naha vastu omandab ta negatiivse elektrilaengu. Keemiliselt on väävel aktiivne element. Reageerib normaaltingimustel leelismetallide,leelismuldmetallide, elavhõbeda, vase ja hõbedaga. Soojendamisel kulgevad reaktsioonid ka alumiiniumi, raua, tsingi ja pliiga. Veidi suurem on aktivatsioonienergia väävli reageerimiseks mittem...
Vesinik - H2 Isotoobid: prootium 1p,1e deuteerium 1p,1n,1e triitium 1p,2n,1e • Lõhnatu,maitsetu, värvusetu gaas • kõige kergem gaas • vees väga vähe lahustuv • madal kt • redutseerija, o.a. enamasti +1, aktiivsete metallidega oksüd. -> hüdriidid, kus o.a. on -1 • molekulaarne vesinik-püsiv, atomaarne-ebapüsiv • puhas H2 põleb õhus sinaka leegiga, moodustades vee, temp. Kuni 2000oc • segu õhu või O2-ga plahvatusohtlik! • Vesiniku saamine a) tööstuses: 2H20 (elektrolüüs) -> 2H2 + O2 b) laboris: Metall+hape -> sool + vesinik nt. Zn + 2HCl -> ZnCl2 + H2 (reageeriv metall peab reageerima happega!) • kasutatakse raketikütusena, autode kütuseelemendis, metallurgias metallide reduts. oksiididest, ammoniaagi ja org. ainete tootmisel. Halogeenid - F2, Cl2, Br2, I2 • gaasid • o.a. enamasti -...
VI A rühma mittemetalle nim kalkogeenideks. Väävel leidub looduses a)ehedalt b)ühenditena (püriit,vaskläik) Väävli allotroobid 1.monokliinne väävel väävel sulatatakse ja jahutatakse aeglaselt. Tekivad nõeljad väävli kristallid 2.plastiline väävel (ebapüsiv, seismisel muutub rombiliseks väävliks) 3.rombiline väävel looduslik ja püsiv vorm. Väävli keemilised omadused: On aktiivne mittemetall, Oksüdeerijana käitub metallide ja endast vähemaktiivsete mittemetallide suhtes, Redutseerijana käitub aktiivsete mittemetallide ja tugevate Oksüdeerijate suhtes. Väävli Kasutamine: 1.tuletikutööstus 2. meditsiin (väävlisalvid) 3.väävelhappe tootmine 4.musta püssirohu komponent. Divesiniksulfiid: Saamine: H2 + S= H2S Laboris saadakse sulfiidide reageerimisel happega Na2S + 2HCl = 2NaCl + H2S. Tekkimine - valkainete lagunemisel. Looduses leidub naftagaaside, vulkaaniliste gaaside koostises. Füüsikalised omadused: 1.värvuseta 2.mädamuna lõhnaga 3.mü...
Väävel Aatomi ehitus Elektronskeem: S:+16|2)8)6) Elektronvalem: 1s22s22p63s23p4 Väliskihi ruutskeem: Leidumine looduses Väävlit leidub looduses nii ehedalt kui ka ühendite koostises ( FeS2 , PbS) Õhku saastavaid gaasilisi väävliühendeid (H2S, SO2) võib eralduda vulkaanipurskel Väävel on oluline bioelement, ta kuulub valkude koostisesse Väävli füüsikalised omadused Väävel on kollase värvusega rabe kristallaine Vees praktiliselt ei lahustu Väävli allotroopsed teisendid Rombiline väävel (püsivaim) (a) Monokliinne väävel (b) Plastiline väävel (c, d) Väävli keemilised omadused Enamiku metallidega reageerib väävel alles kuumutamisel Käitub nii redutseerija kui ka oksüdeerijana Väävli reageerimisel metallidega tekivad sulfiidid : Al+S= ......... Zn+S= .......... Väävli keemilised omadused Reageerimisel vesinikuga tekib ..... ...
VÄÄVEL 2017 Väävel on aktiivne mittemetall 16 Keemiline sümbol: S (Sulfur) Järjenumber/aatomnumber: 16 Asub 3. perioodis (elektronkattes 3 kihti) S 32,064 6 8 2 VÄÄVEL Asub VIA rühmas (väliselektrone 6) Elektronskeem: S: +16|2)8)6) Pilt 1: Vääveli paiknemine perioodilidudtsbelis KEEMILISED OMADUSED Väävel lihtainena S on nii oksüdeerija, kui redutseerija Väävli kõige madalam oksüdatsiooniaste on II. See esineb metalliühendites (sulfiidid) ja vesinikühendis (divesiniksulfiid) Väävli kõige kõrgem oksüdatsiooniaste on + VI (sulfaadid, väävelhape...
Väävel Omadused Väävlil on 4 stabiilset isotoopi, massiarvudega 32, 33, 34 ja 36. Väävel on mittemetall. Tal on rohkelt allotroopseid vorme. See on kollane, rabe, elektrit ja soojust mittejuhtiv kristallne aine. Vees kristallne väävel ei lahustu, vähesel määral lahustub orgaanilistes lahustites nagu benseen ja etanool. Keemiliselt on väävel aktiivne element. Reageerib normaaltingimustel leelismetallide, leelismuldmetallide, elavhõbeda, vase ja hõbedaga. Soojendamisel kulgevad reaktsioonid ka alumiiniumi raua, tsingi ja pliiga. Veidi suurem on aktivatsioonienergia väävli reageerimiseks mittemetallidega, mistõttu toimuvad sellised reaktsioonid kõrgematel temperatuuridel. Väävel ei reageeri kulla, plaatina, joodi, lämmastiku ja väärisgaasidega. Väävli stabiilsemad oksüdatsiooniastmed on -2, 0, 4 ja 6. Oksüdeerivas keskkonnas valdab oksüdatsiooniaste 6; redutseerivas keskkonnas on oksüdatsiooniastmed -2...
1. Allotroopia- üks ja sama keemiline element esineb mitme lihtainena. Enamasti on tingitud kahest asjaolust: 1) aatomite arv molekulis võib olla erinev. Hapnik O2 dihapnik ( harilik Värvitu gaas ( vedelana ja tahkena rõhu all kahvatusinine) molekulaarne hapnik O=O ) Lõhnatu, vees suhteliselt vähelahustuv , läbipaistev, õhust veidi raskem gaas. St0C 219 , Kt0C 183 Eluks vajalik, põlemiseks vajalik Püsiv , kuumutamisel aktiivne, oksüdeerija ( Va. F2 suhtes) 2H2 + O2 2H2O CH4 + 2O2 CO2 + 2H2O Saamine Tööstuses õhust fraktsioneerival destillatsioonil Vee...
Vask värvus varieerub punasest kuldpruunini, niiskes õhus tekib vase pinnale aja jooksul pruuni või roheka värvusega paatinakiht Teemant värvusetu, valge, hall, kollane, sinakas, must, lõhenevus täiuslik, süngoonia kuubiline, kõige kõvem mineraal, lõhenevuspindade vahele jäävad osad on oktaeedrilised Hõbe väärismetall, suhteliselt pehme, peegeldab hästi valgust Galeniit värvuselt hall, kõvadus 2,5, lõhenevus täiuslik, süngoonia kuubiline, kriips hallikasmust, läige metalne Kuld metalliläige, lõhenevus ja magnetilisus pu...
VÄÄVEL - S (Pildiallikas http://www.ut.ee/BGGM/miner/vaavel4.jpg ) Leidumine Väävel esineb looduses nii ehedal kujul kui ka ühendite koostises. Ehedalt võib väävlit leida maapinna lähedal vulkaanilistes piirkondades. (Pildiallikas http://staff.ttu.ee/~mari/Is2/s222vulkaan.jpg ) Tuntumatest väävliühenditest leidub looduses kõige enam sulfiide (FeS2 püriit, PbS galeniit , HgS kinaver jt) ja sulfaate ( CaSO4*2H2O kips jt) püriit galeniit Koostanud: Janno Puks Tallinna Arte ja Kristiine Gümnaasium kinaver kips (Pildiallikad http://www.geocities.jp/senribb/jewels/Pyrite2.jpg , http://images.geo.web.ru/pubd/2001/05/15/0001159819/pics/galenite-09-45.jpg , http://uploa...
Kordamisküsimused: VÄÄVEL 1.Väävli leidumine looduses, allotroopia (allotroobi nimi, aatomite kuju ja paiknemine, omadused erinevatel temperatuuridel Leidumine: Ehedalt võib väävlit leida maapinna lähedal vulkaanilistes piirkondades. Tuntumatest väävliühenditest leidub looduses kõige enam sulfiide (FeS2 püriit, PbS- galeniit , HgS kinaver jt) ja sulfaate ( CaSO4*2H2O kips jt) Väävel kuulub elemendina ka kivisöe, põlevkivi, nafta ja teiste fosiilsete kütuste koostisse. Väävel on tähtis element ka eluslooduses. Ta on mitme aminohappe ja valkude koostises. Keskmisest enam on väävlit juustes, karvades, küüntes, sarvedes ja sulgedes. Allotroopia-1)rombiline väävel- 2.Väävli füüsikalised omadused, väävli oksüdatsiooniastmed, oksüdatsiooniastmete arvutamine. Väävel on kollane, rabe, elektrit mittejuhtiv kristalne aine tihedusega 2,07 g/cm³. Vees kristalne väävel ei lahustu, vähesel määral lahustub...
VÄÄVEL 1)Leidumine looduses: nii ehedalt kui ka ühenditena (püriit, vaskläik) 2)Füüsikalised omadused: a) kollase värvusega b) tahke c) rabe d) vees ei lahustu e) halb soojus-ja elektrijuht. 3.Väävli allotroopsed teisendid: a) rombiline väävel: on looduslik ja püsiv vorm b) monokliinne väävel : Väävel sulatatakse ja jahutatakse aeglaselt. Tekivad nõeljad väävli kristallid. c) plastiline väävel: väävel sulatatakse ja jahutatakse kiiresti. Tekib pruun veniv mass. 4.Keemilised omadused: On aktiivne mittemetall. a) vesiniku ja metallidega käitub oksüdeerijana H2 + S = H2S Ca + S = CaS b) reaktsioonil hapnikuga käitub redutseerijana S +O2 = SO2 5. Kasutamine: tuletikutööstus, meditsiinis (salvid), musta püssirohu koostises, väävelhappe tootmiseks. ...
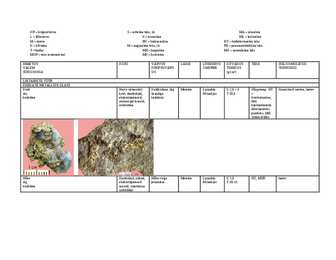
KR kriipsuvärvus S setteline teke, sh MA aluseline L lõhenevus K keemiline ML leeliseline M murre BK biokeemiline HT hüdrotermaalne teke K kõvadus M magmaline teke, sh PN pneumatolüütiline teke T- tihedus MH happeline MO moondeline teke MUR teke murenemisel MK keskmine NIMETUS KUJU VÄRVUS LÄIGE LÕHENEVU KÕVADUS TEKE ISELOOMULIKUD VALEM KRIIPSUVÄRV S MURRE TIHEDUS TUNNUSED SÜNGOO...
Kordamisküsimused riigieksamiks II Mittemetallid 1. Mis on : · Isotoop elemendi teisendid, mille tuumas on erinev arv neutrone. · Allotroopia üks ja sama keemiline element esineb mitme lihtainena. · Sublimatsioon aine muutub tahkest otse gaasiks. · Halogeen VII A rühma elemendid. · Kalkogeen VI A rühma elemendid. (mittemetallid) · Penteel V A rühma elemendid. · Tetreel IV A rühma elemendid. (mittemetallid) · Väärisgaasid VIII A rühma elemendid. · Nuuskpiiritus NH3 10% lahus · Kuningvesi H2SO4 + HNO3 konsentreeritud segu ½ vahekorras 2. Mittemetalli aatomite ehituse iseärasused. · Aatomitel tuumalaeng suhteliselt suur. · Aatomi raadius on suhteliselt suur. · Aatomite väliskihil on 4-7 elektroni (v.a. Boor) · Suhteliselt suur elektronegatiivsus. 3. Miks võivad mittemetallid oll...
HALOGEENID 1. Üldiseloomustus · Halogeenid on kõik VIIA rühma elemendid: fluor (F), kloor (Cl), broom (Br), jood (I) ja radioaktiivne astaat (At). · Lihtainena koosnevad 2 aatomilistest molekulidest (F2, Cl2, Br2, I2), kus on mittepolaarne kovalentne side. · Kõige aktiivsemad mittemetallid. · Nad kõik on omavahel sarnaste omadustega. · Kuna nad on väga aktiivsed, siis looduses neid lihtainena (puhtal kujul) ei leidu. Neid leidub mitmesuguste sooladena (NaCl). (halogeenid - soolatekitajad). · Välisel elektronkihil on 7 elektroni. Selleks et saavutada püsiv väliselektronkiht, võetakse 1 elektron juurde ja tekivad halogeniidioonid laenguga -I (Cl-, Br-). · Kõrge elektronegatiivsusega elemendid (eriti F)=>halogeenides on iooniline side. 2. Omadused · Lahustuvad vees vähe (Cl2 + H2O kloorivesi). Sama ka broomi ja ioodiga. Kloorivesi...
KEEMIA Halogeenid Halogeenid on VII a rühma elemendid. Nimetus halogeenid tähendab tõlkes soolatekitajad st et nad reageerivad metallidaga toimub ühinemis reaktsioon ja tekib sool. Sool on metall ja F2 Cl2 Br2 happeanioon halogeenid esinevad lihtainetena järgmisel kujul: J 2 F Cl Br Happeanioodides aga järgmiselt J Ja nimetustega- fluoriid -Kloriid -Bromiid -jodiid Kloor Lihtaine valem Cl2 tavatingimustes rohekas kollane õhust raskem gaas kloori lahustumisel vees saadakse kloorvesi kloorveel on tugevad oksüdeeruvad omadused sel...
Mittemetallid Omadused · Mittemetallilised omadused tugenevad vasakult paremale ja alt üles · Perioodilisustabelis paiknevad paremal ja üleval · Väliskihil on palju elektrone · Enamasti liidavad elektrone · Maksimaalne o-a on väliskihi elektronide arv ehk rühma number · Minimaalne o-a saadakse arvutamisel: väliskihi el arv 8 Erandid hapnik II ja flour I · Mittemetalli aatomid hoiavad elektrone tugevaltkinni seega on neil suur elektronegatiivsus ja raadius väike · Võivad esineda igas olekus · Ei juhi elektrit ega ka soojust · Erinevat värvi · Erinevad sulamistemperatuurid ALLOROOPIA nähtus kus üks element moodustab, mitu lihtainet · Keemilistes reaktsioonides metallidega käituvad mittemetallid alati oksüdeerijatena 2Mg +O2 2MgO · Mittemetallide omavahelistes reaktsioonides on oksüdeerija (liidab...
Mittemetalliliste elementide aatomiehituse iseärasused Mõõtmed on suhteliselt väiksemad, kui metallilistel elementidel ning neil on väliskihil rohkem elektrone, kui metallilistel elementidel. Elementidemittemetallilised omadused on seotud aatomite võimega liita elektrone. Fluor saab elektrone ainult liita. Metallid käituvad oksüdeerijana reageerimisel metallidega ja endast vähem aktiivsete mittemetallidega. Mittemetallid käituvad redutseerijana reageerimisel endast aktiivsemate mittemetallidega. Max. o.-a on vastavuses rühma numbriga. Min. o.-a. on vastavuses n-8. Vahepealne o.-a. on püsivast o.-a. 2 võrra väiksem. Püsivad o.-a. H(I); B(III); C, Si(IV); N(-III); P,As(V); O, S(-II); Se, Te(VI); F, Cl, Br, I(-I). Poolmetallid on metalliliste ja mittemetalliliste omadustega elemendid. Neil on läige, haprad, raskesti töödeldavad, elektrijuhtivuselt vahepealsed(pooljuhid) Mittemetallide ühised füüsikalised omadused · Kõik on väga erineva...
Keemia kordamisküsimused 1. Mittemetallide üldised omadused? Enamik elusorganisme sisaldavad neid. Paiknevad perioodilisuses tabelis paremal ja üleval. Maakoores on rohkem. Õhu peamised koostisosad. Väliskihil palju elektrone (4-7).Aatomiraadius suhteliselt väike, suur elektronegatiivsus. Saavad liita kui ka loovutada elektrone. Tugenevad metallidele vastupidi. Füüsikalised omadused on üksteise suhtes väga erinevad(värvus, sulamistemp.),ei juhi elektrit ega soojust, rabedad. 2. Allotroopia - nähtus, kus üks ja sama element saab esineda mitme erineva lihtainena. Isotoopia - keemilise elemendi aatomi tüüp, mis erineb massiarvu poolest. Halogeenid - VIIA rühma elemendid fluor, kloor, broom, jood, astaat. Osoon ehk trihapnik(O3) - sinakas, mürgine, terava lõhnaga gaas, laguneb. Kasut. joogivee desinfitseerimiseks. Berthollet - sool KclO3 ehk kaaluimkloraat, plahvatusohtlik, lõhk...
METALLID JA MITTEMETALLID Metallid Asukoht perioodilisussüsteemis ja aatomi ehitus Enamik nüüdisajal tuntud 118 keemilisest elemendist on metallid. Perioodilisuse tabelis asuvad nad vasak- ja keskosas ( tabeli parempoolse osa täidavad mittemetallid). Kui vaadelda perioodilisust süsteemi rühmade kaupa, siis esimene, teine ja kolmas(va. Boor) peaalarühm(A- alarühm) koosnevad ainult metallidest. Kuna peaalarühma (A- alarühm) number näitab ka välimisel elektronkihil olevate elektronide arvu, neis asuvate metallide oksüdatsioniaste ühendites on vastavalt +I, +II ja + III. Kõrvalalarühmades (B- alarühm) asuvate metallide välisel elektronkihihtidel on samuti peamiselt 1-2 elektroni. Siit järeldus- metalliaatomite välisel elektronkihil on peamiselt 1-3 elektroni. Eranditeks on Ge, Sn, Pb- väliskihil 4 elektroni; Sb, Bi- 5 elektroni. Liikumisel perioodis vasakult paremale suureneb tuumala...
Biosfäär ja selle koostisosad Biosfäär ja selle koostisosad- on see osa Maast ja teda ümbritsevast, kus on levinud elusorganismid. Haarab alumise osa troposfääri, kuni osoonikihin ca. 20km, hüdrosfääri; maakoore st litosfääri ülemise osa · Troposfäär · Hüdrosfäär · Litosfääri ülemine osa · Elusaine ehk biomass Fotosüntees: CO2+H2O+hv->CH2O+O2 CH2O-karbohüdraat- protsess, kus anorgaanilistest ainetest päikeseenergia toimel toodetakse orgaanilist ainet ja vabaneb hapnik. Atmosfääri koostis- on piirialaks Maa ja kosmose vahel. Tema kaudu toimub Maa ainevahetus kosmosega. Põhilisteks koostisosadeks on lämmastik(kaalu78,08%; mahu 75,5%) ja hapnik(20,95%;23,16%) ja veel mõned hulga teised gaasilised ained(argoon, süsinikdioksiid). Hüdrosfäär- on Maad ümbritsev veekiht. Vesi esineb kõigis kolmes agrekaatolekus. Vesi- hästi liikuv, auruna(pilvedena), on hea lahusti. Sisaldab 35 promilli lahustunud aineid, katioonides peamise...
MITTEMETALLID Mittemetallide üldiseloomustus. Mittemetalle on 22. Lihtainetena esinevad nad gaaside (H2, O2, N2, F2, Cl2, väärisgaasid), vedeliku (Br2) või tahketena (B, Si, C, P, S, I2 jt.). Perioodilisuse süsteemis paiknevad mittemetallid perioodide lõpus. Mittemetallide aatomite väliselektronkihil on enamikul juhtudesl üle kolme elektroni. Mittemetalli aatomitele on iseloomulik liita keemiliste reaktsioonide käigus elektrone. Seejuures aktiivsemad mittemetallid moodustavad negatiivselt laetud ioone (halogeniidioonid). Neil juhtudel esinevad mittemetallid oksüdeerijatena. Elementide aatomite omadus liita elektrone suureneb perioodis väärisgaasi suunas; rühmas suureneb alt ülespoole (aatomiraadiuse vähenemise suunas). Kõige aktiivsem mittemetall on fluor. Mittemetallide elektronnegatiivsus ning keemiline aktiivsus väheneb reas: F, O, Cl, N, Br, I, S, C, H, P, Si, Xe Tüüpiliste mittemetall...
1. KEEMIA PÕHIMÕISTED Gümnaasiumi lõpetaja teab ainekavas esitatud põhimõisteid ja seaduspärasusi. Gümnaasiumi lõpetaja oskab neid rakendada keemiliste nähtuste kirjeldamisel ja seletamisel, arvutus-ning probleemülesannete lahendamisel. 1)Aatom on keemilise elemendi kõige väiksem osa. Aatom koosneb tuumast ja elektronidest. 2)Tuumalaeng on aatomi tuuma positiivne laeng. On määratud prootonite arvuga tuumas. 3) Elektronkate on aatomituuma ümber tiirlevate elektronide kogum, koosneb elektronkihtidest. Väliselektronkiht on aatomituumast kõige kaugemal asuv elektronkiht, selle elektronide arv määrab elemendi omadused. 4)Keemiline element on kindla tuumalaenguga aatomite liik. 5) Ioon on laenguga osake. Positiivne ioon on katioon , negatiivne ioon on anioon. 6)Molekul on aine kõige väiksem osake. Molekul koosneb aatomitest. 7)Aatommass on aatomi mass aatommassiühikutes. 8)a)Mool on aine hulk, mis sisaldab sama pa...
Vesinik –, 1s1, esimesena sai Paracelsis, uuris Cavendish ja Lavoisier, maakoores massi järgi 0,87%, leviku poolest maal 9.kohal, universumis kõige rohkem. Saamine– suurtootmises looduslikest ja tööstuslikest gaasidest sügavjahutamise või katalüütilisel töötlemisel. Om - mõõduka aktiivsusega, lihtsaim ja kergeim element (14,5Xkergem kui õhk), o-a 1, 0, -1, molekul kaheaatomiline H2 , parim gaasiline soojusjuht, keemist 20,4K sulamist 14K, difundeerud kiiresti läbi paljude materj, lah halvasti vees ja org lahustes, raskesti poleriseeritav. Kasut – keemiatööstustes, raketikütustes, tuumaenergeetikas, termotuumapommis, keevitamisel. Ühendid – 1) hüdriidid (kui H o -a on -1), 2) vesi H2O – tähtsaim ja levinuim ühend, ¾ maa pinnast on vesi, lood vesi sis alati lisandeid (mered, ookeanid – kloriidid, mageveekogud – vesinikkarbonaadid), puhatatakse – destillatsioon, ioonvahetus, jää sulamisel ruumala väh 9%, soojusmahtuvus kasvab 2X, 3) deutee...
Keemia ja füüsika üleminekueksam 1) AATOMI EHITUSE PLANETAARNE MUDEL · Kõik ained koosnevad molekulidest ning need omakorda aatomitest. · Planetaarse mudelile rajas aluse E. Rutherford aastal 1909. · Mudeli järgi koosneb aatom tuumast, milles asuvad positiivse laenguga prootonid ja ilma laenguta neutronid. Tuuma ümber on elektronkate, mis koosneb elektronkihtidest, kus asuvad elektronid, millel on negatiivne laeng. Aatomil puudub summaarne laeng, sest prootonite ja elektronide arv on võrdne. · Elektronid tiirlevad ümber tuuma kindla raadiusega ringikujulisel orbiidil. Seespoolsed elektornkihid on kõige madalama energiaga, tuumast kaugemad on suurema energiaga. Elektronkihid täituvad energia kasvu järjekorras: esmalt kõige väiksema energiaga kihid, siis suurema energiaga. · Igasse elektronkihti mahub kindel arv elek...
Keemia 28.08.08 Sissejuhatus 1. Nimetada igapäevases elus kasutatavaid keemiatööstuse tooteid. 2. Keemilise reaktsiooni olemus, näide loodusest. 3. Mille alusel liigitatakse aineid klassidesse? 4. Lihtainete mõiste, jagunemine. 5. Liitainete mõiste, jagunemine. 1. Sool, suhkur, äädikas, jood, seep, piiritus, lõhnaõli, kodukeemia. 2. Keemilise reaktsiooni käigus toimub ühe aine muundumine teiseks. Näiteks looduses muundub vesi veeauruks, raud roostetab jne. 3. Nende koostise ja keemiliste omaduste järgi. 4. Lihtained koosnevad ainult ühe aine elementidest, jagunevad metallideks ja mittemetallideks. 5. Liitained koosnevad mitme erineva aine elementidest, jagunevad oksiidideks, hapeteks, alusteks ja sooladeks. Oksiidid Oksiidid on sellised liitained, mis koosnevad kahest elemendist, millest üks on hapnik. Oksiidid tekivad: 1) lihtaine ühinemisel hapnikuga (C+O2 -> CO...
Oksiidid Oksiidid koosnavad kahest elemendist, millest üks on hapnik. Liigitus: Metallioksiidid Mi ttemetallioksiidid Aluselised oksiidid Amfoteersed oksiidid Happelised oksiidid Neutraalsed oksiidid K2O, CaO, MgO, Al2O3, ZnO, Cr2O3 SO2, SO3, CO2, P4O10, NO2, NO, N2O, CO Na2O, FeO, BaO N2O5, N2O3, SiO2,(CrO3, Mn2O7) Keemilised omadused: Saamin e: I Aluseline oksiid+ HAPE = sool+ vesi 1.)Lihtainete põlemisel Aluseline oksiid+HAPPELINE OKSIID =sool 2.)Liitainete põlemisel Aluseline oksiid+vesi ...
1.Tähtsamad perioodilised seosed aatomite omadustes. Selgitage, kuidas muutuvad aatomiraadius, ionisatsioonienergia, elektronafiinsus, elektronegatiivsus ja polariseeritavus perioodilisustabelis. · Aatomiraadiused vähenevad perioodis vasakult paremale ja rühmas kasvavad ülalt alla. · Esimesed ionisatsioonienergiad I1 kasvavad perioodis vasakult paremale ja rühmas vähenevad ülalt alla. · Elektronafiinsused Ea on suurimad tabeli paremas ülanurgas (fluor, hapnik). · Aatomite elektronegatiivsused kasvavad perioodis vasakult paremale ja rühmas vähenevad ülalt alla. · Aatomite polariseeritavused vähenevad perioodis vasakult paremale ja rühmas kasvavad ülalt alla. Anioonid on polariseeritavamad kui vastavad aatomid tänu oma suuremale raadiusele. Polariseerivad omadused on intensiivsemad väikese raadiusega ioonidel 2.Selgitage inertpaari efekti mõne näite abil. [Omadus moodustada ioone, mille laeng on 2 võrra väiksem valentselektronide ar...
1.Vesinik Arvatavasti sai vesiniku esmakordselt 16.saj. saksa loodusteadlane T.Paracelsus. Uuris põhjalikumalt ja vesiniku avastajaks peetakse hoopis H. Cavendishi (1776). Elementaarse loomuse avastajaks on A. Lavoisier 1783. Elemendina: mõõduka aktiivsusega, o.-a. 1, 0, -1 3 isotoopi: 1H prootium ("taval." vesinik) see on nn harilik vesinik, mille aatomi tuumas on ainult üks prooton. 2H = D deuteerium ("raske vesinik") aatomi tuumas on 1 prooton ja 1 neutron. looduses (Maal) 6800 korda vähem aatomeid ; D 2 kasut. aeglustina aatomienergeetikas ja vesinikupommi komponendina. Avastati H. C. Urey jt poolt 1931.a. 3H = T triitium ("üliraske vesinik") aatomi tuumas on 1 prooton ja 2 neutronit. Sisaldus maakoores massi järgi väike (0,87%); aatomite arvu järgi suur (17% aatomi-%); leviku poolest Maal 9. kohal; universumis kõige levinum element; T on radioaktiivne beetakiirgur, mille lagunemisel tekib heeliumi isotoop. T...
Kordamisküsimused 2016/2017 õppeaastal YKI 3030 Keemia ja materjaliõpetus 1. Mateeria ja aine mõisted. Mateeria- kogu meid ümbritseva maailma mitmekesisus oma nähtuste ja asjade koguga. Mateeria peamised avaldumisvormid on aine ja kiirgus. Aine on mateeria eksisteerimise vorm, mis omab kindlat või püsivat koostist ja iseloomulikke omadusi (vesi, ammoniaak, kuld, hapnik). 2. Keemilise elemendi-, keemilise ühendi ja molekuli mõisted. Element on kogum ühesuguse tuumalaenguga (prootonite arvuga) aatomeid. Element on aine, mida ei saa keemiliste meetoditega enam lihtsamateks aineteks jagada. (109 elementi, 83 looduses) Keemilised ühendid on keemiliste elementide kogumid, väikseim iseseisev osake on molekul. Molekul - aine väikseim osake, millel on antud aine keemilised omadused ning mis võib iseseisvalt eksisteerida (O2, CO2, H2O) 3. Ainete klassifikatsioon, liht ja liitainete mõisted, näited. *Ano...
Tehnomaterjali eksami materjal 1.Metallide põhilised kristallvõred (tähised, koordinatsiooni arv, baas) Tähis tähisega tähistatakse metalli kristallivõret, nätikes K6, K8, H6 ja H12 on ka T4 ja T8. Koordinatsiooniarv on võreelemendis antud aatomile lähimal ja võrdsel kaugusel olevate aatomite arv (koordinatsiooniarv on aluseks ka kristallvõrede tähistamisel: nii tähistatakse lihtsat kuupvõre kordinatsiooniarvuga 6 tähisega K6; ruumkesendatud kuupvõret K8, tahkkesendatud kupvõret K12; lihtsat heksagonaalvõret H6, kompaktset heksagonaalvõret H12; lihtsat tetragonaalvõret T4, ruumkesendatud tetragonaalvõret T8). Baas on aatomite arv, mis tuleb võreelemnedi kohta. Kuupvõre korral kuulub tipus olev aatom 1/8-ga võreelemendile, serval 1/4-ga, aatom tahul 1/2-ga ja aatom võre sees tervenisti võreelemendile, heksagonaalvõre korral kuulub tippus olev aatom 1/6-ga võreelemendile jne. a)Ruumkesendatud kuupvõre Tähis K8; Koordi...
"Keemia alused" 3. kontrolltöö Küsimused, mis on toodud kaldkirjas, ei tule kontrolltöösse, kuid võivad esineda eksamiküsimustes. Tudeng peab teadma erinevate rühmade elementide peamiste ühendite nimetusi, oskama kirjutama ühendile vastavat keemilist valemit või vastupidi. Tudeng peab oskama kirjutama erinevate rühmade elementide peamiste ühendite tekkereaktsioone ning neid tasakaalustama. 1. Tähtsamad perioodilised seosed aatomite omadustes. Selgitage, kuidas muutuvad aatomiraadius, ionisatsioonienergia, elektronafiinsus, elektronegatiivsus ja polariseeritavus perioodilisustabelis. Aatomiraadiused vähenevad perioodis vasakult paremale ja rühmas kasvavad ülevalt alla. Aatomi raadius väheneb perioodilisuse tabelis vasakult paremale ja suureneb ülevalt alla. Igas uues perioodis lisanduvad uued elektronid järjest välimistele elektronkihtidele, mis asuvad aina kaugemal tuumast ja seetõttu suureneb raadius üleva...
1.Mateeria ja aine: Aine on mateeria eksisteerimise vorm, mis omab kindlat või püsivat koostist ja iseloomulikke omadusi (vesi, ammoniaak, kuld, hapnik).Mateeria- kogu meid ümbritseva maailma mitmekesisus oma nähtuste ja asjade koguga. Mateeria peamised avaldumisvormid on aine ja kiirgus. 2.Keemiline element on kogum ühesuguse tuumalaenguga (prootonite arvuga) aatomeid. Element on aine, mida ei saa keemiliste meetoditega enam lihtsamateks aineteks jagada. (109 elementi, 83 looduses). 3. Keemilised ühendid moodustuvad keemiliste elementide ühinemisel, kus väikseim iseseisev osake on molekul. Molekul - aine väikseim osake, millel on antud aine keemilised omadused ning mis võib iseseisvalt eksisteerida (O2, CO2, H2O). Aatomid molekulis on seotud keemiliste sidemetega. 4. lihtaine- moodustub ainult ühe ja sama keemilise elemendi aatomitest. Näiteks: hapnik, raud, elavhõbe, väävel. liitaine- koosneb erinevatest keemilistest elementidest. Näi...
YKI 3030 Keemia ja materjaliõpetus Dots. Viia Lepane rühmad 1. Mateeria ja aine mõisted. Mateeria- kogu meid ümbritseva maailma mitmekesisus oma nähtuste ja asjade koguga. Mateeria peamised avaldumisvormid on aine ja kiirgus. Aine on mateeria eksisteerimise vorm, mis omab kindlat või püsivat koostist ja iseloomulikke omadusi (vesi, ammoniaak, kuld, hapnik). 2. Keemilise elemendi mõiste. Element on kogum ühesuguse tuumalaenguga (prootonite arvuga) aatomeid. Element on aine, mida ei saa keemiliste meetoditega enam lihtsamateks aineteks jagada. (109 elementi, 83 looduses) 3. Keemiline ühend. Keemilised ühendid on keemiliste elementide kogumid, väikseim iseseisev osake on molekul. 4. Ainete klassifikatsioon, liht ja liitained. *Anorgaanilised *Orgaanilised lihtaine- moodustub ainult ühe ja sama keemilise elemendi aatomitest...
Keemia ja materjaliõpetus Kordamisküsimused 2014/2015 õppeaastal 1. Mateeria ja aine mõisted. Mateeria – kogu meid ümbritseva maailma mitmekesisus oma nähtuste ja asjade koguga. Aine – mateeria eksisteerimise vorm, mis omab kindlat või püsivat koostist ja iseloomulikke omadusi (kuld, hapnik). Keemia uurib ainete omadusi, nende koostist ja ehitust ning reaktsioone ainete vahel. 2. Keemilise elemendi mõiste. Keemiline element – Ühesuguse aatominumbriga aatomite kogum, kuulub kas liht- või liitainete koostisse. Perioodilisussüsteemis on 118 elementi. 3. Keemiline ühend. Keemiline ühend on keemiline aine, mis koosneb kahest või enamast erinevast keemilisest elemendist, mis on omavahel seotud keemiliste sidemetega. Keemilist ühendit iseloomustab alljärgnev: homogeenne molekulis olevate koostiselementide suhteline sisaldus on muutumatu molekulis on aatomid seotud kindlas järjestuses ja kindlate keemiliste sidemete kaudu, ...
KEEMIA Mateeria kogu meid ümbritseva maailma mitmekesisus oma nähtuste ja asjade koguga. Peamised avaldumisvormid on aine ja kiirgus. Aine mateeria eksisteerimise vorm, mis omab kindlat või püsivat koostist ja iseloomulikke omadusi. Keemia teadus ainete muundumisest ning nendega kaasnevatest nähtustest, uurib ainete omadusi, nende koostist ja ehitust ning reaktsioone ainete vahel, mille tulemusena moodustuvad uued ained. Element kogum ühesuguse tuumalaenguga aatomeid. (Aine, mida ei saa keemiliselt enam lihtsamateks aineteks jagada) Keemiline ühend keemiliste elementite ühinemisel moodustuv ühend. Keemiliseks aineks ei loeta sulameid ja muid segusid (nt. õhk). Molekul aine väikseim osake, millel on antud aine keemilised omadused ning mis võib iseseisvalt eksisteerida. Lihtaine moodustub ainult ühe ja sama keemilise elemendi aatomitest (O; Fe, Hg, S). Liitaine koosneb eri...
1. Mateeria ja aine mõisted. Mateeria- kogu meid ümbritseva maailma mitmekesisus oma nähtuste ja asjade koguga. Mateeria peamised avaldumisvormid on aine ja kiirgus. Aine on mateeria eksisteerimise vorm, mis omab kindlat või püsivat koostist ja iseloomulikke omadusi (vesi, ammoniaak, kuld, hapnik). 2. Keemilise elemendi-, keemilise ühendi ja molekuli mõisted. Element on kogum ühesuguse tuumalaenguga (prootonite arvuga) aatomeid. Keemilised ühendid moodustuvad keemiliste elementide ühinemisel, väikseim iseseisev osake on molekul. Molekul - aine väikseim osake, millel on antud aine keemilised omadused ning mis võib iseseisvalt eksisteerida 3. Ainete klassifikatsioon, liht ja liitainete mõisted, näited. Lihtaine - moodustub ainult ühe ja sama keemilise elemendi aatomitest. Näiteks: hapnik, raud, elavhõbe, väävel Liitaine - koosneb erinevatest keemilistest elementidest. Näiteks: vesi, lubi, süsinikdioksiid Nii liht- kui liitained võivad e...
1. Mateeria ja aine mõisted. 11. Tahkete materjalide klassifikatsioon. Mateeria- kogu meid ümbritseva maailma mitmekesisus oma nähtuste ja n Tahked materjalid (aluseks keemiline koostis): asjade koguga. 1) metallid; Mateeria peamised avaldumisvormid on aine ja kiirgus. 2) keraamika; Aine on mateeria eksisteerimise vorm, mis omab kindlat või 3) polümeerid; püsivat koostist ja iseloomulikke omadusi (vesi, ammoniaak, kuld, hapnik). 4) komposiidid- 2 või enamat materjali koos; 5) kõrgtehnoloogilised nn. "advanced" materjalid-pooljuhid, biomaterjalid, targad ("smart") materjalid, nanotehnoloogilised materjal...
1. Mateeria ja aine mõisted. Mateeria kogu meid ümbritseva maailma mitmekesisus oma nähtuste ja asjade koguga. Mateeria peamised avaldumisvormid on aine ja kiirgus. 11. Tahkete materjalide klassifikatsioon. n Tahked materjalid (aluseks keemiline koostis): Aine on mateeria eksisteerimise vorm, mis omab kindlat või 1) metallid; püsivat koostist ja iseloomulikke omadusi (vesi, ammoniaak, kuld, hapnik). 2) keraamika; 3) polümeerid; 2. Keemilise elemendi mõiste. 4) komposiidid 2 või enamat materjali...
Põhimõisted Mateeria on kõik, mis täidab ruumi ja omab massi. Aine on mateeria vorm, millel on väga erinev koostis ja struktuur. Keemia on teadus, mis uurib aineid ja nendega toimuvaid muundumisi ja muudatustele kaasnevaid nähtusi. Aatom koosneb aatomituumast ja elektronidest, elektriliselt neutraalne. Keemiline element on aatomite liik, millel on ühesugune tuumalaeng (111 elementi, 83 looduses). Molekul koosneb mitmest ühe või mitme elemendi aatomitest (samasugustest või erinevatest). Molekul on lihtvõi liitaine väikseim osake, millel on sellele ainele iseloomulikud keemilised omadused. Ioon on aatom või omavahel seotud aatomite grupp, mis on kas andnud ära või liitnud ühe või enam elektroni, omades seetõttu kas positiivse (katioon) või negatiivse laengu (anioon). Aatom, molekul Aatom koosneb aatomituumast ja elektronidest. Aatomituum koosneb prootonitest ja neutronitest. Prootonid ja neutronid ei ole jagamatud, vaid koosnevad kvarkid...
1. ELEMENTIDE RÜHMITAMISE PÕHIMÕTTED 1.1. Elementide jaotus IUPAC’i süsteemis Reeglid ja põhimõtted, kohaldatuna eesti keelele: Karik, H., jt. (koost.) Inglise-eesti-vene keemia sõnaraamat Tallinn: Eesti Entsüklopeediakirjastus, 1998, lk. 24-28 Rühmitamine alanivoode täitumise põhjal 2. ELEMENDID Vesinik Lihtsaim, kergeim element Elektronvalem 1s1, 1 valentselektron, mille kergesti loovutab → H+-ioon (prooton, vesinik(1+)ioon) võib ka siduda elektroni → H- (hüdriidioon, esineb hüdriidides) Perioodilisusesüsteemis paigutatakse (tänapäeval) 1. rühma 2.1.1. Üldiseloomustus Gaasiline vesinik – sai esimesena Paracelsus XVI saj. – uuris põhjalikult H.Cavendish, 1776 – elementaarne loomus: A.Lavoisier, 1783 Elemendina: mõõduka aktiivsusega, o.-a. 1, 0, -1 3 isotoopi: 1 H – prootium (“taval.” vesinik) 2 H = D – deutee...
Kordamisküsimused 2015/2016 õppeaastal YKI 3030 Keemia ja materjaliõpetus 1. Mateeria ja aine mõisted. Mateeria- kogu meid ümbritseva maailma mitmekesisus oma nähtuste ja asjade koguga. Mateeria peamised avaldumisvormid on aine ja kiirgus. Aine on mateeria eksisteerimise vorm, mis omab kindlat või püsivat koostist ja iseloomulikke omadusi (vesi, ammoniaak, kuld, hapnik). 2. Keemilise elemendi-, keemilise ühendi ja molekuli mõisted. Element on kogum ühesuguse tuumalaenguga (prootonite arvuga) aatomeid. Element on aine, mida ei saa keemiliste meetoditega enam lihtsamateks aineteks jagada. (109 elementi, 83 looduses) Keemilised ühendid on keemiliste elementide kogumid, väikseim iseseisev osake on molekul. Molekul - aine väikseim osake, millel on antud aine keemilised omadused ning mis võib i...
Keemia ja materjaliõpetus 1. Sõnastage ja kommenteerige (millistel juhtudel on vaja neid arvestada või kasutada) Elementide ja nende ühendite omaduste muutumise perioodilisus: Keemil elem ja nendest moodust liht-ja liitainete omad on perioodilises sõltuvuses elementide aatomite tuumalaengust (elementide aatommassidest). Iga periood v.a. esimene algab aktiivse metalliga, lõpeb väärisgaasiga. Perioodi piires elementide järjenumbri kasvamisel nõrgenevad metallilised ja tugevnevad mittemetallilised omad. Suurtes perioodides nn pea- kui ka kõrvalalarühmade elementide omad korduvad perioodiliselt. Kahe esimese peaalarühma elemendid asuvad perioodi paarisarvulistes, ülejäänud paarituarvulistes ridades. Paarisarvulistes ridades on ülekaalus metallilised omad. Metallilised omadused tugevnevad peaalarühmas ülalt alla, mittemetallilised omadused ag...
1.Elemendi ja lihtaine mõisted ja nimetused ning nende mõistete õige kasutamine praktikas. Süsteemsuse olemus ja süsteemse töötamise vajalikkus inseneritöös. Näiteid praktikast. Milline on süsteemne materjalide korrosioonitõrje? Element Keemiline element ehk element on aatomituumas sama arvu prootoneid omavate (ehk sama aatomnumbriga) aatomite klass.Teise definitsiooni järgi on keemiline element aine, milles esinevad ainult ainult ühe ja sama aatomnumbriga aatomid. Lihtaine - Lihtaine on keemiline aine, mis koosneb ainult ühe keemilise elemendi aatomitest. Lihtaines võivad elemendi aatomid olla isoleeritud või moodustada mitmest ühesugusest aatomist koosnevad molekulid. Näiteks kloor ja fluor esinevad ainetena Cl2 ja F2, Süsteemsus Kõik keemilised tehis- ja looduslikud protsessid kujutavad endast süsteemi, milles on ained, kemikaalid, seadmed, keskkond ja mõjutegurid. Näited: Etanooli valmistamine. Koosneb tooraine (kartul, teravil...
Autorid: Priit Kulu Jakob Kübarsepp Enn Hendre Tiit Metusala Olev Tapupere Materjalid Tallinn 2001 © P.Kulu, J.Kübarsepp, E.Hendre, T.Metusala, O.Tapupere; 2001 SISUKORD SISSEJUHATUS ................................................................................................................................................ 4 1. MATERJALIÕPETUS.............................................................................................................................. 5 1.1. Materjalide struktuur ja omadused ...................................................................................................... 5 1.1.1. Materjalide aatomstruktuur........................................................................................................... 5 1.1.2. M...
Keemia ja materjaliõpetus 1. Elemendi ja lihtaine mõisted/nimetused ning nende mõistete õige kasutamine praktikas. Süsteemsuse olemus ja süsteemse töötamise vajalikkus inseneritöös. Näiteid praktikast. Milline on süsteemne materjalide korrosioonitõrje? Keemiline element ehk element on aatomituumas sama arvu prootoneid omavate aatomite klass. Teise definitsiooni järgi on keemiline element aine, milles esinevad ainult ühe ja sama aatomnumbriga aatomid. Seega keemiline element on aine, mida ei saa keemiliste meetodite abil lihtsamateks aineteks lahutada. Lihtaine on keemiline aine, mis koosneb ainult ühe keemilise elemendi aatomitest. Näiteks puhtad metallid ja gaasid. Elementide ja nendest moodustunud lihtainetel on enamikel juhtudel üks ja sama nimi, st tuleb alati selgitada, kas tegemist on mingi elemendi aatomitega mõnes aines või selle elemendi aatomitest moodustunud puhta lihtainega või ...
1. Keemiline element ehk element on aatomituumas sama arvu prootoneid omavate (ehk sama aatomnumbriga) aatomite klass. Lihtaine on keemiline aine, milles esinevad ainult ühe elemendi aatomid, keemilises reakts ei saa seda lõhkuda lihtsamateks aineteks. Lihtaine valemina kasut vastavate elementide sümboleid (üheaatomilised: Fe, Au, Ag, C, S; kaheaatomilised: H2, O2, F2, C12, Br2). Enamik elementidele vastavaid lihtaineid on toatemp-l tahked ained või gaasid. Kasutamine: kui otsime mõnda elementi mendelejevi tabelist või tahame kirja panna reaktsiooni võrrandit. Keemiliste elementide ja nendest moodustunud liht- ja lihtsamate liitainete omadused on perioodilises sõltuvuses elementide aatomite tuumalaengust (elementide aatommassidest). (Iga periood v.a. esimene algab aktiivse metalliga, lõpeb väärisgaasiga. Perioodi piires elementide järjenumbri kasvamisel nõrgenevad metallilised ja tugevnevad mittemetallilised omadused. Metallilised omadu...
www.eaei-ttu.extra.hu 1) Elementide omaduste perioodilisusseadus: Keemiliste elementide ja nendest moodustunud liht- ja lihtsamate liitainete omadused on perioodilises sõltuvuses elementide aatomite tuumalaengust (elementide aatommassidest). (Iga periood v.a. esimene algab aktiivse metalliga, lõpeb väärisgaasiga. Periodi piires elementide järjenumbri kasvamisel nõrgenevad metallilised ja tugevnevad mittemetallilised omadused. Suurtes perioodides nii pea- kui ka kõrvalalarühmade elementide omadused korduvad perioodiliselt. Kahe esimese peaalarühma elemendid asuvad perioodi paarisarvulistes, ülejäänud paarituarvulistes ridades. Paarisarvulistes ridades on ülekaalus metallilised omadused. Metallilised omadused tugevnevad peaalarühmas ülalt alla, mittemetallilised omadused aga nõrgenevad. VII peaalarühmas on tüüpilised mittemetallid. Alates III peaalarühmast nim suurte perioodide paarisarvuliste ridade elemente siirdeelementideks. ...