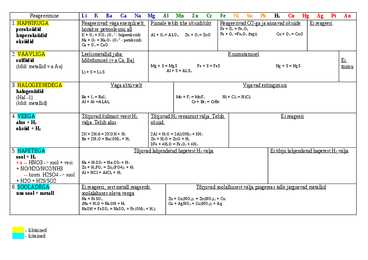
Reageerimine Li K Ba Ca Na Mg Al Mn Zn Cr Fe Ni Sn Pb H2 Cu Hg Ag Pt Au 1. HAPNIKUGA Reageerivad väga energiliselt, Pinnale tekib tihe oksiidikiht Reageerivad O2-ga ja annavad oksiide Ei reageeri peroksiidid hoitakse petrooleumi all Fe + O2 = Fe2O3 hüperoksiidid K + O2 = KO2 (O2-1 - hüperoksiid) Al + O2 = Al2O3 Zn + O2 = ZnO Fe + O2 =Fe3O4 (tagi) Cu + O2 = CuO oksiidid Na + O2 = Na2O2 (O2-2 - peroksiid) Ca + O2 = CaO 2. VÄÄVLIGA Leelismetallid juba Kuumutamisel sulfiidid hõõrdumisel (v.a Ca, Ba) ...
Orgaaniline keemia kordamine 1) Mis on orgaaniline keemia? Süsinikühendite ja kovalentsete sidemete keemia. 2) Millised elemnedid kuuluvad org. elementide koostisesse? Põhilised elemendid on hapnik, lämmastik, vesinik, väävel, halogeenid, fosfor, räni jt. 3) Põhielementide valentsid ja valentsolekud. C valents 4, valentsolekuid 3; N valents 3, valentsolekuid 3; O valents 2, valentsolekuid 2; H valents 1, valentsolekuid 1. 4) Süsiniku o.a ja selle arvutamine. Süsiniku o.a väärtused ulatuvad -4 kuni +4. VIHIKUST?? 5) Mis on süsivesinikud? Keemilised ained, mis koosnevad ainult süsinikust ja vesinikust. 6) Mis on isomeeria? Ühendid, millel on sarnane summaarne valem kuid erinev struktuur. 7) Mis on alkaanid? Süsivesinikud, mille molekulis süsinike aatomite vahel on ainult ühekordsed kovalentsed sidemed. 8) Alkaanide füüsikalised omadused. Ve...
Areenid. Areenid aromaatsed süsivesinikud, mis sisaldavad benseeni tuuma. Benseeni tuumas on süsinike vahel nn. pooleteistkordsed sidemed. Benseeni füüsikalised omadused: Veest kergem Iseloomuliku lõhnaga Värvusetu vedelik Keemis temp. 80 C Sulamis temp. 5,5 C Ei lahustu vees Lahustub hästi orgaanilistes lahustites Benseen ja tema aurud on mürgised ja õhu käes kergesti süttivad. Benseen on ise hea lahusti rasvadele, valkudele ja paljudele süsivesinikele. Keemilised omadused: 1) Reageerimine lämmastikhappega 2) Reageerimine Halogeenidega Katalüsaator AlCl abil ERAND! Kui Benseeni tuuma juures on juba aktiveeriv rühm (aminorühm, alküülrühm, hüdroksüülrühm) siis toimub asendusreaktsioon 2, 4 ja 6 süsiniku juures . 3) Fenoolide (aromaatsed alkoholid) reageerimine leelistega . 4) Aromaatsed nitroühendid regutseeruvad ja tekivad aromaatsed amiinid. 5) E...
Leelismetallid Li, Na, K, Rb, Cs, Fr Leidumine looduses: · Looduses leidub neid ainult ühenditena. · Põhilielt esinevad kloriididena: naatriumkloriid(merevees,pinnases), kaaliumkloriid(pinnases, taimedes), liitiumkloriid, teised esinevad maakide koostises · Karbonaatidena: Na2CO3 · Sulfaatidena: Na2SO4, K2SO4 · Nitraatide ehk salpeetritena: NaNO3, KNO3 Aatomi ehitus: Na e=11, p1=11, n1=12 Na+11|2)8)1) 1s2 2s2 2p6 3s1 o-a.1 · Leelismetallide aatomid paiknevad kristallvõres suhteliselt hõredalt, see tingib nende väga väikese tiheduse. · Pehmed metallid, kergesti lõigatavad Füüsikalised omadused · Tahkes olekus · Hõbedased, v.a tseesium, mis on kollakat värvi · Tihedus on väike (Liitium, kaalium, naatrium veest kergemad) · Suhteliselt madala keemistemperatuuriga · Head soojus- ja elektrijuhid · Omavad läiget Keemilised omadused · Väga tugevad redutseeriad (loo...
Elavhõbe ja hõbe 1. Metallide üldine iseloomustus: Füüsikalised omadused: hea elektri- ja soojusjuhtivus plastilisus ja hea sepistatavus (survega töödelda metalne läige enamasti hallikas värvus (hõbevalgest terashallini). Füüsikaliste omaduste järgi erinevad järgmiste omaduste poolest: tihedus jaotuvad kerg- ja raskmetallideks. sulamistemperatuur kõvadus kõige kõvem metall on kroom ja kõige pehmemad on leelismetallid. värvus magnetiseeritavus - magnetväljasse suhtuvad metallid erinevalt o Ferromagneerilised- magnetiseeruvad nõrgas magnetväljas- Fe, Co, Ni. Nendest metallidest valmistatakse magneteid. Keemilised omadused: Metallid jaotuvad aktiivseteks, keskmise aktiivsusega ja mitteaktiivseteks. Metallid on redutseerijad ehk nad loovutavad elektrone. Reageerimine lahjendatud...
Keemia teooria Metallide iseloomulikud füüsikalised omadused hea elektri- ja soojusjuhtivus plastilisus ja hea sepistatavus metalne läige enamasti hallikas värvus (hõbevalgest terashallini). Metallide iseloomulikud omadused on tingitud metallilisest sidemest: metallides on aatomite väliskihi elektronid muutunud kõigile aatomitele ühiseks. Füüsikalised omadused, mille poolest metallid üksteisest erinevad tihedus (kergmetallid ja raskmetallid) sulamistemperatuur kõvadus (kõige kõvem on Cr ja pehmed on leelismetallid) värvus (Au kollane, Cu punane, ülejäänud valged või hallid) magnetiseeritavus (Fe, Co, Ni) Igapäevasel kasutatakse enamasti väheaktiivseid või keskmise aktiivsusega metalle, kuna aktiivsed metallid reageerivad tugevalt paljude ainetega. Metallide keemilised omadused 1. Reageerimine lahjendatud hapetega (v.a HNO3) ...
Kordamisküsimused kontrolltööks (Õpik lk 51- 85) 1.Alkaanide mõiste. Alkaanid on süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega 2. Tuntumad alkaanid: Metaan - kasutatakse laialdaselt kütusena ja soojuselektrijaamades elektri tootmiseks, ka valgustamiseks ja õli tootmiseks. Metaan sisaldub majapidamisgaasis. Metanool, ammoniaak. Etaan – Propaan - Kasutatakse kõrgahju kütusena, terase lõikamisel ja keevitamisel(segus hapnikuga) 3. Homoloogilise rea mõiste. Ainete keemistemperatuuri muutus homoloogilises reas Homoloogiline rida - samasse aineklassi kuuluvate sarnaste omaduste ja struktuuriga keemiliste ühendite rida. Süsiniku aatomite arvu kasvades kasvavad homoloogilise rea liikmete tihedus, sulamis-ja keemistemperatuur, väheneb aga lahustuvus vees. 4. Alkaanide nomenklatuur - reeglistik nimetus...
Alkeenid: on kllastumata ssivesinikud.Tema molekul koosneb ssinikust ja vesinikust ning C-de vahel on vhemalt ks kahekordne kovalentne side. nimetuse kpp -een ldvalem CnH2n alkeenidest vivad prineda ka ssinikradikaalid -CH---CH2 e. vinl (krval side) alkaanidl esinevad ka isomeerid, vivad olla ka tskloalkaanid.Alkeenide isomeerid: trans vi cis ja nad on omavahel isomeerid. Alkaanide saamine: 1)laboratoorsel teel- alkoholide dehdraatimine(vee ra vtmise teel) nt. CH3CH2OH->H2O+CH2=CH2 2)tstuslikul teel- alkaanide dehdrogeenimiselt CH3CH2CH3->H2+CH2=CH-CH3 Alkaanide fsikalised omadused: 1)homoloogilises reas 3 esimest liiget gaasid,jrgmised vedelikud ning alates 18-dast ssinikust on alkeenid tahked. 2)keemistemp-d suurenevad molekulmassi kasvuga.sulamistemp. vheneb molekulmassi kasvuga. 3)on hdrofoobsed ained-seetttu ei lahustu vees.4)alkeenid on lhnavad ained.5)sulamis-ja keemistemp. on alkeenidel tavaliselt madalamad, kui neile vastavatel...
Orgaaniline keemia. 1. Mis on orgaaniline keemia? Süsinikuühendite ja kovolentsete ühendite (mittemetallide) vaheline keemia. 2. Süsiniku, vesiniku, hapniku ja lämmastiku valents ja valentsolekud. C (süsinik) valents 4, valentsolekuid 4 H (vesinik) vaents 1, valentsolekuid 1 O (hapnik) valents 2, valentsolekuid 2 N (lämmastik) valents 3, valentsolekuid 3 3. Mis on süsivesinikud? Ained, mis koosnevad süsinikust ja vesinikust. 4. Isomeeria mõiste. (mis need on?) Isomeerid on ained, millel on ühesugune summaarne valem, kuid erinev struktuur. Moodustub alates kolme süsinikuga ühendites. Tv. Lk. 13. ül. D 5. Süsiniku oksüdatsiooniaste ja selle arvutamine. Võib olla IV kuni IV 6. Mis on alkaanid? (struktuur) Alkaanid on küllastunud süsivesinikud, kus süsiniku aatomite vahel on ainult 1 kordsed kovolentsed sidemed Lisandub nim. lõpp aan Üldvalem homoloogide arvutamiseks on CnH...
METALLID FÜÜSIKALISED OMADUSED · Plastilised (üks plastilisemaid on kuld). · Head valguse peegeldajad (kõige paremini hõbe, alumiinium ja indium). · Head elektri- ja soojusjuhid (parimad Au, Ag, Cu, Al). · Käega katsudes külmad. · Sulamistemperatuurid on väga erinevad (Hg -39 oC, W 3422 oC). · Värvuselt on enamik metalle hõbevalged, kuid neil võib olla oma iseloomulik helk (Cr sinakas, Bi punakas, Ni - kollakas). Iseloomuliku värvusega on kuld kollane, vask punakas, tseesium kollakas. · Tihedused on väga erinevad. Enamik on veest raskemad välja arvatud leelismetallid liitium (Li) ja naatrium (Na). · Kõvadus on metallidel väga erinev. Leelismetallid (naatrium, kaalium, liitium) on väga pehmed (noaga lõigatavad). Kõige kõvem metall on kroom. Väga kõvad on ka paljude metallide sulamid. METALLILINE SIDE · Enamik metallide väliskih...
METALLID FÜÜSIKALISED OMADUSED · Plastilised (üks plastilisemaid on kuld). · Head valguse peegeldajad (kõige paremini hõbe, alumiinium ja indium). · Head elektri- ja soojusjuhid (parimad Au, Ag, Cu, Al). · Käega katsudes külmad. · Sulamistemperatuurid on väga erinevad (Hg -39 oC, W 3422 oC). · Värvuselt on enamik metalle hõbevalged, kuid neil võib olla oma iseloomulik helk (Cr sinakas, Bi punakas, Ni - kollakas). Iseloomuliku värvusega on kuld kollane, vask punakas, tseesium kollakas. · Tihedused on väga erinevad. Enamik on veest raskemad välja arvatud leelismetallid liitium (Li) ja naatrium (Na). · Kõvadus on metallidel väga erinev. Leelismetallid (naatrium, kaalium, liitium) on väga pehmed (noaga lõigatavad). Kõige kõvem metall on kroom. Väga kõvad on ka paljude metallide sulamid. METALLILINE SIDE · Enamik metallide väliskih...
LIITIUM Karlis Litvinjuk Avastamine 1817.a avastas Jöns Jacob Berzeliuse labori noor assistent Johann August Arfvedson mineraali petaliidi, analüüsil liitiumi, kuid vaba metalli tal eraldada ei õnnestunud. Järgmisel aastal eraldas inglise teadlane Humphry Davy, liitiumoksiidi elektrolüüsil metalse Li. Liitium Keemiline element järjenumbriga 3. Liitium tuletati kreekakeelsest sõnast lithos, Mis tähendab kivi. Suuremad liitiumiühendite leiukohad asuvad Kanadas, U.S.A.s, KaguAafrikas, Kasahstanis ja KeskAasias. Liitium on hõbevalge ja erakordselt kerge metall, mis sulab temperatuuril 180°C. Keemiliselt on ta väga aktiivne. Omadused Li reageerib kergesti paljude lihtainetega, lämmasikuga, hapnikuga, halogeenidega, väävliga Li reageerimine veega ei toimu nii aktiivselt kui teiste leelismetallide puhul ...
BROOM Siim Starke 10R TKG Üldine info · Keemiline sümbol - Br · VII rühma element · Mittemetall · Järjenumber 35 · Aatommass 79,904 · Elektronvalem: Br +35|1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 3d10, 4p5 · Elektronskeem : Br +35 |2)8)18)7 · Esineb kahe stabiilse isotoobina (79Br ja 81Br) Füüsikalised omadused · Punakas pruun vedelik · Mürgine · Terava ärritava lõhnaga · Sööbiva toimega · Keemis temperatuur: 58.8 °C · Sulamis temperatuur: -7,2 °C · Tihedus: 3,1 g/cm3 · Toatemperatuuril aurustub kiiresti (aurud oranzpruunid) Keemilised omadused · Halogeen · On vähem aktiivsem kloorist · Reageerib kõikide metallidega peale plaatina · Reageerib paljude mittemetallidega · Tugev oksüdeerija · Vähese vees lahustuvusega Kasutamine · 1,2-dibromoetaani tootmine (kütuste oktaaniarvu tõstmine) · Värvainete tootmine · Juuksehooldusvahendid · Pisargaas · Tulekustutus vahendina · Ravimid · Plastide tulekindl...
KEEMIA 1) Tea metallide keemilisi omadusi, oska kirjutada neid iseloomustavaid keemilisi reaktsioonivõrrandeid . Metalliliste elementidel on reeglina väliskihil elektrone vähe (1-3) ja neid hoitakse nõrgalt kinni. · Ehitus lihtainena: aatomid paiknevad lähestikku välised elektronkihid kattuvad osaliselt väliskihi elektronidel võime liikuda aatomi juurest aatomi juurde üle kogu kristalli. Metallid jaotatakse aktiivseteks, keskmise aktiivsusega ja väheaktiivseteks metallideks metall + hapnik-- oksiid metall + hape-- sool + vesinik metall + vesi leelis (hüdroksiid, alus) + vesinik metall + soolalahus uus metall + uus sool (Aktiivsem metall on võimeline tõrjuma välja vähemaktiivsema metalli tema soola lahusest.) 1. Reageerimine lahjendatud hapetega (v.a HNO3) Pingereas vesinikust paremal pool olevad metallid ei reageeri lahjendatud hapetega. 2. Reageerimine veega Aktiivsed metallid...
Leelised ehk I A rühma metallid Ajalooliselt tuleneb sõna leelismetall sellest, et nende metallide hüdroksiide tunti juba ammu ja neid nimetati leelisteks. Tänapäevane selgitus võiks olla lihtsalt selline, et nende metallide veega reageerimisel tekivad leelised. Leelismetallid on kõige metalsemad elemendid. Aatomi ehituselt kuuluvad nad s-elementide hulka, kuna nende aatomite välisel orbitaalil on üks elektron. Sellest tulenevalt on kõikide leelismetallide aatomite väliskihi elektronvalemiks ns ja oksüdatsiooniastmeks ühendis +I. Kuna leelismetallidel on väliskihis ainult üks elektron, siis seetõttu nad loovutavad selle erakordselt kergesti. Kusjuures mida kaugemal väliselektron aatomituumast asub, seda kergemini see loovutatakse. Just sel põhjusel on leelismetallid väga tugevad redutseerijad ja keemiliste omaduste poolest nad kuuluvad kõige aktiivsemate metallide hulka. Elektroni loovutamise tagajärjel muutuvad leelismetallide aatom...
Alumiinium Koostaja: Keidi Kõiv 10a Juhendaja: Erkki Tempel Üldiselt Järjenumber 13 Asukoht 3.perioodis III A rühmas Elektronskeem: Al: +13 | 2) 8) 3) Hõbevalge Tihedus 2,7 g/cm³ Sulamistemperatuur 660 °C Reageerib paljude lihtainete ja hapetega Püsivamates ühendites on oksüdatsiooniaste +3 Toodetakse sulatatud boksiidi (alumiiniumoksiidi) elektrolüüsil Leidumine looduses Levikult kolmas element maakoores Moodustab 8,2% maakoore massist Lihtainena looduses ei leidu Looduslik alumiiniumoksiid esineb korundina Kuulub ka vulkaaniliste kivimite koostisesse Maakoores on iga kahekümnes aatom alumiinium Tähtsamad ühendid on boksiit (pildil )(Al2O3*nH2O) ja kaoliin (Al2O3*2SiO2*2H2O) Füüsikalised omadused Peegeldab hästi valgust Tuhm pind Kergmetall Suhteliselt kergelt sulav Hea elektri-ja soojusjuhtivusega Suhteliselt pehme Kerg...
KEEMIA KT METALLID Metallide reageerimine mittemetallidega Aktiivsed metallid reageerivad halogeenide, hapniku ja väävliga energiliselt juba toatemperatuuril või nõrgal soojendamisel. Vähemaktiivsed metallid reageerivad mittemetallidega enamasti alles kuumutamisel. Väärismetallid reageerivad vähe. Redutseerija (aine, mille osakesed loovutavad elektrone) on metall. Redutseerimine- elektronide liitumine redoksreaktsioonis, elemendi oks. aste väheneb Oksüdeerija (aine, mille osakesed liidavad elektrone) on mittemetall. Oksüdeerimine- elektronide loovutamine redoksreaktsioonis, elemendi oks.aste kasvab. Redoksreaktsioon- keemiline reaktsioon, milles toimub elektronide üleminek ühtedelt osakestelt teistele, sellega kaasneb elementide oksüdatsiooniastme muutus. Metallide reageerimisel hapnikuga tekivad oksiidid. Metallide reageerimisel väävliga tekivad sulfiidid Metallide reageerimisel halogeenidega (I2,Br...
Loeng 1........................................................................................................................................2 Loeng 2........................................................................................................................................2 Väärismetallid.........................................................................................................................4 Jootmine. Joodis......................................................................................................................5 Loeng 3........................................................................................................................................6 Reaktsioonid metallidega........................................................................................................6 Redoksreaktsioonid.........................................................................................
Mõisted · Alkaan süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega. Mõnikord nimetatakse alkaane ka parafiinideks. (metaan, CH4) · Alkeen küllastumata süsivesinikud, mille molekulides on vähemalt üks kaksikside süsiniku aatomite vahel. Alkeene nimetatakse mõnikord ka olefiinideks. (eteen, C2H4) · Alküün küllastumata süsivesinikud, mille molekulides esineb kovalentne kolmikside. (etüün, C2H2) · Detergendid sünteetilised keemilised ühendid (pindaktiivsed ained), mida kasutatakse pesemis- ja puhastustoime parandajatena. Detergendi ja seebi erinevus seisneb selles, et detergendis puuduvad leeliselised aktiivsed ained. · Dihapped looduses üsna levinud. Lihtsaim neist etaandihape ehk oblikhape HOOCCOOH. On mürgine aine mida leidub spinatis, hapuoblikas, rabarbris mitte küll ohtlikes kogustes. · Esterdumine estrite tekkere...
Tallinna Rahumäe Põhikool Magneesium Nele Reimets 8A Tallinn 2/15/2011 Magneesium Magneesium on keemiline element järjenumbriga 12. Magneesium asub kolmandas perioodis, IIA rühmas. Maal ei leidu teda looduses vabalt, vaid ainult ühendite koosseisus oksüdeerituna. Magneesium lihtainena Magneesiumi tihedus on normaaltingimustel (20 °C) 1,738 g/cm3. See on väike tihedus, umbes 1/4 terase tihedusest. Magneesium sulab temperatuuril 648,8 °C, keemistemperatuur on 1107 °C või 1095 °C. Magneesium on hõbevalget värvi ja läikiv. Ta on metall. Berülliumist on ta pehmem ja plastilisem. Magneesium on keemiliselt küllaltki aktiivne. Õhu käes moodustub tavalistel temperatuuridel magneesiumi pinnale õhuke, kuid tihe mati värvusvarjundiga oksiidikiht, mis kaitseb metalli edasise reageerimise eest õhuhapnikuga. Reageerimine külma veega on väga aeglane. Magneesium lahustub hapetes väga energiliselt. Ta reageerib ka paljude teiste elementidega. K...
SÜSIVESINIKUD Ained, mis koosnevad vaid süsinikust ja vesinikust. Süsivesinikud võivad moodustada alates 3ndast süsinikust isomeere. Isomeerid on ained, mille summaarne valem on sarnane, kuid struktuur on erinev C4H10 butaan CCCC 2metüülpropaan CCC C Süsivesinikud on võimelised moodustama ka homoloogilisi ridu. Homoloog aine, mille struktuur ja keemilised omadused on sarnased. Iga järgnev homoloog erineb eelmisest CH2 rühma võrra. 1. met 2. et 3. prop 4. but 5. pent 6. heks 7. hept 8. okt 9. non 10. dek Alkaanid CnH2n+2 Alkeenid CnH2n Alküünid CnH2n2 ALKAANID Alkaanid CnH2n+2 Alkaanid on küllastunud süsivesinikud, kus molekuli koostises süsinike vahel esinevad ainult ühekordsed kovalentsed sidemed. Nimetuse lõpp: aan Nt. Butaan C4H10 Metaan CH4 summaa...
Alumiinium Stefani Kask Pirita Majandusgümnaasium 10.A Mis on alumiinium? Alumiinium (Al) on keemiline element järjenumbriga 13. Alumiinium asub perioodilisussüsteemis 3. perioodis, III A rühmas, oksüdatsiooniastmeks ühendites on +III. Ta on hõbevalge hästi reageeriv pehme metall, tihedusega 2,7 g/cm³ ja sulamistemperatuuriga 660 °C. Avastamine Arheoloogilistel väljakaevamistel leiti ühe Hiina väejuhi 3. sajandi algusest pärit hauakambrist alumiiniumehteid. Viimaste spektraalanalüüsil selgus, et need sisaldasid 85 % alumiiniumi. Alumiiniumi nimetus tuleneb ladinakeelest sõnast alumen, s.t. maarjas. Maarjas oli aine, mida saadi toota hapete abil savist. Lõngu, kangaid ja sõjariistu immutati maarjases, et nende värvused muutuksid erksamaks ja tulekindlamaks, muutes neid mittesüttivaks. Sinisavi, milles leidub alumiiniumi Leidumine looduses/ Saamine Alumiinium on kolmas kõige levinum metalne element lo...
Mis on orgaaniline keemia? Süsinikühendite ja kovalentsete sidemete keemia. Sinna alla ei kuulu CO, CO2, H2CO3 ja CaCO3. Millised elemnedid kuuluvad org. elementide koostisesse? Põhilised elemendid on hapnik, lämmastik, vesinik, väävel, halogeenid, fosfor, räni jt. Orgaanilistes ühendites on enamasti C-H side, lisaks süsiniku ja vesiniku aatomitele võivad orgaanilised ühendid sisaldada ka hapniku, lämmastiku, halogeenide ja teiste elementide aatomeid (fosfor, väävel, raud...). Põhielementide valentsid ja valentsolekud. C valents 4, valentsolekuid 3; N valents 3, valentsolekuid 3; O valents 2, valentsolekuid 2; H valents 1, valentsolekuid 1. Süsiniku o.a ja selle arvutamine. Süsiniku o.a väärtused ulatuvad -4 kuni +4. iga vesinik annab -1 juurde, iga süsinik annab 0 juurde ja hapnik ja kõik muu annab +1 juurde Keskmise arvutamine.NT: C5H12 H12=12 , et saad...
Metallid Leidumine: 4/5 elementidest on metallid. Enamlevinud on Al, Fe, Ca, Na, K, Mg. Ehedana leidub väheaktiivseid metalle: Cu, Hg, Ag, Au, Pt, enamuses metallidest leiduvad ühenditena maakide koostises. Maagid võivad olla oksiidsed(Fe2O3, Al2O3), sulfiidsed( Cu2S, HgS, FeS2), kloriidsed ( NaCl, KCl), karbonaatsed, ... jt.sooladena. Aatomi ehitus ja paiknemine per. süsteemis: Per. süsteemis- vasakul all; väliskihis 1-3 elektroni, aatomiraadius suhteliselt suur; elektronegatiivsus suhteliselt väike; loovutavad elektrone; on redutseerijad; ühendites omandavad positiivse oksüdatsiooniastme. Metalliline side: Metallioonide ja "vabade elektronide" vaheline side. Füüsikalised omadused: Üldised: hea elektri .ja soojusjuhtivus, metalliline läige, plastilisus. Erinevused: 1. Läige ja peegeldumisvõime (sile poleeritud pind): parimad peegeldusvõimelt hõbe(Ag). alumiinium(Al), kul...
METALLID Aktiivsed metallid(IjaII A rühm) reageerivad VIIA rühma metallidega(halogeenidega), hapniku ja väävliga energiliselt juba toatemperatuuril või nõrgal soojendamisel. Vähemaktiivsed metallid reageerivad mittemetallidega alles kuumutamisel. Väärismetallid on oksüdeerumise suhtes vastupidavad. Ei reageeri hapnikuga isegi kuumutamisel. (kuld ja plaatina) Õhu käes seismisel tekib metalli pinnale õhuke oksiidkiht, mistõttu metall muutub tuhmiks. METALLI aatomid loovutavad elektrone, muutudes metalli katioonideks. ON REDUTSEERIJAD. oksüdeerumine. MITTEMETALLI aatomid liidavad elektrone, muutudes anioonideks. ON OKSÜDEERIJAD. Metallide reageerimine teiste ühenditega on alati redoksreaktsioon, kus üks element liidab ja teine loovutab elektrone. Fe + O2 -> Fe3O4 rauatagi FeO . Fe2O3 kuumutades Fe + Cl2 -> FeCl3 sest on tugev oksüdeerija Metallide reageerimine hapetega Metallid reageeriva...
Kordamine kontrolltööks: Alkaanid 1. Keemiliste sidemete arv koos põhjendusega. C- 4, sest viimasel kihil 4 vaba elektroni. P- 5, sest tal on tal on viimasel kihil 3 vaba elektroni > saab moodustada 5 sidet. 2. Hüdrofoobsus vett tõrjuvad ained (Nt. Rasvad, alkaanid, eeter) Hüdrofiilsus vett armastavad ained (Nt. Alkoholid, suhkrud, soolad) 3. Isomeeria. Joonistada! Põhjendada keemistemperatuuri ja tihedust! Mida suurem on alkaani molekulmass, seda kõrgem on tema sulamis- ja keemistemperatuur. Isomeeride puhul on keemistemperatuur seda kõrgem ja tihedus seda suurem, mida vähem hargnenud on ahel. On ju hargnemata ahelaga molekulidel omavaheline kokkupuutepind suurem, mistõttu molekulidevahelised vastastikmõjud on tugevamad...
Jõhvi Gümnaasim Signe Viiksaar 11. A klass MAGNEESIUM Referaat Juhendaja Kristelle Kaarmaa Jõhvi 2018 SISSEJUHATUS Magneesium on keemiline element järjenumbriga 12. Tema asukoht on kolmandas perioodis. Tema elektronkonfiguratsioon on [Ne]3s2. Magneesiumi ioonil Mg2+ on sama elektronkon- figuratsioon nagu neoonil, sest kaks 3s-elektroni on ioonil puudu. Tal on kolm stabiilset isotoopi massiarvudega 24, 25 ja 26. Suhteline aatommass on 24,305. Magneesium on s-element ning asub teise rühma peaalarühmas. Omadustelt on magneesium metall. Mõnikord arvatakse ta leelismuldmetallide hulka; sel juhul on ta nende seas berülliumi järel teine element. Metallide elektrokeemilises pingereas on magneesium vesinikust eespool. Tema standardpotentsiaal on 2,372 V. Magneesium lehtmetalli ...
Keemia Alkoholid R-OH (-ool) 1. CH3 CH CH3 propaan 2 ool OH 2. CH3 CH2 CH2 OH Propaan 1 ool 3. CH2 CH2 CH2 PROPAAN 1,3 - diool OH OH Aatomite arv Struktuuri valem Lihtsustatud strukt Molekuli valem N=1 H CH3OH metanool e metaan H-C-H-O CH3 CH2 CH2 OH H N=2 HH C2H5 etanool e piiritus H-C-C-O-H CH3CH2OH HH N=3 HHH CH3CH2CH2OH Propaan-1-ool H-C-C-C-OH OHCH2CH2CH3 HHH Alkoholide omadused etanooli näite põhjal CH3CH2OH ja OHCH2CH3 Füüsikalised omadused · On värvuseta iseloomuli...
Keemiaküsimused 10. klassile Metallid,metallide tootmine ja rakendusi praktikas õ.lk. 8-75 1.Millised metallid esinevad looduses ehedana? Kuld, hõbe, alumiinium, raud, kaltsium ja naatrium 2.Mis on maak? Maak on mineraalne maavara, enamasti mõeldakse maagi all maavara, millest eraldatakse metalle. 3.Milliste ühenditena esinevad looduses tähtsamad metallid? Naatrium- Na Kaltsium- K Magneesium- Mg Alumiinium- Al Raud- Fe Tsink- Zn Vask-Cu 4.Mis on kõige levinum metalliline element looduses? Kõige levinum metalliline element looduses on alumiinium 5.Millised metallid on elusorganismides väga vajalikud ja mille jaoks vajalikud? Raud(seob hapniku), kaltsium (luude jaoks), naatrium (juuste ja küünte jaoks) 6.Metallide füüsikalised omadused. hea elektri- ja soojusjuhtivus plastilisus ja hea sepistatavus metalne läige enamasti hallikas värvus 7.Metallide keemilised omadused (reageerimine hapnikuga, väävliga,halogeenidega, v...
Tarmo Soots ALUMIINIUM JA TEMA SULAMID REFERAAT Õppeaines: TEHNOMATERJALID Mehaanikateaduskond Õpperühm: KMI11 Juhendaja: Annika Koitmäe Tallinn 2011 1. SISSEJUHATUS 1827 a sai Saksa keemik, kes oli hariduselt arst, Friedrich Wöhler metalli, mida keegi polnud kunagi näinud. Algul eraldas ta metalli keemilisest ühendist halli pulbrina, mis peenestamisel omandas metalse läike. Katsed saada seda metalli kangina või suurte teradenajäid esialgu tulemuseta. Alles 1845 a, peale 18 aastat püsivaid otsinguid sai Wöhler uut metalli nööpnõelapea suuruste teradena. Väliselt oli see sarnane hõbedaga, kuid 4 korda kergem. Kuna uue metalli saamise lähteaineks oli ammu tuntud maarjased ( ladina keeles alumen), siis hakati ka seda metalli kutsuma alumiiniumiks. Veel 100 aastat tagasi oli alumiinium väga haruldane ja hinnaline metall, millest valmistati vaid luksusesemeid. Tänapäeval kas...
Tsingi ajalugu Sõna ,,tsink" on ebatavaline ja selle päritolu pole teada. Tõenäoliselt kasutas esmakordselt seda nime Paracelsus, Sveitsis sündinud sakslasest keemik, kes kasutas sõna ,,Zincum" 16. sajandil. See sõna tähendab saksa keeles ilmselt ,,hamba-sarnanast, teravaotsalist või sakilist osa", ja kuna tsingi metalli kristallid on okka-sarnased, siis näib selle päritolu üsna usaldustäratav. Iidses Indias oli tsingi tootmine väga levinud. Paljud kaevandamiskohad ,,Zawari kaevandustes" töötasid isegi vahemikus 1300-1000 e.Kr. Tsingisulamid on kasutusel olnud sajandeid. Messingist esemeid, mis pärinevad aastatest 1400-1000 e.Kr on leitud Iisraeli aladel ning 87%-ilise tsingisisaldusega asju on leitud eelajaloolises Transilvaanias. Madala keemistemperatuuri ja selle metalli tugeva reageerimisvõime tõttu ei suudetud iidsetel aegadel mõista selle metalli tõelist loomust. Sulatamine ja ebapuhta tsingi era...
Aatom koosneb aatomituumast ja elektronkattest, tuum prootonitest ja neutronitest, elektronkate elektronidest. Elektronide maksimumarv kihil = 2* n-ruudus Orbitaalid s,p ja d Massiarv = prootonite arv + neutronite arv. Elektronegatiivsus - Tõmbevõime keemilises sidemes. Metallid loovutavad elektrone Mittemetallid seovad elektrone. Muidu suureneb elektronegatiivsus paremalt vasakule ja ülevalt alla, aga B-rühmas alt üles. Ioon Laenguga aatom või aatomirühm Katioon positiivne. Anioon negatiivne. Oksüdatsiooniaste(o.a.) iooni laengu suurus. A-rühma metallidel on püsiv o.a. Maksimaalne o.a. On oksiidi valemis ja minimaalne on mittemetalli vesinikühendis. Molekul koosneb aatomitest Molekulaarsed ained koosnevad molekulidest. Mittemolekulaarsed ioonidest või aatomitest. Keemilise sideme tekkel eraldub energiat, eksotermiline. Sideme lõhkumisel neeldub energiat, endotermiline protsess. Mittepolaarne kovalentne side esineb ühe...
Raud. Fe. Ferrum Raud (Ferrum) on keemiline element järjenumbriga 26. Raud asub Perioodilisussüsteemi VIII B rühmas ja 4. perioodis. Tal on neli stabiilset isotoopi massiarvudega 54, 56, 57 ja 58. Omadustelt on raud metall. Normaaltingimustel on raud tahke aine tihedusega 7,87 g/cm 3. Raua sulamistemperatuur on 1535 Celsiuse kraadi. Raud esineb madalal rõhul nelja kristallmodifikatsioonina olenevalt temperatuurist. Raud on inimesele tuntud väga ammu. Oli ju pärast pronksiaega rauaaeg, mis Eestiski algas juba e. m. a. Metallidest on levikult raud teisel kohal pärast alumiiniumi, kuid toodangult esikohal, sest on kõige kättesaadavam metall. Rauda leidub taimedes ja inimeses. Inimese veres oleva hemoglobiini keskmeks on raua aatom, mis seobki hapniku, mille veri organismi laiali kannab. Nii vee...
Keemia 28.08.08 Sissejuhatus 1. Nimetada igapäevases elus kasutatavaid keemiatööstuse tooteid. 2. Keemilise reaktsiooni olemus, näide loodusest. 3. Mille alusel liigitatakse aineid klassidesse? 4. Lihtainete mõiste, jagunemine. 5. Liitainete mõiste, jagunemine. 1. Sool, suhkur, äädikas, jood, seep, piiritus, lõhnaõli, kodukeemia. 2. Keemilise reaktsiooni käigus toimub ühe aine muundumine teiseks. Näiteks looduses muundub vesi veeauruks, raud roostetab jne. 3. Nende koostise ja keemiliste omaduste järgi. 4. Lihtained koosnevad ainult ühe aine elementidest, jagunevad metallideks ja mittemetallideks. 5. Liitained koosnevad mitme erineva aine elementidest, jagunevad oksiidideks, hapeteks, alusteks ja sooladeks. Oksiidid Oksiidid on sellised liitained, mis koosnevad kahest elemendist, millest üks on hapnik. Oksiidid tekivad: 1) lihtaine ühinemisel hapnikuga (C+O2 -> CO...
Aineklass Nimetuste süsteem Füüsikalised omadused Keemilised omadused Leidumine/kasutamine alkaan Järelliide –aan Hüdrofoobsed. 1) Täielik põlemine kiire oksüdatsioon Maagaas (CH4) CnH2n+2 C1-C4 –gaasiline Süsinikahela pikenedes C6H12 + 8O2 → 5CO2 + 6H2O Nafta (vedelate alkaanide segu C5-C8 –vedel tihedus, st°,kt°suurenevad. 2) Oksüdeerumine halogeeniga Parafiin (tahke-te alkaanide segu) Nt. CH4 –metaan Sama süsinike arvu korral on Radikaaliline asendus, tekivad halogeeniühendid C5-C9 (bensiin) C4H10 –butaan hargnenud ahela puhul CH4 + Cl2 → CH3Cl + HCl Alkaane saadakse põhil. naftast r,st°,kt° väiksem 3...
Soolad Soolad koosnevad tavaliselt metalli katioonist ja happeanioonist. Soolad on liitained, milles metalliioonid on seotud happejääkioonidega. Soolad on ioonsed ühendid, mis koosnevad (aluse) katioonidest ja (happe) anioonidest. Liigitus 1. Tavasoolad (lihtsoolad) : NaCl, FeSO4, CuCO3, Na3PO4 ... 2. Vesiniksoolad happe vesinikioonid asenduvad täielikult või osaliselt metalliiooniga Cu(HCO3)2 vask(II)vesinikkarbonaat NaH2PO4 naatriumdivesinikfosfaat Na2HPO4 naatriumvesinikfosfaat 3. Hüdroksiidsoolad aluse hüdroksiidioonid asenduvad täielikult või osaliselt metalliga MgOHCl magneesiumhüdroksi...
KEEMIA EKSAMI KÜSIMUSED JA VASTUSED 1.Keemiliste elementide perioodilisus seadus, perioodilisus tabel ja selle rakendus keemiliste elementide iseloomustamisel. Keemiliste elementide, ning neist moodustunud liht- ja liitainete omadused on perioodilises sõltuvuses aatommassist. Perioodilises süsteemi ahela koostas Mendelev, kus igale elemendile on oma lahter, koos aatomi numbriga, selle aatommassiga, nimega ja sümboliga. Iseloomustamisel saab tabeli perioodi numbrist teada aatoni elektronkihi arvu, aatomi number on prootonite ja neutronite koguarv, gruppist tuleb viimase kihi elektronide arv. 2.Metallide asukoht keemiliste elementide perioodilisus tabelis Elementide metalliliste omaduste muutus perioodis (III perioodi näitel). Kõik perioodid algavad aktiivsete metallidega. Liikudes vasakult paremale nõrgenevad metallilised omadused nagu välises elektronkihis suureneb elektronite arv (väheneb arv elektro...
Küllastumata ühendid 1. Aromaatne ühend orgaaniline ühend, mille molekulis sisaldub aromaatne tsükkel. 2. Küllastumata ühend alkaanid on küllastunud ühendid. Alkeenid ja alküünid on küllastumata ühendid. Küllastumata ühenditel on lisaks sidemele ka üks või kaks sidet. 3. Alkeenid süsinikuvahelise kaksiksidemega ühendid. Näiteks: CH2=CHCH3 (propeen), liide -een Eteen ehk etüleen CH2=CH2 on värvusetu, nõrga meeldiva lõhna ja narkootilise toimega gaas. Eteeni saadakse nafta töötlemisel ja ta on kõige suuremas koguses tööstuslikult toodetav orgaaniline aine. Suurem osa toodetud eteenist kulub polüeteeni valmistamiseks. Eteenist saadakse ka etanooli CH2=CH2_CH3CH2OH , kuid ka vastupidi mõnel maal toodetakse eteeni etanoolist. Eteen põhjustab viljade valmimist, seda eritavad küpsed puuviljad. 4. Alküünid süsinikuvahelise kolmiksidemega ühendid. Näiteks:...
Kordamisküsimused aines Rakenduskeemia Sissejuhatus: BBC Chemistry A VOLATILE HISTORY Discovering the Elements 1. Mis elementi saab toota uriinist? Kirjeldage eksperimendi. Eksperimenteeriti uriiniga, mis sisaldab märkimisväärsetes kogustes lahustunud fosfaate. Hamburgis töötades üritas Brand luua tarkade kivi. Ta destilleeris mõnd soola, aurustades uriini ning selle tulemusena tekkis valge materjal, mis helendas pimedas ja põles hämmastavalt hästi. Esmalt lasi ta uriinil mõne päeva seista, kuni see hakkas halvasti lõhnama. Edasi keetis ta uriini pastaks, kuumutas selle kõrgel temperatuuril ja juhtis auru läbi vee. Ta lootis, et aur kondenseerub kullaks, aga hoopis tekkis valge vahane aine, mis helendas pimedas. Nii avastas Brand fosfori esimese elemendi, mis avastati pärast antiikaega. Kuigi kogused olid enam-vähem õiged (läks vaja 1,1 liitrit uriini, et toota 60 g fosforit), ei olnud vaja lasta uriinil roiskuma minna. Teadlased ...
Tartu Kivilinna Gümnaasium Liitium Koostas: Juhendaja: Tartu 2009 Sissejuhatus Liitium on keemiline element järjenumbriga 3. Liitium tuletati kreekakeelsest sõnast lithos, Mis tähendab kivi. Looduses on liitiumi suhteliselt palju, ta moodustab 0,02% maakoore aatomite üldhulgast. Suuremad liitiumiühendite leiukohad asuvad Kanadas, U.S.A.-s, Kagu-Aafrikas, Kasahstanis ja Kesk-Aasias. Liitium on hõbevalge ja erakordselt kerge metall, mis sulab temperaturril 180°C. Ta on kõrge väiksema tihedusega metall ja üldse kõige väiksema tihedusega normaaltingimusel tahke lihtaine: tema tihedus on 0,535g/cm³. Liitium on esikohal metallide hulgas kerguse poolest. Ta on viis korda kergem kui alumiinium ja kaks korda kergem kui vesi. Seepärast ujub liitium mitte ainult veepinnal vaid isegi petrooleumis. Liitium on leelismetall. Keemili...
Orgaaniline keemia Süsinikuühendeid nimetatakse orgaanilisteks ühenditeks, süsinikuühendite keemiat aga orgaaniliseks keemiaks. Vitalism ehk elujõuõpetus. Kõik orgaanilised ained sisaldavad süsinikku ning nende molekulmass on tavaliselt suur. Anorgaaniliste ja orgaaniliste ühendite võrdlus: Omadus või tunnus Anorgaaniline keemia Orgaaniline keemia Keemiline side Paljudel ühenditel iooniline Peamiselt kovalentne side Sulamistemp. Tavaliselt üle 350oC Tavaliselt alla 350oC Keemistemp. Tavaliselt üle 750oC Tavaliselt alla 750oC Lahustuvus a) Vees Enamasti lahutuvad Enamasti ei lahustu (sarnane lahustub sarnases) b) mittepolaarsetes Enamasti ei lahustu Enamasti lahustuvad ...
Tartu Kivilinna Gümnaasium (konspekt) Koostas: Riho Rosin Klass: 11A Juhendas: Helgi Muoni Tartu 2004 Created by Riho Rosin 1 13666324649407.doc.doc Orgaaniline keemia Süsinikuühendeid nimetatakse orgaanilisteks ühenditeks, süsinikuühendite keemiat aga orgaaniliseks keemiaks. Vitalism ehk elujõuõpetus. Kõik orgaanilised ained sisaldavad süsinikku ning nende molekulmass on tavaliselt suur. Anorgaaniliste ja orgaaniliste ühendite võrdlus: Omadus või tunnus Anorgaaniline keemia Orgaaniline keemia Keemiline side Paljudel ühenditel iooniline Peamiselt kovalentne side Sulamistemp...
MOLEKULAAR-ATOMISTLIK TEOORIA Põhiseisukohad: · molekul on aine väikseim osake, millel säilivad selle aine keemilised omadused · molekulid koosnevad aatomitest · keemilistes reaktsioonides aatomid väiksemateks osakesteks ei lagune · keemiliste reaktsioonide käigus toimub aatomite ümberjaotumine lähtainete molekulidest reaktsioonisaaduste molekulidesse FÜÜSIKALISED NÄHTUSED aine olek või keha kuju muutub KEEMILISED NÄHTUSED üks aine muutub teiseks PUHAS AINE aine ei sisalda lisandina teisi aineid (nt puhas H2O) SEGU koosneb mitmetest ainetest (nt õhk) FÜÜSIKALISED OMADUSED: KEEMILISED OMADUSED: · keemis- ja sulamistemperatuur reageerimine lihtainetega · tihedus (nt O2, H2, C, halogeenidega jt, · värvus põlemisvõime) · lahustuvus vees ...
Oksiidid Oksiidid koosnavad kahest elemendist, millest üks on hapnik. Liigitus: Metallioksiidid Mi ttemetallioksiidid Aluselised oksiidid Amfoteersed oksiidid Happelised oksiidid Neutraalsed oksiidid K2O, CaO, MgO, Al2O3, ZnO, Cr2O3 SO2, SO3, CO2, P4O10, NO2, NO, N2O, CO Na2O, FeO, BaO N2O5, N2O3, SiO2,(CrO3, Mn2O7) Keemilised omadused: Saamin e: I Aluseline oksiid+ HAPE = sool+ vesi 1.)Lihtainete põlemisel Aluseline oksiid+HAPPELINE OKSIID =sool 2.)Liitainete põlemisel Aluseline oksiid+vesi ...
Põlula Gümnaasium Pilvi Mets MAGNEESIUM Referaat Põlula 2015 ÜLDISELT Magneesium on keemiline element järjenumbriga 12. Magneesium asub kolmandas perioodis. Tema elektronkonfiguratsioon on [Ne]3s2. Magneesiumi ioonilMg2+ on sama elektronkonfiguratsioon nagu neoonil, sest kaks 3s-elektroni on ioonil puudu. Tal on kolm stabiilset isotoopi massiarvudega 24, 25 ja 26 (magneesium-24, magneesium- 25 jamagneesium-26). Saadud on ka tehisisotoope.[1] Suhteline aatommass on 24,305. Magneesium on s-element ning asub teise rühma peaalarühmas. Omadustelt on magneesium metall. Mõnikord arvatakse ta leelismuldmetallide hulka; sel juhul on ta nende seas berülliumi järel teine element. Metallide elektrokeemilises pingereas on magneesium vesinikust eespool[1]. Temastandardpotentsiaal on –2,372 V. LEVIK Iso...
1. Mis elementi saab toota uriinist? Kirjeldage eksperimendi. Uriinist saab toota fosforit. Seda tõestas oma katse tulemusena Brand. Destilleerides mõnda soola, aurustades uriini ning selle tulemusena tekkis valge materjal, mis helendas pimedas ja põles hästi. Katsetades tahtis saaada ta uriinist kulda või tarkade kivi,et seda saada lasi ta uriinil mõne päeva seista, kuni see hakkas halvasti lõhnama. Siis keetis ta uriini pastaks, kuumutas selle kõrgel temperatuuril ja juhtis auru läbi vee. Ta lootis, et aur kondenseerub kullaks, aga hoopis tekkis valge vahane aine, mis helendas pimedas. Nii avastas Brand fosfori – esimese elemendi, mis avastati pärast antiikaega. Kuigi kogused olid enam-vähem õiged (läks vaja 1,1 liitrit uriini, et toota 60 g fosforit), ei olnud vaja lasta uriinil roiskuma minna. 2. Kes ja kuidas avastas vesiniku. Kirjutage reaktsiooni võrrandit. Vesiniku avastas 1766 aastal füüsiku ja keemiku juuurtega inglane Henry C...
1 2. II A RÜHMA METALLID 2.1 II A rühma metallide üldiseloomustus II A rühma metallideks on berüllium, magneesium, kaltsium, strontsium, baarium ja raadium. Nelja viimast elementi ehk kaltsiumit, strontsiumit, baariumit ja raadiumit nimetatakse ka leelismuldmetallideks. Ajalooliselt tuleneb sõna leelismuldmetall sellest, et nende metallide oksiidid moodustavad veega reageerides leeliseid. Sõna muld kasutati juba keskajal rasksulavate metallioksiidide ja teiste kõrgel temperatuuril sulavate ainete kohta. Aatomi ehitusel kuulvad nad s- elementide hulka, nagu ka leelismetallid. Nende aatomite välisel elekt-2 ronkihil on kaks elektroni, mistõttu nende aatomite väliskihi elektronvalemiks on ns ja nende oksüdatsiooniastmeks ühendites on + II. Kuna II A rühma elementidel on kaks väliselektroni, siis sarnaselt leelismetallidele, loovutavad nad oma väliselektrone üsna kergelt ja on ühtlasi tugevateks redutseerijateks. Kusjuures, mida allpool met...
1. I A RÜHMA METALLID 1.1 I A rühma metallide üldiseloomustus I A rühma metallideks on liitium, naatrium, kaalium, rubiidium, tseesium ja frantsium. I A rühma metalle nimetatakse ka leelismetallideks. Ajalooliselt tuleneb sõna leelismetall sellest, et nende metallide hüdroksiide tunti juba ammu ja neid nimetati leelisteks. Tänapäevane selgitus võiks olla lihtsalt selline, et nende metallide veega reageerimisel tekivad leelised. Leelismetallid on kõige metalsemad elemendid. Aatomi ehituselt kuuluvad nad s-elementide hulka, kuna nende aatomite välisel orbitaalil on üks elekt- 1 ron. Sellest tulenevalt on kõikide leelismetallide aatomite väliskihi elektronvalemiks ns ja oksüdatsiooniastmeks ühendis +I. Kuna leelismetallidel on väliskihis ainult üks elektron, siis seetõttu nad loovutavad selle ...
Põltsamaa Ametikool Materjaliõpetus A1 Andres Asson Kaarlimõisa 2009 Sisukord 1.Metallid.............................................................................................................3 1.1 Metallide füüsilised omadused.......................................................................3 1.2 Metallide keemilised omadused.....................................................................3 1.3 Metallide tehnoloogilised omadused..............................................................3 2.Metallid..............................................................................................................4 2.1 Füüsikalised om...
MAGNEESIUM Ajalugu Magneesiumiühendeid tunti ammu enne elemendi avastamist. Magnesia usta nime all tunti magneesiumoksiidi, magnesia alba nime all magneesiumkarbonaati või magneesiumoksiidi ja magneesiumkarbonaadi määramata vahekorras hüdratiseeritud segu. Nende nimetuste järgi on element nime saanud. Arvatavasti on magnesia nime saanud Vana-Kreeka maakonna Tessaalia piirkonna Magneesia järgi: sealt saadi nimetatud aineid. Esimene, kes magneesiumi ühendeid süstemaatiliselt uuris, oli soti füüsik ja keemik Joseph Black. Aastal 1755 näitas ta teoses "De humore acido a cibis orto et Magnesia alba", et lubjakivi ja magnesia alba, mida tol ajal sageli segi aeti, on erinevad ained. Ta käsitles magnesia alba't uue elemendi karbonaadina. Sellepärast nimetatakse Blacki sageli magneesiumi avastajaks, kuigi ta ei saanud magneesiumi lihtainena. Aastal 1808 sai Humphry Davy magneesiumi, elektrolüüsides niisutatud magn...