Traditsioon laulda, meenutades kokkuhoiduvust ja usku vabadusse, on tänaseni säilinud, sest seda on vaja, see on osa igast eestlasest, kes vähegi oma rahva eest seisab ja kannatab. Ameerika luuletaja Delmore Schwartzi süvamõtteline fraas kinnitas mu oletust, et inimene on alati igatsenud igikestvust. ,,Ainult minevik on surematu," väärikalt kõlav tõde, mis õigustab religiooni, alkeemikute ja maagide elutööd: otsida võimalust jääda ajalukku, kinnitada osake endast traditsioonidega ülekoormatud igavikku. Daniel Vaariku tähelepanek võrdleb seda tungi saada osa surematusest kõikvõimsa looduse seadustega: ,,Traditsioonidele on iseloomulik mineviku venitamine tagurpidi pikksilmaks, mille toru otsast sisse vaadates jääb mulje, et mingi asi on olnud aegade algusest peale, vahel jääb mulje, et tegemist on lausa loodusseadusega." Siit leiab veel ühe põhjenduse, miks on traditsioone vaja: saamaks rahuldatud soovi osaleda
Mina kui osake ühiskonnast Igaüht meist ümbritseb mingisugne ühiskond. Koolis ümbritseb õpilasi õpetajad, töötajaid tööl teised töötajad ja tänaval jalutades ümbritsevad meid teised inimesed. Kas ühiskond on alati mingi kindel inimgrupp? Ei pea olema. vahel on meid ümbritsev ühiskond lihtsalt mets ja linnulaul. Millist rolli mängin mina ühiskonnas? Kes moodustab minu ümber kõige lähedasema ühiskonna? Selleks grupiks võin ma lugeda enda perekonda. Iga päev, hommikust õhtuni, puutun ma kokku oma perekonnaga. On olemas ema, kes teeb mulle süüa ja isa, keda ma aitan igasugustes abitöödes. Millist rolli etendan mina enda perekonnas? Kindlasti ei saa ma öelda, et ma olen ainult vaatamisobjekt, kelle eest hoolitsetaks. Ma olen muutunud enda perekonnas asendamatuks ja selleks ma ka jään. Siis, kui on vaja teha mingit tööd, siis olen ma alati see inimene, kes aitab. Teise olulise grup...
AATOMIFÜÜSIKA Aatom (vana-kr atomus jagamatu) on keemilise elemendi väiksem osake. 19.saj. lõpus avastati et aatom ei ole jagamatu. 1897.a. avastati ELEKTRON(-), väike osake, mis pesitseb aatomis. J.J.Thompson. Th aatomimudel e. Rosinakukkel. E.Rutherford palus pommitada õhukest kuldlehte alfaosakestega. Avastas aat tuuma 1911 selle katsega. Planetaarne mudel e RUTHERFORDI mudel on vastuolus klassikalise füüsikaga 1) Tiirlev elektron peaks tekitama elektromagnetlaineid 2)kiirgav elektron peaks kiirgama energiat ja kukkuma vastu tuuma. DE BROGLIE HÜPOTEES Igal osakesel on olemas laine omadused, mille lainepikkust saab
majandusliku õitsengu ja tunneb ka majanduskriisist tekkinud raskusi, võin väita, et iga inimene, kes riigis elab, tunnetab ühiskonna käekäiku. Nii nagu tööpuudus kajastub eelkõige töötuks jäänud inimeste näol, nii ka paremaid aegu näeb läbi meie endi rahakottide. Kindlasti aitame me kõik kaasa ühiskonna heaolu saavutamisele. Nii maksude maksmisega kui ka lihtsamate asjadega, milleks on eestimaiste toodete tarbimine, kui ka prügisorteerimine. Mina, kui osake ühiskonnast, võin julgelt öelda, et olen olnud kohusetundlik maksumaksja, suvel ametlikult tööl olles, kavatsen riigikogu valimistel hääletada, andes sellega oma panuse riigi heaolu nimel ning kindlasti hoian loodust ning olen alati abivalmis ning koostöövõimeline. Inimese sotsiaalne olemine on alati olnud ning on edaspidigi korrastatud elamisviis ning pole kahtlustki, et see meid omamoodi kujundab. Lihtsaim näide on
Valgus – osake ja/või laine Valgus on elektromagnetlained mis levivad ruumis. Elektromagnetlainete spekter on lõpmatult lai ehk valguseks nimetatakse spektriosa mis jääb raadiolainete ja röntgendiapasooni vahele. Seega on valgusel nii lainete kui osakeste omadused. Mida kõrgema sagedusega, energiaga, on kiirgus seda rohkem on tegemist osakeste omadustega ja vastupidi. Nähtav valgus on vahemikus 400-700 nm. Ja seega omab samuti mõlemaid omadusi. Valguse olemuse kohta tekkis 17. sajandil paralleelselt kaks teooriat (vaata ka pilti): Isaac Newton oletas, et valgus on valgusallikast igas suunas väljuvate osakeste voog (valgus on erilise „valgusaine“ edasikandumine ruumis). Christiaan Hygens oletas, et valgus on eriliste lainete voog, mis levib ruumi täitvas ja kõikidesse kehadesse tungivas keskkonnas – eetris. 19. sajandi alguses avastati elektromagnetlained (M...
"Valgus - osake või/ja laine?" Kõigile on teada, mis on valgus ja milline see välja näeb. Esmaselt enamasti nimetavad valguse tähenduse all päikest ja lampe. Teadupärast on valgus energia allikas ja valguse kätte jäävad kehad soojenevad tänu siseenergia suurenemisele. Aga kas valgus on osake või laine? Või hoopiski mõlemat? Tegelikult on valgus elektromagnetlaine, mis tekib elektrilaengute kiirendusega liikumisel. Valgus on ainuke elektromagnetlaine, mis on inimese silmale nähtav. Valgus on ka muutuv ja see oleneb valguseallikast. See tähendab, et erinevatel lainepikkustel on valguse värv erinev. Seda saab vaadelda näiteks difraktsiooni võrega. Difraktsioon on nähtus kus valgus paindub läbi avade või tõkete varju piirkonda.
Fukushima kriisi tagajärgede aktuaalsusest 2014 a alguses Ülivõimas maavärin ja selle põhjustatud tohutu hiidlaine põhjustasid 2011. aasta märtsis Fukushima reaktorite sulamise ning sundisid evakueerima kümneid tuhandeid inimesi. Tegemist oli rängima tuumaõnnetusega pärast 1986. aasta Tsernobõli katastroofi. Tappis 15,884 inimest ja 2,636 on endiselt kadunud. Radioaktiivne vesi Fukushima tuumaelektrijaamas on siiani suurim probleem, mis takistab kriisi tagajärgede puhastusprotsessi. Radioaktiivset vett lekib mahutitest koguaeg. Kandub Vaiksesse ookeani, kust triivib hoovuste tõttu umbes 5 aastaga USA läänerannikule. Reaktorite südamike tegelikku olukorda ei tea keegi, sest elektroonika (kaamerad, robotid) ei pea sealsele kiiritushulgale vastu. Kardetakse, et kolm 100 tonnist kütuseollust on tunginud läbi reaktori vundamendi. Oht seisneb selles, et kui sulanud tuumakütuse reostus maapõues leiab tee Tokyo vesikonda, siis evakueeritaks...
Millal on keha elektriliselt laetud? Kui tal on omadus teisi kehasid enda poole tõmmata. Millised on kaks võimalust tema laadimiseks? Kui neid hõõrutakse omavahel (klaaspulk ja siid, tõmbavad pärast enda poole pabertükikesi) või kui ühelt kehalt kandub elektrilaeng ka teisele (kui elektriseeritud klaaspulk puudutab niidi otsas metallkera). Milline osake põhjustab elektrinähtusi ja millal see osake avastati? Elektron, aastal 1897. Iseloomusta elektrilaengut. Elektrilaenguta osakest või keha nimetatakse elektriliselt neutraalseks. Elektrilaenguid nimetatakse positiivseteks ja negatiivseteks. iseloomustab elektromagnetilises vastastikmõjus osalemise ja elektromagnetvälja tekitamise ning sellele allumise intensiivsust ja viisi. Elektrilaengu tähis on tavaliselt Q või q. Elektrilaengu mõõtühik SI-süsteemis on kulon (tähis: C).
Does the Higgs Field do something? Dmitri Martila ([email protected]) Latter affiliation: Tartu University (Dated: September 16, 2016) Abstract Is studied the possibility to replace the Dark Matter and the Dark Energy with the single Higgs Field (or fields). The study in close direction was made in arXiv:1603.06242, and in “The Higgs Boson May Disintegrate into Dark Matter” (the Google News). Just because the physics is physical, then the Higgs Field do exist, do exist throughout the spacetime, and even acts on curvature of the spacetime even in the cosmic void (the places without the baryonic matter). In case of the places with the baryonic matter the Higgs Field emits the Higgs Boson to give the baryonic matter the right amount of mass: therefore the density of the Higgs Fie...
Elektrivool Elektrivool kujutab endast vabade laetud osakeste suunatud liikumst. Vaba laetud osake pole seotud oma aatomiga. Vabadeks laetud osakesteks võivad olla elektronid, ioonid või augud. Elektriväli mõjutab laetud osakestele elektrijõuga ja see paneb nad liikuma. Seega, elektrivoolu tekkimise tingimusteks on 2 asjaolu: 1) Vabade laetud osakeste olemasolu 2) Elektrivälja olemasolu Metallis on vabu elektrone. Elektriliste omaduste poolest jaotatakse ained kolmeks: 1) Elektrijuhid(Juhid) – Kõik ained, mis juhivad elektrit, eriti head on hõbe, kuld, vask, alumiinium
RADIOAKTIIVSUS (Avastas Becquerel) AATOMI TUUM A Z X Tuumas on Z prootonit ja N neutronit. Tuumamass A=Z+N 209 84 Po (Z=84, N=209-84=125 neutronit) (Alates 84 radioaktiivsed) Radioaktiivse kiirguse omadused: Intensiivsus on muutumatu/mõjutamatu Kiirgus kannav endaga energiat. Radioaktiivse kiirguse tulemusena üks keemiline element muundub teiseks. Radioaktiivse kiirguse liigid: -osake heeliumi aatomi tuum. Omadused: Positiivselt laetud. Väikseim läbitungimisvõime. Magnet-ja elektriväli kallutavad neid väga nõrgalt.(1 elementaarlaengu kohta 2 aatommassiühiku suurune mass. Laeng võrgne kahekordse elementaarlaenguga.) -elektronide voog Omadused: -osakeste kiirused pole ühesuurused, kiirguses esineb väga erinevate kiirgustega liikuvaid osakesi.kalduvad nii magnet- kui ka elektriväljas oma esialgsest teest tugevasti kõrvale. Vaögusega lähedase kiirusega
Kokkuvõte Koostatud Bioloogia IX klassile õpiku põhjal 1) Raku ehitus 1) Raku tähtsam osa on tuum, mis juhib raku tegevust, tuumas paiknevad kromosoomid, mis sisaldavad geene. Rakutuuma ümbritsevad kaks membraani. Membraanideks on poorid. Tuumaväline osa kaetud tsütoplasmaga. 2) Rakk on kõige väiksem osake, millel on omane elutegevus ja mis võib elada iseseisvalt 3) Ühesuguse tekke, ehituse ja talitlusega rakud moodustavad kogumikke, mida nimetatakse kudedeks st. koed koosnevad rakkudest. Tähtsamad organellid on mitokondrid nad varustavad rakku energiaga, mida on vaja elutegevuseks Ribosoomid neis sünteesitakse valke Lüsosoomid membraaniga ümbritsetud põiekesed, mis sisaldavad lõhustavaid ensüüme Vakuoolid õhukese membraaniga ümbritsetud rakumahla mahutid
KONTROLLTÖÖ KÜSIMUSED 1) Aatom on väike osake, mille hulgast kõik asjad maailmas koosnevad. Nimi on seetõttu, et see tuleb Kreeka keelest ning tähendab jagunematut, mis tähendab seda, et aatomit enam väiksemaks osaks jaotada ei saa. 2) Thomsoni aatomimudel - ruumlaeng võrdne ja vastasmärgiline elektroni omale. Bohri aatomimudel - elektronid ei kiirga, kuid tiirlevad Rutherfordi mudel - planetaarmudel 3) See, et elektronide hajumisnurk on seda suurem, mida väiksem on osakeste arv. Jõudis selleni, et
C2H6(keemistemp etaan C7H16(keemist. heptaan -89) 98) C3H8(keemistemp propaan C8H18(keemist. oktaan -42) 126) C4H10(keemist- butaan C9H20(keemist. nonaan 0,5) 151) C5H12(keemist. pentaan C10H22(keemist.1 dekaan 36) 74) Radikaal – osake, millel on üks paardumata elektron. Alkaanide tüüpilised reaktsioonid on pürolüüs ja oksüdeerumine. Elektrofiil on tühja orbitaali ja positiivse laengu osake. Nukleofiil on vaba elektronpaariga osake ja kannab negatiivset laengut. Alkaanide füüsikalised omadused: Homoloogilises reas C aatomite lisandudes muutuvad kõrgemaks tihedus, sulamistemp., keemistemp. Alkaani nimetuse kirjutamise skeem - nr- asendaja-nr-asendaja-tüviühendi nimetus
MIS ON MAJANDUSTEADUS? Majandusteadlane Alfred Marshall (1842-1924) ütles, et majandusteadus on ,,osake igapäevaelust". Otsustamine on inimeste igapäevane tegevus. Inimesed otsustavad iga päev , kuidas oma vajadusi rahuldada. Majandusteadus on sotsiaalteadus, mis uurib seda, kuidas inimesed, tegutsedes üksi või rühmiti, otsustavad, kuidas kasutada nappe ressursse oma vajaduste rahuldamiseks. Tootmine on protsess, mis ühendab majandusressursid nii, et müügile antakse kaubad ja teenused. RESSURSID: esimene samm vajaduste rahuldamiseks. Ressursid on
~ 50 kg. 10.Kust saadakse ahelreaktsiooni käivitavad neutronid? Loodusest, teised tekivad reaktsiooni käigus. 11.Kirjelda tuumareaktori ehitust. Betoonümbris, tuumkütus, juhtvardad, aeglusti, neutronipeegeldi. 12.Milleks kasutatakse tuumareaktoreid? Tuumajaamades elektri tootmiseks, allveelaevades samuti. 13.Millised on tuumaasjandusega seotud põhilised looduskaitseprobleemid? Radioaktiivsed jäätmed. 14.Millised on bioloogilistele organismidele ohtlikud kiirgused? -osake ; -osake ; -osake 15.Mis on kiirgusdoos?Millistes ühikutes seda mõõdetakse? Kiirguse hulk. Mõõdetakse greides. 16.Mis on dosimeeter? Kiirgusmõõdik. 17.Mis on kiiritushaigus? Haigus, mis kaasneb ülemäärase kiirguse doosist. 18.Millised on kiiritushaiguse esmased nähud? Erutus, peapööritus, peavalu, iiveldus, oksendamine, palavik, hingamise ja südametegevuse kiirenemine. 19.Millised on põhilised kiirguskaitse meetmed? Heledad riided, kiirguse eest varjumine,
elektronkihid, prootoni, neutroni ja elektroni laengud ja massi. 3. Tooge välja aatomi ehituse seosed perioodilisustabeliga (tuumalaeng, prootonite, neutronite ja elektronide koguarv, elektronkihtide arv, e arv väliskihil, elektronskeem). 4. Selgitage mõisted: liht- ja liitaine. Liht- ja liitainete eristamine valemi põhjal. Tooge näiteid nimetuste ja valemitega liht- ja liitainetest 1. Keemiline elemen on kindla tuumalaenguga aatomite liik Aatom on üli väike aine osake, mis koosneb tuumas ja elektronidest Prooton on aatomi tuuma osa , millel on positiivne laend Neutron on aatomi tuuma osa ja sellel puudub laeng see tähendab, et ta on neutraalne Elektroonid on üliväikesed negatiivsete laengudega osakesed, mis moodustavad aatom tuuma ümber elektroonkatte Lihtaine on aine, mis koosneb ainult 1 aine okestest. Liitaine on aine mis koosneb vähemalt kahe erineva aine osakestest. Molekul on väike aine osake, mis koosneb omavahel seotud aatomitest
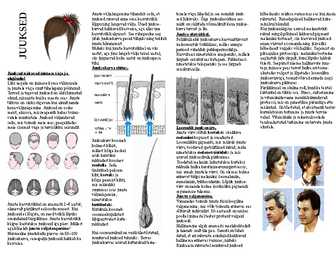
Stress, suitsetamine olnud, nii naiste kui ka meeste seas. Juuste ja vitamiinidevaene menüü kiirendavad tähtsus on siiski sügavam kui ainult nende protsessi, mis on geneetilise pärandiga ette kena väljanägemine. Juuksed on osake määratud. On tõestatud, et eksisteerib teatav meist, elusosa, mis reageerib kehas toimu- korrelatsioon toitumise ja juuste tervise vatele muutustele. Juuksed väljendavad vahel
5. TUNTUSE SAABUNIME LÄBI TUNDEKÜLLASE "PIPI"......................................11 KOKKUVÕTE.................................................................................................................. 13 KASUTATUD KIRJANDUS............................................................................................14 2 SISSEJUHATUS Astrid Lindgren on osake meie elust. Mitu põlvkonda on ammutanud temalt rõõmu ja jõudu. Need, kes lugesid "Pipi Pikksukka" 40-ndatel aastatel Rootsis ja 60-ndatel aastatel Eestis, loevad seda nüüd oma lastele ja lastelastele. Astrid Lindgrenile on jagatud tunnustust ja auhindu kogu maailmas, tema raamatuid armastatakse kõikjal. Lindgreni jutud kajastavad humoorikalt ja sisendusjõuliselt laste tundemaailma ja argielu. Käesoleva referaadi eesmärgiks on tutvustada lähemalt kuulsat lastekirjanikku,
Halogeenühendis on elektronpaar suunatud elektronegatiivsema Side süsiniku ja elemendi kloori vahel ehk kloori katkeb ningpoole, tekib seetõttu OH - ja OH moodustab süsinikuga sideme, ning tõrjub Cl-i - onCmolekulis vahele osalaengud. välja (on ründav osake). Keemilised omadused Eelnev reaktsioon võrrandina + - + - H3C Cl + KOH H3C OH + KCl elektro-nukleo- elekt-nukleo- fiil fiil rofiil fiil elektrofiil elektrofiil nukleofiil nukleofiil Rebane kui tugevam nukleofiil sai nõrgamalt nukleofiilit kätte elektrofiili Toimus asendusreaktsioon elektrofiil elektrofiil
radikaal- Radikaal on aatom või aatomite rühm, millel on paaritu arv elektrone. pürolüüs- Aine või materjali lagunemine kõrge temperatuuri toimel. halogeeniühend- Süsinik-halogeen sidet sisaldav orgaaniline ühend. ahelisomeeria- süsinikahela kuju on erinev asendiisomeeria- kordsed sidemed või funktsionaalrühmad paiknevad ühesuguse süsinikahela korral erinevalt. osalaeng- negatiivne või positiivne laeng BETAplus/miinus elektrofiil- elektroniarmastaja, ühend või osake, millel on elektrofiilne tsenter. (tühja orbitaali ja positiivse laenguga) elektrofiilne tsenter- aatom, millel on tühi või osaliselt täitmata orbitaal ning pos laeng või osalaeng. nukleofiil- tuumaarmastaja, ühend või osake, millel on sukleofiilne tsenter.(vaba elektronpaariga osake, omab negatiivset laengut) nukleofiilne tsenter- nukleofiili koostisse kuuluv vaba (sidemeks kasutamata) elektroni-paariga aatom ründav osake- reaktsiooni alustav osake (asendusreakts
isomeerid- ühesuguse atomaarse koostise (molekulaarvalemi) ja molekulmassiga, kuid struktuurilt ning füüsikalistelt ja keemilistelt omadustelt erinevad keemilised ained. vesinikside- side, mille moodustab positiivse osalaenguga vesiniku aatom mittemetallide (F,O,N) vaba elektronpaariga (ja negatiivse osalaenguga) aatomiga. hüdrofoobsus- veetõrjuvus, ühendi võimetus vaststikmõjuks veega. hüdrofiilsus- veelembus, ühendi võime vastastikmõjuks veega. radikaal- osake, millel on paardumata elektron. pürolüüs- aine muundumine kõrge temperatuuri toimel. halogeeniühend- orgaanilised ühendid, kus süsiniku aatom on seotud halogeeni aatomi või aatomitega,enamasti vedelikud või tahked, harva gaasid, veest raskemad, hüdrofoobsed. ahelaisomeeria- tuleneb süsiniku aatomite vaheliste sidemete erisugusest järjestusest süsinikahelas. asendiisomeeria- tuleneb funktsionaalsete rühmade erisugusest paigutusest ühesuguse süsinikahelaga molekulides.
1. aineosakesed- aatom,molekul,ioon. * keemiline element- teatud kindel aatomite liik * aatom- keemilise elemendi väiksem osake, molekuli koostisosa * molekul- aine väiksem osake, koosneb aatomitest * ioon- laenguga aatom (aatomite rühm) - positiivne ioon e. katioon tekib kui aatom loovutab väliskihilt elektrone - negatiivne ioon e. anioon tekib kui aatom liidab väliskihile elektrone 2. Elementaarosakased- prooton,neutron,elektron, asuvad aatomis (aatomi sees) * prooton- aatomtuuma positiivse laenguga osake (laenguga+1,mass 1,asub tuumas * neutron- aatomtuuma laenguta osake? (laenguga 0, mass 1,asub tuumas) * elektron- elektronkatte negatiivse laenguga osake
Halogeenühendid- org.ained, mille C aatomid on seotud halogeeni aatomiga. Füüsikalised omadused: 1)ei moodusta vesinik ühendeid (hüdrofoobsed) 2)suure tihedusega, veest raskemad. 3) lahustuvad piirituses ja bensiinis. Füsioloogilised omadused: 1) Mürgised. 2) narkootilise toimega. 3) kahjustavad kesknärvisüsteemi ja maksa. MÕISTED: 1) nukleofiil- vaba elektronpaariga ja neg laenguga aine osake. 2)Elektrofiil- tühja orbitaliga ja pos.laenguga aineosake. 3)nukleofiilne tsentner- neg.osalaenguga aine osake molekulis/ aines. 4) lektrofiilsus tsentner- pos. Osalaenguga aine osake molekulis/ aines. 5) nukleofiilne asendusreaktsioon- reaktsioon, mille tulemusena elektrofiilsed ja nukleofiilsed rühmad ühinevad. 6) Radikaal- osake millel on paadumata elektron.
Asendusnomenklatuur asendusrühma tüviühenduga liitumise kohta tähistatakse kohanumbriga. Funktsionaalnomenklatuur halogeeniühendi nimi moodustatakse süsivesinikrühma nimetusest, millele lisatakse liide. Elektrofiil on tühja orbitaali ja positiivse laenguga osake. Nukleofiil on vaba elektronipaariga osake ja kannab negatiivset laengut. Nukleofiilse asendusreaktsiooni korral: nukleofiil on ründav osake; reaktsioonitsenter on elektrofiilne tsenter; lahkuv rühm eraldub nukleofiilina. Elektrofiilne asendusreaktsioon: elektrofiil ründab nukleofiilset reaktsioonitsentrit; lahkuv rühm eraldub elektrofiilina. Reaktsiooni analüüsimine: *Selgita välja elektrofiilus, *tee kindlaks milline on ründav osake, milline on lahkuv rühm. Freoonid madala molekulmassiga alkaanide, enamasti metaani või etaani fluoro-kloroderivaadid. Plastiidid bioloogiliselt aktiivsed
KEEMIA KT keemiline element- kindla tuumalaenguga aatomite liik aatom- neutraalne osake, mis koosneb aatomituumast ja elektronkattest prooton- positiivse laenguga osake, mis kuulub aatomi koostisesse neutron- laenguta osake, mis kuulub aatomi koostisesse elektron- negaiivse leanguga osake, mis kuulub aatomi koostisesse lihtaine- koosneb ühe keemilise aine osakestest liitaine- koosneb mitme keemilise aine osakestest molekul- aineosake, mis koosneb aatomitest ioon- laengu omandanud aatomite katioon- positiivne ioon anioon- negatiivne ioon kovalentne side- ühiste mittematalli aatomite elektronpaaride abil tekkinud side iooniline side- vastasmärgiliste ioonide tõmbumine metalliline side- metalli aatomite vahel molekulaarsed ained- molekulidest koosnevad ained
·Madalamad halogeeniühendid aurustuvad kergesti, magusa lõhnaga Hüdrofoobsed => ei lahustu vees Suur tihedus (veest raskemad) Enamus on mürgised HALOGEENIÜHENDITE NOMENKLATUUR · Asendusnomenklatuur asendusrühmad + tüviühend fluoro-, kloro-, bromo-, jodo- · Funktsionaalnomenklatuur -süsivesinikrühm + aineklass fluoriid, -kloriid, -bromiid, -jodiid Halogeenühendite nomenklatuuri näited Elektrofiil tühja orbitaaliga osake · Elektrofiilsustsenter - elektrofiili koostisse kuuluv tühja või osaliselt tühja orbitaaliga aatom · Positiivne laeng või osalaeng + · Püüavad moodustada keemilist sidet, täites oma tühja orbitaali teise osakese vaba elektronipaariga · C, H Nukleofiil vaba elektronipaariga osake · Nukleofiilsustsenter nukleofiili koostisse kuuluv vaba (sidemeks kasutamata) elektronipaariga aatom · Negatiivne laeng või osalaeng -
elektrofiil- tühja orbitaaliga osake nukleofiil- vaba elektronpaariga osake elektrofiilsus tsenter- aatom, millel on positiivne laeng või osa laeng nukleofiilsus tsenter- aatom, millel on negatiivne laeng või osa laeng lahkuv rühm- rühm, mis tõrjutakse välja asendusreaktsioonist freoonid- klorofluoroalkaan pestitsiid- haigustekitajate, taimekahjurite või umbrohtude tõrjeks kasutatav mürkkemikaal Vähesed hü on toatemp gaasilised. Enamik vedelikud või tahked ained. Nad on hüdrofoobsed ega lahustu vees, tihedus on üpris suur
· hüdrofoobsed, ei lahustu vees · suur tihedus · halogeenid veest raskemad, alkaanid kergemad Füsioloogilised omadused: · mürgised · kergesti lenduvad (narkootiline toime) · põhjustavad raskeid kesknärvisüsteemi ja maksa kahjustusi Elektrofiilsustsenter on pos. osalaenguga või pos. laenguga aatom aines. Nuklofiilsustsenter on neg. osalaenguga või neg laenguga aatom aines. Elektrofiil on tühja orbitaaliga ja positiivse laenguga aine osake. Nukleofiil on vaba elektronbaariga ja negatiivse laenguga aine osake. Radikaal on osake, millel on paardumata elektron. Nukleofiilne asendus on reaktsioon, mille tulemusena elektrofiilse tsentri juures üks nukleofiilne rühm asendub teisega. Halogeeni ühenditele on iseloomulik nukleofiilne asendusreaktsioon. 1) Nukleofiilse asendusreaktsiooni kutsub esile nukleofiil.(ründav osake) 2) Ründab halogeeniühendis elektrofiilsustsentrit
Et vastata pealkirjas toodud küsimusele, tuleb uurida laetud osakeste käitumist homogeenses ja mittehomogeenses magnetväljas. Järgneval joonisel on vasakul kujutatud homogeenset ja paremal mittehomogeenset magnetvälja. Homogeense magnetvälja korral on B vektor kogu ruumis ühesuguse pikkuse ja suunaga. Homogeense välja magnetilise induktsiooni jooned (jõujooned) on omavahel paralleelsed sirged, mille vahekaugus ei muutu. Kui laetud osake lendab homogeensesse magnetvälja risti magnetilise induktsiooni joontega, hakkab ta liikuma ringjoonelisel orbiidil. See on nii sellepärast, et Lorenzi jõud on igal hetkel risti osakese kiirusvektoriga. Kõrvaloleval joonisel on skemaatiliselt kujutatud elektroni ja prootoni liikumistrajektoorid homogeenses magnetväljas. Newtoni teise seaduse (F=ma) järgi evB=mv2/R, millest trajektoori kõverusraadius R=mv/eB Kõrvalekaldumise suund määratakse vasaku käe reegliga.
Reklaamid kui internetis edu saavutajad Tänapäeval on reklaamid kõikjal meie ümber. Telekas, raadios, linnatänavatel ja isegi ühistranspordis ja autodel . Reklaamid on juba osake meie ühiskonnast ning laieneb iga aastaga . Reklaamid ise on kas mingit toodet või teenust tutvustav video, pilt või heli. Reklaami eesmärkideks saab pidada tarbija ligimeelitamist ja toote või teenuse teadlikkuse edendamist, mõlemate juhtude puhul on tegu turundusliku eesmärgiga . Reklaamid võivad olla ka manipuleerivad ning neid saab liigitada mitmeti: meediakanalite, teemade/valdkondade, piirkonna ja tellijate järgi. Kuidas
asendusderivaati funktsionaalnomenklatuur + nt orgaaniliste ühendite nimetamise moodus, mille järgi ühendiklassi nimetus koostatakse tüvistruktuuri nimetusest ja sellele järgnevast ühendiklassi kirjeldavast liitest osalaeng- , erinev ioonlaengust. Kasutatakse orgaanilises keemias, kuna elektronpilt on tõmmatud elektronegatiivsema elemendi poole elektrofiil ühend või osake, millel on elektrofiilne tsenter nukleofiil- ühend või osake, millel on nukleofiilne tsenter reaktsioonitsenter- aatom või aatomite rühm, mis osaleb ning muundub reaktsiooni käigus lahkuv rühm- rühm, mis tõrjutakse välja asendusreaktsioonid asendiisomeeria- tuleneb funktsionaalsele rühmade erisugusest paigutusest ühesuguse süsinik- ahelaga molekulides ahelaisomeeria- tuleneb süsiniku aatomite vaheliste sidemete erisugusest järjestusest süsinikahelas
Molekul- aine väikseim osake, millel on samad omadused nagu ainel ja ta võib keemilises reaktsioonis laguneda.Aatom- aine väikseim osake, mis koosneb aatomituumast ja elektronkattest.Aatomituum- koosneb prootonites ja neut laneg +.Nukleon- tuumaosakesed prootonid ja neutronid.Prooton- laeng+ mass 1 määrab keemilise lemendi.Neutron- laeng0 mass1.Elektron- elektronkihi üks osa.Ioon- laenguga energia osake,kus elektrone on rohkem või vähem prootonite arvust.Isotoop- sama laenguga erineva massiarvuga element.Laenguarv-Z koosneb prootonite arvust.Massiarv- A tuumaosakeste arv kokku.Tuumajõud- jõud, mis hoiab tuumaosakesi koos.Seosenergia- on võrdne minimaalse tööga,mis kulub liitosakeste lahutamiseks koostisosadeks.Tuumareaktsioon- tuumaenergia muutub elektrienergiaks.Termotuumareaktsioon- kergete tuumade ühinemine kõrgel temp
HALOGEENIDE MÕISTED 1)polaarne kovalentne side moodustub erinevate mittemetallide vahel ühiste elektronpaaride abil. 2)halogeeniühend orgaaniline ühend, milles süsiniku aatom(id) on seotud halogeeni aatomi või aatomitega 3)osalaeng - väiksem elektroni laengust. Väga väike laen 4)elektrofiil on OSAKE, millel on tühi orbital ja/või + laeng 5)elektrofiilne tsenter on AATOM , millel on tühi orbital ja/või + laeng 6)elektrofiilne asendusreaktsioon nukleofiilse tsentri juures üks elektrofiil asendub teisega. 7)nukleofiil on OSAKE, millel on vaba elektronpaar või/ja laeng 8)nukleofiilne tsenter on AATOM, millel on vaba elektronpaar ja/või laeng 9)nukleofiilne asendureaktsioon elektrofiilse tsentri juures üks nukleofiil asendub teisega.
Sellist nomeklatuuri nim. asendus nomeklatuuriks. Lihtsamate hol.ühendite puhul võib kasutada ka funksionaal nomeklatuuri. Nt: CH3-CH2-Br bromoetaan või 2-dietüülbromiid. Elektrofiilid- C ja halogeenide vahel on polaarne kovalentne side. C-l on positiivne osalaeng ja holgeenil negatiivne (osalaengut tähistatakse deltaga). Inooniline dissotsastsioon toimuvad lahustes. CH3 CH2+ : Cl- CH3 : Cl CH3+Cl Elektrofiil on tühja orbitaaliga ja pos. laenguga osake. Nukleofiid on vaba el. paariga osake, millel on neg. osalaeng. Radikaalne dissotsatsioon (tavaliselt gaasidel) H H H :C: H H :C + H H H Radikaal on suure energiaga osake, mis püüab leida teise osakese, millel on üksik elektron. CH3CH2 + H CH3CH3 JÄTA MEELDE 1. Nuklefiid ühineb elektrofiiliga ja vastupidi. 2. Elekrtofiil ei ühine elektrofiiliga, nukleofiid nuklefiiliga. 3. Elektrofiilsus tsentri tunneme ära pos
Hüdrofoobsus-puudub vastasmõj veega,ei moodus vesiniksidemeid. Hüdrofiilsus-veelembus Füsik om-toatemp üldiselt tahked v vedelad, ei moodust vesiniksidemeid e hüdrofoob, tihedus vee omast suurem. Füsoloogil-kõik v.a polümeerid on mürgised-kesknärvisüst,maksa kahjust, narkootilised,ladest organismi,looteea mürgitus muudab vaimne aren(alakaalus imik) Kem om-elektronegat,süsinik ning vesinik seega omavad negat osalaengut. Elektrofiil-fiil=armastama,osake,millel on pos laen v osalaeng soovib liit elektroni(katioon) osakesel on tühi orbitaal. Nukleofiil-osake,millel on negat laeng v osalaeng,soovib liit prootonit(anioon) osakesel on vaba elektronpaar Elektrofiilne tsenter-aatom molekulis,millel pos laeng v osalaeng Nukleofiilne tsen-aatom molekulis,negat laeng v osalaeng. Ründav osake-millel on LAENG(molek ioonide side) metII/I A+mittemet tugev, katkeb keemiline side Reakt tsent-koht molekulis kus toimub rühmade vahetumine
Esimesse kuuluvad seadmed, mis reageerivad osakese läbilennufakti ja võimaldavad mõnel juhul määrata ka tema energiat. Teise rühma kuuluvad nn. jäljekambrid, s.o. seadmed, mis lasevad vaadelda jälgi aines. Registreerivate seadmete hulka kuuluvad ionisatsioonikambrid, proportsionaal ehk võrdelised loendurid ja Geigeri Mülleri loendurid. Laialdase kasutuse said ka Tserenkovi ja stsintillatsiooniloendurid. Aines liikuv laetud osake mitte ainult ei ioniseeri aatomeid, vaid ka ergastab neid. Siirdudes ergastatud olekust põhiolekusse, kiirgavad aatomid nähtavat valgust. Aineid, milles laetud osakesed ergastuvad märgatava välke (stsintillatsiooni), nimetatakse fosfoorideks. Fosfoore on orgaanilisi (benseen, naftaleen, antratseen jt.) ja anorgaanilisi. Kõige enam tarvitatavad anorgaanilised fosfoorid on ZnS-Ag (hõbedaga aktiveeritud tsinksulfiidid) ja NaI-Tl. Prootonite loenduritena kasutatakse tavaliselt plastmass
Fermionid järgivad Pauli keeluprintsiipi. Bosonid ei allu Pauli keeluprintiibile 3) Hadronid ja leptonid. Mis on jaotuse aluseks, millised on vastavate liikide näited. Osakeste jaotus neile mõjuvate jõudude alusel Hadronid: Osakesed, millele mõjub tugev vastastikmõju. Nt: prooton, neutron, piion (pi meson) Leptonid: Osakesed, millele ei mõju tugev vastastikmõju. Nt: elektron, neutriino 4) Osake ja antiosake. Algselt olid osakesed: prooton,neutron, elektron ning nende harvaesinevad antiosakesed: antiprooton, antineutron ja positron. Leptonid: Nõrga vastastikmõju osakesed. Võivad esineda vabade iseseisvate osakestena. Kuna prooton, neutron on elementaarosakesed, siis nim kvarke fundamentaalosakesteks. Igal osakesel peaks olema teisik, vastand – antiosake: * sama massiga osake; * vastand elektrilaenguga osake.
Ca2+, Na+, K+, Mg2+, Cl- • Mikrobioelemendid, minimaalne esinemine inimorganismis on eluks hädavajalik • MIKROBIOELEMENDID: Fe, Cu, Zn, Mn, Co, I, Mo, V, Ni, F, Cr, Se, Si, Sn, B, As Biomolekulid • Biomolekulid: • Sahhariidid • Lipiidid • Valgud • Nukleiinhapped Biomolekulid ei esine väljaspool elusorganisme. Suuremad ja keerulisemad kui teised molekulid. Nimetatakse ka makromolekulideks. • Molekul – aine väikseim osake, mis võib iseseisvalt eksisteerida ja millel on antud aine keemilised omadused. • Aatom – keemilise elemendi väikseim osake, elektriliselt neutraalne • Keemiline element esineb liht – ja liitainete molekulides aatomitena • Molekulid koosnevad aatomitest • Aatomituum – positiivse laenguga aine tihe kogum aatomi keskosas, koosneb prootonitest, neutronitest ja elektronidest • Elektron – negatiivse laenguga osake aatomituumas.
KORDAMISKÜSIMUSED 1. Mille tekitab liikuv osake ja mille paigal seisev osake? Liikuv osake: ¤ magnetvälja Paigal seisev: ¤ elektrivälja ¤ elektrivälja 2. Mida nim. püsimagnetiks? Püsimagnetiks nim. keha, mida ümbritseb alati elektriväli. 3. Valem: jõu arvutamiseks kahe vooluga juhtme vahel. F= K----- K- konstant; l- pikkus; d- juhtmete vaheline kaugus; K= ------ I- voolutugevus; 4. Ampere seadus. F= BIlsin B-magnetvälja induktsioon; I- voolutugevus; l- pikkus;
2) peab pärast looduskeskk. kasut. kiiresti lagunema 3)ei tohi edasi kanduda toiduahelates ega kuhjuda organismides Nukleofiil - : Elektrofiil + Radikaal . (üksikelektron) 1. 1)Pol.kov.side- moodustub erinevate mittemetallide aatomite vahel ühiste el.paaride abil 2)Halogeeniühend- orgaanilised ühendid, milles süsiniku aatomid on seotud halogeeni aatomi või aatomitega 3)Osalaeng- väga väike laeng, väiksem kui elektroni laeng 4)Elektrofiil- ühend või osake, millel on elektrofiilne tsenter 5)Nukleofiil- ühend või osake, millel on nukleofiilne tsenter 6)Elektrofiilne tsenter- aatom, millel on tühi või osaliselt täitmata orbitaal ning posit. laeng või osalaeng 7)Nukleof. tsenter- aatom, millel on vaba või osaliselt vaba elektronipaar ning neg. laeng või osalaeng 8)Radikaal- osake, millel on paardumata elektron 9)Freoon- madala molekulmassiga alkaanide, enamasti metaani või etaani fluoro-kloroderivaadid
Lähemal kui 0,5f muutub tõmbumine tõukumiseks. *Tuumajõud ei olene osakeste elektrilaengust, nad mõjuvad ühetugevuselt kõigi nukleonide vahel. Looduslik radioaktiivsus: *Aatomi tuumade iseenesliku muutusega kaasnev kiirgus. *Kiirgus koosneb 3eriliiki kiirtest. *Erinevad kiirgused käituvad magnetväljas erinevalt ja nende aine läbimisvõime on erinev. Alfa-kiirgus : *Magnetväljas kaldub kõrvale nagu positiivsete osakeste voog. *alfa-osake on heeliumi aatomi tuum. *Ioniseerib ainet tugevasti, läbimitungimis võime väike.Neeldub juba paberilehes. Beeta-kiirgus : *Kaldub kõrvale nagu negatiivsete osakeste voog. * alfa-kiirgus on erineva kiirusega elektronide voog. Ioniseerimis võime väiksem, läbimisvõime suurem kui beeta-osakesel. Beeta-osake: *Magnetväli ei kaldu kõrvale. *Suure energiaga prootonite voog. *Läbimisvõime väga tugev, ei ole olemas ainet, mida ta ei suudaks läbida, saab aint nõrgestada.
vaba elektronpaari omav reagent nukleofiil atakeerib substraadi molekuli, millel on elektronodefitsiitne tsenter, ning tulemusena substraadi molekulis mingi aatom või aatomite rühm asendub mõne teise aatomi või rühmaga. Elektrofiilsustsenter elektrofiili koostisse kuuluv tühja või osaliselt tühja orbitaaliga aatom Reaktsioonitsenter- nukleofiilsus-, elektrofiilsus- või radikaaltsenter, kuhu ühineb ründav osake Ründav osake reaktsiooni alustav osake (asendusreakts. korral asendab teise sama tüüpi osakese reakts. tsentri juures, liitumisreaktsiooni korral ühineb esimesena vastasnimelise reaktsioonitsentriga) Lahkuv rühm asendusreaktsiooni korral väljatõrjutav osake
järgi Kuuma plasma kokkusurumise eksperimendid algasid Ameerika Ühendriikides juba 1938. aastal Tõsine uurimistöö Külma sõja ajal (vesinikpomm) Aatomid rahu nimel konverents (~1950) Energiabarjääri ületamise meetodid Vajalik on energia, mida saab anda mitmel moel: Tuumade kiirendamine Termotuumareaktsioon Külm tuumaühinemine katalüsaatorite abil Tuumade kiirendamine Aatomituumade kiirendamine elementaarosakeste kiirendis Osake-märklaud Osake-osake CERNis (Euroopa tuumauuringute keskus) Large Hadron Collider (LHC) ehk Suur Hadronite Põrkur (1954) Termotuumareaktsioon Tuumadest koosneva plasma kuumutamine temperatuurini, mille puhul tuumad põrkuvad tänu nende soojusliikumisele Tokamak-reaktsioon Plasma kokkusurumine gravitatsiooni poolt, toimub ainult tähtedes Plahvatuslik kokkusurumine Tokamak-reaktsioon Masin, millega toroidaalse (sõõriku-kujulise) magnetvälja abil sulustada plasmat (Tamm ja Sahharov)
rühm/rühmad. Aminohape aminorühmaga asendatud karboksüülhape. Valk - ehk proteiin on biopolümeer, mille monomeerideks on aminohappejäägid. Valgu molekul koosneb paljudest üksteise järele seotud aminohapetest. Fenool benseenituum, mille küljes on 1 OH rühm. Süsivesik ehk sahhariid, on polühüdroksükarbonüülühendite, nende oligo- ja polümeeride üldnimetus. Elektrofiil tühja orbitaaliga osake, millel on elektrofiilne tsenter. Positiivne laeng/osalaeng.(C, H, metalliioonid) Nukleofiil vaba elektronpaariga osake, millel on nukleofiilne tsenter. Negatiivne laeng/osalaeng. (:OH ja :CN tugevad; :Hal nõrk) Radikaal osake, millel on paardumata elektron. Hüdrogeenimine H liitumine ainega. Dehüdrogeenimine H eraldumine aine molekulist. Hüdraatimine H2O liitumine ainega. Dehüdraatimine H2O eraldumine aine molekulist. Hüdrolüüs aine lagunemine vee toimel.
o Molekulmassi kasvades tihedus, sulamis- ja keemistemperatuur kasvab o C1-C4 gaasilised; C5-C16 vedelikud; C17-C... - tahked o Gaasilistel puudub lõhn, vedelatel bensiini lõhn, tahked lõhnatud · Keemilised omadused o Oksüdeerijate suhtes üpris püsivad Reaktsioonide kulgemiseks on vaja side(med) lõhkuda, et võiksid moodustada uued sidemed Osake, millel on üksik paardumata elektron, kannab nimetust radikaal - moodustub metüülradikaal ja vesinikradikaal o Põlemine Täielik a. 2 C4H10 + 13 O2 8 CO2 + 10 H2O Mittetäielik a. 2 C4H10 + 9 O2 8 CO + 10 H2O o Pürolüüs alkaanide lagunemine või isomeerumine kõrgemal
täidetud orbitaal rea mõiste alusel. vabaradikaalsedreaktsioonid: dissotsiatsioon; rekombinatsioon IUPACi nomenklatuur: põhineb hargnemata ahelaga süsivesinike ja asendamata tsüklite nimetusel. · Nukleofiil- vaba elektronpaariga osake, kannab neg laengut (anioonid) · Tüviühend: hargne-nud/-mata või tsükliline struktuur, millega on elektrofiil- tühja orbitaali ja pos laenguga osake (prootonid, seotud H-aatomid metallikatiooniid) Asendusrühm: aatom või rühm, mis asendab tüvistruktuuris H- nukleofiil ühineb elektrofiiliga!! aatomit
Kasutatakse lühikese ja sirgeahelaliste, ühe halogeeniaatomiga ühendite puhul. CH3Cl metüülkloriid CH3CH2Br etüülbromiid Ahelisomeeria: ühendite erinevus on ahela kujus Näide: CH3- CH2- CH2 -CH3 butaan CH3- CH - CH3 isobutaan CH3 Asendiisomeeria:ühendite erinevus on sidemete või funktsionaalrühmade erinevas paiknemises Näide: 1- klorobutaan ja 2-klorobutaan Elektrofiil tühja orbitaali ja positiivse laenguga osake (, metallikatioonid) Nukleofiil vaba elektronpaariga osake, millel on negatiivne laeng (, halogeenid, ) Elektrofiilse tsentri tunneb ära positiivse laengu järgi aatomil. Nuklefiilse tsentri tunneb ära negatiivse laengu järgi aatomil. Nukleofiil ühineb elektrofiiliga. Elektrofiil ei ühine elektrofiiliga ega nukleofiil nukleofiiliga. Nukleofiilse asendusreaktsiooni korral: nukleofiil on ründav osake; reaktsioonitsenter on
Alküünid on kolmiksidemega ühendid(CnH2n-2). Isomeerid on ained, millel on ühesugune molekulvalem, kuid erinev struktuur ja omadused. Monomeer on üksiklüli, millest tekib polümeer. Polümeerisatsioon on polümeeri teke monomeeridest. Fünktsionaalne rühm on aatom või aatomite rühm, mis määrab aine omadused. Radikaal on vaba elektroniga osakesed; reaktsiooni võimelised. Nukleofiil on vaba või osaliselt vaba elektronpaariga negatiivselt laetud osake. Elektrofiil on tühja või osaliselt täitmata orbitaaliga positiivselt laetud osake.
Keemia arvestuse kokkuvõte Aineosakesed- aatom,molekul,ioon. * keemiline element: kindla tuuma laenguga aatomite liik. * aatom: keemilise elemendi väiksem osake, molekuli koostisosa * molekulaarne aine: aine väiksem osake, koosneb aatomitest * molekul: koosneb omavahel seostunud aatomitest. Molekulideks liitumisel lähevad aatomid üle püsivasse olekusse, kus nende energia on madalam. * molekuli valem: näitab, millistest aatomitest molekul koosneb. * indeks: näitab sama elemendi aatomite arvu molekulis. * ioon: laenguga aatom (aatomite rühm) - positiivne ioon e. katioon tekib kui aatom loovutab väliskihilt elektrone - negatiivne ioon e. anioon tekib kui aatom liidab väliskihile elektrone