Süsinikevahelise kaksiksidemega ühendeid nimetatakse alkeenideks. Süsinikevahelise kolmiksidemega ühendeid nimetatakse alküünideks. Süsivesinikke liike on kolm: alkaanid, alkeenid, alküünid. Alkaanid on küllastunud ühendid, alkeenid ja alküünid küllastumata ühendid. Süsinike arv Alkaani Alkeeni Alküüni ahelas nimetus nimetus nimetus CnH2n+2 CnH2n CnH2n-n 1 Metaan - - CH4 2 Etaan Eteen Etüün C2H6 C2H4 C2H2
- Orgaanilised ühendid C; H; O; N; S. - Anorgaanilised ühendid kõik keemilised elemendid. - Anorgaanilised ühendid ca 100 tuhat. - Orgaanilised ühendid üle 10 miljoni ja pidevalt kasvab. - Orgaanilised ühendid sulamis temperatuur on reeglina madal. - Anorgaaniliste ühendite tuleohtlikus on madal, aga orgaanilistel ühenditel on tuleohtlikus väga kõrge. - Termiline püsivus on orgaanilistel ühenditel madal, ja anorgaanilistel ühenditel kõrge. - VALENTS mitu keemilist sidet elemendid moodustavad. Süsiniku valents on 4. - Molekuli valem näitab molekuli elemendilise koostise. - Struktuurvalem - näitab molekuli ehituse e. Aatomite paigutuse. Orgaaniliste ühendite struktuuri teooria: - Igal ühendil on kindel koostis ja temale omane ehitus. SÜSIVESINIKUD Koostis: - C;H Liigid: - Alkaanid nafta; maagaas mootorikütused; lahustid. - Alkeenid nafta; maagaas plastmass; lahustid.
1. Mis on alkeenid? Osata tuua näiteid ( 101, 110 konspekt) Alkeenideks nimetatakse küllastumata süsivesinikke, kus süsiniku aatomite vahel esineb üks kovalentne kaksikside. Alkeenide nimetuse tunnuseks on lõpuliide EEN, mis viitabki kaksiksideme olemasolule süsivesiniku molekulis. Alkeenide üldvalem on CnH2n Laboratoorselt saadakse alkeene alkoholide dehüdratatsioonil (vee eraldamisel): CH3CH2OH CH2=CH2 + H2O Tööstuslikult toodetakse alkeene alkaanide dehüdrogeenimisel (vesiniku eraldamisel): CH3- CH2-CH3 -- H2 + CH3-CH=CH2 (propeen). Tuntum esindaja on ETEEN ehk ETÜLEEN C2H4 2. Mis on alküünid? Osata tuua näiteid Alküünideks nimetatakse küllastumata süsivesinikke, kus süsiniku aatomite vahel esineb üks kovalentne kolmikside. Alküünide nimetuse tunnuseks on lõpuliide ÜÜN, mis viitabki kolmiksideme olemasolule süsivesiniku molekulis. Alküünide üldvalem on CnH2n-2. Alküünide tähtsamaks esindajaks on etüün ehk atsetüleen HCCH. Laboratoorselt
err.ee/artikkel?id=5474&cat=205& (keemia-Nobel 2011) · Orgaaniline keemia on õpetus kõigist süsinikku sisaldavatest ühenditest, välja arvatud karbonaadid ja süsiniku oksiidid. · Orgaanilised ühendid erinevad anorgaanilistest: 1) sisaldavad süsinikku ja molekulmass on suur 2) põlevad 3) kuumutamisel lagunevad madalamal temperatuuril 4) molekulis on aatomite vahel kovalentne side 5) keemilised reaktsioonid toimuvad aeglaselt 6) vees ei lahustu Molekulvalem · Molekulvalem näitab, kui paljudest ja millistest aatomitest molekul koosneb. Näit. C2H6 etaan koosneb 2 aatomist süsinikust ja 6 aatomist vesinikust Struktuurvalem · Struktuurvalem näitab, millises järjekorras on molekulis aatomid asetatud. Näit. H H C alati 4-valentne, I I H alati 1-valentne HCC-H I I H H Isomeeria
ALKAANID JA NENDE NOMENKLATUUR Süsini- Arv- ALKAAN ALKÜÜLRÜHM ehk TSÜKLOALKAAN ke C sõna Üldvalem CnH2n+2 ASENDUSRÜHM Üldvalem CnH2n arv n Üldvalem CnH2n+1 Valem Nimetus Valem Nimetus Valem Nimetus 1 Mono CH4 metaan CH3- metüül- - - 2 Di C2H6 etaan C2H5- etüül- - - 3 Tri C3H8 propaan C3H7- propüül- C3H6 tsüklopropaan 4 Tetra C4H10 butaan C4H9- butüül- C4H8 tsüklobutaan 5 Penta C5H12 pentaan C5H11- pentüül- C5H10 tsüklopentaan 6 Heksa C6H14 heksaan C6H13- heksüül- C6H12 tsükloheksaan
ORGAANILINE KEEMIA II osa (Pildiallikas: http://crdp.ac-amiens.fr/edd/compression/bio/hevea.jpg ) 7.2 ALKEENID Alkeenideks nimetatakse küllastumata süsivesinikke, kus süsiniku aatomite vahel esineb üks kovalentne kaksikside. Alkeenide nimetuse tunnuseks on lõpuliide EEN, mis viitabki kaksiksideme olemasolule süsivesiniku molekulis. Alkeenide üldvalem on CnH2n ALKEENIDE HOMOLOOGILINE RIDA JA NIMETUSTE ANDMINE Küllastumata süsivesinike homoloogilised read algavad süsiniku aatomite arvust kaks, sest mitmikside saab tekkida ainult kahe süsiniku aatomi vahel
Orgaaniliste ühendite nomenklatuur 1. Küllastunud süsivesinikud ALKAANID · Alkaanide homoloogilise rea üldvalem: CnH2n+2 . · Alkaanide molekulis on ainult üks kovalentne üksikside. · Alkaanide homoloogilise rea nelja esimese liikme puhul kasutatakse nimetusi: metaan, etaan, propaan ja butaan. Järgmiste süsivesinike nimetused tuletatakse kreekakeelsete arvsõnade tüvest lõpu aan abil (5 pentaan, 6 heksaan jne). · Ühevalentse radikaali alküülradikaali (kui küllastunud süsivesinikust on eemaldatud üks vesiniku aatom) nimetus tuletatakse süsivesiniku nimetuse lõpu aan asendamisel lõpuga üül (alkaan alküül, etaan etüül, pentaan pentüül). Alkaan (CnH2n+2) Vastav alküülradikaal (CnH2n+1)
· 1,2-diasendus orto- (o), · 1,3-diasendus meta- (m), · 1,4-diasendus para- (p). · Tri- ja enamasendatud benseen numereeritakse tsükkel (asendajatele tuleb anda väikseimad võimalikud kohanumbrid). · Kasutatakse triviaalnimetust nummerdamist alustatakse nimetust andva rühmaga seotud süsinikuaatomist. 1.2. Alifaatsed süsivesinikud Ei sisalda benseenituuma. Jagunevad kolme rühma: alkaanid, alkeenid ja alküünid, millest alkaanid on küllastunud ning alkeenid ja alküünid on küllastumata (sisaldavad kordseid sidemeid). 1.2.1. Alkaanid Lahtise ahelaga küllastunud (süsiniku aatomite vahel üksiksidemed) süsivesinikud. Üldvalem CnH2n+2 Nimetus: lõppliide -aan, mis liidetakse C-aatomite arvu näitavale eesliitele. Alkaanide homoloogilise rea neli esimest liiget kirjeldatakse triviaalnimetustega (kokkuleppelised
mitmiksidemeid) Alifaatne ( ka atsükliline) molekulis pole tsükleid Alkaanid jagunevad normaal(ahelaga) alkaanideks sirgeks pole teda ilus kutsuda , sest nurk on ikkagi ~1100 ja hargneva ahelaga alkaanideks Nimetused Normaalahelaga alkaane nimetatakse Metaan CH4 Pentaan C5H12 Nonaan C9H20 Etaan C2H6 Heksaan C6H14 Dekaan C10H22 Propaan C3H8 Heptaan C7H16 Undekaan C11H24 Butaan C4H10 Oktaan C8H18 Dodekaan C12H26 jne Hargneva ahela korral loetakse pikim ahel peaahelaks ja muud ahelad kõrvalahelateks Peaahel määrab nime lõpu Kõrvalahelate asukoht (mitmenda peaahela süsiniku küljes) näidatakse numbriga
üksik side alkaan Homoloogiline rida: 1. metaan CH4 2. etaan C2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptaan C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22 kaksikside alkeen 12. eteen C2H4 13. propeen C3H6 14. buteen C4H8 15. penteen C5H10 16. hekseen C6H12 17. hepteen C7H14 18. okteen C8H16 19. noneen C9H18 20. dekeen C10H20 kolmikside alküün 32
Created by Riho Rosin 3 13666324649407.doc.doc SÜSIVESINIK Atsükliline Tsükliline Küllastunud Küllastumata Küllastunud Küllastumata Aromaatne (areen) Alkeen Alküün Alkeen Alküün Isomeerianähtus Isomeerid on keemilised ühendid, millel on ühesugune koostis ja molekulmass, kuid erinev molekuli ehitus ning füüsikalised- ja keemilised omadused. Isomeerianähtus on orgaaniliste ühendite arvukuse ja mitmekesisuse põhjuseks. 1. AHELISOMEERIA on tingitud süsiniku aatomite ahela kujust: NT: butaani ja isobutaani molekulivalem on C4H10, ahela kuju erinev:
CCC butaan isobutaan Süsiniku aatomite ahela hargnemine on üheks levinumaks isomeeriavormiks. Ahelisomeeride füüsikalised omadused on erinevad. 2. ASENDIISOMEERIA on tingitud funktsionaalsete rühmade või sidemete erinevatest asendist molekulides. Alkeenide isomeeria sõltub kaksiksideme asukohast. NT: CH2 = CH CH2 CH3 CH3 CH = CH CH3 molekulvalem 1-buteen; but-1-een 2-buteen; but-2-een C4H8 Süsivesinike halogeeniderivaatide puhul põhjustab isomeeriat halogeeni aatomi asukoht. NT: CH3 CH2 CH2Cl CH3 CHCl CH3 molekulvalem 1-kloropropaan 2-kloropropaan C3H7Cl Alkoholide isomeeria põhjuseks on hüdroksüülrühma asend: NT: CH3 CH2 CH2 CH2 CH2 OH molekulivalem
III etapp ahela katkemine toimub siis, kui põrkuvad kaks aktiivset osakest. Kuna nad paiknevad väga hõredalt, siis juhtub 11. klassi Orgaanika konspekt Jaan Usin 2 seda harva ja üks aktiivne osake jõuab põhjustada sadu muundumisi Näiteks. H. + Cl. à HCl või 2H. à H2 ja muud Alkaanid Küllastunud, alifaatsed süsivesinikud, mille üldvalem on CnH2n+2 Küllastunud = molekulis on ainult üksiksidemed (pole mitmiksidemeid) Alifaatne ( ka atsükliline) molekulis pole tsükleid Alkaanid jagunevad normaal(ahelaga) alkaanideks ( sirgeks pole teda ilus
süsiniktetrakloriid. Vesiniku asendamine klooriga on ka redoksreaktsioon ja CCl4 -jas on süsiniku oks.aste maksimaalne 11. klassi Orgaanika konspekt Jaan Usin 2 (+IV). Süsiniktetrakloriid ei saa järelikult põleda ja on üks väga vähestest mittepõlevatest rasvade ja vaikude lahustitest. Kahjuks on ta üpris mürgine Alkaanid Küllastunud, alifaatsed süsivesinikud, mille üldvalem on CnH2n+2 Küllastunud = molekulis on ainult üksiksidemed (pole mitmiksidemeid) Alifaatne ( ka atsükliline) molekulis pole tsükleid Alkaanid jagunevad normaal(ahelaga) alkaanideks ( sirgeks pole teda ilus
ALKAANID Alkaanid on küllastunud süsivesinikud, mis koosnevad süsinikust ja vesinikust ning sisaldavad sp3 süsinikku ehk tetraeedrilist süsinikku ehk nelja üksiksidemega süsinikku. Kovalentseid üksiksidemeid nimetatakse -sidemeteks. Ahela ehituse järgi jaotatakse alkaanid: 1) tsüklit mittesisaldavad (atsüklilised) alkaanid , üldvalemiga C nH2n+2 Need jaotatakse omakorda a)hargnemata ahelaga ehk normaalalkaanid ja b)hargnenud ahelaga . 2) tsüklilised alkaanid ehk tsükloalkaanid , üldvalemiga C nH2n. Nomenklatuur on aine struktuuri ja aine nimetust siduvate reeglite kogu. 1. Hargnemata ahelaga atsükliliste alkaanide valemid ja nimetused ( C nH2n+2 -aan ) 1) CH4 metaan 2) C2H6 etaan CH3-CH3 3) C3H8 propaan CH3-CH2-CH3 4) C4H10 butaan CH3-CH2-CH2-CH3 5) C5H12 pentaan
eeskätt redutseerijad. Nad põlevad C3H6 + 9/2O2 = 3CO2 + 3H2O. Etüüniga (atsetüleeniga ) keevitatakse- Ilma lisaõhuta on leek tahmav, sest vesinikusisaldus on väike C2H2 + 3/2O2 = 2CO2 + H2O Alkeene võib oksüdeerida aldehüüdideks ja hapeteks. Alküüne hapeteks Eteenist saab etanaali C2H4 + 1/2O2 = CH3CHO Hüdreerimine on ühtlasi redutseerimine, selles reaktsioonis on küllastumata ühendid oksüdeerijad C2H4 + H2 C2H6 Kuna küllastumata ühendid on kallimad, siis alkeene praktiliselt ei hüdreerita Pigem vastupidi, alkaanide dehüdreerimisel toodetakse alkeene. Proov kaaliumpermanganaadiga KMnO4 Õrnroosa lahuse toimel oksüdeeruvad alkeenid dioolideks, kuna värvus seejuures kaob (valastumine) saab ka seda reaktsiooni kasutada küllastumata ühendite tõestamiseks. Võrrand on keeruline. R-CH=CH2 R -CH(OH)-CH2OH Tähtsamad esindajad Eteen H2C == CH2
H-C=C-C-C H H-C=C-C-C H H H HH HH CH2=CH-CH2-CH3 C4H8 Üldvalem CnH2n CnH2n-2 Küllastumata süsivesinike omadused lähtudes eteenist Küllastumata süsivesinikud on keemiliselt aktiivsed, kuna kordsesideme koostises olev -side on nõrk ja katkeb kergesti. -nõrk side C-C C=C C=C Alkaan alkeen alküün Keemiline akt suureneb Nii nagu alkaanid on ka esimesed kõige kergemad küllastumata ühendid gaasilised ained, järgnevad vedelad ained (u C5-C6) ja raskemad süsivesikud on tahked. Ükski süsivesinik ei lahustu vees nad on hüdrofoobsed. Enamik neist ei ole mürgised. Keemilised omadused 1. Küllastumata ühendid põlvad a. Täielikul põlemisel tekib happegaas ja vesi CH2=CH2 + O2 2CO2 + 2H2O b. Mittetäielikul põlemisel tekib lisaks CO2-le ja veele vaba süsinik, mis eraldub tahma kujul. CH=CH+O2 CO2 + H2O + C 2
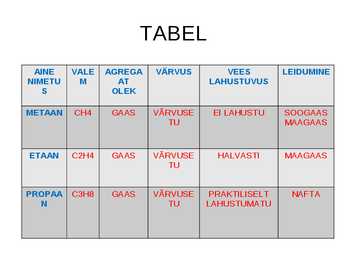
METAAN CH4 GAAS VÄRVUSE EI LAHUSTU SOOGAAS TU MAAGAAS ETAAN C2H4 GAAS VÄRVUSE HALVASTI MAAGAAS TU PROPAA C3H8 GAAS VÄRVUSE PRAKTILISELT NAFTA N TU LAHUSTUMATU ALKAANIDE ÜLDVALEM CnH2n+2 C-aatomite arv Nimetus Valem Olek 1 METAAN CH4 G 2 ETAAN C2H6 A 3 PROPAAN C3H8 A 4 BUTAAN C4H10 S 5 PENTAAN C5H12 6 HEKSAAN C6H14 7 HEPTAAN C7H16 VEDELIK 8 OKTAAN C8H18 9 NONAAN C9H20 10 DEKAAN C10H22 · Alkaanid-lõppsilp-aan Alkeenid-lõpp-een · Keemiliselt on aktiivsemad alkeenid · Metaani esineb:maa,-soo,-kaevandusgaasis
Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline keemia (õpik gümnaasiumile). ,,Avita", Tallinn. Eelnimetatud õpik on ka gümnaasiumi orgaanilise keemia kursuse põhiõpikuks. 3 Sisukord Sissejuhatus orgaanilisse keemiasse 4 Alkaanid 6 Halogeeniühendid 10 Alkoholid 13 Amiinid 15 Küllastamata ühendid 16 Areenid 18 Fenoolid ja aromaatsed amiinid 20 Karbonüülühendid 22 Karboksüülhapped 24
Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline keemia (õpik gümnaasiumile). ,,Avita", Tallinn. Eelnimetatud õpik on ka gümnaasiumi orgaanilise keemia kursuse põhiõpikuks. 3 Sisukord Sissejuhatus orgaanilisse keemiasse 4 Alkaanid 6 Halogeeniühendid 10 Alkoholid 13 Amiinid 15 Küllastamata ühendid 16 Areenid 18 Fenoolid ja aromaatsed amiinid 20 Karbonüülühendid 22 Karboksüülhapped 24
Tallinn 2005 2 Suurem osa konspektis sisalduvast õppematerjalist põhineb gümnaasiumi orgaanilise keemia õpikul: Tuulmets, A. 2002. Orgaaniline keemia (õpik gümnaasiumile). ,,Avita", Tallinn. Eelnimetatud õpik on ka gümnaasiumi orgaanilise keemia kursuse põhiõpikuks. 3 Sisukord Sissejuhatus orgaanilisse keemiasse 4 Alkaanid 6 Halogeeniühendid 10 Alkoholid 13 Amiinid 15 Küllastamata ühendid 16 Areenid 18 Fenoolid ja aromaatsed amiinid 20 Karbonüülühendid 22 Karboksüülhapped 24
ORGAANILINE KEEMIA lühikonspekt gümnaasiumile (II) ALKAANID 1. Sissejuhatus Süsivesinikud orgaanilised ühendid, mis koosnevad ainult süsiniku ja vesiniku aatomitest. Üldvalem CnH2n+2 Alkaanid sisaldavad ainult tetraeedrilisi süsinikke (kõik aatomid on omavahel seotud ühekordsete -sidemetega). Triviaalsed nimetused ühendite nimetused, mis on inimene ühenditele juhuslikult andnud. Need nimetused ei ole süstemaatilised ega väljenda aine keemilist koostist ega struktuuri. Näiteks soogaas, mille süstemaatiline nimetus on metaan (CH4). Süstemaatilised nimetused kajastavad ühendi keemilist struktuuri. Neid on võimalik struktuuri järgi üles märkida.
sio- üldvalem, järelliited omadused saamine, naalne mõiste nimetuses kasutamine rühm -aan CH4 metaan C1-C4 gaasid Maagaas(CH4) 1.)Põlemine(täielik oksüdeerumine) Alkaanid C2H6 etaan C5-C16 vedel. Nafta(vedelate CH4+2O2CO2+2H2O CnH2n+2 alkaanide segu C3H8 propaan C17-...tahked 2.)Pürolüüs(kuumutamine õhu juurdepääsuta) Küllastunud Parafiin(tahke-te süsivesinkud, C4H10 butaan Hüdrofoobsed alkaanide segu) a
aldehüüdid levinud, arvatavasti aldehüüdrühma suure keemilise aktiivsuse tõttu. Enamik suhkruid on siiski aldehüüdide derivaadid. Kuid glükoosi vesilahuses eksisteerib üksnes väike osa glükoosist aldehüüdi kujul. Lineaar Alkeeni sed alka Alküünid d anid nimetus valem nimetus valem nimetus Valem Metaan CH4 Etaan C2H6 Eteen C2H4 Etüün C2H2 Propaan C3H8 Propeen C3H6 Propüün C3H4 Butaan C4H10 Buteen C4H8 Butüün C4H6 Pentaan C5H12 Penteen C5H10 Pentüün C5H8 Heksaan C6H14 Hekseen C6H12 Heksüün C6H10 Heptaan C7H16 Hepteen C7H14 Heptüün C7H12 Oktaan C8H18 Okteen C8H16 Oktüün C8H14 Nonaan C9H20 Noneen C9H18 Nonüün C9H16 Dekaan C10H22 Dekeen C10H20 Deküün C10H18
Ande Andekas-Lammutaja Keemia - Alkaanid Alkaanide üldvalemiks on CnH2n+2 ning nimetuse lõpuks aan. Alkaanid on küllastunud süsivesinikud, kus süsiniku aatomi vahel on kõik ühekordsed sidemed. Küllastunud tähendab seda, et nad sisaldavad maksimaalselt võimalikku arvu vesiniku aatomeid. Süsinik neis ühendeis on kõige suuremal määral redutseerunud. Kõik alkaanid on veest kergemad, ei lahustu vees, värvusetud. Gaasilised alkaanid on lõhnata, vedelad bensiini lõhnaga. Homoloogilises reas muutub aine olek järgnevalt: C1 C4 on gaasilised, C5 C16 vedelikud ning C17 - ... tahked
· Triviaalsed nimetused inimene andis keemilistele ainetele nimed juhuslikult, sageli saamisviisi või omaduste järgi · Süstemaatilised nimetused Kajastavad ühendi keemilist struktuuri, need on ka keemikutele olulisemad · Nomenklatuur aine struktuuri ja nimetust siduvate reeglite kogu Alkaan Nimi Alküülrühm Alküülrühma nimet. CH4 Metaan CH3 Metüül C2H6 Etaan C2H5 Etüül C3H8 Propaan C3H7 Propüül C4H10 Butaan C4H9 Butüül C5H12 Pentaan C5H11 Pentüül C6H14 Heksaan C6H13 Heksüül C7H16 Heptaan C7H15 Heptüül C8H18 Oktaan C8H17 Oktüül
(avatud ahel) (suletud ahel) K arbotsüklilised H eterotsüklilised K üllastatud K üllastam ata (ainult C -aatom id) (C -aatom id ja heteroaatom id) (alkaanid ja nende (alkeenid ja alküün id - küllastatud derivaadid) ja nende derivaadid ) (alitsüklilised) - küllastatud - küllastam ata - küllastam ata (m ittearom aatsed) (m ittearom aatsed) - arom aatsed - arom aatsed
kriit, A portselan,O paber,O kilematerjal,O alumiinium,O teras,O maagaas,O tsellofaan,A süsihappegaas Millised neist ainetest põlevad: CH4 põleb HCl H2O CO C2H2 põleb NH3 H2CO3 H2S Page 13 HBr C2H6 Põleb BaCl H2S Süsiniku ahelad võivad olla hargnematta, hargenud a tsükliks sulgunud. Süsiniku valents on orgaanlistes ühendites alati neli Valents näitab, mitu kovaletset sidet võib antud aatom moodustada. Kui element on ühekordse sama elemendiga on tegemist kovalente üksisksidemega. Kahe elektronpaari abil tekib kovalentne kasksiksida, kolme elektronpaariga kolmikside Nende põhimõtete abil saab kirjutada struktuur valemeid. 1. Metaan CH4 2. Etaan C2H6 3. Propaan C3H8 4. Butaan C4H10 5. Pentaan C5H12
· Polüsahhariidid e polüoosid: · taimedes leiduv tärklis , mis koosneb glükoosi jääkidest ja laguneb inimese seedekulglas ensüümide toimel glükoosiks, loomades ja seentes olev glükogeen. Ülekaalukalt on meie toidu peamine süsivesik tärklis, mida me saame kartulit ja teraviljade teriseid süües. Juhul kui me sööme maksa, liha ja seeni satub meie seedetrakti teatud kogus glükogeeni. 80. + 38. alkaanid looduses ja nende omadused + metaani omadused. Alkaanid on orgaaniliste ühendite rühm, millesse kuuluvad tsükliteta küllastunud süsivesinikud. Alkaanid on atsüklilised süsivesinikud, mille molekulis on maksimaalne võimalik arv vesinikuaatomeid, nii et nad ei sisalda mitmiksidemeid, vaid üksnes üksiksidemeid ehk sigmasidemeid. Laiemas mõttes arvatakse alkaanide alla ka tsükloalkaanid, mis ei sisalda mitmiksidemeid, kuid sisaldavad tsükleid
..........................................................................11 Eetrid.................................................................................................................................... 11 Amiinid.................................................................................................................................12 Alkeenid ja alküünid................................................................................................................13 Alkeenid................................................................................................................................13 Alküünid...............................................................................................................................13 Alkeenide ja alküünide isomeeria....................................................................................... 13 Keemilised omadused................................................................................
molekulides on aatomite vahel valdavalt kovalentsed sidemed. · kuumutamisel õhu juurdepääsuta lagunevad paljud org. ained juba 400C juures (paljud anorg. ained isegi ei sula sellel temp.'l). · org. ühendid põlevad. · valdav osa org. ühendeid esineb nii gaasilises, vedelas kui tahkes olekus molekulidena, anorg. aga kas ioonidest või aatomitest, kuna need pole molekulaarse ehitusega. Süsinikuaatomi ehitus ja valentsmudelid Süsiniku valents on orgaanilistes ühendites alati neli. Valents näitab, mitu kovalentset sidet võib antud aatom moodustada. Süsiniku jaoks saame kasutada kolme erinevat valentsmudelit, s.t. süsinikul on kolm valentsmudelit. Isomeeria Isomeeria on nähtus, kus ainetel on ühesugune elementkoostis ja molekulmass, kuid erinev struktuur ning seetõttu ka erinevad omadused (nt. pentaan ja metüüeutaan (C 5H12). Süsivesinikud Need on sellised orgaanilised ühendid, mis koosnevad süsinikust ja vesinikust
elementidega peab ta väljaspoolt energiat juurde saama. Selle tulemusena 1 elektron s- orbitalilt läheb üle kõrgema energiga p-orbitalile ning nende energiad ühtlustuvad, s.t. läheb üle ergastatud olekusse. Süsinik saab moodustada 4-sidet (neljavalentne). Valentsmudelid tähistavad kolme eri sorti süsiniku aatomit, mis erinevad üksteisest eletronstruktuuri poolest. Süsinikul ja lämmastikul on 3 valentsolekut, hapnikul 2 ning vesinikul 1. -(valents näitab, mitu sidet võib aatomil olla) ALKAANID TETRAEEDRILINE SÜSINIK sp³-süsinik on tetraeedriline süsinik. Lihtsaim näide on mentaan CH H H C H H Süsinikahel olukord, kus mitu tetraeedrilist süsinikku on omavahel seotud.
Alküülrühm alkaanist pärit asendusrühm Nomenklatuur keemiliste ainete nimetuste süsteem Hüdrofiilsus veelembus on aine võime vastastikuliseks mõjuks veega Hüdrofoobsus aine omadus, mille puhul ainel puudub vastasmõju vedelikuga ning aine ei märgu ega lahustu vedelikus ja aine ei saa moodustada vesiniksidemeid Molekuli graafiline kujutis struktuuri lihtsustatud kujutusviis, kus tähistatakse vaid C-C sidemed, funktsionaalrühmad ja sideme nendega Lihtsustatud struktuurvalem valem, mis näitab, millised aatomite rühmad on omavahel seotud. Isomeer ühesuguse atomaarse koostise (molekulaarvalemi) ja molekulmassiga, kuid struktuurilt ning füüsikalistelt ja keemilistelt omadustelt erinevad orgaanilised ühendid Isomeeria ühesuguse elementkoostise ja molekulmassiga, kuid erisuguse struktuuri ning erisuguste füüsikaliste ja keemiliste omadustega ühendite isomeeride olemasolu 2. Isomeeride struktuurvalemite koostamine, nimetuste andmine.