(lammas, kits, küülik jm.) ketramiseks kõlbulikke karvu, mis on saadud pügamisel või kammimisel. · Lambavill on maailma tekstiilitööstuses tähtsaim tooraine, millest valmistatakse täis ja poolvillaseid riideid, vaipu ning mitmesuguseid villaseid esemeid. Villal on mitmeid väärtuslikke omadusi. Vill on suhteliselt kerge ja elastne, värvub hästi, on hügroskoopne ja laseb hästi läbi õhku ning ultraviolettkiiri. OMADUSED pikkus peenus villkarvade säbarus tugevus venitatavus vetruvus elastsus pehmus ja karedus värvus läige VILLA KASVU JA OMADUSI MÕJUTAVAD TEGURID · Lamba villatoodang määratakse aastase villakogusega. Villa kasvu ja selle omadusi mõjutavad paljud tegurid, millest olulisemaks peetakse lamba sugu, iga, tõugu ja füsioloogilist seisundit ning söötmist ja pidamist.
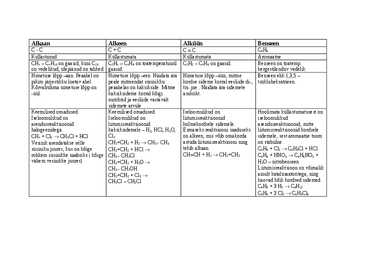
Benseen Lühikokkuvõte Mis on benseen? Benseen, valemiga C6H6 ( vananenud nimega bensool) on lihtsaim aromaatne süsivesinik. Benseeni avastas 1825. aastal M. Faraday. Benseeni saamine. Benseeni saadakse naftasüsivesinikke pürolüüsides või katalüütiliselt aromaatides koksistades. Benseeni füüsikalised omadused. Benseen on omapärase lõhnaga varvusetu vedelik, mille sulamistemperatuur on 5,53°C ja keemistemperatuur 80,10°C. Benseeni keemilised omadused. Benseen ei lahustu vees ja lahustub halvasti metanoolis. Seguneb igas vahekorras bensiini, petrooleumi ja teiste mittepolaarsete lahustitega. Benseen lahustab näiteks rasvu, vaike, kautsukit, tõrva, väävlit, fosforit, joodi. Õhuga moodustab benseen plahvatava segu. Benseen on suure reageerimisvõimega ühend: reageerib hõlpsasti elektrofiilsete reagentidega, näiteks halogeenide ning kontsertreeritud väävel-ja lämmastikhappega, andes asendussaadusi näiteks nitrobenseeni.
docstxt/135334929134.txt
Laiskus ja aktiivsus Austatud kuulajad, iga inimene on oma elu jooksul kogenud eluetappe kus avaldub nii tema laiskus kui ka aktiivsus. Meie seas leidub mõlema iseloomujoone omajaid. Kuid mis on laiskuse ning aktiivsuse negatiivsed ja positiivsed küljed. Laisavõitu inimestel kipuvad kohustused üle pea kuhjuma, kuna nad põikavad nendest kohe kõrvale. Tõenäoliselt ei saavuta laisad isiksused elus kunagi edu ja laiskus võib olla see, mis neid tagasi hoiab. Inimesed ei saa nende abile loota, kuna tõenäoliselt ei püsi neil midagi meeles. Sa pead olema aktiivne ja kinni haarama kõikidest võimalustest, mida elu sulle pakub. Nõnda tagad selle, et ei lase ühelgi suurepärasel võimalusel oma elus raisku minna ning inimesed hakkavad märkama milline kaunis isiksus sa oled. Paljudele meeldib vaadata, kui keegi teine püüdleb enda unistuste poole, saavutades selle mille üle ta on uhke. Aktiivse inimesena tulevad pal...
TTÜ EESTI MEREAKADEEMIA Metallide tehnoloogia, materjalid I Kodutöö nr: 4 Teema: Materjalide struktuur ja omadused. Metallide margivastavus. Variant: 4 Üliõpilane: Valery Fedorishchev Õppejõud: A. Lill Tallinn 2017 1. Materjalide struktuur ja omadused Рис.1 – изображена кристаллическая решетка и объемная модель натрия (Na) Атомная масса: 22,98976928(2) а. е. м. (г/моль) Радиус атома: 190 пм Структура решетки: кубическая объёмно-центрированная Параметры решетки: 4,2820 Å Рис
.......... Tallinn 2018 SISUKORD 1.Sissejuhatus..............................................................................................................................3 2.Leidumine looduses.................................................................................................................4 3.Omadused.................................................................................................................................5 Füüsikalised omadused...........................................................................................................5 Keemilised omadused.............................................................................................................5 4.Kasutamine...............................................................................................................................6 5.Füsioloogiline toime............................................................................................
Tombaught Arizonas Lowelli observatooriumis väga hoolika taevavaatluse ja leidis pluuto . Nimi ''Pluuto'' Pluuto sai oma nime Rooma Mütoloogia allmaailma jumala Pluuto (Kreeka: Hades) järgi. Planeedile omistati see nimi (pärast paljusid teisi soovitusi) võib-olla sellepärast, et ta on nii kaugel Päikesest, et ta on pidevas pimeduses ja võib-olla sellepärast, et "PL" on initsiaalid Percival Lowell-st. PLUUTO OMADUSED Kaugeim planeet päikesest. Pluuto on väikseim seitsmest päikesesüsteemi kuust (Kuu, Io, Europa,Titan ,Triton, Callisten, Canymedes). Diameeter on 2274 km. Orbiit on 5913520000 km. päikesest Pinnatemperatuur on Pluutol -235*C ja -210*C vahel. Päikesevalgus ei ulatu temani ning sellepärast on seal pime. Koosneb kivi ja jää segust. Kuid Pluuto keemiline koostis on teadmata. Pluuto on kõige kaugemal ja kõige väiksem planeet.
Leia vastused: a)Millised atmosfäärinähtused kujunevad troposfääris? b)Mismoodi on inimese elutegevus seotud stratosfääriga? c)Nimeta atmosfääri nähtusi, mis tekib kõrgemates õhukihtides, kuid aegajalt on maa pealt jälgitavad: d)miks troposfääri ülemistes kihtides on õhutemperatuur madalam kui maa peal, kuidi ollakse Päikesele lähemal? 2.ÕHU KOOSTIS , OMADUSED ja NÄHTUSED Lämmastik (N) 78,8 %) ÕHUTEMPERATUUR VIRMALISED Hapnik (0) 20,9% Õhu soojenemine ja jahtumine, temp. Argoon ja väärisgaasid 0,93% langeb 6-8° km kohta ÄIKE Süsihappegaas (CO2) 0,03% ÕHUNIISKUS SADEMED(vihm,rahe,lörts, lumi) Veeaur (H2O) 0,01-0,02 g liitris Küllastunud õhk
Väävel Kätlin Viilukas Sisukord Omadused Allotroobid Sulfiidid Sulfaadid Kasutusalad Väävel looduses Happevihmad Lõpp Omadused Mittemetall Elektrit mitte juhtiv Keemiline valem S8 4 stabiilset isotoopi Palju allotroopseid vorme Madala sulamistemperatuuriga Kollane (rohekas punakas), rabe, Lahustub mitmetes orgaanilistes ainetes Keemiliselt aktiivne metall Allotroobid Rombiline väävel (a) Peenepulpriline väävliõis S8 rombikujulistest molekulidest. Monokliinne väävel (b) Peenete nõeljate kristallidega allotroop, mis on saadud sulatatud
Essee Kes on ellujääjad. Hetke majandusliku olukorda vaadates, tekib aegajalt ikka küsimu, et kes on need inimesed kes suudavad toime tulla ja vaatamata kõigile raskustele, sellest olukorrast võitjana välja tulla. Kui suur tähtsus isiksuse omadustel selles on? Oma pooleteist aastase psühholoogia õpingu jooksul olen teada saanud, et isiksuse tuuma moodustavad, Costa ja McCrae suur viisik ehk viis joont: neurotism, ekstravertsus, meelekindlus, avatus ja sotsiaalsus. Kõige rohkem on neist tähelepanu pööratud neurotismile, kuna kõrge neurootilisusega inimestel on kalduvus käituda emotsionaalselt. Neurootilisuse tuum on kalduvus kogeda mitmesuguseid negatiivseid emotsioone, mistõttu neurootilistel inimestel on raske kontrollida oma impulsse ja toime tulla stressiga. (Costa, McCrae 1992). Stressiga mitte toimetulemine juba näitab, et hetkel raske majanduslik olukord võib kõrgema neurootilisusega inimestele tunduda ületamatu. Olukorda negati...
Alkaanid on niisugused süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega. Mõnikord nimetatakse alkaane ka parafiinideks. · Metaani ja temaga sarnaste süsivesinike - alkaanide omadused muutuvad korrapäraselt süsiniku aatomite arvu suurenemisega molekulis. · Metaan ja temale järgnevad alkaanid erinevad üksteisest aatomite rühma - CH2 - võrra. Niisugust ühendite rida nimetatakse homoloogiliseks reaks. Rea üldvalem on CnH2n + 2 · Metaani homoloogilise rea 4 esimest ühendit on gaasid, viiendast kuni kuueteistkümnendani vedelikud ja kõrgemad on tahked ained. Molekulmassi
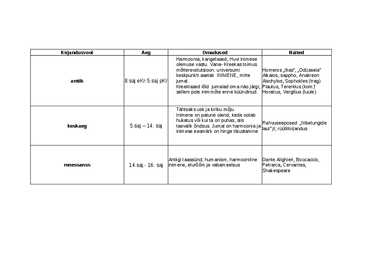
Kirjandusvool Aeg Omadused Näited Harmoonia, kangelased, Huvi inimese olemuse vastu. Vana- Kreekas toimus mõtterevolutsioon: universumi Homeros ,,Ilias", ,,Odüsseia" keskpunkti asetati INIMENE, mitte Alkaios, sappho, Anakreon antiik 8.saj eKr-5.saj pKr jumal
Elu on mateeria osa, mis suudab end ise kasvatada ja paljundada. Tunnused: sisekeskkonna stabiilsus, rakuline ehitus, aine- ja energia vahetus ja paljunemine. Eluslooduse organiseerituse tasemed: …Tase Bioloogia haru Elualad Molekul Molekulaarbioloogia Toiduainetööstus, materjaliteadus. Rakuline tase Tsütoloogia ehk rakubioloogia Taimekasvataja, kunstlik viljastamine Kude Histoloogia Ilukirurg, karusnahatööstus, lihunik, puidutööstus Elundkond Kardioloogia, nefroloogia Organism Anatoomia,...
Füüsika 9. klassile Elekter ja elektriväli Staatiline elekter Staatiline elekter tekib, kui kahte keha omavahel hõõruda. Hõõrumise tagajärjel saavad kehad laengu. Laengud Samaliigilised laengud tõukuvad, eriliigilised tõmbuvad: + ja + tõukuvad (pluss ja pluss) -Ja tõukuvad (miinus ja miinus) + ja - tõmbuvad (pluss ja miinus) Elektrijõud sõltub: · Laengu suurustest · Kehade kaugusest · Keha massist Elektroskoop seade, millega laengu olemasolu kindlaks teha. Millised ained ja kehad on head elektrijuhid, millised mitte? Juhid Mittejuhid Metall Klaas Vesi Plastik Inimkeha Puit (kuiv) Kumm Paber Destilleeritu...
üldist Raud on levikult maakoores neljas element, metallidest teisel kohal alumiiniumi järel Puhas raud on suhteliselt pehme metall, mis on küllaltki püsiv õhu ja vee toime suhtes. Raua põhilised oksüdatsiooniastmed ühendites on II ja III. Raud(II)ühendid ei ole enamasti kuigi püsivad, vaid oksüdeeruvad kergesti raud(III)ühenditeks Looduslik vesi võib sisaldada raud(II)vesinikkarbonaati Raua füüsikalised ja keemilised omadused Hõbevalge keskmise kõvadusega metall Raua tihedus 7874 kg/m3 Sulamistemperatuur 1538°C Plastiline Hea soojus ja elektrijuht Magnetiseeritav Kristallvõre muutub erinevatel temperatuuridel Looduses leiduvad rauamaagid Hematiit ehk punane rauamaak Fe2O3 Magnetiit ehk must rauamaak Fe3O4 Püriit FeS2 Pruun rauamaak Fe2O3 * m H2O raudpagu ehk sideriit FeCO2 tähtsaimad rauasulamid Teras süsinikku (kuni 2%)
(koobaltsinine, kinaverpunane), rahvapärased nimetused tulenevad sarnasusest (tinahall, salatiroheline). Enamikus maailma keeltes ongi kõige vanemad sõnad must, valge ja punane. algul tähistas valge kõiki heledaid ja sooje värve, must aga tumedaid ja külmi. Siis alles tekkisid punast värvi tähistavad sõnad ja ülejäänud värvinimetused. Värvide puhul saab rääkida nii objektiivsetest omadustest kui ka subjektiivsetest omadustest: · Objektiivsed omadused on värvitoon; värvisus ehk kromaatilisus; värvi küllasus ehk eredus ja tuhmus; heledus ja tumedus ning akromaatilisus. Värvide teisi omadusi tajuvad inimesed erinevalt, seega on värvide soojus ja külmus; kergus ja raskus; lähedus ja kaugus ning värvide aktiivsus subjektiivsed omadused. Valguse spekter sisaldab lõpmata palju värve, ainult inimese silma eristusvõime on piiratud. Inimene eristab spektris umbes 130-140 tooni
Terase legeerivad elemendid – kroom, koobalt ja vanaadium ning nende omadused ja kasutusalad Terase sulameile lisatakse erinevaid elemente ehk terasega legeerivaid aineid, et teras saavutaks vajalikud omadused. Enim levinud legeerivaid elemente, mida terase sulameis kasutatakse, on kokku umbes kümmekond. Alljärgnevalt on välja toodud kolme –kroomi, koobalti ja vanaadiumi omadused ja legeermise saadused. Kroom on kõva valge läikiv metall, mille leiab Mendelejevi tabelis 24. kohalt. Tavalisel toatemperatuuril on kroom üsna vastupidav õhu ja vee suhtes. Kroomi sulamistemperatuur on 1800˚ C ning erikaal 7,14. Kroom lahustub lahjendatud väävel- ja soolhappes, eraldades vesinikku. Külmas lämmastikhappes aga kroom ei lahustu ja muutub lämmastikhappega töötlemisel passiivseks nagu alumiiniumgi
TELESKOOP Nimi Klass Koht aasta Sisukord Sissejuhatus ....................................................................................................................... 3 Teleskoopide tüübid ......................................................................................................... 3 Teleskoope iseloomustavad omadused ........................................................................... 4 Fookused ........................................................................................................................... 4 Suured ja väikesed teleskoobid ....................................................................................... 5 Järgmise põlvkonna kosmoseteleskoop .......................................................................... 6 Kokkuvõte ...........................
Sisukord...................................................................................................................................... 2 Sissejuhatus.................................................................................................................................3 Saamismeetodid.......................................................................................................................... 4 Füüsikalised omadused............................................................................................................... 5 Keemilised omadused................................................................................................................. 6 Kasutusalad.................................................................................................................................9 Ohutusnõuded..............................................................................................
Raud Raud (ferrum) on keemiline element järjenumbriga 26. Raud asub perioodilisussüsteemi VIII B rühmas ja 4. perioodis. Tal on neli stabiilset isotoopi massiarvudega 54,56,57 ja 58. Omaduselt on raud metall. Raud on kõige levinum element Maa koostises ning levimuselt maakoores metallidest alumiiniumi järel teisel kohal. Raua füüsikalised omadused Raud on hõbevalge keskmise kõvadusega metall. Lisandid muudavad raua kõvemaks. Raua tihedus on 7874kg/m3 Raua sulamistemperatuu on 1535 kraadi. Raud muutub kuumutamisel palstiliseks, milletõttu seda on võimalik sepitseda ja valtsida. Ta on hea soojus- ja elektrijuht. Raud on magnetiseeritav. Raua keemilised omadused Raud on keemiliselt keskmise aktiivsusega metall. Raua kristallvõre muutub erinevatel tempareatuuridel. Kuivas õhus ta
Okasnahksed Palade PK nimi . Klass 03.05.2012 Okasnahksed Meritähed Merisiilikud Meripurad MERITÄHED · Okasnahksete hõimkond. · Viiekiireline ( enamasti) . · Esineb arvukalt Lääne- ja Põhjamere rannikul. ISELOOMULIKUD OMADUSED · Keskkettaga lame keha. · Suuava paikneb keha alapoolel . · Pärak ülapoolel, veidike külje peal . · Lubiplaatidest koosnev lubiskelett säilitab meretähe kuju ja vormi . · Väikesed tangikujulised haarlad . · Hiljusejalakesed . · Paapulid. TOITUMINE · Püüavad erandatult saaki. · Sõeluvad veest toitaineid. · Keemilised signaalid. · Spetsialiseerunud liistaklõpuseste püügile. · Tulevad toime tugevasti sulgunud kodadega.
KTkarbonüülühendidaldehüüdid ja ketoonid,karboksüülhapped ja aminohapped,nende valemite koostamine,nimetuste andmine,füüsikalised ja keemilised omadused(võrrandid),metanaali,etanaali,metaanhappe ja etaanhappe omadused ja kasutamine. Karbonüülühendid: ühendid, mis sisaldavad karbonüülrühma. Aldehüüdid: ühendid, mis sisaldavad karbonüülrühma ja aldehüüdrühma. Ketoonid: ühendid, mis sisaldavad karbonüülrühma ja ketorühma. (Füüsikalisised omadused: kergesti lenduvad vedelikud,vees lahustuvad hästi, narkootilise toimega, kesknärvisüsteem) Metanaal: HCHO (gaasilises olekus, lahustub vees ja mürgine )( desifintseerimisvahend, anatoomilised preparaadid, vaikude tootmisel) Etanaal: CH3CHO ( kergesti keev vedelik (21'C) , mürgine, tekib organismis etanooli oksüdeerumisel) (kasutatakse vajalik aine keemiatööstustes) Metaanhape ehk sipelghape
Kahjuliku mõjuga on kolesterool siis, kui tema sisaldus veres ületab 2 g liitri kohta. Kanamuna rikastatakse -3-rasvhapetega. -3-rasvhapetel on tervistav mõju (ennetab südame-veresoonkonna haigusi, vähendab vereliistakute kleepuvust ja trombide tekke ohtu). -3-rasvhapped on keeruka koostisega polüküllastamata rasvhapped (-linoleenhape, mida rohkelt leidub lina- ja rapsiõlis). Rikastamiseks kasutatakse söödale lisatavaid lina-ja rapsiõli. Munade ja linnuliha väga head dieetilised omadused Noorlindude (broilerite) lihakehas on rasva 4...8%, v.a veelinnubroilerid (täiskasvanud nuumatud hanel kuni 40%). Lihakehas olev rasv on umbes 2/3 osas talletatud nahaaluse ja sisemise rasvana, mida on soovi korral kerge lihast eraldada. Linnurasv sisaldab võrreldes teiste loomsete rasvadega palju rohkem küllastamata rasvhappeid. Linnuliha on kõrge valgusisaldusega (kana- ja kalkunibroilerite rinnalihastes kuni 22%).
Aldehüüdid, ketoonid: struktuur, omadused, näited ainetest tööstuses, tarbimises ja elukeskkonnas ALDEHÜÜDID Struktuur: Keemilised ühendid, mis sisaldavad aldehüüdrühma ( -CHO). Aldehüüdide tunnuseks on liide -aal , mis lisatakse tüviühendi nimetusele: CH3CH2CHO- propanaal ● Aldehüüdid kuuluvad karbonüülühendite hulka. Omadused: ● Aldehüüdid moodustuvad alkoholide oksüdeerumisel. ● Oksüdeeruvad kergesti. ● Aldehüüdid ise oksüdeeruvad karboksüülhapeteks. ● Aldehüüdide keemistemperatuurid on tunduvalt madalamad võrreldes alkoholidega, sest aldehüüdis olev hapnik ei suuda vesiniksidemeid moodustada. ● Lühikese ahela korral (metanaal...propanaal) lahustuvad vees. ● Pikem ahel hüdrofoobne- ei lahustu KETOONID Struktuur: Keemilised ühendid, milles karbonüülrühm ( C=O ) on seotud kahe süsiniku aatomiga. Ketoonide tunnuseks on liide ...
Tartu Kutsehariduskeskus Auto- ja masinaremondi osakond MATERJALIÕPETUS Õpimapp Tartu 2015 SISUKORD SISUKORD.......................................................................................................................2 1.MUSTAD JA VÄRVILISED METALLID.....................................................................4 Omadused......................................................................................................................4 Mustad metallid..........................................................................................................4 Sulamid..........................................................................................................................4 Korrosioon.........................................................................................................
3 A Rühma metallid(va Al) on looduses haruldased ja mineraale ei moodusta. Al on keemiliselt aktiivne. Nende pind on kaetud õhukese oksiidi kihiga mis katseb edasise oksüdeerumise eest. 3 A Rühma metallide omadused : Hallika värvusega, kerged, plastilised, peegeldavad hästi, head soojus ja elektrijuhid. Alumiiniumi eelised : Kerge, Vastupidav õhule ja veele, hea soojus ja elektrijuht, madal hind. Kasutatakse(foolium, peeglid, autoosad,elektrijuhtmed) Alumiiniumi puudused : Pehme, Aktiivne hapete suhtes, vähe vastupidav. Aluminotermia on reaktsioon kus Al reageerib temast vähem aktiivse metalli oksiidiga. Duralumiinium : Kerge, tugev, korrosiooni kindel.
VESINIKU ISOTOOBID · Põhiline vesiniku isotoop looduses on vesinik e. Prootium · Prootiumi massiarv on 1 · Aatomituum koosneb vaid ühest prootonist · Teine leviv raske vesinik looduses on deuteerium. · Massiarv on 2 · Aatomituumas on ka üks neutron · Vett, mille koostisesse kuulub deuteerium nimetatakse ,,raskeks veeks" · Tuntakse ka vesiniku radioaktiivset isotoopi massiarvuga 3, see on üliraske vesinik ehk triitium. VESINIKU KEEMILISED OMADUSED · Vesinik on tavatingimustes küllaltki keemiliselt väheaktiivne. · Vesiniku väikeste aatomite tõttu on nende vaheline kovalentne side tugevam kui üheski teises üksiksidemega molekulis. · Kuumutamisel muutub vesinik oluliselt aktiivsemaks, käitudes peamiselt üsna tugeva redutseerijana. VESINIK KUI REDUTSEERIJA · Kuumutamisel käitub vesinik redutseerijana aktiivsemate mittemetallide ja paljude ühendite suhtes. · Nendes ühendites on vesiniku oksüdatsiooniaste l
TEEMANT iga süsinik seotud nelja naabersüsinikuga elektrit ei juhi kõrge sulamistemperatuuriga väga kõva (klaasinoad, puuriotsad) hea peegeldumisvõime (ehete valmistamine: briljandid) GRAFIIT iga süsinik seotud kolme naabersüsinikuga; kihiline (pliiatsisüdamikud) kõrge sulamistemperatuuriga (sulatustiiglite valmistamine) metalse läikega, pehme (määrdeainete valmistamine) juhib elektrit (elektroodid) Füüsikalised omadused Süsinik moodustab mitmeid lihtaineid, mis erinevad üksteisest oamduste poolest. Tuntumad süsiniku allotroobid on teemant ja grafiit. Omadus Teemant Grafiit Värvus värvuseta tumehall Kõvadus väga kõva väga pehme Tihedus 3,5 g/ 2,25 g/ Teemant Sulamistemperatuur Sulamistemperatuur C (muutub (aurustub) grafiidiks)
Analüütlise keemia laboratoorse töö protokoll Mona- Theresa Võlma praktikum IV B-1 102074 Töö 8 : Lahuste kolligatiivsed omadused Katse 1: Suhkru molaarmassi määramine krüoskoopilisel meetodil Töö eesmärk : Reaktiivid: C12H22O11 ; H2O Töö käik: 100cm3 kuiva katseklaasi pipteerida 50 cm3 destilleeritud vett ja asetada 300 cm3 keeduklaasis olevasse lumest ja NaCl segust valmistatud klahusesse (100:5). Märkida vee temperatuur momendil, mil tekivad esimesed jääkristallid. Vee külmumistemperatuur mõõta termomeetriga 0,1oC täpsusega. Allajahtumisevältimiseks tuleb katse ajal vett klaaspulgaga segada
Soolad Fe(HCO3)2 raud(II)vesinikkarbonaat, leidub looduslikes vetes, muudab katlakivi pruunikaks. FeSO4*7H2O raudvitriol (raud(III)sulfaat-vesi) - kasutatakse taimekaitsevahendina seenhaiguste tõrjeks - kasutatakse peitsina riide värvimisel - kasututakse keeduvärvide valmisstamisel FeCl3 raud(III)kloriid on punakaspruun väga hügroskoopne aine. Kasutatakse metallide söövitamisel. Raua keemilised omadused Puhas raud on must, pehme, keemiliselt väheaktiivne metall. Lisandeid sisaldav raud roostetab niiskes õhus kiiresti. 4Fe+2O2 + nH2O-> 2Fe2O3*nH2O (rauarooste) Kuivas õhus katub raud musta segaoksiidi kihiga(rauatagiga), mis kaitseb rauda edasise oksüdeerumise eest ( näiteks sepistatud raudesemed). 3Fe+2O2 -> Fe3O4 Aktiivse etallina reageerib raud lahjendatud hapetega: Fe+2HCl -> FeCl2 + H2 Raua tootmine
tahke aine 1) kindel kuju, raske muuta 2)kindel ruumala, raske muuta, sest aine osad paiknevad kindlalt kristallvõre tippudes 3)soojusliikumine on osadeliikumine kristallvõre tippudes vedelik 1)kindel ruumala, 2) võtab anuma kuju, kuna on suuteline voolama 3)osad paiknevad korrapäratult 4)tõmbe- ja tõukejõud on väikesed, soojusliikum. seisneb võnkumises ja kohavahetuses 5)tahke keha ruumala on tavaliselt vedeliku omast väiksem gaas 1)puudub kindel kuju ja ruumala 2)võtab anuma kuju ja täidab selle täielikult 3)gaasi osad saavad vabalt liikuda, sirgjooneline liikumine 4)tõmbe- ja tõukejõudu peaaegu polegi, toimub ainult põrkumisel 5)osad paiknevad korrapäratult difusioon- ainete iseenesest segunemine soojusliikumise tõttu. soojuspaisumine- nähtus, kus keha...
Sn e. Tina TinekeKätlin Vöö Iseloomustus Hõbevalge Pehme Hästi taotav venitatav madala sulamistemperatuurig a metall. Füüsikalised omadused on 50. , tina tuumalaeng on 50 ja ümber tuuma tiirleb 50 elektroni. Molaarmass 118,9 g/mol elektronegatiivsus on 1,7 sulamistemperatuur on 2320C ja keemistemperatuur 26870C tihedus on 7,29 g/cm3 Tina sulamid Tinasulamid on metallisulamid, kus tinasisaldus ületab iga teise sulamisse kuuluva elemendi sisalduse, tingimusel, et: muude elementide summaarne sisaldus sulamis on üle 1 % massist
· Rasvad on glütseriini ehk propaantriooli ja kõrgemate karboksüülhapete(rasvhapete) estrid, mille olek toatemperatuuril on tahke. Elusorganismid kasutavad rasvades valdavalt paarisarvu süsinikega (kuni 20) rasvhappeid. Kõrgemate karboksüülhapete estrid, mille olek toatemperatuuril on vedel, on õlid. · Rasvhapped on kas 16 või 18 süsinikulised, ning kas tegemist on õlide või tahkete rasvadega vaadatakse kordseid sidemeid. Kui rasvhappes esineb kordne süsiniksüsinik side, siis on tegemist õliga. · Rasvad on värvuseta, lõhnata, maitseta, vedelad või tahked ained, mis vees ei lahustu. · Rasvade olek sõltub rasvhappe radikaalist s.t. küllastunud radikaali puhul (kõik üksiksidemed) on rasv tahke ja küllastumata radikaali puhul (vähemalt 1 kaksikside) on rasv vedel õli. · Loomsed rasvad on tahked, välja arvatud hülge ja vaalarasv. · Looduslike rasvade vä...
Tartu Kristjan Jaak Petersoni gümnaasium Osmium Referaat Autor: Kirke Fischer 11.b klass Tartu 2018 Sisukord: 1. Osmiumi tutvustus 2. Leidumine looduses 3. Saamine, tootmine 4. Füüsikalised ja keemilised omadused 5. Ühendid 6. Füsioloogiline toime 7. Kokkuvõtte 8. Kasutatud allikad 1. Elemendi tutvustus Osmium (tähis Os) on keemiline element. Osmium asub perioodilisustabelis kuuendas perioodis, kaheksandas rühmas (ehk B rühmas). Osmium avastati 1803.aastal Londonis ja tema avastajateks olid Smithson Tennant ja William Hyde Wollaston. Analüüsides plaattinamaagi töötlemist kuningveega. Nüüd teame, et see oli osmiumi ja iriidiumi sulam, mis ei reageeri
peamiselt lubjase aluspinnaga aladel. Lupja vajavad limused oma kodade arenguks ning seal, kus esineb tigusid, viibivad alati ka neist toituvad jaanimardikate vastsed. Jaanimardikad veedavad päeva varjualuses. Neid on küll lihtne leida piisab vaid kivi ülestõstmisest. Emased väljuvad oma varjupaikadest hämaras. Sageli näeb ühes kohas mitut emast. Kui neid ehmatada, lõpetavad nad helendamise, kui aga ettevaatlikult läheneda, jätkavad helendamist. JAANIMARDIKA ISELOOMULIKUD OMADUSED Emane: Tiivutu. Tema lüliline keha meenutab vastse oma. Helenduselund paikneb tagakeha tipul. Isane: Emasest väiksem. Suurte silmade ja hea nägemisega. Isane on tiibadega ning lennuvõimeline. Kattetiivad kaitsevad kilejaid tiibu ajal, mil putukas ei lenda. Vastsed: Võimsate suistega varustatud röövloomad. Neilgi on tagakeha lõpul helenduselundid. SUURUS Pikkus: Emasel 10-18 mm, isasel 10-13 mm. Välimus: Emasel ja vastsetel on pikk lüliline keha, isastel on tiivad ning nad on
kcal/mol. Nüüdisaegsete vaadete kohaselt paiknevad süsinikuaatomid benseeni molekulis korrapärase tasapinnalise kuusnurgana; igaüks neist on seotud kolme 0´- sidemega, mille telgede vaheline nurk on 120*(kraadi). Kuus hübridiseerumata p-elektroni moodustavad ühise suletud PII-elektroni pilve, mis on võrdeliselt jaotunud kõikide süsinikuaatomite vahel. Seetõttu on kõikidel süsinikuaatomitevahelistel sidemetel ühesugused omadused ning nende kordsus on keskmine. Et benseeni tõelist ehitust väljendavale struktuurvalemile I pole rahuldavat graafilist kuju leitud, kasutas A. Kekule 1865. aastal esitatud valemit II ( sisuliselt ebaõige), milles vahelduvad üksik- ja kaksiksidemed, või kuusnurka, mille sisse on joonistatud ring III Benseen on väga mürgine ning on tunnistatud kesknärvi- ja vereloomesüsteemi mõjutavaks aineks. Pikaajaline kokkupuude benseeniga võib põhjustada/esile
Alkoholid ühendid, mis sisaldavas molekulis hüdroksüülrühma OH (R-OH).Seda tüüpi ühendid on aluselised alkoholid. Alkoholi nimetused tuletatakse süsivesiniku nimetusest,mille molekulis on nii palju süsinikku aatomeid ja lõpu ool abil. füüsikalised omadused värvuseta, omapärane lõhn,põletava maitsega,hea lahustuvus vees, head lahusti omadused,lahustuvad hästi orgaanilisi ühendeid. Füsioloogiline toime Avaldavad inimorganismile tugevat toimet.Alkoholid oksüdeeruvad ensüümide toimel järk järgult, algul aldehüüdideks, siis karboksüülhappeks ning peale mitmeid ainevahetusreaktsioone süsinikdioksiidiks ja veeks. Etanool oksüdeerub etanooliks ja etaanhappeks ja kolesterooli sünteesiks. Kõige suurem mõju on peaajule ja kesknärvissüsteemile.
Lanktanoidid (4f) Aktonoidid (5f) Näited: Zn: 1s22s22p63s23p64s23d10 O: 1s12s22p4 Pt: 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d8 2 2 6 2 6 2 10 6 2 10 6 2 14 Na: 1s22s22p63s1 f-elemendid s-elemendid d-elemendid p-elemendid · Elemendi keemilised omadused määrab ära peamiselt väline elektronkiht. · Perioodilisusseadus keemiliste elementide ja nendest moodustunud lihtainete ning ühendite omadused on perioodilises sõltuvuses elementide aatomite tuumalaengust. · Oksüdatsiooniaste tegelikkuses ei eksisteeri. Temaga iseloomustatakse keemiliste elementide omadusi. O.-a. väärtuste abil koostatakse ühendite valemeid ja redoksreaktsioonide võrrandeid
Leelismetallid on : Liitium, Naatrium, Kaalium, Rubiidium, Tseesium ja Frantsium. Leelismuldmetallid on : Kaltsium, Strontsium, Baarium ja Raadium. Sulamistemperatuur metallidel on väga erinevad sulamis temperatuurid. Madalaima sulamistemperatuuriga metall on elavhõbe (-39ºC). Naatrium sulab 98ºC juures, tina sulamistemperatuur on 232ºC. Zn - 420ºC, Al - 660ºC, Cu - 1085ºC, Fe - 1538ºC, W - 3422ºC. Metallide füüsikalised omadused: · Sarnased: tahked, läikivad, hea soojusjuhtivusega, hea elektrijuhtivusega, enamus on palstilised, hõbehalli värvi (va. Kuld, vask). · Erinevad: sulamistemperatuurid, tihedus, kõvadus (pehmed: plii, kuld, naatrium) · Mustmetallid raud ja tema sulamid, töötlemata olekus kaetud musta oksiidi kihiga. Asend perioodilisussüsteemis: Metallid asuvad perioodide alguses ja rühmade lõpus. Elektronide arv väliskihil: 1-3 põhiliselt. Elektronide loovutamine ja liitmine:
Mittemetallid Mittemetall Leidumine Omadused Tähtsamad ühendid ja kasutamine 1 Vesinik H2 Leidub maakoores Ta on värvitu, lõhnatu Vesi hapniku ja vesiniku tähtsam ühend. hüdrosfääris ja ja maitsetu gaas, Vees on vesiniksidemed. Kasutatakse atmosfääris. väikseima karetikütustes, metallurgias, molekulimassiga keemiatööstustes.
Tallinna Tehnikaülikool 2014/ 2015 õ.a Materjalitehnika instituut Materjaliõpetuse õppetool Praktikumi nr. 1 aruanne aines tehnomaterjalid Üliõpilane: Keiu Simm Rühm: MATB11 Esitatud: 20.10.2014 Töö eesmärk: Praktikumitöö eesmärgiks oli tutvuda põhiliste konstruktsioonimaterjalide mehaaniliste omaduste ja nende määramise meetoditega, sealhulgas tutvuda 1. metallide, plastide, komposiitmaterjalide katsetamisega tõmbele, analüüsida tõmbediagrammi ning määrata selle põhjal tugevus- ja plastsusnäitajad. Võrrelda erinevaid katsetatavaid maeterjale ning määrata võimalik kasutusala; 2. polümeersete omadustega materjalide katsetamisega survele ja võrrelda nende surve- ning tõmbetugevust; 3. metalsete omadustega materjalide kat...
Tallinna Tehnikaülikool 2018 Mehaanika ja tööstustehnika instituut Praktikumi nr. 1 aruanne aines MTX0010 Materjalitehnika Üliõpilane: Rühm: Esitatud: Töö eesmärk: Tutvuda põhiliste konstruktsioonimaterjalide mehaaniliste omaduste ja nende määramise meetoditega. Kasutatud töövahendid: Löökpaindeteim koos katsekehaga. Katsetulemused: Löökpaindeteim: Materjal Teimiku Nurgad Purustustöö Katsetus- Purunemis- soone tüüp KU või KV temperatuur pinna kraad J iseloom C30 U-tüüpi = 150° KU = 158 J 20-22°C Pooleks rebitud löögi = 84° ...
Kordamisküsimused: VÄÄVEL 1.Väävli leidumine looduses, allotroopia (allotroobi nimi, aatomite kuju ja paiknemine, omadused erinevatel temperatuuridel Leidumine: Ehedalt võib väävlit leida maapinna lähedal vulkaanilistes piirkondades. Tuntumatest väävliühenditest leidub looduses kõige enam sulfiide (FeS2 püriit, PbS- galeniit , HgS kinaver jt) ja sulfaate ( CaSO4*2H2O kips jt) Väävel kuulub elemendina ka kivisöe, põlevkivi, nafta ja teiste fosiilsete kütuste koostisse. Väävel on tähtis element ka eluslooduses. Ta on mitme aminohappe ja valkude koostises. Keskmisest
TALLINNA TEHNIKAÜLIKOOL Materjalitehnika instituut Jüri Pirso KÕVASULAMID e. KERMISED Loengukonspekt aines KÕVASULAMID Tallinn 2004 1 EESSÕNA . Käesolev loengukonspekt käsitleb kõvasulamite e. kermiste koostist, valmistamise tehnoloogiat, omadusi ja kasutamist. On toodud nende omadused ja näidatud kuidas materjalide keemilise koostise ja tehnoloogia ning struktuuri muutmisega saab muuta kõvasulamite mehaanilisi (kõvadus, tugevus, purunemissitkus) ja keemilisi (oksüdeerumist, korrodeeruvust hapetes ja korrosioon- erosiooni) omadusi. Eestikeelne kirjandus selles valdkonnas praktiliselt puudub. Mõningast informatsiooni kermiste koostise, tehnoloogia ja omaduste kohta on
pikim järjestikku loetav ahel. peale mitmendat süsinikku kordse sideme korral eesliide di-, tsükloheksatrieen. Kõrvalrühma nimetuse lõpp on peaahelas on kaksikside. Mitme tri- jne.. Näidata ära sidemete -üül. kaksiksideme korral kõigi asukoht. numbrid ja eesliide vastavalt sidemete arvule Keemilised omadused: Keemilised omadused: Iseloomulikud on Hoolimata küllastumatusest on Iseloomulikud on Iseloomulikud on liitumisreaktsioonid iseloomulikud asendusreaktsioonid liitumisreaktsioonid kolmekordsele sidemele. asendusreaktsioonid, mitte halogeenidega. kaksiksidemele H2, HCl, H2O, Esmaseks reaktsiooni saaduseks liitumisreaktsioonid kordsele CH4 + Cl2 CH3Cl + HCl Cl2
METALLID ÕPPEMATERJAL 9. KLASSILE KOOSTAJA: KÜLLI PÄRTELSON © Külli Pärtelson, 2001 SISUKORD 1. METALLID ARGIELUS 2. ÜLDOMADUSED 3. AATOMI EHITUSE ERIPÄRA 4. KEEMILISED OMADUSED 5. KOKKUVÕTE I. METALLID ARGIELUS IGAPÄEVAELUS HEADE OMADUSTE ASENDAMATU TÕTTU MATERJAL KASUTATAKSE VÄGA LAIALDASELT SUHTELISELT HÄSTI TOODETAKSE JUBA TÖÖDELDAVAD 6000 - 7000 AASTAT ALUMIINIUM KÖÖGINÕUD, KONSERVIKARBID ELEKTRIJUHTMED PEEGLID VÄRVID AUTO- JA LENNUKI OSAD RAUD TÖÖRIISTAD
Lahuste pH = 8. Selle seebi kasutamisega on probleeme, ta eemaldab mustust halvasti, sest isegi isegi destilleeritud vees moodustab halvasti vahtu ning lahus on küllaltki aluseline. Kuigi seebid nõrga happe ja tugeva aluse sooladena hüdrolüüsuvad vees, mistõttu seebivesi tundub alati libe ning pH on seitsmest kõrgem, ei soovitaks viimase seebiga pesta villasest ja siidist esemeid ning seda eriti kõrgemal temperatuuril, kus seepide pesevad omadused on paremad. Halva vahutekke ning teistest kõrgema pH põhjuseks võib olla mittetäielikult toimunud seebistamine, mille tulemusena võis segusse jääda reageerimata naatriumhüdroksiidi ning rasva. Tabel 2. Seebi lahuste pH-d Seebi lahus Tindi Fa asia Fa Isekeedet Isekeedetud spa Energi- ud seep seep zing sport õliga kookosrasva
Referaat Koostajad: Juhendaja: Tallinn 2009 1 SISUKORD SISUKORD.................................................................................................................................2 1.Sissejuhatus..............................................................................................................................3 2.Füüsikalis- keemilised omadused............................................................................................ 4 3.Kineetika ja metabolism...........................................................................................................5 4.Käitumine looduses..................................................................................................................7 5.Toksilisus...........................................................................................................................
Lühendid I Sissejuhatus 1,1 Ajalooline areng 1.2 Optilise andmeside põhimõte 1.2.1Optilise andmeside omadused 1.3 Kaablikonstruktsioonide areng 2. Optilised kiud 2.1 Kiu toimis printsiip ehk tööpõhimõte 2.2 Kiudude põhitüübid 2.3 Materjalid ja mehhaanilised omadused 2.4 Optilised omadused 2.4.1 Sumbuvus 2.4.2 Ühe laine kiu dispersioonid 2.4.3 Ebalineaarsed nähtused 2.4.4 laine kiu pii-lainepikkus 2.4.5 Mitme laine kiu ribalaius 2.4.6 Numbriline auk 3. Valguskaablid 3.1 Kaablistruktuurid 3.1.1 Kiud ja nende kaitstavus 3.1.2 Kaabli tuumastruktuurid 3.1.3 Täiteained 3.1.4 Tõmbe- ja tugevduselemendid 3.1.5 Kest 3.2 Kaablite omadused 3.2.1 Mehhaanilised omadused ja temeratuuri piirkonnad 3.2.2 Sise-ja väliskaablite põhierinevused 3.2.3 Sisekaablite omadused 3.2
ALKÜÜNID Küllastumata süsivesinikud, kus süsinike vahel esineb kovalentne kolmikside. Nimetuse lõpp üün Üldvalem CnH2n2 Füüsikalised omadused sarnased alkeenidele. Füüsikalised omadused Homoloogilise rea 3 esimest liiget on gaasid(C 2C4), järgmised vedelikud(C5C17), alates 18ndast süsinikust on alkeenid tahked Süsiniku arvu kasvuga suureneb keemistemperatuur ja väheneb sulamistemperatuur. Sama süsinikuarvuga alkeenidel on võrreldes alkaanidega madalamad sulamis ja keemisto Hüdrofoobsed ained ja seetõttu ei lahustu vees Alkeenid on lõhnavad ühendid, narkootilise toimega Keemilised omadused