Ketamiin Ketamiin (raviminimi Ketalar® või Ketanest®, slänginimetus "K-vitamiin", "K") on narkoosiaine, mida meditsiinis veel praegugi kasutatakse. Süstimislahuseid valmistatakse apteegis ja hoitakse klaaspurkides. Ketamiin tekitab joovet, kuid ta toime ei ole nii tugev kui PCP1. Ketamiini hakati kontrollima pärast seda, kui ELis tekkis 2000. a mure nende uimastite kuritarvitamise tõttu meelelahutuslikel eesmärkidel.(130) ÜRO rahvusvaheline uimastite kontrolli büroo (International Narcotics Control Board, INCB) lisas 2001. a märtsis GHB rahvusvaheliselt reguleeritavate uimastite nimekirja ning seejärel on kõik ELi liikmesriigid ajakohastanud oma vastavaid õigusakte. Hiljuti, 2006. a märtsis, soovitas ÜRO rahvusvaheline uimastite kontrolli büroo Maailma Terviseorganisatsioonil kiirendada oma revisjoni selles kohta, kas ketamiin peaks olema rahvusvahelise kontrolli all ($fn,$fn). Siseriiklikul ...
Orgaanilise keemia algtõed Alkaanid Alkeenid Alküünid Alkoholid Orghapped Üldvalem: CnH2n+2 CnH2n CnH2n2 CnH2n+1OH CnH2n+1COOH CnH2n1OH CnHn+1COOH CnHn+1OH CnH2n3COOH Reegel: Alkaanidel Alkeenidel Alküünidel Alkoholides esi- Orgaanilistes hape- esineb ühen- esineb ühen- esineb ühen- nevad aanide, tes esineb COOH dites ühe- dites kahe- dites kolme- -eenide ja rühm. Võib olla kordne side. kordne side. kordne side. üünide tüved OH ühendis ka OH rühma-ga. rühm. Lõpuliited -aan -een -üün -anool -aat ...
LIIVALAIA GÜMNAASIUM Andero Mardo Klaas Referaat Tallinn 2006 Nii ehitusel kui ka mujal on tähtis läbipaistev klaas. Klaasi lähteaineks on sooda (Na2CO3), kriit või marmor (CaCO3) ja valge kvartsliiv (SiO2). Kui tehakse harilikku pudeliklaasi, pannakse liiv potti, lisatakse soodat ja kriiti ning asetatakse erilisse ahju. Pott peab olema tulekindlast savist, s. o. niisugusest, mis ei sula suurest kuumusest. Kõik kolm ainet - liiv, sooda ja kriit - keevad kuumutamisel kokku. Lõpuks saadakse sulanud klaas, vedel kui vesi. Kuid klaas on ainult pealtnäha veega sarnane. Jahtudes käitub ta hoopis teisiti kui vesi. Kui vett jahutada, jääb ta vedelaks, kuni temperatuur langeb 0 kraadini. Kui kraadiklaas näitab miinuskraade, vesi külmub ja muutub kõvaks jääks. Hoopis teisiti toimub vedela, sulanud klaasiga. Jahtudes tiheneb ta väga pikkamisi. 1200 kraadi juures sarnaneb ta siirupiga, 100...
Aluseline Hüdrok- Hape Sool Vesi Metall Happeline oksiid siid oksiid Aluselin Sool+ vesi Hüdroksiid Sool e oksiid + vesi Hüdrok- Sool+ vesi Hüdroksiid+ LAHUS Sool+ vesi siid sool Hape Sool+ vesi Sool+ vesi Sool+ hape LAHUS Sool+ vesinik Sool Hüdrok Sool+ hape Sool+ sool LAHUS Sool+ metall siid+ sool Vesi Hüdroksiid + LAHUS LAHUS LAHUS Hape vesi...
Korrosioon Mis on korrosioon? - See nimetus tuleneb ladinakeelsest sõnast corrodere, mis tähendab puruks närimist. Korrosioon on redoksprotsess, mille käigus metallide aatomid oksüdeeruvad ja muutuvad ioonideks. Lihtsamalt öelduna on korrosioon metallide hävimine ümbritseva keskkonna toimel. Metalli korrosiooni kiirus sõltub metalli iseloomust, temperatuurist, lahuse koostisest, õhuhapniku juurdevoolust, metallis esinevatest lisanditest jt. Metall mis sisaldab lisandina vähemaktiivseid metalle, korrodeerub kiiremini kui puhas metall. Lisandeid sisaldava metalli korrosioonil jaotuvad oksüdeerumis- ja redutseerumis reaktsioonid erinevate pinnaosade vahel: metall oksüdeerub, vabanenud, elektronide arvel toimub vähem aktiivsel lisandil vesinikioonide ja hapniku redutseerumine. Selline protsesside jaotumine kiirendab korrosiooni. Raud kuulub keskmise akti...
docstxt/12111423782268.txt
Kanep · ÜLDANDMED Kanep ehk Cannabis üks levinumaid narkootikume, mis näiteks Hollandis on legaliseeritud. Kanep jaguneb omakorda marihuaanaks, hashiseks ja vedelaks hashiseks ehk vedelaks kanepiks. Marihuaana on kanepi emastaimede kuivatatud ja peenestatud ladvad ja õisikuosad. Hashis on tavaliselt valmistatud kanepi näärmerakkude vaigutaolisest eritisest käsitsi. Vedel hashis on valmistatud hashise lahustamisel atsetoonis või alkoholis. Marihuaana sisaldab kanepi narkootilist mõjuainet THK-d kõige vähem, 1%- 12%, aga on leitud ka 25% THK-d sisaldavat marihuaanat. Hashis sisaldab THK-d tunduvalt rohkem, umbes 8%-25%. Vedel hashis sisaldab THK-d kuni 60%. · NIMETUSED MARIHUAANA - travka, trava, anasha, smail, rohi, mari HASHIS - plastiliin, afganka, maroko · VÄLIMUS Kanepivaik meenutab väikeseid pruune klombikesi, kanepi lehed, varred ja seemned meenutavad rohekaspr...
galliumi oma käes ", oli õigus. Galliumi tihedus oli tõepoolest 5,84. Lavrentsium(Lr) avastati 1961 a. USA´s, California kiirguslaboris. Lavrentsiumi avastajateks olid Albert Ghiorso, Torbjorn Sikkeland, Almon Larshja Robert M. Latimer. Nad pommitasid kaliforniumi aatomeid booriioonidega. Neil õnnestus saada umbes 2 milligrammi kaliforniumi. Nõukogude teadlased soovitasid lavrentsiumi nim. Inglise teadlase E. Ruthefordi auks raderfordiumiks. Ameerika keemiaühingu liikmed eelistasid lavrentsiumi nimetada California kiirguslabori looja E. O. Lawrence´i järgi. 1817. aastal avastas rootsi keemik A.Arfedson suhteliselt haruldase mineraali pentaliidi analüüsil uue keemilise elemendi. Hiljem avastati see element ka mõnedes mineraalides, mis kuuluvad kõvade kivimite koostisse. Seda elementi nimetati Liitiumiks(Li). See sõna tuletati kreekakeelsest sõnast lithos, Mis tähendab kivi.
Kaltsiumoksiid Kus leidub? Leidub lubjakivis, on kasutatud ka klaasi tootmisel. Kuidas saada? Saadakse tööstuses lubjakivi lagundamisel kõrgel temeperatuuril. Lubjakivi põhikoostisaine CaCO3 laguneb kuumutamisel vastavalt reaktsioonivõrrandile: CaCO3 CaO + CO2 Laboratoorselt valmistatakse kaltsiumoksiidi samuti peamiselt kaltsiumkarbonaadi termilisel lagundamisel. Väikesi koguseid saab valmistada ka kaltsiumi oksüdatsioonil, kaltsiumhüdroksiidi termilisel lagundamisel ja muul teel. Võrrand: Ca + O CaO Valem: CaO Molaarmass: Mr(CaO) = 40 + 16 = 56g/mol Olek: Tahke. Omadused: · Kaltsiumoksiid on sööbiv. · Valge, hallikasvalge, kahvatukollane või kahvatuhall aine. · Kristalne aine. · Lahustub hästi vees. · Ei lendu ning on lõhnatu. · Sulamistemperatuur on 2572 °C. · Keemistemperatuur on 2850 °C. · Kaltsiumoksiid reageerib eksotermiliselt veega, tekib kalt...
Süsivesinikud Ained, mis koosnevad ainult süsinikust ja vesinikust. Süsinik on kõigis orgaanilistes ühendites 4- valentne. H HH HHH H-C-H H-C-C-H H-C-C-C-H H HH HHH Metaan Etaan Propaan Ch4 Ch3-Ch3 Ch2-Ch2-Ch2 Orgaanilistes ainetes veel võib olla lämastikku, hapnikku, halogeene. Elemendi laeng näitab sidemekriipsude arvu. Isomeerid on ained, millel on sama koostis, aga erinev struktuur. Süsivesinikud võivad olla sirge ahelaga, hargnenud või tsüklilised. Tsüklilised ühendid ei ole isomeerid. Ainult üksiksidemetega on alkaanid Etaan Kaksiksidemega on alkeenid Eteen Kolmiksidemega on alküünid Etüün Saamine ja omadused: C-C4 Süsinike arvuga 1-4 (metaan, etaan, propaan, butaan) on gaasid. Ka alkaanid on gaasid. Maagaas, naftagaas C5-C16 on vedelad C17- tahked Tahke ja vedel koos on näiteks nafta puhul. Värvus on mustast helepruunini ja süsinike ar...
Ch4 ehk metaan Lihtsain süsiniku ja vesiniku ühend. Leidub looduses, õhust kergem, ei lahustu vees ning on lõhna- ja maitsetu. Kasutatakse gaasilise kütusena. Segu õhust ja metaanist plahvatab kergesti. Aatomid seotud 4 kovalentse üksiksidemega. C keskel, Hd igas ilmakaares ümber. Metaan on teisisõnu maagaas. Tekib ka orgaanilise aine lagunemisel nt. Prügilates. Metaani põlemine Ch4 + 2 O2 --- Co2 + 2 H2O Mida suurem on oksüdatsiooniastme muutus, seda suurem on kütteväärtus. Selles võrrandis on süsiniku oa muutus 8 ja see on ka maksimaalne. Co ehk süsinik monooksiid ehk vingugaas Mittetäielik põlemine lõpeb vingugaasiga. Süsiniku oksüdatsiooniaste on siin 2. Co saab võimaluse korral oksüdeeruda edasi Co2ks. Co on neutraalne oksiid. Hapete ja alustega ta ei reageeri. Co2 ehk süsinik dioksiid Põlemise lõppsaadus. Võib reageerida veega ja aluseliste oksiidisega. Tekib sool. Co2 ei põle ega toeta põlemist. Co ja Co2 abil saab metallurgi...
.............................................................................................................5 2 Haapsalu Kutsehariduskeskus Viljo Kozlovski Korrosiooni tekke Korrosioon on metallide hävimine ümbritseva kekskkonna toimel. Metallide korrosioon on alati redoksreaktsioon.Keemia jagab korrosiooni siiski protsesside kaudu ja siis on neid kaks: Keemiline ja elektrokeemiline. Keemiline tekib eelkõige kuivade gaasiliste ainete reageerimisel metalliga.Intensiivistub kõrgemal temperatuuril. Metalli aatomid reageerivad aine molekulidega otseselt. Esineb ka mitmesuguste orgaaniliste ainete reageerimisel metallidega kõrgel temperatuuril. Elektrokeemilises kulgeb ka tavatingimustes. Redoksreaktsioon toimub metalli
Sahhariidid e. süsivesikud Koostis: süsinik, vesinik, hapnik. *Veesõbralikud ained. Suhkruteks nimetatakse väikese molekuliga sahhariide, mis on magusad ja lahustuvad hästi vees. Siirupiteks nimetatakse suure kontsentratsiooniga suhkrulahuseid. GLÜKOOS (C6 H12 O6) *leidub paljudes taimedes, eriti viinamarjades. *käärib lahustes väga hästi *tähtis toitaine Kasutamine: 1) lisatakse mõrudele ravimitele, et nende maitset paremaks muuta. FRUKTOOS (C6 H12 O6) *laialt levinud puuviljades *kõige magusam suhkur *käärib ja seedub raskemini kui glükoos SAHHAROOS (C12 H22 O11) *tavaline suhkur *leidub suhkrupeedis ja suhkruroos *laguneb glükoosiks ja fruktoosiks. Laktoos, maltoos. TÄRKLIS (C6 H10 O5)n *valge pulbriline aine *ei lahustu külmas vees, kuumas vees moodustab KLIISTRI. *tärklis annab joodiga reageerides lillakassinise värvuse. *taimede peamine varuaine *tähtis toitaine *laguneb suhkruks TSELLULOOS (C6 H10 O5)n *kiulise ehitusega aine...
Metallid 1.Üldiseloomustus: Kui maailmas on üldse kahte sorti aatomeid, siis metallid on need, mis on oma väliskihi elektrone loovutanud. + nad on plastilised (saab sepistada, valtsida ja traadiks tõmmata) + omavad läiget (peegelduvõime) nt. Kuld, hõbe, vask + kõvadus teemanti skaalal + head elektri- ja soojusjuhid (aines elektrongaasi) + tihedus (kui tihedus on alla 5 g/cm3, on metall kergemetall ja kui tihedus on suuem, siis on tegemist raskemetallidega) + värvus (enamik hõbevalged, raud ja selle sulamid on mustad ning ülejäänud on värvilised) + väärismetallide hind seisneb vastupidavuses, harulduses vms. 2.Metallilisus: Elektronide loovutamise võime. Mida paremini ta seda teeb, seda metallim ta on. Mida kaugemal on elektron tuumast, seda aktiivsem ta on ning metallilisus kasvab. Aatomi raadius on tuuma kaugus viimasest elektronkihist. Rühma number näitas väliskihi elektronide arvu. Perioodi number näitas Arühma metallide e...
Aineklassid Sisukord Aineklassid Oksiidid Happed Alused Soolad Tuntumad ained Millest saab mis? Aineklassid Hape Oksiidid (happeline, aluseline) Sool Alus Oksiidid Oksiid on kahes elemendist koosnev ühend, millest üks on hapnik. Oksiidid jagunevad Happeline oksiid Aluseline oksiid Hapetele vastavaid oksiide Aluseline oksiid on alusele nimetatakse happelisteks (hüdroksiidile) vastav oksiid. oksiidideks. Enamasti on Happelised oksiidid mitte- metallioksiid. Oksiide nimetatakse a)Oksüdatsiooniastme kaudu b)Eesliidete järgi Haped Haped on liitained, mis annavad lahusesse. vesinikioone. Hapete iseloomulikuks on hapu maitse. Hapet...
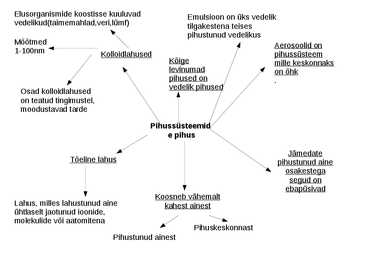
Elusorganismide koostisse kuuluvad Emulsioon on üks vedelik vedelikud(taimemahlad,veri,lümf) tilgakestena teises pihustunud vedelikus Mõõtmed Aerosoolid on 1-100nm Kolloidlahused pihussüsteem Kõige mille keskonnaks levinumad on õhk pihused on . vedelik pihused Osad kolloidlahused on teatud tingimustel, moodustavad tarde Pihussüsteemid e pihus ...
METALLID 1. Füüsikalised omadused · Peaaegu kõik metallid on toatemperatuuril tahked ained, erandiks on elavhõbe (Hg). · Enamik metalle on hallika värvitooniga (erand on punakasroosa vask ning kollane kuld). Metallid peegeldavad tavaliselt hästi valgust neile on omane metalne läige. · Metallid on head soojusjuhid ja elektrijuhid. · Enamik metalle on suhteliselt plastilised, hästi sepistatavad. 2. Metallilised elemendid ja perioodilisuse süsteem Enamik elemente on metallilised. Nad asuvad nii A- kui ka B-rühmades. Kõik perioodid peale esimese algavad metallilise elemendiga ja lõppevad mittemetallilisega. A-rühma number võrdub elemendi aatomi väliskihi elektronide arvuga, B-rühma elementidel on enamasti väliskihil 2 elektroni (erandiks on näiteks ühe elektroniga vask, hõbe ja kuld). Niisiis on metalliliste elementidel aatomitel tavaliselt väliskihil võrdlem...
Muidugi ka kõiksugused mud ehted, mis sisaldavad nikklit võivad tekitada allergilist reaktsiooni. Nikkel ja nikliühendid põhjustavad soodustavad vähi teket inimese organismis. Peamiselt kopsuvähki nendel, kes tegelevad nikli maagi kaevandamisega ja töötlemisega. Kokkuvõttes on melhior vase ( Cu ) ja nikkli ( Ni ) sulam. Melhior võib veel sisaldada muid keemilisi elemente. Melhiorit kasutatakse erinevata ehete, mööblitarbeid, peenraha, jne. MELHIOR Keemia referaat koostas: Kaja Tiidema kool:Gustav Adolfi Gümnaasium klass: 9b õpetaja: Aino Abiline 18.10.2007
1. Hapete definitsioon happed on ained, mis annavad lahusesse vesinikioone(H+). Happed koosnevad vesinikioonidest ja happeanioonidest. Happeaniooni laeng võrdub vesiniku aatomite arvuga happemolekulis. 2. Hapete valemid ja nimetused, happeanioonide valemid ja nimetused HF vesinikfluoriidhape, F - HCL vesinikkloriidhape(soolhape), Cl - kloriidioon HBr vesinikbromiidhape, Br - bromiidioon HI jodiidhape,I - jodiidioon HNO2 lämmastikkushape,NO2 - nime ei tea HNO3 lämmastikhape,NO3 - nitraatioon H2S divesiniksulfiidhape,S2 - sulfiidioon H2SO3 väävlishpe,SO32 - sulfitioon H2SO4 väävelhape,SO42 - sulfaatioon H2CO3 süsihape,CO32 - karbonaatioon H4SiO4 ortoränihape, SiO44 - silikaatioon H3PO4 fosforhape,PO43 - fosfaatioon HMnO4 permangaanhape,MnO4 Veel anioone - OH - hüdrooksiidioon , HCO3 - vesinikkarbonaatioon 3. Hapete liigitus Tugevad, keskmise tugevusega, nõrgad. 4. Happelised oksiidid ja neile vastavad happed Happ...
1. Nim 2 võimalust kuidas saab muuta küllastamata lahus küllastunud lahuseks? Lisada rohkem ainet lahusesse 2. Nim 2 võimalust kuidas saab muuta küllastunud lahus küllastamata lahuseks?Lisada lahustit näitkeks vett. 3. Millest ja Kuidas sõltub gaaside lahustuvus vees? 4. Nim 2 võimalust Kuidas saab suurendada süsinikdioksiidi lahustuvust vees? 5. Lahus- Ühtlane segu, koosneb lahustist ja lahustunud ainest 6. Lahustuvus- Suurim aine kogus, mis võib lahustuda kindlas lahusti (või lahuse) koguses kindlal temperatuuril 7. Tõeline lahus- lahus, milles lahustunud aine on ühtlaselt jaotunud ioonide, molekulide või aatomitena 8. Koloid lahus- Pihussüsteem, milles pihustunud aine osakeste mõõtmed on 10-7 - 10-5 cm (1-100nm) 9. Suspensioon- pihussüsteem, milles tahke aine on pihustunud vedelikus 10. Emulsioon- pihussüsteem, milles üks vedelik on pihustunud teises 11. Kirjelda ioonilise aine lahustvusprotsessi vees .Vee molekulid av...
Rakvere kool 9. klass Alumiinium Referaat Koostaja: Mihkel Juhendaja: õpetaja Õppeaasta 2004/2005 Avastamise lugu 1808. a. kinnitas Sir Humphry Davy alumiiniumi olemasolu ja nimetas selle. Algul eraldati metalli keemilisest ühendist halli pulbrina, mis peenestamisel omandas metallilise läike. Katsed saada metalli kangina või suurte teradena jäid tulemusteta. Enne kui neid katseid kroonis 1845.a. edu, kulus 18 aastat püsivaid otsinguid. Väliselt oli ta sarnane hõbedaga, kuid erinevalt viimasest erakordselt kerge, 4 korda kergem hõbedast, 3,5 korda kergem vasest ja peaaegu 5 korda kergem rauast. Kuna uue metalli saamise lähtaineks olid ammu tuntud maarjased (ladina keeles alumen ), siis hakati ka metalli nimetama alumiiniumiks. Alumiinium Alumiinium on tänapäeval üks tuntumaid ja enamkasutatavaid metalle(tähtsuselt teisel kohal raua järel...
Süsinik Lihtaine: valemiga C Tuleb tast alati 4 keemilist sidet. Näiteks: teemant, grafiit, süsi (antratsiit, kivisüsi, põlevkivi, puusüsi), karbüünid, fullereenid See on süsiniku allotroopia! (Sama element esieb mitme erineva lihtainena) Liitainetes: Co2 süsihappegaas Co vingugaas H2O + Co2 --- H2Co3 süsihape Ca(HCo3)2 vee karedus CaCo3 erinevad karbonaadid Näiteks: marmor, katlakivi, paekivi, kriit Kõik orgaanilsed ühendid on süsinikuühendid!!! C + O2 --- Co2 Redutseerijaks süsinik C ja Co redutseerivaid omadusi kasutatakse metallurgias metallide tootmiseks.
(elavhõbedaauru lambid) laboriaparatuuris, elektroodides, patareides ja kosmeetikas. Elavhõbedat kasutatakse veel kulla eraldamiseks kivimitest ja elavhõbe(II)fulminadi (paukelavhõbeda) tootmiseks, mida tarvitatakse mäeasjanduses lõhkamistöödel. Tänapäeval vajatakse elavhõbedat kõige rohkem elektrivoolualaldite ja kvartslampide valmistamiseks. Viimaseid kasutatakse meditsiinis bakterite hävitamiseks. Metallilist elavhõbedat ja anorgaanilisi ühendeid kasutatakse keemia- ja metallitööstuses, elektrivarustuse tootmisel (lülitid, halogeenlambid, patareid), farmaatsiatööstuses (diureetikumid, kõhulahtistid, silmatilgad, ninatilgad, nahasalvid ja vaktsiinid), meditsiinis (termomeetrid, baromeetrid, desinfektsioonivahendid), hambaravis (amalgaamplommides on 50% elavhõbedat), värvides ja värvainetes. Anorgaanilisi elavhõbeda ühendeid kasutatakse puidutööstuses hallituse tõrjeks.
meelekohtade ja otsaesise piirkonnas, tihti peavõru kujuline, peapööritus. Oksendamine (tihti korduv), meelemärkuse kaotus. Raskendatud hingamine. Ravi: 100% hapniku hingamine rõhu all üksnes akende avamisest ei piisa. Kasutatud kirjandus INTERNET http://lepo.it.da.ut.ee/~pedaste/tubakas/vingugaas.html http://www.advent.ee/tervis/?op=pohimote&id=44 http://www.folklore.ee/~renata/myrk/gaasid.html KIRJANDUS Hergi Karik "Keemia koduõpetaja" Hergi Karik "Üldine keemia" "Ene"
Metallid ja nende kasutamine Essee Metallide kasutamine igapäevaelus sõltub paljuski nende omadustest. Metallid on suhteliselt hästi töödeldavad. Nendest on võimalik venitada traati, valtsida õhukesi lehti, sepistada väga erineva kujuga esemeid. Sulatatud metalle saab valada vajaliku kujuga vormidesse. Metallide heaks omaduseks on ka see, et neid on võimalik kokku keevitada. Metalli valikul tuleb silmas pidada tema keemilist vastupidavust antud tingimustes. Olulised on aga ka metallide füüsikalised omadused: tihedus, sulamistemperatuur, kõvadus jne. Lisaks metalli omadustele tuleb arvestada ka tema kättesaadavust ning hinda. Mida haruldasem on vastav element looduses ning mida keerulisem ja kulukam on metalli tootmine maagist, seda kõrgem on metalli hind. Kergesti sulavaid metalle (näiteks tina ja plii) ei saa kasutada kõrgel temperatuuril töötavate seadmete valmistamiseks. Õnn...
Füüsikaline nähtus Ainetega toimuvad muutused kusjuures ained ise jäävad samaks. Keemiline nähtus Ühtedest ainetest tekivad teised kulgeb keemiline reaktsioon. tunnus värvuse muutus , lõhna teke , sademe teke gaasimullide teeke , soojuse eraldumine ja valguseefekt tingimused kuumutamine , süütamine,valgustamine,elektri läbijuhtimine lahus on ühtlane segu Ainet kus oskaesed om ühtlaselt jaotatud nim- lahustiks aine mis teises ühtlaselt jaotunud nim lahustunud aineks. Lahustuvus näitab suurimat aine kogust mis võib kindlal temperatuuril lahustuda mingis kindlas lahusti koguses Valguse levimise kiirus võrdub teepikkus jagatud ajaga. ( v = s / t ) V=valguse levimise kiirus ( 300 000 km / s) s = teepikkus t = aeg Optiline tugevus võrdub fookuskauguse pöörd väärtusega ( D = 1 / f ) D = optiline kaugus f = fookuskaugus D jagatud 1m = f
Anorgaaniliste ainete põhiklassid 1. Oksiidid Oksiidid on liitained, mis koosnevad kahest elemendist, millest üks on alati hapnik. Metalli oksiidid Mittemetalli oksiidid (aluseline oksiid) (happeline oksiid) ZnO CO2 Fe2O3 SO3 Na2O Eesliited: 2 di; 3 tri; 4 tetra; 5 penta; 6 heksa; 7 hepta; 8 okta; 9 nona; 10 deka SO3 vääveltrioksiid Ag2O dihõbeoksiid Nimetused: IV -II SO2 väävel(IV)oksiid III -II N2O3 lämmastik(III)oksiid Arseen(IV)oksiid IV -II Ar2O4 ArO2 Püsiva oksüdatsiooni astmega metallide oksiididel oksüdatsiooniastet ei märgita. (I-IIIA rühm) CaO kaltsiumoksiid Al2O3 alumiiniumoksiid 2. Happed Happed on liitained, mis koosnevad vesinikioonidest ja happeanioonidest. 1) Liigitus tugevuse järgi; Tugevad happed; HCl vesinikkloriidhape e. soolhape; HBr vesinikbromiidhape; HI vesinikj...
Happed ja soolad Hapeteks nimetatakse liitaineid mille molekul koosneb ühest või mitmest vesiniku ioonist ja happejäägist. Sooladeks nimetatakse liitaineid mille molekul koosneb metallist ja happejäägist. Happe nimetus Happe valem Soola nimetus Näidis VESINIKKLORIIDHAPE -I kloriid CaCl2 (SOOLHAPE) HCl VÄÄVELHAPE -II sulfaat K2SO4 H2SO4 VÄÄVLISHAPE -II sulfit Na2SO3 H2SO3 DIVESINIKSULFIID- -II sulfiid Al2S3 HAPE H2S LÄMMASTIKHAPE -I nitraat KNO3 ...
Kordamine keemia kontrolltööks Kordamine, 9. klass Elemendi järjenumber = elektronide, prootonite arvuga ja tuumalaenguga. Neutronite arv on ümardatud aatommassi ja järjekorranumbri vahe. Elektron kihtide arv = perioodi nr-iga. Kui element asub A rühmas siis on tema elektronide arv viimasel kihil = rühma nr-iga. Reaktsioonivõrrandid Hape H ja happejääk, nt HCl Alus Hüdroksiid, OH lõpuga Mittemetalli oksiid Mittemetall + S+O2, SO2 Metalli oksiid Metall + O2 Sool Ca(NO3)2 ; NaCl ; CaCl2 ; Na2CO3 1. Alus + hape = sool + vesi Nt: NaOH + HCl = NaCl + H2O 2. (mitte)metalli oksiid + hape = sool + vesi Nt: CaO + 2HCl = CaCl2 + H2O 3. Mittemetalli oksiid + metallioksiid = sool Nt. CO2 + CaO = CaCO3 4. metall + hape = sool + vesinikust Nt: Mg + 2HCl = MgCl2 + H2 5. mittemetalli oksiid + vesi = hape Nt: CO2 + H2O = H2CO3 6. Metalli oksiid + vesi = hüdrooksiid Nt: Na2O + H2O = 2NaOH Happed ...
Gmo-miks on see hea? Geneetiliselt muundatud organism ehk GMO on elusolend (bakter, taim, loom), kelle pärilikkuse ainet on geenitehnoloogilisi võtteid kasutades kunstlikult muudetud. Võrreldes tavapäraste sordi- ja tõuaretusmeetoditega on geneetilise muundamise suureks erinevuseks võimalus kombineerida väga kaugete liikide geene (nt. siirdada geene kalalt tomatitaimele) või sisestada organismi tehisgeene. Muundamisel on tegu looduse poolt seatud liigipiiride ületamisega. Geenitehnoloogiline põllumajandus on kõige mahedam, st kõige vähem keskkonda ja meie toitu saastavaid kemikaale kasutav põllumajandus. Seega on geenitehnoloogiline toit puhtam kui see, mida me hetkel sööme. Tänu sellele püsiks meie nähtud vaev hoida loodust puhtana ka edasi. Geenitehnoloogia võimaldab meie toitu muuta senisest täisväärtuslikumaks, seda nt vajalike vitamiinide biosünteesi, mikroelementide akumula...
Järgnevalt on toodud lühiülevaade sellest, milliseid aineid võib sisaldada pesupulber ja millised on neist ohtlikud. Pesupulbrite koostisosadeks on pindaktiivsed ained, polüfosfaadid, perboraadid, persulfaadid, pleegitusained, lõhnaained, jms. Pindaktiivsed ained: puhastus-vahendites ja pesupulbrites leidub peamiselt anioonsed, vähem ka neutraalsed pindaktiivsed ained. Sünteetiliste pesuainete leviku tõttu 1940 aastatel hakkas vahutama jõgede ja järvede vesi, milledesse juhiti linnade heitveed. See oli tingitud sellest, et sünteetilised pindaktiivsed ained ei lagunenud looduskeskkonnas. Alates 1960. aastatest nõutakse enamikes maailma riikides, et sünteetilised pesuvahendid peavad põhiliselt koosnema bioloogiliselt lagunevatest ainetest - see hoiab ära kahjulike ühendite kuhjumise keskkonnas. Fosfaadid: Tavalised pesupulbrid sisaldavad fosfaate kuni 5%, ümberarvestatud fosforile. Fosfaate lisatakse pesuainetele vee pehmendamise eesm...
Alkoholid H H H H H-C-H H-C-OH H-C-C-OH H H H H metaan metanool etanool Alkoholid sisaldavad O ja H ühendit! Ei tohi sisaldada kaksiksidet. Alkaan Radikaal Alkohol R-OH CnH2n+2 CnH2n+1 CnH2n+1OH n= 1 Ch4 Ch3 Ch3OH n=2 C2H6 C2H5 C2H5OH n=3 C3H8 C3H7 C3H7OH jne Radikaali iseloomustab poolik side (võib tekkida pürolüüsi käigus), seal on 1 vesiniku võrra vähem kui alkaanis. Kui aga radikaalile lisada OH saab alkoholi. Alkaanide oksüdeerumisel on võimalik saada vastavaid alkohole. Alkoholid ise oksüdeeruvad ise ka edasi. Pohmelli põhjus on alkoholi oksüdatsiooniproduktid, mis ladestuvad organismi. 2 süsinikuga aldehüüdi mürgistus ongi pohm. Pohm lõppeb .... Alkohol i...
Pesemisvahendid 1 Sisukord Tiitelleht.................................................................................................lk 1 Sisukord.................................................................................................lk 2 Seep........................................................................................................lk 3 Pildid......................................................................................................lk 5 Kasutatud materjal.................................................................................lk 6 2 Seep Milleks on meil vaja pesemisvahendeid? Pesemisvahendite ülesandeks on aidata meil lahti saada mustusest. Paljud loomariigi esindajadki pesevad ennast, näiteks kass, kes teeb s...
Kaltsiumoksiid Lubjakivist saab põletada lupja. Kõrgel temperatuuril kaltsiumkarbonaat laguneb ja süsihappegaas lendub. Järele jääb põletatud(kustutatud) lubi kaltsiumoksiid. Kasutavad ehitajad ning põllumehed.Mullas vähendab põletatud lubi selle happesust. Kaltsiumoksiidi toodetakse tööstuses tavaliselt lubjakivi või muude kaltsiumkarbonaati sisaldavate ainete termilise lagundamise teel. Kaltsiumoksiidi on kasutatud ka klaasi tootmisel. Kaltsiumoksiidi saadakse : Ca+O2=CaO Keemiline valem on CaO. Molaarmass 56,08 g/mol Normaaltingimustel tahke .Värvuselt valge, hallikasvalge, kahvatukollane või kahvatuhall aine Tööstuslikult toodetud kaltsiumoksiidil on rauasisalduse tõttu kollakas või pruunikas varjund.Kaltsiumoksiid on kristalne aine. Sulamistemperatuur on 2572 °C.Keemistemperatuur on 2850 °C. Normaalsel temperatuuril ja rõhul on kaltsiumoksiid keemiliselt stabiilne. Kaltsiumoksiid on sööbiv. ...
Karboksüülhapped Karboksüülrühma kuuluv hape. Nimi konstrueeritakse vastavalt süsinike arvule. Happed reageerivad (ka. karboksüülid): 1) alustega 2) metallidega 3) metallioksiididega 4) nõrgema happe (aluselise) soolaga HCOOH- sipelghape (metaanhape) CH3COOH- äädikhape (etaanhape) CH3CHOHCOOH- piimhape HOOC-COOH- oblikhape (etaandihape) Karboksüülrühmas on kõigil C, kahe sidemega O ja ühe sidemega OH HCl vees on H+Cl Vesinikioon on happelisuse kandja. Ainete omaduseld sõltuvad sellest, millest nad koosnevad:D HCl+NaOH--- NaCl+H2O HCOOH+ NaOH--- HCOONa+ H2O HCl+ Zn--- ZnCl2+H2 CH3COOH+ Zn--- (CH3)2COOZn+ H2 Fe2O3+ HCl --- FeCl3+ H2O Fe2O3+HCOOH --- Fe(HCOOH)3 + H2O CaCO3+ HCl --- CaCl2+ H2Co3 Vahetusreaktsioon tekkib alati tugevama happe poolt nõrgema happe poole. "Üle mõistuse soe vesi," ütles blondiin kui oli nabast saadik vees.
tõkestamiseks kasutatakse mitmesuguseid tehnoloogilisi võtteid nagu pindade katmine mitmesuguste metallidega, mille korrosioonivõime on kõrge, katmine lakkide värvide ja plastmassiga. 3 Kasutatud kirjandus · Korrosioon? - http://et.wikipedia.org/wiki/Korrosioon · Pilt et.pandapedia.com/wiki/Redoksreaktsioon · Ülejäänud teave tuttavalt ehitusinsenerilt. · Avita keemia õpik IX klassile II osa 4
Oksiidid meie elus Oksiide leidub maailmas kõikjal ning neid kasutatakse paljudeks asjadeks. Ilma mõne oksiidita ei leiduks maal isegi elu. Vesi, mida loetakse elu aluseks, koosneb 2-st vesiniku ja ühest hapniku aatomist ning seda nimetatakse divesinikoksiidiks. Ilma veeta ei saaks maal kasvada taimed, mis on eluks maal samuti hädavajalikud. Taimedele on eluks vajalik ka süsinikdioksiid, mida toodavad teised elusolendid hingamisel. Näiteks ainet nimega divesinikdioksiid kasutatakse valgendamisel. Veel kasutatakse seda ka meditsiinis kergemate haavade raviks. Divesinikdioksiidi tuntakse ka vesinikperoksiidi nime all. Kaltsiumoksiid (keemiline valem CaO) on laialdaselt kasutatav keemiline aine. Toiduainetes kasutatakse teda happesuse regulaatorina. Ka kasutatakse teda suhkru puhastamisel lisaainetest ning pagaritööstuses kui stabilisaatorit. Teda on kasutatud ka sisikondade puhastamiseks vorsti too...
KLOOR Cl2 (kr.k chloros kahvaturoheline) Kloori avastas 1774 Sveitsi teadlane Karl Wilhelm Scheele. Kuid nimetuse sellele rohkekaskollasele gaasile andis teadlane Davy, kes tundis kloori ära kui keemilse elemendi. 1811. aastal andis ta kloorile ka nime tema roheka värvuse järgi. Samal aastal võeti kasutusele termin halogeen. Kirjeldati seda kui kloori võimet reageerida metallidega, et moodustada soolasid. 19 saj. algul kasutati kloori enamasti tekstiilitööstuses valgendajana või desinfektsioonivahendina, et vältida haiguste levikut. Peale selle hakati tootma ka soodat, mille leiutas prantslane NicolasLeblanc. Samuti kasutatakse kloori joogivee steriliseerimiseks, kuid ka basseinide vete puhul. Paljud ained nagu paber, petroolium, tekstiilid, värvid, tulekustutid, plastikained ja putukamürk sisaldavad kloori või on kasutatud kloori nende valmistamiseks. Kloor oli ...
KAALIUM (kalium-potassium) SÖÖMISES Toit kui ilu saladus Parimad söögid piisava kaaliumi koguse saamiseks on värsked töötlemata toidud, sealhulgas liha, kala, köögiviljad (eriti kartulid), puuviljad (avokaadod, kuivatatud aprikoosid ja banaanid), tsitrusmahlad (näiteks apelsini mahl), meieri-ja täisteraviljatooted. Suurema osa kaaliumist, mida vajame, saame kätte süües mitmekesist toitu koos piisava piima, liha, teravil...
Hapeteks nim. Liitaineid,mis koosnevad vesinikust ja happejäägist. H2SO4(happejääk) Happejäägiks nim.happe molekuli osa,mis jääb järele peale vesiniku aatomite eraldamist. Happejäägi o-a.näitab happes olevate vesiniku aatomite arv.H2SO4 HJ on SO4 H3 po4 Happeid liigitatakse tugevuse järgi Happed:1)hapnikku sisaldavad HNO3,H2CO3,H2SO4 2)hapnikku mittesisaldavad HCL,HBR Tugevad H2SO4,HNO3,HCL kesk.tugevusH3PO4,H2SO3,nõrgad H2CO3,H4SIO4,H2s H.atomite järgi1 protolisd HCL,HNO3,HBR 2proH2SO4,H2SO3,H2CO3 3jaenam H3BO4 H4SIO4. Hapete füsa omad. 1)hapetel on hapu maitse2)enam. happd on vedelikud3)tugvd happd on sööbivad ja mürgis. Keem.oma. Vees lagunevad happemolekulid ioonideks. 1)HCL-H+Cl(ioon)H2SO4-2H+SO4 2)H ioonide tõttu muudavad indi. Värvi ühtmoodi. Indikaator-nim. Aineid,mis muudavad oma värvi happelises või alustelises keskkonnas. -lakmus sinine-happs punane/metüüloranz punane/universaa indikas.kollane.nätb lahuse ph-d happed...
Tina Tina on keemiline element järjekorranumbriga 50, metall. Sümbol Sn. Tal on 10 stabiilset isotoopi, massiarvudega 112, 114, 115, 116, 117, 118, 119, 120, 122 ja 124. Tal on kõigist elementidest kõige rohkem stabiilseid isotoope. Tina esineb 3 kristallmodifikatsioonina. Normaaltingimustel on stabiilne valge tina, mis on hõbehall pehme tahke aine tihedusega 7,31 g/cm³ ja juhib elektrit kui metall. Temperatuuril alla 13,2 °C on stabiilseim hall tina, mis on hall, habras pooljuht tihedusega 5,5 g/cm³. Temperatuuril üle 160 °C on ta stabiilne habras tina, mis on habras, kuid metalne. Aatomnumber: 50 Klassifikatsioon: p-elemendid Aatomi ehitus: Elektronvalem: 1s2 2s2p6 3s2p6d10 4s2p6d10 5s2p2 Elektronskeem: +50|2)8)18)18)4) Elektronite arv: 50 Neutronite arv: 69 Prootonite arv: 50 Oksüdatsiooniast(m)e(d) ühendites: -IV, 0, II, IV Kristalli struktuur: tetragonaalne Füüsikalised omadused: Aatomma...
Loodus jaguneb kaheks-elus,eluta Elu-mateeria osa mis suudab end ise kasvatada ja paljuneda Rakk-kõige väiksem üksus elu omadustega Ainuraksed-bakterid,protistid Aine ja energiavahetus Autotroofid-taimed Heterotroofid-organismid Reageerimine-inimesel-aju ,närvid,lo-meeleorg Paljunemine-mittesuguline,vegetatiivne-taimed eostega-seened Areng.sugulisel-algab viljastumisega,mittesugulisel eraldumisega vanemorganismist Looduse organiseeritus 1.aatomid-tuum,elektronid,neutronid,prootonid 2.molekulid-dna,valgud,lipiidid,sahhariidid 3.organellid-mitokonder,golgi kompleks 4.rakud.5.koed 6.organid-kindla ül kudede kogu nt süda maks jne 7.organsüsteemid ehkelundkonnad 8.organism.9.populatsioon 10.liigid-sarnase ehituse,geneetika,ja talitusega org 11.ökosüsteem Loodusteadus-uurib elus ja eluta loodust Kõik elus organismid koosnevad orgaanilistest ainetest- biomolekulid ,bioaktiivsed ained-hormoonid,ensüümid, vitamiinid,sahhariidid-süsinik,vesinik j...
Sahhariidid, lipiidid, valgud · Sahhariidid on orgaanilised ained, mille koostises on süsinik, vesinik ja hapnik · Sahhariidi jagunevad: 1. Monosahhariidid süsinikuaatomite arv molekulis on 3 kuni 6. 2. Oligosahhariidid - 2-3 monosahhariidi jääki on omavahel liitunud. - Maltoos linasesuhkur glükoosi jäägid. - Sahharoos peedisuhkur glükoosi ja fruktoosi jäägid. - Laktoos piimasuhkur galaktoosi ja glükoosi jäägid 3. Polüsahhariidid polümeerid, mille monomeerideks on monosahhariidide jäägid. - Tärklis glükoosi jäägid, vees ei lahustu, koguneb taimedes viljadesse ja mugulatesse. - Tselluloos glükoosi jäägid, vees ei lahustu, põleb, pole magus - Glükogeen ei ole magus, ei lahustu vees. · Tärklise ja tselluloosi erinevus seisneb glükoosijääkide erinevatest asenditest. (Tselluloosi hapniku molekulid on 180° kraadise...
Igaühele meeldib olla puhas, aga naha tervena hoidmiseks on vajalik naha pinnalt regulaarselt eemaldada meiki, liigset rasu, mustust ja surnud rakke. Seda ülesannet täidavad mitmesugused puhastusvahendid. Erinevate nahatüüpide jaoks on töötatud välja erinevaid puhastusvahendeid. Neid võib toota seepide, vedelike, geelide, kreemide, sampoonide, maskide jt. kujul. Puhastusvahendite koostis Puhastusvahendites on põhiliseks toimeaineks erinevad surfaktantide segud. Need on aktiivsed ühendid, mis sisaldavad rasvlahustuvat ja veeslahustuvat osa. Rasvlahustuv osa ühineb rasu ja mustusega, veeslahustuv osa võimaldab vahendi mahapesemist. Puhastusvahendid võivad sisaldada järgmisi komponente: · vett · surfaktantide segusid (näiteks naatriumlaurüülsulfaat, naatriumsulfosuktsinaat jt), mis puhastavad, panevad toote vahutama ja jätavad nahale meeldiva tunde · emulgaatoreid (näiteks die...
RAUD o Rauatoodang moodustab 90% kõigi metallide aastasest toodangust. o Levikult maakoores on raud üldjärjestuses neljas element. o Tuuma koostises on kõige rohkem rauda. o Looduses esineb raud pealmiselt ühenditena, kuid vähesel määral võib teda leida ka ehedana. o Lisandina on rauda kõikjal liiva koostises, savides, kivimites, looduslikus vees ja mujal. o Tähtsamad rauamaagid sisaldavad rauda oksiididena. o Pruuni ja punase rauamaagi põhikoostisaineks on raud(III) oksiid Fe2O3. o Mustas rauamaagis ehk magnetiidis aga Fe3O4. o Magnetiidi nimetus tuleb tema magnetilistest omadustest. o Varem oodeti Eesti rauda soorauamaagist (sisaldab rauda pealmiselt hüdroksiidina). o Rauda leidub ka vere punalibledes. o Raud kuulub siirdemetallide hulka. o Raud kuulub keskmise aktiivsusega metallide hulka. o Väga puhas raud on vee ning õhuhapniku suhtes küllaltki vastupidav. ...
ALUMIINIUM · Ei leidu looduses lihtainena · Suure keemilise aktiivsuse tõttu esineb ta vaid ühendite koostises · Alumiiniumiühendid on looduses väga laialt levinud · Al esineb koos hapniku ja räniga paljude kivimite, savide ja teiste mineraalide koostises. · Levikult on Al maakoores hapniku ja räni järel kolmandal kohal (massi järgi). · Tähtsam Al tooraine on mineraal boksiit, mille põhiline koostisaine on Al2O3. · Al ühendid on väga (keemiliselt)püsivad. · Et saada neist metallilist alumiiniumit, tuleb kasutada väga tugevaid redutseerijaid. · Al saamine keemiliste reaktsioonide abil on keeruline ja kulukas · Al tootmine elektrivoolu abil, muutis Al suhteliselt odavaks ja kättesaadavaks metalliks. Füüsikalised omadused : · Hõbevalge läikiv metall, peegeldab hästi valg...
Hapete omadused Soolhape ehk vesinikkloriidhape HCl Saadakse vesinikkloriidi juhtimisel vette seal lahustuvad need vesinikioonideks ja kloriidioonideks. Soolhape on tugev hape. Vesinikkloriid annab soolhappele terava lõhna, see kahjustab hingamisteid. Soolhape kuulub maomahla koostisse (0,5%), ta aitab toiduaineid lagundada. Üle- või alahappelisus põhjustab seedehäireid, mis on tervisele kahjulikud. Divesiniksulfiidhape H2S Saadakse lahustades vees gaasilist vesiniksulfiidi. Divesiniksulfiid on väga mürgine aine. See tekib nt valkude lagunemisel ilma õhu juurdepääsuta. Divesiniksulfiid haiseb nagu mädamuna. Väävelhape H2SO4 Väävelhape on üks tugevamaid happeid. Kontsentreeritud väävelhape on tugev oksüdeerija raske õli taoline vedelik, mis seob tugevasti õhuniiskust. Seda tuleb säilitada õhukindlalt suletud anumates. Süsinikuühendid söestuvad selle toimel. Väävelhape on üks tähtsamaid ja enamkasuta...
Referaat Naatriumhüdroksiid ehk seebikivi Timo Stogov 10a Valga 2008 Naatrumhüdroksiid Naatriumhüdroksiid ehk Seebikivi keemiline valem on NaOH. Naatriumhüdroksiidi esineb : Naatriumhüdroksiid lahusena, graanulitena Seebikivina , kaustilise soodana , leelisena. Füüsikalistest ja keemilistest omadustest tingitud ohtlikkus: Aine ei ole tule ega plahvatusohtlik. Aine rekstsioonil mõnede metallidega tekib plahvatusohtlik gaas: H2. Reaktsioonil ammooniumsooladega tekib tuleohtlik gaasiline ammoniaak. Sissehingamisel Terviseohtlikkus : Aine on tugevalt söövitav. Nii aine kui tema vesilahus on sööbiv, tekitab naha, silmade, lihasmembraani ja hingamisteede ärritust ning põletust. ...
Alkoholi mõju inimesele Eestis on alkoholi tarbimise arvestuslik kogus ca 13 liitrit puhast piiritust inimese kohta aastas ja sellega oleme Euroopa Liidus häbiväärsel esimesel kohal. Mujal riikides tarbitakse keskmiselt kuni 5 liitrit absoluutset alkoholi inimese kohta. Seega on alkoholism Eestis tõsiseks probleemiks. Alkoholi mõju inimesele sõltub soost, vanusest, rassist, kehakaalust ja sellest, kas kõht on täis. Mehed kannatavad alkoholi kuni kolm korda rohkem kui naised, sest naiste maos toodetakse kolm korda vähem etanooli lagundavaid ensüüme. Võrreldes täiskasvanuga, on lapse organism hoopis tundlikum alkoholi kahjuliku mõju suhtes. Väike laps võib surra 6070 g korraga joodud viinast, samal ajal on täiskasvanud inimest surmav annus 11,5 liitrit. Isegi ühekordne, suhteliselt väikese alkoholiannuse joomine, võib lapsel esile kutsuda tugeva joobe. Alkohoolsete jookide tarvit...
SOOLAD Soolaeks nimetatakse liitaineid, mis koosnevad metallist ja happe jäägist. Metalli ioonidest ja happejäägist ioonideks metall on + (katioon) ja on anioon. Näiteks Al2(SO4)3 on AL Metall ja SO4 on Happejääk anioon Soolade nimed pannakse happejäägi ioonide järgi HNO3 NO3 Nitraat ioon Sool ja nitraat Kui soola koostises on muutuva oksuldatsiooniastmega metall siis öeldakse OKA sisse. (muutuad metallid on : raud, tina, vask, kroom) Mõisted: 1. Aluselised oksiidid Alusele vastav oksiid 2. Anioon Negatiivse laenguga ioon 3.Hape Aine mis annab lahusesse vesinikioone 4.Sool Kristalne aine, mis koosneb (aluse) katioonidest ja (happe) anioonidest 5.Redutseerimine Elektronide liitmine. 6.Oksüdeerimine elektronide loovutamine, sellele vastab elemendi oksüdatsiooni astme suurenemine 7. Leelis Vees lahustuv tugev alus (hüdroksiid) Soolade Füüsi...
Alumiinium. 1827 a sai välja paistev saksa keemik, hariduselt arst, Friedrich Wöhler metalli, mida mitte keegi ei olnud kunagi näinud. Veidi varem sai seda metalli Oersted. Algul eraldas Wöhler metalli keemilisest ühendist halli pulbrina, mis peenestamisel omandas metallilise läike. Katsed saada metalli kangina või suurte teradena jäid tulemusteta. Enne kui neid katseid kroonis 1845a edu, kulus 18 aastat püsivaid otsinguid. Wöhler sai uut metalli nööpnõelapeasuuruste teradena. Väliselt oli ta sarnane hõbedaga, kuid erinevalt viimasest erakordselt kerge,4 korda kergem hõbedast, 3,5 korda kergem vasest ja peaaegu 5 korda kergem rauast. Kuna uue metalli saamise lähtaineks olid ammu tuntud maarjased , siis hakati ka metalli nimetama alumiiniumiks.Alumiinium, keemiliste elementide perioodilisussüsteemi III rühma element. Järjenumber on 13,aatommass 26,98154. Alumiinium on tänapäeval üks tuntumaid ja enamkasutatavaid metalle(tähtsuselt teise...
Kool Nimi Klass KOKA JA KOKAIIN Referaat Juhendaja: Aasta Sisukord 1. Kesknärvisüsteemi stimuleerivad ained....................................................3 1.2 Koka ja kokaiin.......................................................................3 1.3 Kokaiini mõju.........................................................................4 1.4 Kahjustused...........................................................................4 1.5 Sõltuvus................................................................................5 2. Sünteetilised kesknärvisüsteemi stimulaatorid.............................................6 2.1 Ainete valmistamine ja kasutamine...............................................6 2.2 Amfetamiin.......................................................................
kool nimi klass MORFIIN Referaat Juhendaja: aasta Sisukord 1. Sissejuhatus ....................................................................................... 3 2. Morfiin ............................................................................................ 4 3. Kokkuvõte .... .................................................................................... 6 4. Lisa ................................................................................................. 7 2 Sissejuhatus Morfiini valmistatakse oopiumiekstraktist. Süstimiseks lisatakse lähteainele askorbiin, - sidrun- või viinhapet ning seejärel kuumutatakse - nii saadakse vajalik lahus, sest otse ta muidu vees ei lahustu. 3 Morfiin Oopiumiks nimetatakse unimaguna tardunud (kuivanud) pii...
1. aluseline oksiid + hape sool + vesi 2. aluseline oksiid + vesi leelis 3. happeline oksiid + alus sool + vesi 4. happeline oksiid + vesi hape 5. aluseline oksiid + happeline oksiid sool 6. lihtaine + hapnik oksiid 7. alus(veeslahustumatu temp. aluseline oksiid + vesi 8. vesinik + element vesinikühend 9. metal + hape sool + vesinik( lahjendatud hapetega reageerivad pingereas vasakul pool olevad metallid, paremal pool olevad mitte) 10. alus + hape sool + vesi 11. sool + hape sool + hape ( reaktsioon toimub kui tugevam hape tõrjub nõrgema happe soolast välja) 12. veeslahustumatu hüdroksiid temp. aluseline oksiid + vesi 13. leelis + sool veeslahustumatu alus + sool(ainult leelised reageerivad sooladega) 14. aktiivne metall + vesi leelis + vesinik 15. metall + sool metall + sool(aktiivsem metall tõrjub vähem aktiivsema soolast välja, vastupidi ei toimu) 16. sool + hape sool + hape 17...
1.Keemilise reaktsiooni kiirus ja seda mõjutavad tegurid Keemilise reaktsiooni mõiste ainete muundumine teisteks aineteks (ühtedest ainetest tekivad teised ained). Keemilise reaktsiooni kiiruse mõiste osakeste vaheliste põrgete arv kindal ajahetkel kindlas ruumalaühikus. Keemilise reaktsiooni kiirust mõõdetakse kas lähteainete kontsentratsiooni vähenemisel või saaduste kontsentratsiooni suurenemisel kindlas ajaühikus ja kindlas ruumalaühikus. Aine kontsentratsioon väljendab aine hulka ruumalaühikus (tähis c ja põhiühik mol/dm3). 1.1 Reaktsiooni kiirust mõjutavad tegurid Reageerivate ainete iseloom vaata metallide aktiivsusrida (vaskul aktiivsemad, paremal vähemaktiivsed), tugevad ja nõrgad happed. Reageerivate ainete kontsentratsioon läheteainete kontsentratsiooni suurendamisel reaktsiooni kiirus kasvab. Gaasi rõhk gaasiliste ainete osavõtul kulgevate reaktsioonide kiirus rõhu tõstmisel kasvab. Reageerivate ainete kokk...
elektroni. Hapnik on värvitu, lõhnata, maitseta õhust raskem gaas. Et saavutada püsivat väliskihti, on hapniku aatomil vaja liita veel 2 elektroni Looduses on Hapniku elementides kõige rohkem, ta moodustab umbes 50% maakoore massist. Vaba elemendina leidub teda õhus 20,95% mahu järgi, seotuna vees 85,8%, mineraalidesumbes 50%, inimorganismis 65% jm. Hapniku toodetakse vedelat õhku rektifitseerides, õhku fraktsioneeriivalt veeldades või vett elektrolüüsides.Hapniku tarvitatakse keemia-, metallurgia-, jm tööstusts, meditsiinis jm. Hapnik on üks levinumaid ja olulisemaid elemente Maal. Maa atmosfääris on hapnikku umbes 21% ja teda tekib pidevalt fotosünteesi käigus juurde. Samas aga väheneb hapniku hulk atmosfääris, kuna ta osaleb paljudes keemilistes reaktsioonides. Hapnikku kasutavad hingamiseks kõik aeroobsed elusorganismid. Ta osaleb ka teistes looduslikes oksüdatsioonireaktsioonides: kõdunemis-, mädanemis- ja põlemisprotsessides, mille
Anorgaaniliste ainete keemilised omadused OKSIIDID Aluseliste oksiidide keemilised omadused Aluseline oksiid ehk metallioksiid 1) Reageerimine veega Saadus on leelis (tugev alus) + - Li2O + H2O > 2LiOH 2+ - CaO + H2O > Ca(OH)2 Veega reageerivad ainult I ja II A rühma, alates kaltsiumist, nende metallide oksiidid. 2) Reageerimine happega Saadused on sool ja vesi. + - + - Na2O + 2HCl > 2NaCl + H2O III -II + -2 3+ 2- Fe2O3 + 3H2SO4 > Fe2(SO4)3 + 3H2O 2+ - BaO + 2HI > BaI2 + H2O 3) Reageerimine happelise oksiidiga Saaduseks on sool. + 2- K2O + CO2 > K2CO3 Happeliste oksiidide keemilised omadused 1) Reageerimine veega Saaduseks on hape. + 2- CO2 + H2O > H2CO3 + 3- P4O10 + 6H2O > 4H3PO4 SiO2 + H2O Ei toimu, sest SiO2 on liiv. 2) Reageerimine alustega Saadused on s...
1. Sahhariidid on elutähtsad ühendid, mis koosnevad süsinikust, vesinikust ja hapnikust (vesiniku ja hapniku aatomie arvude suhe on enamasti 2:1) CnH2nOn. 2. Monosahhariidid süsinike aatomite arv on 3-6 (glükoos, fruktoos) Oligosahhariidid 2-3 monosahhariiti on omavahel liitunud (sahharoos) Polüsahhariidid polümeerid, mille monomeerideks on monosahhariidide jäägid (tärklis, tselluloos) 3. Tselluloosil on need ühendid 180 kraadi. 4. Sahhariidide molekulid sisaldavad OH- rühmi. 5. Joodireaktsioon - joodi tuleb peale valada, kui muudab värvi, siis on tärklis (siniseks) 6. Sahhariidid on eluks vajalikud, kõik asjad koosnevad sahhariididest, neid saab süüa 7. Rasvad on elutähtsad ühendid, mis koosnevad glütserooli ja suurema molekuliga karobksüülhapete(rasvhapete jääkidest) 8. Lihtlipiidid - glütseroolist ja rasvhapetest moodustunud ühendid Õlid taimsed rasvad Liitlipiidid - Rakumembraani koostises ...
Toiduainete keemia Toiduaine tööstuse lisaained: Säilitusained Antioksüdandid Emulgaatorid, stabilisaatorid, tihendusained Lõhna- ja maitsetugevdajad Magusained Aroomid ja toiduvärvid Maitseainesegud Mille jaoks kasutatakse? Lihale ja lihatoodetele sageli lisatavad säilitusained nitritid ja nitraadid suruvad alla bakterite elutegevuse, andes samas lihale ja lihatoodetele roosa värvuse. Jookides sageli kasutatavad säilitusained on sorbiin hape ja sorbaadid ning bensoehape ja bensoaadid. Rasvarikaste toitude puhul on vaja kasutada antioksüdante, et kaitsta tooteid rasva rääsumise, värvuse ja maitse muutuste ning toiteväär tuse alanemise eest. Üks enamlevinud antioksüdant on askorbiin hape. Toiduvärve kasutatakse kõige enam kond...
Keemia ja keskkond Jaan Vihalemm Tallinna Nõmme Gümnaasium 9B klass Tallinn 2008 Sissejuhatus Keskkond ökoloogias on organismi mõjutavate väliste biootiliste ja abiootiliste tegurite kogum. Abiootilised tegurid on näiteks valgus, temperatuur, vesi jne. Biootilised tegurid on liigikaaslased ja kõik muud organismi ümbritsevad ja mõjutavad elusorganismid. Argielus puutub inimkond kokku paljude keemiliste ainete ning ühenditega, mis on ohtlikud ja nende keerukad nimetused võivad põhjustada arusaamatust ja hirmu. Sissevõtmisel võivad tekkida mürgistused ja nahaga kokkupuutel ärritus või põletikud. Sageli ohtlikkust siiski kas ülehinnatakse või alahinnatakse. Keskkonnakaitsega seonduvad teemad nagu kliimamuutus, veereostus ja taastuvenergia pakuvad pidevalt kõikjal kõneainet, ning nende tähtsus tõuseb ...
Oksiid liitaine, mille üks element on hapnik põlemisreaktsioon ühinemisreaktsioon hapnikuga Redoksreaktsioon keemiline reaktsioon, millega kaasneb eletronide liitmine ja loovutamine ning elementide oksüdatsiooniastme muutus. oksüdatsiooniaste arvutuslik suurus, mis näitab elemendi oksüdeerumise astet ühendis. Oksüdeerija aine, mille osakesed liidavad elektrone(ise redutseerudes) redutseerija aine, mille osakesed loovutavad elektrone (ise oksüdeerudes) Redutseerumine elektronide liitmine redoksreaktsioonis. O-A väheneb oksüdeerumine elektronide loovutamine redoksreaktsioonis. O-A suureneb. Õhu tähtsamad koostisosad on lämmastik (78%), hapnik (21%) ja ülejäänud õhus leiduvad gaasilised osakesed( argoon, süsihappegaas, veeaur) moodustavad 1%. Laboris saadakse hapniku kasutades vee elektrolüüsi või mõnede vähepüsivate hapnikku sisaldavate ainete lagundamisel( KMnO4) Puhas õhk koosneb hapnikust ja lämmastikust. Saastunud ...
Mis on molekul? Molekul on aine väikseim osake, milleni sda on võimalik peenestada. Molekulid koosnevad aatomitest. | koosneb omavahel seotud aatomitest. Molekulideks liitumisel lähevad aatomid üle püsivamasse olekusse, kus nende energia on väiksem. Lihtainete molekulikd sisaldavad ainult ühe elemendi aatomeid.Lihtained on ained, mis koosnevad ainult ühe keemilise elemendi aatomitest. Suurem osa lihtaineid esineb tahkete kristallidena, mis koosnevad paljuest omavahel keemilise sidemega seotud aatomitest. Sellisteks aineteks on metallid ja ka mitmed mittemetallid, nt C ja unane fosfor. Liitaine molekulid koosnvad erinevate elementid aatomitest. Liitained võivad esineda 1) üksik aatomitena (VIIA rühma elemendid) 2) molekulidena (enbamik gaasilisi lihtaineid esineb kahe aatomiliste molekulidena) O 2, H2, N2, F2, Cl2, mitmed tahked lihtained kooosnevad ka molekulidest S 8, P4. 3) Suurem osa lihtained esineb tahkete kris...
Kiirgus kaitse IONISEERIVA KIIRGUSE OHUD Vastavalt ICRP praegu kehtivale ametlikule hinnangule tõstab 1 Sv doos (vastab ligikaudu doosile, mille said Jaapani aatomipommi plahvatuses ellujäänud) vähisurma tõenäosuse 25%-lt (mis vastab loomulikule vähisagedusele) kuni 30%- ni. Siin on tegemist inimese stohhastilise või tõenäolise vähki suremise riski ja 1 Sv doosist saadava 5%-se lisariski summaga, arvutatuna keskmise elaniku kohta. Kui lühikese ajavahemiku jooksul saadakse oluliselt kõrgemaid <;loose, ilmnevad mõne päeva või nädala pärast nn deterministlikud mõjud. Doosi puhul alla 1 Sv seisneb põhimõju suurenenud vähiriskis. Haigus võib avalduda mõne aja pärast ja kulgeb siis nagu tavaline samatüübiline vähk. Inimtegevusega kaasneb alati mingi oht ja nii on ICRP püüdnud leida võimalikku vastuvõetavat riskitaset, millest lähtuvalt fikseerida kiirgusdoosi piirmäärad. Nende määrade eesmärgiks on saavutada kindelohutuse tase, seejuures kiir...
Kiirguskaitse KIIRGUSKAITSE EESKIRJAD öötajate ja elanikkonnakaitseks ning juurdepääsu tõkestamiseks ntrollitavatele aladele kehtivad spetsiaalsed eeskirjad. vakodanikel ei ole sellistele aladele sissepääsu, id nad võivad siiski vabrikute või haiglate külastamisel radioaktiivse allika hedusse sattudes kiiritust saada. Ka siin ei tohi ületada doosi piirmäärasid mis on 1 mSv aastas, seega allpool kiirgustöötajatele ettenähtud doosi piirmäära). eed ioniseeriva kiirguse doosid, mida patsient saab ravimisel haiglas, allu sellisele kontrollile, kuna kiirgus on patsiendi ravi osa. aitsemeetodid olenevad ka kiirgusallika liigist. Kiirgusallikas võib olla suletud anda välist kiirgust või lahtine ja sattuda organismi, hjustades sisemist kiiritust. NISEERIVA KIIRGUSE KINDLAKSTEGEM riva kiirguse olemasolu saame kindlaks teha kassetti asetatud fotofilmiga. Film on kaitstud valguse mõju eest ja peale ilmutamist enemine võrdeline saadu...
Alkohol Juba umbes 10 000 aastat on inimesed joonud kääritatud jooke ning samas ka vaielnud nende jookida headest ja halbadest külgedest. See arutlus kestab veel tänapäevani, arvamusi on seinast seina, kas alkohol on meile hea või halb. Väga sobiv on öelda, et alkohol on mõlemat toonik ja mürk. Erinevus seisneb mahus, kui palju tarbida. Tagasihoidlik joomine näib olevat südame- ja vereringesüsteemile hea ning kaitseb veidi ka sapikivide ja suhkruhaiguse eest. Rohke joomine on peamine põhjus surmale, mida saaks ära hoida, paljudes maades. Üldiselt on alkohol mängus üle poolte surmaga lõppenud autoavariides. Alkoholi liigtarbimine võib kahjustada maksa ja südant, teeb liiga sündimata lapsele, suurendab võimalust rinna- või mõnele muule vähile, aitab kaasa depressioonile ja vägivallale, segab inimeste vahelisi suhteid. Alkoholi kahepalgeline loomus ei tohiks tulla üllatusena. Alkohoolsete jookide aktiivne ...
Anioonid Katioonid Li OH¯ Na Cl¯ K Br¯ NH I¯ Mg² S ²¯ Ca² SO³¯ Ba² CO²¯ Al³ SiO²¯ Pb² SiO¯ Fe² Fe³ Cu³ Ag Zn² OKSIID HAPPE HÜDROKSIID SOOL Suvaline aine + hapnik Vesinikioon + OH¯ + metalli o.a Metall + CaO ; AlO ;PO happeanioon sulgudes happeanioon HNO ; HSO ; Ca(OH) ; Al(OH) ; Ca(NO) ; HPO NaOH Al(SO) ; NaPO
Sissejuhatus Värv on värvainet või pigmenti ja sideainet sisaldav pastataoline, vedel või tahke aine. Värvaineid ja pigmente võib klassifitseeerida vastavalt päritolule, värvusele, keemilisele koostisele. Nende lähteaineteks on mullad, mineraalid, oksiidid, soolad, samuti taimsed ja loomsed ained. Vanad naturaalsed värvained on näiteks sinerõigas ja indigo, karmiin ja krapp, safran ja värvireseeda, safloor jt. Väga kaugest ajast pärinevad pigmendid on maavärvid(kollased, punased ja pruunid), süsinikmust, kriit, malahhiit ja asuriit, kinaver, punane ja valge tina jpt. Vanaaegsed meistrid valmistasid enamasti kõik vajaminevad materjalid ise ette, siis tänapäeval kunstnikud võtavad värvide või kruntide valmistamisest harva osa. Kõik värvid koosnevad peamiselt värvainest (pigmendist) ja sideainest. Värve saab jaotada vastavalt nende füüsikalistele omadustele, tooraine päritolule või selle järgi, kui...
Oksiidid - ained, mis koosnevad kahest elemendist, millest üks osa on hapnik (oa II) Aluselised, amforteersed oksiidid on mittemolekulaarsed. Happelised, neutraalsed oksiidid aga molekulaarsed. Amfoteersed oksiidid oksiidid, millel võivad avalduda nii happelised kui ka aluselised omadused. Vähemaktiivsed metallid on need. Tavaliselt on o-a III, ehk alumiinium, raud, kroom, tsink (ZnO). Amfoteersed hüdroksiidid on vees lahustumatud, ehk veega nad ei reageeri. Neutraalsed oksiidid ei reageeri hapete, leeliste ega veega. Neutraalsed oksiidid on CO, NO, N2O. Hape aine, mis vesilahuses jaguneb vesinikioonides ja happe anioonideks. Happeid saab liigitada: 1) hapnikusisaldus (O või ei ole O) 2) prootonite arvu järgi (mitu H molekuli on [H; H2; H3]) 3) happe tugevuse järgi. Tugevad: väävelhape, lämmastikhape, soolhape, vesinikbromiidhape, vesinikjodiidhape Keskmised: fosforhape, väävlishape, vesinikfluorii...
Toiduaine 1kg hind kogus summa liha 84,00 110g 9,24 kala 54,50 119g 5,995 piim 12,90 0,5l 6,45 juust 105,00 30g 3,15 või 15,50 20g 0,31 õli 25,90 20g 0,518 kartulid 4,50 250g 1,125 sai 29,70 6g 0,178 leib 42,50 6g 0,225 suhkur 11,90 30g 0,357 juurviljad(porgand) 6,50 200g 1,3 puuviljad(banaan) 21,90 250g 5,475 Summa: 34,32
1) Kirjuta alkoholide ja karboksüülhapete üldvalemid ning tähtsamate esindajate valemid ning nimetused. Alkoholide üldvalem on ROH (metanool CH3OH , etanool CH3CH2OH, propaantriool ehk glütserool HOCH2CH(OH)CH2OH) ja karboksüülhapete üldvalem on RCOOH (Metaanhape HCOOH, etaanhape CH3COOH) 2) Millised on metanooli ja etanooli omadused? Metaan on gaas, mis lahustub vees vähe ning ei ole mürgine. Metanool on värvitu, põletava maitsega mürgine vedelik, mis keeb temperatuuril 65 °C ja seguneb veega igasuguses vahekorras. Etanool on metanooliga välimuse, lõhna ja maitse poolest väga sarnane. See keeb 78 °C juures. Ta on vähem mürgine kui metanool ja see põhjustab joovet, suuremate koguste sissevõtmisel teadvusekaotust ja mürgitust, mis võib lõppeda ka surmaga. Sellest võib tekkida ka sõltuvus alkoholism. 3) Kus kasutatakse etanooli ja metanooli? Etanooli kasutatakse alkohoolsete jookide tegemiseks (peamiselt...