Kui ta süstib endale liiga palju insuliini võib ta samuti koomasse langeda, sest närvirakud jäävad nälga. Esimesel juhul on väljahingatavas õhus atsetooni teisel juhul on väljahingatav õhk ilma iseloomuliku lõhnata. Arvatavasti pole just palju diagnoose, mille kiirabi parameedik paneb lõhna järgi - eksida ei tohi, sest ravi on mõlemal seisundil täpselt vastupidine, saate ehk isegi aru miks. Molekuli ehitus Ahelvorm: CH2OH - CHOH- CHOH- CHOH- CHOH-CHO seega aldehüüdalkohol Ahelvormi on tasakaalulises segus väga vähe, toatemperatuuril umbes 0,3% ometi määrab just ahelvorm glükoosi keemilised omadused, sest ainult ahelvormi molekulis on olemas aldehüüdrühm. Aldehüüdid teatavasti reageerivad alkoholidega andes (pool)atsetaaali. Sama protsess leiab aset ka glükoosi molekulis ja tekib tsükkel. Tsüklisse kuulub ka aldehüüdrühmast pärit hapniku aatom. Kuna seitsmelülised tsüklid on mõnevõrra
Kui ta süstib endale liiga palju insuliini võib ta samuti koomasse langeda, sest närvirakud jäävad nälga. Esimesel juhul on väljahingatavas õhus atsetooni teisel juhul on väljahingatav õhk ilma iseloomuliku lõhnata. Arvatavasti pole just palju diagnoose, mille kiirabi parameedik paneb lõhna järgi - eksida ei tohi, sest ravi on mõlemal seisundil täpselt vastupidine, saate ehk isegi aru miks. Molekuli ehitus Ahelvorm: CH2OH - CHOH- CHOH- CHOH- CHOH-CHO seega aldehüüdalkohol Ahelvormi on tasakaalulises segus väga vähe, toatemperatuuril umbes 0,3% ometi määrab just ahelvorm glükoosi keemilised omadused, sest ainult ahelvormi molekulis on olemas aldehüüdrühm. Aldehüüdid teatavasti reageerivad alkoholidega andes (pool)atsetaaali. Sama protsess leiab aset ka glükoosi molekulis ja tekib tsükkel. Tsüklisse kuulub ka aldehüüdrühmast pärit hapniku aatom. 2
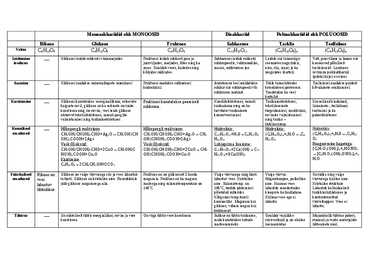
tärklisesiirup. Keemilised Hõbepeegli reaktsioon Hõbepeegli reaktsioon Hüdrolüüs: Hüdrolüüs: Hüdrolüüs: omadused CH2OH(CHOH)4CHO+Ag2OCH2OH(CH CH2OH(CHOH)4CHO+Ag2OCH2 C12H22O11+H20C6H12O6 (C6H10O5)n+nH2OnC6 (C6H10O5)n+nH20nC6H12 OH)4COOH+2Ag OH(CHOH)4COOH+2Ag H12O6 H12O6 O6
lüüsil. KASUTAMINE Glükoosi kasutatakse ravi- mina, energiaallikana mitme- suguste haiguste ravil, mitmete ravimite koostisosa, tekstiilitööstuses, peeglite- valmistamisel, toiduaine-ja kondiitritööstuses. KEEMILISED OMADUSED vask (II) oksiid: CH2OH(CHOH)4CHO+2CuO-> CH2OH(CHOH)4COOH+Cu2O hõbepeegli reaktsioon: CH2OH(CHOH)4CHO+Ag2O -> CH2OH(CHOH)4COOH+2Ag Lubjaveega: C6H12O62CH3CH2OH+2CO2 FÜÜSIKALISED OMADUSED Kristlane aine, mis lahustub Vees lahustuv lihtsuhkur. hästi vees. Värvuselt valge. Magusa maitsega, sulamis
8. Fosünteesi Z-skeem on kujutatud loeng 20 slaid 17 ja 18. Redokspotensiaalide suurenemise suund tagab elektronide liikumise termodünaamiliselt soodsas suunas. 9. Calvin-Bensoni tsükli lähteühendiks loetakse ribuloos-1,5-difosfaati. Seda tsüklit käsitletakse seepärast lähteühendina, kuna ta seob iga ringiga CO 2. P CH2O CO CHOH CHOH CH2O P 10. Calvin-Bensoni tsükli keskseks intermediaadiks loetakse glütseeraldehüüd-3-fosfaati. Selle ühendi kaudu sünteesitakse glükoos ja sealt edasi süsivesikud (suhkur jne). OHC CHOH CH2O P 11. Taimerakud sünteesivad fotosünteesikäigus glükoos baasil tärklist, tselluloosi ja sahharoosi (oligo- ja polüsahariide). 12. a) Vale. Elektronid liiguvad H2O-lt NADPH-le b) Õige
Metanool ja etanool Metanool Metanool ehk metüülalkohol on keemiline ühend valemiga CHOH. Metanooli tuntakse ka puupiitituse nime all, kuna kunagi toodeti kuivdestillatsiooni abil puidust. Tänapäeval saadakse metanooli sünteetiliselt süsinikoksiidi ja vesiniku juhtimisel üle katalüsaatorite (ZnO, Cr2O3) temperatuuril 350-400 ºC ja kõrgel rõhul (200-300 atm). CO + 2H CHOH Metanool tekib looduses mõningate anaeroobsete bakterite ainevahetuse tulemusena, päikesevalguse toimel oksüdeerub see aja jooksul taas süsihappegaasiks ja veeks. Metanooli kasutatakse tööstuses suurtes kogustes eelkõige hea lahustina (lahustab nii polaarseid kui ka mittepolaarseid aineid nagu etanoolgi), kuid ka mootorikütusena (1,7 g metanooli vastab 1 g bensiinile), värvide, lakkide saamisel ning lõhna, värvainete, ravimite,
Siis jahutasin mõlemat katseklaasi jäävannis. Mikroskoobiall oli mõlemale lähtesuhkrule iseloomulik osasoonistruktuur hästi näha. Järeldus Taandavad suhkrud glükoos ja fruktoos reageerimisel fenüülhüdrasiiniga tekitasid osasoonid, mis keetmisel kristallusid hõlpsasti välja. Tekkinud kristallide kuju on lähtesuhkrule iseloomulikud. H OH C HC N NH CHOH C N NH O CHOH CHOH + 2 NH NH2 CHOH CHOH CH CHOH CH2 OH CH2 OH 1.2.3. Hõbepeegli reaktsioon Hoolikalt pestud katseklaasi valasin 1 ml 1%-list AgNO3 lahust, lisasin 0,5 ml
.:C-H2 Polaarsete molekulide liitumisel kaksiksidemele on kaksiksideme polaarsus oluline ja määrab kuhu liitub positiivne ja kuhu negatiivne osa Hüdraatimine tulemuseks on alkohol R-C+H = C-H2 + H+ OH- à RCH(OH) - CH3 CH3-CH = CH2 + HOH à CH3-CH(OH)-CH3 tekib 2-propanool Alküünide hüdraatimisel ei teki püsivat alkoholi , sest kaksiksideme juures ei või OH rühm olla, sellised alkoholid pole püsivad ja isomeeruvad edasi vastavaks aldehüüdiks või ketooniks CH:::CH + HOH à CH2=CHOH à CH3CHO etanaal CH3-C:::CH + HOH à CH3- C(OH) = CH2 à CH3-CO-CH3 propanoon e atsetoon Reageerimine vesinikhalogeniididega R-CH == CH2 + H+Cl- à R-CHCl- CH3 CH3-CH = CH2 + HCl à CH3-CH(Cl)-CH3 tekib 2-kloropropaan 11. klassi Orgaanika konspekt Jaan Usin 13 Redoksomadused Võrreldes küllastunud ühenditega on nad mõnevõrra rohkem oksüdeerunud, kuid siiski eeskätt redutseerijad. Nad põlevad
.:C-H2 Polaarsete molekulide liitumisel kaksiksidemele on kaksiksideme polaarsus oluline ja määrab kuhu liitub positiivne ja kuhu negatiivne osa Hüdraatimine tulemuseks on alkohol R-C+H = C-H2 + H+ OH- RCH(OH) - CH3 CH3-CH = CH2 + HOH CH3-CH(OH)-CH3 tekib 2-propanool Alküünide hüdraatimisel ei teki püsivat alkoholi , sest kaksiksideme juures ei või OH rühm olla, sellised alkoholid pole püsivad ja isomeeruvad edasi vastavaks aldehüüdiks või ketooniks CH:::CH + HOH CH2=CHOH CH3CHO etanaal CH3-C:::CH + HOH CH3- C(OH) = CH2 CH3-CO-CH3 propanoon e atsetoon Reageerimine vesinikhalogeniididega R-CH == CH2 + H+Cl- R-CHCl- CH3 CH3-CH = CH2 + HCl CH3-CH(Cl)-CH3 tekib 2-kloropropaan Redoksomadused Võrreldes küllastunud ühenditega on nad mõnevõrra rohkem oksüdeerunud, kuid siiski eeskätt redutseerijad. Nad põlevad C3H6 + 9/2O2 = 3CO2 + 3H2O. Etüüniga (atsetüleeniga ) keevitatakse-Ilma lisaõhuta on leek tahmav, sest vesinikusisaldus on
Osasoonid kristalluvad lahustest hõlpsasti välja,kusjuures tekkivate kristallide kuju järgi on võimalik eristada ka neid suhkruid,mille stereostruktuurid erinevad vaid ühe kiraalse tsentri konfiguratsiooni poolest. H OH HC N NH C C N NH CHOH CHOH CHOH O + 2 NH CHOH CHOH CHOH
Mitmealuselised: Glütserool, C3H5(OH)3 Nimetused Nimetused -OH rühmaga ühendite nimetuste lõpus on "-ool". Sõna esimese poole saab tuletada temale vastavast alkaanist. Näiteks: CH3OH metanool (üks vesiniku aatom on asendunud hüdroksüülrühmaga) CH3CH2OH etanool CH3CH2CH2OH propanool CH3CH2CH2CH2OH butanool OH rühm ei pruugi paikneda süsinikuahela lõpus, vaid võib olla ahela mis tahes osas. Näiteks: HOCH2CH2OH 1,2-etaandiool HOCHCH2(OH)CHOH 1,2,3-propaantriool (glütserool) Keemilised omadused Alkoholide hüdroksüülrühm on väga nõrgalt happeline, reageerides näiteks aktiivsete metallidega: 2CH3OH + 2Li -> 2CH3OLi + H2 Alkoholid reageerivad orgaaniliste hapetega, moodustades estreid. Alkoholid reageerivad halogeenhapetega, moodustades alküülhalogeniide. CH3CH2OH + HBr -> CH3CH2Br + H2O
kürvetamisel pannil, mürgine, · PROPANOON o Atsetoon CH3COCH3 o Hea lahusti, mürgine · DIHÜDROKSÜATSETOON o DHA HOCH2COCH2OH o Annab kunstliku päevituse(kreemid, geelid), reageerib valguga, · SAAMINE o Alkoholide oksüdeerimisel CH3CH2OH +[O]= CH3COH +H2O o Primaarsete alkoholide oksüdeerimisel (1 OH) o Ketoone saadakse alkoholide oksüdeerimisel, milles OH rühm on kekskel CH3-CHOH-CH3+[O]=CH3-CO-CH3+H2O o Karboksüülhapete redutseerumisel CH3COOH +2[O]=CH3COH+H2O
6. Oblikhape? ehk etaanihappe. Väga mürgine tahke aine. Leidub vähestes kogustes: spinatis, rabarberis. Oblikhape moodustab kaltsiumi vees lahutumatu soola. 7. Rasvhappe? suureolekuline karboksüülhape, mida saadakse rasvade lagunemisel. 8. Rasvad, valgud, süsivesinikud- vaata leht. 9. Alkoholide põlemisreaktsioonide võrrand. CHOH + O2= CO2 + H2O 10. Mõisted: Alkoholid- süsinikuühendid, kus süsiniku aatomid on vahetult seotud ohe või mitme hüdroksüülrühmaga- OH. Karboksüülhape- nimetatakse süsinikuühendid mis sisaldavad ühte või mitut karboksüülrühma- COOH. Süsivesinikud- süsiniku rohkearvuline looduslik ühend. (?) Jää-äädikhape- etaanhape temperatuuril 16-17 C veevaba etaan
Etüüni reaktsioon vesinikkloriidhappega on suure praktilise tähtsusega, kuna siis moodustub vinüülkloriid e. kloroeteen, mille baasil valmistatakse plastmasse, kunstnahka, vahariiet. Etüünist saab veel äädikhapet, polüstürooli, kummi, lahusteid, pleksiklaasi. Hüdrogeenimine: CHCH + H2 CH2=CH2 CH3CH3 Halogeenimine: CHCH + Cl2 CHCl=CHCl CHCl2CHCl2 Vesinikhalogeenidega: CHCH + HCl CH2=CHCl CH3CHCl2 Hüdraatimine: CHCH + H2O CH2=CHOH CH3CH(OH)2 Põlemine: CHCH + 3O2 2H2O + 2CO2 + 2C Homoloogiline rida: 1. - 2. etüün C2H2 3. propüün C3H4 4. butüün C4H6 5. pentüün C5H8 6. heksüün C6H10 7. heptüün C7H12 8. oktüün C8H14 9. nonüün C9H16 10. deküün C10H18 V = n * Vm n = m/M = m/V M molaarmass Vm molaarruumala (22,4) m mass n moolide arv tihedus mol/mol; m/M; V/Vm (gaas); V/M (vedelik)
Alkoholid on sellised süsivesinikest tuletatud ühendid, milles üks või enam vesiniku aatomit on asendatud ühe või enama hüdroksüülrühmaga. Tähtsamad alkoholeon metanool ja etanool. Metanool: · CHOH · Suurim süsinikuühendite rühma - alkoholide kõige lihtsam esindaja. · Metanooli võib saada metaan oksüdeerimisel. · Lihtsam on metanooli saada CO redutseerumisel. · Metanool on värvitu, põletava maitsega mürgine vedelik. · Keemis temperatuur 65° · Seguneb veega igasuguses vahekorras. · Metanooli väiksemate koguste sisse võtmisel võib see põhjustada pimedaks jäämist jt raskeid tervisehäireid.
Alates penteenist on vedelikud ja süsinku arvust 18 (C18H36) tahked ained. Keemilised omadused:kolmikside on kaksiksidemega võrreldes veidi püsivam ning alküünidele iseloomulikud reaktsioonid kulgevad aeglasemalt võrreldes alkeenidega. Hüdrogeenimine: CH≡CH + H2 → CH2=CH2 → CH3–CH3 Halogeenimine: CH≡CH + Cl2 → CHCl=CHCl → CHCl2–CHCl2 Vesinikhalogeenidega: CH≡CH + HCl → CH2=CHCl → CH3–CHCl2 Hüdraatimine: CH≡CH + H2O → CH2=CHOH → CH3–CH(OH)2 Põlemine: CH≡CH + 3O2 → 2H2O + 2CO2 + 2C Polümerisatsioon:nCH2=CH2→(-CH2-CH2-)n Terpeenid on looduslike süsivesinike klass üldvalemiga (C5H8)n, mille molekulis sisaldub 2 või enam isopreeni molekulist tulenevat lüli: n=2, 3, 4 ..Etüün– C2H2Täielikult puhas etüün on lõhnata, värvuseta, vees lahustumatu, õhust veidi kergem, väga plahvatusohtlik ja narkootilise toimega gaas
paiknevad kolesterooli ning valgud apoliproteiinid. Joonist vaata loeng 23 slaid 30. Funktsioon: trantsportivad vees lahustumatuid lipiide vereringes. 11. Maksarakkude mitokondrites toimub ketokehade (=ketoonkehade) süntees. Sünteesi lähteaineteks on atsüül- CoA. Ketokehadena tuntakse: atsetooni (CH3 CO CH3), atsetoatsetaati (CH3 CO CH2 COO-)ja hüdroksübutüraati (CH3 CHOH CH2 COO-). 12. Ketogeneesi (ketokehade süntees) aktiivsus tasakaalustatud ainevahetuses on tagasihoidlik, aga diabeedikute puhul aktiivsus suurenenud. Bioloogiline roll: energiaallikas teatud kudedes (maksas). Omavad mõningat tähtsust energiaallikana ajus st energiaallikas ajule nälgimisperioodil, südame ja skeletilihastes. Diabeedikute puhul veres palju glükoosi, aga seda ei suudeta omastada, seega sünteesitakse ketokehasid juurde.
Alkoholid on alkaanidest tuletatud ühendid, mille molekulis üks või enam vesiniku aatomit on asendatud hüdroksüülrühmaga, mis on veesõbralikud, mis lahustuvad vees palju paremini kui alkaanid, mis ei muuda vesilahuse keskkonda. 2 Mõned alkoholid on mürgised. Tähtsaimad alkoholid on: metanool CH3OH etanool CH3CH2OH glütserool HOCHCH2(OH)CHOH 7) 100-protsendiline alkohol 100-protsendiline alkohol ehk absoluutne alkohol on puhastatud etanool, mis ei sisalda vett. Tavaliselt käib selle mõiste alla etanool veesisaldusega alla ühe mahuprotsendi. Absoluutset alkoholi pole võimalik saada lihtsa fraktsioneeriva destillatsiooni teel, sest segu, mis sisaldab umbes 95,6% etanooli ja 4,4% vett, (rektifitseerirud piiritus) on aseotroopne segu. Üks harilik tööstuslik meetod 100-protsendilise alkoholi saamiseks seisneb selles, et
Polaarsete molekulide liitumisel kaksiksidemele on kaksiksideme polaarsus oluline ja määrab kuhu liitub positiivne ja kuhu negatiivne osa Hüdraatimine tulemuseks on alkohol R-C+H == C-H2 + H OH RCH(OH) - CH3 CH3-CH = CH2 + HOH CH3-CH(OH)-CH3 tekib 2-propanool Alküünide hüdraatimisel ei teki püsivat alkoholi , sest kaksiksideme juures ei või OH rühm olla, sellised alkoholid pole püsivad ja isomeeruvad edasi vastavaks aldehüüdiks või ketooniks CH:::CH + HOH CH2=CHOH CH3CHO etanaal CH3-C:::CH + HOH CH3- C(OH) = CH2 CH3-CO-CH3 propanoon e atsetoon Reageerimine vesinikhalogeniididega R-CH == CH2 + H+Cl- R-CHCl- CH3 CH3-CH = CH2 + HCl CH3-CH(Cl)-CH3 tekib 2-kloropropaan Redoksomadused Võrreldes küllastunud ühenditega on nad mõnevõrra rohkem oksüdeerunud, kuid siiski eeskätt redutseerijad. Nad põlevad C3H6 + 9/2O2 = 3CO2 + 3H2O. Etüüniga (atsetüleeniga ) keevitatakse-
Nimetused -OH rühmaga ühendite nimetuste lõpus on "-ool". Sõna esimese poole saab tuletada temale vastavast alkaanist. Näiteks: · CH3OH metanool (üks vesiniku aatom on asendunud hüdroksüülrühmaga) · CH3CH2OH etanool · CH3CH2CH2OH propanool · CH3CH2CH2CH2OH butanool OH rühm ei pruugi paikneda süsinikuahela lõpus, vaid võib olla ahela mis tahes osas. Näiteks: · HOCH2CH2OH 1,2-etaandiool · HOCHCH2(OH)CHOH 1,2,3-propaantriool (glütserool) 4 Keemilised omadused Alkoholide hüdroksüülrühm on väga nõrgalt happeline, reageerides näiteks aktiivsete metallidega: 2CH3OH + 2Li -> 2CH3OLi + H2 Alkoholid reageerivad orgaaniliste hapetega, moodustades estreid. Alkoholid reageerivad halogeenhapetega, moodustades alküülhalogeniide. CH3CH2OH + HBr -> CH3CH2Br + H2O 5 Glütserool
3) polüsahhariidid on kõrgemolekulaarsed ühendid, milles on omavahel seotud väga palju monosahhariidide jääke - [C6H10O5]n- tärklis, tselluloos, glükogeen Tsüklilise sisemolekulaarse poolatsetaali teke: Glükoosi keemilised omadused: 1. oksüdeerimine (hõbepeegli reaktsioon) C5H11- CHO + Ag2O C5H11O5COOH + 2Ag Glükoonhape 2. redutseerimine (+H2) C5H11O5CHO + H2 CH2OH(CHOH)4CH2OH Sonbiit 3. käärimine a) alkoholikäärimine C6H12O6 2C2H5OH + 2CO2 kõik alkohoolsed joogid Etanool b) piimhappeline käärimine C6H12O6 2C6H6O3 Piimhape CH3CH(OH)COOH 4. Molekulisisene poolatsetaali tekkimine: Glükoosi ahelvormist tekib kas - või - glükoos 5. Molekulidevahelise glükoosiidsideme teke
Ibuprofen's action as a painkiller and fever-reducing compound is due to its ability to inhibit the synthesis of prostaglandins It does this by interfering with the action of an enzyme called cyclooxygenase which catalyzes the conversion of a compound called arachidonic acid into prostaglandins 4 step Ibuprofen synthesis First step: Nucleophilic addition Reduction of the carbonyl group C=O by sodium tetrahydridoborate produces a secondary alcohol group CHOH. Second step: Sn1 nucleophilic substitution of the hydroxyl group To improve reactivity of alcohols the leaving anion OH is converted into H2O CH3)3COH + HCl (37%) (CH3)3COH2(+) Cl() (CH3)3C(+) Cl() + H2O (CH3)3CCl + H2O (SN1 ) Third step: During this step Grignard reagent is formed. Forth step: The nucleophilic addition : carboxylic acid production H-NMR
tasakaalu? Reageerimisel leelistega moodustuvad estrist happe sool ja alkohol. CH3 -- COOCH3 + NaOH CH3 -- COONa + CH3 -- OH Happelisel hüdrolüüsil moodustuvad hape ja alkohol.Katalüsaatorina kasutatakse tugevaid happeid, näiteks HSO. CH3 -- COOCH3 + H2O + H3O CH3 -- COOH + CH3 -- OH + H3O Estreid saadakse happe ja alkoholi omavahelisel reaktsioonil happelises keskkonnas (tavaliselt H2SO4 juuresolekul). HSO CHCOOH + CHOH CHCOOCH +HO. Katalüsaator kiirendab reaktsiooni. 5. Millised reaktsioonid on omased amiididele? Kuidas amiide saadakse? Amiidid reageerivad leelistega, tekivad sool ja ammoniaak. Amiidi happelisel hüdrolüüsil saadakse karboksüülhape ja moodustub ammooniumkatioon (NH). Amiide saadakse karboksüülhapete derivaatidest. R -- COOR + R'NH2 R -- CONHR' + ROH 6. Milleks estreid kasutatakse ja kus neid esineb?
Ole(iin)hape C18:1, 9-oktadetseenhape (joonista ise omale!) 6. Rasvad glütserooli (propaantriooli) ja rasvhapete estrid. Sisaldavad kahe või kolme erineva rasvhappe radikaale. CH2O(I rasvhappe)CHO(II rasvhape)CH2O(III rasvhape) Vahad rasvhapete ja pika süsinikuahelaga alkoholide (nn rasvalkoholide) estrid. R1-CO-O-R2 Sfingolipiidid liitlipiid, mille aluseks on sfingosiin ehk kahealuseline aminoalkohol. (CH3 (CH2)12-CH=CH)CHOH(NH2)CH-CH2OH; rasvhape liitub N külge ja täiendav komponent võib samuti N külge veel lisaks liituda või/ja viimase OH juurde. Glütserofosfolipiid sisaldab glütserooli, kahte rasvhappejääki ning fosforüleeritud alkoholi, on glütserooli estrid, milles kaks OH-rühma on esterdatud rasvhapetega ja üks fosforhappega. (R-CO-O)CH2(R'-CO-O)CH(O-POOH-O-X)CH2. Steriid ehk sterüülester rasvhape seostub sterooliga estersidemega 3. pos. OH-rühma kaudu
Katseklaase loksutatakse. Seejärel lisatakse mõlemasse 4 ml destilleeritud vett ja loksutatakse veel. Lipiidi sisaldavas katseklaasis muutub segu häguseks. Järeldused Hägusus tekkis esimest proovi sisaldavas katseklaasis. Tekkis õli-vees tüüpi emulsioon. 1.3.3 Akroleiiniproov Glütserooli kuumutamisel tekib terava lõhnaga propenaal (akroleiin). Sama juhtub ka rasvade ja glütserofosfolipiidedega, kuid mitte lipiididega, mis ei sisalda glütserooli. CH2OH-CHOH-CH2OH CH2=CH-CHO + H2O Glütserool (propaantriool) Akroleiin (propenaal) Töö käik Kahte kuiva katseklaasi pannakse ~1g KHSO 4 või NaHSO4 ja lisatakse mõni tilk akroleiintesti proovidest 1 ja 2. Katseklaase kuumutatakse tõmbekapis gaasipõleti kohal kuni soola sulab ja proov tumeneb, mis annab märku akroleiini moodustumisest. Käega õhku enda suunas tõmmates, tehakse nuusutamise teel kindlaks, kumb proov sisaldas lipiidi. Järeldused
ALKOHOLID Orgaanilises keemias on alkoholid aineklass, mille molekulis on hüdroksüülrühm(ad) (OH) seotud süsinikuaatomiga, millel pole teisi sidemeid hapnikuga, küll aga süsiniku või vesinikuga. Teisiti sõnastatuna on alkohol süsivesinik, milles üks (või mitu) vesiniku aatom(it) on asendunud hüdroksüülrühma(de)ga. Alkoholide nomenklatuursed nimetused lõpevad sufiksiga 'ool'. Alkohol (keemilise nimetusega etanool või etüülalkohol) on joovet tekitav keemiline aine, mida sisaldavad kõik alkohoolsed joogid. Alkoholi manustamine põhjustab inimesel emotsionaalseid muutusi, taju, kõne, mälu, koordinatsiooni ja tasakaaluhäireid. Alkohol on kõige tugevama toimega sõltuvust tekitav narkootiline aine, mis on enamikes riikides legaalne. Alkoholid on rühm orgaanilisi keemilisi ühendeid, mille koostises on hüdroksüülrühm (OH). Seetõttu on tegemist polaarsete solventidega, mis lahustavad paljusid orgaanilisi ja anorgaanilisi saasteaineid. ...
OH OH OH OH OH 1,2-etaandiool 1,2,3-propaantriool (glütserool) II SAAMINE 1. alkeen + H2O CH2 = CH2 + H2O CH3 CH2OH 2. halogeenühend + H2O CH3CH2Cl + KOH CH3 CH2OH + KCl 3. aldehüüdi redutseerumine CH3CHO + H2 CH3CH2OH 4. ketooni redutseerumine CH3 CO CH3 + H2 CH3 CHOH CH3 III KEEMILISED OMADUSED 1. täielik põlemine CH3CH2OH + 3O2 2CO2 + 3H2O 2. katalüütiline oksüdatsioon 2CH3CH2OH + O2 2CH3CHO + 2H2O etanaal CH3CH2OH + O2 CH3COOH + H2O etaanhape 3. metalliga 2CH3CH2OH + 2Na 2CH3CH2ONa + H2 4. katalüütiline oksüdatsioon 2CH3 CHOH CH3 + O2 2CH3COCH3 + 2H2O 5. dehüdratsioon (dehüdraatimine) CH3CH2CH2OH CH3 CH = CH2 + H2O
1,2-etaandiool 1,2,3-propaantriool (glütserool) Created by Riho Rosin 10 13666324649407.doc.doc II SAAMINE 1. alkeen + H2O CH2 = CH2 + H2O CH3 CH2OH 2. halogeenühend + H2O CH3CH2Cl + KOH CH3 CH2OH + KCl 3. aldehüüdi redutseerumine CH3CHO + H2 CH3CH2OH 4. ketooni redutseerumine CH3 CO CH3 + H2 CH3 CHOH CH3 III KEEMILISED OMADUSED 1. täielik põlemine CH3CH2OH + 3O2 2CO2 + 3H2O 2. katalüütiline oksüdatsioon 2CH3CH2OH + O2 2CH3CHO + 2H2O etanaal CH3CH2OH + O2 CH3COOH + H2O etaanhape 3. metalliga 2CH3CH2OH + 2Na 2CH3CH2ONa + H2 4. katalüütiline oksüdatsioon 2CH3 CHOH CH3 + O2 2CH3COCH3 + 2H2O 5. dehüdratsioon (dehüdraatimine) CH3CH2CH2OH CH3 CH = CH2 + H2O
kaksiksideme ründajaks prooton (hüdrooniumioon), mis võib olla pärit mis tahes happe vesilahusest. Prooton ühineb algul alkeeniga ja reaktsiooni lõpus vabaneb uuesti. Ühinedes alkeeniga tekitab prooton väga reageerimisvõimelise vahesaaduse, mis reageerides veega moodustab alkoholi. Ilma prootoni osaluseta poleks alkeen saanud veega reageerida. Järelikult on prooton selles reaktsioonis katalüsaatoriks. Liitumisreaktsioon veega CH2=CH-CH2-CH=CH2 +H2O-> CH2=CH-CH2-CH2-CHOH e) Polümerisatsioon Polümeerid on ühendid, mille molekulid koosnevad pikkadest ühesugustest korduvatest kovalentsete sidemetega seotud strutktuurilülidest. Polümeeride moodustumise protsessi nimetatakse polümeriseerumiseks ehk polümerisatsiooniks. Tavaliselt nimetatakse polümeerideks aineid, mille ahelas on üle saja struktuuri- ehk elementaarlüli ja molaarmass võib ulatuda üle 1000. Seepärast on polümeerid ka kõrgmolekulaarsed ained
Bad / Very bad / OK ¿Cómo se llama usted? ¿Cómo te llamas? Me llamo... / Mi nombre es... koh-moh say yah-mah oo-sted koh-moh tay yah-mahs may yah-moh / mee nohm-breh ess What is your name? (formal) What is your name? (informal) My name is... Mucho gusto. / Encantado. Señor / Señora / Señorita Igualmente. moo-choh goo-stoh / en-cahn- sayn-yor / sayn-yor-ah / ee-guahl-mehn-tay tah-doh sayn-yor-ee-tah Same here. / Same to you. Nice to meet you. Mister / Mrs. / Miss ¿De dónde eres? ¿De dónde es usted? Yo soy de...
Mitmealuselised alkoholid Glütserool, C3H5(OH)3 Nimetused -OH rühmaga ühendite nimetuste lõpus on "-ool". Sõna esimese poole saab tuletada temale vastavast alkaanist. Näiteks: CH3OH metanool (üks vesiniku aatom on asendunud hüdroksüülrühmaga) CH3CH2OH etanool CH3CH2CH2OH propanool CH3CH2CH2CH2OH butanool OH rühm ei pruugi paikneda süsinikuahela lõpus, vaid võib olla ahela mis tahes osas. Näiteks: HOCH2CH2OH 1,2-etaandiool HOCHCH2(OH)CHOH 1,2,3-propaantriool (glütserool) Keemilised omadused Alkoholide hüdroksüülrühm on väga nõrgalt happeline, reageerides näiteks aktiivsete metallidega: 2CH3OH + 2Li -> 2CH3OLi + H2 Alkoholid reageerivad orgaaniliste hapetega, moodustades estreid. Alkoholid reageerivad halogeenhapetega, moodustades alküülhalogeniide. CH3CH2OH + HBr -> CH3CH2Br + H2O Alkoholide keemilised omadused Täielik põlemine CH3CH2OH + 3O2 2CO2 + 3H2O Reageerimine leelismetallidega
Samuti kasutatakse seda naha määrdeainena ja kaitsjana. Kuna lanoliin on vees lahustuv ning imbub nahka, võtab see kaasa ka teisi toit- ja mineraalaineid ning antioksüdante. Lanoliin on inimestele kahjulik, sest see kuulub 10 enam allergiat tekitava aine hulka. Sellepärast ei kasutatagi tänapäeval lanoliini seebi tegemises. (Soapers choice, 2002) 2.4.6. Propüleenglükool Propüleenglükool ehk propaan-1,2-diool, tuntud ka kui antifriis, on orgaaniline ühend valemiga HO-CH2-CHOH-CH3 ning selle joonvalem on näidatud joonisel 13. See on värvitu peaaegu lõhnatu, selge, viskoosne vedelik. Propüleenglükool on kergelt magusa maitsega, hügroskoopne ning vees täielikult lahustuv. Selle sulamistemperatuur on -59oC ning keemistemperatuur 188oC. (Wikipedia, 2013) Propüleenglükooli kasutatakse enesehooldusvahendites lahustina ning niisutajana. Pikaajaline kokkupuude propüleenglükooliga sisuliselt ei ärrita nahka, kuid
Etüüni reaktsioon vesinikkloriidhappega on suure praktilise tähtsusega, kuna siis moodustub vinüülkloriid e. kloroeteen, mille baasil valmistatakse plastmasse, kunstnahka, vahariiet. Etüünist saab veel äädikhapet, polüstürooli, kummi, lahusteid, pleksiklaasi. Hüdrogeenimine: CHCH + H2 CH2=CH2 CH3CH3 Halogeenimine: CHCH + Cl2 CHCl=CHCl CHCl2CHCl2 Vesinikhalogeenidega: CHCH + HCl CH2=CHCl CH3CHCl2 Hüdraatimine: CHCH + H2O CH2=CHOH CH3CH(OH)2 Põlemine: CHCH + 3O2 2H2O + 2CO2 + 2C Homoloogiline rida: 31.- 32. etüün C2H2 33. propüün C3H4 34. butüün C4H6 35. pentüün C5H8 36. heksüün C6H10 37. heptüün C7H12 38. oktüün C8H14 39. nonüün C9H16 40. deküün C10H18 V = n * Vm n = m/M = m/V M molaarmass Vm molaarruumala (22,4) m mass n moolide arv tihedus mol/mol; m/M; V/Vm (gaas); V/M (vedelik)
• asendi-isomeere: ⇒ isomerism tuleneb kaksik- või kolmiksideme erinevast paigutusest CH2=CH-CH=CH2 C4H6 CH2=C=CH-CH3 1,3-Butadieen Butadieen 1,2-Butadieen ⇒ isomerism tuleneb samasuguste funktsionaalsete rühmade (asendajate) erinevast paigutusest CH3-CH2-CH2-OH CH3-CHOH-CH3 1-Propanool 2-Propanool Br Br Br Br Br Br 1,2-Dibromobenseen 1,3-Dibromobenseen 1,4-Dibromobenseen