TTÜ Materjaliteaduse Instituut Füüsikalise keemia õppetool Kolloidkeemia laboratoorne töö 23a Sahharoosi ensüümreaktsiooni kineetiliste parameetrite määramine Eesmärgiks on ensüümreaktsiooni kineetiliste konstantide Km ja vmax määramine Lineweaver- Burki koordinaatides ehitatud graafiku abil (1/v sõltuvana 1/S). Samuti on võimalik määrata ensüümi aktiivsust (1 sekundi jooksul ärareageerivate substraadi moolide arv 1 grammi ensüümi toimel 1 sekundi jooksul ehk teiste sõnadega reaktsiooni kiirus ühikulise hulga ensüümi toimel). Töö ettevalmistamine: Reagentideks on: substraadiks suhkrulahus ja ensüümiks invertaasi lahus. Ensüümi lahus
TTÜ Materjaliteaduse Instituut Füüsikalise keemia õppetool Kolloidkeemia laboratoorne töö 23a Sahharoosi ensüümreaktsiooni kineetiliste parameetrite määramine Tallinn 2013 Eesmärgiks on ensüümreaktsiooni kineetiliste konstantide Km ja vmax määramine Lineweaver- Burki koordinaatides ehitatud graafiku abil (1/v sõltuvana 1/S). Samuti on võimalik määrata ensüümi aktiivsust (1 sekundi jooksul ärareageerivate substraadi moolide arv 1 grammi ensüümi toimel 1 sekundi jooksul ehk teiste sõnadega reaktsiooni kiirus ühikulise hulga ensüümi toimel). Töö ettevalmistamine: Reagentideks on: substraadiks suhkrulahus ja ensüümiks invertaasi lahus. Ensüümi lahus
Tallinna Tehnikaülikool Materjaliteaduse instituut Füüsikalise keemia õppetool Üliõpilane: Teostatud: 22.02.2012. Õpperühm: Kontrollitud: Töö nr. 23FK Arvestatud: FK23a Sahharoosi ensüümreaktsiooni kineetiliste parameetrite määramine Töö eesmärk ja üldmõisted: Eesmärgiks on ensüümreaktsiooni kineetiliste konstantide Km ja vmax määramine Lineweaver- Burki koordinaatides ehitatud graafiku abil (1/v sõltuvana 1/S). Samuti on võimalik määrata ensüümi aktiivsust (1 sekundi jooksul ärareageerivate substraadi moolide arv 1 grammi ensüümi toimel 1 sekundi jooksul ehk teiste sõnadega reaktsiooni kiirus ühikulise hulga ensüümi toimel). Üldmõisted: Erinevalt esimest järku kineetilisest võrrandist kirjeldub reaktsiooni kiirus
Tallinna Tehnikaülikool Materjaliteaduse instituut Füüsikalise keemia õppetool Üliõpilane: Teostatud: 22.02.2012. Õpperühm: YAGB42 Kontrollitud: Töö nr. 23FK Arvestatud: Sahharoosi ensüümreaktsiooni kineetiliste parameetrite määramine Töö eesmärk: · Ensüümreaktsiooni kineetiliste konstantide K m ja Vmax määramine Lineweaver- Burki koordinaatides ehitatud graaafiku abil (1/v sõltuvana 1/S ). · Ensüümi aktiivsuse määramine (1 sekundi jooksul ärareageerivate substraadi moolide arv 1 grammi ensüümi toimel 1 sekundi jooksul). Üldmõisted: On olemas esimest järku ja teist järku kineetilised võrrandid. 1) Esimest järku kineetiline võrrand: k ühik: 2) Teist järku kineetiline võrrand: k ühik:
KYF0280 Füüsikaline keemia Üliõpilase nimi: Franz Mathias Ints Töö nr: FK23 Töö pealkiri: Sahharoosi Ensüümreaktsiooni Kineetiliste Parameetrit keskkonnatehnoloogia Instituut 280 Füüsikaline keemia Õpperühm: EANB31 Töö teostamise kuupäev: 21.10.2020 mreaktsiooni Kineetiliste Parameetrite Määramine Töö eesmärk (või töö ülesanne). sahharoosi ensüümreaktsiooni kineetiliste konstantide Km ja vmax määramine koordinaatides ehitatud graafiku abil (1/v sõltuvana 1/S). Teooria Ensüüm reaktsiooni kineetikat kirjeldab Michaelis-Menteni vôrrand: kus v0 – reaktsiooni algkiirus; S0 – substraadi algkontsentratsioon; Km- Michae maksimaalne kiirus Konstandi Km sisuline tähendus: kui [S]0 = Km, siis v0 = e kontsentratsioon, mille juures reaktsiooni kiirus on pool maksimaalsest. Järeldu madalama substraadi kontsentratsiooni juures töötab ensüüm (ferment) efekti
KYF0280 Füüsikaline keemia Üliõpilase nimi: Rebecca Pärtel Töö nr: FK8 SAHHAROOSI ENSÜÜMREAKTSIOONI KINEETILISTE PARAMEETR Siia tuleb sisestada aparatuuri joonis. keskkonnatehnoloogia Instituut 280 Füüsikaline keemia Õpperühm: EANB31 Töö teostamise kuupäev: 21.10 ONI KINEETILISTE PARAMEETRITE MÄÄRAMINE Töö eesmärk (või töö ülesanne). sahharoosi ensüümreaktsiooni kineetiliste konstantide Km ja vmax määramine koordinaatides ehitatud graafiku abil (1/v sõltuvana 1/S). Teooria. Sahharoosi inversioonireaktsiooni (hüdrolüüsi) produktideks on glükoos ja frukt invertaas C6H12O6 + C6H12O6 Reaktsioon kulgeb vesilahuses (kusjuures vee suurem sahharoosi kontsentratsioonist) esimest järku reaktsioonina. Inversioon neutraalses keskkonnas väga väike, seetõttu kiirendatakse reaktsiooni katalüs või (antud töös) ensüümkatalüsaatorite – abil. Reaktsiooni kiirust mõõdetakse
Küveti laius: l=0,5 cm Ekstinktsioonikoefitsent: ε410 nm=18400 M-1cm-1 Reaktsiooniaeg: t=15 min Arvutused: Produkti kontsentratsiooni arvutan optilise tiheduse järgi (Lambert-Beeri A seadus A=C produkt ∗ε∗l ) = > C produkt = , ε = 18400 M-1/cm-1) ja ε∗l reaktsiooni kiiruse ( v =C produkt /t ) Selleks, et koostada graafik teljestikus v/E, pean leidma E ehk ensüümi kontsentratsiooni. Arvutan ensüümi kontsentratsiooni alglahuses: A∗C 0∗89 C ens= . A 0∗120000 Võtan arvesse, et valgu kontsentratsioonile 1 mg/ml vastab lainepikkusel 280 nm optiline tihedus 1 ning ensüümi alglahuse 89 kordse lahjenduse optiline tihedus lainepikkusel 280 nm on 0,059, seega 0,059∗1∗89 −5 mg μg
Keemiliste reaktsioonide puhul reageerivate ainete kontsentratsioonide muutus ajas. Nt [ATP] on õige tähis. Mõõtmiseks kasutame molaarset kontsentratsiooni. Molaarne kontsentratsioon on numbriline konts, näitab osakeste arvu ruumala ühikus 1M=1mol/L. Milli (-3), mikro (-6), nano (-9), pento (-12), fento (-15). Vee c on ülempiir. Reaktsiooni kiiruse määrab kokkupõrge. Kokkupõrke sagedus sõltub osakeste arvust. Numbriline konts üks molekul põrkab teisega, toimub reaktsioon sõltumata molekulide massist vms. v=dc/dt (hetkkiirus). v=c/t=c2-c1/t2-t1 (keskmine kiirus), seega =lõppolek-algolek. Kui lõpmata väike, siis d. on muutus ja see tähendab erinevust lõppoleku ja algoleku vahel. C= Ct2- Ct1. abil väljendamine diskreetne suurus mingi kindel väärtus. Keskmine kiirus vaatab ainult kahe oleku vahet, see, mis vahepeal toimus, seda ei näe. näiteks. =lõpp-algus
13. Kuidas on vabaenergia muutus seotud muutusega entalpias ja entroopias (valem, ühikud)? G = H TS G =kJ/mol H=kJ/mol S=kJ/mol*K T=K 14. Kuidas on reaktsiooni vabaenergia muutus seotud reaktsioonist osavõtvate ainete kontsentratsioonidega (valem, ühikud)? Glükoos + ATP Glc-6-fosfaat + ADP G = Gº + RT ln ([produktid]/[lähteained]) Vabaenergia ühik-J 15. Milline on isevoolulise reaktsiooni G märk? Negatiivne 16. Reaktsioon: glütseeraldehüüdfosfaat dihüdroksüatsetoonfosfaat on jõudnud tasakaalu. Milline on reaktsiooni G märk sellel hetkel? Tasakaaluolekus deltaG=0 deltaG<0 17. . Kas tasakaaluolekus on reeglina suurem pärisuunalise või vastassuunalise reaktsiooni kiirus? Tasakaaluolekus on pärisuunalise ja vastassuunalise reaktsiooni kiirus võrdsed. 18. Kas reaktsioon on isevooluline ja kuidas võib muutuda reaktsiooni isevoolulisus temperatuuri tõustes, kui
Tallinn 2010 SISUKORD 1. AINETE TUVASTAMINE KVALITATIIVSETE REAKTSIOONIDEGA ........................... 4 1.1 VALKUDE REAKTSIOONID ............................................................................... 4 1.1.1 Biureedireaktsioon ....................................................................................... 9 1.1.2 Ksantoproteiinreaktsioon (Mulderi reaktsioon) ........................................... 10 1.1.3 Milloni reaktsioon ....................................................................................... 10 1.1.4 Sulfhüdrüüli- e tioolireaktsioon ................................................................... 11 1.1.5 Valkude sadestamine trikloroäädikhappega............................................... 11 1.1.6 Valkude väljasoolastamine (globuliinide ja albumiinide eraldamine) .......... 12 1.1.7 Valkude termiline denatureerimine ja lahustuvuse sõltuvus pH-st ............. 12
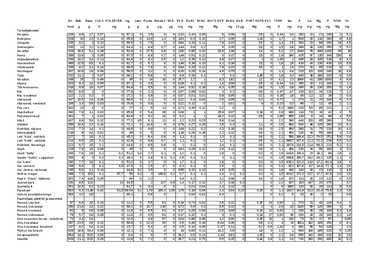
KTUD.RH. küllastatud rasvhapped Toitainete sisaldus tabelis tähendab... C16 palmitiinhape 0 C18 steariinhape MKTA.RH. monoküllastamata rasvhapped PKTA.RH. polüküllastamata rasvhapped C18:2 linoolhape C18:3 linoleenhape VL.KIUDAINED vees lahustuvad kiudained RET.EKV. retinooli ekvivalent NIATS.EKV. niatsiini ekvivalent PANT.HAPE pantoteenhape R% sisaldab x% rasva KLASS E tailiha sisaldus üle 55% KLASS O tailiha sisaldus 40-45% (0.9) söödav osa 90% Sul. sulatatud Rasvas. rasvasusega Toitainete sisaldus tabelis tähendab... vastava toitaine sisaldus antud toiduaines on 0 või minimaalne andmed toitaine sisalduse kohta antud toiduaines puuduvad ENERGIA (kcal) ENERGIA (kJ)
En. Valk Rasv. C18:3 KOLESTER. mg Lakt. Kiuda Ret.ekv Vit.D Vit.E Vit.B1 Vit.B2 NIATS.EKV Vit.B6 Vit.B PANT.HAPE Vit.C TUHK Na K Ca Mg P RÄNI Fe kcal g g G mg g g g g g mg mg mg Mg mg 12 g Mg mg G mg mg mg mg mg Mg mg Teraviljatooted. Nisujahu 328 9,9 1,7 0,07 0 67,1 0 3,5 0 0 0,32 0,43 0,05 5 0,08 0 0,5 0 0,44 0,4 150 13 21 100 2 5,2 Rukkijahu 328 10 2,3 0,14 0 65,6 0 13,6 1,1 0 1,63 0,3 0,13 2,7 0,35 0 1,34 0 1,7 1 500 30 110 360 8 4,9 Odrajahu
kanaleid. Kas tulemuseks on: a) mürkide selektiivne liikumine rakku b) ainete valimatu liikumine läbi rakumembraani c) toitainete selektiivne liikumine rakust välja 11. Milline väide on sobivaim. Pooride vahendatud passiivne transport on oluliselt kiirendatud juhul kui temperatuur on: a) kõrgem kui membraani faasiülemineku temperatuur b) madalam kui membraani faasiülemineku temperatuur c) ei sõltu oluliselt temperatuurist 12. Joonistage graafik, mis esitab aine transpordi kiiruse sõltuvuse membraanil esinevast aine kontsentratsiooni gradiendist. Kujutage graafikul passiivsele transpordile ja vahendatud passiivsele transpordile vastav kõver. 13. Primaarne aktiivne transport kasutab ATP hüdrolüüsi energiat: a) vahetult b) kaudselt c) ei kasuta (sama küsimus ka sekundaarse aktiivse transpordi ja vahendatud passiivse transpordi kohta). sekundaarne aktiivne transport - Kaudselt 14
Nisujahu Rukkijahu Odrajahu Grahamjahu Nisukliid Karna ENERGIA, kcal 328,3 328,1 334,8 335,4 328,7 357,6 ENERGIA, KJ 1373,6 1372,6 1400,9 1403,4 1375,3 1496,1 VESI, g 14 14 14 14 14 14 VALGUD, g 9,9 10 9,2 11 16,6 13,8 RASVAD, g 1,7 2,3 3 3,2 5,1 3 KTUD,RH., g 0,19 0,3 0,54 0,38 0,82 0,4 C16,g 0,17 0,29 0,52 0,34 0,77 0,37 C18,g 0,02 0 0,02 0,03 0,05 0,02 MKTA,RH, g 0,24 0,23 0,26 0,48 0,81 0,85 PKTA,RH, g 0,71 1,15 1,39 1,44 2,62 0,94 C18:2, g 0,65 1,01 1,26 1,31 2,43 0,89 C18:3, g 0,
Elu Maal ei ole isoleeritud süsteem; lisaenergiat ammutatakse Päikeselt. 9. Kuidas on vabaenergia muutus seotud muutusega entalpias ja entroopias (valem, ühikud)? dG=dH dST, kus d tähistab deltat e muutust. 10. Kuidas on vabaenergia muutus seotud reaktsioonist osavõtvate ainete kontsentratsioonidega (valem, ühikud)? Glükoos + ATP Glc 6fosfaat + ADP 11. Milline on isevoolulise reaktsiooni G märk? Isevoolulised protsessid kulgevad Gibbsi energia vähenemise suunas, G< 0. 12. Reaktsioon: glütseeraldehüüdfosfaat dihüdroksüatsetoonfosfaat on jõudnud tasakaalu. Milline on reaktsiooni G märk sellel hetkel? G=0 13. Kas tasakaaluolekus on reeglina suurem pärisuunalise või vastassuunalise reaktsiooni kiirus? Tasakaaluolekus ei ole soodustatud ei pärisuunaline ega vastassuunaline reaktsioon. G=0 14. Kas reaktsioon on isevooluline ja kuidas võib muutuda reaktsiooni isevoolulisus temperatuuri tõustes, kui
504.064.38 (, , , , , .), . ..................................................................................................4 1. ..............5 1.1. ....................................................................................5 1.2. .........................................................................................5 1.3. .....................................................................................6 1.4. ....................................................................................7 1.5. ........................................................................................7 2. 30 /.....................................................................9 2.1. ..................................................................................9 2.2. .......
Pikett 0+00 1+00 2+00 2+38,03 3+00 3+75,86 4+00 4+45,16 5+00 5+25,76 6+00 7+00 7+20 7+66,2 8+00 9+00 9+14,44 10+00 10+98,72 11+00 12+00 12+94,44 13+00 14+00 15+00 16+00 17+00 18+00 19+00 19+28,57 20+00 21+00 21+28,57 21+55 22+00 23+00 23+65,17 24+00 25+00 25+7,81 26+00 26+11,43 26+25,96 26+27,7 26+55 26+59,64 26+75 27+00 27+0,22 27+32,3 27+34,07 27+48,82 27+50 28+00 29+00 30+00 Töömahtude koondtabel Algpikett 0+00 1+00 2+00 3+00 4+00 5+00 6+00 7+00 8+00 9+00 10+00 11+00 12+00 13+00 14+00 15+00 16+00 17+00 18+00 19+00 20+00 21+00 22+00 23+00 24+00 25+00 26+00 27+00 28+00 29+00 Masinvahetuste arvu määramine Kasvupinnase eemalda
Ensümoloogia alused. Kordamisküsimused Ensüüm kui valk: valgu struktuur, aminohapped, mittekovalentsed interaktsioonid, vesilahused ja unikaalsed vee omadused. Valgu funktsioneerimise tagab tema struktuur. Ensüüm kui katalüsaator: keemiline reaktsioon, termodünaamika, kineetika, katalüüs, mehhanism, ensüümide kasutamine tööstuses. Ensüüm kui bioloogiline katalüsaator: sidustatud reaktsioonid, bioenergeetika, metabolism, regulatsioon, klassifikatsioon ja nomenklatuur. Ensüümid on organismide tööhobused. 1) Ensüümkatalüüsi põhimõisted ja printsiibid + Ensüümkatalüüsi peamised tunnus- jooned. · Ensüümkatalüüs põhineb rangelt füüsikalistel ja keemilistel vastasmõjudel.
dG=dHdST, kus d tähistab deltat e muutust. 10. Kuidas on vabaenergia muutus seotud reaktsioonist osavõtvate ainete kontsentratsioonidega (valem, ühikud)? Glükoos + ATP Glc6fosfaat + ADP (võivad olla erinevad reaktsioonid) G = Gº + RT ln ([produktid]/[lähteained]) Vabaenergia ühikJ 11. Milline on isevoolulise reaktsiooni G märk? Isevoolulised protsessid kulgevad Gibbsi energia vähenemise suunas, G< 0. 12. Reaktsioon: glütseeraldehüüdfosfaat dihüdroksüatsetoonfosfaat on jõudnud tasakaalu. Milline on reaktsiooni G märk sellel hetkel? (võivad olla erinevad reaktsioonid) G=0 13. Kas tasakaaluolekus on reeglina suurem pärisuunalise või vastassuunalise reaktsiooni kiirus? Tasakaaluolekus ei ole soodustatud ei pärisuunaline ega vastassuunaline reaktsioon. G=0 14. Kas reaktsioon on isevooluline ja kuidas võib muutuda reaktsiooni isevoolulisus temperatuuri tõustes, kui a) H > 0
FI 25 25 20 15/10a Sideaine ( 50/70) 70/100 100/150 PMB 75/130-65 PMB 75/130-75 a tavaline liiklus/raskeliiklus Segu omadus Ühik Tähis Sideaine sisaldus % Bmin Vmax Poorsus % Vmin VFBmax Pooride täidetus bituumeniga % VFBmin Skeletipoorsus % VMAmin
võrdne esimest järku tuletisega kontsentratsioonist aja järgi: dc v =± . (2) dt Keemilise reaktsiooni kiirus sõltub paljudest teguritest. Põhilisemad nendest on reageerivate ainete iseloom ja kontsentratsioon, rõhk (kui reaktsioonist võtavad osa gaasilised ained), temperatuur, katalüsaatori juuresolek. Heterogeensete protsesside korral, kui reaktsioon toimub faasidevahelisel piirpinnal, sõltub reaktsiooni kiirus selle piirpinna suurusest (seega ainete peenestatuse astmest) ja omadustest. Reaktsiooni kiiruse sõltuvus kontsentratsioonist lihtsate (s.o. ühestaadiumiliste) homogeensete reaktsioonide korral on määratud massitoimeseadusega: reaktsiooni kiirus on võrdeline reageerivate ainete kontsentratsioonide korrutisega (astmetes, mis vastavad reaktsiooni võrrandi kordajatele).
TALLINNA TEHNIKAÜLIKOOL MEHHATROONIKAINSTITUUT ELEKTRIAJAMIGA TRUMMELVINTS PROJEKT ÜLIÕPILANE: KOOD: JUHENDAJA: TALLINN 2010 TALLINNA TEHNIKAÜLIKOOL MEHHATROONIKAINSTITUUT MASINATEHNIKA PROJEKT MHE0062 l D v Projekteerida elektriajamiga vints. Tõstetav mass m = 680 kg Maksimaalne liikumiskiirus v = 0,1 m/s Trumli pikkus l = 300 mm Mootori ja trumli ühendus kettülekanne Esitada: seletuskiri, mastaabis eskiisid, koostejoonis, detaili joonised Joonis esitada formaadil A2 A4 Töö välja antud: 05.02.2010.a.
metallitüki massi. Järeldus:Vead võisid tulla sellest, et osad andmed saadakse vaatluse tulemusena ja silm on tihti ebatäpne.Näiteks kui võtsime vee algtemperatuuri.Siis arvutustel on palju komakohti ning ümardamisel tekivad ebatäpsused.Ka ei katnud me kalorimeetrit kaanega,kui seal sees oli metallitükk ning Töö nr. 3 keemilise reaktsiooni kiirus a) Töö eesmärk: reaktsiooni kiiruse sõltuvus reageerivate ainete konsentratsioonist Töö käik: Nelja katseklaasi mõõta 6cm3 2%-list väävelhapet. Naatriumisulfaadi lahuste valmistamiseks võtta neli katseklaasi ja need nummerdada 1-4. Vastavalt altoodud tabelile mõõta katseklaasidesse naatriumsulfaadi 2%-list lahust ja vet erinevates vahekordades, saades nii, neli erineva konsentratsiooniga naatriumsulfaadi lahust. Esimesele naatriumsulfaadi lahusele valada varem
20 0,013 0,0089 0,01 7 8,2 5,4 5 4 0,009 40 0 0,0120 0,01 5 5,5 5,4 5 0,006 60 0 0,0111 0,01 5 3,7 5,9 5 0,004 80 0 0,0071 0,01 1 2,4 4,6 5 0,002 100 7 0,0031 0,01 7 1,6 2,5 5 23,81 25 21,4 5 25 5.1 Empiirilise jaotuse histogramm graafik 8 7 6 5 4 Empiiriline 3 2 1 0 20 40 60 80 100 5.2 hüpoteesile 4.1 vastava normaaljaotuse tiheduse ja sellele vastava hüpoteetilise histogrammi graafik Normaaljaotus 8.0 0.0150 6.0 ni(norm) 0.0100 f(norm) 4.0 0.0050 2.0 0.0 0.0000
väliskihtide erinevat tihedust (plaatide niiskus 8 % ) Qt x k x k G= 1,08 x 1,08 plaatide niiskust arvestav tegur k - antud kihi paksus, mm k - antud kihi tihedus, kg/m 3 - lihvitud plaadi paksus, mm Tiheduste erinevus sõltub kihtide puiduosakeste fraktsioonilisest koostisest, niiskusest ja pressimistehnoloogiast. Plaadi tiheduse ja kihtide tiheduse vaheline sõltuvus väljendub järgmise valemiga = v iv + s i s Arvutan väliskihi tiheduse v v - väliskihtide tihedus, kg/m 3 s - sisekihi tihedus, kg/m 3 i v = 0,25 0,50 väliskihtide osakaal ( antud juhul 0,35 % ) i s = 0,50 0,75 sisekihi osakaal ( antud juhul 0,65 % ) - v iv 659 - 595 x 0,35 Seega s = = 0,65 = 777,85 kg/m 3 693 kg/m3
3 8 ( x - µ )2 1 - 1 f norm = 2 e 2 f ühtl = 2 f eksp = e - x b-a 1) empiirilise jaotuse histogrammi graafik 2) hüpoteesile 4.1 vastava normaaljaotuse tiheduse ja sellele vastava hüpoteetilise histogrammi graafik 3) hüpoteesile 4.2 vastava eksponentjaotuse tiheduse ja sellele vastava hüpoteetilise histogrammi graafik 4) hüpoteesile 4.3 vastava ühtlase jaotuse tiheduse ja sellele vastava hüpoteetilise histogrammi graafik Kõik graafikud koos: 6. Graafikute koostamine: 1) empiirilise jaotusfunktsiooni graafik.
Haridus- ja Teadusministeerium Võrumaa Kutsehariduskeskus Puidutehnoloogia PTo-07 Andres Kooser Praktiline töö Vineeri tootmine Juhendaja: Taivo Tering Väimela 2010 1 Vineeri tootmine. Metoodiline juhend praktiliste tööde teostamiseks. Vineer kujutab endast treispoonilehtede kokkuliimimisel saadud kihilist materjali. Sõltuvalt kasutatavast liimi tüübist jagatakse vineer kahte gruppi: a) fenoolformaldehüüdliimide baasil valmistatud kõrgendatud veekindlusega vineer. b) karbamiidformaldehüüdliimide baasil valmistatud keskmise veekindlusega vineer. Käesolevas praktiliste tööde juhendis on toodud vineeri valmistamise tehnoloogiliste operatsioonide loetelu, toorainekoguse arvutamise metoodika ning seadmete valiku ja arvutuse alused. Praktiliste tööde koosseisu kuuluvad veel joonised: a) spooni valmistamise jaoskonna
Time Channel 1 Seconds °C 0 12,62 1 12,6 24 2 12,57 22 3 12,53 4 12,5 20 5 12,47 18 16 6 12,43 14 7 12,4 12 8 12,36 10 9 12,33 t,C 8 10 12,29 11 12,26 6 12 12,24 4 13 12,2 14 12,16 2 15 12,13 0 16 12,1 0 200 400 600 800 1000 1200 14 17 12,07 -2 18 12,03 19 12 -4 20 11,
4 kui pinnaseveetase on külmumissügavusele kapillaartõusu kõrgusest lähemal. Migreeruva vee hulk sõltub pinnase veejuhtivusest. Seepärast on kõige külmatundlikumad keskmise terasuurusega pinnased, milles kapillaartõusu kõrgus ja veejuhtivus on suhteliselt suured. Paljudest külmatundlikkuse hindamise kriteeriumitest on joonisel 4.4 esitatud Casagrande graafik ja Soome uurimustel (Friberg, Slunga 1989) põhinev lühendatud tabel 4.1. Pinnased, mis ei jää tabeli 4.1 piiridesse, vajavad eriuuringuid. Külmakindlas pinnases ei sõltu vundamendi süvis Tabel 4.1 Pinnase külmatundlikus Plastsusarv Voolavuspiir Voolavusarv Kapillaartõusu Külmatundlikkus Pinnaseliik Ip % wL % IL kõrgus m
51- Omanik/FI 10- E või ev Pm.maa, 12-Pm.maa, juht 1 - omandis, 11-Pm.maa, ühiskasutuse Maakasutus v_toojou_a jrk Aasta 5_Maakond ha renditud, ha s, ha kokku astauhik X1 X3 X4 X5 X6 X7 X8 1 2000 Jõgeva 0,00 2 177,00 0,00 2 177,00 0,00 2 2000 Jõgeva 0,00 872,00 0,00 872,00 0,00 3 2000 Jõgeva 46,70 38,00 0,00 84,70
Tallinna teeninduskool Suurköögi eksam Rühmatöö, grupp 1 Juhendaja: Kristi Tiido Koostajad: Reelika Oissar, Helen Paju, Ants Morel, Maksim Odnenko, Britta Luup Tallinn 2014 2 Sisukord Sisukord ..................................................................................................................................... 3 Idee .............................................................................................................................................4 Toidud......................................................................................................................................... 5 Koorene lõhesupp..............................................................................................................
6. ELEKTRIAJAMITE ÜLESANDED Tootmises kasutatakse töömasinate käitamiseks rõhuvas enamuses elektriajameid. Ka pneumo- ja hüdroajamid saavad oma energia ikka elektrimootoritega käitatavatelt kompressoritelt ja hüdropumpadelt. Elektriajam koosneb elektrimootorist ja juhtimissüsteemist, mõnikord on vajalik veel muundur ja ülekanne. Elektriajamite kursuse põhieesmärk on valida võimsuse poolest otstarbekas elektrimootor, arvestades ka kiiruse reguleerimise vajadust ja võimalikult head kasutegurit. Järgnevad ülesanded käsitlevad selle valikuprotsessi erinevaid külgi. 6.1. Rööpergutusmootori mehaaniliste tunnusjoonte arvutus Ülesanne 6.1 Arvutada ja joonestada rööpergutusmootorile loomulik ja reostaattunnusjoon. Mootori nimivõimsus Pn = 20 kW, nimipinge Un = 220 V, ankruvool Ia = 105 A, nimi- pöörlemissagedus nn = 1000 min-1, ankruahela takistus (ankru- ja lisapooluste mähised) Ra = 0,2 ja ankruahelasse on lülitatud lisatakisti takistu
konstantne) Nihe (teepikkus) ühtlaselt muutuval sirgjoonelisel liikumisel s = v 0 t+ 2 a t 2 3 Kiiruse sõltuvus ajast ühtlaselt muutuval sirgjoonelisel liikumisel v = v 0+ a t Kiirendus võib olla ka negatiivne, siis kiirus väheneb. v Kiirendus kiiruse muudu (v-v0) ja selleks kuluva aja (t-t0) jagatis a = t Tuletatud valem ühtlaselt muutuva liikumise kohta v