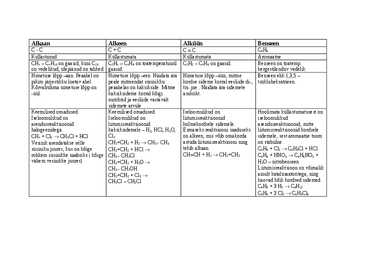
Alkeenide homogeenilises reas on esimesed 4 alkeeni gaasid, järgmised 5-17 on vedelikud ja alates 18-ndast on tahked ained. Süsiniku arvu kasvu ja vesinike arvu vähenemisega suureneb tihedus ja keemistemperatuur, sulamistemperatuur väheneb. Alkeenid on vees vähelahustuvad ja väga iseloomuliku lõhnaga. Keemilistest omadustest on iseloomulikud põlemine (leek on nähtav, kuna süsinik ei põle täielikult ära) ning liitumisreaktsioonid. Hüdrogeenimine on liitumisreaktsioon vesinikuga (H2), hüdraatimine on liitumisreaktsioon veega (H2O). Dehüdrogeenimine on vesiniku, dehüdrautimine on vee eraldumine. Alkadieenides on süsinike vahel kaks kaksiksidet. Täielik põlemine: C2H4 + 3O2 2CO2 + 2H2O Mittetäielik põlemine: C2H4 + 2O2 CO2 + 2H2O + C Halogeenidega (VIIA): CH2 = CH2 + Br2 CH2Br CH2Br Vesinikhalogeenidega: CH2 = CH2 + HCl CH3 CH2Cl Hüdrogeenimine: CH2=CH2 + H2 CH3 CH3 Hüdraatimine: CH2 = CH2 + H2O CH3 CH2OH (H rohkem H-d)
sidemest ning selliselt seotud süsiniku aatomid on tasandilised. Kaksikside käitub nagu nukleofiilne tsenter. Seda ründavad elektrofiilid. Küllastumata ühendite reaktsioonid algavadki elektrofiili ühinemisega, millele järgneb nukleofiilseosakese ühinemine. Küllastumata ühenditega liituvad halogeenid, vesinikhalogeenid, vesi (hapekatalüütiliselt), vesinik (katalüsaatori abil). Kolmikside on -side + kaks -sidet. Kaksik- või kolmikside on nukleofiilne tsenter. Liitumisreaktsioon küllastumata ühendiga algab elektrofiilse osakese ühinemisega. Küllastumata ühendid on ühendid, kus süsiniku aatomite vahel esineb kahekordne side ehk kaksikside või kolmekordne side ehk kolmikside. Esimesed neist kaanavad nime alkeenid (nimetuse lõpp een), teised nime alküünid (nimetuse lõpp üün). Nimetused antakse lähtuvalt süsiniku aatomite arvust, kordse sideme asukoht määratakse ära selle süsiniku järgi, mille järel ta asub. CH 2=CH
Kaksikside on keemiline side, kus on ühinenud kaks elektronpaari.Kaksikside kuulub kovalentsete sidemete hulka. Kolmikside on keemiline side, kus on ühinenud kolm elektronpaari.Kolmikside kuulub kovalentsete sidemete hulka. Alküülimine on alküülrühmaga asenduse teostamine. Fenoolid (ka hüdroksüareenid) on aromaatsed ühendid, milles üks või mitu benseenituuma kuuluvat süsinikuaatomit on seotud hüdroksüülrühmaga. Hüdraatimine on keemiline liitumisreaktsioon veega. Dehüdrogeenimine on vesiniku eraldumine keemilise reaktsiooni käigus. Aromaatne ühend orgaaniline ühend, mille molekulis sisaldub aromaatne tsükkel. Heterotsükliline ühend aine, mille molekul sisaldab hüdroksüülrühma. Delokalisatsioon elektronide või laengute jaotumine(,,laialimäärimine'') aatomite vahel.
Küllastumata süsivesinikud. II poolaasta tasemetöö kordamiseks Küllastumata süsivesinik- süsiniku aatomite vahel võib esineda kaksik- või kolmiksidet. Alkeen- süsiku aatomite vahel kaksiksidemed een, Eteen C2h4. Alküün- süsiniku aatomite vahel kolmiksidemed üün, Etüün C2H2. Hüdrogeenimine- vesiniku molekuli liitmine keemilise reaktsiooni käigus. Hüdraatimine- keemiline liitumisreaktsioon veega. Nitreerimine- nitrorühma (NO2) viimine orgaanilise ühendi koostisse. Benseeni füs omadused- värvusetu, veest kergem, iseloomuliku lõhnaga vedelik, vees ei lahustu, lahustub bensiinis ja etanoolis. Karbonüülühendid- sisaldavad karbonüülrühma ehk süsinikku, mis on kaksiksidemega seotud hapniku külge. Aldehüüdid- keemilised ühendid, mis sisaldavad põhilise funktsionaalse rühmana aldehüüdrühma (CHO), Pentanaal, aal. Ketoonid- ühendid, milles karbonüülrühm
eteen Alkeenidel esineb isomeeria: 1) Kaksiksideme asukoha muutusest H3C H2C HC = CH2 -> H3C HC = CH - H3C 2) Süsivesinikahela lagunemisel H3C H2C HC = CH CH3 -> 3) Tsükliliste struktuuride ühendite tekkest Keemilised omadused eteeni näitel: C2H4 -> H2C = CH2 1) Põlemine C2H4 + 3O2 -> 2CO2 + 2H2O 2) Astuvad liitumisreaktsioon a) Br2 -> H2C = CH2 + Br2 -> CH2 BrCH2 Br b) HCl -> H2C = CH2 + HCl -> CH3CH2Cl c) H2O -> H2C = CH2 + H2O -> CH3CH2OH 3) Hüdrogeenimine H2C = CH2 + H2 -> CH3CH3 4) Võivad oksüdeerida (KMnO4 toimel) diool aldehüüd NB! H2 ühinemine hüdrogeenimine, H2 eemaldumine dehüdrogeenimine.
lahus, milles rohkem pole võimalik ainet lahustada. · Lahustuvus suspensioon · Emulsioon · Vaht · Aerosool · Elektrolüüt aine, mille lahus juhib elektrivoolu. Tema elektrijuhtivus põhineb vabade ioonide liikumisel. · Mitteelektrolüüt aine, mis ei juhi elektrit. · Elektrolüütiline dissotsatsioon · Hüdraatumine keemiline liitumisreaktsioon veega. · Dissotsatisoonimäär · Neutralisatsioon happe ja aluse vaheline reaktsioon, mille saadused on sool ja vesi. · Soola hüdrolüüs 2. Oska eristada : · Elektrolüüte ja mitteelektrolüüte · Tugevaid ja nõrku elektrolüüte 3. Oska kirjutada elektrolüütilise dissotsiatsiooni võrrandeid ja neid ülesannetes kasutada. 4. Vahetusreaktsioonide toimumise tingimused !!! 5
polaarseks reagendiks on tavaliselt oksoühend ise ja ühe karbonüülse kaksiksideme katkemisel vabanenud valentsid küllastatakse teise samasuguse molekuli fragmentidega. Tavaline liitumisreaktsioon. Töö käik Kõigepealt atsetofenoon, mis kujutas endast Friedel Craftsi reaktsiooni O O + o CH3 O CH3 + H3C 2 OH Siis bensaalatsetofenoon: Aparatuur 5 6 5 6 4 7 4 7
süsiniku juures, kus on kõige CH2=CH2 + HCl tekib alkaan. C6H6 + Cl2 C6H5Cl + HCl rohkem süsinikke naabriks ( kõige CH3 - CH2Cl CHCH + H2 CH2=CH2 C6H6 + HNO3 C6H5NO2 + vähem vesinikke juures) CH2=CH2 + H2O H2O nitrobenseen CH3 - CH2OH Liitumisreaktsioon on võimalik CH2=CH2 + Cl2 ainult katalüsaatoritega, ning CH2Cl CH2Cl kaovad kõik kordsed sidemed. C6H6 + 3 H2 C6H12
kaksik- või kolmiksidemed. Nimeta eteeni ja etüüni füüsikalisi omadusi. Eteen! Molekulvalem: C2H4 lihtsaim alkeen värvusetu nõrk meeldiv lõhn narkootilise toimega gaas saadakse nafta töötlemisel Etüün Molekulvalem: C2H2 lihtsaim alküün ,värvusetu,meeldiva lõhnaga ,narkootiliste omadustega gaas toodetakse metaanist kõrgtemperatuurilise pürolüüsi teel Mis on hüdraatimine, nitreerimine, hüdrogeenimine? Hüdraatimine - on liitumisreaktsioon veega (H2O) Nitreerimine on nitrorühma (NO2) viimine orgaanilise ühendi koostisse temasse lämmastikoksiidide või nitreerimisseguga toimides. Hüdrogeenimine on vesiniku molekuli liitmine keemilise reaktsiooni käigus Nimeta benseeni füüsikalisi omadusi. värvitu, iseloomuliku lõhnaga (mürgine!), vees lahustamatu, on ise hea lahusti lahustab hästi rasvu ja muid hüdrofoobseid aineid. Mis on alkeenid ja alküünid? Seleta mõisted ja too iga rühma kohta üks näide.
Keemia referaat Pentadieen Liisi Tari 11b klass Valga Gümnaasium 2008 Sisukord Tiitelleht.........................................................................................................................1 Sisukord..........................................................................................................................2 Sissejuhatus....................................................................................................................3 Alkadieenide jagunemine...............................................................................................4 Alkadieenide saamine.....................................................................................................5 Alkadieenide ehitus........................................................................................................6 Alkadie...
Nahale sattumisel tekib päevitus. -kiirgus on elektromagnetlaine voog, mis levib valguskiirusel. Koosneb elektromagnetvälja kvantidest, millel on väga suur energia. On väga suure läbitungimisvõimega, kiirguse eest kaitseb spetsiaalne varjend . Tuumareaktsioonides tekivad uued keemilised elemendid, isotoobid. Neid kasutatakse peamiselt looduses mitteesinevate isotoopide tootmiseks.Kui tuuma satub neutron, siis muutub tuuma massiarv ühe võrra ja tekib uus isotoop. Kergete tuumade liitumisreaktsioon on termotuumareaktsioon. Termotuumareaktsioonideks on vaja ülikõrget temperatuuri, kuna tuumade ühinemisel peavad tuumad ületama elektrilised tõukejõud ja seda saab teha kiiruse abil, kuid mida suurem on kiirus, seda kõrgem on ka temperatuur. Maa peal ei saa termotuuma reaktsioone tekitada. Päikese ja tähtede energiaallikas on termotuumareaktsioon. Isotoopideks nimetatakse ühe elemendi erineva massiarvuga tuumi. Näiteks tehneesium ja promeetium ja plutoonium
· Rasvad on glütseriini ehk propaantriooli ja kõrgemate karboksüülhapete(rasvhapete) estrid, mille olek toatemperatuuril on tahke. Elusorganismid kasutavad rasvades valdavalt paarisarvu süsinikega (kuni 20) rasvhappeid. Kõrgemate karboksüülhapete estrid, mille olek toatemperatuuril on vedel, on õlid. · Rasvhapped on kas 16 või 18 süsinikulised, ning kas tegemist on õlide või tahkete rasvadega vaadatakse kordseid sidemeid. Kui rasvhappes esineb kordne süsiniksüsinik side, siis on tegemist õliga. · Rasvad on värvuseta, lõhnata, maitseta, vedelad või tahked ained, mis vees ei lahustu. · Rasvade olek sõltub rasvhappe radikaalist s.t. küllastunud radikaali puhul (kõik üksiksidemed) on rasv tahke ja küllastumata radikaali puhul (vähemalt 1 kaksikside) on rasv vedel õli. · Loomsed rasvad on tahked, välja arvatud hülge ja vaalarasv. · Looduslike rasvade vä...
Fenoolide eripära põhjuseks on hüdroksürühma ja aromaatse tsükli vastastikmõju. Tänu sellele on fenool happelisem kui alkohol. 8.Aromaatsete amiinide ja alküülamiinide aluselisuse võrdlus. 9.Benseeni, fenooli ja aniliini reaktsioonivõime võrdlus. 10.Reaktsioonivõrrandid: TV ül. 8 /58 + vihikus. areeni täielik oksüdeerumine (põlemine) benseen / aniliin / fenool + broom / lämmastikhape / halogeeniühend benseeni liitumisreaktsioon vesinikuga / halogeeniga fenool + leelis alküülbenseeni oksüdeerimine 11.Areenide leidumine ja kasutamine. Areene toodetakse naftast ja kivisöetõrvast. Kasutatakse lahustina ning teiste areenide saamiseks. 12.Aromaatsete ühenditega seotud keskkonnaprobleemid.
Fenoolide eripära põhjuseks on hüdroksürühma ja aromaatse tsükli vastastikmõju. Tänu sellele on fenool happelisem kui alkohol. 8.Aromaatsete amiinide ja alküülamiinide aluselisuse võrdlus. 9.Benseeni, fenooli ja aniliini reaktsioonivõime võrdlus. 10.Reaktsioonivõrrandid: TV ül. 8 /58 + vihikus. areeni täielik oksüdeerumine (põlemine) benseen / aniliin / fenool + broom / lämmastikhape / halogeeniühend benseeni liitumisreaktsioon vesinikuga / halogeeniga fenool + leelis alküülbenseeni oksüdeerimine 11.Areenide leidumine ja kasutamine. Areene toodetakse naftast ja kivisöetõrvast. Kasutatakse lahustina ning teiste areenide saamiseks. 12.Aromaatsete ühenditega seotud keskkonnaprobleemid.
värviaine) Kokkuvõte: Süsinikevahelist kaksiksidet sisaldavad ühendid on alkeenid, kolmiksidemega ühendid aga alküünid. Kaksikside käitub nagu nukleofiilne tsenter. Seda ründavad elektrofiilid. Küllastumata ühendite reaktsioonid algavadki elektrofiili ühinemisega, mille järgneb nukleofiilse osakese ühinemine. Küllastumata ühenditega liituvad halogeenid, vesinikhalogeeniidid, vesi, vesinik. Alkeenid ja alküünid on küllastumata ühendid. Kordne side on nukleofiilne tsenter. Liitumisreaktsioon küllastumata ühendiga algab elektrofiilse osakese ühenemisega.
Kristalse org aine süntees, puhastamine ja uurimine: · Dibensalatsetoon (C17H14O) ei ole mürgine (väikestes kogustes) ja kasutatakse laialdaselt päikesekreemide koostisainena. · Kondensatsioonireaktsioon kujutab endast niisugust liitumist oksoühendiga, kus polaarseks reagendiks on tavaliselt oksoühend ise ja ühe karbonüülse kaksiksideme katkemisel vabanenud valentsid küllastatakse teise samasuguse molekuli fragmentidega. Tavaline liitumisreaktsioon. · Aldoolkondensatsiooniks nimetatakse kondensatsiooni, kui reaktsioon lõpeb hüdroküaldehüüdi või -ketooni moodustumisega. Katalüüsivad alused. Klassikaline aldoolkondensatsioon toimub tavaliselt kahe ühesuguse aldehüüdi molekuli vahel, kahe ühesuguse ketooni molekuli vahel või ühe aldehüüdi ja ühe ketooni molekuli vahel. Ümber kristallimine: · Kristalsete orgaaniliste aine puhastamiseks kasutatakse tihti ümberkristallimist.
5. Hüdrogeenimine- on vedelate õlide töötlemine kõrge rõhu ja temperatuuri juures vesinikuga. Sealjuures saavad küllastumata rasvhapetest küllastunud rasvhapped. Hüdratatsioon- veega ühildumine Dehüdratatsioon- veest eraldumine Dehüdrogeenimine- Hüdrogeenimise pöördprotsess e. Vesiniku ära võtmine Polümerisatsioon- küllastumata ühendite liitumisreaktsioon , mille tulemusena moodustub sama koostise, kuid suurema molekulimassiga aine. Kopolümerisatsioon- kui polümeeritakse mitme erineva monomeeri segu. Kondensatsioon- aine ülemineks gaasilisest olekust vedelasse (või tahkesse), liitumisreaktsioon, millega kaasneb mõne lihtsa aine nt. vee eraldumine. Vulkaniseerimine- pikad lineaarsed polümeeriahelad ühendatakse sillakestega omavahel ruumiliseks struktuuriks, mis annab materjalidele paremad mehaanilised omadused ja
2) pii-side: kahe p-orbitaali kattumisel kahes ruumiosas (alkeenid) (brutoreaktsiooni) olemuse kirjeldus kõikide üksteisele järgnevate elementaarreaktsioonide kaudu. · Reaktsioonid: · Lewise definitsioonid: hape elektronpaari aktseptor; - liitumisreaktsioon: a + b = c alus- elektronpaari doonor - elimineerimisreaktsioon: a = b + c - asendusreaksioon: a-b + c-d = a-c + b-d (lähteainete rühmad · Happed on seda tugevamad, mida hoolsamalt nad prootoneid vahetavad kohti) loovutavad ja mida vähem tekkinud anioon seda tagasi liita soovid.
oksüdeeruvad. IA → leelismetallid →väliskihil 1 elektron → o -a. alati I. N. Na2O, K2SO4, LiOH II A → leelismuldmetallid→väliskihil 2 elektroni → o.-a. alati II. N. CaO, CaCl2, Ba(OH)2 III A väliskihil 3 elektroni → o.-a. alati III. N. Al2O3, Al(OH)3 Üljäänud metallide o.-a. on muutuv. Näit. Sn ja Pb - II ja IV; Fe - II ja III; Cu I ja II Keemilised omadused: 1.metallid reageerivad aktiivsete mittemetallidega. toimub liitumisreaktsioon, mis on ühtlasi redoksreaktsioon a) metall+ O2 → oksiid. N. 2Mg +O2 → 2MgO Mg -2e → Mg2+ O +2e → O2- b) metall + halogeen (F2 Cl2 Br2 I2 ) →´ vesinikhalogeniidhapete sool N. Ca + Cl2 →CaCl2 2 2Fe+ 3Cl2 → 2FeCl3 Fe -3e → Fe3+ Cl +1e →Cl- c) metall + väävel S → divesiniksulfiidhappe H2S sool N.Fe + S →FeS Fe-2e → Fe2+ S + 2e → S2- 2.metallid reageerivad liitainetega, toimub asendusreaktsioon vastavalt metallide aktiivsuse reale (pingerida)
AINE EHITUS JA KEEMILINE SIDE • metall + mittemetall → iooniline side → ioonivõre → mittemolekulaarne •metall lihtainena → metalliline side → metallivõre → mittemolekulaarne •mittemet + mittemet → kovalentne polaarne side →aatomvõre → mitte molekulaarne •mittemetall lihtainena → kovalentne mittepolaarne side →molekulvõre →molekulaarne •Keemilise sideme tekkel eraldub energia, molekulide või kristallide energia on madalam kui üksikaatomitel. Liitumisreaktsioon → eksotermiline → energia neeldub ∆H<0 Lagunemine → endotermiline → energia eraldub ∆H>0 (kõik oksüdatsioonid) •Vesinikside F-H, O-H, N-H on nõrgem kui kovalentne side, kuid tugevam kui tavaline molekulide vaheline side. Põhjustab ainete sulamis- ja keemistemperatuuri tõusu, soodustab lahustamisprotsessi molekulide vahel. •lihtaine, liitaine – ELEMENT Puhas aine, segu – AINE KEEMILISE REAKTSIOONI KIIRUS JA TASAKAAL TASAKAAL Te...
Rasvad Mõiste Rasvad on glütseriini ehk propaantriooli ja kõrgemate karboksüülhapete (rasvhapete) estrid, mille olek toatemperatuuril on tahke. Elusorganismid kasutavad rasvades valdavalt paarisarvu süsinikega (kuni 20) rasvhappeid. Kõrgemate karboksüülhapete estrid, mille olek toatemperatuuril on vedel, on õlid. Rasvhapped on kas 16 või 18 süsinikulised, ning kas tegemist on õlide või tahkete rasvadega vaadatakse kordseid sidemeid. Kui rasvhappes esineb kordne süsinik-süsinik side, siis on tegemist õliga. · Pika C-ahelaga (sagedamini 12 26) monokarboksüülhapped · Sisaldavad enamasti paaris arvu C-aatomeid · Küllastunud või küllastumata C-ahel · Küllastumata rasvhapped reeglina cis-isomeerses vormis 3 tähtsamat rasvhapet: 1) Palmitiinhape ehk palmithape on sageli loomades ja taimedes leiduv rasvhape. Aine keemiline valem on CH3(CH2)14COOH. ...
Karbonüülrühma hapnikul asub nukleofiilne tsenter ning süsinikul elektrofiilne tsenter. Karbonüülühendite omadused: Füüsikalised omadused: 1. Kergesti keevad vedelikud. 2. Ei moodusta vesiniksidet, sest seal ei ole -OH rühma ega -NH2, seega ei lahustu vees. 3. Väikesed molekulid lahustuvad küll nt. etanaal. OK Keemilised omadused: | 1. Liitumisreaktsioon CH3CH2CH2K + CH3CHO CH3 C H | CH2CH2CH3 2. Hõbepeegli reaktsioon aldehüüdide oksüdeerumine (tekib karboksüülhape), saab teha kindlaks, kas aine on aldehüüd või mitte. (NB! Reaktsioon ainult aldehüüdidega) Ag2O + HCHO HCOOH + 2Ag
miljardit aastat, pool on elatud. Kui Päike on muutunud Punaseks Hiiuks, hakkab järgnevalt toimuma tema kokkutõmbumine planeedi suuruseks. Järgnevalt tekib Pruun Kääbus. Termotuumapomm koosneb aatom- ja vesinikpommist. Vesinikpommi südamikus on tavaline lõhustumistuumapomm. Selle lõhkamisel tekib ülikõrge temperatuur, mis käivitab termotuumareaktsiooni. Termotuumakütust (LiD) saab paigutada pommi kuitahes palju, suurendades niiviisi pommi võimsust. Kergete tuumade liitumisreaktsioon on termotuumareaktsioon. Selle tekitamiseks on vaja ületada jõud nende osakeste vahel, mis toimub temperatuuril 10 8°C. A 4 A- 4 A aatommass (prootonite ja neutronite summa) Z X 2 He+ Z - 2Y Z järjekorra number (prootonite arv tuumas, elektronide arv A 0 A
Tallinn Tehnikaülikool Lõputöö protokoll Dibensaalatsetoon atsetoonist Liisi Kink 095675 YAGB 22 Tallinn 2010 Etapp 1 Atsetoon Sissejuhatus Üldiselt käsitletakse keemias oksüdeerimisena nähtust, kus element loovutab elektrone. Orgaanilises keemias käsitletakse oksüdeerimisena iga protsessi, mis põhjustab süsiniku elektrontiheduse vähenemist. Alkoholide osalisel oksüdatsioonil erinevate reagentide toimel oksüdeerub primaarne alkohol esmalt karbonüülühendiks ja seejärel karboksüülhappeks. Sõltuvalt sellest, kas on tegu primaarse või sekundaarse alkoholiga, saame esmaseks reaktsiooniproduktiks vastavalt kas aldehüüdi või ketooni. Aldehüüdid võivad edasi oksüdeeruda karboksüülhapeteni, ketoonid neid tingimustes ei oksüdeeru. ...
Tsükloalkaane leidub mõnede leiukohtade naftas. II FÜÜSIKALISED OMADUSED Tsüklopropaan on normaaltingimustel gaas, tsüklobutaan madala keemistemperatuuriga vedelik, järgmised homoloogid on vedelikud ning suurema molekulmassiga tsükloalkaanid on tahked. Tsükloalkaanide keemistemperatuurid on umbes 10oC võrra kõrgemad kui sama süsiniku aatomite arvuga alkaanid. III KEEMILISED OMADUSED 1. Tsüklopropaanile, tsüklobutaanile ja tsüklopentaanile a) liitumisreaktsioon H2-ga. + H2 CH3 CH2 CH3 b) liitumisreaktsioon halogeeniga (+) + Cl2 CH2Cl CH2 CH2 CH2Cl c) liitumisreaktsioon vesinikhalogeniidiga (HCl; HBr) + HCl CH3 CH2 CH2Cl 2. Tsükloheksaan Cl a) + Cl2 + HCl asendusr. klorotsükloheksaan. b) + 3H2 3. Tsükloalkaanid põlevad täielikult C3H6 + 4,5O2 3CO2 +3H2O IV KASUTAMINE Tsüklopropaani kasutatakse meditsiinis valuvaigistina.
Tsükloalkaane leidub mõnede leiukohtade naftas. II FÜÜSIKALISED OMADUSED Tsüklopropaan on normaaltingimustel gaas, tsüklobutaan madala keemistemperatuuriga vedelik, järgmised homoloogid on vedelikud ning suurema molekulmassiga tsükloalkaanid on tahked. Tsükloalkaanide keemistemperatuurid on umbes 10oC võrra kõrgemad kui sama süsiniku aatomite arvuga alkaanid. III KEEMILISED OMADUSED 1. Tsüklopropaanile, tsüklobutaanile ja tsüklopentaanile a) liitumisreaktsioon H2-ga. + H2 CH3 CH2 CH3 b) liitumisreaktsioon halogeeniga (+) + Cl2 CH2Cl CH2 CH2 CH2Cl c) liitumisreaktsioon vesinikhalogeniidiga (HCl; HBr) + HCl CH3 CH2 CH2Cl 2. Tsükloheksaan Cl a) + Cl2 + HCl asendusr. klorotsükloheksaan. b) + 3H2 3. Tsükloalkaanid põlevad täielikult C3H6 + 4,5O2 3CO2 +3H2O IV KASUTAMINE Tsüklopropaani kasutatakse meditsiinis valuvaigistina.
süsinikskelett pole muutunud. Lewise struktuurid näitavad sidemete ja vabade elektronpaaride ligikaudset paiknemist molekulis. Lihtsamate ja keerukamate molekulide kuju kirjeldamiseks antakse sidemepikkused, nurgad sidemete vahel , nurgad tasandite vahel. Nomenklatuur: 1) trivaalsed nimetused(uurea); 2) pooltrivaalsed nimetused(atsetoon) ; 3) süstemaatilised nimetused (IUPAC) (etaanhape); Vt harjutustunni vihik Brutoreaktsioonide tüübid o Liitumisreaktsioon kahest reagendist tekib uus aine o Elimineerimisreaktsioon - Üks reagent laguneb, andes kaks produkti. o Asendusreaktsioon kaks reagenti vahetavad üksikuid osi, andes kaks uut produkti o Ümberasetusreaktsioon ühe reagendi sidemete ja aatomite ümberpaigutuse tulemusena moodustub teine, esimesega võrrelde isomeerne produkt Reaktsioonimehhanism kirjeldab: o Millised sidemed katkevad, tekivad
Nukleofiilse asendusreaktsiooni korral: nukleofiil on ründav osake, reaktsioonitsenter on elektrofiilne tsenter, lahkuv rühm eraldub nukleofiilina. Elektrofiilse asendusreaktsiooni korral: elektrofiil ründab nukleofiilset reaktsioonitsentrit,lahkuv rühm eraldub elektrofiilina.(isel. aromaatsele tuumale- halogeenimine, nitreerimine jne) Elimineerimisreaktsioonid: kui nukleofiil käitub alusena,rebides molekulist ära prootoni. R-Hal + NaOH R-OH + NaHal Elektrofiilne liitumisreaktsioon kaksiksidemele: Ühinemisreaktsionil liitub elektrofiilne osake (prooton) kordse sideme selle C-ga, millega on seotud rohkem vesinikke, nukleofiilne osake (Hal- või OH-) selle C-ga, mille juures on rohkem C-C sidemeid. 7. Nomenklatuurisüsteemid, orgaanilisele ühendile nime andmise põhimõtted. Nomenklatuurisüsteemid: *Ratsionaalse nomenklatuuri-süsteemi võimalused suhteliselt piiratud. *Universaalne süstemaatiline nomenklatuur, kooskõlas IUPAC-i reeglitega e. nn. Genfi
vesinikust ja hapnikust, kus enamusel juhul vesiniku ja hapniku vahekord on (H2O)n Glükoos valge suhkur Fruktoos puuviljasuhkur Valgud on looduslikud kõrgmolekulaarsed ühendid, mille molekuli koostisesse kuulub C, H, O ja N. Valgud koosnevad aminohapete jääkidest, mis on omavahel seotud peptiidsidemega. Aminohape- NH2 Aminohape - 2-aminobutaanhape 10 Reaktsioonitüübid: 1. Ühinemisreaktsioon ehk liitumisreaktsioon on reaktsioon, kus kahest või enamast lähteainest tekib üks uus aine. 2 Ca + O2 = 2 Ca O 2. Lagunemisreaktsioon on reaktsioon, kus ühe aine lagunemisel tekib kaks või enamat uut ainet Ca CO3 = Ca O + CO2 (kuumutamine) 3. Asendusreaktsioon on reaktsioon, kus lihtaine aatomid asenduvad liitaine koostisesse kuuluva teise elemendi aatomiga Zn + 2H Cl = Zn Cl2 + H2 4. Vahetusreaktsioon on reaktsioon, mis toimub kahe liitaine vahel ja mille
2H (deuteerium)(1pr, 1ne) 3)p(+)-><-n= 21D(deuteerium) 4)p&n-><-p&n=21D+21D tekivad kõik elemendid kuni rauani Termotuumapomm koosneb aatom- ja vesinikpommist. Vesinikpommi südamikus on tavaline lõhustumistuumapomm. Selle lõhkamisel tekib ülikõrge temperatuur, mis käivitab termotuumareaktsiooni. Termotuumakütust (LiD) saab paigutada pommi kuitahes palju, suurendades niiviisi pommi võimsust. Kergete tuumade liitumisreaktsioon on termotuumareaktsioon. Selle tekitamiseks on vaja ületada jõud nende osakeste vahel, mis toimub temperatuuril 108°C. VESINIK(TERMOTUUMA)POMM- Külma sõja ajal katsetati. Vaja ülisuurt energiat tuumapommi plahvatust (soojus+neutronid-suur energia), kasutatakse LiD vahelist reaktsiooni (Li-tahke, hea transport. D-gaas) - kallis -energia mis vabaneb on tohutu TULEVIK- Suur projekt kasut. termotuuma reakts. Tehisting. (jaapan/FRA?) 1
kõrvaahelaks. Alfa-süsiniku küljes peab olema ka vähemalt üks vesinik? α-süsinik – molekuli tähtsaimale karbonüülrühmale järgnev süsinik? 20 aminohappe struktuurid – [Pilt]. Liigitus kõrvalahela omaduste alusel – aminohapete kõrvaahelad võivad olla kas mittepolaarsed, polaarsed, aromaatsed, positiivse laenguga (aluselised) või negatiivse laenguga (happelised). Aminohapete neelduvus UV alas Kondensatsioonireaktsioon – liitumisreaktsioon, mille käigus eraldub vesi. Nt. aminohapete, suhkrujääkide jms liitumine üksteisega. Resonantsstruktuur – ühend või tema osa, kus esinevad nn. pooleteisekordsed sidemed; “liikuvad” elektronid, mis liiguvad kas mööda tsüklit ringi või kahe lähedal oleva elektronegatiivse aatomi vahel (keskel vähem elektronegatiivne aatom) vms. Asjaga seotud sidemed on lühemad kui “normaalsed” üksiksidemed, kuid pikemad kui kaksiksidemed.
1.Aatomi ehituse kvantitatiivse teooria loomisel, mis võimaldaks selgitada aatomite spektrite seaduspärasusi, avastati uued mikroosakeste liikumise seadused kvantmehaanika seadused. Thomsoni mudel oli esimene välja pakutud aatomimudel. Thomson oletas, et positiivne laeng täidab ühesuguse tihedusega kogu aatomi ruumala. Lihtsaim aatom, vesiniku aatom, kujutab endast positiivselt laetud kera raadiusega umb 10 astmel -8cm, mille sees asub elektron. Keerukamates aatomites asub positiivselt laetud kera sees mitu elektroni. Aatom sarnaneb keeskiga, milles rosinate rollis on elektronid. Rutherfordi katsed. Elektronide mass on aatomite massist tuhandeid kordi väiksem. Kuna aatom on tervikuna nautraalne, siis langeb järelikult aatomi massi põhiosa aatomi positiivsele laengule. Ta soovitas aatomi positiivse laengu uurimiseks aatomi sondeerimist alfaosekestega, need tekivad raadiumi ja mõnede teiste keemiliste elementide radioaktiivsel lagunem...
Alkeenide homogeenilises reas on esimesed 4 alkeeni gaasid, järgmised 5-17 on vedelikud ja alates 18-ndast on tahked ained. Süsiniku arvu kasvu ja vesinike arvu vähenemisega suureneb tihedus ja keemistemperatuur, sulamistemperatuur väheneb. Alkeenid on vees vähelahustuvad ja väga iseloomuliku lõhnaga. Keemilistest omadustest on iseloomulikud põlemine (leek on nähtav, kuna süsinik ei põle täielikult ära) ning liitumisreaktsioonid. Hüdrogeenimine on liitumisreaktsioon vesinikuga (H2), hüdraatimine on liitumisreaktsioon veega (H2O). Dehüdrogeenimine on vesiniku, dehüdrautimine on vee eraldumine. Alkadieenides on süsinike vahel kaks kaksiksidet. Täielik põlemine: C2H4 + 3O2 2CO2 + 2H2O Mittetäielik põlemine: C2H4 + 2O2 CO2 + 2H2O + C Halogeenidega (VIIA): CH2 = CH2 + Br2 CH2Br CH2Br Vesinikhalogeenidega: CH2 = CH2 + HCl CH3 CH2Cl Hüdrogeenimine: CH2=CH2 + H2 CH3 CH3 Hüdraatimine: CH2 = CH2 + H2O CH3 CH2OH (H rohkem H-d)
7. Valime näiteks tsüklopentaani saamise n-pentaanist: + H2 Need kaks ainet ei saa olla isomeerid, kuna nende atomaarne koostis on erinev. Vesiniku eraldumine molekulist on alati oksüdeerumisprotsess. Selles võid veenduda kui arvutate kummagi ühendi keskmise oksüdatsiooniastme (need on vastavalt 2,4 ja 2). 8. A. Üldisem reaktsioonitüüp on liitumisreaktsioon. B. Alkeenide reaktsioonid algavad elektrofiilse osakese või tsentri rünnakuga ühele süsinikule. C. Küllastumata ühenditega reageerivad vesinik, halogeenid, vesinikhalogeniidid, vesi ja hapnik. 13 9. 1) CH3 CH CH2 + H2 CH3 CH2 CH3 2) CH3 CH CH2 + Cl 2 CH3 CH CH2 Cl