Metaan Kaspar Kaare Markus Sepp Metaan Metaan ehk metüülhüdriid (molekulvalem CH4) on lihtsaim alkaan ja süsivesinik, küllastunud süsivesinike homoloogilise rea esimene liige. Metaani avastas ja isoleeris esimesena Alessandro Volta ajavahemikus 1776 1778, uurides Lago Maggiore soogaasi. Füüsikalised omadused Metaan on värvitu ja lõhnatu ning maitsetu gaas. Metaani molaarmass on 16,0425 g/mol. Metaani sulamistemperatuur -182,5 °C [1], keemistemperatuur -161,6 °C Metaani molekul on tetraeedrilise kujuga. Sidemenurgad on 109,5 kraadi. Süsiniku ja vesiniku aatomi vaheline kaugus on 108,70 pikomeetrit. Metaan on hüdrofoobne. Keemilised omadused Metaan põleb sinise leegiga. Tema leekpunkt on -188 °C, süttimistemperatuur +537 °C ja maksimaalne
Metaan ja kliima soojenemine Metaan ja kliimasoojenemine on temaatikad, mis on tänasel päeval igal juhul huvitavad ja aktuaalsed. Sellega käib kaasas ka palju erinevaid probleeme, millele oodatakse lahendusi. Suuremal osal Maa ajaloost on kliima olnud praegusest tunduvalt soojem. Küsimusele, kas tulevikus on taas oodata jääaega, võib väikese liialdusega vastata, et ei, ta juba ongi kohal. Jääaja asemel oleks siin õigem kasutada terminit külmhooneperiood
0 Aine iseloomustus CH4 metaan CO vingugaas CO2 süsihappegaas 1. Süsiniku oksüdatsiooniaste selles ühendis,ioonis molekulis. 2. Kas süsiniku ühend CH4+2O2CO2+2H2O 2CO+O22CO2 CO2+O2ei toimu reageerib hapnikuga ja kui reageerib siis võrrand 3
Metaan ja kliima soojenemine Metaan (CH4) on kasvuhoonegaas. Metaani keemilised omadused ja reaktsioonid atmosfääris põhjustavad kasvuhooneefekti. Atmosfääris imab metaan maalt tulnud infrapuna kiirgust, mis pääseks muidu maailmaruumi, mistõttu tekib maa atmosfääri soojenemine. Metaani eraldub maapõuest iseeneslikult, samuti moodustuvad väga suured metaanikogused biosfääri elutegevuse kõrvalsaadusena. Seepärast ei ole kogu kasvuhooneefekt tingitud üksnes inimtegevusest. Tööstusrevolutsiooni algusest on atmosfääri metaani sisaldus kahekordistunud, mõjutades kasvuhooneefekti suurenemist umbes 20% ulatuses.
Ch4 ehk metaan Lihtsain süsiniku ja vesiniku ühend. Leidub looduses, õhust kergem, ei lahustu vees ning on lõhna- ja maitsetu. Kasutatakse gaasilise kütusena. Segu õhust ja metaanist plahvatab kergesti. Aatomid seotud 4 kovalentse üksiksidemega. C keskel, Hd igas ilmakaares ümber. Metaan on teisisõnu maagaas. Tekib ka orgaanilise aine lagunemisel nt. Prügilates. Metaani põlemine Ch4 + 2 O2 --- Co2 + 2 H2O Mida suurem on oksüdatsiooniastme muutus, seda suurem on kütteväärtus. Selles võrrandis on süsiniku oa muutus 8 ja see on ka maksimaalne. Co ehk süsinik monooksiid ehk vingugaas Mittetäielik põlemine lõpeb vingugaasiga. Süsiniku oksüdatsiooniaste on siin 2. Co saab võimaluse korral oksüdeeruda edasi Co2ks. Co on neutraalne oksiid
docstxt/136241782249.txt
Karbonaadid mittelahustuvad karbonaadid lagunevad kuumutamisel, on ühendid, mis sisaldavad CO3-iooni, reageerivad hapetega, mille tulemusena eraldub CO2 Kaltsiumkarbonaat CaCO3 (paekivi, kriit, marmor) CaCO3 > CaO+CO2 Dolomiit MgCO3*CaCO3 kerge töödelda: MgCO3*CaCO3>MgO+CaO+2CO2 Kaltsiumvesinikkarbonaat: Ca(HCO3)2 Kuumutamisel: Ca(HCO3)2 > CaCO3+H2O+CO2 Söögisooda(NaHCO3+HCl) ja pesusooda (Na2CO3*10H2O) NaHCO3+HCl>NaCl+H2O+CO2 (uus sool+H2O+CO2 tekivad alati) Metaan CH4 (soogaas) Füüsikalised omadused: värvitu,lõhnatu,vees lahustumatu,õhust 2x kergem,toatemperatuuril gaas,keemistemp.-161kraadi , plahvatusohtlik, kergelt narkootilise toimega Keemilised omadused: *põleb CH4+2O2>CO2+2H2O täieliku põlemise saadused on süsiniku ja vesiniku ühenditel CO2 ja H2O *laguneb kuumutamisel CH4>C+2H2 (tahm) 2CH4>C2H2+3H2 Kasutamine: küttegaasina, lahustite tootmiseks (kloroform)
GRAFIIT: pehme-pliiatsites, määrdesegudes kõrge salamis temp.-raketi düüs, tiigel hea elektrijuht-elektroodides TEEMANT: ilus läige-ehted kõvadus-puurides, lihvimis pulbrites, klaasinoad 6.SÜSI(TEKE, KOOSTIS, KASUTAMINE, FÜÜSIKALISED OMADUSED). teke-orgaaniliste ainete kuumutamisel õhu juurde pääsuta omadused-poorne, ei lahustu üheski lahuses, hea elektrijuht, raskesti sulav kasutamine-meditsiinis koostis-koosneb grafiidist , C 7.METAAN: valem-CH4 ehitus- füüsikalised omadused(4)-värvusetu, lõhnatu, maitsetu, mürgine kasutamine(2)-kütus, tooraine põlemise võrrand-CH4+2O2->CO2+2H2O 8.SÜSINIKOKSIID: valem-CO rahvapärane nimetus-vingugaas füüsikalised omadused(4)-värvusetu gaas, lõhnatu, väga mürgine, vees eriti ei lahustu tekke võrrand-2C+O2->2CO keemilised omadused-põleb kasutamine(2)-metallide redutseerimine 9.SÜSINIKDIOKSIID: valem-CO2 tõestamine-põlev pird kustub
Tallinna Ülikool Matemaatika ja Loodusteaduste Instituut Triin Rannak ALKAANID JA NENDE KASUTAMINE: METAAN, ETAAN, PROPAAN Referaat Tallinn 2012 1 ALKAANID Alkaanide ehk küllastunud süsivesinike vahel on ainult üksiksidemed. [2] Alkaanid on ainult tetraeedrilisi süsinikke sisaldavad süsivesinikud. Igal alkaanil on oma nimetus, mõnel isegi mitu. Nimetused pandi kunagi juhuslikult, tihti saamisviisi või omaduste järgi ning need on triviaalsed nimetused. Keemikud kasutavad ise süstemaatilisi nimetusi
KEEMIA 1. Mõisted 1) süsivesinikud- keemilised ained, mille molekul koosneb ainult süsiniku ja vesiniku aatomitest. NT metaan- CH4 2) alkaanid- süsivesinik, mille molekul sisaldab ainult sigma-sidemeid. Nt: heksaan C6H14 3) alküülrühm- alkaanist tulenev asendusrühm. Nt. CH3- metüül 4) trivaalnimetus- aine (peamiselt ajalooline) nimetus, mis ei vasta nomenklatuuri reeglitele.Nt. Met(aan) 5) süstemaatiline nimetus- aine nimetus, mis on antud nomenklatuurireegleid järgides. Nt soogaas, süstemaatiline nimetus metaan(CH4)
Alkaanid on niisugused süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega. Mõnikord nimetatakse alkaane ka parafiinideks. · Metaani ja temaga sarnaste süsivesinike - alkaanide omadused muutuvad korrapäraselt süsiniku aatomite arvu suurenemisega molekulis. · Metaan ja temale järgnevad alkaanid erinevad üksteisest aatomite rühma - CH2 - võrra. Niisugust ühendite rida nimetatakse homoloogiliseks reaks. Rea üldvalem on CnH2n + 2 · Metaani homoloogilise rea 4 esimest ühendit on gaasid, viiendast kuni kuueteistkümnendani vedelikud ja kõrgemad on tahked ained. Molekulmassi kasvuga homoloogilises reas suureneb alkaanide tihedus ning kasvab sulamis- ja keemistemperatuur.
süsinikdioksiidi molekulil aega kaks sajandit Maad soojendada. See tähendab omakorda seda, et kui antropogeensed süsinikdioksiidi emissioonid täna lakkaksid, kuluks süsinikdioksiidi tööstusajastu eelse kontsentratsiooni (ja vastava globaalse keskmise õhutemperatuuri) taastumiseks umbes kaks sajandit. Maailmamere temperatuur stabiliseeruks tema suure soojusmahtuvuse tõttu alles aastatuhande möödudes alates ajast, kui süsinikdioksiidi emissioonid endisele tasemele langevad. CH4 metaan Metaani kontsentratsioon atmosfääris on märgatavalt madalam kui süsinikdioksiidi oma - 1770 ppb lähedal (ppb - parts per billion ehk osa miljardi kohta molaarse ainehulga põhjal, 1000 ppb = 1 ppm)[4]. Metaan on ühikulise kontsentratsiooni kohta palju tugvam kasvuhoonegaas kui süsinikdioksiid. Enne tööstusrevolutsiooni oli metaani kontsentratsioon atmosfääris umbes 715 ppb, mis jääb viimase 650 000 aasta looduslikku vahemikku (320-790 ppb)
(Soomes suurem probleem kui näiteks Põhja-Eestis). 5. Mõju inimese tervisele. Sagenevad hingamisteede haigused (bronhiit, astma, kopsuvähk). Happesademed võivad kahju tekitada kaugel nende tekkekohast. Kasvuhooneefekt Lühilaineline päikesekiirgus läbib atmosfääri, kuid pikalainelise soojuskiirguse väljumine on takistatud. See neeldub õhus, mille tagajärjel atmosfäär soojeneb. Peamiseks soojuskiirguse neelajaks on veeaur, lisaks veel süsihappegaas CO2, metaan CH4, naerugaas N2O, maalähedane osoon 03 jt gaasid, samuti aerosool. Kokku on selliseid gaase atmosfääris üle 40 ja neid nimetatakse kasvuhoonegaasideks. Kasvuhooneefekt on looduslik protsess, mis on atmosfääris esinenud kas suuremal või vähemal määral kogu aeg. Nendel geoloogilistel ajastutel, kui CO2 sisaldus oli suur, valitses maakeral soe kliima, ja kui see oli väike, siis domineeris külm kliima koos mandri-ja mägijäätumisega. Viimastel aastakümnetel on
Kasvuhooneefekt Päikeselt lähtuv valguskiirgus läbib Maad ümbritsevad atmosfääri ja neeldub maapinnale. Selle tulemusena maapind soojeneb ja kiirgab soojust atmosfääri tagasi. Soojuskiirguse hajumist kosmosesse takistavad atmosfääris esinevad kasvuhoonegaasid. Nede hulka kuuluvad nt veeaur, süsinikdioksiid, dilämmastikoksiid, metaan. Üks osa Maalt lähtuvast soojuskiirgusest neeldub nendes gaasides, teine osa aga peegeldub maapinnale tagasi seda nimetatakse kasvuhooneefektiks. Kui kogu Maalt tagasipeegelduv infravalgus hajuks kosmosesse ei oleks meie planeet enam elamiskõlblik. Seega on kasvuhooneefekt üks peamisi tegureid, mis võimaldab elul Maal eksisteerida. Metaan moodustub looduslikult bakterite ja teiste mikroorganismide ainevahetuse tulemusena, eraldub ka märgaladelt nt soodest, riisikasvandustest.
teiste planeetidega. Võrdpäevsuse lähedasel ajal on Päike suunatud ekvaatorile, mistõttu on sellel perioodil öö ja päeva vaheldumine sarnane enamiku teiste planeetide ööpäevade vaheldumisega. Uraani viimane ekvinoktsium oli 2007. aasta 7. detsembril. Koostis Uraani atmosfääri koostis erineb ülejäänud planeedi keemilisest koostisest, koosnedes peamiselt divesinikust ja heeliumist. Uraani atmosfääri kolmandaks oluliseks koostisosaks on metaan (CH4). Metaanis neeldub rohkesti päikesekiirguse kollast ja punast spektriosa, mistõttu peegelduvad tagasi sinised ja rohelised kiired. Seetõttu paistabki Uraan meile sinakasrohelisena. Kliima Uraani atmosfäär on ultraviolettkiirguse ja nähtava valguse lainepikkustel erakordselt ühtlane ja ilmetu, võrreldes teiste hiidplaneetidega. Kui Voyager 2 möödus Uraanist 1986. aastal, registreeriti tervel planeedil kokku kümme pilve.
Alkaanid ja nende kasutamine: metaan, etaan, propaan Jane Tõevere, Triin Rannak LB-2 Alkaanid Lahtise ahelaga küllastunud süsivesinikud Üldvalem: CnH2n+2 Rühma lihtsaimaks esindajaks metaan Veest kergemad Lahustuvad halvasti Peamiseks saamisallikaks on nafta ehk maaõli. Metaan Omadused: lõhnatu, värvitu, hüdrofoobne gaas Tekkimine: orgaanilise aine lagunemisel toidu käärimise tagajärjel Metaani kasutamine Kütus (peamisena) Elektrijõu genereerimisel Keemiatööstuses toorainena ainete saamiseks Kummitööstuses tahmana Etaani kasutamine Keemiatööstuses eteeni tootmisel Jahutusseadmetes Uurimistöödes veerikaste proovide klaasistamiseks Plaan toota äädikhapet Propaan Ideaalne energiaallikas Leek ei tahma ega erita väävlit ja
d)c1-c4=gaasilised, c5-c16=vedelikud, c16-c..=tahkised e)vedelad alkaanid on bensiini lõhnaga, gaasilised lõhnatud f)molekulmassi kasvuga suureneb tihedus, sulamis-ja keemistemp. g)tahked alkaanid ei märgu h)vedelad alkaanid on head lahustid paljudele ainetele 9.keemilised om.: a)kõik alkaanid põlevad b)termiline lagunemine c)regeerimine halogeenidega(VII A rühma elemendid) d)konvensioon veeauruga(toimub kõrgel temp, 1000C, nikkelkatalüsaatori toimel) e)oksüdeerimine alkoholiks 12.metaan: tekib looduses looma ja taimejäänuste anaeroobsel käärimisel, olles loodusliku gaasi ehk maagaasi peamine koostisosa.tekib märgaladel, nim ka soogaasiks.kaevandustes kogubeb söekihtide peale ja vahele, tuntakse ka kaevandusgaasina.leidub teda looduslikus gaasis olenevalt leikohast 70-90%, aga ka naftagaasides ja lahustatuna veidi ka naftas.palju on teda ka atmosfääris.peamised tekitajad on riisipõllud ja ka loomakarjad nt lambakarjad.omadused.värvuseta,maitseta,
......................... 5 Allikad......................................................................................................................... 6 Veeldatud gaasid ja nende omadused Veedldatud gaasiks nimetatakse normaaltemperatuuri ja-rõhul gaasilises olekus oleva aine vedelat olekut. Veeldatud gaasid jaotatakse looduslikeks ja keemilisteks gaasideks. Looduslikku gaasi saadakse kas gaasi-või naftaleiukohtades või nafta töötlemise tulemusena. Peamiseks looduslikuks gaasiks on metaan ehk kaevandusgaas. Keemilised gaasid saadakse kas nafta või teiste gaaside keemilisel töötlemisel. IMO (Rahvusvaheline Merendusorganisatsioon) määratluse järgi nimetatakse veeldatud gaasiks vedelikke, mille auru absoluutne rõhk temperatuuril 37,8C on suurem kui 2,8 baari. Looduslikud gaasid Veeldatud maagaas (LNG) on kogu maailmas aktiivsemalt kasutusel olnud juba ligikaudu 50 aastat. LNG ohtlikkus seisnebki peaasjalikult tema aurustumisproduktide tuleohtlikkuses.
Kütus ehk kütteaine on aine, mille põletamisel eraldub palju soojust ja mida seetõttu kasutatakse energiaallikana, näiteks elektrienergia saamiseks. Kütust kasutatakse toidu valmistamiseks, eluaseme soojendamiseks, transpordivahendite ja masinate mootoreis, tööstuses jne. Põlevad õhus Jagunemine: > Maagaasiks > Vedelgaasiks > Tehisgaasiks > Biogaasiks > kaasnev gaas Põhiliselt metaan Leidub koos naftaga või eraldi Lõhnatu ja värvitu Suurimad leiukohad: > Venemaal > Iraanis > Ameerika Ühendriikides Kodupidamistes kütteks ja toidu valmistamiseks Generaatorgaas Kõrgahjugaas Kasutatakse mitmes tööstusharus ja majapidamisgaasina Propaan ja butaan Vedelas olekus, põleb gaasina Kasutatakse > Majapidamisgaasina maagaasi asemel > Metallide lõikamisel > Kuumutamisel > Jootmisel > Soojapuhurite
o lämmastik, hapnik, fosfor või väävel. Miks on head? PHA-d on keskkonnasõbralikud bioplastid, mis valmistatakse taastuvast toormest ja looduses täielikult lagunevad. Inimkond tunneb nende vastu üha rohkem huvi, sest polühüdroksüalkanoaate saab kasutada sünteesitud plastide asendajana, ent hetkel on selle tootmise hind väga kõrge. PHA-d on biolagunevad ained, mis aeroobsetes tingimustes lagunevad süsinikdioksiidiks ja veeks, anaeroobsetes tinigimustes on jääkproduktiks metaan ja süsinikdioksiid. Antud polümeeri biolagundatavus sõltub temperatuurist, niiskusest, pH-st ja ka materjali keemilisest koostisest, lisaainetest ja kristallilise faasi osakaalust (mis võib olla kuni 70%). Milline struktuur? PHA-d on lineaarsed polüestrid, mille monomeerideks on hüdroksüalkanoaadid. Neil on 2 erinevat biofüüsikalist olekut- raku sees on ta amorfne, ahelad liikuvad ja entroopia on kõrge.
raske end selle eest juba kaitsta. Ka dikloroetaan ehk taimekaitsevahend on mürgine ja väga tuleohtlik .Kuulub püsivate orgaaniliste ainete hulka ja võib kanduda kaugele . Atmosfääris laguneb dikloroetaan 30300 päeva jooksul teisteks kemikaalideks, eeskätt CO2 ja HCl (viimane on hapestumist ja udu tekitav ühend). Mõjub nii putukatele kui ka taimedele mürgiselt . Tetraklorometaan Inimese tervisele ja loodusele sellel otsest mõju ei ole, kuid metaan osaleb atmosfääris keemilistes reaktsioonides ning on üks olulistest kasvuhoonegaasidest. Metaani eluiga atmosfääris on umbes 10 aastat. Ta on väga kergesti süttiv ja võib koos õhuga moodustada plahvatusohtliku segu. Tal on ka kerge narkootiline toime.
kümneid või sadu kordi suurem ning joogivesi põhjustab seal spetsiifilisi haigusi (nn mustjalg), mitmesuguseid nahahaigusi, vähktõvevorme jm. Arseen ja selle ühendid võivad olla ka kasulikud. Nimetame vaid efektiivseid puiduimmutusvahendeid, mis aitavad mädanemise vastu, pooljuhtmaterjale, eriklaase ja ravimeid. Naatriumarsenit on efektiivne ravim leukeemia puhul. Arseeni sissehingamisest tingitud ajalooliste surmade kohta saab lugeda siit. Metaan (Methane - prügila gaas) Metaan tekib looduses anaeroobsetes tingimustes mikroorganismide (bakterite) elutegevuse käigus orgaanilise aine, eriti tselluloosi lagunemisel (anaeroobne lagunemine). Seda esineb näiteks soodes ja mudastel aladel. Palju metaani on imetajate soolegaasides ning seda eraldub ka mäletsejate sõnnikust. Rohkesti metaani tuleb ka riisipõldudelt. Suurem osa atmosfääri metaanist pärinebki tänapäeval karjakasvatusest ja riisikasvatusest. Metaan on maagaasi (6090%) ja soogaasi peamine komponent
I valentsolek neli üksiksidet 109028´ CH4 jne Tetraeeder II valentsolek 2 üksiksidet ja 1200 1 kaksikside Tasapind CH2= CH2 III valentsolek üksikside ja kolmikside 1800 =C= O=C=O Või 2 kaksiksidet Sirge -C::: CH:::CH Metaan CH4 Lihtsaim süsivesinik, Õhust kergem ja ilma lõhna ning maitseta. Vees ei lahustu ja oluliselt mürgine pole. Eraldatakse maagaasist, mille põhikomponent ta on. Keemilised omadused Metaan on redutseerija Sest ta on süsiniku kõige madalama oksüdatsiooniastmega (-IV) ühend. Põlemisel oksüdeerub lõpuni ( oksüdatsiooniastmeni +IV) CH4 + 2O2 = CO2 + 2H2O Katalüsaatorite manulusel saab metaani oksüdeerida ka osaliselt
põlevkivi, maagaas ning kivisüsi, põletamisel; metsade mahavõtmisel (CO 2 on neeldunud puudesse, kuid kui metsa raiutakse, pääseb suur kogus süsihappegaasi atmosfääri; eriti on see probleem troopilistel aladel, kus massiliselt hävitatakse vihmametsi); lubja (kaltsiumoksiidi ehk tsemendi) tootmisel. CO 2 hulk atmosfääris on viimase 100 aasta jooksul kasvanud umbes 17%, seega tuleks selle stabiliseerimiseks kahandada süsinikuheidet 60-80%. 2) Metaan CH4 värvusetu lõhnatu õhust kergem gaas - maagaasi põhikomponent, mida kasutatakse kütusena. Suur osa metaani eraldub märgaladest, eriti riisikasvatustest, teda paiskub õhku koduloomade (nt veiste) väljaheidetest ning prügilatest. Metaani moodustub rohkesti ka soodes ja rabades. Enamasti toodavad seda gaasi bakterid ja teised mikroorganismid vesinikust ja süsihappegaasist.
suuremaks ka Ganymedesest ja arvati üldse, et Titan on Päikesesüsteemi suurim kuu. Atmosfäär on nähtavas valguses läbipaistmatu seal hõljuvate osakeste tõttu. Titani atmosfäärirõhk pinnal on 146,7 kPa ehk 1,45 Maa atmosfäärirõhku. Sellist õhku oleks võimeline inimene hingama, kuid Titani atmosfäär on väga mürgine. 98,4 % Titani atmosfäärist on lämmastik ja 1,6% metaan, lisaks väikestes kogustes ka etaani, propaani, atsetüleeni jms. Titani gravitatsioon on nii väike ja atmosfäär nii tihe, et inimestel oleks võimalik seal lennata, kui nende käte külge kinnitada tiivad, mida lehvitada. Titanil on avastatud heledad ja tumedad alad. Uurimise käigus jõuti selgusele, et heledad alad on jääst ja tumedad alad on paigad, kuhu metaanvihm uhub orgaanilist setet. Heledate ja tumedate alade kõrguse vahe võib olla kuni 100 meetrit
Alkoholid on sellised süsivesinikest tuletatud ühendid, milles üks või enam vesiniku aatomit on asendatud ühe või enama hüdroksüülrühmaga. Tähtsamad alkoholeon metanool ja etanool. Metanool: · CHOH · Suurim süsinikuühendite rühma - alkoholide kõige lihtsam esindaja. · Metanooli võib saada metaan oksüdeerimisel. · Lihtsam on metanooli saada CO redutseerumisel. · Metanool on värvitu, põletava maitsega mürgine vedelik. · Keemis temperatuur 65° · Seguneb veega igasuguses vahekorras. · Metanooli väiksemate koguste sisse võtmisel võib see põhjustada pimedaks jäämist jt raskeid tervisehäireid. · Metanooli kasutatakse tööstuses lahustina, mootorikütusena ja mitmesuguste ainete valmistamiseks. Etanool: · CHCHOH
Katekooriliselt keelatud kasutada sulameid, mis sisaldavad rohkem kui 70% vaske. Propaan. (C3 H8) Propaan on läbipaistev, terava lõhnaga gaas. Teda saadakse naftasaaduste ümbertöötlemisel. Propaani ja hapniku leegi temperatuur on suhteliselt madal ega ületa 2600 oC. Propaani ja butaani segu kasutatakse teraste lõikamisel, kergsulavate värviliste metallide keevitamisel ning jootmisel, karastamisel, plastmasside gaasikeevitamisel. Looduslik gaas. Looduslikus gaasis on põhiliselt metaan (77-98%) ja vähesel määral ka propaani, butaani ja teisi gaase. Peaaegu lõhnatu gaas ning lekete avastamiseks lisatakse talle erilisi teravlõhnalisi aineid. Leegi temperatuur on 2100 2200 oC. Kasutatakse põhiliselt termolõikamisel. Vesinik. (H2) Värvitu ja lõhnatu põlevgaas. Vesinik on üks kergemaid gaase. Vesnikuga keevitamisel tuleb järgida rangelt ohutusnõudeid kuna ta võib moodustada õhu hapnikuga plahvatusohtlike segusid
SÜSIVESINIKUD.- sisaldavad ainult H ja C aatomeid. Küllastunud süsivesinikud. C vahel on ainult üksiksidemed Alkaanid. Üldvalem: CnH2n+2 Metaan CH4 Vees mittelahustuvad gaasid. Etaan C2H6 Lõhnata, maitseta. Kas. Küttegaasina jm. Propaan C3H8 Butaan C4H10 C5 C15 Vees mittelahustuvad, veest kergemad, bensiini lõhnaga vedelikud. Nendest koosnebki bensiin ja petrooleum. Bensiin-hea lahusti. Alkaani nimetusel on lõpp- aan Alkaani nimetused on alusteks kõigi teiste ainete nimetuste moodustamisel. Süsivesinike täielikul põlemisel tekib CO2 ja H2O
Nimetus Valem Omadused Kasutusala Metaan CH4 · Värvusetu · Gaasiline kütus · Lõhnatu · Maagaas · Maitsetu · Gaas · Vees lahustub halvasti
oma pinnale mitmesuguseid lisaaineid .Süsi juhib elektrit . Kõrgel temperatuuril töödeldud veeauruga süsi on eriti suure sidumisvõimega . Söe abil saab lahustest eemaldada lahustunud värvilisi aineid . Söetablette antakse sisse kõhuvalu puhul, et siduda seedeorganites kahjulikke aineid. 8. Mis on koks ? Kivisöest saadav süsi on koks . 9. Metaani valem, süsinikuoksüdatsiooniaste metaanis . Metaan CH4 . Süsiniku oksüdatsiooniaste on IV . 10. Metaani omadused . Metaan on : 1) Värvusetu , 2) Lõhnatu , 3) maitsetu . Vees lahustub võrdlemisi vähe . Õhust on tublisti kergem. Põleb hästi . 11. Metaani leidumine looduses. Metaan on maagaasi põhiline koostisosa . Metaani leidub Ka mitmesugustes gaasides , mis tekivad orgaaniliste ainete lagunemisel ilma õhu juurdepääsuta (soogaas ) . Kasutatakse
Keemia, 10.klass Gerli, Stella, Kätlin Väikese molekuliga alkaanid ehk C1 C3 on gaasilised alkaanid. Gaasilised alkaanid on lõhnata või vedelad bensiini lõhnaga. Nelja esimese alkaani(C1-C3) puhul on need sõnatüve met(aan), et(aan) ja prop(aan) triviaalsed. Maagaas koosneb põhiliselt metaanist ja etaanist, vedelgaas ehk balloonigaas (veeldatud naftagaas) aga propaanist ja butaanist Kõige lihtsam alkaan metaan (CH4) on kõikidele looduslike gaaside ( maagaas, kaevandusgaas, soogaas ) peamiseks koostisosaks. Kõrvuti metaaniga sisaldub neis etaani, propaani, butaani, ja teisi alkaane. Alkaan Nimetus CH4 metaan C2H6 etaan C3H8 propaan Alkaanid on süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega. Mõnikord nimetatakse alkaane ka parafiinideks.
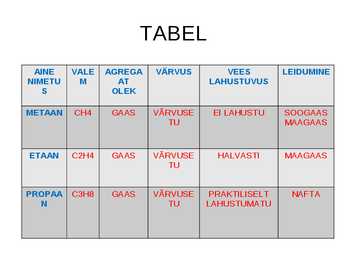
TABEL AINE VALE AGREGA VÄRVUS VEES LEIDUMINE NIMETU M AT LAHUSTUVUS S OLEK METAAN CH4 GAAS VÄRVUSE EI LAHUSTU SOOGAAS TU MAAGAAS ETAAN C2H4 GAAS VÄRVUSE HALVASTI MAAGAAS TU PROPAA C3H8 GAAS VÄRVUSE PRAKTILISELT NAFTA N TU LAHUSTUMATU ALKAANIDE ÜLDVALEM CnH2n+2 C-aatomite arv Nimetus Valem Olek 1 METAAN CH4 G
Sisukord: 1. Mis on alkaanid. 2. Keemilised omadused. 3. Füüsikalised omadused. 4. Füsioloogilised omadused. 5. Alkaanide leidumine. 1.Alkaanide üldvalemiks on CnH2n+2 · Alkaani tunnuseks on liide aan · Sõnatüvi kirjeldab süsinikahela pikkust · Neli esimest alkaani (metaan, etaan, propaan ja butaan) on triviaalsed ja nned tuleb lihtsalt meelde jätta · Alates C5 kasutatakse kreekakeelsete arvsõnade tüvisid: (pentaan penta, heksaan heksa jne). · Tsüklilist ahelat tähistab eeslide tsüklo (N: tsüklobutaan) Alkaanid on küllastunud süsivesinikud, kus süsiniku aatomi vahel on kovalentsed üksiksidemed. Küllastunud tähendab seda, et nad sisaldavad maksimaalselt võimalikku arvu
Nimi Erinevad gaasid ja kasutus Iseseisev töö Juhendaja : Tartu 2012 Sisukord 1. Sissejuhatus .......................................................................... 3 2. Hapnik .................................................................... 4 3. Propaan...............................................................4 4. Metaan ...............................................................4 5. Butaan ........................................................................ 5 6. Lämmastik ............................................................. 5 7. Vesinik ...................................................................... 5 8. Kasutatud kirjandus .............................................................. 7 Erinevad gaasid ja kasutus
Gaaskütused Erki, Ron, Kristina, Christjan 11b Gaaskütused · Põlevad õhus · On piisavalt kasulikud · Torud, Tankrid · Jagunemine: Maagaasiks Vedelgaasiks Tehisgaasiks Biogaasiks kaasnev gaas Maagaas · Põhiliselt metaan · Koos naftaga või eraldi · Lõhnatu ja värvitu · Leiukohad: Venemaal Iraanis Ameerika Ühendriikides · Kodupidamistes kütteks ja toidu valmistamiseks Tehisgaasid · Generaatorgaas · Kõrgahjugaas · Põlevkivigaas · Kivisöegaas · Utmine: peenestatud kivisütt kuumutatakse õhu juurdepääsuta 900... 1000 °C juures. Vedelgaas · Propaan ja butaan · Vedelas olekus, põleb gaasina · Kasutatakse
Anorgaaniline: Keemiline side-iooniline side NaCl, Sulamistemp- üle 350 o, Keemistemp üle 750o, Lahustuvus a)vees-hea, b)orgaanilistes ainetes halb, süttivus-enamasti ei sütti, Elektrijuhtivus- enamasti juhivad. Orgaaniline: Keemiline side- enamasti kovalentne side CH 4-metaan, Sulamistemp alla 350o, Keemistemp alla 750o, l ahustuvus a)vees- enamasti halb, b) Orga. Ainetes hea, süttivus enamasti süttivad, Elektrijuhtvus- enamasti ei juhi. Isomeeria: On nähtus kus ainetel n ühesugune element koostis ja molekulmass, kuid erinev struktuur ja seetõttu ka erinevad omadused. Valents olek: -C- Neli üksiksidet, -C= 2 üksiksidet 1 kaksik side, =C= 2 kaksikside, -C= 1 üksikside ja 1 kolmikside
1. Selgitage mõisteid.Tooge iga mõiste kohta ka üks näide. Elektrolüütiline dissotsiatsioon- Elektrolüütide jagunemine ioonideks nende lahustumisel vees. Põhjustab hüdraatumine vee molekulide seostumine ioonidega. Nt soola dissotsiatsioon:KCO 2K+CO² Mitteelektrolüüdid-ained, mille vesilahused ei sisalda ioone , ei juhi elektrivoolu.(Lihtained nt O-hapnik, oksiidid nt CaO-kaltsiumoksiid, paljud orgaanilised ained nt metaan-CH) Nõrk elektrolüüt-lahuses esinevad nii molekulid, kui ka ioonid.(nõrgad happed, nõrgad alused) Tugev elektrolüüt- esinevad lahuses ainult ioonidega( tugevad happed, leelised, soolad) Nt HCl H+Cl 2. Millised järgmistest ainetest kuuluvad tugevate elektrolüutide, millised nõrkade elektrolüütide ja millised mitteelektroluütide hulka: a) naatriumjodiid, b) jood, c) suhkur, d) kaltsiumoksiid, e) väävelhape, hapnik, metaan? Tugevad elektrolüüdid: väävelhape,
Sissejuhatus Alkaanid - süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega. Mõnikord nimetatakse alkaane ka parafiinideks. 3 Leidumine ja saamine Kõige lihtsam alkaan - metaan (CH4) on looduslike gaaside (maagaas, kaevandusgaas, soogaas) peamine koostisosa. Kõrvuti metaaniga sisaldavad nad etaani, propaani, butaani ja teisi alkaane. Sünteetiliselt võib metaani saada juhtides vesinikku kõrgel temperatuuril läbi hõõguvate süte: C + 2H2 → CH4 4 Tuntumad esindajad METAAN: Maagaas (70-90%) Naftagaas
süsivesnikud · Triviaalsed nimetused inimene andis keemilistele ainetele nimed juhuslikult, sageli saamisviisi või omaduste järgi · Süstemaatilised nimetused Kajastavad ühendi keemilist struktuuri, need on ka keemikutele olulisemad · Nomenklatuur aine struktuuri ja nimetust siduvate reeglite kogu Alkaan Nimi Alküülrühm Alküülrühma nimet. CH4 Metaan CH3 Metüül C2H6 Etaan C2H5 Etüül C3H8 Propaan C3H7 Propüül C4H10 Butaan C4H9 Butüül C5H12 Pentaan C5H11 Pentüül C6H14 Heksaan C6H13 Heksüül C7H16 Heptaan C7H15 Heptüül C8H18 Oktaan C8H17 Oktüül
molekulmass, tihedus, sulamis- ja keemistemperatuur, väheneb aga ainete lahustuvus vees. 6. Tahkeid alkaane kutsutakse parafiinideks. 7. Alkaanid on veest kergemad. 8. Alkaanid ei märgu ega lahustu vees, seega nad on hüdrofoobsed ained. 9. Alkaanid on keemiliselt kõige passiivsemad orgaanilised ained. 10. Alkaanidel esineb 3 liiki keemilisi reaktsioone: põlemine, pürolüüs ja asendusreaktsioonid halogeenidega (halogeenimine). 11. Metaan on loodusliku gaasi ehk maagaasi peamine koostisosa. Teda leidub maagaasis 70 kuni 90% Metaan on värvuseta, maitseta ja lõhnata õhust kergem gaas. Metaan on ka kasvuhoonegaas. Biogaas sisaldab samuti 70% metaani. 12. Etaani leidub looduslikus gaasis kuni 10% 13. Propaani leidub looduslikus gaasis ja lahustununa naftas. 14. Butaani leidub samuti looduslikus gaasis ja naftas. 15. Teda kasutatakse koos propaaniga kütusena ja viimasel ajal ka
Kui aga Jupiteril on pind siiski olemas, asub see planeedi pilvede ülemisest piirist vähemalt 1000 kilomeetrit allpool. Jupiteri keskmine pinnatemperatuur on 145oC. 2 Jupiteri tihedas õhkkonnas on leitud mitmesuguseid keemilisi ühendeid, nende hulgas ka keerulisi molekule. Põhilisteks on küll vesinik ja heelium, kuid viimast on oodatust poole vähem. Olulisemad lisandid planeedi atmosfääris on ammoniaak (NH3), metaan (CH4) ja etaan (C2H6). Kõige huvitavam objekt Jupiteri nähtaval pinnal on Suur Punane Laik. Esimesena märkas seda itaalia rahvusest Prantsuse astronoom Giovanni Cassini 1666. aastal. 1878. aastast tänaseni vaadeldakse seda pidevalt. Laigu pikem külg võrdub 50 000 kilomeetriga, lühema külje pikkus on 30 000 kilomeetrit. Punase värvi annab laigule fosfiin (PH3). Jupiteri rõngad paiknevad planeedi ekvatoriaaltasandil umbes 55 000 km kaugusel pilvepiirist
Alkaanid on süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega. Alkaane nimetatakse vahel ka parafiinideks. Kõige lihtsam alkaan on metaan ning metaan on looduslike gaaside peamine koostisosa. Looduslikud gaasid on näiteks maagaas, kaevandusgaas ja soogaas. Lisaks metaanile sisaldavad need gaasid ka etaani, propaani, butaani ning teisi alkaane. Füüsikalised omadused: Alkaanide omadused muutuvad korrapäraselt süsiniku aatomite arvu suurenemisega molekulis. Metaan ja temale järgnevad alkaanid erinevad üksteisest aatomite rühma – CH2 – võrra. Metaani homoloogilise rea 4
Side süsinik-hapnik on palju püsivam kui side vesinik hapnik. Alkoksiidioon on väga nõrga happe anioon. Alkohol on on hape. Alkoholaat on alkoholi sool. Metanool- Ch3Oh puupiiritus. Etanool C2H5OH piiritus. Puskari õli on destillatsioonijääk etanooli eraldamisel käärimissegust. See koosneb kahest pentanooli isomeerist. Etandiool HOCH2CH2OH-etüleenglükool- diool. Antifriis-mootori jahutussegu. Glütserool- HOCH2CHOHCH2OH-looduslik. Alkaanid- CH4-metaan C2H6-etaan C3h8-propaan Alkeenid- C2H4-eteen C3H6-propeen Alküünid- C2H2-etüün C3H4-propeen Alkoholid- ch3oh-metanool c2h5oh- etanool c3h7oh- propanool Karboksüülhapped- hcooh-metaanhape ch3cooh-etaanhape C2h5cooh-propaanhape Sahhariidid- c6h12o6-glükoos c6h12o6-fruktoos c12h22o11-sahharoos (c6h10o5)n-tärklis tselluloos Aineid, mille molekulis tetraeedrilise süsiniku aatomi juures asuv vesinik on asendatud hüdroksüülrühmaga oh, nimetatakse alkoholideks
Metaanhüdraat - kas oht keskkonnale või tuleviku kütus? Metaanhüdraat ehk põlev jää on jääsarnane kristalliline aine, mida leidub ookeani sügavustes. See koosneb jääst ja kergestisüttivast gaasist metaanist. Metaan moodustub muda sees elavate mikroobide elutegevuse käigus. Need mikroobid lagundavad ookeani põhja vajunud orgaanilist ainet. Metaan ühineb peaaegu külmunud veega, misjärel moodustuvad metaanhüdraadi kristallid. Need kristallid on nagu imetilluksed jääpuurid, mis metaani enda sees hoiavad. Et kristallid saaksid moodustuda, peab vee temperatuur olema külmumispunktist veidi kõrgem ning mere sügavus peab olema vähemalt 500 meetrit. Kui need tingimused on täidetud, hakkavad metaanhüdraadi kristallid kasvama, moodustades kobrutavat lumetaolist ollust
SÜSIVESINIKUD On orgaanilisedühendid mis koosnevad süsinikust ja vesinikust Alkaanides on 1-4 liiget gaasid ja alates 5. on vedelikud. ALKAANID 1) Metaan CH4 2) Etaan C2H6 3) Propaan C3H8 4) Butaan C4H10 5) Pentaan C5H12 6) Heksaan C6H14 7) Heptaan C7H16 8) Oktaan C8H18 9) Nonaan - C9H20 10) Dekaan C10H2 ALKOHOOLID Alkohoolide nimetus on tuletatud süsivesinikest, millest üks või mitu on hüdroksiid. Alkohoolide nimed pannakse lähtudes alkaanide reast C-de(süsinike) arvu järgi. CnH2 + 2 = AAN lõpuga 1) CH4 metaan ---- CH3OH = metanool ehk puupiiritus
Ahela ehituse järgi jaotatakse alkaanid: 1) tsüklit mittesisaldavad (atsüklilised) alkaanid , üldvalemiga C nH2n+2 Need jaotatakse omakorda a)hargnemata ahelaga ehk normaalalkaanid ja b)hargnenud ahelaga . 2) tsüklilised alkaanid ehk tsükloalkaanid , üldvalemiga C nH2n. Nomenklatuur on aine struktuuri ja aine nimetust siduvate reeglite kogu. 1. Hargnemata ahelaga atsükliliste alkaanide valemid ja nimetused ( C nH2n+2 -aan ) 1) CH4 metaan 2) C2H6 etaan CH3-CH3 3) C3H8 propaan CH3-CH2-CH3 4) C4H10 butaan CH3-CH2-CH2-CH3 5) C5H12 pentaan 6) C6H14 heksaan 7) C7H14 heptaan 8) C8H18 oktaan 9) C9H20 nonaan 10) C10H22 dekaan 2. Tsükloalkaanide valemid ja nimetused (C nH2n) tsüklopropaan tsüklobutaan tsüklopentaan tsükloheksaan ∆ □ ⌂ (graafilised kujutised) 3. Hargnenud ahelaga alkaanide nimetamine valemi järgi
Kasvuhooneefekt Evelin & Pilleriin Kasvuhooneefekt Kasvuhoonegaasid Algupäraselt looduslik nähtus Hädavajalik maakera elustikule Maa keskmine temp. oleks -18°C praeguse +15°C asemel Tähtsamad kasvuhoonegaasid Süsihappegaas ehk süsinikdioksiin CO2 fossiilsed kütused lubja tootmine Tähtsamad kasvuhoonegaasid Metaan CH4 Maagaasi põhikomponent Koduloomade väljaheidetes Prügilad Sood ja rabad Muu Prügimäed Metaan Riisikasvatus Karjakasvatus 0% 10% 20% 30% 40% Tähtsamad kasvuhoonegaasid Dilämmastikoksiidid N2O Autoheitgaasid
· Aeroobsetes tingimustes vabaneb CO2 orgaanilistest ainetest loomade, taimede, inimeste ja mikroorganismide hingamise tulemusena. CO2 arvel moodustavad orgaanilist ainet taimed, vetikad, tsüanobakterid ja kemolitotroofsed bakterid. · Anaeroobsetes tingimustes vabaneb CO2 orgaanilistest ainetest kääritajate ja anaeroobsete hingajate vahendusel. CO2 arvel sünteesivad orgaanilist ainet fotosünteesivad purpur- ja rohevetikad. Metaan moodustub anaeroobsetes tingimustes metanogeenide vahendusel. Süsinikuringe esimene osa on fotosüntees - taimed võtavad õhust süsihappegaasi ja muudavad selle päikeseenergia toimel süsivesikuteks. Süsinikuringe produktid on seega orgaanilised molekulid ja hapnik. Põlemisel, hingamisel ja kõdunemisel moodustunud CO 2 läheb õhku. Sealt seovad seda rohelised taimed, mis fotosünteesil muundub CO 2 orgaanilisteks ühenditeks (suhkrud,
ALKAANID Süsivesinikud on ............................. ·Alkaan -süsivesinik, mis sisaldab ainult tetraeedrilisi süsinikke. · ALKAANIDE NOMENKLATUUR - aine struktuuri ja nimetust siduvate reeglite kogum. 1) Triviaalsed nimetused Näiteks metaan ehk ............................ Metaanhape ehk ............................ 2) Süstemaatilised nimetused moodustatakse molekuli struktuuri järgi kindlaid reegleid kasutades. ALKAANI tunnuseks on liide aan. TV 2.1. Alkaanist pärit asendusrühma nim alküülrühmaks. alküülrühmaks Tähis R- alkaan alküülrühm metaan CH4 metüül CH3 etaan CH3CH3 etüül CH3CH2
Füüsikalised omadused · o Metaani ja temaga sarnaste süsivesinike - alkaanide omadused muutuvad korrapäraselt süsiniku aatomite arvu suurenemisega molekulis. o Metaan ja temale järgnevad alkaanid erinevad üksteisest aatomite rühma - CH2 - võrra. Niisugust ühendite rida nimetatakse homoloogiliseks reaks. Rea üldvalem on CnH2n +2 o Metaani homoloogilise rea 4 esimest ühendit on gaasid, viiendast kuni kuueteistkümnendani vedelikud ja kõrgemad on tahked ained. Molekulmassi kasvuga homoloogilises reas suureneb alkaanide tihedus ning