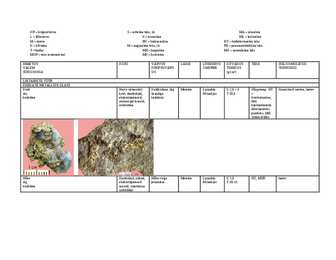
SÜNGOONIA US (g/cm3) LIHTAINETE TÜÜP EHEDATE METALLIDE KLASS Kuld Harva oktaeedril. Kuldkollane (Ag Metalne L puudub K 2,5 3 Kõrgetemp. HT Keemiliselt inertne, taotav Au krist; dendriitjad, lisandiga M haakjas T 19,3 kuubiline ebakorrapärased, heledam) kvartsisoontes; soomusjad massid, tihti suletistena kontsentreerub alluviaalsetes
3. Adventsiaalkest (tagaosas trahheaalnäärmed) Bronh: 1. Limaskest · Mitmerealine ripsepiteel · Proopria · Limaskesta lihaskiht · Submuukooskiht 2. Kondrofibrooskest (hüaliinse kõhrkoe plaadikestest) 3. Adventsiaalkest (hulgaliselt rasvkudet) Bronhioolid: · Ei sisalda kõhrkude ega näärmeid · Suurtes kahe või üherealine ripsepiteel, väikestes bronhioolides kuubiline ripsepiteel · Proopria · Tsirkulaarne lihaskiht · Terminaalsed bronhioolid · Respiratoorsed bronhioolid katkendlik kuubiline ripsepiteel, alveolaarjuhad, alveolaarkotid, alveoolid Kusejuha: 1. Limaskest · Trasitoorne epiteel · Proopia · submukoosa 2. Lihaskest · Sisemine pikikiht · Keskmine ringkiht · Välimine pikikiht 3
Vask värvus varieerub punasest kuldpruunini, niiskes õhus tekib vase pinnale aja jooksul pruuni või roheka värvusega paatinakiht Teemant värvusetu, valge, hall, kollane, sinakas, must, lõhenevus täiuslik, süngoonia kuubiline, kõige kõvem mineraal, lõhenevuspindade vahele jäävad osad on oktaeedrilised Hõbe väärismetall, suhteliselt pehme, peegeldab hästi valgust Galeniit värvuselt hall, kõvadus 2,5, lõhenevus täiuslik, süngoonia kuubiline, kriips hallikasmust,
raku füsioloogias, kus kaltsiumiiooni (Ca2+) liikumine tsütoplasmasse ja sellest välja toimib olulise signaalina mitmetes rakuprotsessides. Keemia poolest on kaltsium üks reaktiivsemaid ning pehmemaid metalle. Võrreldes teiste leelismetallidega, on kaltsiumi ja vee vaheline reaktsioon aeglasem osalt seetõttu, et reaktsioonil tekkiv lahustumatu, valge kaltsiumhüdroksiid takistab vee ligipääsu metallilisele kaltsiumile. Kaltsiumil on kaks allotroopi: tahktsentreeritud kuubiline, mis eksisteerib kuni 464 °C ning ruumtsentreeritud kuubiline süngoonia, mis eksisteerib 464 °C kuni sulamistemperatuurini. Kaltsiumi sulamistemperatuur on 848 °C. Omadused: Kaltsiumil on suurem elektriline takistus ning parem elektrijuhtivus kui vasel või alumiiniumil, kuid kaltsiumi reaalset kasutamist elektriseadmetes takistab selle suur reaktiivsus õhuga kokkupuutel. Maitse poolest tundub lahustunud kaltsiumiioon inimesele pisut soolane ning hapukas
Omadused Keemiline valem C Mineraaliklass ehedad elemendid Molekulmass 12,01 Värvus värvitu, valge, hall, kollane, sinakas, must Tihedus (g/cm³) 3,50...3,53 Kõvadus 10 (etalonmineraal) Lõhenevus täiuslik Süngoonia kuubiline Punktigrupp kuubiline heksoktaeedriline Kriips värvitu Murdepind karpjas Läige teemandi Grafiit/Graphite Koostis / struktuur Keemilise elemendi süsiniku (Carbon, C) allotroopne vorm. Koosneb tasanditest, milles süsiniku aatomid on seotud tugevate kovalentsete sidemetega, moodustades korrapärastest kuusnurkadest koosneva struktuuri. Üks taoline kvaasilõpmatu tasand kannab grafeeni nimetust
➔ Väärisgaas Ar36, Ar38, Ar40 ➔ Järjenumbriga 18Aatommass on ~ ➔ VIIIA rühmas 402 1s 2s2 2p6 3s2 3p6 ➔ 3. perioodis Tähis on Ar. Põhiline info Sulamistemperat -189,4°C Prootonite uur ja -185,87°C elektrontie Keemistemperatu arv - 18 Kristallvõre ur on Neutronite kuubiline. arv - 22 Pilt on Wikipediast. Avastamine Henry Cavendish algselt kahtlustas argooni olemasolu õhus. (1785) Aastal 1894 Lord Rayleigh ja Sir William Ramsay poolt. Argoon on esimene avastatud väärisgaas. Üldomadused Keemiliselt Lõhnatu ning mitteaktiivne. värvitu. ➔ Välja arvatud kõrge rõhu ja temperatuuri Kõrgelt inertne. mõjul
Koobalt Co Koobalt on keemiline element, mille aatominumber perioodilisustabelis on 27. Koobalti avastas Georg Brandt (1964- 1768), Rootsi keemik ja mineraloog. Ta oli esimene inimene kes avastas metalli, mis polnud juba „iidsetel aegadel“ avastatud. Koobalti kristalli struktuur on kuusnurkne, tahukeskne kuubiline. Oksüdatsiooniaste ühendites on +1, +2, +3 või +4. Põhilised on +2 ja +3. +4 on harvem esinev ja üldjuhul ebapüsiv. +1 oksüdatsiooniastmega on õnnestunud ka mõned ühendid sünteesida. Omadustelt on koobalt metall. Tihedus normaaltingimustel on 8,9 g/cm3, sulamistemperatuur on 1495 oC ja keemistemperatuuriks 2927 oC. Aatommassiks on 58,9332. Koobalti värvus on hõbevalge. Toatemperatuuril on koobalt tahke. Koobaltit kasutatakse kuuma- ja happekindlates sulamites
VASK Greetel Kala 10a Koostis Struktuur *Keemiline element *Kristallstruktuur : vask (Cuprum, Cu) tahkkeskendatud kuubiline võre Omadused *Punakas-kollaka värvusega *Tihedus 8920 kg/m3 *Hea elektri- ja soojusjuht (eritakistus 1.7·10-8 Wm) *Sulamistemperatuur 1084.62 °C *Pealispinnale võib ajajooksul tekkida rohekas kattekiht (hüdraatsoolade segu(sulfaadid,karbonaadid)) Omadused *Kaks stabiilset isotoopi massiarvudega 63 ja 65 *Aatommass on 63,54. *Vase elektronskeem näeb välja: 2) 8) 18) 1) *Vase eritakistus 20 °C juures on 16,78 nΩ·m Saamine *Vähesel määral leidub looduses ehedal kujul
Alumiinium Pirgit Toots MJ-111 Koostis/struktuur Keemiline element alumiinium (Al), kristallstruktuur tahkkeskendatud kuubiline võre. Omadused Hõbedase värvusega kerge (tihedus 2700 kg/m3) pehme metall hea elektri- ja soojusjuht (eritakistus 2.65·10-8 Wm ) Alumiinium sulab temperatuuril 933.47 K (660.32 °C). Hea vormitavus Alumiiniumi saamine Alumiiniumi looduses ehedalt ei esine, kuigi ta on maakoores üks levinumaid elemente (massisisaldus maakoores 8,2 %, kolmas element hapniku ja räni järel). Alumiiniumi saadakse maakidest (boksiit)
Aatomnumber: 19 Aatommass: 39,098 Klassifikatsioon: leelismetallid, s-elemendid Aatomi ehitus: · Elektronvalem: 1s2 2s2p6 3s2p6 4s1 · Elektronskeem: +19|2)8)8)1) · Elektronite arv: 19 · Neutronite arv: 20 · Prootonite arv: 19 · Oksüdatsiooniast(m)e(d) ühendites: 0, I · Kristalli struktuur: ruumikeskne kuubiline Füüsikalised omadused: · Aatommass: 39,098 · Sulamistemperatuur: 63,25 °C · Keemistemperatuur: 759,9 °C · Tihedus: 0,862 g/cm3 · Värvus: hõbevalge · Agregaatolek toatemperatuuril: tahke · Kõvadus Mohsi järgi: 0,4 · Isotoobid: Nukliid Levimus (%) Mass Poolestusaeg 39 K 93,22 38,9637 - 40
laialdaselt kasutatav keemiline aine, kaltsiumi oksiid. Toidulisandina (happesuse regulaator) on aine koodiks E529. Füüsikalised omadused Kaltsiumoksiid on valge, hallikasvalge, kahvatukollane või kahvatuhall aine. Tööstuslikult toodetud kaltsiumoksiidil on rauasisalduse tõttu kollakas või pruunikas varjund. Kaltsiumioksiid on kristalne aine (kõva teraline mass või pulber). Struktuur on tahkkesendatud kuubiline. Molaarmass on 56,08 g/mol. Normaaltingimustel on ta tahke, sulamistemperatuur on 2572 °C (2845 K). Keemistemperatuur on 2850 °C (3123 K). Tihedus on 3,37...3,38 g/cm³. Aur on veeaurust 1,9 korda tihedam. Auru rõhk on 1455 °C juures 1,8×106 mmHg. Lahustub hästi vees. Kaltsiumoksiid ei lendu ning on lõhnatu. Soojuspaisumistegur on 3,92...6,73×105 /K. Keemilised omadused Kaltsiumoksiid reageerib eksotermiliselt veega, tekib kaltsiumhüdroksiid: CaO + H2O Ca(OH)2
Ettekanne Kristina Hertmann 10K Juhendaja : Anna Perova Üldiseloomustus Aatominumber: 37 Aatomimass: 85,4678 Klassifikatsioon: Leelismetallid, s-elemendid Aatomi ehitus: · Elektronvalem: 1s2 2s2p6 3s2p6d10 4s2p6 5s1 · Elektronskeem: +37|2)8)18)8)1) · Elektronite arv: 37 · Neutronite arv: 48 · Prootonite arv: 37 · Oksüdatsiooniast(m)e(d) ühendites: 0, I · Kristalli struktuur: ruumikeskne kuubiline Avastamine: R.W. Bunsen & G.R. Kirchoff, 1861, Heidelberg, Saksamaa Avastati see mineraal lepidokrokiidist, kasutades spektroskoopi. Nimi rubiidium tuleneb ladina keelsest sõnast "ruber", mis tähendab sügavpunast. Sellist nime põhjustasid rubiidiumi erepunased spektroskoopilised jooned. Leidumine looduses Rubiidiumi (Rb) puudust looduses ei ole. Teda leidub rohkem kui kulda, hõbedat või tina jne. Rubiidium kuulub kohekümne kolme kõige rikkalikuma elemendi hulka, mida
b) ruumkesendatud lisaks võreelemendi tippudes olevaile aatomeile paikneb üks aatom võreelemendi sees; c) tahkkesendatud lisaks võreelemendi tippudes olevaile aatomeile paiknevad aatomid iga tahu keskel; d) põhitahkkesendatud lisaks võreelemendi tippudes olevaile aatomeile paiknevad aatomid põhitahkude keskel. Eri kristallivõre tüüpides võib paikneda enam aatomeid kui neid mahub kristallivõre sõlmpunktidesse. Enamikul kasutatavatel metallidel on kuubiline või heksagonaalne kristallivõre: - ruumkesendatud kuupvõre: Cr, Fe, Mn, Mo, V, W; - tahkkesendatud kuupvõre: Ag, Al, Cu, Co, Cu, Fe, Ni, Pb, Pt, Sn; - kompaktne heksagonaalvõre: Be, Cd, Co, Cr, Mg, Ti, Zn. A a to m itu u m P ro o to n N e u tro n E le k tr o n
aatomid või ioonid tahkes kehas on paigutatud nii, et nende järjestus kordab iseennast kõigis kolmes dimensioonis 2. Mis on ruumvõre? Aatomite paigutust tahkes kehas võib kirjeldada esitades aatomid punktidena 3 dimensioonis kulgevate joontevõrgu lõikekohtades 3. Mis on elementaarrakk? Elementaarrakuks nimetatakse kristalse aine väikseimat osakest, mille kordne moodustab tervikliku aine Loetle 7 võimalikku kristallsüsteemi? Kuubiline, Tetragonaalne, Ortorombiline, Monokliinne, Romboheedriline, Heksagonaalne, trikliinne 4. Millised variatsioonid on võimalikud kuubilises kristallsüsteemis? lihtne kuubiline elementaar-rakk; ruumtsentreeritud elementaar-rakk, pindtsentreeritud elementaar-rakk. Millised on võimalikud variatsioonid tetragonaases süsteemis? Lihtne elementaar-rakk; ruumtsentreeritud elementaar-rakk. 5. Millised variatsioonid on võimalikud ortorombilises süstemis
prootonite arv 28 ja neutronite arv on 31. Prootonite arv määrab ära tuumalaengu ja on ühtlasi ka järjenumbriks. Elektronkihtide arv on 4. [1] Sele 1. Nikli aatom: Elektronskeem: +28|2)8)16)2) [2] 3 2. NIKLI KRISTALLSTRUKTUUR Kristalliseerumine ehk kristallatsioon on vedela oleku üleminek tahkesse. Nikli kristalli struktuur on tahukeskne kuubiline K12. Nikkel võib muuta oma struktuuri peale tardumist ka tahkes olekus jahtudes kuni toatemperatuurini sekundaarse kristalliseerumise etapil. Metallide seda omadust nimetatakse allotroopiaks ehk polümorfismiks. Sele 2. Nikli kristalli struktuur [2] Puhas nikkel on väga hea korrosioonikindlusega aluste ja hapete suhtes, seetõttu kasutatakse teda keemiatööstuse seadmeis ja toiduainetetööstuses. Kuigi niklil on suurepärane korrosioonikindlus,
mittemetallidest juhib grafiit elektrit, sellepärast peaks tema struktuuris leiduma vabu elektrone (tuleta meelde metallide elektrijuhtivust). Õhu käes kõrgel temperatuuril põleb grafiit nagu teemantki CO2-ks. Mittetäielikul põlemisel saadavat peent söetolmu (tahma) kasutatakse musta värvi valmistamiseks. Pressitud süsi sarnaneb omadustelt grafiidiga, kuid on palju odavam. Koostis / struktuur Keemiline element räni (Silicium, Si), kristallstruktuur tahkkeskendatud kuubiline (teemandi struktuur) kahe aatomiga elementaarrakus. Omadused Hõbedase läikega, kerge (2330 kg/m 3) materjal. Pooljuht (legeerimata räni eritakistus toatemperatuuril ca 10-3 Wm). Saamine Kuigi räni on maakoores hapniku järel kõige levinum element (27 massi%) , puhtal kujul teda looduses ei esine. Räni saadakse ränidioksiidi (kvartsliiv) taandamisel süsinikuga temperatuuridel ligi 2000 °C elektrikaarahjus.
.............7 Kasutatud kirjandus:................................................................................................................... 8 Naatriumi kohta tutvustus: Na Naatrium -metall Aatomnumber: 11 Aatommass: 22,989 Klassifikatsioon: leelismetallid, s-elemendid Aatomi ehitus: Elektronvalem: 1s2 2s2p6 3s1 Elektronskeem: +11|2)8)1) Elektronite arv: 11 Neutronite arv: 12 Prootonite arv: 11 Oksüdatsiooniast(m)e(d) ühendites: -I, 0, I Kristalli struktuur: ruumikeskne kuubiline Füüsikalised omadused: Aatommass: 22,989 Sulamistemperatuur: 97,81 °C Keemistemperatuur: 882,9 °C Tihedus: 0,971 g/cm3 Värvus: hõbevalge Agregaatolek toatemperatuuril: tahke Kõvadus Mohsi järgi: 0,5 Isotoobid: Nukliid Levimus (%) Mass Poolestusaeg 22 Na 0 21,9944 2,605 aastat 23
seega veest 7,29 korda raskem. Tina kõvadus Mohsi järgi on 1,8. Tina on hõbevalge, pehme, hästi taotav ja venitatav madala sulamistemperatuuriga metall. Ta on teiste metallide seast kergesti äratuntav seetõttu, et tinaplaadi või tinakristallide vastastikkuse nihkumise tõttu. Tina on polümorfne. Harilik valge tina ß-Sn on tetragonaalse kristallvõrega ja püsiv temperatuuril üle 13,20C. Sellest madalama temperatuuril esineb hallitina a-Sn, mille on kuubiline struktuur. Üleminekul ß-Sn ? a-Sn suureneb tina ruumala ja metall muutub halliks pulbriks. Rahvapäraselt nimetatakse üleminekut ß-Sn ? a-Sn tinakatkuks. See protsess kulgeb kiiresti madalal temperatuuril, mil tinaesemed muutuvad halliks pulbriks. ß-Sn on metall, aga a-Sn pooljuht. Temperatuuril üle 1610C esineb tina kolmanda allotroopse erimini, nn. Hapra tinana. ?-Sn on rombilise kristallstruktuuriga. ? -Sn on uhmris kergesti peenestav. Tina
Teised põhilised tootjad on Ameerika Ühendriigid, Austraalia, Hiina, Venemaa ja Peruu. Kulla sünteesimine teistest ainetest on tänapäeval võimalik, aga majanduslikult on see mõttetu, sest kulla sünteesimine läheb maksma tunduvalt rohkem kui saadud kulla enda väärtust on. Kuid juba vanadel aegadel üritati seda saavutada, antud nn teaduse nimi oli alkeemia. Koostis / struktuur: Keemiline element kuld (Aurum, Au), kristallstruktuur tahkkeskendatud kuubiline võre. Omadused: Keemilistelt omadustelt on kuld väheaktiivne metall. Ei reageeri vee ega hapetega. Kollane, pehme (kõvadus 2,5), raske (tihedus 19 300 kg/m3) metall. Sulab temperatuuril 1337.33 K (1064.18 °C). Hea elektrijuht (eritakistus 2,2108 Wm). Keemiliselt inertne viimane väide aga lakkab olemast õige, kui tegemist on väga väikeste kullaosakestega. Nn. nanokuld on näiteks väga efektiivne
organismi veetasakaalu reguleerimiseks ja südamerütmi normaliseerimiseks. Vajalik lihaste ja närvide funktsioneerimiseks. Aatomnumber: 19 Aatommass: 39,098 Klassifikatsioon: leelismetallid, s-elemendid Aatomi ehitus: · Elektronvalem: 1s2 2s2p6 3s2p6 4s1 · Elektronskeem: +19|2)8)8)1) · Elektronite arv: 19 · Neutronite arv: 20 · Prootonite arv: 19 · Oksüdatsiooniast(m)e(d) ühendites: 0, I · Kristalli struktuur: ruumikeskne kuubiline Füüsikalised omadused: · Aatommass: 39,098 · Sulamistemperatuur: 63,25 °C · Keemistemperatuur: 759,9 °C · Tihedus: 0,862 g/cm3 · Värvus: hõbevalge · Agregaatolek toatemperatuuril: tahke · Kõvadus Mohsi järgi: 0,4 eemilised omadused: · Elektronegatiivsus Paulingu järgi: 0,82 · Oksiidi tüüp: tugevaluseline · Ühendid: Fluoriidid: KF Kloriidid: KCl
Tartu Kutsehariduskeskus Majutus- ja toitlustusosakond Referaat Alumiinium Koostaja: Andres Leima Tartu 2009 Alumiinium( Al) Koostis / struktuur: Keemiline element alumiinium (Al), kristallstruktuur tahkkeskendatud kuubiline võre. Saamine: Alumiiniumi looduses ehedalt ei esine, kuigi ta on maakoores üks levinumaid elemente (massisisaldus maakoores 8,2 %, kolmas element hapniku ja räni järel). Alumiiniumi saadakse maakidest (boksiit) elektrometallurgilisel menetlusel. Suurim alumiiniumitootja ühe elaniku kohta on maailmas Island (2001. aastal üle 900 kg metalli elaniku kohta), kus selleks kasutatakse odavat geotermaalset energiat. Alumiiniumi kasutamine
on 19,7 g/cm³. Kulla sulamistemperatuur on 1064°C Kuld mineraalina Kuld on isotroopne kuubilise süngoonia mineraal. Polarisatsioonimikroskoobis on ta maakmineraalile tüüpilisena läbipaistmatu. Lõhenevus ja magnetilisus puuduvad. Kullal on metalliläige. Maailma suurimad kullavarud asuvad Lõuna-Aafrika vabariigis Koostis / struktuur Keemiline element kuld (Aurum, Au)kristallstruktuur tahkkeskendatud kuubiline võre Omadused Kollane, pehme (kõvadus 2,5), Sulab temperatuuril 1337.33 K (1064.18 °C). Hea elektrijuht Keemiliselt inertne viimane väide aga lakkab olemast õige, kui tegemist on väga väikeste kullaosakestega Saamine Kulda leitakse looduses ehedana, nt. mineraal kvartsi pragudes ("kullasooned"), terakestena kulda sisaldunud kivimitest tekkinud liivas (kullaliiv). Uute kullaleiukohtade avastamine on sageli esile kutsunud nn. kullapalaviku (nt. 1897-1898
Elektronegatiivsus suurem,pehmemad.Tihti peetakse neid metalloidideks e. Poolmetallideks. Metallide kristallstruktuur- Mitmed paralleelsed kristallograafiliste tasandite kogum moodustab kristallivõre.On olemas: lihtsad(aatomid ainult võreelemendi sõlmedes),ruumkesendatud(lisaks võrelemendi tippudele ka diagonaalides sõlmes),tahkkesendatud(lisaks võre tippudele ka iga tahu keskel), põhitahkkesendatud(lisaks võre tippudele ka põhitahkude diagonaalide sõlmedes).Enamikel metallidel kas kuubiline või heksagonaalne.Polümorfismiks nim erinevate kristallivõrede esinemist ühel metallil.nt raud ja titaan.Isomorfismiks nim erinevate metallide kristallivõrede samakujulisust.nt Ag ja Au.Kristalli defektid-kristalli sisestruktuur ei ole täiesti korrapärane.Kristallis esinevad mitmesugused defektid,mis mõjutavad metallid omadusi.Kristallides esinevaid defekte liigitatakse:punktdefektid,
· vaakumtehnika · elektrilambid · meditsiinis -4- Andmed Aatomnumber: 55 Aatommass: 132,905 Klassifikatsioon: leelismetallid, s-elemendid Aatomi ehitus: · Elektronvalem: 1s2 2s2p6 3s2p6d10 4s2p6d10 5s2p6 6s1 · Elektronskeem: +55|2)8)18)18)8)1) · Elektronite arv: 55 · Neutronite arv: 78 · Prootonite arv: 55 · Oksüdatsiooniast(m)e(d) ühendites: 0, 1 · Kristalli struktuur: ruumikeskne , kuubiline Füüsikalised omadused: · Aatommass: 132,905 · Sulamistemperatuur: 28,4 °C · Keemistemperatuur: 705 °C · Tihedus: 1,873 g/cm3 · Värvus: kuldkollane · Agregaatolek toatemperatuuril: tahke · Kõvadus Mohsi järgi: 0,2 · Isotoobid: -5- Nukliid Levimus (%) Mass Poolestusaeg 126 Cs 0 126 1,64 minutit
kergem rauast. Kuna uue metalli saamise lähtaineks olid ammu tuntud maarjased (ladina keeles alumen ), siis hakati ka metalli nim alumiiniumiks. Alumiinium, keemiliste elementide perioodilisussüsteemi III rühma element. Järjenumber on 13,aatommass 26,98154. Alumiiniumi sulamistemperatuur on 660C ja keemistemperatuur 2060C. Alumiiniumi tihedus on 2,7 Mg/m. Alumiiniumi koostis / struktuur: Keemiline element alumiinium (Al), kristallstruktuur tahkekeskendatud kuubiline võre. Alumiiniumi Omadused : Hõbedase värvusega, kerge (tihedus 2700 kg/m3), pehme metall, hea elektri- ja soojusjuht (eritakistus 2.65·10-8 m ). Alumiinium sulab temperatuuril 660.32 °C (933.47 K). Alumiinium on võrreldamatult hea materjal uste, fassaadide, valguskatuste, talveaedade ja akende valmistamiseks, sest see ei korrodeeru ja seda on kerge töödelda. Alumiiniumist konstruktsioonid on pikaealised ja kergesti hooldatavad.
· Elektronite arv: 3 · Neutronite arv: 4 · Prootonite arv: 3 · Oksüdatsiooniast(m)e(d) ühendites: 0, I · Kristalli struktuur: ruumikeskne kuubiline Füüsikalised omadused: · Aatommass: 6,947 · Sulamistemperatuur: 180,54 °C · Keemistemperatuur: 1342 °C · Tihedus: 0,53 g/cm3 · Värvus: hõbevalge/hall · Agregaatolek toatemperatuuril: tahke · Kõvadus Mohsi järgi: 0,6 · Isotoobid: Nukliid Levimus (%) Mass Poolestusaeg 6 Li 7,42 6,0151 - 7
Õhus oksüdeerub kaalium energiliselt. Keemilised omadused: Oksiidi tüüp: tugevaluseline Aatomnumber: 19, Aatommass: 39,098, Klassifikatsioon: leelismetallid, s- elemendid Aatomi ehitus: Elektronvalem: 1s2 2s2p6 3s2p6 4s1 Elektronskeem: +19|2)8)8)1) Elektronite arv: 19 Neutronite arv: 20 Prootonite arv: 19 Oksüdatsiooniast(m)e(d) ühendites: 0, I Kristalli struktuur: ruumikeskne kuubiline Lihtaine saamine: Kaaliumit saadakse sulatatud KOH elektrolüüsil: 4KOH 4K (katoodil) + 2H2O + O2 (anoodil) Nüüdisajal toodetakse kaaliumi metalse naatriumi ja kaaliumkloriidi sulandist 850 ºC juures: Na + KCl NaCl + K K eraldub auruna, mis kondenseeritakse metalse kaaliumi saamiseks. Kaaliumi eraldumine sulatatud kaaliumkloriidi elektrolüüsil on raskendatud, sest K lahustub sulas kaaliumkloriidis. Mis jaoks?
aatomeile paikneb üks aatom võreelemendi sees diagonaalide sõlmpunktides KRISTALLVÕRE TÜÜBID Tahkkesendatud – lisaks võreelemendi tippudes olevatele aatomitele paiknevad aatomid iga tahu keskel diagonaalide sõlmpunktides Põhitahkkesendatud – liskas võreelemendi tippudes olevatele aatomitele paiknevad aatomid põhitahkude keskel diagonaalide lõikepunktides Kristallvõre tüübid Enamikul kasutatavatel metallidel on kuubiline või heksagonaalne kristallvõre. Põhitahkkesendatud heksagonaalvõres võib paikneda veel 3 aatomit, moodustades kompaktse heksagonaalvõre. Kristallvõre tüübid ruumkesendatud kuupvõre (K8): Ba, Crα, Feα, K, Mnα, Mo, Na, Uβ, V, Wβ; tahkkesendatud kuupvõre (K12): Ag, Al, Cu, Ca, Coβ, Cu, Feγ, Ni, Pb, Pt, Snα; kompaktne heksagonaalvõre (H12): Beα, Cd, Coα, Crβ, Mg, Tiα, Zn Kristallvõre tüübid
Süsinikusisaldus teeb raua kõvemaks ja suurendab tunduvalt tõmbetugevust, kuid teras on rauast rabedam. Legeerterased Legeerterased sisaldavad peale raua ja süsiniku veel legeerivaid lisaaineid, mis parandavad mitmeid terase omadusi. Enamkasutatavad legeerivad terased on : nikkel, kroom, mangaan, räni, vask ja volfram. Vask Keemiline element vask (Cuprum, Cu), kristallstruktuur tahkkeskendatud kuubiline võre. Punakas-kollaka värvusega metall, tihedus 8920 kg/m3 , hea elektri- ja soojusjuht (eritakistus 1.7·10-8 Wm). Sulamistemperatuur 1084.62 °C. Välistingimustes tekib vase pinnale aja jooksul rohekas kattekiht (paatina) [15.08.04], mis kujutab endast erinevate vase hüdraatsoolade segu (sulfaat, karbonaadid). Vase sulamitest on peamised messing ja pronks. Messing on vase ja tsingi sylam. Pronks on vase ja inglistina sulam, harvem on ta vase ja alumiiniumi sulam. Vase
uks aatom voreelemendi sees diagonaalide solmpunktides Tahkkesendatud (face-centered)- lisaks voreelemendi tippudes olevaile aatomeile paiknevad aatomid iga tahu keskel diagonaalide solmpunktides Põhitahkkesendatud (base-centered)- lisaks voreelemendi tippudes olevaile aatomeile paiknevad aatomid pohitahkude keskel diagonaalide loikepunktides Lihtne trikiliinne Lihtne monokliinne Lihtne Rombiline Heksagonaalne Rombeedriline Lihtne tetragonaalne Ruumkesendatud tetragonaalne Tahkkesendatud kuubiline Kristallvõret iseloomustavad suurused: Võreperiood Võrebaas (n) Võre koordinatsiooniarv (k) Aatomi raadius (R) Võre kompaktsusaste ehk ruumpakketihedus () Polümorfism (polymorphism)- metalli voi mittemetalli erinevate kristallivorede esinemine. Isomorfism- erinevate metallide kristallivorede samakujulisus. Isomorfsete ainete kristallivoredel on ligilahedased voreperioodid, aatomi raadiused. 5. Metallide ja sulamite füüsikalised omadused. Tihedus. Sulamistemperatuur. Kõvadus. Elastus.
Munajuha tuba uterina salpinx X Emakas uterus metra X Tupp vagina colpos X 9. Munasari Ehitus Munasari kaalub ~510 g. Munasari on lapikovaalne ploomikivi meenutava kujuga sugunääre. Munasari on kaetud sidekoelise valgundkestaga, mille välispinda katab kuubiline epiteel. Ülemine ots on suunatud munajuha poole, alumine ühendub emakaga. Munasarja siseehituses eristatakse koort ja säsi. Funktsioon toimub munarakkude kasvamine ja areng ning toodetakse naissuguhormoone. 10. Selgitage mõisted: Folliikulid Põiekesed, kus on sees munarakud. Ühes põies on sees 1 munarakk. Ovogenees munaraku valmimine ovogoonoist meioosi käigus Spermatogenees Spermi valmimine meioosi käigus spermatogoonist
Kullast ja hõbedast on vaske aga tunduvalt rohkem. Vasemaagiräbu vanuseks hinnatakse 8000 aastat. Seni leitud suurima eheda vasetüki mass on 420 tonni. Aatomi ehitus: Aatomnumber: 29 Aatommass: 63,546 · Elektronvalem: 1s2 2s2p6 3s2p6d10 4s1 · Elektronskeem: +29|2)8)18)1) · Elektronite arv: 29 · Neutronite arv: 35 · Prootonite arv: 29 · Oksüdatsiooniast(m)e(d) ühendites: 0, I, II, III, IV Kristalli struktuur: tahukeskne kuubiline Vase füüsikalised omadused: · Aatommass: 63,546 · Sulamistemperatuur: 1083,4 °C · Keemistemperatuur: 2567 °C · Tihedus: 8,96 g/cm3 · Värvus: punakas · Agregaatolek toatemperatuuril: tahke · Kõvadus Mohsi järgi: 3,0 Vase keemilised omadused: · Elektronegatiivsus Paulingu järgi: 1,9 · Oksiidi tüüp: nõrkaluseline · Ühendid: Fluoriidid: CuF, CuF2 Kloriidid: CuCl, CuCl2, CuCl2 · 2H2O Bromiidid: CuBr, CuBr2
muudab tükk ka oma kuju. Kuna sool lahustub vees ei tohi mitte mingil juhul soolalampi õue asetada ega ei tohi niiskelt puhastada. [1] Keedusoola põhistruktuur on lihtne kuubikujuline kristallisüsteem. Soolakristallid on puhtas olekus värvitud ja läbipaistvad. Üksikutel kuupidel võib serva pikkus olla mitu sentimeetrit. On leitud koguni soolakuupe, mille serva pikkus ulatub lausa meetrini. Soolalambi kivisoolakamaka struktuur on samuti kuubiline. Oma spetsiifilise värvi saab sool suletistelt. Oranzpunaka värvi annab raud (III) oksiid. Sinised ja lillad värvitoonid tekivad haliidi kiiritamisel. Halli värvi tekitavad bituumeni või savi osakesed, pruun ja must toon tulenevad aga orgaaniliste ainete suletistest. Lambist eralduv soojus just nagu aktiveeriks soola, suurendades selle kiirguse intensiivsust ja ulatust. Isegi ainult teeküünlaga väike soolalamp võib ruumi atmosfääri märgatavalt parandada
Leidumine( tootmine): Kaltsiumoksiidi (CaO) toodetakse tööstuses tavaliselt lubjakivi või muude kaltsiumkarbonaati sisaldavate ainete termilise lagundamise teel. Põletatakse lubjakivi Omadused: Kaltsiumoksiid on valge, hallikasvalge, kahvatukollane või kahvatuhall aine. Tööstuslikult toodetud kaltsiumoksiidil on rauasisalduse tõttu kollakas või pruunikas varjund. Kaltsiumioksiid on kristalne aine (kõva teraline mass või pulber). Struktuur on tahkkesendatud kuubiline. Molaarmass on 56,08 g/mol. Normaaltingimustel on ta tahke, sulamistemperatuur on 2572 °C (2845 K). Keemistemperatuur on 2850 °C (3123 K). Tihedus on 3,37...3,38 g/cm³. Aur on veeaurust 1,9 korda tihedam. Auru rõhk on 1455 °C juures 1,8×10-6 mmHg. Lahustub hästi vees. Kaltsiumoksiid ei lendu ning on lõhnatu. Soojuspaisumistegur on 3,92...6,73×10-5 /K. Kasutamine: Kaltsiumoksiid reageerib ägedalt veega, nii et tekib kaltsiumhüdroksiid ehk kustutatud lubi
Stelliidiga kaetakse ainult lõikeinstrumendi hammaste tipud Saekettad Raamsaed Lintsaed . Ülikõvad materjalid Puidu töötlemiseks on välja töötatud sünteetilised ülikõvad materjalid, millel on väga suur kõvadus ja kulumiskindlus Sellised teramaterjale kasutatakse, kui on vaja suure tootlikkusega töödelda selliseid teravanulikke materjale nagu ristvineer puitlaasplaat, MDF-plaat . Kuubiline boornitriid (BN) TOOtenimi Borazon Materjalil on kuubiline kristallvõte ja oma ehituselt ja omadustelt on ta sarnane teemandile. Borazonil on isegi suurem temperatuuri kindlus kui teemandil . Kõvadus on teemandiga võrreldav . Boornitriidi valmistatakse 8…10 mm ja 1 cm pikkuse silindritena, mis joodetakse lõikeriista korpused külge. Kui lõikeserv on pikem, kui tuleb kõrvuti joota mitu silndrit .
säilitada nimi Kupfernickel, lühendades selle Nickel'iks. Tema avastust kinnitasid ka teised teadlased. Asukoht tabelis. Nikkel paigutatakse keemiliste elementide perioodilisussüsteemis VIIIB rühma. Nikli aatommass on 59 ning järjenumber 28. Elektronvalem: 1s2 2s2p6 3s2p6d8 4s2 Elektronskeem: +28|2)8)16)2) Elektronide arv: 28 Neutronite arv: 31 Prootonite arv: 28 Oksüdatsiooniast(m)e(d) ühendites: -I...II...IV Kristalli struktuur: tahukeskne kuubiline Nikli aatomi ehitus: -1- Energia levelid : 4 Esimene energia level: 2 Teine energia level: 8 Kolmas energia level: 16 Neljas energia level: 2 Elemendi saamine: Elementide leidumisest maakoores on nikkel 25ndal kohal. Looduses leidub niklit ainult ühenditena.Tähtsamad mineraalid on nikeliin NiAs, pentlandtiin (Fe,Ni)9S8 ja milleriit NiS. Tuntakse mitmeid nikli maake, kuid peamiselt toodetakse niklit sulfiidsetest maakidest (NiS)
kaasa 1440. aastatel prindi operaatorite mürgitamise. Samal ajal leiutati ka tulirelvad ning pliist hakati tegema kuule. 20. sajandi lõpul hakati tootma pliiakut. (wikipedia.ee) 2. PEAMISED MAAGID JA LEIUKOHAD 2.1 Peamised maagid Tähtsaimad mineraalid on galeniit (pliiläik) PbS ja anglesiit PbSO4. Pliid leidub alati uraani- ja tooriummineraalides (moodustab nende radioaktiivse lagunemise). Galeniit on raske sulfiidne mineraal, mis on peamine pliimaak. Ta on hõbehalli värvi, kuubiline ja läikiv. (Kaevats, Varrak, 1994) 2.2 Peamised leiukohad Pliid võib leiduda nii kosmoses kui ka maa peal. Kosmoses toimuvad erinevad protsessid, mille käigus tekib plii. Kosmoses toimub kaks protsessi - Aeglane (slow-s) ja kiire (rapid-r). Mõlemad protsessid toimuvad tähtede sees või nende ümber. Aeglases (s) protsessis toimub plii loomine aastate või sajandite vältel. Pika aja jooksul muutuvad vähem stabiilsed tuumad beetakiirguse all stabiilseteks tuumadeks
Suurt osa metallist kasutatakse ainult üks kord, selle korduvkasutus on liiga kulukas. NB!! Elavhõbe ja tema ühendid on väga mürgised. Väga mürgine on ka elavhõbeda aur. Elavhõbe on mürgine nii inimese, kala kui ka looma närvisüsteemile. Elavhõbe siseneb kehasse elavhõbeda auru sissehingamisel või tilga imbumisel läbi naha. Väikesed elavhõbeda tilgad aurustuvad isegi toatemperatuuril. Plii (Pb) Keemiline element Plii (Plumbum, Pb), tahkkeskendatud kuubiline võre. Keemiliste elementide perioodilisustabelis asub Plii IVA rühmas ja 6.perioodis. Sinakas-valkjas pehme (kõvadus 1,5) raske (tihedus 11340 kg/m3) metall. Sulamistemperatuur 327.46 °C. Plii on radioaktiivsete elementide lagunemisridade stabiilne lõpp-produkt. Plii ei ole eriti hea elektrijuht (eritakistus 2,08·10-7 Wm) võrreldes hästi elektrit juhtivate metallide kulla, hõbeda, vase ja alumiiniumiga, muutub aga ülijuhiks
Koostis / struktuur : Element plii (Plumbum, Pb), tahkkeskendatud kuubiline võre. Omadused : Sinakas-valkjas pehme (kõvadus 1,5) raske (tihedus 11340 kg/m3) metall. Sulamistemperatuur 327.46 °C. Plii on radioaktiivsete elementide lagunemisridade stabiilne lõpp-produkt. Plii ei ole eriti hea elektrijuht (eritakistus 2,08·10-7 Wm) võrreldes hästi elektrit juhtivate metallide kulla, hõbeda, vase ja alumiiniumiga, muutub aga ülijuhiks elementaarmetallidest kõige kõrgemal temperatuuril (7,196 K). Saamine :
kõrge rõhk) , vähemlevinud Tina 0 3 -tina -tavaline hõbevalge tetragonaaln püsiv üle 13,2 C Tihedus 7,28 g/cm tina e kristallvõre 0 -tina - HALL, Teemanti 13,2 C madalamal temperatuuril kuubiline 3 PULBRILINE TINA tüüpi kristallvõre, POOLJUHT. Tihedus 5,75 g/cm kristallvõre Madalatel temperaturidel hõbevalge metall pudeneb halliks pulbriks ( ruumala suureneb 25 %) Seda nähtust nimetatkse TINAKATKUKS
tunnus. 13. Mis on Mohsi kõvadusskaala ? Kõvadus on mineraalidel iseloomulik ja tähtis tunnus. Etaloniks on võetud 10 mineraali, kus iga mineraali kõvadus tähistab teatud kõvadusastet: Talk 1; kips 2; kaltsiit 3; fluoriit 4; apatiit 5; Ortoklass 6; kvarts 7; topaas 8; korund 9; teemant 10; 14. Kuidas jaotatakse kristallid vastavalt sümmeetriarikkusele ? Jaotatakse seitsmesse kristallograafilisse süngooniasse. Need on: Kuubiline, heksagonaalne, tetragonaalne, trigonaalne, rombiline, monokliinne, trikliinne. 15. Mida nimetatakse kivimiks ja kuidas neid eristatakse ? Kivimit võiks määratleda kui kindla koostise ja ehitusega mineraalide kogumit maakoores, mis on tekkinud geoloogiliste protsesside tulemusena. Sõltuvalt kivimi teket põhjustatud teguritest eristatakse kolme kivimirühma tardkivimeid, settekivimeid ja moondekivimeid. 16
säilinud kristalli sümmeetria elemendid. Elementaarraku küljed ja nurgad on võre parameetrid. Võre baasiks nimetatakse aatomite gruppi, mis kuulub elementaarrakku. Ideaalne kristall saadakse sellise grupi lõpmatukordsel kordamisel järjestikusel nihutamisel võre vektorite suundades. Vastavalt elementaarrakus asetsevate aatomite asukoha järgi on elementaarrakul seitse klassi (trikliinne, monokliinne, rombiline (ortorombiline), heksagonaalne, romboeedriline, tetragonaalne ja kuubiline). Neile vastab 14 Bravais' võret. Sama süngoonia piires eristuvad Bravais' võred võresõlmede asendite poolest: primitiivsed (P, võresõlmed vaid kokkuleppelise raku tippudes), ruumtsentreeritud (I, lisaks üks kokkuleppeline võresõlm), tahktsentreeritud (F, lisaks neli kokkuleppelist võresõlme) ja baastsentreeritud (C, lisaks kaks kokkuleppelist võresõlme) võred. Bravais' võre sõlmed võivad aga ei pea kokku langema füüsiliste aatomite asukohtadega. Kui vaadata kristalli
Kuld on väärismetall.Normaaltingimustel on ta võrdlemisi pehme kollane metall, mille tihedus on 19,7 g/cm³. Kulla sulamistemperatuur on 1064°C.Kuld on isotroopne kuubilise süngoonia mineraal. Polarisatsioonimikroskoobis on ta maakmineraalile tüüpilisena läbipaistmatu. Lõhenevus ja magnetilisus puuduvad. Kullal on metalliläige.Maailma suurimad kullavarud asuvad Lõuna-Aafrika Vabariigis. Koostis / struktuur Keemiline element kuld (Aurum, Au), kristallstruktuur tahkkeskendatud kuubiline võre. Omadused Kollane, pehme (kõvadus 2,5), raske (tihedus 19 300 kg/m3) metall. Sulab temperatuuril 1337.33 K (1064.18 °C). Hea elektrijuht (eritakistus 2,2·10-8 Wm). Keemiliselt inertne viimane väide aga lakkab olemast õige, kui tegemist on väga väikeste kullaosakestega. Nn. nanokuld on näiteks väga efektiivne vingugaasi (toatemperatuurse) osüdatsiooni katalüsaator . Saamine Kulda leitakse looduses ehedana, nt. mineraal kvartsi pragudes ("kullasooned"),
.......................................................................................... 31 4.2. Ruumvõre ja ühikrakk (joonis 3.2)........................................................................... 31 4.3. Kristallsüsteemid ja Bravais võred (joonis 3.3, 3.4). ................................................ 31 4.4. Põhimised kristallstruktuurid metallides (joonis 3.7, 3.8) ....................................... 32 4.4.1. Ruumtsentreeritud kuubiline kristallstruktuur (joonis 3.9, 3.10, 3.11). ......... 33 4.4.2. Pindtsentreeritud kuubiline kristallstruktuur (joonis 3.12, 3.13, 3.14). .......... 33 4.4.3. Heksagonaalse tihedaima pakkimisega kristallsüsteem (joonis 3.15, 3.16) ... 34 4.5. Kuubiline elementaar-rakk ...................................................................................... 34 4.5.1. Aatomite asendid kuubilises elementaarrakus (joonis 3.17) ........................
raudbetoonkonstruktsioonile, *Lintakem, *Vaba põhiplaan, kaldtee, *Lamekatus ja katusead. Mason Cook, Villa Meyer, Graches´i Villa, Poissy Savoye Villa, Mason Dom- Ino. Frank Lloyd Wright ja tema loomingu erinevad etapid (preeriastiil, orgaaniline arhitektuur, Broadacre City) Linna vastane. Katsatas raudbetoonist konsoole. Arhitektuuril USA ühiskonda ümberkorraldav roll.USONIA Preeriastiil- traditsioonilised materjalid ja ehitusviis. Maalähedane vormikõne. Raudbetoon ja klaas-kuubiline, tahuline arhitektuur, klaas. tekib hoone kaalutu efekt. Postideta põhiplaan. Orgaaniline arhitektuur- betooni kasutamine looduläheda vormina.vormi ja ruumi ökonoomset loomist kooskõlas looduses peituvate põhimõtetega. Broadacare city- tulevikulinn on kõikjal ja ei kusagil. See kerkib ise ja juhuslikult. Mehaniseeritud väiketööstused. Mies van der Rohe looming Euroopas (funktsionalism) ja USA-s (minimalism) Bauhausi direktor. Internatsionaalse modernismi peaesindaja. Tehnika
mille juures tahk lõikab vastavat telge elementaarrakus. 31. Millise valemiga kirjeldatakse elektronide difraktsiooni? 32. Mis on elementaarrakk? Kristalses aines paiknevad aatomid kindla seaduspärasuse järgi, moodustades kolmemõõtmelise korduva struktuuri. Kõige väiksemat struktuuriühikut selles nimetatakse aine elementaarrakuks. Kõige lihtsam elementaarrakk on kuubi kujuline ja kõige lihtsam kristallvõre on kuubiline võre. 33. Mis on kristalne aine? Kristalses aines paiknevad aatomid kindla seaduspärasuse järgi, moodustades kolmemõõtmelise korduva struktuuri. 34. Mis on polükristalne materjal? Polükristall, aine juhuslikult orienteeritud kristalliitide kogum. 35. Mis vahe on mono ja polükristalli difraktsioonipildil? Monokristalli difraktsioonipildis on kõik difraktsioonipunktid selgelt eristatavad. Kui
kõrge elektri ja soojusjuhtivus, teiseks on nad tavalistes tingimustes kõrge kordinatsiooniarvuga kristallilised ained. Esimesesest iseärasusest järeldub, et vähemalt osa elektrone võib liikuda kogu metalli ulatuses. Teisest küljest võib metallide struktuuri tundes väita, et aatomid pole üksteisega ühinenud lokaliseeritud kaheelektroniliste sidemetega, sest aatomi valentselektronide arv ei ole piisav selliste sidemete moodustamiseks naaberaatomitega. Nii näiteks on liitiumil kuubiline ruumtsentreeritud võre, mistõttu igat kristalli aatomit ümbritseb kaheksa naaberaatomit. Sellise struktuuri korral peaks kaheelektroniliste sidemete moodustamiseks iga Li aatom andma kaheksa elektroni. See ei ole aga võimalik, sest liitiumi aatomil on vaid 2 1 üks valentselektron (1s 2s ). Seega seob metallides teatud arv elektrone üheaegselt paljude tuumade tsentreid. Elektronid võivad metallis ümber paigutuda, mistõttu metallides on tugevasti
aatom võreelemendi sees. c) Tahkkesendatud lisaks võrseelemendi tippudes olevatele aatomitele paiknevad aatomid iga tahu keskel. d) Põhitahkkesendatud lisaks võrdeelemendi tippudes olevatele aatomtele paiknevad aatomid põhitahkude keskel. Eri kristallvõre tüüpides võib paikneda enam aatomeid kui neid mahub kristallvõre sõlmpunktidesse. Enamikul kasutatavatel metallidel on kuubiline või heksagonaalne kristallvõre: · Ruumkesendatud kuupvõre: Cr; Fe; Mn; Mo; V; W · Tahkkesendatud kuupvõre: Ag; Al; Cu; Co; Fe; Ni; Pb; Pt; Sn · Kompaktne heksagonaalvõre: Be; Cd; Co; Cr; Mg; Ti; Zn Kristallvõret iseloomustadad suurused a) Võre periood teljesihiline aatomite vaheline kaugus on 0-0,7 mm b) Võrebaas võreelemendi kohta tulevate aatomite arv c) Võre koordinatsiooniarv võreelemendi mistahes aatomile lähimal ja võrdsel
jahutusvedelikku kasutatakse peamisel automaatpinkidel, kus on vaja säilitada pikem lõikuri püsivusaeg. Pinnakaredus- on pinna reljeef, mille moodustavad töötlemisel pinnasse jäänud konarused. Lõikurimaterjlid: Legeertööristaterase erirühma moodustavad kõrge volframi- ja vanaadiumi-sisaludsega terased. Kiirlõiketerasest lõikuri kõvadus pärast termotöötlemist on HRC 62...65 ja soojuskindlus kuni 600...640 C. Ülikõvade materjalide rühma moodustavad tehisteemant ja kuubiline boornitriit. Tehisteemanti ja kuublist boornitriidi sünteesitakse kahel kujul: pulbrina ja polükristallidena. Lõikuri teriku geomeetria: Lõikeprotsessist võtavad vahetult osa järgmised teriku pinnad. Esipind-on pind, millesse siseneb lõikekiiruse vektor. Lõikeserv- on teriku eri- ja tagapinna lõikumisel tekkiv lõikejoon. Tipp- on pea- ja abilõikeservade liitekoht. Lõikesrevanurk ja abilõikeservanurk määravad otseselt pinnakareduse.
materjalid) sumbub osa võngetest kristallivõre tühemikes - väiksem sooojuspaisumine. Keraamika soojuspaisumine võib olla anisotroopne. 5.4 Kõvadus Kõvadus on oluliseim kulumiskindluse seisukohast. Suur kõvadus võidakse saavutada ainult pinnakihis (keraamiline pinne) või kogu materjali mahus. Kõvadus säilib kõrgete temperatuuridel kuni 1000 °C. Keraamiliste materjalide hulgas on suurima kõvadusega materjalid: teemat, kuubiline boornitriid, ränikarbiid. Keraamilisi materjale kasutatakse palju abrasiividena. Lõplik kõvadus saadakse peale paagutust, peale seda saab töödelda vaid (teemant)lihvimise abil. 5.5 Elektrilised omadused Enamik keraamilisi materjale on isolaatorid. Eriotstarbelise keraamika hulka võivad siiski kuuluda elektrijuhid, pooljuhid. Keraamilistel materjalidel võivad olla ka para-, ferro-, ja piesoselektrilised omadused. Sõltuvalt vajadusest võidakse omadusi reguleerida koostise,