Joonistel on kujutatud gaaside kogumise erinevad võimalused. Millistel meetoditel saab koguda järgmiste omadustega gaase (märkige lünkadesse sobiva(te)le meetodi(te)le vastava(te) joonis(t)e ees olevad numbrid). Kirjutage iga gaasi tüübi kohta näide (vastava gaasilise aine valem). Meetodi(te) Gaasi valem number(rid) A. Gaas on õhust raskem ja tema lahustuvus vees on väga väike _________ __________ B. Gaas on õhust kergem ja tema lahustuvus vees on väga väike _________ __________ C. Gaas on õhust raskem ja lahustub (suhteliselt) hästi vees _________ __________ D. Gaas on õhust kergem ja lahustub (suhteliselt) hästi vees _________ __________ 2 ÜLESANNE 6 (6 punkti) Kirjutage lõpuni järgmiste vesilahuses kulgevate reaktsioonide lühendatud ioonvõrrandid.
steriliseeritakse, suhkrut ei lisata Kondenseeritud piima ja koore säilivusaeg 1 aasta,väljastatakse metalltaaras Kuivatatud piimatooted Saadakse tooraine kuivatamisel pihustus- või kontaktmeetodil, mille tulemusel saadakse pulber. Toorained on: piim, lõss, rõõsk koor, pett ( võipiim) ja vadak ( hapupiimavesi) *pihustusmeetod tooraine pihustatakse spets. Kambris, kuivatatakse kuuma ja kuiva õhuga, lahustuvus 98-99% *kontaktmeetod tooraine suunatakse peenikese joana kuumale pöörlevale trumlile, mis kuivabkilena trumli pinnale. Eemaldatakse ja jahvatatakse, madalama kvaliteediga, lahustuvus 70 - 85% Liigitus: ·olenevalt kuumutamise astmelt: - kõrgelt kuumutatud piimatooted - keskmiselt kuumutatud piimatooted - madalalt kuumutatud piimatooted ·Rasvasisalduse ja tooraine järgi: - koorepulber
Polümeeride liigitus: termoplastsed – lineaarstruktuuriga(kuumutamisel lähevad voolavasse olekusse) ja termoreaktiivsed – võrkstruktuuriga(kuumutamisel ei lähe voolavasse olekusse). 20. Mis on lahus? Millest see koosneb? Nimeta agregaatoleku järgi eristatavaid lahuseid! Lahus on homogeene süsteem, mis koosneb lahustist ning lahustunud ainest. Lahused: gaas-gaas, gaas-vedel, gaas-tahke, vedelik-vedelik, vedelik-tahke, tahke-tahke. 21. Lahustumise põhireeglid. Temp tõustes lahustuvus kasvab, igal lahustil küllastuspunkt. 22. Mis on lahustuvus? Mis on küllastuspunkt? Lahustuvus on aine omadus lahustuda lahuses. Küllastuspunkt on punkt, millal lahustisse ei saa enam ainet lahustuda. 23. Kuidas jagatakse lahuseid lahustunud aine sisalduse järgi? Iseloomusta lühidalt! Küllastumata lahus – lahustis saab veel ainet lahustuda. Küllastunud lahus – antud temp ja rõhul maksimaalselt ainet lahustunud lahustis
Soolade ja hüdroksiidide lahustumine vees, vee elektrijuhtivus, rasklahustuvate ühendite lahustuvus, lahustuvuskorrutised, sademe tekkimine. Vee karedus, mööduv ja jääv karedus. Lämmastiku- ja fosforiühendid vees, nende kontsentratsioonide väljendusviisid. Lämmastikuühendite transformatsioon keskkonnas, nitrifikatsioon, denitrifikatsioon. Veekogude eutrofeerumine. Orgaanilised saasteained keskkonnas. Orgaaniliste saasteainete keskkonnaohtlikkus, näiteid orgaanilistest saasteainetest; orgaaniliste ainete lagunemine keskkonnas, biolagunemine ja
Raua ja süsiniku ke D. Raua ja süsiniku eu Score: 1,5/1,5 9. Mis on ferriit (F) Student Response A. Süsiniku tardlahus B. Süsiniku tardlahus C. Raua ja süsiniku ke D. Raua ja süsiniku eu Score: 1,5/1,5 10. Palju on Ferriidi süsiniku lahustuvus toatemperatuuril tasakaaluolekus(massiprotsentides)? Student Response A. 0.01% B. 0.02% C. 0.8% D. 6.67% Score: 1,5/1,5 11. Palju on Austeniidi maksimaalne süsiniku lahustuvus 1147 C (massiprotsentides)?
1. Sissejuhatus. Lahus on kahest või enamast komponendist (lahustunud ained, lahusti) koosnev homogeenne süsteem. Sarnane lahustub sarnases. Ioonvõrega ja polaarsed ühendid lahustuvad üldjuhul paremini polaarsetes lahustites (soolad, alused, happed vees), mittepolaarsed ühendid mittepolaarsetes lahustites. Gaaside lahustuvus Gaaside lahustuvus väheneb temperatuuri tõusuga ja suureneb rõhu kasvuga. Gaaside lahustuvus vees väheneb, kui vesi sisaldab lahustunud soolasid. Henry seadus. Gaasi lahustuvus vedelikus on proportsionaalses sõltuvuses gaasi osarõhuga lahuse kohal CM k h p kus, 1.1 CM – gaasi molaarne kontsentratsioon lahuses mol/dm3 p – gaasi osarõhk lahuse kohal atm kh – antud gaasile temperatuurist sõltuv konstant (nn Henry konstant). Lahuste kontsentratsioon
p p10 X 1 p 20 X 2 p10 (1 X 2 ) p 20 X 2 p10 ( p10 p 20 ) X 2 . Seega püsival temperatuuril on ideaalse lahuse aururõhk koostise lineaarseks funktsiooniks. 4. Kõrvalekalded ideaalsest lahusest 5. Lõpmata lahjad lahused. Henry seadus. Lõpmata lahja lahus – väga lahja lahus, käitub peaaegu ideaalse lahusena. Lõpmata lahjades lahustes puuduvad vastastikmõjud lahustunud aine osakeste vahel. Henry seadus: Gaaside lahustuvus konstantsel temperatuuril on proportsionaalne nende osarõhkudega: C = KH P kus, KH on Henry konstant (mol/1 atm); C – gaasi kontsentratsioon lahuses (mol/l); P – gaasi osarõhk lahuse korral (atm). Võrrandit kasutatakse gaaside lahustumise iseloomustamiseks vedelikes. Võrrand kehtib ainult püsivalt lahjade lahuste korral. 6. Gaaside lahustumine vedelikes Gaaside lahustuvus väheneb temperatuuri tõusuga ja suureneb rõhu kasvuga. Gaaside lahustuvus vedelikes
Sademed võivad eralduda kristalliliste või koaguleerunud kolloidsete e amorfsete sademetena. Erineva iseloomuga sademete teket seletatakse tekkivate mikrokristallide erineva pindpinevusega lahuses. Sadestamine toimub lahjadest lahustest. Sadestaise puhul on ideaaliks jämekristalliline lisanditest vaba ade, mims on hästi pestav ja filtreeritav. Ei ole päris selge Osakeste suurust mõjutavad tegurid: - sademe lahustuvus, - temperatuur, - reageerivate ainete kontsentratsioon, - reageerivate ainete kokkusegamise kiirus Suhteline üleküllastus- SÜK = Q-S/S, kus Q kontsentratsioon, S lahustuvus Kõrge SÜKväikesed osakesed kolloidne sade Väike SÜK suured osakesed kristalne sade *tuumakeste moodustumine *osakeste suurenemine Edasi sõltub kumb on kiirem protsess: Kui tuumakeste moodustumine: sade koosneb suurest arvust väikestest osakestest;
Pindaktiivsed ained kogunevad gaas-vedelik, vedelik-vedelik, või vedelik-tahke aine piirpinnale ja orienteeruvad seal nii, et polaarne (hüdrofiilne) ots on pööratud polaarse keskkonna (vee) poole. Sel teel võivad pindaktiivsed ained mustusosakesi pinnalt lahti kangutada. Kuna pindaktiivsus ja adsorptsioonivõime kasvavad süsivesinikahela pikenedes, on mõjusamad sellised pindaktiivsed ained, mille molekulis on 12-18 C aatomit. Edasisel süsinikahela pikenemisel lahustuvus väheneb. Mitmete ainete, näiteks karboksüülhapete, amiinide, alkoholide puhul piirab pindaktiivsuse mõjule pääsemist aine vähene lahustuvus vees. Üks vanemaid ja tuntuimad detergente on seep. Kuid seebil, kui pesemisvahendil on ka mõningaid puudusi. Karedas vees moodustuvad rasvhapete kaltsiumi- ja magneesiumisoolad: 2RCOONa + Ca(HCO3)2 (RCOO)2Ca + 2NaHCO3 Need soolad vees ei lahustu ja sadenedes riidekiududele, takistavad pesemist
Aldehüüdid ja omadused ! Aldehüüdide nimetuse lõppliide on aal. Aldehüüdrühma süsinik võetakse tüviühendi süsinike nummerdamisel esimeseks (etanaal või etaan-1-aal, 3-metüülbutanaal või 3-metüülbutaan-1-aal) Vesiniksidemeid praktiliselt ei moodusta Enamik aldehüüde ja ketoone on kergesti lenduvad vedelikud. Metanaal, etanaal ja propanaal lahustuvad vees väga hästi kuid süsinikahela pikenedes lahustuvus väheneb. Aldehüüdid ja ketoonid on narkootilise toimega ja kahjustavad kesknärvisüsteemi. Mõjuvad ärritavalt limaskestale ja tekitavad põletikke. Aldehüüdid on mürgisemad kui ketoonid Aldehüüdide esindajad: Propenaal e akroleiin CH2=CHCHO Kergesti lenduv mürgine vedelik, lakrimaator (silmi ja nina ärritav, pisaraid tekitav) Tekib rasva kõrvetamisel pannil Bensaldehüüd C6H5-CHO Meeldiva lõhnaga vedelik Maitse- ja lõhnaaine (vanilliini saamine)
Kütuste põlemisel satub atmosfääri happelised oksiidid, mis reageerivad veeauruga ja tekib happelise reaktsiooniga sademed. (Keskkonna saastumine happeliste oksiididega: äike, vulkaanipursked, põlengud) Oksiidid, mis põhjustavad happevihmasid: vääveloksiidid (SO2 ja SO3) Lämmastikoksiidid (NO ja NO2) Süsihappegaas (CO2) TAGAJÄRJED: · Happesademed muudavad mullastiku keemilist koostist. Mulla hapestumisega mõnede anorgaaniliste ühendite lahustuvus paranab. Esialgu soodustab taime kasvu, kuid edasisel hapestumisel areng seiskub. · Taimede kasvu pidurdumine tuleneb sellest, et vajalikud keemilised elemendid uhutakse maapinna alumistesse kihtidesse. · Lisaks aeglustub ka orgaaniliste ainete lagundamine lagundajate poolt (happelises keskkonnas). · Metsade ulatuslik hävimine nt. Okaspuude hukkumine okaste kahjustumise tõttu. HAPPESADEMETE ÄRA HOIDMISEKS:
Füüsikaline nähtus Ainetega toimuvad muutused kusjuures ained ise jäävad samaks. Keemiline nähtus Ühtedest ainetest tekivad teised kulgeb keemiline reaktsioon. tunnus värvuse muutus , lõhna teke , sademe teke gaasimullide teeke , soojuse eraldumine ja valguseefekt tingimused kuumutamine , süütamine,valgustamine,elektri läbijuhtimine lahus on ühtlane segu Ainet kus oskaesed om ühtlaselt jaotatud nim- lahustiks aine mis teises ühtlaselt jaotunud nim lahustunud aineks. Lahustuvus näitab suurimat aine kogust mis võib kindlal temperatuuril lahustuda mingis kindlas lahusti koguses Valguse levimise kiirus võrdub teepikkus jagatud ajaga. ( v = s / t ) V=valguse levimise kiirus ( 300 000 km / s) s = teepikkus t = aeg Optiline tugevus võrdub fookuskauguse pöörd väärtusega ( D = 1 / f ) D = optiline kaugus f = fookuskaugus D jagatud 1m = f
PESUVALGENDI (NaClO) CAS number: 7681-52-9 Nimetus: Naatriumhüpokloriid Valem: NaClO, molaarmassiga 74.442 g/mol Teised nimetused: Antiformin, Modifitseeritud Dakini lahus, Surgical chlorinated soda solution, Carrel-Dakin'i lahus Omadused: Rohekas kollane tahke aine, magusja lõhnaga. Sulab 18 kraadi ja keeb 101 kraadi juures Celsiuse järgi. Vees lahustuvus on 29.3g/100ml. Toimib pesuvalgendina, plekieemaldina. Tüüpiliselt on kodukasutuses pesuvalgendina lahus 3-8% naatriumhüpokloriidi sisaldusega. Veepuhastina kasutatakse 12-15% sisaldusega lahust. Veel kasutatakse seda lõhna/plekieemalduseks, disinfektsiooniks. Keskkonda sattudes moodustab püsivaid kloororgaanilisi ühendeid. Satuvad nt. reoveepuhastitesse heitveena. Tugev oksüdeerija, võib kahjustada nahka või silmi.
Aeroioonid: posit (H2O +, O2+ jt) ja neg (O3, O, O2, H2O) Neg kasulikud elusorganismidele, teeb õhu värskemaks. Tööstuse ja transpordi heitgaasid, soojuse ja elektrijaamade tootmine > saastumine 4) Kristallvõre tüübid I Aatomvõre kristallivõre sõlmedes asuvad aatomid, mis on omavahel seotud kovalentse sidemega. Tugeva sideme tõttu on ainetel suur kõvadus, kõrge sulamistemp, väike lahustuvus ja lenduvus. II Molekulivõre sõlmpunktides neutraalsed molekulid, mis on seotud nõrkade van der Waalsi jõududega. Tüüpiline anorg ühenditele ja tahkestunud gaasidele: H2O, HF Madal võreenergia Kergsulavad, sublimeeruvad III Ioonvõre kristallvõre sõlmedes on vaheldumisi posit ja neg ioonid Suur kõvadus, kõrge keemis ja sulamistemperatuur
· Destilleerimine · Aurutamine · Jaotuslehter LAHUSED Mõisted · Lahus Kahest või enamast ainest koosnev ühtlane segu. · Lahusti Aine, milles lahustunud aine on ühtlaselt jaotunud. · Lahustunud aine Aine, mis on lahustis ühtlaselt jagunenud. · Küllastunud lahus Lahus, lahustunud aine sisaldus antud tingimustel on maksimaalne. · Küllastumata lahus Lahus, milles antud tingimustel saab veel ainet lahustada. · Lahustuvus Suurim aine kogus, mis võib lahustuda kindlas lahusti (või lahuse) koguses kindlal temperatuuril. · Pihussüsteem ehk pihus Segu, milles üks aine on suhteliselt ühtlaselt pihustunud teises. · Kolloidlahus - Pihus, milles pihustunud aine osakeste mõõtmed on 10-7 10-5 cm. · Aerosool Vedelik on pihustunud gaasis. · Emulsioon Vedelik on pihustunud vedelikus. · Suspensioon Tahke aine on pihustunud vedelikus.
Küllastunud lahus- lahus, mis sisaldab antud temperatuuril ja rõdul maksimaalse koguse lahustunud ainet ( tasakaaluolek). Üleküllastunud lahus- aeglasel jahtumisel saadud ebapüsiv süsteem, mis sisaldab lahustunud ainet üle lahustuvusega määratud koguse. Vähesel mõjutamisel ( loksutamine, tahke aine kristallikese lisamine) liigne ainehulk eraldub. Väljasadenemine- lahustunud aine eraldumine lahusest Henry seadus- gaasi lahustuvus vedelikus on proportsionaalses sõltuvuses gaasi osarõhuga lahuse kohal. Cm=kh*p · Massiprotsent maine *100 C% = mlahus · Molaarne konsentratsioon(CM) naine m * Vlahus CM = = aine Vlahus M aine · Molaalsus (Cm) n aine Cm = mlahusti · Moolimurd (Cx) naine Cx = naine + nlahusti
IUPAC nimi: 1,2,3,4,5-pentaklorobenseen Struktuurvalem: C6HCl5 3 Füüsikalised omadused o Suhteline tihedus: 1.8 (vesi = 1) o Auru rõhk, Pa 25°C: ligikaudu 2 o Auru suhteline tihedus (õhk = 1): 8.6 o Auru / õhu suhteline tihedus 20 °C (õhk = 1): 1.00 o Molekulaarmass: 250.337 Sulamistemperatuur: 86°C Keemistemperatuur: 275-277°C Vees lahustuvus: 0.831 mg/L (25°C juures) Etanoolis lahustuvus: ei lahustu. Muudes lahustites lahustuvus: lahustub kloroformis, benseenis, eeteris, süsiniktetrakloriidis, süsinikdisulfiidis. log POW: 5.03-5.63 KOC: 17,378 Henry seaduse konstant H: 7,03*10-4 atm*m3/mol Kineetika ja metabolism Pentaklorobenseen jõuab organismi süües või juues saastunud sööki ja vett ning hingates sisse saastunud õhku
Select one or more: 1. Al-Mg sulamid ehk magnaaliumid 2. Al-Si sulamid ehk silumiinid 3. puhas Al 4. Al-Cu sulamid ehk duralumiiniumid Question 4 Correct Mark 4.00 out of 4.00 Question text Mis asjaolul põhineb alumiiniumisulamite termotöötluse võimalikkus (karastamine ja vanandamine)? Select one: 1. Kuumutamise käigus muutuvad sulami omadused pinnakihi läheduses - nt. nitriitimine, tsementiitimine 2. Sulamites esineb piiratud lahustuvus, mis erineb suuresti madalal ja kõrgel temperatuuril - nt. toatemperatuuril Cu lahustuvus Al-s max. 0,2% ning 548 oC juures max. 5,7% 3. Termotöötluse võimalikkus põhineb Gaussi teoreemil 4. Õige kuumutustemperatuuri valiku ja jahutusreziimi põhjal on enamus sulameid termotöödeldavad Question 5 Correct Mark 4.00 out of 4.00 Question text Millised on karastatud duralumiiniumisulami omadused ning mikrostruktuur (kõrgele temperatuurile kuumutatud sulam on jahutatud kiirelt)
Polüpeptiidid e. valguahelad on peptiidsidemetega seotud aminohappejääkide ahelad, millest koosnevad valgud. 2. Ühine Sisaldavad karboksüülrühma (-COOH) Erinev aminohapped sisaldavad aminorühma (-NH2) 3. Karboksüülrühm on happeliste omaduste kandja see tähendab prootoni doonor (loovutab vesinikiooni). Füüsikalised omadused üsna kõrge keemistemperatuur (normaaltingimustel vedelad või tahked), lahustuvad hästi vees, kuid süsinikahela pikenedes, lahustuvus kiiresti väheneb. Madalamad karboksüülhapped on terava lõhnaga värvuseta vedelikud, mis segunevad veega igas vahekorras. Kõrgemad karboksüülhapped on tahked ja vees lahustumatud. Keemilised omadused - side hapniku- ja vesinikuaatomi vahel on nõrk. Seetõttu katkeb see side kergesti ja vesinikioonide eraldumisel põhjustavad karboksüülhapped lahuses happelisi omadusi. Sellest tulenevalt on karboksüülhapped alkoholidest ja fenoolidest tugevamad happed. 4
molekulvõre molekulid; molekulide toatemp vedel; vaheline H-side on lahustuvad; vesilahus tugevam kui teised võib juhtida elektrit molekulivahelised jõud iooniline ioonvõre Krist..... asuvad Kõrge temp; toatemp erimärgilised laetud tahke; lahustuvus ioonid, mida hoiab sõltub sulamistemp koos elektrostaatiline (madalam=parem) tõmbejõud Metalliline metallvõre Krist.... asuvad ioonid Head või aatomid; elektri/soojusjuhid; kristallvõret hoiavad peegeldavad valgust,
MOOL Osakeste arv Kasuta Mool Kasuta Mass, grammid N= n* NA n m = n*M NA = 6,02*1023 osakest/mol M Kasuta Kasuta Vm= 22,4 dm3/mol tihedust Gaasilise aine Tahke või vedela ruumala ( nt) aine ruumala, dm3 V = n* Vm V= m/ Osake on aatom, molekul,elektron, neutron, neutriino jne.. Lihtained, mille molekul koosneb alati kahest aatomist H2, O2, N2, F2, Cl2, ...
karbonüülrühma elektrofiilse tsentriga süsinikuga. Füüsikalised omadused: Karbonüülrühm on polaarne molekuliosa, kuid vesiniksidemeid ta praktiliselt ei moodusta. Seepärast on nii karbonüülühendi molekulide omavaheline vastastikmõju kui ka vastastikmõju veega nõrk. Enamik aldehüüde ja ketoone on kergesti lenduvad vedelikud. Madalamad esindajad lahustuvad vees väga hästi, kuid süsinikahela pikenedes lahustuvus väheneb kiiresti. Füsioloogiline toime: Aldehüüdid ja ketoonid on narkootilise toimega ja kahjustavad kesknärvisüsteemi. Limaskestale mõjuvad ärritavalt. Aldehüüdid on üldiselt ketoonidest mürgisemad. Sattunud nahale, tekitavad aldehüüdid põletikku, organismist eralduvad väga aeglaselt. Millisele meeleelundile mõjuvad sageli karbonüülühendid? Ninale. Tekib etanooli oksüdeerumisel? Etanaal.
FeO Raud(II)oksiid (keemiline valem FeO) on keemiline ühend, mille molekul koosneb ühest raua ja ühest hapniku aatomist. Omadused: Molekulivalem FeO Molaarmass 71,844 g / mol Välimus Mustad kristallid Tihedus 5,745 g / cm 3 Sulamispunkt 1377 ° C (2511 ° F; 1650 K)[ 1 ] Keemispunkt 3414 ° C (6177 ° F; 3687 K) Vees Mittelahustuv Lahustuvus lahustumatu leelise , alkohol lahustub happes Murdumisnäitaja (n D) 2.23 Keemilised ohud: Aine võib süttida kokkupuutel kuumutamisel üle 200°C õhuga. Aine oksüdeerub kergesti õhu toimel ja absorbeerib süsinikdioksiidi. Esinemine looduses: Raud (II) oksiidi moodustab umbes 9% Maa vahevööst. See võib olla elektri juht, mis võib selgitada...
teist võrdluses elektroodi, mille potentsiaal H+- ioonide kontsentratsioonist ei sõltu. Mõõtes nende kahe suuruste vahet leiame pH. 13. Mis on lahus? Millest see koosneb? Lahus on kahest või enamast komponendist koosnev homogeenne süsteem 14. Lahustumise põhireeglid. Lahustuvuse kuldreegel- sarnane lahustub sarnases; polaarne aine lahustub polaarses lahustis; mittepolaarne aine lahustub mittepolaarses lahustis. 15. Mis on lahustuvus? Mis on küllastuspunkt? Lahustuvus on aine võime moodustada teiste ainetega homogeenseid süsteeme- lahuseid. Küllastuspunkt- sellest alates rohkem ei saa lahustavat ainet lahusesse lahustada. 16. Mis on lahuste kontsentratsioon? Loetle erinevaid kontsentratsiooni väljendusviise? Lahuse kontsentratsioon- moolide arv kindlas ruumalas lahuses. Protsendiline sisaldus (C%), molaarsus- moolide arv ühe kg lahusti kohta; mooliprotsent; massikontsentratsioon; ppm/parts per million- miljonis massiosas lahuses 17
Omadus või tunnus Anorgaaniline ühend Orgaanilinine ühend sulamistemperatuur Üle 350o Alla 350o keemistemperatuur Üle 750o Alla 750o Keemiline side Iooniline side Kovalentne side Lahustuvus: Üldiselt Üldiselt a) Vees lahustuvad Ei lahustu b) Orgaanilistes ühendites Enamasti ei lahustu Enamasti lahustuvad (bensiin, alkohol) süttivus Ei sütti Süttivad Elektrijuhtivus Juhivad Ei juhi Anorgaaniliste ja orgaaniliste ainete võrdlus 2.) süsiniku aatomi ehitus ja valentsmudelid süsinik paineb 1. Perioodis ja 4A rühmas 6 p+= 6 anorgaanilistes ainetes on süsinik posiiivne, ...
Aerosool-süsteem mille tahke aine või vedelik on pihustatud gaasi;esimesel juhul on suitsu tüüp aerosool,teisel juhul udu tüüpi aerosool Emulgaator-aine,mis muudab emulsiooni püsivamaks Emulsioon-veselik,millesse on pihustatud selles lahustumatu vedeliku tilgad Hüdratatsioon-lahustunud aineosake ümbritsemine ja sidumine vee molekulidega Kolloidlahus-vedelik, milles pihustunud aine osakesed on suurusega 10:-7 Küllastumata lahus-lahus mille antud tingimustel võib veel ainet lahustuda Küllastunud lahus-lahus milles antud tingimustel enam ainet ei lahustu Lahus-lahustist ja lahustunud ainest koosnev ainete ühtlane kogum Lahusti-aine millesse lahustunud aine jaotub ühtlaselt Lahustumissoojus-aine lahustumisega kaasnev soojusefekt Lahustunud aine-lahuses esinev ning lahustisjaotunud aine Lahustuvus-aine suurim mass grammides mis lahustub antud tingimustel 100g lahustis Massiprotsent-lahustunud aine mass 100 massiosas lahuses Suspensioon-vedel...
Kordamisküsimused V Lahused 1. Mis on : · Lahus kahest või enamast ainest koosnev homogeenne süsteem. · Lahusti aine (tavaliselt vedelik), milles lahustunud aine on ühtlaselt jaotunud · Küllastumata lahus lahus, millesse lahustunud ainet mahub veel. · Küllastunud lahus antud tingimustes maksimaalse kontsentratsiooniga lahus, milles rohkem pole võimalik ainet lahustada. · Lahustuvus suspensioon · Emulsioon · Vaht · Aerosool · Elektrolüüt aine, mille lahus juhib elektrivoolu. Tema elektrijuhtivus põhineb vabade ioonide liikumisel. · Mitteelektrolüüt aine, mis ei juhi elektrit. · Elektrolüütiline dissotsatsioon · Hüdraatumine keemiline liitumisreaktsioon veega. · Dissotsatisoonimäär
VII A-rühma elemendid halogeenid Omadused F2 Cl2 Br2 I2 Elektrooniline F +9 2)7) +17 2)8)7) +35 2)8)18)7) +53 2)8)18)18)7) valem Oksüdatsiooniaste +7 ja -1 +7 ja -1 +7 ja -1 +7 ja -1 Füüsikalised 1.gaas 1. gaas 1.vedelik 1. tahke omadused 2.kollakas 2.kollakas 2.pruun 2.tume-mustjas 1.olek roheline gaas roheline 3. lahustub vees, 3.lahustub 2.värv ( kollakas) 3.lahustub vees saame broomivee piiritustes ( tahke 3.lahustuvus 3.lahustumisel aine ei lahustu reageerib veega. vees) 4. kuumutamis...
Score: 2/2 Küsimus 9 (2 points) Mis on ferriit (F) Student Response: Õppija Vastuse variandid vastus a. Süsiniku tardlahus rauas. b. Süsiniku tardlahus rauas c. Raua ja süsiniku keemiline ühend d. Raua ja süsiniku eutektoidne mehaaniline segu Score: 2/2 Küsimus 10 (2 points) Palju on Ferriidi süsiniku lahustuvus toatemperatuuril tasakaaluolekus(massiprotsentides)? Student Response: Õppija Vastuse variandid vastus a. 0.01% b. 0.02% c. 0.8% d. 6.67% Score: 2/2 Küsimus 11 (2 points)
Orgaanilise keemia praktikum Keemia instituut Töö pealkiri: Hantschi reaktsioon Teostaja:Marietta Lõo Kursus: Keemia III Töö algus Töö lõpp: Juhendaja: 27.11.2007 03.12.2007 Uno Mäeorg Kasutatud kirjandus: 1) Juhend,mis antud juhendaja poolt 2) Internet 3) ftp://ftp.ttkool.ut.ee/chem/balt/bko0506exp_eng.pdf 4)http://www.organic-chemistry.org/namedreactions/hantzsch-dihydropyridine- synthesis.shtm Meetodi olemus: 1,3-Dikarbonüülühendid koos aldehüüdidega ja ammoonumiga annavad 1,4.Dihüdropüridiini, mis on kirjeldatav Hantschi reaktsiooniga Kasutatavad nõud: 1) 50 ml ümarkolb 2) magnesegaja 3) magnetsegajapulk 4) jahuti 5) pasteuri pipett 6) 25 ümarkolb+ pulk sellele 7)Petri tass 8) silikageeli plaadid Kasutatavd ained: 1) ammooniumatsetaat-2 g kaaluti 2,2...
Komponentide kindla suhte korral moodustub vedelast lahusest mõlema komponendi üheaegse kristalliseerumise tõttu ühtlane peeneteraline struktuur eutektikum. Tahked lahused on sulamid, mille puhul ühe komponendi aatomid paiknevad teise komponendi kristallvõres, moodustades faasi. Asendustüüpi tahketes lahustes on osa põhimetaali aatomeid asendunud teise komponendi aatomitega. Kui aatomite mõõtmete erinevus kuni 8 %, esineb piiramatu (täielik) lahustuvus ; 8-15 % tekivad piiratud lahustuvusega tahked ained ja üle 15% metallid enamasti asendustüüpi tahkeid lahusteid ei moodusta. Sisestustüüpi tahketes lahustes paiknevad lahustuva komponendi aatomid põhimetalli aatomite vahel. Piiratud lahustuvus väheneb temperaturi langedes. Harva on metaalisulameis ka vakantstüüpi tahkeid lahuseid, mille kristallvõresse jääb vabu sõlmi. Sellised lahused moodustuvad vaid keemiliste ühendite alusel.
Alkoholid Alkoholid · Alkoholideks R-OH nimetatakse ühendeid, milles hüdroksüülrühm on seotud esimeses valentsolekus oleva süsinikuaatomiga. Füüsikalised omadused · Kuna hüdroksüülrühma vesinikul on positiivne osalaeng, võib ta hästi osaleda vesiniksideme moodustumisel. Alkoholid võivad moodustada vesiniksidemeid omavahel ja ka vee molekulidega. · Sellest ongi tingitud alkoholide hüdrofiilsus ning hea lahustuvus vees. Füüsikalised omadused · Alkoholide lahustuvus vees sõltub süsinikahela pikkusest lühikese süsinikahelaga alkoholid lahustuvad vees väga hästi, pikema ahelaga halvasti. · Alkoholid on narkootilise toimega ja mürgised. Füüsikalised omadused · Metanool ja kõrgemad alkoholid (alates C6) tekitavad nägemisorganite pöördumatuid kahjustusi. C2 C4 (eriti hargnemata ahela puhul) on vähem mürgised st. nende surmav kogus võib
orienteeruvad seal nii, et polaarne (hüdrofiilne) ots on pööratud polaarse keskkonna (vee) poole. Sel teel võivad pindaktiivsed ained mustusosakesi pinnalt lahti kangutada. Detergente jagatakse anioon ja katioonaktiivseteks ning mitteioonaktiivseteks detergentideks. Kuna pindaktiivsus ja adsorptsioonivõime kasvavad süsivesinikahela pikenedes, on mõjusamad sellised pindaktiivsed ained, mille molekulis on 1218 C aatomit. Edasisel süsinikahela pikenemisel lahustuvus väheneb. Mitmete ainete, näiteks karboksüülhapete, amiinide, alkoholide puhul piirab pindaktiivsuse mõjule pääsemist aine vähene lahustuvus vees. Üks vanemaid ja tuntuimad detergente on seep. Kuid seebil, kui pesemisvahendil on ka mõningaid puudusi. Karedas vees moodustuvad rasvhapete kaltsiumi ja magneesiumisoolad: 2RCOONa + Ca(HCO3)2 (RCOO)2Ca + 2NaHCO3
rohkem kui nelja aromaatset tsüklit sisaldavaid PAH-e “rasketeks” (näiteks benso(a)püreen). “Rasked” PAH-id on enamasti stabiilsemad kui “kerged” PAH-id. PAH-id erinevad füüsikalis-keemiliste omaduste poolest ja mõjuvad elusorganismidele mitut moodi. Reeglina PAH-ide keemilised ja füüsikalised omadused sõltuvad tugevasti molekulmassist: molekulmassi suurenedes vähenevad PAH-ide vees lahustuvus, aururõhk ning PAH-ide vastupanuvõime redutseerumise ja oksüdeerumise suhtes, kuid suurenevad sulamistemperatuur, keemistemperatuur ning suureneb PAH-i lahustuvus rasvades. Elusorganismidele mürgiseks loetakse PAH-e, mille molekulmass jääb vahemikku 128,16–300,36 g/mol, sest tänu oma madalale molekulmassile on nad keskkonnas liikuvamad kui suurema molekulmassiga PAH-id. Suurema molekulmassiga PAH-id (molekulmass suurem kui 300,36 g/mol) on vähem liikuvad
2. Anioon Negatiivse laenguga ioon 3.Hape Aine mis annab lahusesse vesinikioone 4.Sool Kristalne aine, mis koosneb (aluse) katioonidest ja (happe) anioonidest 5.Redutseerimine Elektronide liitmine. 6.Oksüdeerimine elektronide loovutamine, sellele vastab elemendi oksüdatsiooni astme suurenemine 7. Leelis Vees lahustuv tugev alus (hüdroksiid) Soolade Füüsikalised Omadused : 1) Tahked 2) Erinev värvus (põhiliselt valge) 3) Vees lahustuv on ka erinev ( vaata lahustuvus tabelist) Soolade Keemilised Omadused : 1. Sool + Alus (mõlemad peavad olema lahustuvad) ja üks saadustest peab olema sade 2. Soolad reageerivad tugevamate hapetega 3. SOOL + HAPE = UUS SOOL + UUS HAPE vana hape on tugevam ja uus nõrgem ;) TUGEVAD HAPPED ON : H2SO4 kõige tugevam HCL HNO3
Alkohol Ained, mille molekulis tetraeedrilise süsiniku aatomi juures asuv vesinik on asendatud hüdroksüülrühmaga OH. Eeter Orgaaniline ühend üldvalemiga R-O-R. Amiin Ammoniaagi derivaat, kus vesiniku aatomi(te) asemel on orgaaniline rühm või rühmad. Hüdrofiilsus Veelembus, ühendi võime vastastikmõjuks veega. Alkoholide füüsikalised omadused: Füüsikalised omadused on määratud vesiniksidemete moodustamise võimalustest ja süsivesiniku ahelast. Alkoholidel on hea lahustuvus vees ehk hüdrofiilsus ning madal keemistemperatuur. Alkoholide keemilised omadused: Oksüdeerumine Alkoholide oksüdeerumisel saadakse: a) aldehüüde b) ketoone c) karboksüülhappeid Alkoholide kiirel oksüdeerumisel ehk põlemisel tekivad CO2 ja H2O. Alkoholide füsioloogilised omadused: narkootiline toime, alkoholide põlemise vaheühendid võivad olla väga mürgised (kesknärvisüsteemi kahjustused), pikema ahelaga alkoholid tekitavad pöördumatuid nägemisorganite kahjustusi
Milline võib olla süsinikahela kuju molekulis? Süsinikahel võib olla hargnemata, hargnev või tsükliline. Milline on süsivesinike lahustuvus vees? Süsivesinikud ei lahustu vees. Milline on süsivesinike agregaatolek toatemperatuuril? Viis naftasaadust: bensiin, diislikütus, määrdeõlid, masuut, bituumen. Mitu sidet on tavaliselt süsiniku, hapniku, lämmastiku ja vesiniku aatomil? Süsinik: 4 sidet (4 üksiksidet, 1 kaksiksideme ja 2 üksiksidet, 2 kaksiksidet, 1 üksik- ja 1 kolmiksideme. Hapnik: 2 sidet ( 2 üksiksidet, 1 kaksikside). Lämmastik: 3 sidet (3 üksiksidet, 1 kaksik- ja 1 üksikside, 1 kolmikside). Vesinik: 1 side
ALKOHOLID JA EETRID MÕISTED: Mitmehüdroksüülne alkohol alkohol, mille molekulis on mitu hüdroksüülrühma. Funktsionaalne rühm kõige kergemini muunduv osa alkoholi molekulis. Alkoksiidioon alkoholi kui happe anioon. Alkoholaat alkoholi sool. Eeter orgaaniline ühend üldvalemiga R-O-R (R-süsinikahel). Alkoholides esinevad vesiniksidemed. Vesiniksidemed esinevad ainetes, kus on N- H või O-H rühmad. Vesinikside on molekulidevaheline side. Vesinikside põhjustab: a) suuremat keemistemperatuuri b) head lahustuvust vees Alkoholide füüsikalised omadused · hüdrofiilsed a) C 1, 2, 3 lahustuvad vees piiramatult (mida väiksem ahel seda paremini lahustub) b) C 4 ~10ml /100ml vees c) dioolid ja trioolid lahustuvad kõik väga hästi (saavad moodustada rohkem vesiniksidemeid. · Vesiniksideme tõttu kõrgem keemistemperatuur. Mida pikem on ahel seda kõ...
(mürgine, terava lõhna ja toimega ) ( Kasutatakse keemiatööstustes ja ka sipelgate kahjuritõrveks) Etaanhape ehk äädikhape (pole mürgine, külmub 16C kraadi juures) (Kasutatakse tööstustes lahustina ja paljudes keemiatööstustes saaduste valmistamiseks.) Karboksüülhapped: on aine, mis sisaldavad hüdroksüülrühma, karboksüülrühma ja karbonüülrühma. (Füüsikalised omadused: kõrged keemistemperatuurid, vedekas, tahkes olekus, süsinikuahela pikenedes väheneb vees lahustuvus ja kahaneb ka tihedus, happemolekulid moodustavad tugevaid vesiniksidemeid) (keemilised omadused: reageerimine: metallidega, aluseltiste oksiitidega, leelistega, nõrkade hapete sooladega) Aminohapped: on karboksüülhapped, mille alküülrühmas on üks või mitu vesiniku asendatud aminorühmaga. (Füüsikaalised omadused: tahked kristallsed ained, lahustuvad hästi vees, kõrge sulamistemperatuur) (eluks vajalikke aminohappeid on 20 ja millest ehitatakse üles valgud)
põletushaavu. Värvuseta või pruun vedelik. Laialt levinud hapetest üks tugevamaid happeid. Iseloomulik terav lämmatav lõhn, mis pisut meenutab kloori lõhna. Kuulub mineraalhapete ja üheprootoniliste hapete hulka. Lämmastikhapet sisaldub ka happevihmades. Kolmemõõtmeline mudel Füüsikalised omadused Molekuli mass: 63,0 amü Sulamistemperatuur: 231,15 K (-42 °C) Keemistemperatuur: 356,15 K (83 °C) Tihedus: 1,522×10³ kg/m³ Lahustuvus: Segunev Ohutus Suu kaudu manustamine - Võib vigastada seedeelundeid. Nahk - Võib põhjustada tõsiseid põletushaavu, arme, plekke jms. Silmad - Väga ohtlik Keemilised omadused Ühendis maksimaalne oksüdatsiooniaste (+5). samaaegselt nii tugev hape kui ka tugev oksüdeerija. Ei ole keemiliselt eriti stabiilne ja laguneb ka valguse toimel pikkamööda lämmastikdioksiidiks, hapnikuks ja veeks.
Üks tuntumatest alustest Naatriumhüdroksiid (varem ka kaustiline sooda, sööbenaatrium) on keemiline ühend valemiga NaOH. Ta on valge tahke lõhnatu aine, mis lahustub hästi vees eraldades sealjuures palju soojust. Õhu käes seistes seob tugevasti õhuniiskust ning seetõttu tuleb säilitada teda õhukindlalt suletud anumas. Rahvapäraselt on naatriumhüdroksiidi nimetatud seebikiviks. Keemilised omadused: pH: leeliseline , keemispunkt : 1378 oC , suhteline tihedus : 2,13 g/cm3, lahustuvus vees: 107 g / 100g vees 20oC juures, sulamispunkt: 323 oC, molekulmass on 40,0, ei põle, vees täielikult lahustuv, anorgaaniline. Naatriumhüdroksiidi saadakse naatriumkloriidi vesilahust elektrolüüsides (katoodil eraldib vesinik, anoodil kloor, katoodiruumis tekib naatriumhüdroksiid). Keedusoolast seebikivi tootmisel on kõrvalproduktiks kloor. Naatriumhüdroksiid on keemiatööstuse põhitooteid. Teda kasutatakse nafta- (nafta
Klenbuterool Keemiline nimi: klenbuterool vesinikkloriid Keemiline valem: C 12 H18 Cl 2 N2 O Molekulmass: 277,19 Struktuur valem: Välimus: värvitu mikrokristallne pulber (Merck Index) Valge pisut kollakas aine (sponsor) Sulamistemperatuur: 174-175,5 ° C (Merck Index) 170-176°C (sponsor) Lahustuvus: Väga hästi lahustuv vees, metanoolis ja etanoolis, kergesti lahustub kloroformis, lahustumatu benseenis. Kasutamine: Klenbuterooli kasutatakse loomadel näiteks hingamiselundite haiguste ja sünnituskomplikatsioonide puhul. Soovitav ravi kogus on 0,8 mg/kg kohta kaks korda päevas. Maksimaalne ravi kestvus on 10 päeva. Manustada võib suukaudu või süstimise teel. Klenbuterool satub toitu siis, kui loomadel antakse klenbuterooli, mille tagajärel toimub toidu saastumine. Näiteks 2006 aasta septembris sai üle 330 inimese Hiinas mürgistuse süües sealiha...
*Ained peavad omavahel kokku puutuma. Lisatingimused: Süütamine, Kuumutamine, Elektri läbijuhtimine, Valgustamine. Keemilise reaktsiooni tunnused: Värvuse muutus, Lõhna muutus, Gaasi eraldumine, Sademete teke või lahustumine, Soojuse eraldumine, Valguse eraldumine. Lahus: Lahus koosneb lahustist ja lahustunud ainest. Lahustumise kiirus sõltub: 1) Segamisest, 2) Lahustatava tahke aine peenestamisest, 3) Temperatuurist. Aine lahustuvus väljendab aine sisaldust küllastunud lahuses. Lahus on lahusti ja lahustunud aine ühtlane segu. Elektronkate: Elektronid: üliväikesed negatiivse laenguga osakesed, mis moodustavad aatomis tuuma ümbritseva elektronkatte. Elektronkate: Aatomituuma ümber tiirlevate elektronide kogum, koosneb elektronkihtidest. Elektronkiht: elektronkatte osa, koosneb tuumast teatud kaugusel tiirlevatest elektronidest.
Sissejuhatus: Pb2+ -, Ag+ - ja Hg22+ - ioonide eraldamine teiste rühmade katioonidest põhineb nende katioonide kloriidide väga vähesel lahustumisel vees. Seetõttu on I rühma katioonide rühmareaktiiviks lahjendatud HCl lahus, mille toimel need katioonid sadestuvad rasklahustuvate kloriididena - PbCl 2, AgCl ja Hg2Cl2. Kõige suurema lahustuvusega on PbCl2, mille lahustuvus suureneb soojendamisel tunduvalt. Seda omadust kasutatakse Pb2+ - ioonide eraldamiseks teistest I rühma katioonidest. Sadestamisel tuleb vältida Cl - ioonide suurt liiga, sest PbCl2 ja AgCl moodustavad kloriidioonide liiaga lahustuvaid kompleksühendeid [PbCl4]2 ja [AgCl2]. Esimese rühma katioonide eraldamise ja tõestamise skeem: Tõestusreaktsioonid: Pb2+ - ioonide tõestusreaktsioonid a) Cl- - ioonidega
mittevalguline aine, mis äärmiselt tugevatoimelise (umbes 10 000 korda tugevam toksiin kui kaaliumtsüaniid) närvimürgina täidab kaitsefunktsiooni mitmete mereasukate (sealhulgas fugu ehk jaapani kerakala jt) elus. [2, 3] 1.2 Ülevaatlik informatsioon tetrodotoksiinist Molekulvalem: C11H17N3O8 Molaarmass: 319.2706 g/mol Molaarruumala: 114.661 cm3 Lahustuvus vees: Lahustub lahjendatud äädikhappes või väävelhappes, piiratud lahustuvus etanoolis ja eetris, ei lahustu orgaanilistes lahustes. Tabel . Kokkuvõte nimetustest Süstemaatilised nimetused - (4R,4aR,5R,6S,7S,9S,10S,10aR,11S)-2- amino-6-(hüdroksümetüül)-1,4,4a,5,6,7- heksahüdro-5,9-epoksü-7,10a- metanooksotsiino[4,5-d]pürimidiin-
Süsivesikud Süsivesikud · Looduses enamlevinud orgaanilised ühendid · Meie toitumisahelas esimeseks lüliks · Kuuluvad rakkude ja kudede koostisesse · Hästi kättesaadavad, kõrge energeetilise väärtusega · Organismis kerge säilitada Enamlevinud orgaanilised ühendid looduses · Taimedes 75-90% · Loomades 2% · Seentes 3% · Mikroorganismides 12% Toiteväärtus · Süsivesikute arvele langeb meie elutegevuseks vaja minevatest kaloritest 60% · 1g süsivesikute lõhestumisel vabaneb 17kJ energiat · Süsivesikud annavad 50% päevas minevast energiast Jaotus · Jagunevad kolme põhirühma 1) Monoosid 2)Oligosahhariidid 3)Polüsahhariidid Monoosid · Kahte või enamat hüdroksüülrühma aldehüüdid või ketoonid · Liigendatakse funktsionaalse rühma järgi -Aldoosil on aldehüüdrühm -Ketoosil on ketoonrühm Oligosahhariidid · Madalamolekulaarsed orga...
Tunnus Anorgaaniline ühend Orgaaniline ühend 1. keemiline side Iooniline side Kovalentne side 2. Sulamistemp. Üle 350 kraadi alla 350 kraadi 3. Keemistemp. Üle 750 kraadi alla 750 kraadi 4. Lahustuvus a)vees hästi halvasti b)orgaanilistes ainetes halvasti hästi 5. Süttivus halvasti süttivad 6. Elektrijuhtivus enamasti juhivad enamasti ei juhi Süsiniku aatomi ehitus: Asub II perioodis. IV A rühmas. Prootonite arv 6. Neutronite arv 6. Elektronide arv 6. Elektronskeem: C:+6 l 2)4)
2. Alkaanid on süsivesinikud, milles süsinikuaatomite vahel on vaid üksiksidemed. 3. Alkaanide üldvalem on CnH2n+2 n> või = 1. 4. Alkaanide homoloogiline vahe on kahe kõrvuti oleva süsivesiniku rühma -CH2- arv. 5. Alkaanide füüsikalised omadused muutuvad homoloogilises reas seaduspäraselt: Süsiniku aatomite arvu kasvades kasvavad homoloogilistes ridades molekulmass, tihedus, sulamis- ja keemistemperatuur, väheneb aga ainete lahustuvus vees. 6. Tahkeid alkaane kutsutakse parafiinideks. 7. Alkaanid on veest kergemad. 8. Alkaanid ei märgu ega lahustu vees, seega nad on hüdrofoobsed ained. 9. Alkaanid on keemiliselt kõige passiivsemad orgaanilised ained. 10. Alkaanidel esineb 3 liiki keemilisi reaktsioone: põlemine, pürolüüs ja asendusreaktsioonid halogeenidega (halogeenimine). 11. Metaan on loodusliku gaasi ehk maagaasi peamine koostisosa. Teda leidub maagaasis 70 kuni 90%
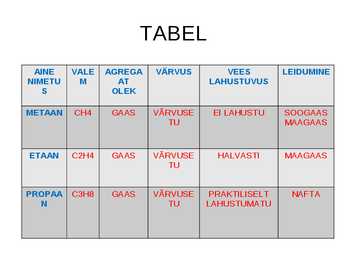
TABEL AINE VALE AGREGA VÄRVUS VEES LEIDUMINE NIMETU M AT LAHUSTUVUS S OLEK METAAN CH4 GAAS VÄRVUSE EI LAHUSTU SOOGAAS TU MAAGAAS ETAAN C2H4 GAAS VÄRVUSE HALVASTI MAAGAAS TU PROPAA C3H8 GAAS VÄRVUSE PRAKTILISELT NAFTA N TU LAHUSTUMATU ALKAANIDE ÜLDVALEM CnH2n+2 C-aatomite arv Nimetus Valem Olek 1 METAAN CH4 G
1.Sahhariidid on keemilised ained, mille molekulid on biomolekulid, mis koosnevad süsiniku, vesiniku ja hapniku aatomitest. Lihtsuhkrud: glükoos, fruktoos. Liitsuhkrud: tärklis. Kiudained: pähklid. 2. Glükoos C6H12O6, fruktoos C6H12O6 ja galaktoos C6H12O6. 3. maltoos C12H22O11. , laktoos C12H22O11 ja sahharoos C12H22O11. 4. Ksantaankumm. 6. α-ja β-glükoosi sruktuurivalemid erinevad üksteisest. α-glükoosil on 1.ja 2. süsiniku aatomi juures asuvad ühel pool molekuli tasapinda. β-glükoosil on aga tasapinna erinevatel pooltel. 7. Disahhariidid moodustuvad monosahhariidide tsükliliste vormide omavahelisel reageerimisel sarnaselt atsetaali moodustumisele karbonüül ühendite korral. 8. Fruktoos on kõige magusam. Kõige eneriarikkam on monosahhariid. 9. Piimhappebakterid oksüdeerivad laktoosi piimhappeks ja tekkiv hapupiim enam laktoosi ei sisalda. Seetõttu talutakse hapendatud piimatooteid, näiteks keefiri. 11. On moodustunud glükoosist. Üks on ...