Küsimused õpingukorralduse I loengu kohta 1. Mis organ on TTÜ nõukogu? 2. Millega tegeleb dekaan? 3. Kes nõustavad üliõpilast? 4. Mis on tüüpõpingukava? 5. Millistest õppetöö vormidest osavõtt on kohustuslik? 6. Mis on vabaaine? 7. Mis on vabaõppe moodul? 8. Mis on eeldusaine? 9. Milliseid vabaaineid saab õppida tasuta? 10. Millal ja mis põhjustel võib õppejõud üliõpilase kuulajaskonnast välja arvata? 1. TTÜ nõukogu on ülikooli kõrgeim otsustusorgan, mis koosneb 41-liikmest ja otsustab olulisemaid TTÜ arengu ja tegevusega seotud küsimusi.
USU- IGUS- ARSTI- FILOSOOFIA- HARIDUS- KEHA- LOODUS- JA MAJANDUS- MATEMAATI- SOTSIAAL- TEADUS- TEADUS- TEADUS- TEADUS- TEADUSKOND KULTUURI- TEHNO- TEADUSKOND KA- TEADUS- KOND KOND KOND KOND Dekaani kt dots TEADUSKOND LOOGIA- Dekaan prof INFORMAA- KOND Dekaan prof Dekaan prof Dekaan prof Dekaan prof Hasso Kukemelk Dekaan prof TEADUSKOND Toomas Haldma TIKATEADUS- Dekaan prof Riho Jaan Ginter Joel Starkopf Valter Lang Mati Psuke Dekaan prof KOND Jaanus Harro
Keemia kontrolltöö 4 )ALKAANID: 1)Aatomite olek molekulis(lk 25, E ): 1) metaan- CH4 C(süsinik)- neli sidet 2) etaan- C2H6 N(lämmastik)-kolm sidet 3) propaan- C3H8 O(hapnik)- kaks sidet 4) butaan- C4H10 H(vesinik)-üks side 5) pentaan- C5H12 6) heksaan- C6 H14 7) heptaan- C7 H16 8) oktaan- C8 H18 9) nonaan- C9 H20 10) dekaan- C10H22 2)Teooria( õp lk 96-111): Alkoholid( üldvalemiga ROH ) Alkoholid-alkaanidest tuletatud ühendid · molekulis üks või enam vesinikuaatomit on asendatud hüdroksüülrühmaga (- OH-rühmaga) · veesõbralikud, lahustuvad vees paremini kui alkaanid · ei muuda vesilahuse keskkonda · mõned alkoholid on mürgised · alkoholid ei ole alused Metanool (CH3OH) e. puupiiritus · saadakse:metaani oksüdeerumisel või CO redutseerumisel
SÜSIVESINIKUD On orgaanilisedühendid mis koosnevad süsinikust ja vesinikust Alkaanides on 1-4 liiget gaasid ja alates 5. on vedelikud. ALKAANID 1) Metaan CH4 2) Etaan C2H6 3) Propaan C3H8 4) Butaan C4H10 5) Pentaan C5H12 6) Heksaan C6H14 7) Heptaan C7H16 8) Oktaan C8H18 9) Nonaan - C9H20 10) Dekaan C10H2 ALKOHOOLID Alkohoolide nimetus on tuletatud süsivesinikest, millest üks või mitu on hüdroksiid. Alkohoolide nimed pannakse lähtudes alkaanide reast C-de(süsinike) arvu järgi. CnH2 + 2 = AAN lõpuga 1) CH4 metaan ---- CH3OH = metanool ehk puupiiritus 2) C2H6 etaan ---- C2H5OH = etanool ehk viin (vodka) ÜLDVALEM: R OH
(ALKAANID) (ASENDUSRÜHM) CH4 Metaan CH3-metüül C2H6 Etaan C2H5- etüül C3H6 Propaan C3H7 -Propüül C4H10 Butaan C4H9 -butüül C5H12- Pentaan JNE.... C6H14- Heksaan C7H16- heptaan C8H18 -oktaan C9H20 - nonaan C10H22- dekaan Valents- näitab mitut kovalantet sidet võib antud aatom moodustada. Orgaanilises ühendites on süsiniku valem alati 4 ORAAGILISED ÜHENDID- a)atsüklilised b) tsüklilised Isomeeria on nähtus, kus ainetel on ühesugune element koostis ja molekulmass aga erinev struktuur ja omadused Molekulvalem- summaarvalem nõitab aine koostist, kui palju ja milliste elementide aatomid on molekulis. Klassikaline e. Tasapinnaline struktuur valem näitab millised aatomid ja milliste sidemetega
5 Penta C5H12 pentaan C5H11- pentüül- C5H10 tsüklopentaan 6 Heksa C6H14 heksaan C6H13- heksüül- C6H12 tsükloheksaan 7 Hepta C7H16 heptaan C7H15- heptüül- C7H14 tsükloheptaan 8 Okta C8H18 oktaan C8H17- oktüül- C8H16 tsüklooktaan 9 Nona C9H20 nonaan C9H19- nonüül- C9H18 tsüklononaan 10 Deka C10H22 dekaan C10H21- detsüül- C10H20 tsüklodekaan CH3 isopropüül- CH3 CH- CH3 isobutüül- CH3 CH- CH2- CH3 CH3 C- tertbutüül- CH3
üksik side alkaan Homoloogiline rida: 1. metaan CH4 2. etaan C2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptaan C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22 kaksikside alkeen 12. eteen C2H4 13. propeen C3H6 14. buteen C4H8 15. penteen C5H10 16. hekseen C6H12 17. hepteen C7H14 18. okteen C8H16 19. noneen C9H18 20. dekeen C10H20 kolmikside alküün 32. etüün C2H2 33. propüün C3H4 34. butüün C4H6 35. pentüün C5H8 36. heksüün C6H10 37. heptüün C7H12 38. oktüün C8H14 39
aatomite vahel on üksikside ehk sigmaside. Üldvalem CnH2n+2 (n on jrk nr) Orgaanilistele ainetele pannakse nimed alkaanide homoloogilise rea alusel. 1. metaan CH4 2. etaan C2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptann C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22 Radikaalid on molekulid või aatomid, mille elektronkihis asub paardumata elektron. 2-metüül propaan Alkaanide keemilised omadused: 1) Põlemine CH4 + 2O2 -> CO2 + 2H2O 2) Asendus reaktsioon hallogeenidega (radikaaliline asendusreaktsioon) CH4 + Cl2 -> CH3Cl +
Halogeeniühendid Halogeeniühendies on süsiniku aatomid seotud halogeeni aatomitega. CH4 = CH3Cl Füüsikalised omadused *Peamiselt vedelikud või tahked ained *Madalamad halogeeniühendid aurustuvad kiiresti Asendusnomenklatuur- asendusrühmad + tüviühend *floro-, kloro-, bromo-,jodo CH3-CH2-CH2-CH2-Cl 1-klorobutaan Ahelisomeeria- süsinikahela kuju on erinev Asendusisomeeria- funktsionaalrühmad paiknevad ühesuguse süsinik arvu ja paigutused süsinikahela korral erinevalt Kõik halogeenid on C-st elektronnegatiivsemad C ja Hal vahel on polaarne kovalentne side C on positiivne osalaeng, sest tema aatom on elektronpilve poolest mõnevõrra vaesem Hal on negatiivne osalaeng, sest elektronpilv on suurem Elektrofiil- tühja orbitaaliga osake Elektrofiilsustsenter- elektrofiili koostisesse kuuluv tühja või osaliselt tühja orbitaalida aatom Nukleofiil- vaba elektronpaariga osake Nukleofiilide suhteline tugevus Nõrgad nukleofiilid *Happeanionid ROOO *Halo...
Nimetus Valem Metaan CH4 Etaan C2H6 Propaan C3H8 Butaan C4H10 Pentaan C5H12 Heksaan C6H14 Heptaan C7H16 Oktaan C8H18 Nonaan C9H20 Dekaan C10H22 Undekaan C11H24 Dodekaan C12 H26 Tridekaan C13H28 Tetradekaan C14H30 Pentadekaan C15H32 Reaktsioonivõrrandis Mittemetallioksiidid + Vesi = Hape Sool + Hape = Uus hapse + Uus sool SiO2 (liiv) veega ei reageeri Tekkiv hape peab olema algsest nõrgem Metallioksiidid + Vesi = Alus Sool + Sool = Sool + Sool Ainult IA/IIA metallid Lähteained peavad vees lahustuma. Üks tekkivatest
Pentaan Hepteen Heptüün Pentanool Pentaanhape Heptaan Septeen Septüün Heptanool Heptaanhape Septaan Okteen Oktüün Septanool Septaanhape Oktaan Noneen Nonüün Oktanool Oktaanhape Nonaan Dekeen Deküün Nonanool Nonaanhape Dekaan Dekanool Dekaanhape Etenool Eteenhape Propenool Propeenhape Butenool Buteenhape Pentenool Penteenhape
ALKOHOLID Alkohol Ained, mille molekulis tetraeedrilise süsiniku aatomi juures asuv vesinik on asendatud hüdroksüülrühmaga OH. Eeter Orgaaniline ühend üldvalemiga R-O-R. Amiin Ammoniaagi derivaat, kus vesiniku aatomi(te) asemel on orgaaniline rühm või rühmad. Hüdrofiilsus Veelembus, ühendi võime vastastikmõjuks veega. Alkoholide füüsikalised omadused: Füüsikalised omadused on määratud vesiniksidemete moodustamise võimalustest ja süsivesiniku ahelast. Alkoholidel on hea lahustuvus vees ehk hüdrofiilsus ning madal keemistemperatuur. Alkoholide keemilised omadused: Oksüdeerumine Alkoholide oksüdeerumisel saadakse: a) aldehüüde b) ketoone c) karboksüülhappeid Alkoholide kiirel oksüdeerumisel ehk põlemisel tekivad CO2 ja H2O. Alkoholide füsioloogilised omadused: narkootiline toime, alkoholide põlemise vaheühendid võivad olla väga mürgised (kesknärvisüsteemi kahjustused), pikema ahelaga alkoh...
5 C5H12 pentaan ... ... 6 C6H14 heksaan ... ... 7 C7H16 heptaan ... ... 8 C8H18 oktaan ... ... 9 C9H20 nonaan ... ... 10 C10H22 dekaan ... ... STRUKTUURIVALEMID Tasapinnaline ehk klassikaline struktuurivalem näitab välja kõik sidemed aatomite vahel. H H H C H H HH C H H H C C C C C H H O H H H C H H H H C C H H O H ;
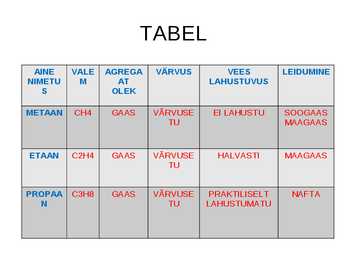
CnH2n+2 C-aatomite arv Nimetus Valem Olek 1 METAAN CH4 G 2 ETAAN C2H6 A 3 PROPAAN C3H8 A 4 BUTAAN C4H10 S 5 PENTAAN C5H12 6 HEKSAAN C6H14 7 HEPTAAN C7H16 VEDELIK 8 OKTAAN C8H18 9 NONAAN C9H20 10 DEKAAN C10H22 · Alkaanid-lõppsilp-aan Alkeenid-lõpp-een · Keemiliselt on aktiivsemad alkeenid · Metaani esineb:maa,-soo,-kaevandusgaasis · Metaan on kasvuhoooneefekti tekitav gaas · Biogaas-orgaaniliste jäätmete kääritamisel hermeetiliselt saadakse biogaas · Parafiinid-sisaldavad tahkeid alkaane · Parafiin-kasutatakse määrdeainete ja õlide ning küünakde välmistamisel · Eteen-saadakse nafta krakkimisel või põlevkivi utmisel ETEEN
ja multimeediakunstnik. Ta alustas aktiivsemat tegutsemist 1990ndate aastate algul, olles siinse neopopi laine juhtautoreid. Ta õppis EKAs graafika erialal ning trükitehnoloogiaid Swedish Royal Art High Schoolis. Mäetamm on teinud isikunäitusi, osalenud grupinäitustel mitmel pool maailmas. Välja andnud 2 raamatut, üks pseüdonüümi all (mida nad Kaido Olega jagavad) ,,John Smith". Marko Mäetamm on täiskohaga EKA vabade kunstide teaduskonna dekaan. Kaido ole viljeleb kaasaegset maalikunsti ja installatsiooni. Tema teosed on nt. ,,Lennukid ja lilled", ,,Fenomen", ,,Worrying view. A floor" ja ,,Liivakast". Minu lemmik maal on ,,Nuttev ingel", sest see on huvitav ja samas ka ilus. On teada, et eelkõige joonistusõppejõud olid Mäetammest vaimustuses, soovitades tal kool nelja aasta asemel kolmega lõpetada. Vive Tolli, üks õppejõududest, meenutab teda siiani kui üle kooli joonistajat.
*etaandiool- jahutusvedelikes *glütserool- kosmeetikas 3) Too kaks näidet igapäevaelust leiduvatest karboksüülhapetest *sidrunhape (sidrunites) *oblikhape (rabarberis) 4) Alkaanid *metaan- CH4 *etaan- C2H6 *propaan- C3H8 *butaan- C4H10 Juergen Guido *pentaan- C5H12 *heksaan- C6H14 *heptaan- C7H16 *oktaan- C8H18 *nonaan- C9H20 *dekaan- C10H22 5) Süsiniku oksüdatsiooniastme arvutamine ühendis *C-H =-1 *C-C =0 *C-O =+1 *C=O =+2 6) Alkoholide ja karboksüülhapete valemite äratundmine CH3OH- metanool C2H5OH- etanool C3H7OH- propanool C4H9OH- butanool C5H11OH- pentanool C6H13OH- heksanool C7H15OH- heptanool C8H17OH- oktanool C9H19OH- nonanool C10H21OH- dekanool C3H5OH- propaan-1,2,3-triool (glütserool) C2H4OH- etaan-1,2-diool (etüleenglükool)
Alkaanid Nimetused tulevad süsiniku aatomite arvu järgi: 1C metaan ; 2C etaan ; 3C propaan ; 4C butaan ; 5C pentaan ; 6C heksaan ; 7C heptaan ; 8C oktaan ; 9C nonaan ; 10C dekaan . Isomeeria CH3CH2CH2CH3 CH3CHCH3 C4H10 - butaan | CH 3 C4H10 - 2metüülpropaan Isoeeridel on ühesugune molekulvalem, aga erinev struktuur. Isomeeridel pole ühesugused omadused. Omadused sõltuvad struktuurist. Lineaarse ahela korral on suurem tihedus, kõrgem sulamis- ja keemistemperatuur. Füüsikaliste omaduste hulka kuuluvad lahustuvus, tihedus, sulamis-, keemistemperatuur. *Hüdrofiilne lahustub vees
· Ühendi omadused sõltuvad molekuli koostisest ja aatomite paigutusest e. Ehitusest · Aatomite paigutuse muutmine muudab järslult ainete omadusi Süsivesinikud C x+ Hy Alkaanid Alkeenid Alküünid Alkaanid 1) Metaan CH4 2) Etaan C2H6 3) Propaan C3H8 4) Butaan C4H10 5) Pentaan C5H12 6) Heksaan C6H14 7) Heptaan C7H16 8) Aktaan C8H18 9) Nonaan C9H20 10) Dekaan C10H22 Alkeenid Cn+H2n ; -een 2) Eteen C2H4 3) Propeen C3H6 CH2=CH-CH3 4) Buteen C4H8 CH3-CH=CH-CH3 5) Penteen C5H10 CH3-CH=CH-CH2-CH3 6) Hekseen C6H12 CH3-CH=CH-CH2-CH3 7) Hepteen C7H14 CH3-CH2-CH2-CH=CH-CH2-CH3 8) Okteen C8H16 CH3-CH2-CH2-CH=CH-CH2-CH2-CH3 9)Noneen C9H18 CH3-CH2-CH2-CH=CH-CH2-CH2-CH2-CH3 10) Dekeen C10H20 CH3-CH2-CH2-CH2-CH2-CH=CH-CH2-CH2-CH3 Alküün CnH2n-2 ; -üül ; 1 kolmikside. 2) Etüün C2H2 H-C(kolmikside)C-H
C4H10 Butaan C4H9 Butüül- C5H12 Pentaan C5H11 Pentüül- C6H14 Heksaan C6H13 Heksüül- C7H16 Heptaan C7H15 Heptüül- C8H18 Oktaan C8H17 Oktüül- C9H20 Nonaan C9H19 Nonüül- C10H22 dekaan C10H21 Deküül- 1
Süsivesinikud on liitained, mille molekul koosneb süsinikust ja vesinikust. 2) Millised ained on alkaanid, nende üldvalem + nimetused Alkaanid on küllastunud süsivesinikud, mille molekulis süsiniku aatomite vahel on ühekordne kovalentne side. Üldvalem: CnH2n+2 Nimetused: CH4 metaan C2H6 etaan C3H8 propaan C4H10 butaan C5H12 pentaan C6H14 heksaan C7H16 heptaan C8H18 oktaan C9H20 nonaan C10H22 dekaan 3) Millised ained on alkeenid, nende üldvalem + nimetused Alkeenid on küllastamata süsivesinikud, mille molekulis süsiniku aatomite vahel on üks kaksikseos. Üldvalem: CnH2n Nimetused tuletatakse vastavast alkaanist, kus lõpp aan asendatakse een'iga. 4) Millised ained on alküünid, nende üldvalem + nimetused Alküüniod on küllastamata süsivesinikud, mille molekulis süsiniku aatomite vahel on üks kolmikseos. Üldvalem: CnH2n2
Teemaks õpetatus. Samal aastal kirjutas ka religioonivastase satiiri "Vaadilugu". Käsitleb usutunnistuste vahelist sõda. Pamflett- publitsistika zanr, milles terava-tooniliselt paljastatakse ja naeruvääristatakse ühiskonna-, poliitika- ja kirjandustegelasi või nähtusi. Satiir- isiku või ühiskonna pahedele ja puudustele hinnangut andev, tauniv , väja naerev suhtumisviis. 1709. aastal ilmus esimene luulekogu "Baucus ja Pihilemon". 1713. aastal sai temast Dublini St Patricu kiriku dekaan. Pani suurt rõhku oma eraelu kaitsmisele. Kirjutas 1710- 1713. aastal Stellale 65 kirja,mis ilmusid peale Stella surma pealkirjaga "Päevik Stellale" . 1724 aastal kirjutas "Kalevikaupmehe kirjad" Kutsus iirlasi vastu seisma Inglismaa laostavale majandustegevusele. 1726.aasta teine luulekogu "Cadenus ja Vanessa". Pühendatud Vanessale Arendas satiiride ja vaimukate artiklite kirjutamist, mis naeruvääristasid kuulsaid inimesi, rumalaid ideid ja absurdseid kombeid.
Ühe teadusharu kõrgkool ei kuulu ülikooli mõiste alla. Vanim ülikool - Bologna ülikool 1119 (privileegid 1158) - Õpilaste organisatsioon, mis palkas endale ise õpetajaid - doktoreid. juhtis rektor. 12. saj Pariisi ülikool, juhtis kantsler.. Oxford, Cambridge, Salamanca... Eeskujuks sai Pariisi ülikool. Alustati kunstide teaduskonnast, hiljem sai valida ka usu-, arsti- ja õigusteaduskonna vahel. Valiti juht, kes sai ametinimetuseks dekaan. Ülikooli privileegid ja luba saadi paavstilt, hiljem riigivalitsejatelt. Skolastika ülikoolides viljeldud teadusi nimetati skolastikaks. Iseloomulik joon on toetumine autoriteetidele - hüljati kogemus. Põhilise autoriteedina tõusis esile Aristoteles. 1210. tühistatud keeld Aristotelese teostel tühistati 1270. Roger Bacon ja empiirilise teaduse algus Vastandiks skolastikale, kogemusele rajatud teadus. (matemaatika, füüsika ja astronoomia)
Vahepeal Peterburi siirdunud ja seal akadeemikuks saanud G. F. Parrot esitas 1828 Peterburi Teaduste Akadeemiale Lenzi aruande ja tema ettepanekul määrati Lenz Peterburi TA adjunktiks füüsika alal. Kaks aastat hiljem sai Emil Lenz akadeemia erakorraliseks ja 1834 korraliseks liikmeks. Mais 1831 alustas Lenz elektriuurimusi, mis tõid talle teadusliku kuulsuse ja tuntuse. 1836. aastast oli Lenz ka Peterburi Ülikooli professor, seejärel ka füüsikateaduskonna dekaan. 1863 valiti ta Peterburi Ülikooli rektoriks. Ta oli abielus Dorothea Emerentiaga ja neil sündis kolm poega. Emil Lenz suri reisil Itaaliasse Roomas 10. veebruaril 1865 ja on maetud Roomasse. Lenzi reegel Induktsiooni voolu suund on selline,et tema magnetväli takistaks muutust,mis voolu põhjustab Induktsiooni vool toimib alati vastupidiselt seda voolu esile kutsuvale põhjusele.
Sigmaside kovalentne side, mida moodustavate elektronide pilv asub aatomeid ühendaval sirgel. Sigmaside võib ka ühendada omavahel süsiniku aatomeid ja ka süsiniku aatomeid teiste elementide aatomitega. Alkaan süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega. Nimetatakse ka parafiiniks. Alkaani tunnuseks on liide aan. (metaan, etaan, propaan, butaan, pentaan, heksaan, heptaan, oktaan, nonaan, dekaan,..) Tüviühend süsinikuaatomite struktuur, millega on seotud ainult vesinikuaatomid. Teisisõnu peaahel. Radikaal molekulid või aatomid, mille elektronkihis asub paardumata elektron. Ehk osake, millel on üksik paardumata elektron. Pürolüüs Aine lagunemine kõrge temperatuuri toimel. Püsolüüsi tulemusena tekib väga erinevaid aineid. Orgaaniliste ainete kuumutamisel õhu juurdepääsuta saadakse mitmeid lenduvaid aineid, sh veeauru
C6H14 C6H12 C6H10 7 Heptaan Hepteen Heptüün C7H16 C7H14 C7H12 8 Oktaan Okteen Oktüün C8H18 C8H16 C8H14 9 Nonaan Noneen Nonüün C9H20 C9H18 C9H16 10 Dekaan Dekeen Deküün C10H22 C10H20 C10H18 Kordsetes sidemetes on alati üks -side ja teine -side näiteks: o Kaksikside on üks -side ja teine -side o Kolmikside on üks -side ja kaks -sidet. Kaksiksidet moodustavad süsiniku aatomid ja nendega seotud muud aatomid asuvad kõik ühes tasapinnas. Nad on planaarsed.
kodanikke Kuidas kaitses linn oma kogukonna vara ja õigusi? kaitses linna õigusega Mis on tsunfti kraa ja milleks see koostati? põhikiri mis määras ära mis tingimustel saadakse meistriks ja tsunfti liikmeks Millest sõltus keskaehse linnaelaniku sotsiaalne staatus? perkondlik seis, varanduslik seis, rahvus, isiklik huvitatus ja õpihimu Praost juhtis kapiitli majanduselu ja oli varavalitseja Dekaan valvad korra järele Skalastik toomhärradest üks mõjukamaid, korraldas noorte õpetamist Paavst - Riia peapiiskop Tartu piiskop Toomkapiitel kihelkonna preestrid Toomkirik piiskopkonna peakirik Visitatsioon kontroll kiriku üle Missa pisulik jumalateenistus Mille poolest sarnanesid ja erinesid Dominiiklased ja Tsistertslased? Levitasid ristiusku, dominiiklased rajasid oma kloostrid eraldatult aga teised rajasid need tsivilisatsiooni
“0” puudulik “1” kasin “2” rahuldav “3” hea “4” väga hea “5” suurepärane Põhieksamit saab sooritada: ainult 1 kord. Ühe deklaratsiooni alusel on võimalik eksamit sooritada kokku: kuni 2 korda. Üks Euroopa ainepunkt vastab 26 tunnile üliõpilase poolt õppeks kulutatud tööle. Infotehnoloogia teaduskonna dekanaat asub ruumis: ICT-407. Sea vastavusse ametikoht ja isik: TTÜ infotehnoloogia teaduskonna dekaan: Gert Jervan. Infotehnoloogia teaduskonna õppekavakomisjoni aseesimees: Ennu Rüstern. TTÜ infotehnoloogia teaduskonna õppeprodekaan ja õppekavakomisjoni esimees: Margus Kruus. TTÜ rektor: Andres Keevallik. TTÜ infotehnoloogia teaduskonna teadus- ja arendusprodekaan: Maarja Kruusmaa. TTÜ õppeprorektor: Jakob Kübarsepp. TTÜ teadusprorektor: Erkki Truve. Arvestusega lõppeva aine sooritamise õigus kehtib ainult deklareerimissemestri lõpupäevani. Tõene.
Nomenklatuur on reeglite kogum, mis seob nimetuse ja struktuuri. Nimetused: · Süstemaatilised annab teavet struktuurist (nt. metaanhape) · Triviaalnimetused antakse mõne omaduse või leidumuse põhjal (nt. sipelghape) Alkaani tunnuseks on sõnalõpp aan. Sõnatüvi kirjeldab süsinikahela pikkust. 1. Met(aan) 2. Et(aan) 3. Prop(aan) 4. But(aan) 5. Pentaan 6. Heksaan 7. Heptaan 8. Oktaan 9. Nonaan 10. Dekaan Tsüklilist ahelat tühistab eesliide tsüklo. Alküülrühma tunnuseks on sõnalõpp üül. 1. Metüül 2. Etüül 3. Propüül Jne.. Kohanumber kirjutatakse kõige ette ning see tähistab hargnemise kohta. Nt: 2 metüülbutaan Süsinike arv Arvsõna Alkaani Alküülrühma Tsükloalkaani ahelas nimetus nimetus nimetus
Linnaõigus Linna sõltumatus teha otsuseid Raad Linnavalitsus Bürgermeister Rae tähtsaim liige Oldermann - Gildi, tsunfti või muu organisatsiooni esimees Tsunft Käsitööliste ühendus Skraa Tsunfti põhimäärus Gild Kaupmeeste ühendus Hansa Läänemerd hõlmav kaubalinnade liit Skolastika Ülikoolides viljeledud teadused kokku Empirism Kogemusele rajatud teadus (mata, füsa) Universitas Ülikool Rektor (keskaja ülikoolis) Ülikooli juht Dekaan Õppejõudude valitud juht Karavell Kaugsõidulaev, võis sõita ookeanil Tordesillase leping Leping Hispaania ja Portugali vahel, jagati Lõuna-Ameerika Reformatsioon Kiriku ja Ühiskonna muutumine ristiusu puhastamisega Hussiidid Jan Husi õpetusest alguse saanud liikumine Indulgentsid Patulunastuskirjad Simoonia Vaimulike ametikohtade ostmine Kalvinism Calvini õpetuse järgi tegutsev ristiusuvool Anglikaani kirik Inglise kirik, mis lahkus Rooma kiriku alluvusest
NT:CH4 + 2O2 -> CO2 + 2H2O. Reageerimine halogeenidega(7A rühm) on asendusreaktsioon.NT: CH3Cl + Cl2 -> CH2Cl2 +HCl Valemite kirjutamine ja alkaanide nimetuste andmine. Homoloogiline järjekord: 1. metaan CH4 2. etaanC2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptann C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22 Arvutusülesanded. Valemid m=roo*V (g) M=NT:( C6H14)=12*6+14*1=86 (g/mol) C=12 ja H=1, seda saab perioodilisus tabelist. n= V/Vm või n=m/M (mol) V=n*Vm (dm3) Vm=22,4 (dm3/mol) roo=m/V (g/cm3)
Eesti kodakondsust, pikaajalise elaniku elamisluba ega alalist elamisõigust. Külalisüliõpilast ei immatrikuleerita. 12. Külalisüliõpilase staatuse saamiseks esitab isik avalduse, millel on kodukõrgkooli ning Tartu Ülikooli nõusolek ja milles on toodud läbitavate õp peainete loetelu. Õppeprorektori korraldus külalisüliõpilaseks arvamise kohta ning avaldus on aluseks külalisüliõpilase õppeainetele registreerimiseks (vt p 63–68). Dekaan võib jätta avalduse rahuldamata, kui avalduse esitaja ei vasta ainekavas või õppekavas kehtestatud tingimustele või kui õppetöös osalejate piirarv on täis. 19. Ekstern on isik, kellele on antud õigus täita õppekava, sh sooritada eksameid ja arvestusi ja/või sooritada lõpueksam või kaitsta lõputöö. Eksterni ei immatrikuleerita. 20. Eksterni staatust võib taotleda vastavale õppekavale õppima asumiseks
heksaan -161) 69) C2H6(keemistemp etaan C7H16(keemist. heptaan -89) 98) C3H8(keemistemp propaan C8H18(keemist. oktaan -42) 126) C4H10(keemist- butaan C9H20(keemist. nonaan 0,5) 151) C5H12(keemist. pentaan C10H22(keemist.1 dekaan 36) 74) Radikaal – osake, millel on üks paardumata elektron. Alkaanide tüüpilised reaktsioonid on pürolüüs ja oksüdeerumine. Elektrofiil on tühja orbitaali ja positiivse laengu osake. Nukleofiil on vaba elektronpaariga osake ja kannab negatiivset laengut. Alkaanide füüsikalised omadused: Homoloogilises reas C aatomite lisandudes muutuvad kõrgemaks tihedus, sulamistemp., keemistemp.
ja kondensatsioon. Alkaanide nimetused/valemid (graafilised, tasapinnalised, lihtsustatud) Tähtsamad alkaanid: CH4 metaan CH3 metüül C2H6 etaan CH3CH2 etüül C3H8 propaan CH3CH2CH2 propüül C4H10 butaan CH3CH2CH2CH2 butüül C5H12 pentaan C6H14 heksaan C7H16 heptaan C8H18 oktaan C9H20 nonaan C10H22 dekaan Isomeerid (Koostamine, füüsikaliste omaduste tuletamine ja põhjendamine) Isomeeride struktuur on erinev, siis erinevad on ka nende omadused ehk omadused sõltuvad aine struktuurist. Füüsikalised omadused: 1. Sulamistemperatuur 2. Keemistemperatuur 3. Tihedus Põlemisreaktsioonid Põlemisel ained oksüdeeruvad hapniku toimel ehk tekivad OKSIIDID Lihtained 2H2 + O2 2H2O Liitained (kõik elemendid (va N) moodustavad oksiidi CH4 + 2O2 CO2 + 2H2O
Ande Andekas-Lammutaja Keemia - Alkaanid Alkaanide üldvalemiks on CnH2n+2 ning nimetuse lõpuks aan. Alkaanid on küllastunud süsivesinikud, kus süsiniku aatomi vahel on kõik ühekordsed sidemed. Küllastunud tähendab seda, et nad sisaldavad maksimaalselt võimalikku arvu vesiniku aatomeid. Süsinik neis ühendeis on kõige suuremal määral redutseerunud. Kõik alkaanid on veest kergemad, ei lahustu vees, värvusetud. Gaasilised alkaanid on lõhnata, vedelad bensiini lõhnaga. Homoloogilises reas muutub aine olek järgnevalt: C1 C4 on gaasilised, C5 C16 vedelikud ning C17 - ... tahked. Süsiniku arvu kasvuga muutub molekulmass, tihedus ning kasvab sulamis- ja keemistemperatuur. Tahked alkaanid ei märgu. Vedelad alkaanid on tüüpilised hüdrofoobsed lahustid, mis lahustavad teisi hüdro...
Keemia Halogeenühendid- org.ühendeid, kus süsiniku aatomid on seotud halogeeni aatomi või aatomitega. Omadused: · Hüdrofoobsed- ei reag. H2O · Tahked ja vedelad(üksikud gaasid nt. CH3Cl) Nimetamine: 1) kasutan holgeenidele vastavaid eesliiteid. · Floro- (F) · Kloror- (Cl) · Bromo- (Br) · Jodo- (I) 2) Nende ette lisatakse arvsõnaga halogeenide arv(di,tri,tetra jne) 3) Kõige ette kirjutatakse halogeeni aatomi või aatomite koha nr-d. Näited: CH3-CH2-CHBr-CH2-CHCl2 1,1-dikloro-3-bromopentaan CH3-CH-CH2-Cl 1-kloro-2metüülpropaan CH3 Sellist nomeklatuuri nim. asendus nomeklatuuriks....
Sündis 30. mail 1879 Kuressaares Konstantini isa oli kauaaegne Lümanda apostliku-õigeusu preester ja nõnda möödusid poisi esimesed eluaastad peamiselt maal mängides. Fakte 6. septembril 1919 valiti Konstantin Ramul Tartu ülikooli filosoofia- ja psühholoogiadotsendiks. Valdas vene, saksa, ladina, kreeka ja prantsuse keelt. Õpetas 56 aastat psühholoogiat Ramul oli rahvusvaheliselt tunnustatud psühholoogia ajaloo uurija Ramul oli ka filosoofiateaduskonna dekaan Didaktilis-metoodilise seminari juhataja Akadeemilise Filosoofilise Seltsi ning NL Psühholoogide Seltsi Eesti osakonna (1960) asutajaid ja esimees ning «Eesti entsüklopeedia» filosoofiaosakonna toimetaja. Ramul uuris psühholoogia üldteoreetilisi probleeme, teaduste kokkupuutepunkte, lapse- ja loomapsühholoogiat ja psühholoogia ajalugu Haridustee Kooliteed alustas ta Kuressaare kreiskoolis, jätkas saksa õppekeelega gümnaasiumis.
C5H12 Pentaan C5H11 pentüül C6H14 Heksaan C6H13 heksüül C7H16 Heptaan C7H15 heptüül C8H18 Oktaan C8H17 oktüül C9H20 Nonaan C9H19 nonüül C10H22 Dekaan C10H21 deküül Struktuurivalemi koostamisel nimetuse põhjal toimitakse järgmiselt : 1. Kirjutame tüviühendi süsinikahela ilma vesinike ning asendusrühmadeta 2. Nummerdame, kas kirjas või mõttes, ahela süsiniku aatomid 3. Paneme paika asendusrühmad nende kohanumbrite järgi 4. Lisame puuduvad vesiniku aatomi Näited: 3.Alkaanide kasutusalad lähtuvalt omadustest
õppejõud 7 KRONOLOOGIA (3) 1939 1941 joonistamise ja joonestamise õpetaja Riigi Tööstuskoolis, Riigi Tööstusõpilaste Koolis ja Poeglaste Ametikoolis 1942 1944 kuulus Jaroslavli eesti kunstnike kollektiivi, rindekunstnik 1943 Eesti NSV Kunstnike Liidu asutajaliige 8 KRONOLOOGIA (4) 1944 dekoratiiv- ja monumentaalmaali eriala dekaan ja monumentaalmaali ning joonistuse õppejõud Tallinna Riiklikus Tarbekunsti Instituudis (1951 aastast Eesti NSV Riiklik Kunstiinstituut) 1954 Eesti Riikliku Kunstiinstituudi professor 9 KRONOLOOGIA (5) 1962 NSVL Kunstide Akadeemia korrespondentliige 1963 Firenze Kunstiakadeemia auliige, NSVL rahvakunstnik 1972 valiti Leningradi Eksliibriste ja Graafika Ühingu auliikmeks
9. Õppetoetust saab taotleda alates 2. semestrist. Täiendava toetuse taotlemise lisatingimus on, et elukoht Eesti rahvastikuregistri andmetel asub väljaspool Tallinnat ja sellega piirnevaid omavalitsusüksusi. Põhitoetust ja täiendavat toetust taotletakse õppeinfosüsteemi kaudu. Toetust saab taotleda viieks õppekuuks kaks korda õppeaastas septembris ja veebruaris vastava kuu viimase kuupäevani. Õppetoetuste määramiseks moodustab dekaan komisjoni, kaasates üliõpilaskonna esindajaid. 10. Eritoetuse fondist toetuse taotlemisel esitatakse taotlus samuti ÕIS-is. Dekanaati tuleb tuua dokumendid, mis näitavad taotluse motiveeritust (tõendid perekonna suuruse ja kõigi täiskasvanud pereliikmete sissetulekute kohta, muidu taotlust ei vaadata). 11. Põhitoetuse määramisel: Lähtutakse õppemahu täitmise protsendist (30 EAP semestris = 100%). Üle 100% täitnud on võrdsed. Võrdse %-ga üliõpilased on pingereas kaalutud
Alkaanide füüsikalised Omadused: *Metaani ja temaga sarnaste süsivesinike - alkaanide omadused muutuvad korrapäraselt süsiniku aatomite arvu suurenemisega molekulis *Metaan ja temale järgnevad alkaanid erinevad üksteisest aatomite rühma - CH 2 - võrra. Niisugust ühendite rida nimetatakse homoloogiliseks reaks. Rea üldvalem on CnH2n + 2. *Metaani homoloogilise rea 4 esimest ühendit on gaasid, viiendast kuni kuueteistkümnendani vedelikud ja kõrgemad on tahked ained. Molekulmassi kasvuga homoloogilises reas suureneb alkaanide tihedus ning kasvab sulamis- ja keemistemperatuur. *Alkaanid on vees peaaegu lahustumatud. Nad on hüdrofoobsed ehk vett-tõrjuvad *Homoloogilises reas muutuvad homoloogilise rea liikmete - homoloogide - füüsikalised omadused korrapäraselt. *alkaanide keemistemperatuur sõltub molekulmassist ehk süsinikahela Pikkusest-molekulmassi suurenemisega kasvab homoloogide tihedus, sulamis- ja keemistemperatuur ning agregaatolek ...
Tuntumad esindajad METAAN: Maagaas (70-90%) Naftagaas Soogaas Kaevandusgaas ETAAN: Metaani järel tähtsuselt teine koostisosa maagaasis PROPAAN, BUTAAN: Looduslikus gaasis Lahustununa naftas 5 Alkaanide nimetused 1. Metaan 2. Etaan 3. Propaan 4. Butaan 5. Pentaan 6. Heksaan 7. Heptaan 8. Oktaan 9. Nonaan 10. Dekaan 11. Undekaan 12. Dodekaan 20. Ikosaan 21. Henikosaan 30.Triakontaan 40.Tetrakontaan 50.Pentakontaan 100. hektaan 6 Füüsikalised ja keemilised omadused FÜÜSIKALISED OMADUSED: Metaani ja temaga sarnaste süsivesinike - alkaanide omadused muutuvad korrapäraselt süsiniku aatomite arvu suurenemisega molekulis. Metaan ja temale järgnevad alkaanid erinevad üksteisest aatomite rühma - CH2 -
ja akt "Pilved". Kronoloogia 28. novembril 1915 sündis Tallinnas 1931 1937 õppis Riigi Kunsttööstuskoolis 1938 1940 õppis samas koolis maalimist 1939 esimene avalik esinemine 1939 1940 Eesti Kujutavate Kunstnikkude Keskühingu liige, Riigi Kunsttööstuskooli õppejõud 1942 1944 Jaroslvalis kunstnike kollektiivis, ringekunstnik 1943 Eesti Kunstnike Liidu asutajaliige 1944 Tallinna Riikliku Tarbekunsti Instituudi dekaan 1954 Eesti Riikliku Kunstiinstituudi professor 1962 NSVL Kunstide Akadeemia korrespondentliige 1963 Firenze Kunstiakadeemia auliige, NSVL rahvakunstnik 1972 Leningradi Eksliibriste ja Graafika ühingu auliige 1975 NSVL Kunstide Akadeemia akadeemik Auhinnad 1948 Eesti NSV Riiklik preemia 1950 Nõukogude Eesti preemia kristallvaasi kujundamise eest 1959 Nõukogude Eesti preemia 1961 Ljubljana IV rahvusvaheline graafikanäitus 1962 NSVL Kunstide Akadeemia hõbemedal
Metaan CH4 Etaan C2H6 Eteen C2H4 Etüün C2H2 Propaan C3H8 Propeen C3H6 Propüün C3H4 Butaan C4H10 Buteen C4H8 Butüün C4H6 Pentaan C5H12 Penteen C5H10 Pentüün C5H8 Heksaan C6H14 Hekseen C6H12 Heksüün C6H10 Heptaan C7H16 Hepteen C7H14 Heptüün C7H12 Oktaan C8H18 Okteen C8H16 Oktüün C8H14 Nonaan C9H20 Noneen C9H18 Nonüün C9H16 Dekaan C10H22 Dekeen C10H20 Deküün C10H18 Karboksüülhapped on orgaanilises keemias happed, mis sisaldavad karboksüülrühma (COOH). CH3CH3 (etaan) -> CH3COOH (etaanhape). Palju on kasutusel ka triviaalnimetusi, eriti biokeemias. Karboksüülhapete füüsikalised omadused on tingitud nende molekulide võimest moodustada tugevaid vesiniksidemeid. Sel põhjusel on neil ka kõrgekeemistemperatuur ning normaaltingimustel on nad vedelad või tahked
b)hargnenud ahelaga . 2) tsüklilised alkaanid ehk tsükloalkaanid , üldvalemiga C nH2n. Nomenklatuur on aine struktuuri ja aine nimetust siduvate reeglite kogu. 1. Hargnemata ahelaga atsükliliste alkaanide valemid ja nimetused ( C nH2n+2 -aan ) 1) CH4 metaan 2) C2H6 etaan CH3-CH3 3) C3H8 propaan CH3-CH2-CH3 4) C4H10 butaan CH3-CH2-CH2-CH3 5) C5H12 pentaan 6) C6H14 heksaan 7) C7H14 heptaan 8) C8H18 oktaan 9) C9H20 nonaan 10) C10H22 dekaan 2. Tsükloalkaanide valemid ja nimetused (C nH2n) tsüklopropaan tsüklobutaan tsüklopentaan tsükloheksaan ∆ □ ⌂ (graafilised kujutised) 3. Hargnenud ahelaga alkaanide nimetamine valemi järgi 1) asendusrühm ehk alküülrühm, tähis -R, üldvalem Cn H2n+1 CH4 metaan → -CH3 metüül C2H6 etaan → -C2H5 etüül JNE.
Retentsiooniaeg tR = to + t'R Homoloogid väljuvad kolonnist ahela suurenemise järjekorras. Parandatud retentsiooniajast t'R= tR-t0 Alkaan tR, min t`R, min C6 Heksaan 1,765 0,654 C7 Heptaan 2,341 1,23 C8 Oktaan 3,336 2,225 C9 Nonaan 4,673 3,562 C10 Dekaan 6,181 6,07 3.2 Kromatograafilised andmed ja ainete identifitseerimine Aine tR, min SH SSH A SH SSH W,min RI Aine nimetus 1 2,859 0 0 4355272,0 126394,416 2,952 0,14 752 Tolueen 2,859 4354373,5 0,149
õppe-kui kõnekeelena, siis kujunes ülikoolide terminoloogiast välja just ladina keeles. Studiosus ehk student (siit eesti keelde mugandatud tudeng) tuletati verbist studere, mis tähendas hoolsalt õppima, millegi poole püüdlema ja mis pidas vähemalt osa üliõpilaste suhtes paika. Õppejõud moodustasid fakulteedi (facultas- võime, s.o. võime ja oskus õpetada mingit teadust.Fakulteedi õppejõudude hulgast valiti dekaan, kes esindas teaduskonda ülikooli juhtkonna ees. Ülikooli juhtis rektor. Rektor valiti kõrgele ametikohale lühikeseks ajaks, tavaliselt pooleks aastaks. Seejuures ei pruukinud ta olla õppejõud, vaid oli sageli keegi mõjukatest üliõpilastest. Rektori peamised ülesanded olid: üliõpilaste immatrikuleerimine ehk kandmine ülikooli nimekirja (matriklisse), suurkooli vara valitsemine, pidulike koosolekute juhatamine, korra eest vastutamine, kohtumõistmine akadeemilise pere
Sellid, kes abiellusid meistri lesega, said meistriks. Gild ühinenud tsunftid Tsunftijänes tsunftiväline käsitööline Hansa Liit - oli 13.17. sajandil tegutsenud Põhja - Saksamaa, Skandinaaviamaade, Madalmaade ja Liivimaa linnade kaubanduslik ja poliitiline liit. Koge - on keskaegne ühe- või kahemastiline purjelaeva tüüp, kasutusel nii kauba- kui sõjalaevana. Universiteet üliõpilasorganisatsioon 13.saj algul Rektor ülikooli juhataja ametinimetus Dekaan kõrgkooli teaduskonna juhi ametinimetus Skolastika - on keskaja filosoofiliste õpetuste kogum, milles usulist maailmavaadet põhjendati Aristotelese loogika abil. Skolastika olulisimaks saavutuseks oli formaalloogika arendamine. Romaani basiilika keskaja kiriku planeering lähtus vana-rooma kohtu ja kaubakojast basiilikast, kus toimusid pärast ristiusu ametlikuks kuulutamist ka esimesed avalikud jumalateenistused
faculty (faculties), department to fail/flunk student hostel/residence hall/dormitory/dorm ühiselamu to retake an exam/make up an exam canteen/cafeteria an incomplete "võlg" rector/president to graduate from a college ülikooli lõpetama vice rector/vice president prorektor a graduate/ an alumnus(pl. Alumni) vilistlane dean dekaan bachelor's degree bakalaureusekraad lecturer, instructor BSc Bachelor of Science tehnikateaduste bakalaureus to give/to deliver lectur BA Bachelor of Arts humanitaarteaduste bakalaureus a diploma thesis (pl theses) diplomitöö master's degree magistrikraad
REEGEL! Suurema kütteväärtusega põlevad need kütused, mille koostises oleva süsiniku o-a on väikseim. 6. Alkaanide koostis. Alkaanid koosnevad C ja H aatomitest ning süsiniku aatomite vahel on ainult üksiksidemed. CH4 metaan C5H12 pentaan C9H20 nonaan C2H6 etaan C6H14 heksaan C10H22 dekaan C3H8 propaan C7H16 heptaan C4H10 butaan C8H18 oktaan 7. Alkaanide leidumine looduses. Metaan- maagaasi koostises. Propaan vedelgaasi koostises. 8. Osata kirjutada alkaanide süstemaatilisi nimetusi, kui on antud struktuurivalem. Hargneva ahela puhul nimetused: CH3
meediakanalitest ka tunnustatud õigusteadlaste sõnavõtte, kes andsid selgitusi ja oma hinnanguid õiguslikule olukorrale. Kahjunõude olemust ja probleeme selgitas meedias Riigikohtu nõunik Irene Kull.1 Vandeadvokaat Leon Glikman põhjendas omapoolses arvamusavalduses, et tema võtaks seadusest välja ,,erandliku asjaolud" mille olemasolu hetkel kehtiv seadus nõuab mittevaralise kahju hüvitamise eeldusena. 2 Tartu ülikooli õigusteaduskonna dekaan Jaan Ginter käis omapoolses sõnavõtus Laiksoo juhtumi varal välja idee moraalse kahju hüvitamisest, kus paika on pandud täpsed tariifid kindlate lähedaste hukkumise puhuks.3 Kuigi riigikogu õiguskomisjoni esimees Marko Pomerants pidas oma arvamusavalduses eraldi ,,hukkunute hinnakirja" kehtestamist problemaatiliseks, pakkus ta välja teatud alternatiive, kuidas riigikohus saaks olukorda leevendada.4 Just selline avalik diskussioon on see, mille tõstatudes meedias ka ühiskond võidab