harusid. Termodünaamika aga uurib igasuguseid energia üleminekuid ühest liigist teise, 11 mitte ainult mehhaanilise energia ja siseenergia vastastikuseid muundumisi. Toome siinkohal mõningaid andmeid aine molekulaarstruktuuri kohta. Anorgaaniliste ainete molekulide läbimõõt on suurusjärgus 10-10 m =100 pm. Molekulid on pidevas kaootilises liikumises. Tahke aine korral tähendab see võnkumist kindla tasakaaluasendi ümber, kusjuures võnkesiht ja -amplituud muutuvad täiesti ettearvamatul viisil kaootiliselt. Vedelikes käituvad molekulid lühiajaliselt nagu tahkes aines, kuid vahetavad siis, jällegi juhuslikul hetkel ja juhuslikus suunas oma asukohta. Tahkes ja vedelas olekus on molekulid vastastikuses mõjustuses naabermolekulidega: tasakaaluasendis on nende molekulaarjõudude
docstxt/1429703051542.txt
FAASISIIRDED - tahke, vedel, gaasiline Faas on ühesuguse keemilise koostise ja füüsikaliste omadustega aineolek. · Ühes agregaatolekus võib olla mitu faasi. · Gaasilises olekus ei eksisteeri erinevaid faase. Faasisiire on protsess, kus aine läheb ühest faasist teise. Faasisiirded: · sulamine (tahkest vedelasse) - tahkumine · aurumine (vedelast gaasilisse) - kondenseerumine · sublimatsioon (tahkest gaasilisse) - härmatumine Soojushulga arvutamine soojenemine <=> jahtumine Qneeldub Qvabaneb Q=cm(t2-t1) Q - soojushulk 1J c - erisoojus J/kgC0 aurumine <=> kondenseerumine Q neeldub Qeraldub Q=Lm L - aurustumissoojus keemistemperatuuril 1J/kg sublimatsioon <=> härmatumine Q=m - sulamissoojus 1J/kg soojushulk kütuse põlemisel Q=km k - kütteväärtus 1J/kg Kriitiline temperatuur on temp. millest kõrgemal väärtusel ei ole võimalik gaasi kokku surudes muuta vedelikuks. Vedeliku pinnal o...
docstxt/.txt
Õppjõuks oli Paesalu.
Füüsika I praktikum nr 25. Tahke keha soojuspaisumine. Tabelid, graafik, arvutused, kaitstud
Kuidas mõista araablasi Sissejuhatus : · kirjaoskus on kasvanud kolmekümne aastaga kahe-või kolmekordseks · araabia naised saavad rohkem haridust · parem tervishoiusüsteem parandab elukvaliteeti ja pikendab eluiga · võtta lääne tsivilisatsioonilt tehniline ja teaduslik teave, heita kõrvale kahjulikud muutused · halim barakat : araabia ühiskond on killustunud, autoritaarne, traditsionalistlik, kannatab patriarhaalsuse, ühtse kodanikuühiskonna puudumise all · lääne haridus alahindab sügavamaid, vaimseid väärtusi, soodustab teaduslikke uurimusi usu arvelt · islam peab tähtsaks teadmiste seostamist vaimsete eesmärkidega · haritud araablased on õppinud leidma tasakaalu tänapäevase elu ja traditsiooniliste väärtuste vahel Fundamentalism : · islamiriikidele omane ühisjoon : lahtiütlemine lääne moraalist ja käitumiskoodeksist, kui se ...
Aine ehituse alused 1.Millistes olekutes võivad ained esineda? (3 punkti) Vedelas Tahkes Gaasilises 2. Millega on määratud aine esinemine erinevates olekutes? (3 punkti) Aine olek on määratud molekulide vahel mõjuvate elektromagneetiliste tõmbe ja tõuke jõududega. 3.Millest koosneb siseenergia? (2 punkti) Siseenergia koosneb kineetilisest ja potensiaalsest energiast 4. Milline energia on gaasides ülekaalus? Miks ? (2 punkti) Gaasides on ülekaalus kineetiline energia, kuna molekulide vahel on palju ruumi ja nad on pidevas liikumises. 5. Milline energia on ülekaalus tahkistes? Miks? (2 punkti) Tahkistes on ülekaalus potentsiaalne energia, kuna molekulid on omavahel tihedalt seotud ja võnguvad. 6. Mille poolest erinevad reaalsed gaasid ideaalsetest? (2 punkti) Reaalsetel gaasidel ei käsitleta molekule punktmassidena, ideaalsel gaasil käsitletakse. Reaalsetel gaasidel arvestatakse molekul...
mikromool produkti 30 kraadi celsiuse järgi. TÖÖ KÄIGUD Töö käigud koosnevad kolmest osast: ensüümipreparaadi valmistamine, ensüümireaktsiooni läbiviimine ja tiitrimine ehk taandatud suhkru kontsentratsiooni määramine. Vajalikud töövahendid, ained ja nende kogused on töökäigus ära märgitud. 1. Ensüümpreparaadi valmistamine Vajalikud töövahendid - Automaat pipett (kuni 1ml-ne) - väike keeduklaas tahke invertaasi koguse kaalumiseks - gradueeritud katseklaas kuhu läheb invertaasi ja atetaatpuhvi lahus - analüütiline kaal (0.0001 grammi täpsusega) - väike lusikas invertaasi üle kandmiseks - väike klaaspulk invertaasi-puhvi lahuse segamiseks Vajalikud ained - 9,5 mg tahket invertaasi - 2,4 ml atsetaatpuhvrit (pH = 4,8) 4 3.1 Invertaasi aktiivsuse määramine Martin Tamm (121006YASB)
1.Tahke keha füüsika Aatomeid seob molekulideks ja kristallideks keemiline side, mille põhiliigid on ioon- ja kovalentsside. Ioonside tekib positiivsete ja negatiivsete ioonide vahel. Kovalentsside tekib elektronpaaride ühistamisel. Kristallid on makroskoopilised hiidmolekulid, milles aatomid või ioonid on paigutanud korrapärasesse ruumvõresse. Tahke keha omadusi saab uurida, kui on teada Fermi nivoo asukohta. 1.1 Ioonilisesideme teke Iooniline side- üks aatom võtab teiselt elektroni ära, iooniline side moodustab kristalli, kuna struktuur võib jätkuda lõpmatuseni. Positiivsete ja negatiivsete ioonide vahel tekib tõmme, mis seostab ioonilise sideme. Kloor tõmbab naatriumi elektroni, et ma pilve aatom oleks ühtlasem ja energia väiksem. 1.1.1 Kristallid Aatomid/ioonid on paigutatud kindlas korras, moodustades ruumvõre
docstxt/14146054359049.txt
Märgamine ja kapillarsus http://gyazo.com/77eb43d64fa0e97c66e976cd802ddb1b Märgamise korral on vedeliku molekulide ja tahke keha molekulide vahelised tõmbejõud suuremad, kui vedelikusiseste molekulide tõmbejõud. http://gyazo.com/dc3a277bb10dc19a32ab7b680854608d Kapillarsus on vedeliku tõusmine või langemine peenikestes torudes ehk kapillarides. Kui vedelik märgab tahket keha, siis ta tõuseb kapillaarsuses ja vastupidi http://gyazo.com/a48e7156c0e3bb3ccab2d97b4dd89951 Kui vedel märgab tahket keha, siis vedelik tõuseb torus seda kõrgemale, mida peenem on toru. http://gyazo
MOLEKULAARFÜÜSIKA ALUSED: Tahke- asukoht: korrapäraselt; liikumine: aineosakesed võnguvad oma kindlas kohas; side: väga tugev. Vedel- asukoht: üksteise lähedal, muutub kergesti; liikumine: aineosakesed võnguvad ja asukoht muutub; side: tugev. Gaas- asukoht: hõre, kaootiline; liikumine: kaootiline; side: väga nõrk. Keerukam on kirjeldada tugevat sidet ja kõige lihtsam kirjeldada gaasi. Gaasi molekulaarkineetiline mudel- eeldused: aine koosneb molekulidest; molekulid on pidevas kaootilises liikumises; molekulide vahel on vastastikumõju. Ideaalse gaasi mudel molekulid on punktmassid; põrked absoluutselt elastsed; vastastikumõju aineosakeste vahel puudub. Normaaltingimustes on gaasid hästi kirjeldatavad. Makrotasandi parameetrid: rõhk-P, temp-T, mass-M, ruumala-V, aine kogus-mool. Mikrotasandil: molekuli mass-m, molekuli kiirus-v, molekulide arv-N. Rõhk näitab missugune jõud mõjub pindala ühikule. Osakeste kiirused: raskemad molekulid...
Aine agregaatolekud Eidapere kool 2009 Aine võib olla erinevates olekutes Muutke teksti laade Teine tase Kolmas tase Neljas tase Viies tase Milline on tahke aine ehitus? Muutke teksti laade Teine tase Kolmas tase Neljas tase Viies tase Milline on vedeliku ehitus? Muutke teksti laade Teine tase Kolmas tase Neljas tase
molekuli kirjeldamisel.Nendeks on näiteks molekuli mass,molekuli kiirus 2. Millised on soojusliikumise kolm põhialust a. Aine koosned molekulidest b. Oskakesed on pidevas liikumises c. Osakesed mõjutavad üksteist tõmbe- ja tõukejõududega.Kauguse suurenedes oskeste vahel saavad ülekaalu tõmbejõud, kauguse üleliigsel vähenemisel aga tõukejõud 3. Võrdle aine ehituse mudeleid(tahke,vedel,gaasiline). a. Tahke-aineosakesed üksteise lähedal b. Vedel-aineoskased liiguvad ringi c. Gaasiline-aineosakesed liiguvad suure amplituudiga, kaootilsielt 4. Mida nimetatakse temperatuuriks? a. Temperatuur iseloomustab kehade soojusastet 5. Millest koosneb termomeeter? a. Elavhõbeda sambast,skaalast,elavhõbeda samba reservuaarist 6. Iseloomusta Celsiuse ja Fahrenheiti skaalat. a. -273C=0K b. 0C=273K c. 100C=373K 7. Kui suur on 1 at(mmHg,Pa) a
Sissejuhatus Töö eesmärgiks oli tahke soola, mis võis olla kaksiksool, või lahuse analüüs. Lahus võis seega sisaldada ühe või kaks katiooni ja ühe aniooni, kusjuures katioonid pidid olema erinevatest rühmadest. Määrata tuli nii katioonid kui anioonid. Töö käik Uuritavaks aineks oli tahke aine VIII. Kuna tegemist oli sinakasrohelise pulbriga, võis ennustada nikliioonide olemasolu. Valmistasin ainest lahuse, selleks panin natuke ainet katseklaasi, lisasin destilleeritud vett ja segasin, kuni sool oli täielikult lahustunud. Ka tekkinud lahus oli sinakasrohelise värvusega. I rühma katioonide tõestamine Katioonide I rühma sadestamiseks lisasin uuritavale lahusele HCl, kuna sadet ei tekkinud, võis välistada I rühma katioonide Pb2+, Hg22+ ja Ag+ olemasolu lahuses.
Referaat Aine agregaatolek (tahke, vedel, gaasiline) Õpilane: Õpetaja: Klass: Aine agregaatolek on aine olekuvorm, mille määrab soojusliikumise laad.Kui välistingimused muutuvad (rõhk, temperatuur, ruumala) siirdub aine pidevalt või hüppeliselt ühest agregaatolekust teisele.
Molekul - aine väikseim osake, millel on antud aine keemilised omadused ning mis võib iseseisvalt eksisteerida 3. Ainete klassifikatsioon, liht ja liitainete mõisted, näited. Lihtaine - moodustub ainult ühe ja sama keemilise elemendi aatomitest. Näiteks: hapnik, raud, elavhõbe, väävel Liitaine - koosneb erinevatest keemilistest elementidest. Näiteks: vesi, lubi, süsinikdioksiid Nii liht- kui liitained võivad esineda gaasilises, vedelas või tahkes olekus. 4. Aine olekud (tahke, vedel, gaas) Tahkes aines on molekulid tihedalt koos ja nende liikumine pole võimalik. Vedelikus on molekulide vaheline kaugus mõnevõrra suurem ja nad võivad üksteisest mööduda. Gaaside puhul on molekulide vaheline kaugus suur ja nad võivad täiesti vabalt liikuda. Molekulide vahelised jõud on väikesed. 5. Aine omadused (füüsikalised, keemilised) Füüsikalisi omadusi saab mõõta ja jälgida ilma ainet ja tema koostist muutmata (värvus,
Polina Murtazina Koostada Venni diagrammid:"Tahke keha ja gaasiline keha. Soojusjuhtivus ja soojuskiirgus." Tahke keha Sarnasus Gaasiline keha On kehade seisundid Liiguvad kaotiliselt, põrkudes Võnguvad kindlate asendite teiste osakestega ümber Kineetiline energiaon väike Koosnevad molekulidest ning Kineetiline energia on suur aatomitest Potensiaalne energia on suur Sublimatsiooni korral tahked Potensiaalne energia
Mõisted aineehituse kohta Aine olek Aine olek ehk agregaatolek on aine vorm, mille määrab tema molekulide soojusliikumise iseloom. Ainel on kolm põhiolekut: tahke, vedel ja gaasiline. Kondensatsioon Aine üleminek gaasilisest vedelasse või tahkesse olekusse. Gaas Aine olek, milles osakesed liiguvad vabalt, olemata vastasmõjus aine teiste osakestega. Vedelik Vedelas olekus olev aine. Aine on voolav ja võtab anuma kuju, mida ta täidab. Ruumala määratletud temperatuuri ja rõhuga. Tahkis Tahkes olekus olev keha. Molekulide vahel mõjuvad tugevad seosejõud. Enamiku ainete puhul on tahkise tihedus vedeliku ja gaasi omast suurem.
Litosfäär- Maa tahke väliskest, koosneb maakoorest ja vahevöö ülaosast (kuni astenosfäärini). Astenosfäär- ülemises vahevöös, u100-300 km sügavusvahemikus paiknev piirkond, valitseva rõhu,kõrge temperatuuri toimel on aine poolvedel:astenosfääri olemasoluga seletatakse litosfäärilaamade liikumist. Litosfäärilaamad- hiiglaslikud plaatjad plokid. Pinnamood e. Reljeef- maapinna ebatasasuste kogum, moodustavad mitmesugused pinnavormid,kujuneb maakoore pideva arenemise tagajärjel. Pinnavorm- geoloogiliste sise-ja välisjõudude toimel maapinnal või merepõhjas tekkinud kõrgend (pos. Pinnavorm: küngas, mägi, vall),süvend(neg pinnav: lohk, süvik, org)või tasand(tasandik), erineb naaberaladest kõrguse,välisilme,tekkeloo poolest. Struktuursed pinnavormid- pinnavormid, mis on tekkinud Maa sisejõudude tegevuse tulemusena. Murenemispinnavormid- Pinnavormid, mis on tekkinud kivimite pealispinna purunemise, lahjustumise tõttu Maa välisjõudude toimel. Kul...
kontsentratsiooni), mida me võime teatud piirides meelevaldselt muuta, ilma et seejuures faaside arv muutuks. Faaside tasakaalu korral on sama keemiline potentsiaal kooseksisteerivatel faasidel ning segu puhul ka segu eri komponentidel. Näiteks tasakaalu korral vedeliku ja tema kohal oleva küllastatud auru vahel on keemilised potentsiaalid kumbaski faasis võrdsed. Keemiline aine võib esineda erinevates vormides: – gaasiline faas; – vedel faas; – tahke faas. Nende faaside vahel on võimalik kolm tasakaali: Tahke - vedel Tahke - gaas Vedel - gaas Paljude ainete korral eksisteerib rida erinevaid tahkeid faase (teemant ja grafiit, erinevad jää vormid). Tasakaalus olevate faaside vahel toimub pöörduv ainevahetus, kus ajavahemikus ühest faasist teise (vastassuunas) üleminevad ainehulgad on võrdsed. 2. Ideaalsete lahuste üdiseloomustus Lahust, mis vastab täpselt Raoult'i seadusele, nimetatakse ideaalseks lahuseks.
Pascali katse tulemusena näeme et vesipurskas välja kõigis suundades. Seega vedelikes ja gaasides erineb rõhk võrreldes tahke kehaga, kus rõhk antakse edasi ainult mõjumise suunas. (nt naela seina läbimine) Pascali seadus: rõhk vedelikes ja gaasides antakse kõigis suunas edasi ühtemoodi. Kasutamine: hüdraulised pidurid. Õhurõhk sõltub kõrgusest mere pinnast. Mida kõrgemale me tõuseme seda väiksem on õhkurõhk (sp et õhukihi paksus väheneb). See väljendub nt mägedes ronimisel (verejooksud jne). Üleslükkejõud sõltub põhiliselt keha vedelikus oleva osa ruumaalast.
Üksiklus kui eluviis? Mis on üksiklus? Üksiklus ehk vallalisus on eluperiood, mil inimesel ei ole püsivat paarisuhet ning ei ole abielus Enamasti elatakse sellisel puhul üksinda või vanemate/sugulaste/sõprade juures Vallalisus võib ka olla eluviisiks, kus ei otsitagi kaaslast Alalise üksikluse juured ulatuvad kaugele minevikku, näiteks ei ole läbi aegade lubatud preestritel, munkadel ning nunnadel omada kaaslast. Selle eesmärgiks on pühendada end täielikult Jumala teenimisele. Tänapäeval on aga usu asemel selle põhjuseks validavalt majanduslikud eelised ning omaenda tõekspidamised. Mis on vallalisuse plussid? Vabadus. Olles üksik, võid teha mida tahad, millal tahad. Ei ole kompromisse. Isegi sobivas suhtes on vaja aegajalt teha järeleandmisi. Üksikelus ei pea millegi suhtes järele andma, kui seda ei soovi. Rohkem...
Maakoor – kõige välimine kõvadest kivimitest koosnev tahke kest. Mandriline maakoor: paksem(kuni 70km), kergemad kivimid, vanem(kuni 4miljr a), väiksema tihedusega(2.7g/cm3), sette, moonde ja tardkivimid,graniit.Ookeaniline maakoor:õhem(kuni 20km), raskemad kivimid, noorem(kuni 18milj a), suurema tihedusega(3), settekivimid ja tardkivimid(basalt).Vahevöö - koosneb kuumast ja tihedast kivimimassis. Jaguneb ülemiseks ja alumiseks vahevööks, kivimeteoriitide sarnastest kivimitest koosnev
See on haigus, mis käib haigestunuga kaasas kogu elu ning vajab pidevat ravi. Hoolimata arenevatest ravimeetoditest ning sellega diabeetikule parema elukvaliteedi võimaldamisest, arenevad aastate jooksul oraganismis muutused. Tekivad diabeedi tüsistused, millest üks tavalisimaid on silma võrkkestahaigus e retinopaatia. Diabeetiline retinopaatia on Eestis 30-65-aastaste hulgas üks peamine pimedaksjäämise põhjus. Referaadi neljas osas uurin diabeetilise retinopaatia erinevaid tahke. Esimeses osas tutvustan diabeeti üldiselt, et mõista haiguse olemust ning sellest lähtuvaid retinopaatia tekkepõhjusi. Teises osas käsitlen juba diabeetilist retinopaatiat lähemalt selle liike ja tunnuseid. Kolmas osa on pühendatud võrkkesta tüsistuste ennetusele ning viimane, neljas selle ravile. Töö eesmärk on saada ülevaade antud seisundist, mis puudutab tihedalt optomeetria valdkonda. Olgugi, et Eestis optometristid retinopaatia raviga ei tegele, on neil oluline
Virtuaalmaailma mõjud ühiskonnale Virtuaalkeskkonna sünd on toonud nii meie igapäevaellu kui ka ühiskonda uusi tahke ja varjundeid. Eestis on raske leida inimest, kes ei oleks sellise keskkonnaga pidevalt ühenduses ega kasutaks selle teenuseid. Kuidas virtuaalmaailm mõjutab tänapäeval inimese maailmapilti ning missugused on selle maailma voorused ning ohud? „Sünteetilised maailmad“ kahandavad meie privaatsust ja muudavad suhtlust inimgruppide vahel. Hiljuti tuli avalikuks info, et USA Riiklik julgeolekuagentuur NSA on ebaeetiliselt kogunud informatsiooni
2 ) soojusliikumine Robert Brown vaatles läbi mikroskoobi karukolla eoseid ja sai aru, et osakesed liiguvad korrapäratult ( nimetatakse Browni liikumiseks ). Osakesed liiguvad korrapäratult, sest nad saavad tõukeid igalt poolt teistelt aineosakestelt. Osakeste liikumine ei lakka kunagi. Mida kiiremini aineosakesed liiguvad, seda soojem on keha , aine temperatuur on kõrgem ( seetõttu nimetatakse ka soojusliikumiseks ). 3 ) tahke, vedel ja gaasiline aine Tahke aine ehk tahkis. Tahkis säilitab kuju. Kristallilistes ainetes ( jää, sool, metallid ) paiknevad aineosakesed korrapäraselt ning on tugevalt omavahel seotud. Osakesed võnguvad oma tasakaaluasendi ümbruses. Kristallilisi aineid kujutatakse kristallvõrena ( aine osakesed on kerad, jooned toovad esile ruumilisuse ). Vedelik. Voolavad ja ei säilita kuju. Aineosakesed paiknevad hõredamalt kui tahkises.
Soojenemise tulemusena suureneb aineosakeste kineetiline energia. Keha aineosakeste kineetilise energia ja potentsiaalse energia summa moodustab keha siseenergia. Siseenergia sõltub aineosakeste liikumise kiirusest ja aineosakeste vastastikusest asendist. Aineosakeste kiirus muutub keha soojenemise või jahtumise tulemusena. Aineosakeste kaugus aines muutub aine oleku muutumise tulemusega: vedeliku tahkumisel või tahke sulamisel, samuti vedeliku aurumisel või auru kondenseerumisel. Keha siseenergia muutub temperatuuri muutumisel kuid ka aine oleku muutumisel. Soojushulgaks nim keha siseenergia hulka, mis kandub sellelt teistele kehadele või teistelt kehadelt antud kehale. Soojushulka tähistatakse tähega Q. Soojushulga ühik on 1 J ja 1 cal. 1 cal=4,2 J 1 kalor on soojushulk, mis on vajalik 1 g vee temperatuuri tõstmiseks 1 C võrra
11.15 1.Töö eesmärk Tutvuda metallide korrosiooni mõningate enamlevinud ilmingutega. 2.Kasutatud mõõteseadmed,töövahendid ja kemikaalid Töövahendid: Katseklaasid, väike keeduklaas (50 cm3), tsentrifuugiklaas Kasutatud ained: 0,1 M soolhape, 0,1 M väävelhape, tsingi- ja alumiiniumigraanulid, vasktraat, vask(II)- sulfaadi lahus, vask(II)kloriidi lahus, raud(II)sulfaadi lahus, kaaliumheksatsüanoferraat(III) lahus, tsingitud raudplekk, tinatatud raudplekk, rauast kirjaklambrid, tahke NaCl, urotropiin. ZnCl2 3.Töö käik 3.1 Galvaanipaari moodustamine Asetasin tsingikraanuli tsentrifuugiklaasi ja valasin peale soolhappelahust. Zn + 2HCl → ZnCl2 + H2 Zn + 2H⁺ → Zn²⁺ + H2 Redutseerija Zn Oksüdeerija H+ Zn - 2e⁻ → Zn²⁺ 2H⁺ + 2e⁻ → H2 3.1.1 Järgnevalt asetasin samasse tsentrifuugiklaasi (soolhappelahusesse) vasktraadi nii, et see ei puutuks kokku tsingiga. Jälgisin, kas vase pinnalt eraldub vesinikku. Vasktraadi
Polaarsetest molekulidest koosnevate ainete lahustumine vees. Polaarse molekuli ümber pöörduvad vee molekulid positiivse laenguga molekuliosa negatiivse poolusega ja vastupidi. Vee molekulide toimel nõrgenevad lahustuva aine molekulide omavahelised sidemed ning aine jaguneb üksikuteks hüdraatunud molekulideks, mis segunevad veega. Missugune on soojusefekt aineosakeste hüdraatumisel? Hüdraatumisel soojus eraldub (eksoterminile protsess). Missugine on soojusefekt tahke aine kristallvõre lagunemisel? Osakestevahelised sidemed katkuvad lahustuva aine kristallis, millega kaasneb soojuse neeldumine (endotermiline protsess). Kuidas sõltub enamiku tahkete ainete lahustuvus temperatuurist? Tahkete ainete lahustuvus vees temperatuuri tõstmisel suureneb. Kõrgel temperatuuril osakestevahelised sidemed muutuvad nõrgemaks, nende lõhkumine muutub kergemaks ja aine lahustuvus suureneb. Kuidas sõltub gaasiliste ainete lahustuvus rõhust ja temperatuurist?
Ekvaatori tasandis ümbritseb Jupiteri Maalt nähtamatu rõngaste süsteem. Jupiteri magnetväli on umbes 14 korda suurem kui Maal. Planeedi orbiit on ovaalse kujuga. Jupiter teeb tiiru ümber Päikese 4333 Maa päevaga ( st peaaegu 12 Maa aastat). Ta tiirleb kiiremini, kui ükski teine planeet. Üks ring ümber oma kujutletava telje võtab aega 9 tundi ja 56 minutit. Jupiteril nagu kõigil hiidplaneetidel puudub tahke pind. Teleskoobis on näha heledad ja tumedad pilvevööndid, mis tiirlevad ümber planeedi eri kiirusega.Diferentsiaalne pöörlemine on hiidplaneetidele ja tähtedele tüüpiline - Jupiteri ekvaatori lähedaste piirkondade pöörlemisperiood on umbes 5 minutit lühem kui pooluste lähedal, vastavalt 9 tundi ja 50.5 minutit ning 9 tundi ja 55.7 minutit. Jupiteri 1000 km paksune atmosfäär koosneb peamiselt vesinikust (70%) ja
Mitteühtlane liikumine on ebaühtlase kiirusega liikumine. 11.Mida nimetatakse jõuks? Nimeta jõu ühik. Jõuks nimetatakse ühe keha mõju suurust teisele kehale. Jõu ühik on 1N- üks njuuton. 12. Mis on raskusjõud? Raskusjõud on maa külgetõmbe jõud. 13.Millal tekib kehas elastsus jõud? Kehas tekib elastsus jõud, kui elastne keha muudab oma kuju. 14.Millega mõõdetakse jõu suurust? Jõu suurust mõõdetakse dünamomeetriga. 15. Nimeta 3 aine olekut. 3 aine olekut on tahke, vedel ja gaasiline. 16. Mis on sulamine? Sulamine on tahke aine muutumine vedelaks. 17. Kirjelda tahke aine ehituse mudelit. Tahke aine säilitab oma kuju, aineosakesed on korrapäraselt ja tihedalt 18.Miks gaas täidab kogu ruumi? Gaas täidab kogu ruumi sellepärast, et aineosakestel on nõrgad sidemed ja saavad vabalt liikuda. 19.Millisel nähtusel põhineb vedelik termomeetri töötamine? Vedelik termomeetri töötamine põhineb soojuspaisumisel. 20. Mida näitab aine tihedus?
Kooskõlas Archimedese seadusega asub 1/10 jää massist ülalpool veepinda. Mis on sellel seost litosfääriga? Ka lotosfääri osad liiguvad vertikaalsuunas, et saavutada isotaatiline tasakaal astenosfääriga. Iseloomusta geotermilist gradienti. Geotermiline gadient näitab, kuidas suureneb temperatuur Maa sisemusele lähemale jõudes. Mida rohkem Maa sisse, seda suuremad on ka rõhu kasvu tingimused. Maa tsentris ületab temperatuur 6000 kraadi. Miks on Maa tuum tahke? Kuigi temperatuur Maa tuumas on kõrge, ei ole see siiski piisavalt kõrge, et tuuma kivimeid üles saaks sulatada. Millised kihid Maa sees on üles sulanud? Vahevöö alumises (u 200 km laiuses piirkonnas) on välistuum üles sulanud. Seal on sulanud kivimid ja mõni protsent astenosfääri materjalist (u 100-200 km sügavusel) on sulanud olekus. Too üks konkreetne näide konvektsioonirakust. Vahevöö-tuuma piiril on materjal
Hõõrdejõud on keha liikumist takistav jõud teise tahke keha või aine suhtes kokkupuutepinnal mõjuvate osakestevahelise jõu tõttu. Mõjutavateks teguriteks on keha raskus jõud ning pindade materjal ja omadused. Elastsusjõud on keha kuju ja mõõtmete muutmisel ehk deformeerimisel tekkiv jõud, mis on vastassuunaline ning suuruselt võrdne jõuga, mis keha antud hetkel deformeerib. Jäikus on keha võime koormuse all vastu panna kuju ja mõõtmete muutumisele ehk deformeerimisele.
Soojusjuhtivus. Argielukogemusest teame, et kuuma tee või segamisel läheb hõbe- või alumiinium lusikas kuumaks, plastlusikas soojeneb aga vähe. Hõbe, vask, alumiinium jt. metallid on head soojusjuhid. Head soojusjuhid on kättevõtmisel külmana, sest nad juhivad soojuse kiiresti ära. Näiteks käepide ja potisangad pole tavaliselt metallist, vaid puidust või plastist, sest metallsangad muutuksid tulel kuumaks. 1.5 Tahke, vedel ja gaasiline olek Üks ja sama aine võib esineda mitmes olekus. Tavalised aine kolm olekut on tahke, vedel ja gaasiline. Käsitlen tahket, vedelat ja gaasilist olekut vee näitel. Suvel on vesi veekogudes vedelas olekus. On ka teada, et vedelikel pole kindlat kuju. Nad (praegusel juhul vesi) omandavad sellise kuju, milline on neid ümbritsev anum. Vedelikud on liikuvad ja võivad voolata. Ainel on alati kindel ruumala. Talvel, kui vesi külmub tekib jää. Talvel aga tahkes olekus
Eksperimentaalne töö 1 Ainete kontsentratsiooni muutuse mõju tasakaalule Töö eesmärk: Le Chatelier' printsiip reaktsiooni tasakaalu nihkumise uurimine lähteainete ja saaduste kontsentratsiooni muutmisel. Kasutatavad ained: FeCl ja NH SCN küllastatud lahused, tahke NH Cl. 3 4 4 Töövahendid: Katseklaaside komplekt. Töö käik: Kirjutada välja tasakaalukonstandi avaldis raud(III)kloriidi ja ammooniumtiotsüanaadi lahuste vahelisele reaktsioonile FeCl3 3 NH 4 SCN Fe( SCN ) 3 3 NH 4 Cl Kc C c * D d A a * B b Kc C Fe( SCN )3 * C NH 4Cl 3 C FeCl3 * C NH4 SCN 3
reageeri ka hapete ning leeliste lahjendatud lahustega. Tähtsaim mineraal on boksiit - settekivim, mis koosnebki alumiiniumoksiidist. Enamtuntud aine looduses on korund, peeneteraline korund e smirgel on kasutusel lihvimispulbrite ja puhastuspastade koostises. Suured korundikristallid on hinnalised vääriskivid. Punaseid korunde nimetatakse rubiinideks, siniseid ja kollaseid safiirideks (kasutatakse laserites). b) Al(OH)3 alumiiniumhüdroksiid Samuti valge ja tahke aine, mis vees ei lahustu. Polümeerne, keeruka struktuuri ning muutuva koostisega aine, mille koostist väljendab tinglik valem Al2O3 x nH2O. Väga nõrk alus, amfoteerne hüdroksiid. Reageerib kergesti hapete ja leelistega. Lisaks on tänapäeval alumiinium mitmete vaktsiinide koostises alumiiniumhüdroksiidi kujul, samuti leidub Al(OH)3 ka ravimites. Ei leidu looduses, kuna tekib alumiiniumi töötlemisel kõrvalsaadusena. c) PbO2 plii(IV)oksiid
Füüsika viimane kontrolltöö TEOORIA OSA Agregaatolekud – aine tahke, vedel ja gaasiline olek. Ülekandenähtused – difusioon, soojusjuhtivus ja sisehõõre. Kolm nähtust, mis on sisuliselt omavahel seotud molekulide kaootilise liikumisega ja molekulidevahelise vastasikmõjuga. Difusioon – Nähtus, mille sisuks on erinevate ainete segunemine soojusliikumise tagajärjel. Soojusjuhtivus – Nähtus, mille sisuks on temperatuuri (siseenergia) ühtlustamine mingi keha ulatuses soojusliikumise tagajärjel.
Keemia TK Aine lahustuvus 1. Setitamine ja nõrutamine Vedeliku eraldamine tahkest, mittelahustuvast ainest. Tahke aine eraldamiseks vedelikust tuleb seega last tal kõigepealt settida (setitamine). Seejärel valatakse ettevaatlikult sademe peale ära (nõrutamine). 2. Filtrimine peeneteraliste hõljuva tahke aine eraldamiseks vedelikust. On vaja filterpaberit, kolbi, lehtrit, klaaspulka, keeduklaasi. Filterpaberiks on vaja tavalist poorset paberit. See asetatakse lehtrisse. Puhastatav vedelik valatakse ettevaatlikult filtrile. Vee väikesed molekulid pääsevad läbi poorse paberi, tahke aine osakesed aga mitte. Selle tulemusena saadud puhta vedeliku nimetatakse filtraadiks. 3. Eraldamine jaotuslehtriga Mittesegunevate ainete (nt vesi ja õli) eraldamiseks
Kuidas suurendada pindpinevust?- madalama temperatuuriga Suhteline õhuniiskus- absol õhuniiskuse ja küllastumata õhuniiskuse suhe kindal temp Absoluutne õhuniiskus- ühes kuupm sisaldav õhumass Kuidas töötab psühromeeter?- koosneb kahest termomeetrist: kuiv ja niiske. Ühte hoitakse kogu aeg niiskena. Kui õhuniiskus on 100% siis vesi märjalt lapilt ei aurustu, kui suhteline õhuni on väiksem siis hakkab märjalt termom vett aurustuma. Tahke ja vedeliku 5 erinevust- ● tahke molekulid on tihedalt seotud ● vedeliku aineosakesed on suvaliselt, ● vedeliku aineo võnkuvad ja põrkuvad, ● vedelik on voolav, ● tahket keha on raske kokku suruda ja teda ei saa laiali valada. ● tahke säilitab oma kuju Tahke ja gaasilise 5 erinevust- ● gaasilise aineo lendlevad, ● ruumala muutub vastavalt anumale, ● Vedeliku ja gaasilise 5 sarnasus- ● mõlema aineo on suvaliselt, ● difusioon, ● voolavad,
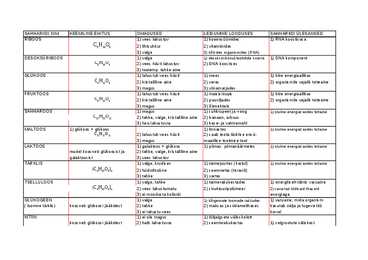
3) valge 3) kõikides organismides (RNA) DESOKSÜRIBOOS 1) valge 1) desoksüribonukleotiidide koostis 1) DNA komponent C5H10O4 2) vees hästi lahustuv 2) DNA koostises 3) toatemp. tahke aine GLÜKOOS 1) lahustub vees hästi 1) mees 1) kiire energiaallikas C6H12O6 2) kristalliline aine 2) veres 2) organismile vajalik toiteaine 3) magus 3) viinamarjades
Sfäär Ulatus Tihedu Keskmine Aineole Keemiline Tähtsus s temperatuur k koostis (kg/m3) (levinumad ained) Sisetuum 5100 12,85 5005°C Tahke Raud ja Magnetväli 6378 km kg/m3 nikkel Maapõue soojus sügavusel Välistuum 2890 km 4400°C Vedelik Magneesium sügavusel kuni , 6100°C hapnik Vahevöö 2900 km Tahke sügavusel
RASVAD Rasvad on glütseriini ehk propaantriooli ja kõrgemate karboksüülhapete(rasvhapete) estrid, mille olek toatemperatuuril on tahke. Kõrgemate karboksüülhapete estrid, mille olek toatemperatuuril on vedel, on õlid. Rasvad on ühed energiarikkamad toitained. 1 gramm rasva annab energiat ca 9 kcal, 1 gramm süsivesikuid 4 kcal ja 1 gramm valku samuti 4 kcal. Rasv on hädavajalik vitamiinide A, D, E ja K imendumiseks ning hormoonide normaalseks sünteesiks. Taimsed rasvhapped on toatemperatuuril vedelad ning asendamatud. Loomsed rasvhapped on toatemperatuuril tahked ning asendatavad. Loomseid
Keemia konspekt I Pihustatud aine + pihustamise keskkond = pihussüsteem gaas, vedelik, tahke gaas, vedelik, tahke PEENPIHUSED tõeline lahus- ei ole nähtav 10-7 cm = molekulid, ioonid kolloidlahus e. kolloidid- nähtav ultramikroskoobiga 10-5 cm = molekulide, ioonide kogum JÄMEPIHUSED suspensioon, emulsioon aerosool, vaht- nähtav palja silmaga 10-3 cm = veel suuremad kogumid Suspensioon: PIHUSTATUD LAHUSTAMATU tahke aine vedelikus. Kriit vees. Emulsioon: vedelik vedelikus. Õli vees. Aerosool: 1) tahke aine gaasis. Suits. 2) vedelik gaasis. Udu. Vaht: 1) gaas vedelikus. 2) gaas tahkes. Tõelise lahuse omadused- läbipaistev, ei kihustu, kiirte käik pole näha. Kolloidid- läbipaistev, kihustub natuke, kiirte käik on näha. Jämepihused- hägune, kihustumine, sadestumine, kiirte käik on näha.
Sulamissoojus -soojushulk, mis sulatab 1kg kristalset ainet sulamistemperatuurini(mis määratakse normaalrõhul). Aurustumissoojus L-soojushulk, mis aurustub 1kg vedeliku, määratakse tavaliselt keemistemp juures(keemistemp määratakse normaalrõhul). Faas ja faasisiired: termodünaamiliseks faasiks nim. kindlate omadustega ainet, mida ümbritsevad teiste omadustega ained. Vesi, õhk, jää-3 erinevat faasi. Faasisiireded: I liiki-agregaatoleku muutused:tahke-vedel-sulamine; vedel-tahke-tahkumine; vedel- gaas-aurustumine; gaas-vedel-kondenseerumine; gaas-tahke-härmatumine; tahke- gaas-sublimatsioon. II liiki: muud oleku muutused. Fe magnetiliste omadustega | t>7770C, mitte magnetiline. Termodünaamika printsiibid: 1) U= ± Q ± A (siseenergia muutus, soojushulk, mehaaniline töö). Keha siseenergia võib muutuda saadud või ära antud soojushulga tagajärjel ning mehaanilise töö tõttu. Kui tööd teevad välisjõud, siis U väheneb
siseenergiat) tööks. I printsiip energia jäävuse seadus. II printsiip protsesside iseeneslikul kulgemisel looduses on kindel suund. Siseenergia keha molekulide kineetilise ja potensiaalse eneria summa. Siseeneriat saab muuta 1)talle soojushulka andes(kuumutamine) 2)mehaanilist tööd tehes(hõõrdumine). Q (juurde antav soojushulk) = delta U (siseeneria muut) + A (välisjõudude vastu tehtud töö). Soojusmasinates kasutatakse gaase sest 1) paisuvad paremini 2) tahke ja vedela aine suur rõhk paisumisel võib masinat kahjustada 3)gaasil on soojushulga üleandmine kergem. Soojusmasina kasuteguriks nim suhet, mis näitab kui palju juurdeantavast soojushulgast on suudetud tsüklis muuta kasulikuks tööks.(=Akas /Q1) Entroopia suurus energia kvaliteedi hindamiseks. Mida kõrgem on kvaliteet, seda madalam on entroopia. Termodünaamika soojusnähtuste ajalooline ja väga oluline makrokäsitlus. Soojusmasin masin, mis muundab soojust (ja ka keha
nim pindpinevus teguriks s=F/l Kuna vedeliku pinnakihis on molekulid erilises olekus, siis on neil seal lisaenergia võrreldes molekulidega vedeliku sees http://www.abiks.pri.ee Vedeliku pinnakihi suurendamiseks näiteks seebimulli puhumisel tuleb teha tööd Vedeliku pinnaosa lisaenergia ja selle pindala suhe on võrde pindpinevusteguriga s=..U/..S MÄRGAMINE ja KAPILLAARSUS Vedeliku ja tahke keha piirpinnal esineb märgamis nähtus. Märgamine tekib vedeliku ja tahke keha molekulide vastastikmõjul ja põhjustab vedeliku pinna kõverdumise tahke keha lähedal Tahke kehaga piirneva vedeliku kuju sõltub sellest, kummad jõud, kas vedeliku ja tahke keha või vedeliku molkulide vahelised on suuremad Kapillaarsuse all mõistetakse vedeliku tõusmist või langemist peentes torudeskapillaarides
· Elektronvalem: 1s2 2s2p6 3s2p6 4s1 · Elektronskeem: +19|2)8)8)1) · Elektronite arv: 19 · Neutronite arv: 20 · Prootonite arv: 19 · Oksüdatsiooniast(m)e(d) ühendites: 0, I · Kristalli struktuur: ruumikeskne kuubiline Füüsikalised omadused: · Aatommass: 39,098 · Sulamistemperatuur: 63,25 °C · Keemistemperatuur: 759,9 °C · Tihedus: 0,862 g/cm3 · Värvus: hõbevalge · Agregaatolek toatemperatuuril: tahke · Kõvadus Mohsi järgi: 0,4 · Isotoobid: Nukliid Levimus (%) Mass Poolestusaeg 39 K 93,22 38,9637 - 40 K 0,118 39,974 1,28 · 109 aastat 41 K 6,77 40,9618 - 42 K 0 41,963 12,36 tundi 43
Väävel S 1,2 2,1 Kloor Cl 0,1 0,9 Lämmastik N 0,2 0,5 Hapnik O 9 - 12 Tabel 2. Kukersidi orgaaniline aine Eestis kaevandatava põlevkivi keskmine kütteväärtus on 8,4 9 MJ/kg (2300 2500 MWh/t) Käesoleval ajal kasutatakse põlevkiviõli tootmisel Eestis kahte meetodit (joonis 1.): gaasilise soojuskandja (GSKm) ja tahke soojuskandja (TSKm) meetodit. Nende meetodite põhiline erinevus seisneb erinevate tehnoloogiate kasutamises, näiteks reaktorite konstruktsioonis. GSKm kasutab ,,Kiviter" gaasigeneraatori püst-retort-tüüpi reaktorit ja TSKm ,,Galoter" õligeneraatori pöörlev-retort-tüüpi reaktorit. 2 Joonis 1. Eesti põlevkiviõli tootmiseks kasutatav tehnika Galoteri protsessi lühiajaloo