Materjaliteaduse instituut TTÜ Füüsikalise keemia õppetool Töö 19 Töö pealkiri KONTSENTRATSIOONIELEMENDI UURIMINE nr (FK) Üliõpilane MIHKEL HEINMAA Õpperühm YAGB41 Töö teostatud 04/04/2011 Arvestatud TÖÖ ÜLESANNE Töös valmistatakse kontsentratsioonielement, mille üks elektrood on asetatud vähelahustuva soola (AgCl, AgBr, AgI jt.) küllastatud lahusesse. Mõõdetakse elemendi elektromotoorjõud ja selle põhjal arvutatakse vähelahustuva soola lahustuvuskorrutis. Näiteks AgCl lahustuvuskorrutise määramiseks valmistatakse element Ag /AgCl / KCl // KNO3 // AgNO3 / Ag. küllast a1 aCl- a2 mille elektromotoorjõud kus + a2 on Ag -ioonide aktiivsus positiivse elektroodi juures,
1. Taimeõli biokeemiline koostis Biokeemiliselt on lipiidid vesilahustumatud, vähemalt kahest komponendist (alkohol, rasvhape) koosnevad biomolekulid (U.Kokassaar,T.Vihalemm,M.Zilmer, 1995) Lipiidid koosnevad triglütseriididest, mille igaühe keskseks osaks on glütserool, mis on seotud kolme rasvhappega. Eelnevat käsitsust järgides on oluline rasvhapete jaotus: keemilise olemuse põhjal räägitakse küllastatud ja mono- ja polüküllastamata rasvhapetest, mis on organismis vajalikud keha koostises leiduvate lipiidide ehituskomponentidena. Samuti esineb mõlemat tüüpi rasvhappeid veres vabas vormis Kirjanduses võib kohata sageli mõisteid küllastatud/küllastamata lipiidid. Vastav termin näitab, millised rasvhapped antud lipiidis domineerivad. Kehtib reegel: taimsetes lipiidides on ülekaalus küllastamata rasvhapped need ühendid on
füüsikalise keemia õppetool Töö nr. Töö pealkiri: PUHTA VEDELIKU KÜLLASTATUD AURURÕHU 6F MÄÄRAMINE DÜNAAMILISEL MEETODIL Üliõpilase nimi ja eesnimi Õpperühm: : Töö teostamise Kontrollitud: Arvestatud: kuupäev: JOONIS Seade vedeliku küllastatud aururõhu määramiseks Tööülesanne Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõõtmisel erinevate rõhkude juures. Vedelik keeb temperatuuril, mil küllastatud aururõhk on võrdne välisrõhuga. Ülesandeks ongi erinevate rõhkude juures keemistemperatuuride mõõtmine, et saaks teada küllastatud aururõhu temperatuuriolenevuse. Sellest tulenevalt same Clapeyroni- Clausiuse võrrandi abil arvutada vedeliku auramissoojuse. Töö käik
15.02.2012 Töö ülesanne Lahuse pH potentsiomeetrilisel määramisel määratakse galvaanielemendi elektromotoorjõud. Element koosneb uuritavasse lahusesse sukeldatud vesinik- või kinhüdroonelektroodist ja võrdluselektroodina hõbe-hõbekloriidelektroodist. Töö käik 1. Uuritavale lahusele lisasin väikese koguse kinhüdrooni (nii, et lahus oli küllastatud). 2. Asetasin lahusesse platineerimata plaatinaelektroodi. 3. Ühendasin elektroodinõu hõbe-hõbekloriidelektroodiga. 4. Mõõtsin elemendi elektromotoorjõu. Valemid Küllastatud hõbe-hõbekloriidelektroodi potentsiaal katsetemperatuuril: Kinhüdroonielektroodi normaalpotentsiaal katsetemperatuuril: Lahuse pH: Kinhüdroonelektroodil toimub reaktsioon: Sellele vastav potentsiaal:
TTÜ keemiainstituut KYF0030 - Füüsikaline keemia - praktikum Laboratoorne töö nr: Töö pealkiri: KONTSENTRATSIOONIELEMENDI UURIMINE 19 Õpperühm: Töö teostaja: Õppejõud: Kalju Lott 12.10.2010 Töö ülesanne. Töös valmistatakse kontsentratsioonielement, mille üks elektrood on asetatud vähelahustuva soola (AgCl, AgBr, AgI jt.) küllastatud lahusesse. Mõõdetakse elemendi elektromotoorjõud ja selle põhjal arvutatakse vähelahustuva soola lahustuvuskorrutis. Näiteks AgCl lahustuvuskorrutise määramiseks valmistatakse element Ag /AgCl / KCl // KNO3 // AgNO3 / Ag. küllast al aCl- a2 mille elektromotoorjõud RT a2 E= ln F a1 kus
kõrgemal) ning oli suurem, kui standardi plekk. Jätkasime GC analüüsiga kandsime metüleerunud proovi proovipudeli mikrosisusse, sulgesime tuubi ning panime proovipudeli GC aparaati. 8. GC analüüsi tulemused ja tulemuste analüüs GC analüüsil tuvastasime proovist 19 rasvhapet. Suurtes kogustes leidus proovis müristüülhapet (5%), palmithapet (26%), palmitolehapet (10%), olehapet (19%), linoolhapet (6%), eikosapentaeenhapet (6%) ja dokosaheksaeenhapet (6%). Küllastatud rasvhappeid oli 35,9%, monoküllastamata rasvhappeid oli 31,0% ja polüküllastatud rasvhappeid oli 26,7%. Ülejäänud osas oli piike, mille järgi polnud võimalik rasvhapet tuvastada. 3 rasvhappeid oli 19,7% ja 6 7,0%. Kirjanduse andmetel on keskmiselt küllastatud rasvhappeid 28%, monoküllastamata 47% ja polüküllastamata 24%. Nendest 3 happeid 19,7% ja 6 happeid 3%. Müristüülhapet leidub 4%, palmithapet 19%, palmitole hapet 5%, olehapet 20%, linoolhapet 1%, eikosapentaeenhapet
Killustiku terade tiheduse määramiseks tuleb katsenõu täita veega mingi kindla nivooni. Esmalt kaalutakse katsenõu mass koos katseproovi ja veega, seejärel katsenõu mass koos veega ning lõpuks kaalutakse pindkuiv katseproov. Seejärel arvutatakse valemi 2 järgi killustiku terade tihedus. m OK = m - (m4 -m ) (Valem 2) 4 2 3 m2 küllastatud täitematerjali ja veega täidetud katsenõu mass [g] m3 veega täidetud katsenõu mass [g] m4 kuiva täitematerjali mass õhus [g] Terade tihedus väljakuivanud olekus: m OK, kuiv = m - (m4 -m ) (Valem 3) 1 2 3 m1 küllastatud pindkuiva täitematerjali mass õhus [g]
Üliõpilase nimi: Franz Mathias Ints Töö nr: FK6 Töö pealkiri: Konsentratsioonielemendi Uurimine Siia tuleb sisestada aparatuuri joonis. keskkonnatehnoloogia Instituut 280 Füüsikaline keemia Õpperühm: EANB31 Töö teostamise kuupäev: 23.09.2020 nsentratsioonielemendi Uurimine Töö eesmärk (või töö ülesanne). Töö ülesanne. Töös valmistatakse kontsentratsioonielement, mille üks elektroo soola (AgCl, AgBr, AgI jt.) küllastatud lahusesse. Mõõdetakse elemendi elektrom arvutatakse vähelahustuva soola lahustuvuskorrutis. Näiteks AgCl lahustuvusk valmistatakse element Ag /AgI / KCl // KNO3 // AgNO3 / Ag Töövahendid. Uuritav galvaanielement, voltmeeter Töö käik. Vastavalt praktikumi juhendaja korraldusele valmistatakse kontsentratsiooniele valmistamiseks valatakse ühte elektroodinõudest ettenähtud kontsentratsioon nõutava kontsentratsiooniga KCl (või KBr, KI jne.) lahus, mida järgnevalt küllast
IV Veeaur õhus 1. Õhu relatiivne niiskus on 25 oC ja õhurõhu 97,2 kPa juures 65%. Kui palju tekib kondensaati õhu temperatuuri alandades 3 oC ja rõhu tõustes 104,5kPa? Andmed tabelist: P küllastatud veeaur = 23,76mmHg (25 oC juures) P küllastatud veeaur = 5,69mmHg (3 oC juures) Lahendus: Pvee aur 25oC juures= 23,76mmHg*0,65 = 15,44mmHg. Põhk = (97,2kPa*760mmHg)/101,3kPa = 729mmHg. Veeauru osarõhu suhe üldrõhku on võrdne veeauru mahuga 100 mahuühikus õhus: Vveeaur 25oC juures = (PH2O*100)/Püld = (15,44mmHg*100)/729mmHg = 2,11% Teiste sõnadega 25 oC juures, 100L õhus on 2,11L veeauru või 21,1L veeauru 1m3 (1000L) õhu kohta. Arvutame vee auru ruumala normaaltingimustel: Kus P0=760mmHg, V0=?, T0=273K.
Füüsikalise keemia õppetool Töö nr. 6 PUHTA VEDELIKU KÜLLASTATUD AURURÕHU MÄÄRAMINE DÜNAAMILISEL MEETODIL Üliõpilane Kristin Obermann Kood 123482KAKB Töö teostatud 07.03.2014 Töö ülesanne. Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõõtmisel erinevate rõhkude juures. Teatavasti keeb vedelik temperatuuril, mille juures tema küllastatud aururõhk on võrdne välisrõhuga. Keemistemperatuuride mõõtmine erinevatel rõhkudel annab küllastatud aururõhu temperatuuriolenevuse. Viimasest saab Clapeyroni- Clausiuse võrrandi abil arvutada vedeliku aurustumissoojuse. Aparatuur (vt joonis) koosneb elektriküttega kolvist 1 ning ebulliomeetrist 2, milles on pesa 3 termomeetri jaoks. Termomeetri tasku on täidetud alumiiniumpulbri suspensiooniga õlis, millel on hea soojusjuhtivus. Kolb 1 on ühendatud vaakumsüsteemiga jahuti 5 kaudu
TTÜ materjaliteaduse instituut Füüsikalise keemia õppetool KYF0080 Füüsikaline ja kolloidkeemia Laboratoorne Töö pealkiri: töö nr: 6 Puhta vedeliku küllastatud aururõhu määramine dünaamilisel meetodil Töö teostaja: Õpperühm: Õppejõud: Töö teostatud: Protokoll esitatud: Protokoll K. Lott 28.02.2011 13.03.2011 arvestatud: 14.03.2011 Skeem: Töö ülesanne Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõõtmisel
FÜÜSIKALISE KEEMIA ÕPPETOOL Üliõpilane: Teostatud: Õpperühm: Kontrollitud: Töö nr : 6 Kaitstud: PUHTA VEDELIKU KÜLLASTATUD AURURÕHU MÄÄRAMINE DÜNAAMILISEL MEETODIL SKEEM Tööülesanne: Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõõtmisel erinevate rõhkude juures. Teatavasti keeb vedelik temperatuuril, mil küllastatud aururõhk on võrdne välisrõhuga. Keemistemperatuuride mõõtmine erinevatel rõhkudel annab küllastatud aururõhu temperatuuriolenevuse. Viimasest saab Clapeyroni-Clausiuse võrrandi abil arvutada vedeliku auramissoojuse. Töö käik: Uuritav vedelik valatakse kuiva kolbi ning ühendatakse lihvi abil aparatuuri külge. Selle hermeetilisus kontrollitakse. Lülitatakse sisse kolvi küte nii, et vedelik hakkaks keema u 10 min jooksul. Märgitakse keemistemperatuur saavutatud rõhul
Kasutatavad ained 10%-ne soolhappelahus, 5,0-10,0 mg metallitük(magneesium) Töövahendid Seade gaasi mahu mõõtmiseks, mõõtesilinder (25cm³), lehter, filterpaber, termomeeter, baromeeter, hügomeeter Katse arvutused Katsetulemused: Vee nivoo büretti enne reaktsioon - V = 13,7mL = 13,7 cm³ Vee nivoo peale reaktsiooni - V = 7,6mL = 7,6 cm³ Eraldunud vesiniku mat - V = V - V = 6,1cm³ Õhurõhk P=101000Pa Temperatuur - t°=21+273=294K Küllastatud veeauru rõhk temperatuuril t° - P(ho)=18,7mmHg (tabelist) Õhu relatiivne niiskus RH=55% 1) Arvutada reaktsioonil eraldunud vesiniku maht normaaltingimustel. Küllastatud veeauru rõhk PH2O tuleb valida tabelist 1. Tabel 1. Küllastatud veeauru rõhud erinevatel temperatuuridel t, P H2 O t, P H2 O t, PH 2 C ,mmHg C ,mmHg C O ,mmHg -10 2,05 17 14,5 24 22,4
Loomne rasv (searasv) Searasva kasutame põhiliselt toidu tegemiseks .Normaalolekus on see tahke ja kuna see on stabiilne, siis on see eelistatuim rasv praadimiseks. Ta on hea D vitamiini allikas ja peale selle sisaldab see veel ka 40% küllastatud rasva, 48% monoküllastamata rasva ning umbes 12% polüküllastamata rasva, mis muidugi sõltub ka loomade toitumisest. Näiteks troopikas on searasv ka hea lauriinhappe allikas (sellel on immuunsust tõstev toime), sest sigu toidetakse seal kookospähklitega. Selle tervislikkusest on erinevaid arvamusi osad usuvad, et sealiha rohke tarbimine on seotud vähiriskiga, enamik aga ei seosta riski seapekist saadud rasvaga seda peetakse ikkagi tervislikuks(mõõdukas koguses) ja ohutuks.
TTÜ Materjaliteaduse Instituut Füüsikalise keemia õppetool Töö nr. 6 PUHTA VEDELIKU KÜLLASTATUD AURURÕHU MÄÄRAMINE DÜNAAMILISEL MEETODIL Üliõpliane: Kood: Töö teostatud: Töö ülesanne. Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõõtmisel erinevate rõhkude juures. Teatavasti keeb vedelik temperatuuril, mil küllastatud aururõhk on võrdne välisrõhuga. Keemistemperatuuride mõõtmine erinevatel rõhkudel annab küllastatud aururõhu temperatuuriolenevuse. Viimasest saab Clapeyroni-Clausiuse võrrandi abil arvutada vedeliku auramissoojuse. Aparatuur (joon. 8) koosneb elektriküttega kolvist 1 ning ebulliomeetrist 2, milles on pesa 3 termomeetri jaoks. Termomeetri tasku on täidetud alumiiniumpulbri suspensiooniga õlis, millel on hea soojusjuhtivus. Kolb 1 on ühendatud vaakumsüsteemiga jahuti 5 kaudu
TTÜ Materjaliteaduse instituut füüsikalise keemia õppetool Töö nr 6. Töö pealkiri: Puhta vedeliku küllastatud aururõhu määramine dünaamilisel meetodil Üliõpilase nimi ja Õpperühm eesnimi : Töö teostamise Kontrollitud: Arvestatud: kuupäev: Töö ülesanne. Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõõtmisel erinevate rõhkude juures. Teatavasti keeb vedelik temperatuuril, mille juures tema küllastatud aururõhk on võrdne välisrõhuga
õppejõu allkiri FK laboratoorne töö 6 PUHTA VEDELIKU KÜLLASTATUD AURURÕHU MÄÄRAMINE DÜNAAMILISEL MEETODIL Töö ülesanne. Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõõtmisel erinevate rõhkude juures. Teatavasti keeb vedelik temperatuuril, mille juurestema küllastatud aururõhk on võrdne välisrõhuga. Keemistemperatuuride mõõtmine erinevatel rõhkudel annab küllastatud aururõhu temperatuuriolenevuse. Viimasest saab Clapeyroni-Clausiuse võrrandi abil arvutada vedeliku aurustumissoojuse. Aparatuur (vt joonis) koosneb elektriküttega kolvist 1 ning ebulliomeetrist 2, milles on pesa 3 termomeetri jaoks. Termomeetri tasku on täidetud alumiiniumpulbri suspensiooniga õlis, millel on hea soojusjuhtivus. Kolb 1 on ühendatud vaakumsüsteemiga jahuti 5 kaudu
Töö nr 6 PUHTA VEDELIKU KÜLLASTATUD AURURÕHU MÄÄRAMINE DÜNAAMILISEL MEETODIL Töö teostamise Kontrollitud: Arvestatud: kuupäev: 19.02.14 Töö ülesanne. Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõõtmisel erinevate rõhkude juures. Teatavasti keeb vedelik temperatuuril, mil küllastatud aururõhk on võrdne välisrõhuga. Keemistemperatuuride mõõtmine erinevatel rõhkudel annab küllastatud aururõhu temperatuuriolenevuse. Viimasest saab Clapeyroni-Clausiuse võrrandi abil arvutada vedeliku auramissoojuse. Töö käik. Katseseadeldis oli juba kokku pandud. Vaakumpumba abil luuakse seadmes hõrendus. Suletakse kraan 10. Kolvi küte lülitatakse sisse mille intensiivsust reguleeritakse tilgaloenduri järgi
hüdrofiilne karboksüülrühm · vabu rasvhappeid ehk esterifitseerimata rasvhappeid esineb inimorganismis lipiidide metabolismi (ainevahetuse) vaheühenditena ja vereplasmas teatud transportvormidena · vabu rasvhappeid kannab veres põhiliselt albumiin · oksüdeerudes kudedes (maksas, südamelihases, skeletilihastes jt) annavad nad rohkesti energiat Inimorganismi lipiidid sisaldavad nii küllastatud kui ka küllastamata rasvhappeid. Inimorganismi normaalne funktsioneerimine vajab nii küllastatud kui ka küllastamata rasvhappeid. Kas rasvhape on küllastatud või küllastamata sõltub temas sisalduvast kaksiksidemest: küllastatud rasvahapetes ei ole kaksiksidet. Küllastatud rasvhapped on toatemperatuuril tahked ained, kui C-aatomite arv on > 10 palmitiinhape (palmithape) steariinhape (stearhape)
TTÜ Materjaliteaduse instituut füüsikalise keemia õppetool Töö nr 6 Töö pealkiri Puhta vedeliku küllastatud aururõhu määramine dünaamilisel meetodil Üliõpilase nimi ja Õpperühm eesnimi Töö teostamise Kontrollitud: Arvestatud: kuupäev: 23.03.2011 TÖÖÜLESANNE Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõõtmisel erinevate rõhkude juures. Teatavasti keeb vedelik temperatuuril, mil küllastatud aururõhk on võrdne välisrõhuga
TTÜ Materjaliteaduse instituut füüsikalise keemia õppetool Töö nr: 6f Töö pealkiri: Puhta vedeliku küllastatud aururõhu määramine dünaamilisel meetodil Üliõpilase nimi ja eesnimi: Õpperühm: Töö teostamise Kontrollitud: Arvestatud: kuupäev: 27.02.2012 Seade küllastunud aururõhu määramiseks Töö ülesanne: Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõõtmisel erinevate rõhkude juures. Teatavasti keeb vedelik temperatuuril, mil küllastatud
Kodused ülesanded: 1. Õhu relatiivne niiskus 20 oC juures on 90%. Kui palju tekib õhu jahtumisel 5 oC-ni kondensaati? Lahendus: Andmed tabelist: P küllastatud veeaur = 17,54mmHg (20 oC juures) P küllastatud veeaur = 6,54mmHg (5 oC juures) Pvee aur 20oC juures= 17,54mmHg*0,90 = 15,8mmHg. Veeauru osarõhu suhe üldrõhku on võrdne veeauru mahuga 100 mahuühikus õhus: Vveeaur 20oC juures = (PH2O*100)/Püld = (15,8mmHg*100)/760mmHg = 2,08% Teiste sõnadega 20 oC juures, 100L õhus on 2,08L veeauru või 20,8L veeauru 1m3 (1000L) õhu kohta. Arvutame vee auru ruumala normaaltingimustel: Kus P0=760mmHg, V0=?, T0=273K. P1=760mmHg, V1=20,8L/1m3, T1=(20+273)=293K
Lahuse pH potentsiomeetrilisel määramisel määratakse galvaanielemendi elektromotoorjõud. Element koosneb uuritavasse lahusesse sukeldatud kinhüdroonelektroodist ja võrdluselektroodina hõbe-hõbekloriidelektroodist. Aparatuur Kinhüdroon- ja hõbe-hõbekloriidelektroodist koosnev galvaanielement. Numbrilise näiduga voltmeeter. Katse käik Uuritava lahuse pH määratakse hõbe-hõbekloroodelektroodi abil. Lahusele lisatakse väike kogus kinhüdrooni (kuid nii, et lahus oleks küllastatud - sademe tekkeni), asetatakse lahusesse platineerimata plaatinaelektrood, ühendatakse elektroodinõu hõbe-hõbekloriidelektroodiga ning mõõdetakse elemendi elektromotoorjõud. Lahuse pH saab arvutada, lähtudes elemendi emj. ja indikaatorelektroodi potentsiaali avaldisest. Mõõtmine kinhüdroonelektroodiga: kinhüdroon hõbe-hõbekloriidelement elektromotoorjõud E = 0,250 V katsetemperatuur t = 25 °C; küllastatud hõbe-hõbekloriidelektroodi potentsiaal katsetemperatuuril
kuupäev: 26/02/2014 Töö ülesanne. Lahuse pH potentsiomeetrilisel määramisel määratakse galvaanielemendi elektromotoorjõud. Element koosneb uuritavasse lahusesse sukeldatud vesinik- või kinhüdroonelektroodist ja võrdluselektroodina hõbe-hõbekloriidelektroodist. Katse käik. Uuritava lahuse pH määratakse hõbe-hõbekloroodelektroodi abil. Lahusele lisatakse väike kogus kinhüdrooni (kuid nii, et lahus oleks küllastatud - sademe tekkeni), asetatakse lahusesse platineerimata plaatinaelektrood, ühendatakse elektroodinõu hõbe-hõbekloriidelektroodiga ning mõõdetakse elemendi elektromotoorjõud. Lahuse pH saab arvutada, lähtudes elemendi emj. ja indikaatorelektroodi potentsiaali avaldisest. Valemid kn= kn0+ loga2H+= kn0-0,059pH, millest pH= edasi tuleb võtta mõõdetud galvaanielemendi elektromotoorjõu avaldis: E= kn- Ag/AgCl, millest kn=E+ Ag/AgCl. Asendades selle ülaltoodud valemisse, saame pH
10 algupärast luuletust ja 36 tõlget ,,Eelõitseng" (1918) kõige varasemad värsid 1904-1913 1981 - MU SÜDA LAULAB. aimuste, puhkeva tundeelu ja õnneootuse luule ,,Sinine puri" ( 1912) jätkub tundelõõm, kuid nähtub rohkem elu vastaspoolsusi ja uute vaatealate võimalusi ,,Eluõitseng" ,,Õnn ei tule, nagu oodand ma ja lootnud, üle öö:/ ta on aastate hool ja valude töö" (,,Õnne ootel") · Luulemaailm: * minakeskne * küllastatud armastusest * küllastatud looduselamustest * muud motiivid sellesse ei pääse * tundesiirus
Kui rasvhappes esineb kordne süsinik-süsinik side siis on tegemist õliga. Rasvad kuuluvad ka põhitoitiainete hulka. Rasvu leidub peaagu igas rakus. Rasv on väga energiarikas toitaine. Rasvarikas toit on maitsev ja rahuldab ka väikestes kogustes kiiresti isu. Võrreldes valkude ning süsivesikutega annavad nad kaks korda rohkem energiat. Rasvad jagunevad loomseteks ja taimseteks rasvadeks. Rasvad sisaldavad kolme tüüpi (küllastatud, mono- ja polüküllastamata) rasvhappeid. Loomsetes rasvades on ülekaalus küllastatud rasvhapped, taimsetes õlides mono- ja polüküllastamata rasvhapped .Rasva leidub vähe puu- ja juurviljades, kõigest mõni protsent. Rasvarikkad toiduained on aga liha, või margariin , pähklid jms. Taimedes leidub rasva kõige enam seemnetes. Loomorganismis talletub rasv nahaaluses koes ning muudes organites. Toon mõned näited ,milline on rasva sisaldus ainetes 100 grammi kohta:
Kristallisatsoon ühest lahusest · Polümorfismide saamises on kasutusel erinevad kristallisatsioonid: a) aeglane solvendi aurustamine: küllastatud lahus filtreeritakse tuumakeste eraldamiseks ja lastakse teatud aja seista rahulikult. Aurustamise kiirust saab reguleerida, kattes anuma spetsiaalse materjaliga (alumiiniumfoolium, Parafilm®), milles on augukesed. b)aeglane küllastatud lahuse jahutamine c)kiire küllastatud lahuse jahutamine. · Aine lahustuvus toatemperatuuril peab olema 5-200 mg/ml. Kui lahustuvus on üle 200 mg/ml, saadakse liiga viskoosne, klaasjas lahus. (nt glütserool) · Lahusti valikul on määrav tegur lahusti keemistemperatuur, samuti dielektriline konstant ja polaarsus. · Tüüpilisemad lahustid on vesi, metanool, etanool, propanool, isopropanool, atsetoon, etüülatsetaat ja heksaan.
AURURÕHU MÄÄRAMINE DÜNAAMILISEL MEETODIL Üliõpilase nimi ja eesnimi: Õpperühm: KAOB-61 Töö teostamise Kontrollitud: Arvestatud: kuupäev: 12.03.2012 Töö ülesanne. Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõõtmisel erinevate rõhkude juures. Teatavasti keeb vedelik temperatuuril, mil küllastatud aururõhk on võrdne välisrõhuga. Keemistemperatuuride mõõtmine erinevatel rõhkudel annab küllastatud aururõhu temperatuuriolenevuse. Viimasest saab Clapeyroni-Clausiuse võrrandi abil arvutada vedeliku auramissoojuse. Aparatuur (joon. 8) koosneb elektriküttega kolvist 1 ning ebulliomeetrist 2, milles on pesa 3 termomeetri jaoks. Termomeetri tasku on täidetud alumiiniumpulbri suspensiooniga õlis, millel on hea soojusjuhtivus. Kolb 1 on ühendatud vaakumsüsteemiga jahuti 5 kaudu
Puhta vedeliku küllastatud aururõhu määramine dünaamilisel meetodi Töö ülesanne. Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride mõ Teatavasti keeb vedelik temperatuuril, mil küllastatud aururõhk on võrdne välisrõhuga. Keemistemp rõhkudel annab küllastatud aururõhu temperatuuriolenevuse. Viimasesr aab Clapeyroni-Clausiuse v Katse käik. Uuritav vedelik valatakse kolbi 1( täidetakse 3/4 kolvist), mis ühendatakse klaaslihvi a Seejärel kontrollitakse seadme hermeetilisust. Selleks avatakse kraan 10 ning vaakumpumba abil l selliselt, et jääkrõhk oleks 20-30 torri võrra suurem rõhust, mille all aine toatemperatuuril keeb. Su hermeetiliseks, kui 10-15 minuti jooksul rõhk seadmes ei kasva rohkem kui 1-2 mm Hg. Seejärel lü
Tasakaalu saavutamise järel (pärast õhu väljatõrjumist süsteemist ja plaatina pinna küllastumist vesinikuga, mis olenevalt süsteemi mahust võtab aega 15 - 20 minutit) mõõdetakse vesinik-kalomelelemendi elekromotoorjõud. Kontrollimiseks korratakse mõõtmisi veel paar korda 5-minutiste vaheaegadega, seejuures vesinikuvoolu katkestamata. Teise uuritava lahuse pH määratakse hõbe-hõbekloroodelektroodi abil. Lahusele lisatakse väike kogus kinhüdrooni (kuid nii, et lahus oleks küllastatud - sademe tekkeni), asetatakse lahusesse platineerimata plaatinaelektrood, ühendatakse elektroodinõu hõbe- hõbekloriidelektroodiga ning mõõdetakse elemendi elektromotoorjõud. Lahuse pH saab arvutada, lähtudes elemendi emj. ja indikaatorelektroodi potentsiaali avaldisest. Arvutused Mõõtmine kinhüdroonelektroodiga: kinhüdroon hõbe-hõbekloriidelement elektromotoorjõud E = 0,223 V; katsetemperatuur t = 25°C;
22. Kinhüdroon hõbe- hõbekloriidelement Töö ülesanne. Lahuse pH potentsiomeetrilisel määramisel määratakse galvaanielemendi elektromotoorjõud. Element koosneb uuritavasse lahusesse sukeldatud kinhüdroonelektroodist ja võrdluselektroodina hõbe-hõbekloriidelektroodist. Määrata lahuse pH kinhüdroonelektroodi abil. Katse käik. Uuritava lahuse pH määratakse hõbe-hõbekloroodelektroodi abil. Lahusele lisatakse väike kogus kinhüdrooni (kuid nii, et lahus oleks küllastatud - sademe tekkeni), asetatakse lahusesse platineerimata plaatinaelektrood, ühendatakse elektroodinõu hõbe-hõbekloriidelektroodiga ning mõõdetakse elemendi elektromotoorjõud. Lahuse pH saab arvutada, lähtudes elemendi emj. ja indikaatorelektroodi potentsiaali avaldisest. Valemid. Koostame elemendi: Hg Hg2Cl2, KCl C6H4O2, C6H4(OH)2, H+(Pt) küllast. pH=?emj E=0,229V E= Kinhüdroonelektroodil toiumub reaktsioon
22. Kinhüdroon hõbe- hõbekloriidelement Töö ülesanne. Lahuse pH potentsiomeetrilisel määramisel määratakse galvaanielemendi elektromotoorjõud. Element koosneb uuritavasse lahusesse sukeldatud kinhüdroonelektroodist ja võrdluselektroodina hõbe-hõbekloriidelektroodist. Määrata lahuse pH kinhüdroonelektroodi abil. Katse käik. Uuritava lahuse pH määratakse hõbe-hõbekloroodelektroodi abil. Lahusele lisatakse väike kogus kinhüdrooni (kuid nii, et lahus oleks küllastatud - sademe tekkeni), asetatakse lahusesse platineerimata plaatinaelektrood, ühendatakse elektroodinõu hõbe-hõbekloriidelektroodiga ning mõõdetakse elemendi elektromotoorjõud. Lahuse pH saab arvutada, lähtudes elemendi emj. ja indikaatorelektroodi potentsiaali avaldisest. Valemid. Koostame elemendi: Hg Hg2Cl2, KCl C6H4O2, C6H4(OH)2, H+(Pt) küllast. pH=?emj E=0,210V E= Kinhüdroonelektroodil toiumub reaktsioon
väldivad rasvaseid toite. See on põhjustanud isegi väga tõsiseid haigusi. Kuid mis asjad on tegelikult rasvad ja mis on nende ülesanne ja tähtsus igapäevaelus. Lipiidideks on rasvhapped, triglütseriidid, fosfolipiidid, glükolipiidid, steroolid (kolesterool). Lipiidid sisaldavad rasvlahustuvaid vitamiine. Terminit "rasvad" kasutatakse triglütseriidide kohta, mis koosnevad kolmest rasvhappemolekulist ning glütseroolist. Rasvad sisaldavad kolme tüüpi (küllastatud, mono- ja polüküllastamata) rasvhappeid. Loomsetes rasvades on ülekaalus küllastatud rasvhapped, taimsetes õlides mono- ja polüküllastamata rasvhapped. Rasvade põhiülesandeks on energia katmine ning säilitamine, nad on ka asendamatute polüküllastamata rasvhapete ja rasvlahustuvate vitamiinide allikas. Fosfatiidid kuuluvad kõikide kudede ja rakkude koostisesse, suuremal hulgal on neid närvikoes ja ajurakkudes.
MÜÜRSEPP, tase 4 TEST I 1. Silikaattellis on valmistatud. a. Kustutatud lubja ja kvartsliiva segust b. Liiva ja savi segust c. Liivast ja tsemendist 2. Keraamiliseks ehitusmaterjaliks nimetatakse: a. lubjast valmistatud ehitusmaterjale b. tsemendist valmistatud ehitusmaterjale c. savist valmistatud ehitusmaterjale 3. Materjali külmakindlus on: a. materjali omadus veega küllastatud olekus taluda paljukordset vahelduvat külmumist ja ülessulatamist vees b. materjali omadus loomulikus olekus taluda paljukordset vahelduvat külmumist ja ülessulatamist vees c. materjali omadus taluda miinuskraade 4. Materjali survetugevus (tugevus) näitab: a. materjalis olevat sideaine hulka b. materjali proovikeha purustamiseks vajalikku survepinget c
22. Kinhüdroon hõbe- hõbekloriidelement Töö ülesanne. Lahuse pH potentsiomeetrilisel määramisel määratakse galvaanielemendi elektromotoorjõud. Element koosneb uuritavasse lahusesse sukeldatud kinhüdroonelektroodist ja võrdluselektroodina hõbe-hõbekloriidelektroodist. Määrata lahuse pH kinhüdroonelektroodi abil. Katse käik. Uuritava lahuse pH määratakse hõbe-hõbekloroodelektroodi abil. Lahusele lisatakse väike kogus kinhüdrooni (kuid nii, et lahus oleks küllastatud - sademe tekkeni), asetatakse lahusesse platineerimata plaatinaelektrood, ühendatakse elektroodinõu hõbe-hõbekloriidelektroodiga ning mõõdetakse elemendi elektromotoorjõud. Lahuse pH saab arvutada, lähtudes elemendi emj. ja indikaatorelektroodi potentsiaali avaldisest. Valemid. Koostame elemendi: Hg Hg2Cl2, KCl C6H4O2, C6H4(OH)2, H+(Pt) küllast. pH=?emj E=0,037V E= Kinhüdroonelektroodil toiumub reaktsioon
kuupäev: 18.03.2015 Joonis. Kinhüdroon – hõbe-hõbekloriidelement Töö ülesanne: Lahuse pH potentsiomeetrilisel määramisel määratakse galvaanielemendi elektromotoorjõud. Element koosneb uuritavasse lahusesse sukeldatud kinhüdroonelektroodist ja võrdluselektroodina hõbe-hõbekloriidelektroodist. Töö käik: Uuritavale lahusele lisatakse väike kogus kinhüdrooni (kuid nii, et lahus oleks küllastatud - sademe tekkeni), asetatakse lahusesse platineerimata plaatinaelektrood, ühendatakse elektroodinõu hõbehõbekloriidelektroodiga ning mõõdetakse elemendi elektromotoorjõud. Lahuse pH saab arvutada, lähtudes elemendi emj. ja indikaatorelektroodi potentsiaali avaldisest. Valemid E - kinhüdroon–hõbe-hõbekloriidelemendi elektromotoorjõud t – katsetemperatuur φhõbe-hõbekloriid = 0,199 – 1,01 ·10-3 (t -25)
Eksperimentaalne töö 1 Ainete kontsentratsiooni muutuse mõju tasakaalule Töö eesmärk: Le Chatelier' printsiip reaktsiooni tasakaalu nihkumise uurimine lähteainete ja saaduste kontsentratsiooni muutmisel. Töövahendid: Katseklaaside komplekt. Kasutatud ained: FeCl3 ja NH4SCN küllastatud lahused, tahke NH4Cl. Töö käik: Kirjutada välja tasakaalukonstandi avaldis raud(III)kloriidi ja ammooniumtiotsüanaadi lahuste vahelisele reaktsioonile. FeCl3(aq)+3NH4SCN(aq) FE(SCN)3(aq)+3NH4Cl(aq) K 1 [ C ] c [ D ] d [ Fe( SCn) 3 ] [ NH 4 Cl ] 1 3 Kc = = =
Eksperimentaalne töö 1 Ainete kontsentratsiooni muutuse mõju tasakaalule Töö eesmärk: Le Chatelier' printsiip – reaktsiooni tasakaalu nihkumise uurimine lähteainete ja saaduste kontsentratsiooni muutmisel. Töövahendid: Katseklaaside komplekt. Kasutatud ained: FeCl3 ja NH4SCN küllastatud lahused, tahke NH4Cl. Töö käik: Kirjutada välja tasakaalukonstandi avaldis raud(III)kloriidi ja ammooniumtiotsüanaadi lahuste vahelisele reaktsioonile. FeCl3(aq)+3NH4SCN(aq)→ FE(SCN)3(aq)+3NH4Cl(aq) K 1 C c D d Fe( SCn) 3 NH 4 Cl 1 3 Kc
Menüüs võid kasutada ka konserveeritud ube, mis on tervislikud, kuna säilitavad kiudainete- ja flavonoididesisalduse ka sellisel viisil töödelduna. www.toitumisnoustaja.com Tervislikud toitumisharjumused Ene Mägi mob.5135660 Rasva on soovitav tarbida 4 -7 portsjonit iga päev, kusjuures üks portsjon küllastamata rasva on näiteks 1spl seemneid, 1tl head õli, 10 mandlit, 5 väiksemat oliivi. Küllastatud rasva üks portsjon on näiteks 1viil peekonit, 1tl võid, 1-2spl koort, 1tl majoneesi ja küllastatud rasva võib olla 1/3 päevasest rasvakogusest. Paljud haigused seostatakse liiga kõrge küllastatud rasvade sisaldusega toidus. Kui räägin tervislikust toitumisest, siis see tähendab, et enamus kaloritest pead saama taimsetest allikatest k.a. taimsed õlid. Heade rasvade allikaks on pähklid ja seemned. Et süüa tervislikult, pead jälgima nii rasva koostist kui kogust toidus
vetthülgavaks e hüdrofoobseks Küllastumata rasvhapped rasvhapped, milles esineb üks või mitu kaksiksidet On ülekaalus taimsetes rasvades, mis esinevad toatemperatuuril vedelas olekus ehk õlina oomega-3 ja oomega-6 rasvhapped. Arv märgib esimest kaksiksidet omavat süsiniku aatomit loetuna ahela otsmisest süsinikust Küllastunud rasvhapped kaksiksidemed puuduvad, sest süsiniku aatomid on vesinike aatomitega küllastatud Leidub eeskätt loomsetes rasvades, mis on toatemperatuuril tahked Normaalseks elutalitluseks vajab inimene nii küllastatud kui ka küllastamata rasvhappeid Inimorganismis hädavajalikud keha koostises leiduvate lipiidide ehituskomponentidena, esinevad samuti veres vabas vormis. Taimsetes lipiidides on ülekaalus küllastamata rasvhapped ja need ühendid on agregaatolekult vedelad - taimsed õlid. Mida rohkem on lipiidides küllastamata rasvhappeid, seda madalamal
termomeetri jaoks. Termomeetri tasku on täidetud alumiiniumpulbri suspensiooniga õlis, millel on hea soojusjuhtivus. Kolb 1 on ühendatud vaakumsüsteemiga jahuti 5 kaudu. Jahutis toimub aurude kondensatsioon, millega välditakse nende kondenseerumine ühendustorudes ja manomeetris 8. Süsteemis on kaks vahepudelit 7 ja 9, millest viimane on kraani 10 kaudu ühendatud Komovski vaakumpumbaga. Joonis. Seade vedeliku küllastatud aururõhu määramiseks Töö käik. Uuritav vedelik valatakse kuiva kolbi 1 (täidetakse 3/4 kolvist), mis ühendatakse klaaslihvi abil ülejäänud seadmega (üldjuhul on seade laborandi poolt juba koostatud). Seejärel kontrollitakse seadme hermeetilisust. Selleks avatakse kraan 10 ning vaakumpumba abil luuakse seadmes hõrendus – elavhõbedasammas tõstetakse veidi kõrgemale sellest, mille juurest mõõtmist vastavalt tööülesandele alustatakse (küsida juhendajalt)
Vastavalt keemilisele ehitusele: küllastunud ja küllastumata rasvhapeteks. Küllastunud: cis ja transrasvhapped Küllastumata rasvhapped: mono ja polüküllastamata rasvhapeteks. Osasid polüküllastumata rasvhappeid (nt oomega3 ehk linoleenhape ja oomega6 ehk linoolhape) nimetatakse asendamatuteks ehk essentsiaalseteks, sest neid ei suuda inimese organism ise sünteesida ja seega tuleb neid saada toiduga. leidumine Loomsetes rasvades on ülekaalus küllastatud rasvhapped, taimsetes õlides mono ja polüküllastamata rasvhapped. Lipiidid koosnevad vähemalt kahest komponendist: alkoholist ja rasvhappejäägist. Nt. fosfolipiidid esinevad rakumembraani koostises. Transrasvhappeid esineb looduslikult vähe, kuid nad võivad tekkida vedelate taimeõlide hüdrogeenimisel ehk tahkestamisel(nt. Margariini tegemine õlist) Näited Nimetus Valem Leidumine Kül Butaanhape (võihape) C3H7COOH Piimarasv;
Täisteratooted sisaldavad madala glükeemilise koormusega süsivesikuid. Saial, valgel riisil, kõikidel nisujahust (v.a. täisteranisujahust) küpsetistel ja pastatoodetel, keedukartulil, praekartulitel ja kartulipüreel on kõrge glükeemiline koormus. Neid toiduaineid soovitab ETA tarvitada piiratud koguses. Rasva on soovitatav tarbida 4-7 portsjonit päevas, kusjuures üks portsjon küllastamata rasva on näiteks 1 supilusikatäis seemneid või 1 teelusikatäis head õli, 10 mandlit. Küllastatud rasvad ei tohi ületada 1/3 päevasest rasvakogusest, 1 portsjon küllastatud rasvu on 1 viil peekonit, 1 teelusikatäis võid. Rasvade tarbimist ei tohi liigselt piirata, neid tuleb aga hoolikalt valida. Küllastamata ja küllastatud rasvhappeid tuleb tarbida õiges vahekorras. Meie toidus peaks olema oomega-3 ja oomega-6 rasvhapete suhe 1 : 2 (kokku võiksid moodustada 6-8 protsenti toiduenergiast). ETA soovitab tarbida häid küllastatud taimseid rasvu, nagu
(õhu) kogurõhk koosneb üksikkomponentide osarõhkude summast [10] n p = p1 + p2 + ... + pn = pi . (1.5) i =1 Niisket õhku võib vaadelda veeauru ja kuiva atmosfääriõhu seguna, mille moolmass µ = 29. Niiske õhu rõhk on veeauru ja kuiva õhu osarõhkude summa [10]. Kuiva õhu ja ülekuumutatud veeauru segu nimetatakse küllastamata niiskeks õhuks, aga kuiva õhu ja küllastatud veeauru segu nimetatakse küllastatud niiskeks õhuks. Õhu niiskusesisaldust (tehniline niiskus) väljendatakse veeauru massina kuiva õhu massiühiku kohta: mva d= , (1.6) mkõ kus mva on veeauru mass, g, mkõ kuiva õhu mass, kg. Niiskusesisalduse võib väljendada ka õhu ühe mahuühiku kohta, siis nimetatakse seda absoluutseks niiskuseks e
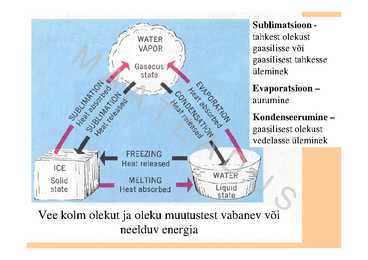
A gaasilisest olekust D vedelasse üleminek U S Vee kolm olekut ja oleku muutustest vabanev või neelduv energia M Õhuniiskuseks nimetatakse õhus leiduvat veeauru. Vastavalt veeauru kahele olekule (küllastamata ja küllastatud) eristatakse ka A küllastamata ja küllastatud niiskust. A Absoluutseks niiskuseks nimetatakse ühes kuupmeetris niiskes õhus T leiduva veeauru massi grammides. ( g/m3 ) E Suhteliseks ehk relatiivseks niiskuseks nimetatakse õhus oleva A veeauru rõhu ja samal temperatuuril õhku küllastava veeauru rõhu D
Inimkehas esineb ainult esterifitseerituna. 1.3 Kolesterool küllastamata tsükliline alkohol. Inimorg-mi steroolide tüüpesindaja. 2. Rasvhaped on karboksüülhaped, mille süsinikshelas on 4-36 süsinikku. RH on lipiidide ehituskomponendid, pisut esineb kudedes lipiide metabolismi vaheühenditena ja vereplasmas transportvormidena. Lipiidides RH-tes on: · pikk hargnemata süsinikahel · paarisarv C-aatomeid (inimkehas 16-22 C-aatomit) 2.1 Küllastatud RH · on vaid üksiksidemed · hargnemata · C-aatomid on paarisarvuga (palmithape 16:0, stearhape 18:0) 2.2 Monoküllastamata RH · üks kaksiside · olehape (18:1(9)) 2.3 Polüküllastamata RH (PUFA) · rohkem kui 1 kaksikside · linoolhape (18:2(9,12)), alfa-linoleenhape (18:3(9,12,15)), palmit-, stear-, ole-,arahhidoonhape.
Üliõpilase nimi: Rebecca Pärtel Töö nr: FK6 PUHTA VEDELIKU KÜLLASTUNUD AURURÕHU MÄÄRAMINE DÜNAAM Siia tuleb sisestada aparatuuri joonis. keskkonnatehnoloogia Instituut 280 Füüsikaline keemia Õpperühm: EANB31 Töö teostamise kuupäev: 23.09.2020 URURÕHU MÄÄRAMINE DÜNAAMILISEL MEETODIL Töö eesmärk (või töö ülesanne). Dünaamiline aururõhu määramise meetod põhineb aine keemistemperatuuride Teatavasti keeb vedelik temperatuuril, mil küllastatud aururõhk on võrdne välis mõõtmine erinevatel rõhkudel annab küllastatud aururõhu temperatuurriolene Clausiuse võrrandi abil arvutada vedeliku auramissoojuse. Teooria. Tegime kokku 8 mõõtmist. Alustasim 100 torrist ja kõige viimane mõõtmine oli Töövahendid. Ebulliomeeter, Vaakumpumba süsteem SC 950, elektriküttega kolb, jahuti, amp Töö käik. Mõõtmisi alustatakse madalamast rõhus ja seejärel suurendasime järkjärgult rõhku se
3 TÖÖ 4: KEEMILINE TASAKAAL 3.1 KATSE 1 – AINETE KONTSENTRATSIOONI MUUTUSE TOIME KEEMILISELE TASAKAALULE. Töö eesmärk: Uurida aine kontsentratsiooni muutuse toimet ainete keemilisele tasakaalule. Töövahendid: Keeduklaas, 4 katseklaasi, pipett, 20 ml destileeritud vett, raud(III)kloriid, küllastunud ammooniumtiotsüanaad Töökäik: Keeduklaasi valati 20 ml destilleeritud vett ning lisati 1 tilk küllastatud raud(III)kloriidi ja 1 tilk küllastunud ammooniumtiotsüanaadi lahust. Saadud lahus segati ja jagati võrdselt nelja katseklaasi vahel. Esimene katseklaas jäeti võrdluseks Teise katseklaasi lisati 2 kuni 3 tilka küllastatud raud(III)kloriidi lahust. Kolmandasse katseklaasi lisati 2 kui 3 tilka küllastatud ammooniumtiotsüanaadi lahust. Neljandasse katseklaasi lisati tahket ammooniumkloriidi ja loksustati tugevalt. Katse andmed:
Töö koosneb kahest osast. Esimeses osas valmistatakse galvaanielement ja mõõdetakse selle elektromotoorjõud. Seejärel mõõdetakse kummagi elektroodi potentsiaalid standardse võrdluselektroodi (kas kalomel- või hõbe-hõbekloriidelektroodi) suhtes. Mõõdetud suurusi võrreldakse Nernsti võrrandi põhjal arvutatud teoreetiliste väärtustega. Töö teises osas valmistatakse kontsentratsioonielement, mille üks elektrood on asetatud vähelahustuva soola (AgCl, AgBr või AgI) küllastatud lahusesse. Mõõdetakse elemendi elektromotoorjõud ja selle põhjal arvutatakse selle vähelahustuva soola lahustuvuskorrutis. Teoreetiline osa: Galvaanielemendi emj. E võrdub juhul, kui difusioonipotentsiaali ei arvestata, elektroodide potentsiaalide vahega: E 2 1 (1) kus 2 ja 1 on vastavalt positiivse elektroodi (katoodi) ja negatiivse elektroodi (anoodi)
Hüdroksokomplekside saamine ja omadused Kompleksühendid, mis koosnevad komplekskatioonist ja kompleksanioonist; Tundumad kompleksioonide iseloomulikud reakstioonid; Komplekside püsivus. Kasutatavad ained ja katsevahendid FeNH4(SO4)2; 1 M H2SO4; NH4SCN; konts. NaOH; BaCl; K3[Fe(CN)6]; 0,25 M CuSO4; 0,5 M NH3H2O; 6M NH3 H2O; 0,2 M NaOH; 0,5 M NH4Cl ; Zn graanulid; 2 M NaOH; 0,2 M NiSO4; 0,2 M NaCl; AgNO; 3 2 küllastatud NaCl; Co(NO ) ·6H2O kristallid; atsetoon; 0,2 M 3 3 3 2 2 4 3 3 2 Bi(NO ) ; 0,25 M KI; tahke KI; 0,2 M Pb(NO ) ; Na SO ; CH COONa; 0,2 M Cd(CH COO) 2 3 4 4 3 3 6 4 4 ; küllastatud Na SO ; etanool; 0,2 M ZnSO ; NiSO ; FeCl ; K [Fe(CN) ] ; FeSO ; CuSO ; 2 4 3 AgNO; 1M H SO ; 1M HNO ; katseklaaside komplekt