ORGAANILINE KEEMIA ALKEENIDES ON KAKSIKSIDE ALKÜÜNIDES ON KOLMIKSIDE DIEENIDES ON KAKS KAKSIKSIDET. ALDEHÜÜD – CHO (nime lõpp -aal) KETOON – R-CO-R (-oon) NO2 - nitrorühm Amiin – sees on N Amiid – CONH2 ester – aat COO 2-metüül-2-buteen 4.metüül-1-pentüün 4-metüül-1,3-pentadieen 2,2,4-trimetüülpentaan etüülmetüüleeter 2-metüül-3-pentanool 3-metüül-1-pentanool 1,2,3-propaantriool ehk glütserool 3-metüül-pentanaal 3-pentanoon 3,4-dimetüülpentaanhape 2-aminopentaanhape 1-nitropropaan 3-hüdroksü-propaanhape trimetüülamiin 2-metüülpropaanamiid etüülpropanaat etüületanaat ELEKTRONEGATIIVSUS MUUTUB ALT ÜLES JA VASAKULT PAREMALE FÜÜSIKALISED OMADUSED Tahked ained toatemperatuuril : • ained, mis ei ole molekulaarsed. Molekulidest saavad koosneda ainult mittemetallilistest elementidest koosnevad ained. Ioonilised (metall-mittemetall, metallid). C, Si, B on tahked ained!!! • H2, Hcl,...
Bhopali avarii Iga päev on nagu väike elu: iga ärkamine ja tõusmine väike sünd, iga värske hommik väike noorus, iga magamaminek ja uinumine väike surm. Tüüp Avarii kemikaalide tööstusel Põhjus Ametlikult ei ole fikseeritud Asukoht Bhopal, Madhya Pradesh Riik India Kuupäev 3. Detsember 1984 Aeg 00.30 Langenu 18 tuhat inimest d Kannata 600 tuhat inimest nudd Kronoloogia • 1970 a. UCC (Union Carbide Corporation) sai luba pestitsiidide tööstuse ehitamiseks Indias. • 1980 aastatel langes selle produktsiooni nõudmine • 1984 tööstust valmistati müümiseks. Ostjat ei leidnud ja tootmine jätkus ohusnõudeid täitamata. Tol ajal toodeti Sevinat, mida tehakse metüül-isotsüonaatist ja α- naftoolist. Need ained olid 60 000 l. tankides maa-all. Põhjus • Trageedia põhjuseks sai juhuslik metüül-isotsüanaati vabanemine. Reservuaari temperatuur jõudis 39 ° C, mis tõi rõhu tõstmist ja ...
Üldvalem CnH2n+2 Nimetus: lõppliide -aan, mis liidetakse C-aatomite arvu näitavale eesliitele. Alkaanide homoloogilise rea neli esimest liiget kirjeldatakse triviaalnimetustega (kokkuleppelised nimetused, mis ei allu kindlatele reeglitele), järgnevad nimetused tulenevad kreeka- või ladinakeelsetest numbritest. C-aatomite arv Valem Alkaan Alküülasendaja Alküülasendaja valem 1 CH4 metaan metüül -CH3 2 C2 H6 etaan etüül -C2H5 3 C3H8 propaan propüül -C3H7 4 C4H10 butaan butüül -C4H9 5 C5H12 pentaan pentüül -C5H11 6 C6H14 heksaan heksüül -C6H13
Küllastumata ühendid on orgaanilised ained, mis sisaldavad kordset sidet. Võivad olla süsivesinikud, küllastumata alkoholid jne. Liigitus: Alkeenid een lõpuga. Alküünid üün lõpuga. Kui aines on nii kaksik-, kui ka kolmikside siis nimetuses tuleb kõigepealt kaksiksideme tunnus ja seejärel kolmiksideme tunnus. Küllastumata ühendid on omega3 rasvhapped (alkeenid) Kui nimetuses on ees di, tri.. siis ei ole üüni/eeni ees heks vaid heksA. Küllastumata ühendite isomeerid: Alkeenidel eristatakse Cis- ja transisomeere. Cisisomeeridel on asendusrühmad ühelpool tasapinda. Transisomeeridel on asendusrühmad erinevatel pooltel tasanditel. Trans- kasulikud rasvad, rakumembraanid on ülesehitatud lipiididest ja nendes peab olema transrasvad. Cisrasvad on halvad. Alkeen ja tsükloalkaan on isomeerid, kui on süsinike arv sama. Alküünid ja tsükloalkeenid ka. Küllastumata ühendite keemilised omadused: Reaktsioonitsentris on kordsesideme juures olevad süsin...
Tallinna Ülikool Matemaatika ja Loodusteaduste Instituut Keskkond ja keemilised elemendid ning ühendite rühmad; ruumiõhk Referaat Keemilised elemendid ja ühendite rühmad Keemiline Elukeskkonda Inimesesse (ja Mõju inimesele Elukeskkonda element sattumise teed teistesse ja inimesesse või elusolenditesse) sattumise ühendi- sattumise viisid vältimise rühm võimalused nii riigi kui ka üksikisi...
KEEMIA 1. Mõisted 1) süsivesinikud- keemilised ained, mille molekul koosneb ainult süsiniku ja vesiniku aatomitest. NT metaan- CH4 2) alkaanid- süsivesinik, mille molekul sisaldab ainult sigma-sidemeid. Nt: heksaan C6H14 3) alküülrühm- alkaanist tulenev asendusrühm. Nt. CH3- metüül 4) trivaalnimetus- aine (peamiselt ajalooline) nimetus, mis ei vasta nomenklatuuri reeglitele.Nt. Met(aan) 5) süstemaatiline nimetus- aine nimetus, mis on antud nomenklatuurireegleid järgides. Nt soogaas, süstemaatiline nimetus metaan(CH4) 6) tetraeedriline süsinik- süsiniku aatom, mille kovalentsed sidemed on suunatud tetraeedi tippudesse. Nt. CH4 7) pürolüüs- aine muundumine kõrge temperatuuri toimel. Nt.
CH2 CH2 CH2 CH2 CH2 CH3 Radikaalid .... on orgaanilised ühendid, kus molekulis leidub üks vaba valents (side). Tänu vabale sidemele on radikaalid väga reaktsioonivõimelised ja liituvad kergesti orgaaniliste ühenditega. Radikaalid saadakse, kui süsivesinike molekulist eemaldada üks vesiniku aatom. Süsivesinik Radikaal Metaan CH4 Metüül CH3 H H H C H H C H H Etaan C2H6 Etüül C2H5 CH3 CH3 CH3 CH2 Propaan C3H8 Propüül C3H7 CH3 CH2 CH3 CH3 CH2 CH2 Isopropüül CH CH3
Aldehüüdid on keemilised ühendid, mis sisaldavad funktsionaalse rühmana aldehüüdrühma (CHO). Selline järjestus tähendab, et hapniku ja vesiniku aatomid pole omavahel seotud (erinevalt alkoholist (ROH)). Lihtsaim aldehüüd on formaldehüüd e. metanaal, mille 37-protsendine vesilahus on formaliin. Aldehüüdi üldvalem. -R on aldehüüdrühmaga seotud radikaal. Ainerühm Funktsionaalrühm Valem Struktuurvalem Eesliide Järelliide Näide Aldehüüdid Aldehüüdrühm RCHO okso- -aal Atseetaldehüüd (Etanaal) Ketoonid on orgaanilises keemias ühendid, milles karbonüülrühm (C=O) on seotud kahe süsiniku aatomiga. Lihtsaim ketoon on 2-propanoon ehk atsetoon (CH3COCH3). Ketooni üldvalem Ainerühm Funktsionaalrühm Valem Struktuurvalem Eesli...
(ALKAANID) (ASENDUSRÜHM) CH4 Metaan CH3-metüül C2H6 Etaan C2H5- etüül C3H6 Propaan C3H7 -Propüül C4H10 Butaan C4H9 -butüül C5H12- Pentaan JNE.... C6H14- Heksaan C7H16- heptaan C8H18 -oktaan C9H20 - nonaan C10H22- dekaan Valents- näitab mitut kovalantet sidet võib antud aatom moodustada. Orgaanilises ühendites on süsiniku valem alati 4 ORAAGILISED ÜHENDID- a)atsüklilised b) tsüklilised Isomeeria on nähtus, kus ainetel on ühesugune element koostis ja molekulmass aga erinev struktuur ja omadused Molekulvalem- summaarvalem nõitab aine koostist, kui palju ja milliste elementide aatomid on molekulis. Klassikaline e. Tasapinnaline struktuur valem näitab millised aatomid ja milliste sidemetega on omavahel seotud. Lihtsustatud struktuurvalem näitab millisedaatomirühmad jamilliste sidemetaga on omavahel seotud. ...
TRINITROTOLUEEN (TNT) TEISED TUNTUMAD NIMED · 2,4,6-TRINITROTOLUEEN · 2,4,6-TRINITROMETÜÜLBENSEEN · 2-METÜÜL-1,3,5-TRINITROBENSEEN · TROTÜÜL ÜLDVALEM C 2H6(NO2)3CH3 SAAMINE KOLM SAMMU TOLUEEN NITREERITAKSE VÄÄVEL JA LÄMMASTIKHAPPE SEGUGA,SAADAKSE MONONITROTOLUEEN SEE OMAKORDA ERALDATAKSE JA NITREERITAKSE UUESTI ET SAADA DINITROTOLUEEN VIIMASEKS SAMMUKS ON DINITROTOLUEENI NITREERIMINE VEEVABA LÄMMASTIKHAPPE JA ÕLI SEGUGA,LÕPPSAADUSEKS ON TRINITROTOLUEEN KASUTAMINE KASUTATAKSE VAHEL REAKTIIVINA KEEMILISTES SÜNTEESIDES AGA ENAMSTI SIISKI LÕHKAINENA TROTÜÜLI LÕHKEVJÕUD ON STANDARDMÕÕT OMADUSED VEES MITTELAHUSTUV EI IMA VETT SIISSE SULAB MADALAL TEMPERATUURIL,80.35C VÄGA STABIILNE DETONATSIOONIKIIRUS 6900m/s KEEMISPUNKT 295C Click to edit Master text styles Second level PILT ...
1) Triviaalsed nimetused Näiteks metaan ehk ............................ Metaanhape ehk ............................ 2) Süstemaatilised nimetused moodustatakse molekuli struktuuri järgi kindlaid reegleid kasutades. ALKAANI tunnuseks on liide aan. TV 2.1. Alkaanist pärit asendusrühma nim alküülrühmaks. alküülrühmaks Tähis R- alkaan alküülrühm metaan CH4 metüül CH3 etaan CH3CH3 etüül CH3CH2 CH3CH2CH2 propaan CH3CH2CH3 CH3CHCH3 Nimetuste andmine hargnenud ahelaga alkaanidele. Kõigepealt leitakse molekuli valemist pikim süsinikahel ahel, milles süsiniku aatomite arv on suurim. Sellele hargnemata ahelale ehk peaahelale vastav süsivesinik olgu tüviühend. Tüviühendi C aatomid nummerdatakse nii, et
ALKAANID JA NENDE NOMENKLATUUR Süsini- Arv- ALKAAN ALKÜÜLRÜHM ehk TSÜKLOALKAAN ke C sõna Üldvalem CnH2n+2 ASENDUSRÜHM Üldvalem CnH2n arv n Üldvalem CnH2n+1 Valem Nimetus Valem Nimetus Valem Nimetus 1 Mono CH4 metaan CH3- metüül- - - 2 Di C2H6 etaan C2H5- etüül- - - 3 Tri C3H8 propaan C3H7- propüül- C3H6 tsüklopropaan 4 Tetra C4H10 butaan C4H9- butüül- C4H8 tsüklobutaan 5 Penta C5H12 pentaan C5H11- pentüül- C5H10 tsüklopentaan 6 Heksa C6H14 heksaan C6H13- heksüül- C6H12 tsükloheksaan 7 Hepta C7H16 heptaan C7H15- heptüül- ...
ALKEENID JA ALKÜÜNID Propeen Propeen on värvuseta ja vees lahustumatu gaas ning ta kuulub alkeenide aineklassi. Keemistemperatuur on -47,6 C Sulamistemperatuur on -185,2 C Keemiline valem on C3H6 Eteen Eteen on normaaltingimusel värvitu gaas. See on lihtsaim alkeen. Molekulvalem on C2H4 Sulamistemperatuur -169.1 °C Keemistemperatuur -103.7 °C Buta-1,3-dieen Isopreen ehk 2-metüülbuta-1,3dieen Isopreen ehk 2-metüül-1,3-butadieen on orgaaniline ühend. Isopreen on madala keemistemperatuuriga (34,067 °C) värvitu vänge lõhnaga vedelik, mis polümeriseerub kergesti. Isopreeni keemiline valem on C5H8 ehk 2=(3) =2. Tööstuslikult saadakse isopreeni nafta termilise krakkimise produktidest. Etüün ehk atsetüleen Atsetüleen on lihtsaim alküün,mis koosneb kahest vesiniku aatomist ja kahest süsiniku aatomist kolmiksidemega seo...
Alkaanideks nimetatakse orgaanilisi aineid, mis koosnevad C ja H'st, ning kus C aatomite vahel on üksikside ehk sigmaside. Üldvalem CnH2n+2 (n on jrk nr) Orgaanilistele ainetele pannakse nimed alkaanide homoloogilise rea alusel. 1. metaan CH4 2. etaan C2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptann C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22 Radikaalid on molekulid või aatomid, mille elektronkihis asub paardumata elektron. 2-metüül propaan Alkaanide keemilised omadused: 1) Põlemine CH4 + 2O2 -> CO2 + 2H2O 2) Asendus reaktsioon hallogeenidega (radikaaliline asendusreaktsioon) ...
Alkohol-ained,mille molekulis C-aatomi juures asuv vesinik on asendatud hüdroksüülrühmaga.CnH2n+1 -OH;R-OH Mitmehüdroksüülne.al-alkoholi mol.on mitu hüdrok.rühma Vesinikside-mol.veheline side mis tekib ühe mol. + osalaenguga H-aatomi & teise mol. vahel.;Hape-loovutab prootoneid;alus-seob prootoneid;Funktsionaalne rühm-Mol. kõige kergemini muundatav osa.;Diool-alkohol , milles 2OH rühma; eetrid-R1 -O-R2 Metanool-CH3OH(puupiiritus) kasut.keemiatööstus. lahustite koostisosana. Väga mürgine,värvuseta,iseloomuliku lõhnaga vedelik,lahustub hästi vees,,hea lahusti. Etanool (samad om.)C2H5OH,piiritus.Kasut. lahustina ja sünteeside lähtainena. Inimesele mõju-mõjutab närvisüsteemi.narkootilise toimega.kahj.maksa ja neere. Etanool-atanaal-etaanhape-CO2+H2O Etaandiool-HOCH2CH2OH, 198¤tp. Lahust.hästi vees,vesilahused madala külmumis temp.kasut. automootorijahutuss.koostises. Propaantriool(glütserool)HOCH2CH(OH)CH2OH Looduslik ühend,isegi toitaine. ...
SÜSIVESINIKE NOMENKLATUUR Kõikide küllastunud ja küllastumata süsivesinike nimetamise süsteem tugineb hargnemata ahelaga alkaanide nimetustele. Süsinike Alkaani valem Alkaani Alküülrühma valem Alküülrühma arv nimetus nimetus 1 CH4 metaan CH3 metüül 2 C2H6 etaan C2H5 ehk CH2CH3 etüül 3 C3H8 propaa C3H7 ehk CH2CH2CH3 propüül n 4 C4H10 butaan C4H9 ehk CH2CH2CH2CH3 butüül 5 C5H12 pentaan ... ... 6 C6H14 heksaan ... ...
Amfetamiin ehk alfa-metüül- fenetüülamiin. Kuidas veel kutsutakse? · Spiid, amff, kiirus, ants, A. Kuidas kasutajat ära tunda? · silmaavad on laienenud; · heaolu ja õnnetunne; · energiline, närviline ja rahutu; C9H13N Miks on kahjulik? · amfetamiin tekitab tugevat sõltuvust. Sõltlane ei suuda ilma aineta elada ja vajab enda hästi tundmiseks üha uusi koguseid; · palju müüakse ebapuhast amfetamiini, see võib põhjustada tugevat mürgitust; · pikaajalised kasutajad jäävad enamasti impotendiks või frigiidseks; · need kasutajad, kes amfetamiini ninna tõmbavad, kahjustavad tõsiselt oma nina ja lõhnataju; · kasutaja võib olla väga halvas tujus, rahutu ja segaduses. Samuti võivad tekkida hirmuhood ning tunne, et teda jälitatakse. Lisaks esinevad palavikuhood ja tal võib minna süda pahaks; · kui uimasti toime hakkab lõppema, ollakse sageli väga...
Asendusrühmadeks on halogeeniaatomid. Nende nimetused on vastavalt fluoro-, kloro-, bromo- ja jodo-. Asendusrühmade arvu väljendatakse samuti eesliidetega di-, tri- jne. Asendusrühma tüviühendiga liitumise kohta tähistatakse kohanumbriga. CH3CHCl2 1,1-dikloroetaan CH3CF(CH3)CH3 2-fluoro-2-metüülpropaan Funktsionaalnomenklatuur: Funktsionaalrühmaks on halogeeni aatom. Selle järgi nimetatakse tüvi: kloriid, bromiid jne. Selle juurde kuulub alküülradikaal: metüül, etüül jne. Kasutatakse lühikese ja sirgeahelaliste, ühe halogeeniaatomiga ühendite puhul. CH3Cl metüülkloriid CH3CH2Br etüülbromiid Füüsikalised omadused · Olek toatemperatuuril: enamus vedelad; mõned lühikeseahelalised on gaasid (klorometaan, kloroetaan jt). Kegesti lenduvad kasutusel jahutusainenea külmkappides, pihustusainena aerosoolides- freoonid. Kahjustavad osoonikihti.
Amiinid Amiinid on ammoniaagi (NH3) derivaadid, kus vesiniku aatomid on asendatud süsi- vesinikega. Eristatakse primaarseid, sekundaarseid ja tertsiaalseid amiine, kus orgaanilise ainega on vastavalt asendatud kas üks, kaks või kolm vesinikku. Amiinid tekivad orgaaniliste materjalide mikrobioloogilisel lagunemisel [Aminohapped valgud (lagunemine) amiinid], eriti õhuhapniku puudumisel, levitades sealjuures ebameeldivat roiskumislõhna. Seetõttu nimetatakse neid ka laibaaineteks. Amiinidevahelised sidemed on nõrgad ning nad oksüdeeruvad kergesti mitmete ainete toimel. Lihtsamad amiinid on toatemperatuuril gaasilised, alates C12 tahked. Vähe süsinikke sisaldavad amiinid on vees lahustuvad, süsinike arvu kasvades lahustuvus väheneb. Amiine kasutatakse ravimite valmistamisel ja keemilistes sünteesides. Näiteks etüülamiin ja trietüülamiin takistavad raua roostetamist. Samuti on amiinidel mõju or...
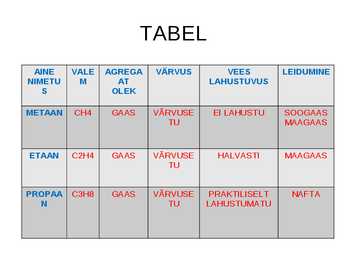
TABEL AINE VALE AGREGA VÄRVUS VEES LEIDUMINE NIMETU M AT LAHUSTUVUS S OLEK METAAN CH4 GAAS VÄRVUSE EI LAHUSTU SOOGAAS TU MAAGAAS ETAAN C2H4 GAAS VÄRVUSE HALVASTI MAAGAAS TU PROPAA C3H8 GAAS VÄRVUSE PRAKTILISELT NAFTA N TU LAHUSTUMATU ALKAANIDE ÜLDVALEM CnH2n+2 C-aatomite arv Nimetus Valem Olek 1 METAAN CH4 G 2 ETAAN C2H6 A 3 PROPAAN C3H8 A 4 BUTAAN C4H10 S 5 PENTAAN C5H12 6 HEKSAAN C6H14 7 HEPTAAN C7H16 VEDELIK 8 OKTAAN C8H18 9 NONAAN ...
Nikotiin Sisukord Nikotiin Leidumine Avastamine ja saamine Keemilised omadused Füüsikalised omadused Füsioloogilised omadused Huvitavad faktid Nikotiin Alkaloid Keemiline valem: C10H14N2 Nomeklatuurnimetus: (S)-3-(1-Metüül-2- pürroli-dinüül)püridiin Potentne närvimürk Leidumine Maavitsaliste sugukonna taimed: Tubakas Tomat Kartul Baklazaan Paprika Kokapõõsa lehed Avastamine ja saamine Biosüntees toimub juurtes, koguneb lehtedele Kogutakse lehtedelt Tehakse nt. sigarette Keemilised omadused Lahustub kergesti vees Reageerib hapnikuga (nikotiinhape) Põleb hästi Füüsikalised omadused Molekulmass: 162.23 g/mol Tihedus: 1.01 g/ml Sulamistemperatuur: -79 °C Keemistemperatuur: 247 °C (laguneb) Isesüttimistemperatuur: 240 °C Õlitaoline värvuseta mõru vedelik Füsioloogilised omadused Tubakasõltuvus Näljatunne väheneb Vere suhkrusisalduse tõus Südame löögisagedus tõuseb Kopsude töövõime langemine Hapete ...
Sisukord Sisukord...................................................................................................................................... 2 Sissejuhatus.................................................................................................................................3 Saamismeetodid.......................................................................................................................... 4 Füüsikalised omadused............................................................................................................... 5 Keemilised omadused................................................................................................................. 6 Kasutusalad.................................................................................................................................9 Ohutusnõuded............................
Nikotiin Liis Kivirand Üldiselt Nikotiin on alkaloid. On leitav maavitsa perekonna taimedest (Solanaceae), eriti tubakast, ja vähemal määral tomatist, kartulist, baklazaanist, rohelisest piprast ja kokapõõsa lehtedest. Puhas nikotiin on õlitaoline värvuseta mõru vedelik, mis lahustub kergesti vees. Nikotiini leidub 0,3 kuni 5% tubakataime kaalust, kus selle biosüntees toimub juurtes ning see koguneb lehtedesse. Valem: C10H14N2 Nomeklatuurnimetus: (S)-3-(1-Metüül-2- pürroli-dinüül)püridiin. Molekulmass: 162.23 g/mol Tihedus: 1.01 g/ml Sulamispunkt: -79 °C Keemispunkt: 247 °C (laguneb) Isesüttimis temperatuur: 240 °C Mõju inimesele Nikotiin tekitab sõltuvuse, seega on ta narkootiline aine. 50 mg nikotiini süstimine verre tapaks inimese. Ühe sigaretiga satub inimorganismi 0,3...1,5 mg nikotiini. Väikeses koguses ergutab nikotiin närvisüsteemi, mistõttu inimene võib muutuda erksamaks, te...
Alkoholide ja eetrite füüsikalised ja füsioloogilised omadused Vesiniksidemed 1. Alkoholide füüsikalised omadused: a) Alkoholid saavad moodustada vesiniksidemeid, kuna hüdroksüülrühma vesinikul on positiivne laeng b) Vesiniksidemed võivad moodustuda nii alkoholi molekulide vahel kui ka vee ja alkoholide molekulide vahel c) Tänu vesiniksidemetele on alkoholid hüdrofiilsed ained: metüül-, etüül ja propüülalkoholid segunevad veega igas vahekorras pikema ahelaga alkoholid segunevad veega piiratud koguses mitme hüdroksüülrühmaga alkoholid (dialkoholid, trialkoholid jne) lahustuvad vees igas vahekorras d) Vesiniksidemed mõjutavad ka alkoholide keemistemperatuure: mida rohkem ja tugevamad vesiniksidemed (ehk mida rohkem OH rühmi), seda kõrgem keemistemperatuur mida pik...
Küllastumata süsivesinikud (küllastumata = molekulis mitmikside) Alkeenid: küllastumata alifaatsed süsivesinikud, mille molekulis on kaksikside CnH2n (Süsinik II valentsolekus 1200) Alküünid: küllastumata alifaatsed süsivesinikud, mille molekulis on kolmikside CnH2n-2 (Süsinik III valentsolekus 1800) (Alka)dieenid: küllastumata alifaatsed süsivesinikud, mille molekulis on kaks kaksiksidet CnH2n-2 analoogiliselt võib rääkida dieenidest, trieenidest ...... polüeenidest Nimetused Kaksiksidet tähistab liide -een ja kolmiksidet -üün Peaahel sisaldab kõige rohkem mitmiksidemeid - kõige olulisemad on just kaksiksidemed Peaahel nummerdatakse nii ,et kaksiksidemed saavad väiksemad numbrid Vajadusel kasutatakse liiteid: di- , tri- , tetra jne. 4. 3. 2. 1. CH3-CH(CH3)-CH=CH2 3-metüül-1-buteen 6. 5. 4. 3. 2. 1. CH:::C- CH(C2H5)-CH2-CH=CH2 4-etüül -5...
Järgmiste süsivesinike nimetused tuletatakse kreekakeelsete arvsõnade tüvest lõpu aan abil (5 pentaan, 6 heksaan jne). · Ühevalentse radikaali alküülradikaali (kui küllastunud süsivesinikust on eemaldatud üks vesiniku aatom) nimetus tuletatakse süsivesiniku nimetuse lõpu aan asendamisel lõpuga üül (alkaan alküül, etaan etüül, pentaan pentüül). Alkaan (CnH2n+2) Vastav alküülradikaal (CnH2n+1) CH4 metaan CH3 metüül C2H6 etaan C2H5 etüül C3H8 propaan C3H7 propüül C4H10 butaan C4H9 butüül C5H12 pentaan C5H11 pentüül C6H14 heksaan C6H13 heksüül C7H16 heptaan C7H15 heptüül C8H18 oktaan C8H17 oktüül C9H20 nonaan C9H19 nonüül C10H22 dekaan C10H21 detsüül · Hargnenud ahelaga alkaane nimetatakse ahela järgi, milles süsiniku aatomite arv on
Ande Andekas-Lammutaja Keemia Eetrid Eetrite üldvalemiks on R O - R. Hapnikuga seotud süsivesinikrühmad (R) võivad olla erinevad. Nimetuses nimetatakse süsivesinikrühmad tähestikulises järjekorras. Kui ühesuguseid süsivesinikrühmasid on rohkem, siis kasutatakse eesliiteid di, -tri jne. Nimetuse lõpuks on eeter. Enamik eetreid on keemiliselt püsivad, sest sidet süsiniku ja hapniku vahel raske lõhkuda (tekivad tugev nukleofiil alkoksiidioon RO ning tugev elektrofiil karbkatioon R +, mis eelistavad ülikiiret taasühinemist). Eetrid oksüdeeruvad suhteliselt kergelt hapnikuga seotud süsiniku juurest. Tekivad peroksiidid, mis on plahvatusohtlikud. Eetrid on väga lenduvad. Ei moodusta omavahel vesiniksidemeid ning ka veega ei anna vesiniksidemeid. Seetõttu ei lahustu hästi ...
Kordamisküsimused /Alkoholid. Eetrid. Fenoolid/ Osata kirjutada alkoholide tasapinnalisi struktuurvalemeid, lihtsustatud struktuurvalemeid, molekulvalemeid ja graafilisi kujutisi. Näide: a) 3-kloro-2-butanool b) 1,2,3-propaantriool c) 3-kloro-3-metüül- heksanool 2) Osata alkohole nimetada EMBED ACD.ChemSketch.20 EMBED ACD.ChemSketch.20 3) Osata iseloomustada ja võrrelda alkoholide füüsikalisi omadusi (sulamistemp, keemistemp, lahustuvus vees) lähtuvalt süsinike arvust ja hargnevusest) Näide: a) kumb lahustub vees paremini- kas propanool või metanool? Põhjenda b) kummal keeb kõrgemal temperatuuril- kas etanool või butanool? Põhjenda. 4) Kuidas tõestada, et alkohol on nõrga happe omadustega? 5) Alkoholide keemilised omadused. Näide: Kirjuta reaktsioonivõrrandid ja anna saadustele nimetused a) etanooli põlemine b) metanool + kaltsium c) propanooli põ...
Kordamisküsimused kontrolltööks (Õpik lk 51- 85) 1.Alkaanide mõiste. Alkaanid on süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega 2. Tuntumad alkaanid: Metaan - kasutatakse laialdaselt kütusena ja soojuselektrijaamades elektri tootmiseks, ka valgustamiseks ja õli tootmiseks. Metaan sisaldub majapidamisgaasis. Metanool, ammoniaak. Etaan – Propaan - Kasutatakse kõrgahju kütusena, terase lõikamisel ja keevitamisel(segus hapnikuga) 3. Homoloogilise rea mõiste. Ainete keemistemperatuuri muutus homoloogilises reas Homoloogiline rida - samasse aineklassi kuuluvate sarnaste omaduste ja struktuuriga keemiliste ühendite rida. Süsiniku aatomite arvu kasvades kasvavad homoloogilise rea liikmete tihedus, sulamis-ja keemistemperatuur, väheneb aga lahustuvus vees. 4. Alkaanide nomenklatuur - reeglistik nimetus...
Nimetused: · Süstemaatilised annab teavet struktuurist (nt. metaanhape) · Triviaalnimetused antakse mõne omaduse või leidumuse põhjal (nt. sipelghape) Alkaani tunnuseks on sõnalõpp aan. Sõnatüvi kirjeldab süsinikahela pikkust. 1. Met(aan) 2. Et(aan) 3. Prop(aan) 4. But(aan) 5. Pentaan 6. Heksaan 7. Heptaan 8. Oktaan 9. Nonaan 10. Dekaan Tsüklilist ahelat tühistab eesliide tsüklo. Alküülrühma tunnuseks on sõnalõpp üül. 1. Metüül 2. Etüül 3. Propüül Jne.. Kohanumber kirjutatakse kõige ette ning see tähistab hargnemise kohta. Nt: 2 metüülbutaan Süsinike arv Arvsõna Alkaani Alküülrühma Tsükloalkaani ahelas nimetus nimetus nimetus 1 Mono Mentaan Metüül - 2 Di Etaan Etüül -
Asendusrühmadeks on halogeeniaatomid. Nende nimetused on vastavalt fluoro-, kloro-, bromo- ja jodo-. Asendusrühmade arvu väljendatakse samuti eesliidetega di-, tri- jne. Asendusrühma tüviühendiga liitumise kohta tähistatakse kohanumbriga. CH3CHCl2 1,1-dikloroetaan CH3CF(CH3)CH3 2-fluoro-2-metüülpropaan Funktsionaalnomenklatuur: Funktsionaalrühmaks on halogeeni aatom. Selle järgi nimetatakse tüvi: kloriid, bromiid jne. Selle juurde kuulub alküülradikaal: metüül, etüül jne. Kasutatakse lühikese ja sirgeahelaliste, ühe halogeeniaatomiga ühendite puhul. CH3Cl metüülkloriid CH3CH2Br etüülbromiid Ahelisomeeria: ühendite erinevus on ahela kujus Näide: CH3- CH2- CH2 -CH3 butaan CH3- CH - CH3 isobutaan CH3 Asendiisomeeria:ühendite erinevus on sidemete või funktsionaalrühmade erinevas paiknemises Näide: 1- klorobutaan ja 2-klorobutaan
HINGAMISELUNDITE RAVIMID GLÜKOKORT M- METÜÜL- EKSPEKT ANTIHIST LEUKOTRI DEKONGES- I-KOIDID KOLINOB KSANIINI O- A- EE-NIDE TANDID LO- D RANDID MIINIKUM ANTA- NB! Üle 7 päeva kasutamine = KAATORI ja KÖHA ID GONISTID medikamentoosne PÄRSSIJA riniit D FLUTIKASOON- IPRAPROO- TEOFÜL- ATSETÜÜL- KLEMAS- ...
Alternatiivkütused ja biokütuste kasutamise võimalused ning sellega seotud riskid Sissejuhatuseks Maailam majandus sõltub tänapäeval naftast, mida kasutatakse enrgia, mootorikütuste ja tarbekaupade tootmiseks. Autode arv ja seega ka nõudlus fossiilkütuste järele on viimastel aastakümnetel suurenenud. See on põhjustanud õhu saatumist tihedalt asustatud aladel, kuid samas on inimesed hakanud teadvustama fossiilsete kütuste kasutamise mõju loodukeskkonnale ja tervisle. Kuna süsinikupõhiste fossiilkütuste kasutamine arvatakse põhjustavat kliima muutusi on see pannud mõtlema alternatiivsete mootorikütuste arendamisele. Alternatiivkütuste ja biokütuste kasutamise võimalused Vedelate biokütuste tootmine ja kasutamine on viimasel ajal hoogustunud tänu erinevatele majandus-poliitilistele meetmetele nende kasutamise soodustamiseks. ● Maailmas toodetakse kõige rohkem biodiislikütust (taimsetest või loomsetest õlidest toodetud, diislikütu...
KT elektrolüüdid 1. Ioonideks lagunemine e. dissotsiatsioon ainult vees lahustuvad ained! 1) Hapete jagunemine ioonideks: HCl -> H+ + Cl- (õigem: HCl + H2O -> H3O+ + Cl-) Happed, milles on rohkem vesinikke, jagunevad ioonideks astmeliselt: H2SO4 -> H+ + HSO4- = I aste HSO4- <-> H+ + SO42- = II aste 2) Soolade jagunemine ioonideks toimub ühes astmes: NaCl -> Na + + Cl- või Na2SO4 -> 2Na+ + SO42- või Na3PO4 -> 3Na+ + PO43- + 2- Cu2SO4 -> 2Cu + SO4 3) Aluste jagunemine ioonideks: NaOH -> Na+ + OH- Toimub astmeliselt, kui OH rühmi on rohkem: Ba(OH) 2 -> BaOH+ + OH- = I aste BaOH+ -> Ba2+ + OH- = II aste 2. Soolalahuse pH, keskkond, indikaatori värv Vees lahustuvad: tugevad alused: IA(Li alla) ja IIA(Ca alla) ja tugevad happed: HCl, HBr, HI, HNO 3, H2SO4 Tugevam aine määrab keskkonna: NaCl (mõlemad tugevad) => nautraalne keskkond pH=7 Na2SO3 (T(ugev) ja N(õrk)) => aluseline pH>7 ZnBr2...
Alkoholid ja karboksüülhapped Alkoholid on sellised süsivesinikest tuletatud ühendid, milles üks või enam vesiniku aatomit on asendatud ühe või enam hüdroksüülrühmaga (-OH- rühmaga) Alkoholid ei muuda indikaatori värvi. R-alküülrühm (tuletatakse alkaani valemist lahustades ühe vesiniku aatomit) R-OH CH4 metaan ; CH3 metüül ; CH3OH metanool Metanool CH3Oh on suure süsinikuühendite rühm alkoholide kõige lihtsam esindaja. Metanooli võib saada metaani oksüdeerumisel: 2CH4 + O2 -> 2 CH3OH Metanool on värvitu, põletava maitsega mürgine vedelik, mis keeb temperatuuril 65C ja seguneb veega igasuguses vahekorras. Vähene kogus metanooli võib põhjustada raskeid tervisehädasid, sealhulgas pimedaks jäämist. Etanool CH3CH2OH on tähtsaim ja tuntuim alkohol.
Vitamiinid Keemiline Tähis Olulised allikad Vaeguse mõju Liigsuse mõju põhinimetus Rasvlahustuvad vitamiinid kala- ja loomamaks, või, põhjustab põhjustab kaheli keedetud porgand, kanapimedust, nägemist, juuste A retinoidid spinat, kõrvits ja kuivsilmsust, sarvkesta väljalangemist, maksa lehtkapsas, melon, pehmumust, suurenemist, iiveldust, aprikoosid, tomat, kasvuhäireid peavalu sibul põhjustab kasvupeetust, kalaõli, põhjustab rahhiiti ja kaltsiumi kogunemist D ...
Nimed Struktuurvalem Omadused Kasutamin esinemin Benseen * omapärase lõhnaga *ravimite, lõhkeainete C6H6 * MÜRGINE mitmesuguste polüme * värvuseta toorainena * kergestisüttiv *rasvade, vaikude ja k * vees halvasti lahustina lahustuv vedelik *mõnikord harva * keemist...
Süsivesinike segu Nafta Looduslik vedelkütus, peamiselt leiduv vedelate süsivesinike segu Krakkimine Nafta ddestilleerimissaaduste lagunemine lühemate ahelatega ühenditeks Fraktsioneeriv destillatsioon - on destillatsioonimeetod kasutades destillatsioonikolonni, milles toimub korduv aurustumine ja kondensatsioon. Alkaanide nimetused/valemid (graafilised, tasapinnalised, lihtsustatud) Tähtsamad alkaanid: CH4 metaan CH3 metüül C2H6 etaan CH3CH2 etüül C3H8 propaan CH3CH2CH2 propüül C4H10 butaan CH3CH2CH2CH2 butüül C5H12 pentaan C6H14 heksaan C7H16 heptaan C8H18 oktaan C9H20 nonaan C10H22 dekaan Isomeerid (Koostamine, füüsikaliste omaduste tuletamine ja põhjendamine) Isomeeride struktuur on erinev, siis erinevad on ka nende omadused ehk omadused sõltuvad aine struktuurist.
NIKOTIIN Mis on nikotiin? · Nikotiin on alkaloid,mis on leitav maavitsaliste sugukonna taimedest. · Nikotiini leiab eriti tubakast , vähemal määral tomatist,kartulist ja paprikast. · Nikotiini alkaloidid on leitavad ka kokapõõsa lehtedest. · Nikotiin on potentne närvimürk ja on lisatud ka mitmetele putukamürkidele · Puhas nikotiin on õlitaoline värvuseta mõru vedelik,mis lahustub kergesti vees. · On väga laiaulatuslik mürk organismis. · On narkootiline aine,tekitab pideval tarbimisel sõltuvuse. · Ühe sigaretiga satub inimorganismi 0,3...1,5 mg nikotiini. · Ainuüksi 50 mg nikotiini süstimine verre tapaks inimese !!! Kuidas mõjub nikotiin inimesele ? · Nikotiin toimib inimeste stressi sumbutajana. · Väikeses koguses ergutab nikotiin närvisüsteemi,inimene muutub erksamaks,enesetunne paraneb ja näljatunne võib väheneda,kui nikotiini pettetunne on lühiaegne. · Nikotiin mõjub otseselt ka neerupealistele. · ...
NIKOTIIN Mis on nikotiin? Nikotiin on alkaloid,mis on leitav maavitsaliste sugukonna taimedest. Nikotiini leiab eriti tubakast , vähemal määral tomatist,kartulist ja paprikast. Nikotiini alkaloidid on leitavad ka kokapõõsa lehtedest. Nikotiin on potentne närvimürk ja on lisatud ka mitmetele putukamürkidele Puhas nikotiin on õlitaoline värvuseta mõru vedelik,mis lahustub kergesti vees. On väga laiaulatuslik mürk organismis. On narkootiline aine,tekitab pideval tarbimisel sõltuvuse. Ühe sigaretiga satub inimorganismi 0,3...1,5 mg nikotiini. Ainuüksi 50 mg nikotiini süstimine verre tapaks inimese !!! Kuidas mõjub nikotiin inimesele ? Nikotiin toimib inimeste stressi sumbutajana. Väikeses koguses ergutab nikotiin närvisüsteemi, inimene muutub erksamaks,enesetunne paraneb ja näljatunne võib väheneda,kui nikotiini pettetunne on lühiaegne. Nikotiin mõjub otseselt ka neerupealistele. K...
tulenevalt süsinikuaatomite arvust, tüviühendi küllastatus või küllastumatus ning aineklassi väljendav lõppliide vastavalt vanimale põhirühmale (funktsionaalrühmale). Seejuures kasutatakse kindlaid kirjavahemärke (vaata näidet). Mingi rühma kordumisel kasutatakse koos rühma nimetusega eesliiteid di-, tri-, tetra- jne. Summaarne valem Nimetus Tuletatud alküülrühm CH4 Metaan CH3 metüül C2H6 Etaan C2H5 etüül C3H8 Propaan C3H7 propüül C4H10 Butaan C4H9 butüül C5H12 Pentaan C5H11 pentüül C6H14 Heksaan C6H13 heksüül C7H16 Heptaan C7H15 heptüül
Propaan C3H8 Heptaan C7H16 Undekaan C11H24 Butaan C4H10 Oktaan C8H18 Dodekaan C12H26 jne Hargneva ahela korral loetakse pikim ahel peaahelaks ja muud ahelad kõrvalahelateks Peaahel määrab nime lõpu Kõrvalahelate asukoht (mitmenda peaahela süsiniku küljes) näidatakse numbriga Kõrvalahelaid nimetatakse nagu radikaale, -aan lõpp asendub lõpuga üül Näiteks: CH3- metüül ; CH3CH2- etüül ; CH3CH2CH2- propüül hargneda võib ka kõrvalahel sellisel juhul on nime andmine keeruline, kuid põhimõtteliselt analoogiline . 3 Lihtsamat hargnevat radikaali CH3CHCH3 kutsutakse isopropüüliks Ühesuguste kõrvalahelate arvu näidatakse eesliidet di-, tri-, jne. Abil Radikaalid järjestatakse tähestiku järjekorras 6. 5. 4. 3. 2
10. Aldoolreaktsioonid Karbonüülrühma -vesinike happelisus Karbonüülühendite teiseks oluliseks iseloomuks on karbonüülrühmaga külgnevate süsinikuaatomite juures olevate vesinike happelisus. Selliseid vesinikuaatomeid nimetatakse -vesinikeks. O H O R C C C R H Karbonüülrühma -vesinike happelisuse põhjused on lihtsad. Karbonüülrühm on tugev elektronaktseptoorne rühm ja kui karbonüülühendist eraldub -prooton, siis tekkinud anioon on resonantsi poolt stabiliseeritud. Aniooni negatiivne laeng on delokaliseerunud. .. - .. .. - :O H :B :O :O : -.. C C C C C C + H B A B Resonantsi po...
4) Parafiin n-alkaanide (C16-C40) segu. Kasutatakse küünalde valmistamisel maskide tegemisel (avab naha poorid, mis võimaldab aktiivainete paremat imendumist alkaanide nimetamine Järelliide: *leia asendusrühmad *asendusrühmad reasta tähestikulises järjekorras *nummerda süsinikuahel alustades sealt otsast, millele asendusrühm on kõige lähemal *asendusrühmade arv näita ära eesliitega *Kui mitu asendusrühma on identsed (NT: 2 metüül rühma) kasuta vastavat arvu näitavat eesliidet (di, tri jne) Isomeerid on ained, mis koosnevad ühesugustest aatomitest (on sama summaarne valem) kuid omavad erinevat ehitust. Sideme tüübid: Kovalentne kumbki aatomitest annab ühe elektroni molekulorbitaali tekkimiseks ühine orbitaal: Ideaalselt kovalentne side moodustub samaliigiliste, rangelt ekvivalentse elektronegatiivsusega aatomite vahel
Alkoholide mõiste ja struktuur Alkoholid on ained, mille molekulis süsiniku aatomi juures asuv vesinik on asendatud hüdroksüülrühmaga ( -OH). Ühendi struktuur on määratud aatomite paigutusega molekulis ja nendevaheliste sidemetega. Isomeeria Isomeerideks nimetatakse ühesuguse elementkoostise ja molekulmassiga, kuid erineva struktuuriga aineid. Isomeeria on ühesuguse koostise, kuid erinevate omadustega aine esinemine. Näiteks: Nimetus: Butaan Metüülpropaan ehk isobutaan Piiritus Eeter Keemistemp: -0,6 C -10,2 C 78 C 35 C PS Eetril ja piiritusel on sama brutovalem (C2H6O) Aine omadused on määratud aine struktuuriga. (nt. mida rohkem C aatomeid, seda kõrgem temp.; mida rohkem hargnenud ahel, seda madalam keemistemp.) Alkoholide füüsikalised ja keemilised omadused Füüsikalised omadused: Kuna hüdroksüülrühma vesinikul on positiivne osalaeng, võib ta hästi osaleda ves...
Kordamisküsimused: polümeerid 1. Selgitada mõisted : polaarne kaksikside mittepolaarne kaksikside - küllastumata ühend - ühendid, kus süsiniku aatomite vahel esineb kahekordne side ehk kaksikside või kolmekordne side ehk kolmikside küllastunud ühend süsivesink, mis ei sisalda kordseid sidemeid polümeer ühend, mille molekul koosneb kovalentsete sidemetega seotud korduvatest struktuurühikustest elementaarlülidest. polümerisatsiooniaste arv, mis näitab elementaarlülide arvu polümeeri molekulis monomeer madalamolekulaarne ühend, mis võib osaleda polümerisatsiooniprotsessis liitumispolümerisatsioon - seisneb monomeeride järjestikus liitumises polükondensatsioon kõrgmolekulaarse ühendi moodustumine, mis kulgeb mitmefunktsionaalsete ühendite omavahelisel reageerimisel vee eraldumisega polümeeri elementaarlüli - homopolümeer polümeer, mis koosneb ühesugustest elementaarlülidest kopolümeer polümeer, mis koosneb erisugustest el...
Alkaanide isomeeria on tingitud süsinikuahela erinevast kujust – nn ahelaisomeeria. Isomeeride valemite koostamine 1) hargnemata ahel 2) peaahel 1 võrra lühem 1 kõrvalharu (erinevates kohtades) 3) peaahel 2 võrra lühem a) kõrvalharuks 2 metüüli b) kõrvalharuks 1 etüül 4) peaahel 3 võrra lühem a) kürvalharuks 3 metüüli b) kõrvalharuks 1 etüül ja 1 metüül c) kõrvalharuks propüül ja 1 isopropüül jne 4. Asendatud alkaanid Asendatud alkaanides on süsivesinikahelas vesiniku aatom asendatud heteroaatomit sisaldava polaarse rühmaga (funktsionaalse rühmaga). nt −Hal, −OH, −NH2 Asendatud alkaanid on alkoholid, amiinid, halogeeniühendid. Struktuuri analüüs: 1) tüviühend; 2) asendusrühmad; 3) tüviühendi süsiniku nummeradamine.
ALKOHOLID Alkoholid on ühendid, mis sisaldavd hüdroksüülrühma (-OH rühma). Nimetuse lõpp ool. CH3CH2OH etanool ehk etaan-1-ool (piiritus 96%-98%, absoluutne alkohol 100%) OHCH2CH2OH etaan-1,2-diool ehk 1,2-etaandiool CH3OH metanool ehk puupiiritus CH2CH2CH2 propaan-1,2,3-triool ehk glütserool OH OH OH ALKOHOLIDE FÜÜSIKALISED OMADUSED Alkoholi molekulis on hapniku side süsiniku ja vesinikuga polaarne. Tekib laengu jaotus (joonis 1). Hapniku aatomil on väisel elektronkihil kaks vaba elektronpaari. Seetõttu on alkoholi molekulid võimelised moodustama omavahel vesiniksidemeid (joonis 2). H H H + - + + - + - + 2 2 2 H--C--O--H H--C--O···H--O--C--H H H H H Joonis 1 Joonis 2 Vesinikside on tugevam kui ...
Toidu lisaained R.Vokk Terminid · Toidu lisaaine on aine, mida lisandatakse kavatsuslikult toidule tehnoloogilises protsessis, et muuta toidu sensoorseid omadusi, säilivust ja kvaliteedi püsimist. Tavaliselt üksikuna ei kaubastata. · Toidulisand on tavatoidule lisaks mõeldud toitainete kontsentraadid (looduslikud segud või ainete segud), mida tarbitakse toidule lisaks. Toidu seadusandlus · Väljaandja : Vabariigi Valitsus · Akti või dokumendi liik : määrus · Teksti liik : terviktekst · Redaktsiooni jõustumise kpv. : 01.04.2008 · Redaktsiooni kehtivuse lõpp : Hetkel kehtiv TOIDUS LUBATUD LISAAINETE LOETELU JA PIIRNORMID TOIDUGRUPPIDE KAUPA, LISAAINETE KASUTAMISE TINGIMUSED JA VIISID NING LISAAINETE MÄRGISTAMISE JA MUUL VIISIL TEABE EDASTAMISE ERINÕUDED JA KORD · Vastu võetud Vabariigi Valitsuse 7.03.2000. a määrusega nr 81 (RT I 2000, 23, 131), jõustunud 31.03.2000. · ...
taandamine ja NADHP produtseerimine); c) valgusest sõltumatud protsessid (Calvin-Bensoni tsükkel) toimub stroomas; d) vee oksüdatsioon toimub tülakoidides ehk luumeni siseosas. 4.Klorofülli molekuli ehitus kujutatud loeng 20 salid 11. Sarnane heemile, st *porfüriin, *tsentris Fe2+ asendatud Mg2+-ga, *mis kordinatiivselt seotud nelja N aatomiga, *II tsükli juures kas metüül või aldehüüdrühm, *V tsükkel on lisa tsükkel, *IV tsüklis o üks kaksikside taandatud ja juurde liitunud pikaahelaline fütüülrühm, *aromaatsus muudab klorofülli efektiivseks nähtava valguse neelajaks, *tasapinnaline. 600 700 nm juures toimub klorofülli neeldumine; karotenoidid 400 - 500 nm. 5.Abipigmendid laiendavad veelgi neeldumisriba sellistel spektritel, kus klorofüllid ei neela.