molekulid, kristallid, mis on energeetiliselt püsivamad. Keemilise sideme tekkimisel vabaneb alati energia ja tekkinud aine osakesed on püsivamad, kui lähteaine osakesed. 2) Mittepolaarne kovalentne side (millisel juhul tekib; osata näidata selle tekkimist täpp skeemina ja ruutskeemina) Mittepolaarne kovalentne side- tekib ühe ja sama mittemetalli aatomi vahel (N2, H2, O2). Ühine elektronpaar kuulub võrdselt mõlemale aatomile. 3) Polaarne kovalentne side(millisel juhul tekib; osata näidata selle tekkimist täpp skeemina ja ruutskeemina) Polaarne kovalentne side- tekib erineva mittemetalli aatomite vahel (HCl; H2O). Ühine elektronpaar on tõmmatud elektronegatiivsema elemendi aatomi poole. 4) Iooniline side (millisel juhul tekib; osata näidata selle tekkimist täpp skeemina ja ruutskeemina) Iooniline side- tekib metalli ja mittemetalli aatomi vahel. Mittemetalli
Keemia KT Halogeeniühendid Mõisted: Halogeen Halogeenid on tugevad oksüdeerijad, sest nende aatomite välisel elektronkihil on puudu üks elektron stabiilsest oktetist. Halogeeniühend Orgaanilised ühendid, kus süsiniku aatom on seotud halogeeni aatomi või aatomitega. Enamasti vedelikud või tahked, harva gaasid. Veest raskemad, hüdrofoobsed. Mürgised, kerglenduvad on narkootilise toimega. Polaarne kovalentne side Elektronpaar, mis seob süsiniku ja halogeeni aatomit, mis on tõmmatud elektronegatiivsema aatomi (halogeeni) poole. Elektronegatiivsus Suurus, mis iseloomustab aatomi suhtelist võimet siduda endaga molekulis või keemilises ühendis elektrone. Osalaeng Elektrontiheduse nihkumine polaarsel sidemel. Nukleofiil Sageli anioon ja alati on ta osake, millel on vaba elektronpaar. Elektrofiil Sageli katioon, positiivne ja alati on tal tühi orbitaal.
Keemiline side on vastastiktoime aatomite vahel molekulides ja ioonide vahel kristallides. Tekib aatomi väliskihi elektronide abil. - osalaeng (väike delta) - Suur delta Keemilise sideme tüübid: 1) Kovalentne side a)polaarne b)mittepolaarne 2)iooniline side 3)metalliline side 4)vesinikside Kovalentne side on ühise või ühiste elektronipaaride abil moodustunud side. Polaarne kov. Sideme korral seob üks aatomitest ühist elektronpaari tugevamini, mistõttu aatomitel tekivad vastasmärgilised osalaengud. Polaarne side: NO2, CO2, CH4 2 mittemetalli. Mittepolaarse kov. Sideme korral on ühine elektronpaar jaotunud võrdselt mõlema aatomi vahel, sest mõlemad aatomid tõmbavad elektronpaari sama tugevusega. Mittepolaarne side: O2, Br2, C- üks aine, Vesinikside on (iselaadne molekulide vaheline side) keemiline side, kus ühe molekuli vesiniku
10. Iooniline side tekib metalli ja mittemetalli seondumisel. 11. Ioonvõre moodustavad kristallivõre keskmetes asuvad ioonid. Ioonvõre hoiab koos ioonne side. 12. Iooniline side on vastasmärgiliste laengutega ioonide vahel esinev tõmbejõud ioonkristallis. 13. Ioonsed ained on kõvad, kuid haprad, neil on kõrge sulamistemperatuur, nad on head elektrijuhid sulatatult, lahustuvad vees küllaltki hästi. 14. iooniline side KF, Na2O, BaCl2 sest koos on metall + mittemetall polaarne side NO2, CO2, CH4 sest koos on kaks mittemetalli mittepolaarne S8, O2, Br2, C sest on ainult üks aine 15. Vesinikside on täiendav side, mille tugevalt positiivse osalaenguga vesiniku aatom saab moodustada negatiivse osalaenguga elektronegatiivse elemendi aatomiga. 16. Vesinikside on oluliselt nõrgem kui kovalentne side. 17. Jää tihedus on väiksem kui vee tihedus, sest jääs tekib vee molekulidest korrapärane struktuur,
Mittepolaarne kovalentne side esineb mittemetalliliste elemendi aatomite vahel. Polaarseks kovalentseks sidemeks nimetatakse kovalentset keemilist sidet, kus aatomeid siduv ühine elektronpaar kuulub rohkem ühe aatomi valdusesse. Seetõttu tekivad molekulil vastaslaenguga poolused. Osalaengud tähistatakse + ja . Negatiivse osalaengu omandab see aatom molekulis, mis tõmbab ühist elektronpaari enda poole tugevama tõmbejõuga. Polaarne kovalentne side esineb mitme erineva mittemetalli aatomite vahel. Elektronnegatiivsuseks nimetatakse keemilist sidet iseloomustavat suhtarvu, mis arvestab aatomi võimet tõmmata enda poole elektrone. Elektronnegatiivsuse aluseks on võetud Liitiumi elektronnegatiivsus (1). Mida suurem on antud aatomi elektronnegatiivsus, seda rohkem on ühine elektronpaar tõmmatud antud aatomi poole.
PÕLLUMAJANDUS põllumajandus eri kliimavöötmetes eeldused põllumajandusega tegelemiseks kliima temperatuur vegetatsiooniperioodi pikkus sademed ja nende aastane jaotus sademete ja aurumise vahekord mullad keda ja mida kasvatada põllumajanduse otstarbekus polaarne kliima polaarne kliima kliima vegetatsiooni perioodita mullad ei kujune põllumajanduslik tegevus ainult kunstlikes tingimustes (kasvuhooned) lähispolaarne kliima lähispolaarne kliima lühike vegetatsiooniperiood mullad õhukesed ja õrnad rändkarjakasvatus rohumaadel paraskliima A B A B B
gradiendi suunast) põhjapoolkeral paremale, lõunapoolkeral vasakule. 3) mandrite ja ookeanide ebaühtlane jaotus Maismaa soojeneb kiiremini kui vesi, vesi jahtub aeglasemalt kui maismaa. Ebaühtlase soojenemise ja jahtumise tõttu tekivad õhuvoolud maismaa ja veekogude vahel. Üldise tsirkulatsiooni ehk üldise õhuringluse võib jagada kolme ossa: 1) troopiline ehk passaatide õhuringlus 2) keskmiste laiuste (parasvöö) õhuringlus 3) polaarne õhuringlus 1) TROOPILINE ÕHURINGLUS · Suhteliselt kitsas ekvatoriaalses vööndis on õhurõhk kogu aasta madal ja puhuvad nõrgad muutliku suunaga tuuled. · Ekvaatori kohal kujuneb madala õhurõhuga vöönd, sest maa ja vesi soojenevad tugevasti. · Tekivad intensiivsed tõusvad õhuvoolud (soe õhk hõre ja kerge, madal rõhk). · Tõustes õhk jahtub, tiheneb ja tema võime veeauru siduda väheneb. Veeaur hakkab kondenseeruma, tekivad sademed.
sest sealne kliima on niiske. Kõrbemullad on väheviljakad ja ei anna saaki. Haritavat maad ca 300 miljonit hektarit. Parasvööde Okasmetsavööndis põllumajanduslikku maad vähe (halvad mullad ja vahel ka igikelts). Lehtmetsade ja rohtlate vööndis on aga suurimad põllumajanduslikult kasutatavad maa-alad. Seal on soojem, niiskem ja paremad mullad. Lähispolaarne Seal on ainult põhjapõtrade karjamaad ja niidud, igikelts. Polaarne Igasugune põllumajanduslik tegevus on võimatu. Segatalud- põllumajandustalu, kus kasvatatakse erinevaid põllukultuure ja peetakse loomi oma tarbeks, kuid toodangu ülejäägid (mõni toode) lähevad müügiks. Kõrgeltarenenud riikides on segatalude arengujärk enamasti läbitud. Arengumaades, kus viiakse läbi agraarreforme, on need vägagi iseloomulikud Hiigelfarm ehk spetsialiseeritud suurtalu- moodne kõrgtootlik taluvorm, kus on spetsialiseeritud enamasti vaid ühele tooteliigile
Eksotermiliste reakts ( sidemete tekkel, osakesed lähevad üle püsivasse olekusse ja energia eraldub). enargia eraldub, endotermilistes reakts.( sidemete katkemisel, tuleb kulutada energiat ja tekkinud osakestel on ebastabiilne olek) Energia neeldub. KOVALENTE SIDE- aatomite vaheline side, mis tekib ühise elektronpaari abil. MITTEPOL. KOV. SIDE- esineb sarnaste mittemetalliliste elementide aatomite vahel. H 2O, CL2, O2, Br2. POLAARNE KOV. SIDE- esineb erinevate mittemetalliliste elementide aatomite vahel. HF, HCL, SO 3, H2O. ELEKTRON.- isel. Elemendi aatomi võimet siduda elektrone. RÜHMAS En kahaneb, siis aatom meelsasti loobub väliskihis olevatest elektronidest. PERIOODIS » En kasvab, siis aatmid meelsasti liidavad väliskihti elektrone. POLAARNE AINE koosneb polaarsetest molekulidest. HF, HCl. MITTEPOL. AINE- ta koosenb mittepolaarsetest molekulidest. Cl2, H2
Keemiline side on ühine elektronpaar Sideme tekkeenergia on ühendi püsivuse mõõt Aatomorbitaalide kattumisel tekib molekulorbitaal Elektronegatiivsus (X) iseloomustab jõudu,millega aatom tõmbab enda poole sidemeks olevaid elektrone. Elektronegatiivsus kasvab perioodilisustabelis noolega näidatud suunas. Sarnaste elementide (X<0,4) vahel tekib kovalentne side · Lihtainetes mittepolaarne kovalentne side HH NN · Liitainetes polaarne kovalentne side - O=C+=O- O- + H H+ Vastandite vahel (X >1,9) tekib iooniline side Na+ Cl:- Metalliline side metallides (Na, Ca, Al, Fe, Cu jne...) Doonor-aktseptorside e. koordinatiivne side :NH3 + H+ NH+4 Vesinikside on doonor-aktseptorsideme erijuht Vesinikside on molekulide vaheline side või molekuli üksikute osadevaheline side (n valgu
Kliimavöötmed Sirje Rits Juhendaja Marika Anissimov Kliimavöötmed Põhivöötmed Ülemineku - ehk lähisvöötmed Polaarne arktiline antarktiline Lähispolaarne Parasvööde Troopiline Lähistroopiline Ekvatoriaalne Lähisekvatoriaalne Ekvatoriaalne Päike kõrgel Temperatuur 25 °27° Õhk niiske Palju sademeid südapäeval äike Liigirikkad metsad Ekvatoriaalne kliimavööde Kliimadiagramm Troopiline kliimavööde Päike kõrgel 20° 32°
2) Maa telg on kaldu orbiidi suhtes Ekliptika-tasand gloobus KLIIMAVÖÖTMED KLIIMAVÖÖTMED Tasandikel laiusvööndilisus Mäestikes kõrgusvööndilisus Kliimavöötmele on iseloomulikud kindlad õhumassid ( temperatuuri- ja sademetereziim) sarnane õhuringlus, kindlad tuuled ühesugune aastaaegade vahetumise kord Kliimavöötmed Põhivöötmed Ülemineku - ehk vahevöötmed Polaarne arktiline antarktiline Lähispolaarne Parasvööde Troopiline Lähistroopiline Ekvatoriaalne Lähisekvatoriaalne Põhikliimavöötmed Põhikliimavöötmes on aastaringselt ühesugune õhumass Ekvatoriaalne õhumass Troopiline õhumass Parasvöötme õhumass Arktiline ja antarktiline õhumass Iseloomusta õhumassi põhiomadusi temperatuur, sademed seos õhuringlusega
322 g/mol- 46 g/mol= 276 g/mol n= m/M= 48,3 / 276 = 0,175 mooli on ülejäänud soolas kui pole naatriumit ja naatriumi ioonide arvu saame kui 0,175- 0,15= 0,025 mol Vastus: Naatriumi ioonide arv on 0,025 mol 3. Määra keemiliste sidemete tüüp järgmistes ühendites CO2 mittepol. kovalentne KCl iooniline H2 mittepol. kovalentne NaF iooniline side Cl2 mittepol. kovalentne CH3Cl mittepol. kovalentne NH3 kovalentne polaarne HCl kovalentne polaarne K2O iooniline SiH4 kovalentne polaarne S8 mittepol. kovalentne Li metalliline H2O kovalentne polaarne CaF2 iooniline Metall + mittemetall = kovalentne polaarne Aktiivne metall + aktiivne metall = iooniline Metall lihtainena = mittepol. kovalentne Metall = metalliline 4. On vaja valmistada 0,25 dm3 20%-list CaCl lahust (tihedus = 1,18 g/cm 3). Mitu g tahket CaCl, mis sisaldab 12% niiskust, tuleb võtta selle lahuse valmistamiseks ning mitu cm3 on vaja juurde lisada vett
Aatom aineosake, mis koosneb aatomituumast ja elektronidest; molekuli koostisosa. Molekul molekulaarse aine väiksem osake, kovalentsete sidemetega seotud aatomite rühmitus Keemiline side aatomite- või ioonidevaheline vastasikmõju, mis seod nad molekuliks või kristalliks Kovalentne keemiline side aatomitevaheline keemiline side, mis tekib ühiste elektronipaaride moodustumisel Polaarne kovalentne side kovalentne side erineva elektronegatiivsusega aatomite vahel, sidet moodustavatel aatomitel tekivad seejuures erinimelised osalaengud. Mittepolaarne kovalentne side kovalentne side, mille ühine elektronipaar kuulub võrdselt mõlemale sidet moodustavale aatomile; esineb võrdse elektronegatiivsusega aatomite vahel Iooniline side ioonidevaheline keemiline side, mis tekib vastasmärgiliste laengutega ioonide tõmbumise tõttu.
vähe sademeid, passaadid. 2 aastaaega(palav, soe) Lähistroopiline: kuiv, päikesepaisteline suvi passaadid, vihmane talv läänetuuled.sademeid aurumisest vähem, Parasvööde: mereline: sajab palju tempi kõikumine väike Parasvööde: mandriline: temp. amplituudi kõikumine surre, vähem sademeid,. Lähispolaarne: lühike suvi, valgusküllane jahe ja niiske, läänetulled . Talv pikk, külm lumevaene, tugevad tuuled, polaarsed idatuuled Polaarne: väga külm, vähe sademeid, maapind aasta läbi jää ja lume all. polaarsed idatuuled, 2 aasaaega. Tsükloni mõju kliimale: Kõrgrõhkkond: ala, mille kohal õhurõhk on kõrgem kui naaberaladel, mille ümber esineb päripäeva pöörlev õhukeeris ja mile keskel esinevad laskuvad õhuvoolid. >Ilm on selge tuulevaikne kuiv. . Antitsükloni mõju kliimale: Madalrõhkkond ala, mille kohal õhurõhk on madalam
Seda moodustavad: a)Vesiniku aatom b) Kloori aatom c) Hapniku aatom 8. Kordne side on keemiline side mis tekib kahe aatomi vahel mitme ühise elektronpaari abil. 9. Täppskeemid 10. Mittepolaarne kovalentne side tekib ühesuguste mittemetalli aatomite vahel nt: 11. Elektronegatiivsus näitab keemilise elemendi võimet tõmmata keemilises sidemes enda poole ühist ekektronpaari. Elektronegatiivsus suurendab tabelis alt üles ka vasakult paremale. 12. Polaarne kovalentne side tekib erinevate mittemetalli aatomite vahel. 13. Polaarne aine aine, mis koosneb polaarsetest molekulidest. Mittepolaarne aine aine, mis koosneb mittepolaarsetest molekulidest Polaarsed ained lahustuvad paremini polaarsetes lahustites. Mitte- polaarsed ained mittepolaarsetes lahustites. Molekuli polaarsus sõltub: a) sidemete polaarsusest b) sidemete paiknemisest molekulis 14
Harjutused ( aatomi ehitus, keemiline side ) 1 Selgitage järgmiste mõistete sisu: anioon , katioon, mittepolaarne kovalentne side, polaarne kovalentne side, polaarne aine (molekul), ainehulk, molaarruumala, elektronskeem, elektronvalem, ioonivõre, molekulivõre, aatomivõre, metallivõre, iooniline side, vesinikside 2. Täitke järgnev tabel Max Kõrgem Min Naatriumi- Element Np Nn elektronskeem elektronvalem o.-a. oksiid o.-a. ühend Al . .
a+b(100kJ)=c+d(160kJ) *H = 160-100= 60kJ, hinemis rekatsioonid on vadvalt eksotermilised,sidemete loomine ja lagunemine on endotermilised. * kovalantne side- aatomeid seob hine elektronpaar:-osalevad ainult vliskihi elektronid,mis on paardumata. 1) ksikside sama liiki aatomite vahel. H+H=(HH),H:H......H+Cl=H:CL-igalpool mber :...... H+O+H= HOH : 2)kordsed sidemed :N:+N: N=N,N2..... kov sideme polaarsus kov,mittepolaarne side? H-H,O=O, N(3x-)N vrdsed elektronkihid polaarne kovalntne side H Cl elektrinegatiivsus: vasakult paremale ja alt les.. F(4,0) polaarsed ja mittepolaarsed ained: polaarne aine koosneb polaaarsetest molekulidest. mittepolaarne aine koosenb ka mittepolaarsetest molekulidest. H2;O2,Cl2;N2 kui molekulis on polaarsed sidemed ja nad asuvad hel sirgel vesi on polaarne aine. Aatomitel peab olema suur elektronegatiivsuste erinevus. 1,9 (suurem vrdne) IA ja IIA- VI ja VII NaCl;LiF;MgBr2;CaCl2;Na2O-kik soolad on joonilise ehitusega.
ning lähteainetest saavad saadused ja vastupidi. Millise soojusefektiga on keemilise sideme lagunemine? Keemilise sideme lagunemine on endotermiline reaktsioon ehk soojus neeldub Kas reaktsioon on ekso või endotermiline? Vastus: Reaktsioon on eksoter miline. Määra keemilise sideme liik! 1)iooniline 2) mittepolaarne kovalentne 3)Polaarne kovalentne 4) mittepolaarne kovalentne 5) iooniline 6)polaarne kovalentne Kujuta struktuurvalemite abil vesiniksidemete teket kolme molekuli vahel. Kuidas mõjutavad molekulidevahelised vesiniksidemed aine keemistemperatuuri? Põhjendus. Vastus : molekulidevahelised vesiniksidemed tõstavad aine keemistemperatuuri. Põhjus selles, et tekkinud sidemete lõhkumiseks läheb vaja rohkem energiat, seega tõuseb ka keemistemperatuur. JOONIS ÜLESANNETE LÕPUS Kui suur ruumala on normaaltingimustel 20 moolil lämmastikul ? n=20 mol
Taimestik on kõik taimed kokku. Taimkate on taimekoosluste kogus (mets, niit). Põhikliimavöötmetes on aasta läbi üks õhumass (polaarne e. arktiline, parasvööde, troopiline, ekvatoriaalne). Vahekliimavöötmetes on pool aastat üks, pool aastat teine õhumass (lähispolaarne, lähistroopiline, lähisekvatoriaalne. Poolustelt ekvaatorini tekivad erinevad taimkattetüübid, sest taimed on kahastunud erinevate ilmastikutingimustega. Loodusvööndis levib vastavalt kliimale, mullale, pinna ehitusele ja veestikule iseloomulik taimkattetüüp. Muld on maakoore pindmine kobe kiht
Jäävöönd on pooluseid ümbritsev ala, kus maapind on kogu aasta jooksul kaetud lume ja jääga, polaarne kliima. Jääkõrb-maapind liustikuga. Külmakõrb-külmad kaljused alad. Jäämagi-mandriliustiku osa. Antarktika-Antarktise manner ja seda ümbritsev ookean koos saartega kuni 60. lõunalaiuseni. Arktika-põhjapoolust ümbritsev P-J koos euraasia ja P-A kitsa igikeltsaga kautud rannikuala. 1819-21 Bellinghausen 1. Nägi Antarktist. 1842-25 Middendorff Põhja-Siber. 1888. Fritjof Nansen. 1909. Robert Peary 1. põhjapoolus. 1911. Amundsen 1. Lõunapoolusele 2. Robert Peary.
energiaga ja ebapüsivad, ühinedes saavad nad püsivaks ja stabiilseks. 2. Elektronoktett kui aatomi väliskihis on 8 elektroni, siis moodustub elektronoktett; Termokeemilised võrrandid reaktsioonivõrrandid, milles märgitakse ära reaktsiooniga kaasnev soojuseffekt (H); Soojusefekt soojuse eraldumine või neeldumine mingi protsessi käigus; Elektronegatiivsus elementide võime tõmmata enda poole elektrone kovalentses sidemes; Polaarne aine - koosneb polaaarsetest molekulidest; Mittepolaarne aine - koosneb mittepolaarsetest molekulidest; Kordne side - keemiline side, mis tekib kahe aatomi vahel mitme ühise elektronpaari abil; Iooniline side - side erinimeliste ioonide vahel; Eksotermiline reaktsioon - keemiline reaktsioon, mille käigus eraldub soojust: Endotermiline reaktsioon - keemiline reaktsioon, mille käigus neeldub soojust. 3. VIIIA rühma elementidel esineb elektronoktett. Aatomid püüava
omavahel seotud keemiliste sidemetega. Molekule nendest ainetes ei esine. Eksotermiline protsess lähteainete energia on suurem kui saaduste energia (ühinemisreaktsioonid) Endotermiline protsess lähteainete energia on väiksem kui saaduste energia (lagunemisreaktsioonid) Kovalentne side moodustub aatomite vahel ühis(t)e elektronpaari(de) abil. Valents aatomi omadus keemiliselt siduda teisi aineid Kordne side keemiline side, mis tekib kahe aatomi vahel mitme ühise elektronpaari abil. Polaarne kovalentne side tekib erinevate elementide aatomite vahel. Kui üks element on märgatavalt mittemetallilisem, tõmbab ta ühist elektronpaari tugevamini enda valdusesse. Ühine elektronpaar on tõnnatud elektronegatiivsema elemendi poole. mittepolaarne kovalentne side ühine elektronpaar on jaotunud võrdelt mõlema aatomi vahel. Iooniline side ioonide vahel tekkinud keemiline side. Metalliline side metalliioonide ja liikuvate ühistatud elektronide vastastikune tõmbumine metallides.
Elektrostaatiline induktsioon-nähtus kus vabad laengud kogunevad juhi pinnale.Juhi sees elektriväli puudub. Dielektrikul puuduvad vabad laetud electronic Polaarne die. ´+ ja - laengu asukohad ei ühti Mittepolaarne die. + ja - laengu asukohad ühtivad. Dielektriku dielektriline läbiatavus....näitab,mitu korda väli dielektrikus on väiksem elektriväljas vaakumis .Valem.... Välise elektrivälja mõjul kvartskristalli mõõtmed perioodiliselt vähenevad.KVARTSKELL Elektrimahutavus-nimetame ühe juhi laengu ja juhtide potensaalide vahe suhet. Valem+tähis Iseloomustab juhtide võimet saleslady elektrilaengut.
Mittepoolarne aine-mittepolaarsetest molekulidest koosnev aine Mittepolaarne kovalentne side-kovalantne side milles ühine elektronipaari kuulub võrdselt mõlemale sidet moodustavale aatomile Molekulaarne aine-molekulidest koosnev aine Molekulidevaheline side-suhteliselt nõrk side molekulide vahel mis hoiab molekule tahkes ja vedelas aines koos Molekulvõre-kristallvõre kus sõlmpunktides asuvad molekulid Oksiid-kahest elemendist koosnev keemiline ühend millest üks on hapnik Polaarne aine-polaarsetest molekulidest koosnev side Polaarne molekul-molekul milles positiivse ja negatiivse laengu keskmed ei lange kokku mistõttu molekuli üks osa on positiivse ja teine negatiivse laenguga Polaarne kovalantne side-kovalantne side erineva elektronegatiivsusega aatomite vahel sidet moodustavatel aatomitel tekivad seejuures erinimelised osalaengud
molekulide vahel (võrreldes keemilise sidemega) Kovalentne side kõige levinum ja olulisem keemilise sideme tüüp, moodustub aatomite vahel ühe või mitme ühise elektronpaari abil. Valents side, mis näitab, mitu elektronpaari saab aine teisega moodustada Kordne side keemiline side, mis tekib kahe aatomi vahel mitme ühise elektronpaari abil Osalaeng positiivse või negatiivse laengu ülekaal ? Polaarne kovalentne side üks aatomitest seob elektroni endaga tugevamini, mistõttu aatomitel tekivad vastasmärgilised osalaengud Mittepolaarne kovalentne side ühine elektronpaar on jaotunud võrdselt mõlema aatomi vahel. Vesinikside täiendav side, mille tugeva positiivse osalaenguga vesiniku aatom saab moodustadanegatiivse osalaneguga hapniku, lämmastiku või fluoriga vms. Iooniline side ioonidevaheline keemiline side, mis tekib vastasmärgiliste laengutega ioonide tõmbumise tõttu.
· Molekulaarne aine · Mittemolekulaarne aine molekulidest koosnev aine. · Keemiline side aatomite või ioonide vaheline side molekulaarses aines. · Kovalentne side ühiste elektronpaaride jagamisel aatomite vahel tekkiv side. · Mittepolaarne kovalentne side kovalentne side, kus ühine elektronpaar on mõlemal elemendil võrdselt. · Polaarne kovalentne side kovalentne side, kus ühine elektronpaar on ühe elemendi poole rohkem tõmmatud. · Valents näitab ühe aatomi poolt moodustatud kovalentsete sidemete arvu. · Üksikside aatomite vaheline keemiline side, mille moodustab üks ühine elektronpaar. · Kaksikside aatomite vaheline keemiline side, mille moodustavad kaks ühist elektronpaari.
Kontrolltöö Keemiline side 1. Täida lüngad. o ...................... side moodustub metalli ja mittemetalli vahel. o Metallide vahel moodustub ....................... side, seega mittemetallide vahel aga ........................ side. o ..................side on alati täiendavaks sidemeks, mis esineb molekulide vahel. 2. Määra polaarsus. Polaarne märgi P-ga ja mittepolaarne MP-ga. o O=O o O=C=O o HOH o O=S=O o Cl Cl H | o HCH | H 3. Täida tabel. Elemendid Ioonide valemid Ioonide arvude suhe Aine valem K+ I - 1:1 Na ja P
ruutskeem (1.4. perioodi elementidel); aatomiehituse seos keemilise elemendi asukohaga perioodilisustabelis; elementide metalliliste ja mittemetalliliste omaduste (elektronegatiivsuse) muutus perioodilisustabelis (A-rühmades; keemiliste elementide tüüpiliste oksüdatsiooniastmete seos aatomiehitusega, tüüpühendite valemid; keemilise sideme energeetiline põhjendus; ekso- ja endotermilised reaktsioonid; mittepolaarne ja polaarne kovalentne side; osalaeng; iooniline side; vesinikside; metalliline side; ainete omaduste sõltuvus keemilise sideme tüübist; molekulidevaheliste jõudude ja keemilise sideme tugevuse võrdlus. 2. ANORGAANILISTE ÜHENDITE PÕHIKLASSID. ELEKTROLÜÜTIDE LAHUSED: oksiidid, happed, alused ja soolad, nende nomenklatuur, keemilised omadused ja saamisviisid; elektrolüüdid ja mitteelektrolüüdid; tugevad ja nõrgad elektrolüüdid; lahuse happelisuse
Oksiidid Oksiidid on keemilised ained, mis koosnevad kahest elemendist, millest üks on hapnik, ning mille molekulis hapnikuaatomite vahel puudub keemiline side. Metallioksiidid on reeglina aluselised ning neis esineb kas iooniline või kovalentne polaarne side. Mittemetallioksiidid on reeglina happelised ning neis esineb kovalentne polaarne side. Oksiidid tekivad kahe lihtaine vahelise redoksreaktsiooni käigus, milles hapnik käitub oksüdeerijana. Oksiide on mõningatel juhtudel võimalik saada ka metalli reageerimisel veega, nad tekivad ka paljude ebapüsivate ainete lagunemisel. Metallioksiidid on erineva värvusega tahked kristalsed ained. Üks tähtsamaid metallioksiide argielus on kaltsiumoksiid CaO ehk kustutamata lubi. Seda saadakse tööstuses lubjakivi lagundamisel kõrgel temperatuuril. Argielus puutume kokku veel
vaakum ning kihid ei saaks kraani pidi välja voolata. 4. Kas planaarkromatograafia on üldiselt kvalitatiivne või kvantitatiivne analüüsimeetod? Põhjenda. Planaarkromatograafia on üldiselt kvalitatiivne, kuna ainete eraldamise eesmärgiks on üksikute komponentide kättesaamine ehk aine olemasolu määramine, et nendega hiljem midagi edasi teha. 5. Kumb planaarkromatograafia faasidest (mobiilne või statsionaarne) oli antud töös polaarne ja kumb mittepolaarne? Planaarkromatograafias on statsionaarseks faasiks absorbendi õhuke kiht, milleks meil oli metall-lehele kantud silikageel ning kuna silikageel on suure polaarsusega ränidioksiid siis võib järeldada, et mobiilne faas oli siin juhul mittepolaarne. 6. Mida väljendab suurus Rf? Rf on kromatograafia kõige olulisem parameeter, mis sõltub aine jaotumisest liikuva ja liikumatu faasi vahel ehk jaotuskoefitsiendist. See näitab kromatograafilisel plaadil liikuva
Mittepolaarne Esineb ühe ja Aatomite vahele Tekib kovalentne sama mitte- tekib ühine mittepolaarn side metalse elektronpaar, mis molekul. elemendi kuulub võrdselt aatomite mõlemale vahel. aatomile. Polaarne Esineb mitme Aatomite vahele Tekib polaar kovalentne erineva mitte- tekib ühine molekul ehk side metalse elektronpaar, mis dipool, mis elemendi on tõmbunud sisaldab aatomite tugevama positiivseid
Mittepolaarne Esineb ühe ja Aatomite vahele Tekib kovalentne sama mitte- tekib ühine mittepolaarn side metalse elektronpaar, mis molekul. elemendi kuulub võrdselt aatomite mõlemale vahel. aatomile. Polaarne Esineb mitme Aatomite vahele Tekib polaar kovalentne erineva mitte- tekib ühine molekul ehk side metalse elektronpaar, mis dipool, mis elemendi on tõmbunud sisaldab aatomite tugevama positiivseid
3) Halogeen + alus sool + 4) Halogeen + sool sool + hape TASAKAALU MUUTUMINE EKSOTERMILISES REAKTSIOONIS, MÕJU REAKTSIOONIKIIRUSELE eksotermiline 1) t° (eksotermilise suunas?) kiireneb 2) p (väiksema moolide arvu suunas) aeglustub 3) lähteaine konsentratsioon kiireneb TASAKAALU MUUTUMINE ENDOTERMILISES REAKTSIOONIS 1) p ei muutu 2) t° 3) lähteainete konsentratsioon KEEMILISTE SIDEMETE LIIGID + SKEEMID POLAARNE KOVALENTNE SIDE 2) IOONILINE SIDE 3) MITTE POLAARNE KOVALENTNE SIDE AINETE LAGUNEMINE a) magneesiumnitraat b) ammooniumkarbonaat c) vask(I)hüdroksiid d) plii(IV)nitraat
Madal sulamis ja keemistemp. Ei lahustu vees,ei juhi elektrit,halb soojus juht. Aatomid,aatomvõre Tugev kovalentne Sulamis ja keemis temp. side Kõrge,vees ei lahustu,ei Polaarne juhi elektrit,ained on kovalentne tahked. side Molekulid,molekulvõre Molekulis on tugev Enamus on toa temp. kov. Side,molekulide Vedelad või vahel on nõrk gaasilised,vees
+ +17 + HCl molekulis tekib Cl aatomil negatiivne ja H aatomil positiivne osalaeng keemiline side kovalentne side iooniline side tekib ühiste elektronpaaride elektriline tõmbumine abil erinimeliste ioonide vahel mittepolaarne polaarne tekib ühesuguste mittemetalliaatomi tekib erinevate mittemetallide te vahel (näit. H2 aatomite vahel (näit. HCl molekulis) molekulis) Naatriumi aatom tuumalaeng +11 elektronkate kolmekihiline viimasel kihil üks +11 paardumata elektron metallid seovad väliskihi elektrone nõrgalt Kloori aatom kloori aatomi tuumalaeng on +17 17 elektronid paiknevad kolme kihina
· Mittemetallid-aatomite vahel on kovalentne side Liitained-koosnevad mitmest erinevast keemilisest elemendist · Ehituse põhjal Molekulaarsed ained- koosnevad molekulidest(mittemetallid,mittemetallioksiidid,happed,orgaanilised ained)Mittemolekulaarsed ained-koosnevad ioonidest või aatomitest(metallid,metallioksiidid,hüdroksiidid,soolad) 1. (aktiivne)metall +(aktiivne)mittemetall iooniline side 2. Mittemetall + mittemetall kovalentne polaarne side 3. Mittemetall lihtainena kovalentne mittepolaarne side 4. Metall lihtainena metalliline side 5. · Keemiline side-on mõõju,mis ühendab aatomid või ioonid molekuliks või kristalliks · Ioonvõre-võrest moodustavate osakeste (ioonide )vahel on tugev iooniline side,mistõttu ained on tahked ning kõrge sulamistemp ja keemistemp,haprad · Aatomvõre-moodustavate osakeste vahel on tugev kovalentne side,mistõttu ained on
Eksotermiline reaktsioon – soojuse (energi) eraldumisega kulgev keemiline reaktsioon. endotermiline reaktsioon – soojuse (energia) neeldumisega kulgev keemiline reaktsioon. Keemiline side – aatomite- või ioonidevaheline vastasmõju, mis seob nad molekulideks või kristallideks Kovalentne side – aatomitevaheline keemiline side, mis tekib ühise elektronpaaride moodustamisel osalaeng – iseloomustab elektrontiheduse nihkumist polaarsel sidemel. polaarne kovalentne side – kovalentne side erinevate elektronegatiivsusega aatomite vahel, sidet moodustavatel aatomitel tekivad seejuures erinimelised osalaengud. mittepolaarne kovalentne side – kovalentne side, milles ühine elektronpaar kuulub võrdselt mõlemale sidet moodustavatele aatomitele. Esineb võrdse (või väga lähedase) elektronegatiivsusega aatomite vahel. Vesinikside – täiendav side, mis tekib selliste molekulide vahele, mis sisaldavad F-O, O-H või N-H sidemeid.
Kõik liikuvad kehad põhjapoolkeral kalduvad otsesuunaga võrreldes paremale. Lõunapoolkeral vastavalt vasakule. -Osata õhumasside liikumist ekvaatori ja pooluste vahel iseloomustada..igat etappi. -Jugavool-troposfääri ülaosas länest itta puhuvate tuulte vöönd.Õhuvoolud kalduvad Coriolisi jõu tüttu. -Jugavoolude looked määravad tsüklonite ja antitsüklonite liikumise ja paiknemise. -Maakera troposääris valitsevad tuuled: polaarne idatuul,läänetuul,kidepassaat,kagupassaat,läänetuul,polaarne idatuul -lõunalaius,idapikkus jms korrata -Passaadid:püsivad tuuled ekvaatori ümbruses ja 30.laiuskraadide vahel. Ka lääne ja idatuuled on püsivad tuuled -Kohalikud tuuled:Mussoonid,Briisid,Föön,Bora,Tromb -N:Mussonid on tuuled,mis puhuvad suvel ja talvel vastupidistest ilmakaartest.Suvel:Niisked mussoonid. Talvel:kuivad mussoonid. Mis põhjustab erinevusI?Maismaa ja ookeani erinev soojenemine ja jahtumine erinevatel
Jää ja külmakõrb MARLEEN MÄEKALA KARIN-MARGARETH EPNER Asend Kliima Polaarne kliima Eristatakse 2 aastaaega Õhumassidest polaarne ja valdavad ida tuuled Lumi ja jää peegeldavad 90% päikesekiirgust tagasi atmosfääri Arktiline Talvel temperatuur kuni −40°C Suvel keskmine õhutemperatuur kuni +5°C Aasta keskmine sademete hulk kuni 250mm Tuule kiirus kuni 120 km/h Antarktiline Talvel keskmine õhutemperatuur mandri keskosas −60..−70°C, mererannikul on õhutemperatuur kõrgem – umbes −30..−35°C Suvel keskmine temperatuur
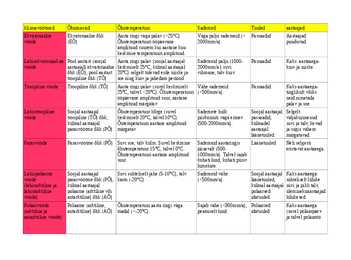
Lähispolaarne Soojal aastaajal Suvi suhteliselt jahe (5-10°C), talv Sademeid vähe. Soojal aastaajal Kaks aastaaega: vööde parasvöötme õhk (PÕ), karm (-20°C). (<500mm/a). läänetuuled, suhteliselt lühike (lähisarktiline ja külmal aastaajal külmal aastaajal suvi ja pikk talv, lähistarktiline polaarne (arktiline või polaarsed üleminekuaastaajad vööde) antarktiline) õhk (AÕ) idatuuled. lühikesed. Polaarvööde Polaarne (arktiline, Õhutemperatuur aasta ringi väga Sajab vähe (<300mm/a), Polaarsed Kaks aastaaega (arktiline ja antarktiline) õhk (AÕ) madal (<-20°C)
katioon positiivse laenguga ioon anioon negatiivse laenguga ioon eksotermiline reaktsioon keemiline reaktsioon, mille käigus eraldub soojust endotermiline reaktsioon keemiline reaktsioon, mille käigus neeldub soojust keemiline side -viis, kuidas kaks või enam aatomit või iooni on aines omavahel seotud kovalentne side ühiste elektronpaaride vahendusel aatomite vahele moodustuv keemiline side polaarne kovalentne side- elektronid mittepolaarne kovalentne side- ioonid ja aatomid vesinik side- täiendav keemiline side, mille moodustab ühe molekuli negatiivse osalaenguga elektronegatiivse elemendi aatom teise molekuli positiivse osalaenguga vesinikaatomiga iooniline side -vastasmärgiliste ioonide tõmbumine (metall <-> mittemetall) metalliline side- moodustub negatiivsete vabade elektronide ja positiivsete
(endotermiline protsess) - neeldub energiat (H>O - lagunemisreaktsioonid, fotosüntees Kovalentne side esineb molekulides mittemetalli aatomite vahel, aatomeid seovad ühised elektronpaarid. · Mittepolaarne kovalentne side - ühesuguste mittemetalli aatomite vahel - H2, Cl2, Br2, N2, P4 - ühised elektronpaarid kuuluvad võrdselt mõlemale aatomile - X=0 · Polaarne kovalentne side - erinevate mittemetallide aatomite vahel - H2O, HCl, H2SO4, SO2, P4O10 - ühised elektronpaarid nihkunud elektronegatiivsema elemendi poole - X<1,9 Elektronegatiivsus on elemendi võime siduda elektrone, mis sõltub tuuma laengust, aatomi raadiusest. - kasvab perioodis vasakult paremalt, rühmas alt üles Valents näitab sidemete arvu.
Mittepolaarne kovalentne side tekib ühe ja sama mittemetalilise elemendi aatomite vahele. Mõlemad aatomid mõjutacad ühist elektronipaari võrdse jõuga ja molekul on mittepolaarne (ei teki poolusi). Mittepolaarne kovalentne side esineb mittemetallides (lihtainetes!), näiteks HH, OO, NN. Kuna C ja H elektronegatiivsuste erinevus on tühine, siis loetakse ka nendevahelised sidemed mittepolaarseteks (näiteks süsivesinikes). Polaarne kovalentne side tekib erinevate mittemetalliliste elementide aatomite vahele. Tavaliselt tõmbab üks aatom ühist elektronipaari tugevama jõuga kui teine (elektronegatiivsused on erinevad, kuid mitte väga palju). Seepärast tekivad molekulis poolused. Osalaeng (väiksem elektroni laengust) iseloomustab elektrontiheduse nihkumist polaarsel sidemel (- või +). Negatiivse osalaengu omandab see aatom, mis tõmbab ühist elektronipaari rohkem enda poole
· Elektronegatiivsus - keemilist elementi iseloomustav suhtarv, mis arvestab aatomi võimet tõmmata · eksotermiline reaktsioon soojuse(energia) vabanemisega toimuv reaktsioon · endotermiline reaktsioon soojuse(energia) neeldumisega toimuv reaktsioon · kovalentne side aatomite vahel ühiste elektronpaaride kaudu moodustunud keemiline side · kovalentne mittepolaarne side side, milles mõlemad aatomid mõjutavad ühist elektronpaari võrdse jõuga · kovalentne polaarne side aatomeid siduv ühine elektronpaar on enam kui ühe aatomi valduses ja molekulide osadel on erinimelised osalaengud · iooniline side ioonide vahel tekkinud keemiline side metalliline side, · molekulaarne aine osakeste vahel olevad nõrgad molekulidevahelised jõud. Madal sulamis- ja keemistemperatuur, pehmed · mittemolekulaarne aine osakeste vahel tugevad keemilised sidemed. Kõrge sulamis- ja keemistemperatuur, kõvad 1
soojem kui Alpide föön.) · Selgitada moisteid Hadley tsirkulatsiooniring, polaarfront,Rossby lained- Hadley tsirkulatsiooniring- Üldine tsirkulatsioon on pohjustatud paikesekiirgusest ja selle ebauhtlasest jaotusest, seejuures voib öelda, et ohuliikumised saavad alguse ekvaatorilt, kus ohk touseb suurtesse korgustesse, hakkab siis jahtudes valguma pooluste suunas ja tekitab moneti suletud ringi (Hadley ring) Polaarfront-kitsas vöönd, kus saavad kokku kulm polaarne ja soe troopiline ohumass Rossby lained-Korgemas troposfaari kihis tekkivad uhtlases laanevoolus tihti ulatuslikud lained, mida nimetatakse Rossby laineteks. · Selgitada moisteid lainetsuklonid,ekvatoriaalne konvergentsivoond, jugavool- lainetsuklonid- hiiglaslikud ohukeerised, mis pidevalt tekivad, arenevad ja haabuvad ekv. Konvergentsivöönd- ekvaatori piirkond, kuhu koonduvad passaattuuled, kust ohk touseb korgele ning valgub pohja/louna suunas laiali
· hapniku valents on kaks (tema väliskihis on kaks paardumata elektroni ja kaks elektronpaari); · lämmastiku valents on kolm (tema väliskihis on üks elektronpaar ja kolm paardumata elektroni); · süsiniku valent on neli (tema väliskihis on tavaolekus üks elektronpaar ja kaks paardumata elektroni, ent ergastades neli paardumata elektroni, sest üks elektron liigub 2s-alakihilt vabale 2p-alakihi orbitaalile) IV. Kovalentse sideme polaarsus: mittepolaarne ja polaarne kovalentne side Kovalentne side moodustub peamiselt mittemetalliliste elementide aatomite vahel. 4.1 Kaks sama mittemetalli aatomit annavad kovalentse mittepolaarse sideme, sest elektronpaar võrdselt mõlema aatomi juures. Ei ole tekkinud molekuli osalaenguid. 4.2 Kui on tegemist kahe erineva elektronegatiivsusega mittemetalli aatomiga, siis moodustub tõenäoliselt kovalentne polaarne side. Nimelt tõmbab suurema elektronegatiivsusega
kordne side-keemiline side, mis tekib kahe aatomi vahel mitme ühise elektronipaari abil. elektronipaar- kaks vastassuunalise magnetväljaga elektroni, mis asuvad ühel orbitaalil, mooustades ühise elektronpilve. Molekulorbitaal-??? kovalentne mittepolaarne side- kovalentne side, mills ühine elektronpaar kuulub võrdselt mõlemale sidet moodustavale aatomile; esineb võrdse (või väga lähedase) elektronegatiivsusega aatomite vahel. kovalentne polaarne side- kovalentne side erineva elektronegatiivsusega aatomite vahel, sidet moodustades tekivad aatomitel seejures erinevad märgid. Elektronegatiivsus näitab keemilise elemendi aatomi võimalust tõmmata keemilises sidemes enda poole ühist elektronpaari. iooniline side- ioonidevaheline keemiline side, mis tekib vastasmärgiliste laengutega ioonide tõmbumise tõttu. Vesinikside- täiendav keemiline side, mille moodustab ühe molekuli negatiivse
kitsas eraldusvöönd kahe erinevate omadustega õhumassi D vahel (nt. külm ja soe, kuiv ja niiske) U võib olla statsionaarne või liikuda, viimasel juhul on kaldu S Õhumasside klassifitseerimine laiuskraadi järgi: M · Arktiline õhk A Põhja-Jäämere ümbrus A · Antarktiline õhk AA Antarktikas A · Polaarne õhk P parasvööde: 50-60°NS T · Troopiline õhk T 20-35°NS E · Ekvatoriaalne õhk E ekvaatori lähedal A kujunemiskoha aluspinna iseloomu järgi D · Mereline õhk - m kujuneb ookeani kohal U · Kontinentaalne õhk - c kujuneb mandri kohal S Peamised õhumassid M
Õhumassid: o Õhumass on ulatuslik õhukogum, mis on kujunenud ühesuguse aluspinna kohal ja on seetõttu ühesuguse temperatuuri ja niiskussisaldusega o Pooluste lähedal kujunevad külmad õhumassid, väikestel laiuskraadidel soojad õhumassid. o Õhumasside piirialal muutuvad õhuomadused Seal hakkab soojem ja kergem õhku tõusma Peamised õhumassid: o ekvatoriaalne (niiske), troopiline (kuiv & niiske), polaarne jaguneb kaheks antarktiline ja arktiline (kuiv & külm, parasvöötme (mereline külm, mandriline soe) Peegeldumine/neeldumine: o Aluspinna albeedo näitab pinnalt tagasi peegelduva ja pinnale langeva kiirguse suhet o Maapinnale jõudnud valgus peegeldatakse atmosfääri tagasi, kui pole pilvi, mis seda takistaks. (ka veepinnad ntks sood on väga peegeldavad) Sellepärast on kõrbel öösiti 0 kraadi ntks