Ch4 ehk metaan Lihtsain süsiniku ja vesiniku ühend. Leidub looduses, õhust kergem, ei lahustu vees ning on lõhna- ja maitsetu. Kasutatakse gaasilise kütusena. Segu õhust ja metaanist plahvatab kergesti. Aatomid seotud 4 kovalentse üksiksidemega. C keskel, Hd igas ilmakaares ümber. Metaan on teisisõnu maagaas. Tekib ka orgaanilise aine lagunemisel nt. Prügilates. Metaani põlemine Ch4 + 2 O2 --- Co2 + 2 H2O Mida suurem on oksüdatsiooniastme muutus, seda suurem on kütteväärtus. Selles võrrandis on süsiniku oa muutus 8 ja see on ka maksimaalne. Co ehk süsinik monooksiid ehk vingugaas Mittetäielik põlemine lõpeb vingugaasiga. Süsiniku oksüdatsiooniaste on siin 2. Co saab võimaluse korral oksüdeeruda edasi Co2ks. Co on neutraalne oksiid. Hapete ja alustega ta ei reageeri. Co2 ehk süsinik dioksiid Põlemise lõppsaadus.
Metaan ja kliima soojenemine Metaan (CH4) on kasvuhoonegaas. Metaani keemilised omadused ja reaktsioonid atmosfääris põhjustavad kasvuhooneefekti. Atmosfääris imab metaan maalt tulnud infrapuna kiirgust, mis pääseks muidu maailmaruumi, mistõttu tekib maa atmosfääri soojenemine. Metaani eraldub maapõuest iseeneslikult, samuti moodustuvad väga suured metaanikogused biosfääri elutegevuse kõrvalsaadusena. Seepärast ei ole kogu kasvuhooneefekt tingitud üksnes inimtegevusest
KEEMIA 1. Mõisted 1) süsivesinikud- keemilised ained, mille molekul koosneb ainult süsiniku ja vesiniku aatomitest. NT metaan- CH4 2) alkaanid- süsivesinik, mille molekul sisaldab ainult sigma-sidemeid. Nt: heksaan C6H14 3) alküülrühm- alkaanist tulenev asendusrühm. Nt. CH3- metüül 4) trivaalnimetus- aine (peamiselt ajalooline) nimetus, mis ei vasta nomenklatuuri reeglitele.Nt. Met(aan) 5) süstemaatiline nimetus- aine nimetus, mis on antud nomenklatuurireegleid järgides. Nt soogaas, süstemaatiline nimetus metaan(CH4)
KASVUHOONEEFEKT Kasvuhooneefekt · Kasvuhooneefekti olemasolu tõestas XX sajandi alguses Nobeli preemia laureaat Svante Arrhenius. · Ta näitas, et CO2 mängib olulist rolli atmosfääri peegelduva soojuskiirguse neeldumisel, mis põhjustabki atmosfääri soojenemise. · Looduslik nähtus · Hädavajalik maakera elustikule Svante Arrhenius Kasvuhooneefekti põhjustavad kasvuhoonegaasid · Veeaur · CO2 ehk süsinikdioksiid e. süsihappegaas · CH4 ehk metaan · N2O ehk lämmastikdioksiid e. naerugaas · O3 ehk osoon · Aerosool · freoonid Kasvuhoonegaasid · ... lasevad läbi Päikeselt Maale saabuva kiirguse, kuid püüavad kinni soojuse tagasipeegeldumise Maalt. · ~ 40 · Ilma kasvuhoonegaasideta atmosfääris oleks Maa keskmine temperatuur ligi 32° külmem, kui ta praegu on. · Probleem tekib siis, kui inimtegevuse käigus lendub atmosfääri liiga palju kasvuhoonegaase. Kasvuhoonegaasid
Parafiin ja polüetüleen on materjalid, mille kokkupuude toiduainetega on lubatud. Vedelate alkaanide veekogudesse sattumisel on paljudele organismidele kahjulikud (naftareostus). Õnneks leidub looduslikes veekogudes mikroorganisme, mis suudavad alkaane oksüdeerida. See puhastusprotsess toimub aga üpris aeglaselt. Pürolüüs on aine lagunemine kõrge temperatuuri toimel (krakkimine, isomeerimine). Alkaane kasutatakse nende suure põlemissoojuse tõttu kütusena. CH4 on peamine loodusliku gaasi koostisosa ning peamine gaas majapidamisgaasis. Propaani (C3H8) ja butaani (C4H10) isomeere kasutatakse vedelgaasis ehk balloonigaasis, mida saadakse nafta töötlemise kõrvalsaadusena. Triklorometaan e. kloroform (CHCl3) on narkoosivahend meditsiinis. Tetraklorometaani (CCl4) kasutatakse tulekustutites, ta on hea lahusti rasvadele ja vaikudele. Diklorodifluorometaani e. freooni (CCl2F2) kasutatakse külmikutes ning aerosoolides pihustusainena. Kloroetaani e
0 Aine iseloomustus CH4 metaan CO vingugaas CO2 süsihappegaas 1. Süsiniku oksüdatsiooniaste selles ühendis,ioonis molekulis. 2. Kas süsiniku ühend CH4+2O2CO2+2H2O 2CO+O22CO2 CO2+O2ei toimu reageerib hapnikuga ja kui reageerib siis võrrand 3. Süsiniku ühendi M(CH4 )=12+14*1=16 M(CO)=12+16=28 M(CO2 )=12+32=44 molaarmass kergem kergem raskem Õhk =29g/mol 4
Millise OA-ga on kõige enam a) Oksüdeerunud süsinik +4 (CO2) b) Redutseerunud süsinik -4 (CH4) Mis moodustub orgaanilise aine täielikul põlemisel? CO2+H2O Mis on pürolüüs? Aine lagunemine kõrge temperatuuri toimel Millal tekib põlemisel tahm? Kui põlemine on mittetäielik või pürolüüsiprotsessis Isomeeria On nähtus, kus ühenditel on ühesugune koostis kuid erinev struktuur ja sellest
Millise OA-ga on kõige enam a) Oksüdeerunud süsinik +4 (CO2) b) Redutseerunud süsinik -4 (CH4) Mis moodustub orgaanilise aine täielikul põlemisel? CO2+H2O Mis on pürolüüs? Aine lagunemine kõrge temperatuuri toimel Millal tekib põlemisel tahm? Kui põlemine on mittetäielik või pürolüüsiprotsessis Isomeeria On nähtus, kus ühenditel on ühesugune koostis kuid erinev struktuur ja sellest
Iga järgnev homoloog erineb eelmisest CH2 rühma võrra. 1. met 2. et 3. prop 4. but 5. pent 6. heks 7. hept 8. okt 9. non 10. dek Alkaanid CnH2n+2 Alkeenid CnH2n Alküünid CnH2n2 ALKAANID Alkaanid CnH2n+2 Alkaanid on küllastunud süsivesinikud, kus molekuli koostises süsinike vahel esinevad ainult ühekordsed kovalentsed sidemed. Nimetuse lõpp: aan Nt. Butaan C4H10 Metaan CH4 summaarne struktuurvalem C2H6 CH3CH3 (lihtsustatud struktuurvalem) etaan Hargenud ahelaga alkaanide nomenklatuur(reeglite kogum) 1) Kõigepealt leitakse molekulivalemist pikim ahel(peaahel e. tüviühend) 2) Hargnenud ahelat käsitletakse nii, nagu oleks tüviühendis teatud vesinikuaatomid asendatud süsivesinikrühmadega. 3) Alkaanist pärit asendusrühma nim. Alküülrühmaks(R). Nimetuse lõpp üül
Kasvuhooneefekt Peamised kasvuhoonegaasid: · H2O, CO2, CH4, O3, NO2 · Kasvuhooneefekt protsess, kus atmosfäär soojeneb kasvuhoonegaaside sisalduse suurenemise tõttu Veeaur(H2O) · Atmosfääris paljukuni 4% · Mõju kasvuhooneefektile 36%66% Süsinikdioksiid (CO2) · Suur kontsentratsioon>selle soojendav efekt atmosfääri püsikomponentidest (va. H2O) suurim · CO2 tekib:fossiilkütuste põletamisel,lageraiete tagajärjel,organismide hingamisel,organismide jäänuste lagunemisel Metaan (CH4)
KEEMIA. ALKAANIDE KEEMILISED OMADUSED PÕLEMINE o ALKAAN + HAPNIK -> SÜSIHAPPEGAAS + VESI CH4 + 2O2 CO2 + 2H2O TERMILINE LAGUNEMINE o LIHTAINEKS CH4 C + 2H2 o ALKÜÜN + VESINIK C4H10 C4H6 + 2H2 (butüün) CnH2n-2 KONDENSATSIOON VEEAURUGA o SÜSINIKOKSIID/VINGUGAAS CH4 + H2O CO + 3H2 o SÜSINIKDIOKSIID/SÜSIHAPPEGAAS CH4 + 2H2O CO2 + 4H2 ASENDUSREAKTSIOON HALOGEENIDEGA o NÄIDE C4H10 + 2Cl2 C4H8Cl2 + 2HCl (diklorobutaan) C arv saaduses ei muutu H indeksi saadusesse saad, kui lahutad algaine vesiniku indeksist halogeeni kordaja – (H)10- 2(Cl 2) = saaduses C4H8Cl2
Sissejuhatus Alkaanid - süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega. Mõnikord nimetatakse alkaane ka parafiinideks. 3 Leidumine ja saamine Kõige lihtsam alkaan - metaan (CH4) on looduslike gaaside (maagaas, kaevandusgaas, soogaas) peamine koostisosa. Kõrvuti metaaniga sisaldavad nad etaani, propaani, butaani ja teisi alkaane. Sünteetiliselt võib metaani saada juhtides vesinikku kõrgel temperatuuril läbi hõõguvate süte: C + 2H2 → CH4 4 Tuntumad esindajad METAAN: Maagaas (70-90%) Naftagaas
Ahela ehituse järgi jaotatakse alkaanid: 1) tsüklit mittesisaldavad (atsüklilised) alkaanid , üldvalemiga C nH2n+2 Need jaotatakse omakorda a)hargnemata ahelaga ehk normaalalkaanid ja b)hargnenud ahelaga . 2) tsüklilised alkaanid ehk tsükloalkaanid , üldvalemiga C nH2n. Nomenklatuur on aine struktuuri ja aine nimetust siduvate reeglite kogu. 1. Hargnemata ahelaga atsükliliste alkaanide valemid ja nimetused ( C nH2n+2 -aan ) 1) CH4 metaan 2) C2H6 etaan CH3-CH3 3) C3H8 propaan CH3-CH2-CH3 4) C4H10 butaan CH3-CH2-CH2-CH3 5) C5H12 pentaan 6) C6H14 heksaan 7) C7H14 heptaan 8) C8H18 oktaan 9) C9H20 nonaan 10) C10H22 dekaan 2. Tsükloalkaanide valemid ja nimetused (C nH2n) tsüklopropaan tsüklobutaan tsüklopentaan tsükloheksaan ∆ □ ⌂ (graafilised kujutised) 3. Hargnenud ahelaga alkaanide nimetamine valemi järgi
1 Süsiniku valentsolekud Orgaanilistes ainetes on süsinik neljavalentne- st. moodustab neli kovalentset sidet I valentsolek neli üksiksidet 109028´ CH4 jne Tetraeeder II valentsolek 2 üksiksidet ja 1200 1 kaksikside Tasapind CH2= CH2 III valentsolek üksikside ja kolmikside 1800 =C= O=C=O Või 2 kaksiksidet Sirge -C::: CH:::CH Metaan CH4
looduslik mineraal, sulamistemperatuur üle 4000kraadi Grafiit: hallikas-must, lõhnatu, poleeritav, rasvase pinnaga, sulamistemperatuur 3750kraadi, elektri pooljuht, halb soojusjuht, kihilise ehitusega Fullereen: C60 molekulaarteisend, must pulber mis leiti tahmas, ei juhi elektrit. Keemilised omadused: *Põleb C+O2 > CO2 süsihappegaas 2C+O2 > 2CO vingugaas *Reageerib metallioksiidiga CuO+C > Cu+CO *Reageerib vesinikuga C+2H2 > CH4 *H2O-aur C+H2O > CO+H2 Kasutamine: *Teemantit: ehtetööstuses ja tehnoloogias, lõiketeradel *Sütt: kütusena (kivisöe, koksina) *Grafiit: elektroodina, kirjutusvahendina *Aktiivsütt: söetablett=adsorbent, söefilter Adsorbent-seob pinnaga Absorbent-seob sisse CO ehk vingugaas ehk süsinikoksiid Füüsikalised omadused:Värvitu, lõhnatu, õhuga u. ühe raskusega, vees lahustumatu, mürgine Keemilised omadused:*põleb 2CO+O2 > 2CO2 *reageerib metallioksiididega Fe2O3+3CO >
Alkaanideks nimetatakse orgaanilisi aineid, mis koosnevad C ja H'st, ning kus C aatomite vahel on üksikside ehk sigmaside. Üldvalem CnH2n+2 (n on jrk nr) Orgaanilistele ainetele pannakse nimed alkaanide homoloogilise rea alusel. 1. metaan CH4 2. etaan C2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptann C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22 Radikaalid on molekulid või aatomid, mille elektronkihis asub paardumata elektron. 2-metüül propaan Alkaanide keemilised omadused:
Polümeer-ained mille suured molekulid koosnevad väga paljudest enamasti üksteisega seotud väikeste Molekulide jääkidest või lõikudest.nafta- majapidamisgaas,bensiin,petroleum,diislikütus,määrdeõlid,parafiin, Bituumen.-alkaanid,destillatsioon.vettõrjuvad,lahus,mare,kütus,asphalt,kreemid.süsiniku allotroopsed Teisendid-allotroopia-keemilise elemendi esinemine mitme lihtainena,alotrobid-puhas lihtaine.teemant, Grafiit,grafeen,fullereenid.alotrop põlemine-CH4+2O2-2CO2,vingugaas-2CO2+O2- 2CO2,süsihappegaas- C+O2-CO2,süsihape-CO2+H2O-H2CO3,metalliga-fe2o3+co-fe+co2, saamine-metanooli-ch4+o2- ch3-oh Co2+h2-ch3-oh, Etanooli-c6h12o6-ch3-ch2-oh+co2 elutähtsad- sahhariidid(c,h,o),rasvad(glütserool rasvhape),valgud(aminohapete jääkidest)allotroobid koosnevad samast elemendist, kuid on erineva struktuuriga.süsiniku reaktsioon vesinikuga c+2H2-CH4(metaan), hõõguv süsi veega C+H2O- Co+H2
TABEL AINE VALE AGREGA VÄRVUS VEES LEIDUMINE NIMETU M AT LAHUSTUVUS S OLEK METAAN CH4 GAAS VÄRVUSE EI LAHUSTU SOOGAAS TU MAAGAAS ETAAN C2H4 GAAS VÄRVUSE HALVASTI MAAGAAS TU PROPAA C3H8 GAAS VÄRVUSE PRAKTILISELT NAFTA N TU LAHUSTUMATU ALKAANIDE ÜLDVALEM CnH2n+2 C-aatomite arv Nimetus Valem Olek 1 METAAN CH4 G
2. Millised on alkaanide füsioloogilised omadused? - keemiliselt inertsed st reageerivad ainetega aeglaselt või ei reageeri üldse, sellegipoolest on alkaanide aurud elusorganismidele ohlikud - omavad tugevat narkootilist toimet, võivad kahj. kesknärvisüsteemi ja olla surmavad sissevõtmisel/-hingamisel - tahked alk. on ohutud 3. Millised on alkaanide keemilised omadused? Kirjelda keemilisi omadusi reaktsioonivõrrandite abil. - iseloomulik asendusreaktsioon CH4 + Cl2 = CH3Cl + HCl - kõik alkaanid põlevad CH4 + 2O2 = 2H2O + CO2 - üldiselt termiliselt väga püsivad, kuid võviad siiski laguneda väga kõrgel temperatuuril ning saadused sõltuvad reaktsiooni toimumise kohast ja ajast CH4 = 2H2 + C 4. Selgita mõisteid: hüdrofoobsed ained ja hüdrofiilsed ained. Hüdrofoobsed: ei märgu ega lahustu, ei moodusta vesiniksidemeid, puudub vastastikmõju veega. 5. Mis on radikaal? Osake, millel on üks paardumata elektron
2. Millised on alkaanide füsioloogilised omadused? - keemiliselt inertsed st reageerivad ainetega aeglaselt või ei reageeri üldse, sellegipoolest on alkaanide aurud elusorganismidele ohlikud - omavad tugevat narkootilist toimet, võivad kahj. kesknärvisüsteemi ja olla surmavad sissevõtmisel/-hingamisel - tahked alk. on ohutud 3. Millised on alkaanide keemilised omadused? Kirjelda keemilisi omadusi reaktsioonivõrrandite abil. - iseloomulik asendusreaktsioon CH4 + Cl2 = CH3Cl + HCl - kõik alkaanid põlevad CH4 + 2O2 = 2H2O + CO2 - üldiselt termiliselt väga püsivad, kuid võviad siiski laguneda väga kõrgel temperatuuril ning saadused sõltuvad reaktsiooni toimumise kohast ja ajast CH4 = 2H2 + C 4. Selgita mõisteid: hüdrofoobsed ained ja hüdrofiilsed ained. Hüdrofoobsed: ei märgu ega lahustu, ei moodusta vesiniksidemeid, puudub vastastikmõju veega. 5. Mis on radikaal? Osake, millel on üks paardumata elektron
Lagunemine kõrgel temperatuuril – Kõrgel temperatuuril alkaanid lagunevad. Gaasilisi alkaane kasutatakse kütte- ja majapidamisgaasina ning vedeltatult vedelgaasina. Vedelad alkaanid kuuluvad ka bensiini, nafta ja petrooleumi koostisesse. Tahked alkaanid moodustavad parafiini. Alkaane tarvitatakse samuti õlide, vaikude, rasvade ja plastmasside lahustitena ning narkoosivahendina, tulekustutusvedelikuna ja parfüümide jms juures pihustusainena. Täielik põlemine: CH4 + 1,5O2 → CO2 + 2H2O Mittetäielik põlemine: 2CH4 + 3O2 → CO2 + 4H2O + C Halogeenidega (VIIA): CH4 + Br2 → CH3Br + HBr Vesinikhalogeenidega: CH4 + HBr → CH3Br + H2 Oksüdeerumine: 2CH4 + O2 → 2CH3OH
Side süsinik-hapnik on palju püsivam kui side vesinik hapnik. Alkoksiidioon on väga nõrga happe anioon. Alkohol on on hape. Alkoholaat on alkoholi sool. Metanool- Ch3Oh puupiiritus. Etanool C2H5OH piiritus. Puskari õli on destillatsioonijääk etanooli eraldamisel käärimissegust. See koosneb kahest pentanooli isomeerist. Etandiool HOCH2CH2OH-etüleenglükool- diool. Antifriis-mootori jahutussegu. Glütserool- HOCH2CHOHCH2OH-looduslik. Alkaanid- CH4-metaan C2H6-etaan C3h8-propaan Alkeenid- C2H4-eteen C3H6-propeen Alküünid- C2H2-etüün C3H4-propeen Alkoholid- ch3oh-metanool c2h5oh- etanool c3h7oh- propanool Karboksüülhapped- hcooh-metaanhape ch3cooh-etaanhape C2h5cooh-propaanhape Sahhariidid- c6h12o6-glükoos c6h12o6-fruktoos c12h22o11-sahharoos (c6h10o5)n-tärklis tselluloos Aineid, mille molekulis tetraeedrilise süsiniku aatomi juures asuv vesinik on asendatud hüdroksüülrühmaga oh, nimetatakse alkoholideks
SÜSIVESINIKUD On orgaanilisedühendid mis koosnevad süsinikust ja vesinikust Alkaanides on 1-4 liiget gaasid ja alates 5. on vedelikud. ALKAANID 1) Metaan CH4 2) Etaan C2H6 3) Propaan C3H8 4) Butaan C4H10 5) Pentaan C5H12 6) Heksaan C6H14 7) Heptaan C7H16 8) Oktaan C8H18 9) Nonaan - C9H20 10) Dekaan C10H2 ALKOHOOLID Alkohoolide nimetus on tuletatud süsivesinikest, millest üks või mitu on hüdroksiid. Alkohoolide nimed pannakse lähtudes alkaanide reast C-de(süsinike) arvu järgi. CnH2 + 2 = AAN lõpuga 1) CH4 metaan ---- CH3OH = metanool ehk puupiiritus
SÜSIVESINIKUD.- sisaldavad ainult H ja C aatomeid. Küllastunud süsivesinikud. C vahel on ainult üksiksidemed Alkaanid. Üldvalem: CnH2n+2 Metaan CH4 Vees mittelahustuvad gaasid. Etaan C2H6 Lõhnata, maitseta. Kas. Küttegaasina jm. Propaan C3H8 Butaan C4H10 C5 C15 Vees mittelahustuvad, veest kergemad, bensiini lõhnaga vedelikud. Nendest koosnebki bensiin ja petrooleum. Bensiin-hea lahusti. Alkaani nimetusel on lõpp- aan Alkaani nimetused on alusteks kõigi teiste ainete nimetuste moodustamisel. Süsivesinike täielikul põlemisel tekib CO2 ja H2O
saadus Keemilised omadused Toatemperatuuril on püsiv ja teiste ainetega ei reageeri, kuumutades põleb ning tekib süsihappegaas C+O2=CO2 Kui hapnikku ei ole piisavalt, tekib mürgine süsinikmonooksiid 2C+O2=2CO Lihtainena on redutseerivad omadused, mistõtu kasutatatkse teda redutseerijana metallide tootmisel 2CuO+C=2Cu+CO2 Keemilised omadused Süsinik oksüdeerijana (redutseerub, st liidab elektrone) süsiniku reageerimine vesinikuga C + 2H2 CH4 Süsinik nii oksüdeerija kui redutseerijana süsiniku reageerimine süsihappegaasiga C + CO2 2 CO Tähtsamad ühendid SÜSINIKDIOKSIID ehk süsihappegaas: CO2, ei põle ega toeta põlemist, sest süsiniku oksüdatsiooniaste on maksimaalne ehk IV, kasutatakse tulekustutites; tahke süsihappegaasi ehk ,,kuiva jää" temperatuur -80ºC, kasutatakse toiduainete transportimisel ja säilitamisel. SÜSINIKOKSIID ehk vingugaas: CO, värvitu ja lõhnatu gaas, vees
Halogeeniühendid Halogeeniühendies on süsiniku aatomid seotud halogeeni aatomitega. CH4 = CH3Cl Füüsikalised omadused *Peamiselt vedelikud või tahked ained *Madalamad halogeeniühendid aurustuvad kiiresti Asendusnomenklatuur- asendusrühmad + tüviühend *floro-, kloro-, bromo-,jodo CH3-CH2-CH2-CH2-Cl 1-klorobutaan Ahelisomeeria- süsinikahela kuju on erinev Asendusisomeeria- funktsionaalrühmad paiknevad ühesuguse süsinik arvu ja paigutused süsinikahela korral erinevalt Kõik halogeenid on C-st elektronnegatiivsemad C ja Hal vahel on polaarne kovalentne side
Kas vuhoone e f e kt Tekkepõhj used Kasvuhoonegaaside, veeauru ja tolmu hulga suurenemine atmosfääris. Kasvuhoonegaasid: o Süsihappegaas (CO2 ) o Metaan (CH4) o Lämmastikoksiidid (NO) o Freoonid (CFCs) o Veeaur o Osoon (O3) Need on kõik looduslikud gaasid, kuid tänu inimtegevusele nende hulk atmosfääris suureneb. Süs i happe gaas Süs i happe gaas o Süsihappegaas ehk süsinikdioksiid eraldub ° fossiilsete kütuste, nagu põlevkivi, maagaas ning kivisüsi, põletamisel(87%); ° metsade mahavõtmisel (11%)(CO2 on neeldunud puudesse, kuid kui metsa raiutakse, pääseb suur
C Si Aaomi +6 | 2) 4) +14 | 2) 8) 4) ehitus 1s² 2s² 2p² 1s² 2s² 2p 3s² 3p² Oksüdat- min: IV (CH4) max: +IV (CO2) min: IV (Mg2Si) max: +IV (SiO2) siooniaste Leidumine 1) ehedalt (teemant, graniit, karbüün) 1) ühenditena 2) ühenditena (kivisüsi, nafta jt kütuste SiO2 - na liiva ja kivimite koostises) koostises 3) taim- ja loomorganismides ränihappe sooladena 4) õhus CO2 5) mineraalid CaCO3, MgCO3
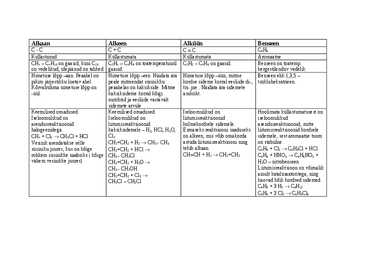
Alkaan Alkeen Alküün Benseen C-C C=C CC C6H6 Küllastunud Küllastumata Küllastumata Aromaatne CH4 C4H10 on gaasid, kuni C10 C2H4 C4H8 on toatemperatuuril C2H2 C4H6 on gaasid. Benseen on toatemp. on vedelikud, ülejäänud on tahked gaasid. kergestilenduv vedelik Nimetuse lõpp aan. Peaahel on Nimetuse lõpp een. Näidata ära Nimetuse lõpp üün, mitme Benseen ehk 1,3,5 pikim järjestikku loetav ahel
Keemia, 10.klass Gerli, Stella, Kätlin Väikese molekuliga alkaanid ehk C1 C3 on gaasilised alkaanid. Gaasilised alkaanid on lõhnata või vedelad bensiini lõhnaga. Nelja esimese alkaani(C1-C3) puhul on need sõnatüve met(aan), et(aan) ja prop(aan) triviaalsed. Maagaas koosneb põhiliselt metaanist ja etaanist, vedelgaas ehk balloonigaas (veeldatud naftagaas) aga propaanist ja butaanist Kõige lihtsam alkaan metaan (CH4) on kõikidele looduslike gaaside ( maagaas, kaevandusgaas, soogaas ) peamiseks koostisosaks. Kõrvuti metaaniga sisaldub neis etaani, propaani, butaani, ja teisi alkaane. Alkaan Nimetus CH4 metaan C2H6 etaan C3H8 propaan Alkaanid on süsiniku ja vesiniku ühendid, mille molekulides süsiniku aatomid on omavahel seotud kovalentse üksiksidemega. Mõnikord nimetatakse alkaane ka parafiinideks.
oma pinnale mitmesuguseid lisaaineid .Süsi juhib elektrit . Kõrgel temperatuuril töödeldud veeauruga süsi on eriti suure sidumisvõimega . Söe abil saab lahustest eemaldada lahustunud värvilisi aineid . Söetablette antakse sisse kõhuvalu puhul, et siduda seedeorganites kahjulikke aineid. 8. Mis on koks ? Kivisöest saadav süsi on koks . 9. Metaani valem, süsinikuoksüdatsiooniaste metaanis . Metaan CH4 . Süsiniku oksüdatsiooniaste on IV . 10. Metaani omadused . Metaan on : 1) Värvusetu , 2) Lõhnatu , 3) maitsetu . Vees lahustub võrdlemisi vähe . Õhust on tublisti kergem. Põleb hästi . 11. Metaani leidumine looduses. Metaan on maagaasi põhiline koostisosa . Metaani leidub Ka mitmesugustes gaasides , mis tekivad orgaaniliste ainete lagunemisel ilma õhu juurdepääsuta (soogaas ) . Kasutatakse
plahvatusohtlik • Metaan: annab 6-13% globaalsest gaasitoodangust • Tavaliselt ei ole plahvatusoht probleemiks. • Prügilat annab rajada nii, et gaasi tekiks vähem või et • Ebasoodne on madalrõhk, sest siis suureneb gaasi lendumine see oksüdeeritaks oluliselt. • Kas CO2 on oluline? On, kuid CH4 on olulisem • Kui nüüd peaks tulema kõvasti vihma, võib see pinnasepoorid täis • Prügila CO2 kutsutakse neutraalseks – see on panna ja gaas ei pääse välja. taastuvatest allikatest • Selle peale hakkab gaas otsima teisi väljapääse ja võib rännata kaugele
GRAFIIT: pehme-pliiatsites, määrdesegudes kõrge salamis temp.-raketi düüs, tiigel hea elektrijuht-elektroodides TEEMANT: ilus läige-ehted kõvadus-puurides, lihvimis pulbrites, klaasinoad 6.SÜSI(TEKE, KOOSTIS, KASUTAMINE, FÜÜSIKALISED OMADUSED). teke-orgaaniliste ainete kuumutamisel õhu juurde pääsuta omadused-poorne, ei lahustu üheski lahuses, hea elektrijuht, raskesti sulav kasutamine-meditsiinis koostis-koosneb grafiidist , C 7.METAAN: valem-CH4 ehitus- füüsikalised omadused(4)-värvusetu, lõhnatu, maitsetu, mürgine kasutamine(2)-kütus, tooraine põlemise võrrand-CH4+2O2->CO2+2H2O 8.SÜSINIKOKSIID: valem-CO rahvapärane nimetus-vingugaas füüsikalised omadused(4)-värvusetu gaas, lõhnatu, väga mürgine, vees eriti ei lahustu tekke võrrand-2C+O2->2CO keemilised omadused-põleb kasutamine(2)-metallide redutseerimine 9.SÜSINIKDIOKSIID: valem-CO2 tõestamine-põlev pird kustub rahvapärane nimetus-
Tunnuslõpp -aan -een -üün -ool -hape Üldvalem CnH2n +2 CnH2n CnH2n-2 R-OH R-COOH Side üksikside kaksikside kolmikside üksikside üksikside Põhiesindaja CH4 -metaan C2H2 -eteen C2H2 - etüün C2H2OH -etanool CH3COOH -metaanhape CH4 metaan - - CH3OH metanool HCOOH etaanhape
.. 1000 °C juures. Vedelgaas · Propaan ja butaan · Vedelas olekus, põleb gaasina · Kasutatakse Majapidamisgaasina maagaasi asemel Metallide lõikamisel Kuumutamisel Jootmisel Soojapuhurite Soojakiirgurite küttena Biogaas · Anaeroobse kääritamise või orgaanilise aine lagundamisega hapnikuta · Metaan ja CO2 · Kasutatakse: Kütusena Elektri tootmiseks Kütmiseks Biogaas koosneb · metaan (CH4) 40 75% · süsihappegaas(CO2) 25 55% · vesi (H2O) 2 10% · divesiniksulfiidhape H2S< 2% · lämmastik N2 <2% · vesinik H2 <1% · Ammoniaak CH3 <1% Metaan (CH4) · Lihtsaim alkaan, värvitu gaas · Palju, põleb puhtalt · Kasvuhoonegaas · Sulamistemp: -182.5 °C (90.6 K, -296.5 °F) · Keemistemp: -161.6 °C (111.55 K, -258.88 °F) · Süttimistemp: 537 °C · Maksimaalne põlemistemp: 2148 °C Etaan (C2H6)
N2, O2 99,030% . . . / . 1020% Ar, CO2 0,967% , . . He,Ne,Kr,Xe,H2,N 2O,CH4 0,003% 2) , : , . , . 6000*10 21 >2 . , . . 1,4*1021
Oksiidid Oksiidid koosnevad kahest elemendist, millest üks on hapnik. OKSIIDIDE LEIDMINE Otsusta, millised valemid kuuluvad oksiididele SO3, HNO3, CaC2, Cl2O7, BaO, CaCO3, NaOH, O2, H2O, CH4, Al2O3, MgSO4, P4O10, NH3 OKSIIDIDE SAAMINE I Metalli või mittemetalli reag. hapnikuga ◦ lihtainete põletamisel õhus või hapnikus liitainete põlemisel C + O2 CO2 CH4 + 2O2 CO2 + 2H2O 2Mg + O2 2MgO OKSIIDIDE SAAMINE II Hapnikku sisaldavat soolade, hapete ja aluste lagundamisel CaCO3 CaO + CO2 H2SO3 H2O + SO2
Õppeaine: Keemia Klass: 8. klass Kooliaste: III kooliaste Koolitaja: Ivari Tiitsu / 9. rühm Lühitutvustus: Esitlus PowerPointis tutvustab oksiide OKSIIDID ON liitained, mis koosnevad kahest elemendist, millest üks on hapnik elemendi ühend hapnikuga hapniku ühend mingi teise keemilise elemendiga OKSIIDIDE SAAMINE I lihtainete põletamisel liitainete põlemisel õhus või hapnikus CH4 + 2O2 CO2 + 2H2O C + O2 CO2 2Mg + O2 2MgO OKSIIDIDE SAAMINE II soolade, hapete ja aluste lagundamisel CaCO3 CaO + CO2 H2SO3 H2O + SO2 2Fe(OH)3 Fe2O3 + 3H2O OKSIIDIDE NIMETUSED 1 Metallioksiidid e. aluselised oksiidid a) kui metallil on püsiv o.a. väärtus Na2O naatriumoksiid Al2O3 alumiiniumoksiid m e t a l l + o k s i i d OKSIIDIDE NIMETUSED 2 b) kui metallil on muutuv o.a. väärtus III
Alkaanide omadused: Põlemine[(CH4+2O2->2CO2+H2O) II- 27513 III-24385 IV-64106] Halogeenimine[Cl2F2 Br2 I2] (CH4+Cl2->CH3Cl+ HCl)Saamine küllastumata ühenditest Füüsikalised omadused:ei lahustu vees, veest kergemad, vesiniksidemed puuduvad, C1-C4=gaasid, -14=vedelad, 15- =tahked, lõhnatu, värvitu(mitte kõik), mürgised, mõjub knsile, kergesti lenduvad. Alkeenide omadused: Põlemine[C2H4+ 302->2O2+2O2 2 C5H10+ O2- >10CO2+10H20]Hüdrogeenimine (H2 liitmine) Halogeenimine(VIIA rühma liitmine) Vesinikhalogeenimine(HF,HBr,HI,HCl) Vee liitmine Ei lahustu
(inimene kiirendab süsinikuringet) 3. Süsinikuringe leidumine Lämmastikuringe Protsessid 1. Atmosfäär 1. Ammonifikatsioon 2. Hüdrosfäär 2. Nitrifikatsioon 3. Pedosfäär 3. Denitrifikatsioon 4. Setted ja settekivimid 4. Millise süsinikuringe osaga on tegemist? Kui on piisavalt hapniku tekib CO2, kui piisavalt hapniku pole tekib CH4 - Lagundamisprotsess Atmosfääri paiskuvad CO2 JA CH4 - Vulkaanipursked Kasutatakse süsihappegaasi ja vett, toodetakse orgaanilist ainet ja hapniku - Fotosüntees Hapniku kasutatakse orgaanilise aine lagundamiseks ning vabandevad CO2 ja veearu - Hingamine Kuidas mõjutavad elusorganismid lämmastikuringet? 1. Bakterite ja seente elutegevuse tulemusena toimub ammonifikatsioon, ilma
b) ammoniaak lahustub vees, kogutakse c) lämmastikdioksiid - 6. Lihtainete omadused esinemine ja kasutamine. H2 gaas, läbipaistev, tihedus õhu suhtes väiksem, 7. Tuntumate liitainete omadused, esinemine, kasutamine. 8. O, C, N ringkäik looduses. 6CO2 + 6H2O -> 6O2 + C6H12O6 N - valkude koostises. Selleks, et in. ja loom saaks valku teha, peavad nad valku sööm(söövad taimi). Taim teeb valku sahhariididest. CH4 + 2O2 > CO2 + 2H2O TÄIELIK PÕLEMINE CH4 + 1,5O2 >CO + 2H2O MITTETÄIELIK PÕLEMINE 9. Kuidas toodetakse klaasi, tsementi? 10. Kütuste põlemine (võrrandina täielik ja mittetäielik). CH4 + 2O2 > CO2 + 2H2O TÄIELIK PÕLEMINE CH4 + 1,5O2 >CO + 2H2O MITTETÄIELIK PÕLEMINE 11. Allotroopia. Isotoopia. Vesinik Millised on vesiniku o-a? VII - -I H2 füüsikalised omadused (olek, lahustumine vees, tihedus õhu suhtes, värv, lõhn).
Süsivesinikud orgaanilised ühendid, mis koosnevad ainult süsiniku ja vesiniku aatomitest. Üldvalem CnH2n+2 Alkaanid sisaldavad ainult tetraeedrilisi süsinikke (kõik aatomid on omavahel seotud ühekordsete -sidemetega). Triviaalsed nimetused ühendite nimetused, mis on inimene ühenditele juhuslikult andnud. Need nimetused ei ole süstemaatilised ega väljenda aine keemilist koostist ega struktuuri. Näiteks soogaas, mille süstemaatiline nimetus on metaan (CH4). Süstemaatilised nimetused kajastavad ühendi keemilist struktuuri. Neid on võimalik struktuuri järgi üles märkida. Nomenklatuur aine struktuuri ja nimetust siduvate reeglite kogu (IUPAC Ineternational Union of Pure and Applied Chemistry). Alkaani tunnusteks on järelliide aan (metaan, etaan, propaan, butaan, pentaan jne...). Sõnatüvi (met-, et-, prop-, but-, pent-) kirjeldab süsinikahela pikkust. Alkaan Nimetus Sõnatüvi
erinevates vormides, nimetame allotroopiaks. Süsiniku puhul on teemant ja grafiit allotroobid. Kas süsinikul on veel allotroope? Otsi vihikust või tuleta meelde mis on hapniku allotroobid? Oskad sa veel mõnda näidet allotroopia kohta tuua? Orgaanilises keemias on süsinikul alati 4 kovalentset sidet (Kui Sa ei mäleta, siis tuleta meelde, mis on kovalentne side!). Hapnikul on alati 2 kovalentset sidet ning vesinikul 1. Orgaanilised süsinikuühendid on näiteks metaan (CH4), etaan (C2H6), jpt. Reeglina koosnevadki orgaanilised süsinikuühendid reeglina süsinikust ja vesinikust - sellest tuleneb ka nende nimetus -süsivesinikud. Tihti on olulised ka hapnik, näiteks molekulides nimega metanool (C2H5OH) või glükoos (C6H12O6), jpt. Vasakul on joonis, kus on klassikalise struktuurivalemi abil kujutatud metaani molekul. Proovi klassikalise struktuurivalemi abil kujutada etaani, propaani ning metanooli ja etanooli
Tekib aatomi väliskihi elektronide abil. - osalaeng (väike delta) - Suur delta Keemilise sideme tüübid: 1) Kovalentne side a)polaarne b)mittepolaarne 2)iooniline side 3)metalliline side 4)vesinikside Kovalentne side on ühise või ühiste elektronipaaride abil moodustunud side. Polaarne kov. Sideme korral seob üks aatomitest ühist elektronpaari tugevamini, mistõttu aatomitel tekivad vastasmärgilised osalaengud. Polaarne side: NO2, CO2, CH4 2 mittemetalli. Mittepolaarse kov. Sideme korral on ühine elektronpaar jaotunud võrdselt mõlema aatomi vahel, sest mõlemad aatomid tõmbavad elektronpaari sama tugevusega. Mittepolaarne side: O2, Br2, C- üks aine, Vesinikside on (iselaadne molekulide vaheline side) keemiline side, kus ühe molekuli vesiniku aatom on seotud teise molekuli hapniku, lämmastiku või fluori aatomiga. Ained, mis moodustavad veega tugevaid vesiniksideme, lahustuvad hästi vees. Näiteks ammoniaak.
Molekulmassi kasvuga homoloogilises reas suureneb alkaanide tihedus ning kasvab sulamis- ja keemistemperatuur. · Alkaanid vees ei lahustu. · Homoloogilises reas muutuvad homoloogilise rea liikmete - homoloogide - füüsikalised omadused korrapäraselt. Molekulmassi suurenemisega kasvab homoloogide tihedus, sulamis- ja keemistemperatuur ning agregaatolek muutub : gaas vedelik tahke. Kõige lihtsam alkaan - metaan ( CH4 ) on kõikidele looduslike gaaside ( maagaas, kaevandusgaas, soogaas ) peamiseks koostisosaks. Kõrvuti metaaniga sisaldub neis etaani, propaani, butaani, ja teisi alkaane. Sünteetiliselt võib metaani saada, juhtides vesinikku kõrgel temperatuuril läbi hõõguvate süte : C + 2H2 CH4 Gaasilised alkaanid leiavad kasutamist kütte- ja majapidamisgaasina ning veeldatult nt. vedelgaasina. Vedelad alkaanid kuuluvad ka bensiini, nafta ja petrooleumi koostisse.
· N2O naerugaas · CO2 tekib täielikul põlemisel, ei põle ega soodusta põlemist, tulekustutites · CO väga mürgine, tekib mittetäielikul põlemisel · H2O2 vesinikperoksiid, haavade puhastamiseks, hapniku saamiseks · SO2 mürgine teravalõhnaline gaas, happesademete põhjustaja · ... 7. KESKKONNAST... · Happesademeid põhjustavad: happelised oksiidid, peamiselt SO2, NOx, ... · Kasvuhooneefekti põhjustavad: peamiselt CO2, CH4 · Mittemetalliühenditest põhjustavad veekogude kinnikasvamist (eutrofeerumist) lämmastikuühendeid sisaldavad väetised ÜLESANDED · Määra reaktsioonides oksüdatsiooniastmed, kirjuta elektronvõrrandid ja tuvasta oksüdeerija, redutseerija. 2 Al + 3 Br2 2 AlBr3 2 Mg + O2 2 MgO 3 Ca + 2 H3PO4 Ca3(PO4)2 + 3 H2 Fe2O3 + 3 CO 2 Fe + 3 CO2 2 KClO3 2 KCl + 3 O2 ÜLESANDED · Kirjuta elektronvõrrandid:
Grafiidi omadused: hallikasmust, läbipaistmatu, väga rasksulav, pehme. Grafiidi struktuur - kihid üksteisega nõrgalt seotud. * võib omada oksüdatsiooniastmeid -4 kuni 4 * kõrgel temperatuuril võib käituda oksüdeerijana või redutseerijana. Süsi - ei ole süsiniku allotroopne teisend.Koosneb peeneteralisest grafiidist nin sisaldab lisandeid. Tekib orgaaniliste ainete kuumutamisel ilma õhu juurdepääsuta. Kivisöest saadav süsi on KOKS. Süsinikuühendid Metaan CH4 - * oa -4 *molekul on ruumiline tetraeeder * sisaldab vaid üksiksidemeid * hästi põlev gaas CH4 + 2O2 = CO2 + 2H20 *õhust kergem, värvusetu, lõhnatu ja maitsetu gaas, vees ei lahustu eriti. *maagaasi põhiline koostisosa. Süsinikoksiid CO - vingugaas *oa on 2 * tekib C ja tema madalama oa ühendite põlemisel hapniku vaeguses. *hästi põlev gaas 2CO + O2 = 2CO2 * mürgine *kuulub mitmete küttegaaside koostisse Süsinikdioksiid CO2 - happeline oksiid! * oa 4
mootorikütusena. Süsivesinike segu Nafta Looduslik vedelkütus, peamiselt leiduv vedelate süsivesinike segu Krakkimine Nafta ddestilleerimissaaduste lagunemine lühemate ahelatega ühenditeks Fraktsioneeriv destillatsioon - on destillatsioonimeetod kasutades destillatsioonikolonni, milles toimub korduv aurustumine ja kondensatsioon. Alkaanide nimetused/valemid (graafilised, tasapinnalised, lihtsustatud) Tähtsamad alkaanid: CH4 metaan CH3 metüül C2H6 etaan CH3CH2 etüül C3H8 propaan CH3CH2CH2 propüül C4H10 butaan CH3CH2CH2CH2 butüül C5H12 pentaan C6H14 heksaan C7H16 heptaan C8H18 oktaan C9H20 nonaan C10H22 dekaan Isomeerid (Koostamine, füüsikaliste omaduste tuletamine ja põhjendamine) Isomeeride struktuur on erinev, siis erinevad on ka nende omadused ehk
Polaaraladel on polaarpäev ja öö. Eestis on sel ajal kevad või sügis. Päev ja öö on ühepikkused. Osooniauk- osoonikihi oluline õhenemine stratosfääris, esinevad polaaraladel. Osooni lagundavad freoonid. Kasvuhooneefekti olemus lühilaineline päikesekiirgus läbib atmosfääri, kuid pikaajaline soojuskiirguse väljumine on takistatud. See neeldub õhus, mille tagajärjel atmosfäär soojeneb. Peamiseks soojuskiirguse neelajaks on: CO2,CH4, N2O, O, O3. · CO2 süsinikdioksiidi hulka suurendavad: metsade maharaiumine, autode heitgaasid, tsemendi tootmine · N2O- naerugaas: autode heitgaasid, põldude väetamine, eraldumine lennukite düüsidest · CH4-metaan: märgaladest õhkupaisumine, riisikasvatustes, prügilatest lendumine, veisekasvatus · Freoonid: eraldumine külmutusseadmetest, deodorantide kasutamine, tulekustutusseadmete kasutamine. Öösel maismaa jahtub kiiremini kui meri, mere kohal madalrõhu ala
36. Miks nimetatakse süsivesinikke, alkohole, karboksüülhappeid, sahhariide,valke ja rasvasid orgaanilisteks ühenditeks? 1. C 2. 2, IV A, mittemetall 3. +6)2)4) 4. 4 kovalentset sidet. 5. Nafta, maagaas, kivisüsi, antratsiit 6. Süsinikdioksiid 7. Grafiit, teemant 8. Grafiidi struktuur on tekkinud kihtide kaupa asetsevatest võrkudest ja ta lõheneb kergesti. 9. Sest ta struktuuris leidub vabu elemente. 10. CO2 ja H2O 11. CO põleb, CO2 ei põle ja CH4 põleb. 12. Vingugaas e. CO 13. Süsinikust ja vesinikust 14. Üksik 15. Propaan= C3H8, butaan= C4H10, etaan= C2H6, metaan=CH4 16. Maagaas ja nafta koosnevad peamiselt metaanist. 17. Naftagaas, bensiin, diislikütus, masuut, määrdeõlid 18. C= 4, N=3, O=2 19. C= 4, N=3, O=2 20. Struktuur 21. CH3OH-metanool 22. Metanool, etanool, glütserool 23. Metanooli kasutatakse tööstuses lahustina, mootorikütusena ja mitmesuguste ainete valmistamiseks