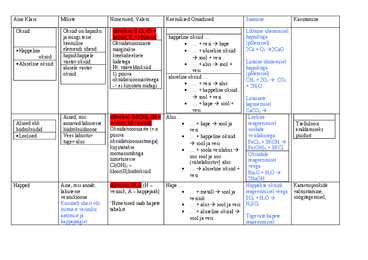
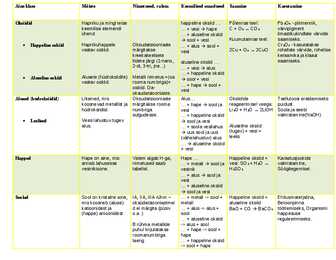
Leelised ehk I A rühma metallid Ajalooliselt tuleneb sõna leelismetall sellest, et nende metallide hüdroksiide tunti juba ammu ja neid nimetati leelisteks. Tänapäevane selgitus võiks olla lihtsalt selline, et nende metallide veega reageerimisel tekivad leelised. Leelismetallid on kõige metalsemad elemendid. Aatomi ehituselt kuuluvad nad s-elementide hulka, kuna nende aatomite välisel orbitaalil on üks elektron. Sellest tulenevalt on kõikide leelismetallide aatomite väliskihi elektronvalemiks ns ja oksüdatsiooniastmeks ühendis +I. Kuna leelismetallidel on väliskihis ainult üks elektron, siis seetõttu nad loovutavad selle erakordselt kergesti. Kusjuures mida kaugemal väliselektron aatomituumast asub, seda kergemini see loovutatakse
NAATRIUM JA KAALIUM AATOMI EHITUS AATOMI OMADUSED NAATRIUM: 1. värvvuselt hõbevalge metall. 2. pehme, saab noaga lõigata, plastiline 3. Naatriumi tihedus on 0,97 g/cm3 4. sulamistemperatuur on 98 kraadi 5. Kõvadus 0,5 (Moshi skaalal) KAALIUM: 1. värvuselt sinakas-hõbevalge metall 2. pehme, saab noaga lõigata, plastiline 3. Tihedus normaaltingimustel on 0,86 g/cm3. 4. Kaaliumi sulamistemperatuur on 63 °C 5. Kõvadus 0,4 (Moshi skaalal) KEEMILISED OMADUSED (VÕRRANDITENA) Mõlemad väga aktiivsed, leelismetallid, oksüdatsiooniastmed ühendites +1. Naatrium ja kaaliumoksiidid on tugevalt aluselised. 1. Reageerivad hapnikuga, moodustub naatriumi puhul naatriumperoksiid, kaaliumiga kaaliumhüperoksiid 2. Reageerivad väga aktiivselt veega. Eksodermiline reaktsioon. Veega reageerides kuumeneb metall nii palju, et ta läheb põlema, kaalium lil...
tuleb need kõigepealt kiiresti ära pesta ja vajaduse korral loputada kahjustatud koht üle lahustatud äädikhappe lahusega ning seejärel uuesti veega. Kätele sattunud alust ei tehta kahjutuks mõne tugeva happe abil, kuna ka happed on tervisele ohtlikud. Alus on aine, mis annab lahusesse hüdroksiidioone. Kõik alustele iseloomulikud omadused, nagu sööbiv toime, võime muuta indikaatorite värvust ning libedus on tingitud nende lahuses esinevatest hüdroksiidioonidest. Leelised on vees lahustuvad söövitava toimega tugevad alused, mis muudavad indikaatorite värvust. Naatriumhüdroksiid (NaOH) on tugev leelis. Ta on valge tahke aine, mis lahustub väga hästi vees, eraldades seejuures palju soojust. Samuti seob ta õhu käes seismisel õhuniiskust. Aluselisteks oksiidideks nimetatakse metallioksiide, mis vastavad mingile alusele (metalli oksüdatsiooniaste on sama). Ba(OH)2 -> BaO . Osa metallioksiide reageerib veega, osa mitte.
Millest on tingitud vee karbonaatne karedus? mööduv. Ca- ja Mg vesinikkarbonaadi esinemine Kuidas seda kõrvaldada? vee kuumutamisel, kuumutamisel vesinikkarbonaadid lahustuvad ning tekkinud raskestilahustuvad karbonaadid sadestuvad põhja (katlakivi) Millest on tingitud vee mittekarbonaatne karedus? jääv. vees lahustunud Ca- ja Mg kloriidid, sulfaadid Kuidas seda kõrvaldada? vee pikemaajalisel keetmisel, vee destilleerimisel, kasutada vee pehmendajaid ioniitide abil Nimeta veekaredusest tingitud kahjulikke tagajärgi. rikuvad kuumutusnõusid, boilereid, torude ummistusi Milliseid metalle nimetatakse leelismetallideks? I A rühma metallid. on kõige metallilisemad elemendid, oksüdats aste on 1 ja väliskihi el valem on ns1 Iseloomusta neid lühidalt(füüsikalised omadused). Füüsikalised omadused - On pehmed, kergesti lõigatavad, madala sulamistemp, head soojus- ja elektrijuhid, keemilised omadused - reageerivad hapniku ja teiste mittemetallide...
LEELISED JA LEELISMULDMETALLID Leelismetallid on IA rühma metallid. Väliskihi elektronvalem ns1-s-metallid. Füüsikalised omadused: · Kerged · Pehmed · Kergsulavad Keemilised omadused: · Reag. veega (leelis + H2) 2Na + 2H2O = 2NaOH + H2 · Reag. hapnikuga 4Li + O2 = 2Li2O (oksiid) 2Na + O2 = Na2O2 (peroksiid) K + O2 = KO2 (hüperoskiid) · Leekreaktsioon muudavad leegi värvust. Na-kollane; K-helelilla Leelismetallide saamine ja kasutamine: Na+ ja K+ reguleerivad rakkude veesisaldust, südametegevust. Taimedele vajalikud kaaliumväetised (KCl, puutuhk). Leelismetallide ühendid: NaOH Seebikivi Seebivalmistamisel Na2CO3 (pesu)...
Mis on alus? Aine, mis koosneb metallioonist ja hüdroksiidioonist Mis on hape? Aine, mis annab lahusesse vesinikioone Mis on oksiid? Aine, mis koosneb kahest elemendist, millest 1 on hapnik. Mis vahe on aluselistel oksiididel ja happelistel oksiididel? Aluselised on metallioksiidid ja happelised on mittemetallioksiidid. Mis on leelised? Leelised on tugevad alused. Lahuse pH. (näitab vesinikiooni sisaldust lahuses) 0-7 happeline ülekaalus H+ -ioonid 7 suurem aluseline ülekaalus OH- -ioonid 7 neutraalne H+ ja OH- -ioone lahuses võrdselt Hapete omadused Hapukas maitse, muudavad indikaatorite värvust, reageerivad aluste ja aluliste oksiididega, reageerivad metallidega eraldades vesinikku. Hapete liigitus Hapniku sisalduse järgi, prootonite arvu järgi, tugevuse järgi. Mis on neutralisatsioonireaktsioon?
1.Milliseid ohutus nõudeid on vaja järgida? a)Leelis -ja leelis muld metallide kasutamisel.Kanda kummikindaid ja prille Laboris tuleb hoida petrooliumi või õli kihi all.Lõikamisel tuleb kanda kindaid ja kasutada kummikindaid. b)Leeliste kasutamisel-tugeva söövitava toimega Kasutada kaitse vahendeid .Tuleb vältida nahale sattumist.Kahjustatud kohta pesta veega. 2.Mis on kare vesi? Vees lahustunud kaltsiumi ja magneesiumi soolad põhjustavad vee karedust 3.Mööduvkaredus-Ca(HCO3)2,Mg(HCO3)2 kõrvaldatakse kuumutamisel.kuumutamisel Mittekarbonaatne-CaCl,CaSO4,MgCl2 kõrvaldatakse ioniitide abil. 4.Mis on katlakivi ja kuidas see tekkib?Tekkib vesinikkarb. Sisaldava kareda vee kuumutamisel. Rikub kuumutamise nõusid.Halvendab soojus juhtivust.Tekkib ülekuumenemine ja on täiendav el.kulu. 5.Millistes perj.ja rühmades asuvad siisdemet.?B rühmades ja 4,5,6,7 perioodis 6.Millise koostisega oks.kiht tekkib raua pinnale? a)niiskes õhus -4Fe+3O2=2Fe2O3...
Keemia 8. Klasside eksami konspekt 1. A) Puhtad ained, b) ainete segud, c) ainete füüsilised omadused. a) Koosneb ainult ühe aine osakestest. b) Koosneb mitme aine osakestest. c) Tahke, vedel ja gaasiline. 2. Keemialaboris kasutatavad anumad, 2b. ohutusnõuded. a) Katseklaas- katsete tegemiseks. b) Keeduklaas- lahuste valmistamine ja keetmine. c) Kolb- lahuste valmistamine, hoidmine. d) Mõõtesilinder- vedeliku koguse mõõtmine. e) Pipett- aine transportimine f) Tilgapipett- sama mis eelmine ainult et tilkades. g) Lehter- abi ümbervalamises. h) Portselankauss- tugevaks kuumutamiseks. i) Portselantiigel- lahtisel leegil kuumutamiseks. j) Tiiglitangid- tiigli hoidmiseks k) Uhmer- aine peenestamiseks. 2b. a) Jälgi tööjuhendit ja õpetajat. b) Ära sea ennast ja teisi ohtu. c) Ole ettevaatlik tulega. ...
OKSIIDID keemilised omadused: ALUSED keemilised omadused: 1. al.oksiid+hape=sool+ves 1. alus+hape=sool+vesi 2. al.oksiid+hap.oksiid=sool 2. alus+hap.oksiid=sool+vesi 3. tugevalt al.oksiid+vesi=leelis 3. leelis+sool=uus sool+uus alus (üks neist 4. nõrgalt al.oksiid+vesi=? sade, esimesed lahustuvad vees) 5. hap.oksiid+alus=vesi+sool 4. lahustumatu alus (t)= oksiid+vesi 6. hap.oksiid+al.oksiid=sool ALUSED saamine: 7. hap.oksiid+vesi=hape 1. akt.metall+vesi=leelis+vesinik 8. amf.oksiid+hape=sool+vesi 2. akt.met.oksiid+vesi=leelis OKSIIDID saamine: 3. sool+leelis=alus+sool (esimesed vees 1. metall+hapnik=oksiid lahustuvad) 2. mit.metall+hapnik=oksiid SOOL...
Ained, mis üldvalem: M(OH)n (H = Alus... Leeliste Alused ehk annavad lahusesse vesinik, M - metall) · ... + hape sool ja reageerimisel Tselluloosi hüdroksiidid hüdroksiidioone Oksüdatsiooniaste (v.a vesi soolade eraldamiseks · Leelised Vees lahustuv püsiva · ... + happeline oksiid vesilahusega puidust tugev alus oksüdatsiooniastmega) sool ja vesi FeCl3 + 3KOH kirjutatakse Fe(OH)3 + 3KCl · ... + soola vesilahus
koosnevad metallist ja märgitakse rooma ... + hape sool ja reageerimisel veega: puidust. hüdroksiidist. numbriga vesi LiO + HO 2LiOH Soola ja seebi sulgudesse. ... + happeline oksiid valmistamine(NaOH). · Leelised Vees lahustuv tugev sool ja vesi alus. ... + soola vesilahus Aluseline oksiid uus sool ja uus (tugev) + vesi = (vähelahustuv) alus leelis
Alused on ained mis annavad lahusesse hüdroksiidioone Liigitamine:Tugevad alused ehk leelised on NaOH, KOH, Ca(OH) 2 , Ba(OH)2Vees praktilist lahustumatud alused Cu(OH)2 , Al(OH)3 , Fe(OH)3 Nimetuse andmine: Kui metall on püsiva oksüdatsiooniastmega, moodustatakse nimetus järgmiselt KOH - kaaliumhüdroksiid Ca(OH)2 - kaltsiumhüdroksiid NaOH - naatriumhüdroksiid Al(OH)3 - alumiiniumhüdroksiid Kui metallil on muutuv oksüdatsiooniaste, näidatakse see järgmiselt:
Alused on hüdroksiidid, mis koosnevad enamasti metallioonist ja hüdr. ioonist OH-.(nt.NaOH,Mg(OH)2,Al(OH)3,Fe(OH)2)Hüdr.ioonide arv aluse valemis sõltub metalliiooni laengust.Vees lahustuvad hüdr.on leelised.Liigitamine:1)Vees lahustuvad alused-leelised,IA ja IIA(alates Ca)rühma metallide hüdroksiidid.2)Vees mittelahustuvad e.rasklahust uvad alused.Kõik ülejäänud alused.Nimetamine:Püsiva metalli o.-a.pu hul->metalli nimi+hüdr.(nt.KOH->kaaliumhüdroksiid,Mg(OH)2->ma gneesiumhüdr)Muutuva metallio.-a.puhul->metalli nimi+metalli o.-a. +hüdr(nt.Fe,Cr,Mn,Cu,Pb,Su)Cu(OH)2->vask(II)hüdr.Fe(OH)3->raud (III)hüdr.Füüs.omadused:1)Leelised:valged kristalsed ained,hügrosko opsed-seovad õhustvell,sööbivad,värvivad indik(fenoolftaleiin-ff)ff värvitu-aluseline keskkond-lillakasroosa,käega katsudes tunduvad libedad. 2)Rasklahust.alused:ei lahustu vees,enamasti värvilised ühendid,ei ole sööbivad,ei anna lahusesse hüdr.ioone ning seetõttu indikaatorite värv...
Laboratoorne töö Metallide keemilised omadused Tallinn 2011 Katse 1 Metallide reageerimine hapete lahustega Katsevahendid: Katseklaas, katseklaasihoidik, HCl, alumiinium, tsink, tina, raud, vask, tikud, piirituslamp. Katsekirjeldus: Valan katseklaasi 1-2 cm³ soolhappe lahjendatud lahust ja lisan sinna sisse erinevaid metalle. Vaatan kuidas erinevad metallid reageerivad. Vaatan, mis aktiivsusega need metallid on. 1. Soolhape + alumiinium / HCl + Al Panin katseklaasi soolhapet ja lisasime sinna alumiiniumtüki. Esialgu reaktsiooni ei toimunud. Soojendasin katseklaasi põletileegil. Reageerimisega läks veidi aega, pärast mida hakkas eralduma veidi vesinikku. Alumiiniumtükk hakkas natukene roostetama, kuid väga märgatavat muutust ei toimunud. Järeldan katsest, et Alumiinium on väheaktiivne metall. Katsetulemus ei ole kooskõlas pingerea asukohaga, kuid tean, et Alumiinium reageerib aeglaselt, sest teda katab õhuke oksii...
Põlema süttib lahusti aurude ja õhu segu, mitte lahusti ise Üldiselt Kui kinnises ruumis tekib lahusti aurude ja õhu segu, võib see suure jõuga plahvatada (nt benssiniaurud). Tahked ained on vähem tuleohtlikud. Plastmassid, mida tänapäeval kasutatakse ei ole eriti tuleohtlikud. Küll aga võib plastmasside lagunemisel tekkida mürgiseid gaasilisi lagunemissaadusi. SÖÖVITAV TOIME Kontsentreeritud happed ja leelised Kõige ohtlikum on 30% -line või kangem etaanhape ehk äädikhape Toitude maitsestamiseks ja marinaadide valmistamiseks aga kasutatakse 6% -list äädikhappelahust Leelised ja nende kontsentreeritud lahused sööbivad eriti tugevasti naha sisse ning söövitatud kohad paranevad kaua Kasutus Tänapäeval ei ole leelised kuigi sageli olmes kasutusel Igasuguste hapete ja leelistega töötades tuleb panna kummikindad kätte
Keemia 8 ja 9 klass. Alused & Happed Alused : Alused on ained mis koosnevad metallist ja OH rühmast. Aluseid on 2 liiki : leelised ja väga vähe lahustuvad alused. Leelised on söövitavad ja kui panna indikaator alusesse näitab see sinist värvi mis tähendab et tema pH on 7(KÕIK ALUSED). Leelised on IA ja II A alates kaltsiumist. Need ained on söövitavad ja kui nendega teha katseid tuleb olla väga ettevaatlik. Neutralisatsioonireaktsioon on aluse ja happe reageerimine , millest tekib sool ja vesi. Sellega tehakse aine neutraalseks (pH 0). Aluseline oksiid on Metall ja Hapnik koos. Aluselisest oksiidist on kõige lihtsam alust saada. Näide : CaO + H2O -> Ca(OH)2 Nii saab aluselisest oksiidist hüdroksiidi. On ka selliseid metalle, mis ei anna hüdroksiidi ioone
vesinikioonid (H+) dissotsiatsioonil eralduvad hüdroksiidioonid metalliioonid) ja anioonidest (happejäägiioonid) Brønsted: Ained, mis loovutavad prootoneid (OH) Brønsted: aineosakesed, mis seovad (p+ = H+) prootoneid Liigitus Üheprotoonsed: HCl , HNO3 ...... Leelised vees lahustuvad hüdroksiidid Mitmeprootonilised: H2SO4 , H3PO4 .... Ia ja enamus IIa rühma metallidest Lihtsoolad : NaCl, K2SO4 , (NH4)3PO4 annavad leeliseid nemad on ka tugevad Vesiniksoolad NaHCO3 , Ca(HCO3)2, KH2PO4
Alused ehk hüdroksiidid on liitained mis koosnevad 1, või mitmest OH rühmast. Saamine 1)Metallioksiid+Vesi Na2O+H20 -> 2NaOH 2)Aktiivne metall+Vesi 2Na+2H2O -> 2NaOH+H2 3)Soolade vesilahuste elektrolüüsil 2NaCl+2H2O -> 2NaOH +H2+Cl2 4)Vees lahustuv alus+sool CuSO4+2NaOH -> Na2SO4+Cu(OH) 2 Liigitus: Veeslahustuvad hüdroksiidid ehk leelised (LiOH;BaOH) ja vees lahustumatud(Cu(OH) 2;Zn(OH) 2). Keemilised omadused: Leelised 1)Reageerivad hapetega 2NaOH+H2SO4 -> Na2SO4+2H2O 2)Reageerivad vees lahustuvate sooladega CuSO4+NaOH -> Na2SO4+Cu(OH) 2 3)Reageerivad happeliste oksiididega Ca(OH) 2+CO2 -> CaCO3+H2O Lahustumatud 1) Reageerivad hapetega Cu(OH) 2+H2SO4 -> CuSO4+2H2O 2)Kuumutamisel lagunevad
Hüdroksiidid Edgar Leht, Tauri Küla 10A 2010 Alused ehk hüdroksiidid · Keemilised ained, mis annavad lahusesse hüdroksiidioone · koosnevad metallioonidest ja hüdroksiidioonidest (OH-). Liigitus · LEELISED - vees lahustuvad hüdroksiidid Mendelejev tabeli I a & II a rühma elementide ühendid. · VEES PRAKTILISELT MITTELAHUSTUVAD ALUSED Kõikide ülejäänute metalli elementide ühendid. Hüdroksiidide keemilised omadused · Kõik hüdroksiidid reag. hapetega. Tulemus: sool ja vesi: KOH+HCl=KCl+H2O · Reag happeliste oksiididega. Tulemus: Sool ja vesi: Ca(OH)2+CO2=CaCO3+H2O · Leelis reag. vees lahustuva soolaga, kui vähemalt üks saadustest on
!!!! Mitteelektrolüüdid Ei esine lahustes ioonidena, vaid lahuses on molekulid või aatomid. Oksiidid, lihtained, enamus orgaanilisi aineid. Hüdrolüüs ainete reagreerimine veega, tekib happeline, aluseline või neutraalne keskkond. Lahuse keskkond 1) Oksiidid aluseline (IA ja II alates Ca) Na2O+H2O --> 2NaOH Happeline(mittemetallioksiidid, v.a. SiO2) N2O5+H2O--> 2HNO3 2) Happed lahustuvad vees ja annavad happelise keskkonna 3) Alused leelised lahustuvad vees ja annavad aluselise keskkonna. Rasklahustuvad alused ei lahustu vees ja annavad neutraalse keskkonna 4) Soolad Na2CO3 NaOH H2CO3 Tugev alus nõrk hape Aluseline keskkond Orgaanilises keemias Aluseline amiinid(NH2) Happeline orgaanilised happed (COOH), alkoholid(OH) lahus neutraalne
Mis on neutralisatsiooni reaktsioon ? Millised ained seejuures reageerivad ja millised saadused tekivad ? Neutralisatsiooni reaktsioon on happe ja aluse vaheline reaktsioon, kus saaduse keskkond on neutraalne, mille saadusteks on sool + vesi. Missugused on tähtsamad ohutusnõuded aluste kasutamisel ? Käes tuleks kanda kindaid, silmade kaitseks prille ja keha võimalikult kinni katta. Kuidas liigitatakse aluseid ? Kas kõik alused on hüdroksiidid ? On vees hästilahustuvad tugevad alused leelised ja nõrgad alused ( enamasti vees praktiliselt lahustumatud ). Kõik alused ei ole hüdroksiidid aga nad kõik sisaldavad anioonidena hüdroksiidioone. Mis on leelis ? Mille poolest nad erinevad teistest alustest ? Leelis on vees hästilahustuv aluseliste omadustega hüdroksiid. Nad erinevad lahustuvuse poolest. Kuidas käitub enamik hüdroksiide kuumutamisel ? Enamik hüdroksiide lagunevad oksiid + vesi 'ks . Kuidas on võimalik saada järgmisi hüdroksiide : LiOH, Cu(OH)2 ?
Elektrolüüdid Elektrolüüdid-ained mis vesilahustes ja sulatatud olekus jagunevad täielikult või osaliselt ioonideks. Elektrlüüdid- happed, alused ja soolad. Ioon- laenguga aatom või aatomite rühmitus. Katioon-positiivse laenguga ioon. Anioon-negatiisve laenguga ioon. Elektrolüütiline dissotsiatsioon on lahustumisega kaasnev aine jagunemine ioonideks. Hüdraatumine ehk hüdratatsioon on lahustunud aine osakeste seostumine vee molekulidega. Mitteelektrolüüdid-ained mis ei esine lahuses mitte ioonide, vaid neutraalsete molekulidena. Tugevad elektrolüüdid- esinevad lahuses ainult ioonidena. Nõrgad elektrolüüdid- esinevad aines nii ioonidena kui ka molekulidena. T elektrolüüdid- soolad, tugevad happed ja tugevad alused (leelised) Soolad: CaCl2, K2SO4, CuSO4, NaCO3, CH3COONa Tugevad happed: HCl, HBr, HI, H2SO4, HNO3 Tugevad alused (leelised): LiOH, NaOH, KOH, Ca(OH) 2, Ba(OH)2 N elektrolüüdid- n...
liikmed (leelised). Vesilahus on käega katsudes libe, pesev ja sööbiv toime. Peaaegu kõik värvitud. 5. Keemilised omadused: Reageerivad hapetega, saaduseks sool + vesi, nim ka neutraliseerimisreaktsioon. NaOH + H2SO4 => Na2SO4 + H2O Peaaegu kõik reageerivad happeliste oksiididega, tekib sool + vesi. 2NaOH + SO2 => Na2SO3 + H20 Leelised reageerivad sooladega, tekib uus alus ja sool. 6NaOH + Al2(SO4)3 => 2AL(OH)3 + 3Na2SO4 Enamik hüdroksiide laguneb kergesti kuumutamisel, va leelised, tekib aluseline oksiid ja vesi. 2Fe(OH)3 =>t Fe2O3 + 3H2O Amoforteersed alused reageerivad leelistega (Al, Zn, Pb), tekib kummalise koostisega sool. NaOH + Zn(OH)2 => Na2(Zn(OH)4) 3. Happed: Koosnevad vesinikust ja happejäägist. H2SO4 Jagunevad: · oksohapped · hapnikuta happed Jaotatakse happed ka 1,2 ja enam prootonilisteks (vesiniku aatomite arvu järgi) Happejäägi iooni laeng võrdub happes olevate vesinike arvuga. 2. nimetused:
.) Vähemaktiivsete metallide hüdroksiidid nõrgad alused, lahustuvad vees halvasti. Soolad ained, mis koosnevad aluse katioonidest ja happe anioonidest. · Al. Oksiid + hape sool + vesi · Al.oksiid + vesi hüdroksiid (nõrgalt aluselised oksiidid veega ei reageeri!) · H. oksiid + alus sool + vesi · h. oksiid + al.oksiid sool · h. oksiid + vesi hape · hüdroksiid metallioksiid + vesi (leelised on vastupidavad) · leelis + vesi alus (hüdroksiid) (aint leelised!) · alus + sool sool + alus · metall + mittemetall sool · metall + hape sool + vesinik (pingerida) · metall + sool metall + sool (metallid reageerivad ainult vees lahustuvate sooladega) · alus + hape sool + vesi (neutralisatsioonireaktsioon)
Hüdroksiidid on keemilised ained, mis annavad lahusesse hüdroksiidioone. Hüdroksiidid koosnevad metallioonidest ja hüdroksiidioonidest (OH-1). Hüdroksiide jaotatakse:1) veeslahustuvad hüdroksiidid ehk leelised- aktiivsete I alarühma ehk leelismetallide ja II alarühma Kaltsiumist allapool asuvate elementide ehk leelismuldmetallide hüdroksiid. 2)vees mittelahustuvad hüdroksiidid(nõrgad alused)- enamuse metallide hüdroksiidid. Hüdroksiidid ehk alused on ained, mis reageerivad hapetega, andes soola ja vee. Hüdroksiidid koosnevad metalliioonidest ja hüdroksiidioonidest (OH -1). Liigitatakse: 1) leelised- vees lahustuvad hüdroksiidid. Need on I a & II a rühma elementide ühendid, välja arvatud Be(OH)2, praktiliselt ei lahustu ka Mg(OH)2 ). 2) vees praktiliselt mittelahustuvad hüdroksiidid - kõik ülejäänud. Leeliseid saadakse 3) Alustegapuutume me kokku iga päev. Näiteks kraanivesi on väga nõrgalt aluseline, aga sellegipoolest ALUSELINE. M...
· Leelis- ja leelismuldmetallid Leelismetallid I Asetus perioodilisussüsteemis ja aatomi ehitus Leelismetallid on IA rühma metallid. Nimetus "leelismetallid" on tuletatud sellest, et nende metallide hüdroksiidid on leelised (st. vees lahustuvad hüdroksiidid). II Leelismetalliühendite kindlakstegemine Leelismetallid ja nende ühendid värvivad leeki. Na-ühendite toimel värvub leek kollaseks, Kühendite toimel violetseks, Li-ühendite toimel punaseks. III Leelismetallide omadused Füüsikalised omadused · kerged · pehmed (saab noaga lõigata) · hõbevalged · madala sulamistemperatuuriga · hea elektri- ja soojusjuhtivusega Keemilised omadused
Keemia oksiid koosneb kahest elemendist, millest üks on hapnik Aluselised oksiidid on aluseliste omadustega, reageerivad hapetega Happelised oksiidid- on happeliste omadustega, reageerivad alustega Tugeval aluseliste oksiidide - reageerimisel veega tekivad tugevad alused ehk leelised. Enamiku happeliste oksiidide reageerimisel veega tekib vastav hape. Veega ei reageeri nõrgalt aluselised ning ka mõned happelised oksiidid nt SiO2 Oksiidide põhilised saamisvõimalused : 1. vastavate lihtainete reageerimine hapnikuga, 2. suhteliselt ebapüsivate hapnikku sisaldavate ühendite lagunemine Aluselised oksiidid on metall oksiidid(ainult I ja II A rühma metallid reageerivad veega) ja happelised oksiid on mittemetal oksiid.
AINETE PÕHIKLASSID JA NENDE VAHELISE SEOSED . Oksiidid. *Oksiid-aine, mis koosneb kahest elemendist, millest üks on hapnik(o/a-II). -aluselised oksiidid (metall + hapnik) reageerivad hapetega. Tugevalt aluseliste oksiidide reageerimisel veega tekivad leelised ehk lahustuvad alused(tugevad alused). Nt. NaOH -happelised oksiidid(mittemetall + hapnik) reageerivad alustega. Happeliste oksiidide reageerimisel veega tekib enamasti hape. Nt. H2SO4. -amfoteersed oksiidid (Al2O3;Cr2O3;Fe2O3;ZnO) reageerivad nii aluste kui hapetega alustega reageerimisel tekivad kompleksühendid. Nt Na[Al(OH)4]. Amfoteersed oksiidid veega ei reageeri. -Neutraalsed oksiidid(CO;NO;N2O) on mittemetallioksiidid, mis veega reageerides hapet ei anna.
3. Lahusti iseloom Mida suurem on lahusti molekulide polaarsus, seda enam ta nõrgendab ioonilisi sidemeid 4. Elektrolüüdi omadustest 5.Samanimelisi ioone sisaldava elektrolüüdi lisamine Elektrolüüdid – ained, mille vesilahused sisaldavad ioone– Kuna ioonid on laengukandjad, siis juhivad elektrolüütide lahused elektrivoolu .Ioonilise ja tugevalt polaarse kovalentse sidemega ained• Tugevad elektrolüüdid – esinevad lahuses ainult ioonidena (tugevad happed, leelised ja soolad) • Nõrgad elektrolüüdid – lahuses esinevad nii molekulid kui ka ioonid (nõrgad happed ja alused)’ Mitteelektrolüüdid – ained, mille vesilahused ei sisalda ioone– Ei juhi elektrivoolu (laengukandjaid pole)• Lahuses on ainult molekulid (paljud orgaanilised ained, lihtained, oksiidid)• Nõrgalt polaarse ja mittepolaarse kovalentse sidemega ained Elektrolüütiline dissotsiatsioon – elektrolüütide jagunemine ioonideks nende lahustumisel vees
hapetega a) eraldub gaa SED Na20+H20-2NaOH v.a.konts. HISO,ja HN03 . Reag. sooladega (ainult leelised) H2S04+NaC1-NaHSO,+HC1t Reag. hapetega CuO+2HC1-CuCleH20 Reag. aluseliste Oksiididega 2HCl*Cuo- b) tekib nórgem vdi lenduv .Reag, happel. oksiididega cuC12+E-120 Leelised muudavad ff. punaseks hape SOz+CaO-CzCOJ . Reag. alustega HCl+NaOH-NaC1+H20 . Lahustumatud alused lagunevad NaNOJ+HSOFNaHS04+H kuumutamisel oksiidideks . Reag. leelistega (tekib Sade) Happelised oksiidid: neutralisatgioonireaktsiaon CuO+H20 1. Reag. veega (mitte k0ik) S02+H20- Reag
Aineklassid Mõisted: 1) Oksiidid on liitained, mis koosnevad kahest elemendist, millest üks on hapnik 2) Happed on liitained, mis koosnevad happevesinikust ja happeanioonist 3) Alused on liitained, mis koosnevad metallikatioonist ja hüdroksiidioonist 4) Soolad on liitained, mis koosnevad metallikatioonist ja happeanioonist 5) Leelised on vees lahustuvad tugevad alused 6) Aluselised oksiidid on oksiidid, mis reageerivad happega moodustades soola ja H2O 7) Amfoteersed oksiidid on oksiidid, mis reageerivad nii happe kui alusega 8) Inertsed oksiidid on oksiidid, mis ei reageeri happe ega alusega 9) Neutralisatsioonireaktsioon on happe ja aluse vaheline reaktsioon 10) Happe lahuse toimul muutub metüüloranž punaseks, lakmus punaseks 11) Aluse lahuse toimel muutub fenoolftaleiin punaseks, lakmus siniseks
H2SO3väävlishape HNO2lämmastikushape H2SO4 väävelhape http://web.zone.ee/gagriigieksam/KeemiaRE_Aineklassidteooria.doc; õppematerjal täiendatud 2012, Ave Vitsut,Viljandi Gümnaasium Alused – hüdroksiidid koosnevad tavaliselt metalli katioonist ja ühest või mitmest hüdroksiidioonist; NaOH, Ca(OH)2, Fe(OH)3 o Tugevuse järgi Tugevad alused ehk leelised – IA ja IIA al Ca-st metallide hüdroksiidid – leelised; lahustuvad vees: NaOH, Ca(OH)2... Nõrgad alused – ülejäänud metallide hüdroksiidid; tavaliselt ei lahustu vees (va NH3∙H2O – ammoniaakhüdraat): Fe(OH)3, Cu(OH)2 Hüdroksiidide nimetused I,II,III A rühma metallide hüdroksiidide nimetustes ei märgita metalli laengut; näiteks Ca(OH)2 kaltsiumhüdroksiid
5. Neutralisatsioonireaktsioon on aluse ja happe vaheline reaktsioon. Neutralisatsioonireaktsioonil reag. omavahel happe vesinikioonid ja aluse hüdroksiidioonid, moodustades väga püsivad vee molekulid. 6. Sattumisel kätele või riietele- pesta veega, loputada lahjendatud äädikhappe lahusega ja uuesti veega. 7. Alused liigitatakse: Vees hästi lahustuvad, tugevad alused (leelised), nõrgad alused-vees praktiliselt lahustumatud. Kõik alused ei ole hüdroksiidid, aga enamik. 8. Leelised on vees lahustuvad tugevate aluseliste omadustega hüdroksiidid. Valged tahked ained, mille Kristallivõre koosnrb metalli katioonidest ja hüdroksiidioonidest. Vesilahused on värvusetud. 2+ + 2+ 9. vastavad metalliioonidele hüdroksiidide valemid Ba Ba(OH)2 ; Cu CuOH ; Fe Fe(OH)2 10. Aluseline oksiid+vesi= hüdroksiid+vesinik 2Na2O+ 2H2O=4Na OH + H2 BaO+H2 O= Ba(OH) 2 11
Olustvere Teenindus- ja Maamajanduskool Loodusmajandus I Talvi Põldma LEESLISELISED AINED Referaat Olustvere 2010 Sisukord Alused Nimetuste määramine Liigitamine Saamine Keemilised omadused Kaltsiumhüdroksiid Kasutatud kirjandus Alused Alused ehk hüdroksiidid on ained, mis reageerivad hapetega ja annavad soola ja vee. (Tegelikult ei ole "alus" ja "hüdroksiid" kattuvad mõisted.) Alused koosnevad metallioonist ja hüdroksiidioonist. Alused on ained, mis liidavad prootoni (H+). Hüdroksiidid koosnevad metalliioonidest ja hüdroksiidioonidest (OH-). Hüdroksiidiooni laeng on -1, seega peab metalliioonide arv valemis olema alati 1 ja hüdroksiidioonide arv võrdub metalli ioonilaengu või oksüdatsiooniastmega. Kõikide hüdroksiidide valemid avalduvad kujul Men+(OH)n - n . Nimetuste määramine Kui metal...
Keemilise sideme liik ja ainete omadused Molekulaarsed ained koosnevad molekulidest ( mittemetallid, mittemetalli elementide ühendid, orgaanilised ained ) Molekulide sees on aatomid omavahel seotud kovalentsete sidemete abil Molekulvõre kristallvõre, mis koosneb omavahel suhteliselt nõrgalt seotud molekulidest. Mittemolekulaarsed ained koosnevad väga suurest hulgast aatomitest või ioonidest, mis on omavahel seotud keemiliste sidemetega. ( soolad, leelised, ioonsed oksiidid, metallid ) Kovalentsete sidemetega mittemolekulaarsed ained (teemant, kvarts, grafiit, punane fosfor, räni). Aatomvõre kristallvõre, mille keskmetes paiknevad kovalentsete sidemetega seotud aatomid. Tahketes ainetes ja vedelikes seovad molekule suhteliselt nõrgad füüsikalised tõmbejõud nn molekulidevahelised jõud Grafiit Teemant
Tähtsamad metallid ja nende ühendid. Kõik esimese A rühma metallid on leelismetallid, sest nende hüdroksiidid (NaOH, KOH) on tugevad leelised: süüvitava toimega, Teise A rühma metallidest, alates Kaltsiumist on muldleelised. Ka nende hüdroksiide nimetatakse leelisteks. Kõik b-rühma metallid on siirde e. ülemineku metallideks. Esimese ja teise rühma A rühma metallid on aktiivsed metallid. Sinna kuuluvad leelismetallid jaleelismuld metallid. Kuna nende väliskihil on üks kuni kaks elektroni. Siis need elemendid loovutavad väliskihi elektrone väga aktiivsed metallid.
ALUSED e. HÜDROKSIIDID on liitained, mis koosnevad metallist ja hüdrooksiidist. Alused reageerivad 1) HAPETEGA - tekib sool ja vesi NaOH + H2SO4 = Na2SO4 + H2O (tasakaalustamata) 2) HAPPELISTE OKSIIDIDEGA tekib sool ja vesi 2NaOH + CO2 = Na2CO3 + H2O 3) AINULT LEELISED REAGEERIVAD SOOLADEGA tekib uus sool ja uus alus 3NaOH + AlCl3 = 3NaCl + Al(OH)3 4) AINULT VEES MITTELAHUSTUVAD HÜDROKSIIDID KUUMUTAMISEL LAGUNEVAD tekib oksiid ja vesi t¤ 2Fe(OH)3 = Fe2O3 + 3H2O
Paljud mürgised kemikaalid imenduvad läbi naha ja sellepärast ei tohi nad nahale sattuda. · Kemikaalidega töötades tuileb olla väga ettevaatlik tuleohutusega. Paljude keemiatooted on väga tuleohtlikud ja kergesti süttivad. Põlema eisütti mitte vedellahusti ise, vaid selle auru ja õh segu. Sellepärast on soovitatav teha kõik tööd ja uurimused kemikaalidega tõmbekapis. · Kontsentreeritud happed ja leelised on söövitava toimega, nende käsitlemisel tuleb kanda kaitseriietust. · 1 - · Kui leelis või hape satub nahale, tuleb kiiresti kokkuputunud koht vee alla panna. Kui oled koolis teavita juhtunust õpetajat, kui oled laboris helista kiirelt arstile ja palu kaastöötajatelt abi. Paljud leelised ja happed on väga tugevalt söövitavad ( HCl,
Elektrolüüdid ja mitteelektrolüüdid. Elektrolüüt on aine, mis sisaldab ioone ja tänu sellele ta juhib sulatatud olekus või vesilahuses elektrivoolu. Elektrolüüdid sisaldavad ioone juba tahkes olekus või moodustavad neid lahustumise protsessis. Tahkes olekus ei juhi elektrolüüdid elektrivoolu, sest tugeva ioonilise sideme tõttu ei suuda ioonid kritallvõrest väljuda. Ioonide liikumine saab võimalikuks kas tahke aine soola sulatamisel või selle lahustamisel vees. Seega elektrijuhtivuse kaudu saabki kindlaks määrata, kas aine on elektrolüüt või mitte. -Keemilise sideme isloomu järgi jaotus: 1) Ioonilised elektrolüüdid. Esindajad: kõik soolad, tugevad alused(leelised). Nt. NaCl(keedusool), LiOH. 2) Molekulaarsed ehk polaarsed elektrolüüdid. Esindajad: happed ja enamik hüdroksiide. Nt. Al(OH)3, H2SO4. -Elektrolüüdid jaotatakse veel: 1) Tugevad elektrolüüdid -> tugevad happed, leelised ja soolad (...
(KO2). · Naatriumi keemilised omadused (NB! Joonisel olevad võrrandid ei ole tasakaalus): 3. Tähtsamaid ühendeid · Leelismetallide oksiidid tahked valged ained, tugevad aluselised omadused. Reageerimisel veega tekib leelis (Na2O + H2O 2NaOH). Naatriumperoksiidi reageerimisel veega tekib lisaks hüdroksiidile ka veel vesinikperoksiid (H2O2). · Leelismetallide hüdroksiidid vees hästi lahustuvad tugevad leelised. Neelavad õhuniiskust (hügroskoopsed). · NaOH keemilised omadused (NB! Joonisel olevad võrrandid ei ole tasakaalus): · Leelismetallide soolad enamasti valged kristalsed ained. Vees hästi lahustuvad. Leelismetalli hüdroksiidi ja tugeva happe soola vesilahus on neutraalne (NaCl, K2SO4). Leelismetalli hüdroksiidi ja nõrga happe soola vesilahus on aluseline (Na2CO3 - sooda). · Na2CO3 (sooda) - kasutatakse pesuvahendina.
Leelis ja leelismuldmetallid 1. Leelis- ja leelismuldmetallide iseloomulikud füüsikalised (kõvadus, sto, tihedus) ja keemilised omadused; Na, K, Mg, Ca levik maakoores ja tähtsus elusloodusele Leelismetallid on IA rühma metallid. Nimetus "leelismetallid" tuleneb sellest, et nimetatud metallide hüdroksiidid on leelised (st. vees lahustuvad hüdroksiidid). Füüsikalised omadused Keemilised omadused · kerged · pehmed (saab noaga lõigata) · Keemilise aktiivsuse tõttu ei · hõbevalged leidu neid looduses lihtainena · madala sulamistemperatuuriga (ehedana), vaid ainult ühendite
Keemia Alused Alused on ained, mis annavad vesilahusesse hüdroksiidiioone OH- NaOH->Na+ + OH- Tüüpilised alused on hüdroksiidid. Hüdroksiidid koosnevad metallioonidest ja hüdroksiidiioonidest. Hüdroksiidide liigitamine Vees lahustuvuse järgi. Vees lahustuvad hüdroksiidid ehk leelised (tugevad alused)- Aktiivsete metallide (|A rühma ja ||A rühma alates Ca)hüdroksiidid. Vees praktiliselt lahustumatud hüdruoksiidid (nõrgad alused)- Enamus metallide hüdruoksiidid. Aluste keemilised omadused Aluste sarnased üldised omadused on tingitud OH- Ioonidest Happeliste oksiididega Vahetus(Vastava happe ja aluse vahel) CO2+Ca(OH)2->CaCO3 +H2O
Alused e. hdroksiidid- Leelised- Na Oh-naatriumhdroksiid K OH-kaaliumhdroksiid Ca Oh-kaltsiumhdroksiid Ba Oh-baariumhdroksiid Vees lahustumatud alused- Fe Oh-raudhdroksiid Fe Oh-raudhdroksiid Cu Oh-vaskhrdoksiid Al Oh-alumiinuimhdroksiid ALUSED KOOSNEVAD MATALLID JA OH RHMAST Oh-hdroksiidirhm 8:15 19.02.2009 Liitained: Oksiidid- 2 elementi,ks on 0 N2O3-alumiiniumoksiid Fe2O3-raudoksiid SO3-vveltioksiid N2O3-dilmmastikpentaoksiid Alused- Metall-OH NaOH-Na-hdroksiid Ca(OH)2-Ca-hdroksiid Fe(OH)2-raudhdraksiid Happed- Vesinik-happeanioona HCl-soolhape H2SO4-vvelhape H3PO4-fofforhape Soolad- Metall-happeanioon NaCl-naatriumkloriid CaSO4-kaltsiumsulfaat K3PO4-kaaliumfosfaat
.. Hapnikhapped: HNO3, H2SO4, H3PO4... o Tugevuse järgi Tugevad happed: H2SO4 > HNO3 > HCl Keskmise tugevusega happed: H3PO4 ja H2SO3 Nõrgad happed: H2S > H2CO3 (nõrgim anorgaaniline hape) · Alused (koosnevad tavaliselt metalli katioonist ja ühest või mitmest hüdroksiidioonist; NaOH, Ca(OH)2, Fe(OH)3...) o Tugevuse järgi Tugevad alused ehk leelised IA ja IIA al Ca-st metallide hüdroksiidid leelised; lahustuvad vees: NaOH, Ca(OH)2... Nõrgad alused ülejäänud metallide hüdroksiidid; tavaliselt ei lahustu vees (va NH3H2O ammoniaakhüdraat, vananenud ammooniumhüdraat NH4OH): Fe(OH)3, Cu(OH)2... · Soolad (koosnevad tavaliselt metalli katioonist ja happeanioonist; NaCl, CaSO4, Fe2(SO4)3...)
mis saaksid vabalt liikuda. Ammoniaagi lahus juhib vähe elektrit, sest seal pole palju vabu ioone, aga ammoniaagi vesilahus juhib, sest seal ioone nagu muda, kuna vesi lõhkus ammoniaagisidemed. ELEKTROLÜÜTIDE JAOTUS MITTEELEKTROLÜÜDID TUGEVAD (palju ioone) NÕRGAD (vähe ioone) 1. Lahuses ei ole ioone. SOOLAD TUGEVA LEELISED NÕRGAD NÕRGAD 2. Lahus ei juhi D HAPPED ALUSED elektrivoolu. HAPPED 3. O2 CaCl2, H2SO4; KOH, H2S; Zn(OH)2; 4. Orgaanilised ained (CH4; K2SO4, HNO3; Ca(OH)2, H2SO3; Cu(OH)2; C5H12O6; CH3CH2OH;
.. Hapnikhapped: HNO3, H2SO4, H3PO4... o Tugevuse järgi Tugevad happed: H2SO4 > HNO3 > HCl Keskmise tugevusega happed: H3PO4 ja H2SO3 Nõrgad happed: H2S > H2CO3 (nõrgim anorgaaniline hape) Alused (koosnevad tavaliselt metalli katioonist ja ühest või mitmest hüdroksiidioonist; NaOH, Ca(OH)2, Fe(OH)3...) o Tugevuse järgi Tugevad alused ehk leelised – IA ja IIA al Ca-st metallide hüdroksiidid – leelised; lahustuvad vees: NaOH, Ca(OH)2... Nõrgad alused – ülejäänud metallide hüdroksiidid; tavaliselt ei lahustu vees (va NH3∙H2O – ammoniaakhüdraat, vananenud ammooniumhüdraat NH4OH): Fe(OH)3, Cu(OH)2... Soolad (koosnevad tavaliselt metalli katioonist ja happeanioonist; NaCl, CaSO4, Fe2(SO4)3...)
Sest happed võivad omakorda nahka, riideid kahjustada ja tekitada söövitavadia auke 5. Mis on alus? Mis on sarnas erinevate aluste koostises? Ained, mis annavad lahusesse hüdroksiidioone. Sarnasuseks see, et koosneb nii vesinikust kui ka hapnikust. 6. Millest on tingitud alustele iseloomulikud omadused? Nim neid omadusi Nende lahuses esinevatest hüdroksiidioonidest. Sööbiv toime, võime muuta indikaatorite värvust. 7. Mis on leelised? Mille poolest erinevad teistes alustes? Tugevad alused, jaotuvad täielikult ioonideks. 8. Millisteks ioonideks jagunevad järgmised hüsroksiidid lahuses: KOH, Ba(OH)2 9. Iseloomusta naatriumhüdroksiidi omadusi Valge, tahke aine, lahustub väga hästi vees, eraldades palju soojust, (seebikivi) 10. Kirjuta järgmistele metallikatioonidele vastavate hüdroksiidide valemid: Mg, Cu, Fe, Cr Lk69 1
OKSIIDIDE REAGEERIMINE VEEGA NB! Lõpeta näidete eeskujul punktides I. ja II reaktsioonivõrrandid. I. aluseline oksiid + vesi alus Veega reageerivad ainult IA ja IIA metallide al Ca-st oksiidid, tekib tugev alus ehk leelis. (Meenutame: olid ju leelised IA ja IIA al Ca-st metallide hüdroksiidid.) Na2O + H2O 2 NaOH CaO + H2O K2O + H2O Fe2O3 + H2O II. Happeline oksiid + vesi hape Happelise oksiidi reageerimisel veega tekib oksiidile vastav hape. (Meenutame: oksiidide ja hapete vastavused on põhikoolis pähe õpitud, tuleb korrata!) Oksiid Hape CO2 H2CO3 SO2 H2SO3 SO3 H2SO4 SiO2 H2SiO3 N2O5 HNO3 P4O10 H3PO4 H2O + CO2 H2CO3 SO2 + H2O P4O10 + H2O SO3 + H2O
Kordamisküsimused · LAHUS koosneb lahustist ja lahustunud ainest. · KÜLLASTUNUD LAHUS on on lahus, milles antud temperatuuril ei saa enam sama ainet veel lahustada.(suhkrusiirup) · KÜLLASTUMATA LAHUS on lahus, milles saab sama ainet veel lahustada. (morss, suhkruvesi) · ELEKTROLÜÜT on aine, mille vesilahus sisaldab ioone.Tugevad elektrolüüdid(tugevad happed, leelised ja soolad) ja nõrgad elektrolüüdid(nõrgad happed ja alused). · MITTEELEKTROLÜÜT on aine, mille vesilahus ei sisalda ioone. Mitteelektrolüüdid on paljud org. ained, lihtained ja oksiidid. · ELEKTROLÜÜTILINE DISSOTSATSIOON on ioone sisaldavate lahuste tekkeprotsess elektrolüütide lahustamisel vees. ( FeBr Fe + 2Br) · KOLLOIDLAHUS on ebapüsiv lahus ehk pihus, mille keskkond on vedel, aine ise tahke ja osakesed on väiksemad kui suspensioonis
Keemia Alused ehk hüdroksiidid. E(OH) E metalliioon (pos. laeng), OH hüdroksiidioon. Tekkimine: Aluseline oksiidi reageerimisel veega. Na2O + H2O= 2NaOH; K2O + H2O=2KOH, CaO + H2O = Ca(OH)2 . Need kõik on vees lahustuvad hüdroksiidid ehk leelised. Leeliste omadused: 1) Vees lahustuvad ained 2) Muudavad indikaatori värvi 3) Kuumutamisel ei lagune 4) Need on söövitava toimega. Indikaatorid: Lakmus sinine, fenoolftalein (ff) punane. Leeliste lahustumisel vees tekivad ioonid: NaOH = Na++OH-, KOH = K+ +OH-, Ca(OH)2 = Ca2++2OH-. Nimetused: NaOH Naatriumhüdroksiid Cu(OH)2 Vask (II)hüdroksiid Raskelahustuvad hüdroksiidid Metallioksiidid veega ei reageeri, vees ei lahustu CuO, FeO, ZnO