Aineklassid Sisukord Aineklassid Oksiidid Happed Alused Soolad Tuntumad ained Millest saab mis? Aineklassid Hape Oksiidid (happeline, aluseline) Sool Alus Oksiidid Oksiid on kahes elemendist koosnev ühend, millest üks on hapnik. Oksiidid jagunevad Happeline oksiid Aluseline oksiid Hapetele vastavaid oksiide Aluseline oksiid on alusele nimetatakse happelisteks (hüdroksiidile) vastav oksiid. oksiidideks. Enamasti on Happelised oksiidid mitte- metallioksiid. Oksiide nimetatakse a)Oksüdatsiooniastme kaudu b)Eesliidete järgi Haped Haped on liitained, mis annavad lahusesse. vesinikioone. Hapete iseloomulikuks on hapu maitse.
Keemia kordamisküsimused 9.klassile 1.Aineklassid ja nendevahelised seosed OKSIIDID-koosnevad kahest elemendist, millest üks on hapnik (O). Oksiidide liigitus:1) Aluselised oksiidid-metalli oksiidid: # tugevalt aluselised, ( leelis ja leelismuld metallid IA ja IIA alates Ca metallide oksiidid) # nõrgalt aluselised oksiidid- vähem aktiivsete metallide oksiidid. 2) Happelised oksiidid-mitte metallide oksiidid. Keemilised omadused: happeline oksiid + vesi = vastavhape ! Veega ei reageeri SiO N: dilämmastikpentaoksiid + vesi happeline oksiid + alus = sool +vesi HAPPED-ained, mis annavad lahusesse vesinikioone. Hapete liigitus erinevate tunnuste järgi:1) Hapniku sisalduse järgi: # hapniku mittesisaldavad happed N: # hapnikhapped N: 2) Prootonite arvu järgi: # üheprootonilised happed N: # mitmeprootonilised happed N: 3) Tugevuse järgi: #
Keemia kordamisküsimused 9.klassile põhikool 1.Aineklassid ja nendevahelised seosed OKSIIDID-koosnevad kahest elemendist, millest üks on hapnik (O). Oksiidide liigitus:1) Aluselised oksiidid-metalli oksiidid: # tugevalt aluselised, ( leelis ja leelismuld metallid IA ja IIA alates Ca metallide oksiidid) # nõrgalt aluselised oksiidid- vähem aktiivsete metallide oksiidid. 2) Happelised oksiidid-mitte metallide oksiidid. Keemilised omadused: happeline oksiid + vesi = vastavhape ! Veega ei reageeri SiO N: dilämmastikpentaoksiid + vesi happeline oksiid + alus = sool +vesi HAPPED-ained, mis annavad lahusesse vesinikioone. Hapete liigitus erinevate tunnuste järgi:1) Hapniku sisalduse järgi: # hapniku mittesisaldavad happed N: # hapnikhapped N: 2) Prootonite arvu järgi: # üheprootonilised happed N: # mitmeprootonilised happed N: 3) Tugevuse järgi: #
Tõstmisel endotermilise protsessi suunas. Alandamisel eksotermilise protsessi suunas. Üheprootonilistes hapetes on üks H, mitmeprootonilistes mitu. Hapnikhapped on hapnikuga Tugevad happed: H2SO4 , HCl, HI, HBr, HNO3. Alused ained, mis annavad lahusesse hüdroksiidioone Leelised tugevad alused, vees lahustuvad hüdroksiidid(I-A rühm ja II-A rühm Ca alates.) Nõrgad alused Vees praktiliselt lahustumatud. Soolad Katioon ja anioon koos (Na2SO4) Vesiniksoolad Happeanioonis on vesinik.(NaHSO4) Kristallhüdraadid Sisaldavad tahkes olekus kristallvett(CuSO4 * 5 H20) Mittemetallisoksiidide nimetuses tähistatakse eesliitega(di-,tri-,jne) Kui metallil on muutuv o.a., siis kirjutatakse see sulgudesse CuO Vask(II)oksiid. Vesiniksoola puhul sõna vesinik (CaHPO4 kaltsiumvesinikfosfaat) Aluselised oksiidid Reageerivad hapetega ---->sool + vesi. CuO + H2SO4-----> CuSO4 + H2O Veega reageerivad ainult aktiivsete metallide(I-A rühm ja II A-rühm alates Ca) oksiidid
CaO- oksiid; SO3- vääveltrioksiid P4O10- tetrafosforheksaoksiid; Fe2O3-diraudtrioksiid H2SO3-väävlishape-hape; H3PO4-fosforhape CuSO4-vask(II)sulfaat- sool; BaCl2-baariumkloriid Ca(NO3)2-kaltsiumnitraat; Na2CO3-naatriumkarbonaat AgNO3-hõbenitraat; Al2(SO3)2-alumiiniumsulfiit Na2S-naatriumsulfiid; K2SiO3-kaaliumsilikaat Mg(OH)2- magneesiumhüdroksiid- alus KOH-kaaliumhüdroksiid ; Fe(OH)3- raud(III)hüdroksiid LiOH- liitiumhüdroksiid Baarium-baariumoksiid- baariumhüdroksiid- baariumnitraat 2Ba+O2->2BaO; BaO+H2O->Ba(OH)2 Ba(OH)2+2HNO3->Ba(NO3)2+2H2O Fosfor-fosfor(V)oksiid-fosforhape-kaltsiumfosfaat 4P+5O2->P4O10; P4O10+6H2O->4H3PO4 2H3PO4+3CaO->Ca3(PO4)2+3H2O Väävel-vääveldioksiid-väävlishape-naatriumsulfit S+O2->SO2; SO2+H2O->H2SO3 H2SO3+2Na->Na2SO3+H2 Vask(II)hüdroksiid-vask(II)oksiid- vask(II)sulfaat-vask Cu(OH)2->CuO+H2O; CuO+H2SO4->CuSO4+H2O CuSO4+Zn->Cu+ZnSO4 Raud(III)hüdroksiid-raud(III)oksiid- raud(III)kloriid- raud(III)hüdroksiid: Fe(OH)3->Fe2O3+H2O; Fe2O3+6HCl-
OKSIID koosneb kahest elemendist, millest üks on hapnik (o.-a. II) ehk siis Lihtaine + hapnik = oksiid Aluseline oksiid on aluseliste omadustega, reageerib hapetega (enamus metallioksiide on aluselised. Aktiivse metalli oksiid + vesi = hüdroksiid ehk leelis ehk tugev alus) Happeline oksiid - on happeliste omadustega, reageerib alustega (enamus mittemetallioksiide on happelised) Enamik happelisi oksiide + vesi = vastav hape HAPE aine, mis annab vesilahusesse vesinikioone (happeid liigitatakse 1. hapnikusisalduse järgi (hapnikhapped ja hapnikuta happed), 2. prootonite arvu järgi, 3. tugevuse järgi (nõrgad ja tugevad). Hapnikhape saadakse: happeline oksiid + vesi ALUS ehk hüdroksiid aine, mis annab vesilahusesse hüdroksiidioone. (aluseid liigitatakse: 1. leelised (vees hästi lahustuvad tugevad alused), 2. nõrgad alused , mis enamasti vees ei lahustu)
AINEKLASSID JA NENDE SAAMISVÕIMALUSED Klass Nimetus Saamine OKSIIDID K2O kaaliumoksiid 1.Oksüdeerumisel: CO2 süsinikdioksiid Metall + hapnik = metallioksiid (aluseline oksiid) Fe2O3 raud(III)oksiid või diraudtrioksiid 2Ca+O2=2CaO Mittemetall+hapnik=mittemetallioksiid (happeline oksiid) C+O2=CO2 2.Lagunemisreaktsioonil (kuumutamine) Sool = metallioksiid + mittemetallioksiid
Vees lahustuvad ained-leelised-tugevad alused(KOH, NaOH,LiOH) Vees mittelahustuvad-nõrgad alused(Mg(OH)2, Fe(OH)3, Cu(OH)2) Universaalindikaatoriga sinine, lakmusega sinine, fenoolftaleiiniga roosakaspunane SOOL-kristalne aine, mis koosneb aluse katioonidest ja happeanioonidest Fe+NO3-raud(III)nitraat NH4+PO4-ammooniumfosfaat Nimetused koosnevad katioonide ning anioonide nimetustest, vesiniksoolade nimetuses märgitakse eesliite abil ka vesinikioonide arv. Kui metall saab moodustada erinevas o-a katioone, märgitakse soola nimetuses ka metalli o-a Oksiid- hapniku ja mingi teise keemilise elemendi ühend Aluseline oksiid-metallioksiid Happeline oksiid-mittemetallioksiid Amfoteerne oksiid-oksiidid,mis ei reageeri veega, vaid hapete ja alustega Neutraalne oksiid-oksiidid, mis ei reageeri veega, hapetega ega alustega Hape-aine, mis annab lahusesse vesinikioone Hapnikhape-hape, mille molekuli koostisesse kuulub hapniku aatomeid
K3PO4 (kaaliumfosfaat) CO3 2- -karbonaat H2CO3 (süsihape) metall-CO3 näit. Na2CO3 (naatriumkarbonaat) SiO3 2- -silikaat H2SiO3 (ränihape) metall-SiO3 näit. Al2(SiO3)3 (alumiiniumsilikaat) NO3 - -nitraat HNO3 (lämmastikhape) metall-NO3 näit. KNO3 (kaaliumnitraat) NO2 - -nitrit HNO2 (lämmastikushape) metall-NO2 näit. NaNO2 (naatriumnitrit) REAKTSIOONIVÕRRANDITE KOOSTAMINE HAPE + ALUS → SOOL + VESI H2SO4 + 2NaOH → Na2SO4 + 2H2O + ALUSELINE OKSIID → SOOL + VESI 2HCl + MgO → MgCl2 + H2O + SOOL → UUS SOOL + UUS HAPE H2SO4 + Na2S → Na2SO4 + H2S↑ + METALL → SOOL + VESINIK 2HCl + Zn → ZnCl2 + H2↑ Cu + 4k. HNO3→ Cu(NO3)2 + 2NO2↑ + 2H2O ALUS + HAPE vaata HAPE + ALUS + HAPPELINE OKSIID → SOOL + VESI 2NaOH + CO2→ Na2CO3 + H2O + SOOL → UUS ALUS + UUS SOOL CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl lagunemine (to) → ALUSELINE OSKIID + VESI Ca(OH)2→(to) CaO + H2O HAPPELINE OSKIID (mittemetalli oksiid) + VESI → HAPE
· B-rühma elementidel on väliskihil tavaliselt 2 elektroni · Ümardatud aatommass = massiarv = prootonite ja neutronite arv kokku · Neutronite arv = ümardatud aatommass järjenumber NÄIDE: Ba aatominumber (järjenumber) = 56. Perioodi number = 6, järelikult 6 elektronkihti. Rühma number II. Ümardatud aatommass on 137. 56 Ba 137,33 Anioon Happeaniooni Vastav hape (alus) Sool nimetus OH- -hüdroksiid metall-OH (NaOH) - Cl- -kloriid HCl (vesinikkloriidhape) metall-Cl näit. KCl (kaaliumkloriid) F- -flouriid HF (vesinikflouriidhape) metall-F näit. NaF (naatriumflouriid) Br- -bromiid HBr (vesinikbromiidhape) metall-Br näit. CaBr2 (kaltsiumbromiid)
· B-rühma elementidel on väliskihil tavaliselt 2 elektroni · Ümardatud aatommass = massiarv = prootonite ja neutronite arv kokku · Neutronite arv = ümardatud aatommass järjenumber NÄIDE: Ba aatominumber (järjenumber) = 56. Perioodi number = 6, järelikult 6 elektronkihti. Rühma number II. Ümardatud aatommass on 137. 56 Ba 137,33 Anioon Happeaniooni Vastav hape (alus) Sool nimetus OH- -hüdroksiid metall-OH (NaOH) - Cl- -kloriid HCl (vesinikkloriidhape) metall-Cl näit. KCl (kaaliumkloriid) F- -flouriid HF (vesinikflouriidhape) metall-F näit. NaF (naatriumflouriid) Br- -bromiid HBr (vesinikbromiidhape) metall-Br näit. CaBr2 (kaltsiumbromiid)
Aineklassid Happed Happed koosnevad vesinikust (H) ja happejäägist. Need jagunevad kaheks: 1) Tugevad happed: 2) Nõrgad happed: HCl, HSO, HNO HSiO, HS, HSO, HCO Happed tekivad: Happeline oksiid + vesi hape (SiO ei reageeri) Reaktsioonivõrrandid: Neutraliseerimise reaktsioon 1) Hape + alus sool + vesi HCl + NaOH NaCl + HO 2) Hape + aluseline oksiid sool + vesi Vaata pingerida! HSO + NaO NaSO + HO 3) Hape + metall sool + vesinik HNO + Na NaNO + H 4) Hape + sool hape + sool CaCO + HCl CaCl + HCO Tingimused: *Tekib nõrgem või lenduvam hape *Tekib sade Oksiidid Oksiidid koosnevad mittemetallist või metallist ja hapnikust (O). Jagunevad samuti kaheks: 1) Aluselised oksiidid: metall + O
1. aluseline oksiid + hape sool + vesi 2. aluseline oksiid + vesi leelis 3. happeline oksiid + alus sool + vesi 4. happeline oksiid + vesi hape 5. aluseline oksiid + happeline oksiid sool 6. lihtaine + hapnik oksiid 7. alus(veeslahustumatu temp. aluseline oksiid + vesi 8. vesinik + element vesinikühend 9. metal + hape sool + vesinik( lahjendatud hapetega reageerivad pingereas vasakul pool olevad metallid, paremal pool olevad mitte) 10. alus + hape sool + vesi 11. sool + hape sool + hape ( reaktsioon toimub kui tugevam hape tõrjub nõrgema happe soolast välja) 12. veeslahustumatu hüdroksiid temp. aluseline oksiid + vesi 13. leelis + sool veeslahustumatu alus + sool(ainult leelised reageerivad sooladega) 14. aktiivne metall + vesi leelis + vesinik 15. metall + sool metall + sool(aktiivsem metall tõrjub vähem aktiivsema soolast välja, vastupidi ei toimu) 16. sool + hape sool + hape 17
H I Cu I ja II F -I Sn II ja IV Pb II ja IV Hapete ja happeanioonide nimetused vastav hape happeline oksiid happeanioon happeaniooni nimi (saadakse veega reageerimisel) SO2 vääveldioksiid H2SO3 väävlishape SO32- -sulfit SO3 vääveltrioksiid H2SO4 väävelhape SO42- -sulfaat
· Ümardatud aatommass = massiarv = prootonite ja neutronite arv kokku · Neutronite arv = ümardatud aatommass järjenumber NÄIDE: Ba aatominumber (järjenumber) = 56. Perioodi number = 6, järelikult 6 elektronkihti. Rühma number II. Ümardatud aatommass on » 137. 56 Ba 137,33 Anioon Happeaniooni Vastav hape (alus) Sool nimetus OH hüdroksiid metallOH (NaOH) Cl kloriid HCl (vesinikkloriidhape) metallCl näit. KCl (kaaliumkloriid) F flouriid HF (vesinikflouriidhape) metallF näit. NaF (naatriumflouriid) Br bromiid HBr (vesinikbromiidhape) metallBr näit. CaBr2 (kaltsiumbromiid)
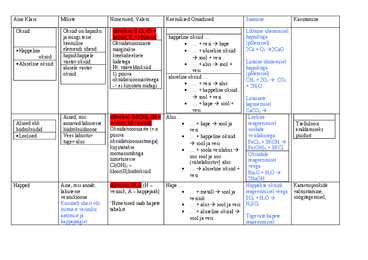
Aine Klass Mõiste Nimetused, Valem Keemilised Omadused Saamine Kasutamine Oksiid Oksiid on hapniku üldvalem: E2On (O = Lihtaine ühenemisel ja mingi teise hapnik, E = element) happeline oksiid ... hapnikuga keemilise Oksüdatsiooniaste · ... + vesi hape (põlemisel) · Happeline elemendi ühend märgitakse · ... + aluseline oksiid 2Ca + O2 2CaO oksiid hapnikhappele kreekakeelsete sool + vesi · Aluseline oksiid vastav oksiid liidetega Liitaine ühinemisel · ... + alus sool +
5. Halogeenühend- ühend, kus halogeeni (Cl, F, Br, I) aatomid on vahetult seotud süsiniku aatomiga. sinik on asendatud halogeeniga 6. Alkohol- nõrgad happed, kus süsinikuühendi molekulis on üks või mitu vesinikku asendatud hüdroksüülrühmaga OH 7. Vesinikside- side, mille moodustavad positiivse osalaenguga vesiniku aatom mittemetallide (F, O, N) vaba elektronpaariga (ja negatiivse osalaenguga) aatomiga. Mida rohkem vesinik sidemeid seda paremini lahustub ja seda kõrgem on sulamis- ja keemis temperatuur 8. Eeter- orgaaniline ühend üldvalemiga R-O-R 9. Amiin- ammoniaagi derivaat, kus vesiniku aatomi(te) asemel on orgaaniline rühm või rühmad 10.Amiini aluselisus (liidab prootoni)- N on elektronegatiivsem kui C ja H. Osalaeng negatiivne, järelikult N on nukleofiil ning N-l on nukleofiilne tsenter (aatom, millel on vaba või osaliselt vaba elektronpaar ning negatiivne laeng või osa laeng
HAPPELISED OKSIIDID HAPPED METALLID 1. Happeline oksiid + vesi = hape 1. Hape + alus = sool + vesi 1. Metall + hapnik = oksiid(v.a. väärismetallid Ag, Au, Pt) ( NB; SiO ei reageeri veega ) HCl + NaOH = NaCl + H2O (* Na, K peamiselt peroksiidid ja hüperoksiidid) 2 2. Hape + aluseline oksiid = sool + vesi 2Ca+ O2 = 2CaO SO3 + H2O = H2SO4
OKSIIDID Oksiid aine, mis koosneb kahest elemendist, millest üks on hapnik. Aluseline oksiid aluseliste omadustega, reageerib hapetega. Happeline oksiid happeliste omadustega, reageerib alustega. Oksiidide saamine: *Põlemise teel: C+O2 CO2 2Ca+O2 2CaO *Kuumutamise teel: 2Cu+O2 2CuO HAPPED Hape aine, mis annab vesilahusesse vesinikioone. Liigitamine: Hapnikusis Prootonite Tugevuse järgi alduse järgi arvu järgi Hapnikhappe Hapnikut Üheprootonilis Mitmeprootonilis Tugevad Nõrgad
Happed Muud asjad HCl vesinikkloriidhape Cl- kloriid ehk soolhape SO3-2 sulfit H2SO3 väävlishape SO4-2 sulfaat H2SO4 väävelhape S-2 sulfiid H2S divesiniksulfiidhape CO3-2 H2CO3 süsihape karbonaat H3PO4 fosforhape PO4-3 fosfaat HNO3 lämmastikhape NO3- nitraat HNO2 lämmastikushape NO2- nitrit 4-tetra; 5-penta; 6-heksa; 7-hepta; 8-okta; 9-nona; 10-deka 1. aluseline oksiid + hape sool + vesi 2. CaO + 2HCl CaCl2 + H2O 3. 4. aluseline oksiid + vesi leelis 5. LiO + H2O 2LiOH 6. 7. happeline oksiid + alus sool + vesi 8. SO2 + 2NaOH Na2SO3 + H2O 9. 10. happeline oksiid + vesi hape 11. P4O10 + 6H2O 4H3PO4 12. 13. aluseline oksiid + happeline oksiid sool 14. CaO + CO2 CaCO3 15. 16. lihtaine + hapnik oksiid 17. C + O2 CO2 18. 19
Keemia 1.*Oksiid: O , hapniku ja mingi teise keemilise elemendi ühend metall hapnik Fe2O3 raud(III)oksiid mittemetall hapnik P2O5 difosforpentaoksiid ·metallioksiid-koosneb metallist ja hapnikust. Metall asub IA,IIA,IIIA rühmas. nt. Na2O – naatriumoksiid BaO – baariumoksiid Al2O3 – alumiiniumoksiid Metall asub B-rühmas, IVA, VA rühmas nt. Fe2O3 – raud(III)oksiid SnO2 – tina(IV)oksiid ·mittemetallioksiid-koosneb mittemetallist ja hapnikust. Indeksite asemel kasutatakse eesliiteid
Anorgaaniliste ainete põhiklassid 1. Selgita mõisteid ja too näiteid: oksiid, hape, alus, sool, happeline oksiid, aluseline oksiid, neutraalne oksiid, amfoteerne oksiid, hüdroksiid, leelis, amfoteerne hüdroksiid, hapnikhape, vesiniksool, neutralisatsioonireaktsioon 2. Hapete ja happeanioonide valemid ja nimetused 3. Oksiidide, hüdroksiidide ja soolade (sh vesiniksoolade) valemite ja nimetuste koostamine 4. Anorgaaniliste ainete liigitamine põhiklassidesse 5. Oksiidide liigitamine keemiliste omaduste põhjal (happelisteks, aluselisteks, amfoteerseteks ja neutraalseteks oksiidideks) 6. Hapete liigitamine (tugevuse, prootonite arvu ja hapniku sisalduse järgi) 7
1) aluselised oks. - reageerib happelise oksiidi ja hapetega, veega tugevalt aluseline. 2) happelised oks. - reageerib alustega, aluselise oksiidiga ja veega. 3) amforteersed oks. - reageerib hapete ja alustega. saamine : *lihtainete vaheline reaktsioon * hüdroksiidide ja soolade lagundamine kuumutamisel Alus - on aine, mis annab vesilahusesse hüdroksiidioone. OM.- *sööbiv toime, *reageerimine hapetega, *reageerimine happeliste oksiididega. Hüdroksiid - on mitte- molaarne kristalne aine. Leelis - vees lahustuv tugev alus. Sool - kristalsed ained, mis koosnevad aluse katioonidest ja happe anioonidest. 1) lihtsoolad Na2CO3 2) vesiniksoolad NaHCO3 3) hüdr.soolad MgClOH OM. - * reageerib leelistega, *hapetega, *metallidega, *sooladega saamine: metall+mittemet.=sool alus+hape=sool+vesi oksiid+hape=sool+vesi aluseline oks.+happeline oks.=sool sool+leelis=alus+sool sool+metall=uus sool + vähem akt
Soola hüdrolüüs -soola reaktsioon veega, mille tulemusena võib tekkida kas happeline või aluseline keskkond Tugev elektrolüüt -elektrolüüt, mis on lahuses praktiliselt täielikult dissotsieerunud ioonideks Vesiniksool -sool, mis sisaldab vesinikku http://www.abiks.pri.ee 2. ÜLESANDED hape + metall =>> sool + H2 -metall aktiivsem vesinikust hape + alus.oks =>> sool + H2O -alati hape + alus =>> sool + H2O -alati hape + sool =>> sool + hape -peab tekkima I happest nõrgem hape või sade alus + hap.oks =>> sool + H2O -alati alus + sool =>> sool + alus -I mõlemad lahustuvad, II üks lahutumatu
Aatom keemilise elemendi väikseim osake, molekuli koostisosa, koosneb tuumast ja elektronidest Aatomi elektronkate aatomituuma umber tiirlevate elektronide kogum, mis koosneb elektronkihtidest Aatommass aatomi mass aatommassiühikutes Aatomi tuum aatomi keskosake, moodustab põhiosa aatomi massist, koosneb prootonitest ja neutronitest Ainete segu mitme aine segu, mis koosneb erinevate ainete osakestest Alus e. hüdroksiid on aine, mis annab lahusesse hüdroksiidioone (OH-), metalli katioonide+ ühend hüdroksiidiooniga - Aluseline keskkond ülekaalus on hüdrosiidioonid (OH-), pH>7 Aluseline oksiid metallioksiid, hapniku ühend metalliga Anioon negatiivse laenguga ioon Elementide rühm Mendelejevi perioodilisuse tabelis kohakuti üksteise all asuvate elementide rida, rühma elementidel väliskihis rühma numbrile vastav arv elektrone
Keemia Perioodilisustabel ja aatom Lahter- Perioodi rühmad- eemiliste elementide perioodilisussüsteem on süsteem, mis jaotab keemilised elemendid nende tuumalaengute järgi rühmadesse ja perioodidesse. Järjekorra number: Keemilise elemendi aatomnumber ehk järjenumber ehk laenguarv on prootonite arv selle elemendi aatomi tuumas. A-rühma numbrist: Kui aktiivne metall on. Perioodi Number: Mitmendas perioodis asub element, Elemendid: 1.Raud : Fe, 2,Vask: Cu, 3,Jood: I, 4,Broom: Br , 5,Tina: Sn , 6,Plii:Pb 7,hõbe: Ag 8, Broom: Br 9, kuld : Au, 10,Elavhõbe : Hg, 11, tsink: Zn, 12,mangaan : Mn, 13 Kroom Cr 14, Baarium: Ba 15,magneesium : Mg 16,naatrium : Na 17,kaalium : K 18,koobalt : Co 19,titann: Ti 20,alumiinum : Al 21,nikkel : Ni 22, Gallium : Ga 23,Iriidium: Ir 24,Plaatina: pt 25,Rubiidium: Rb 26,plii: Pb 27, Indium : In 28,frantsium : Fr 29,Raadium : Ra
püsiv, siis seda nimetuses ei märgita. -SO3 sulfit -NO3 - nitraat Keemilised 1) Aluselised Oksiidid reageerivad: 1) Hapete molekulid dissotsieeruvad 1) Reageerivad happeliste 1) Reageerivad metallidega uus sool ja uus metall. a) hapetega sool ja vesi. Toimub alati. vesilahustes vesinikioonideks ja happe- oksiididega, tekib sool ja vesi: Reageeriv metall peab olema aktiivsem, kui soola koostises omadused b) veega leelis. Ainult aktiivsete metallide anioonideks. CO2+Ca(OH)2 CaCO3+ 2H2O olev metall. oksiidid. 2) Reageerivad metallidega sool ja vesinik
AINF.KLASSIDE VAHELISF.D REAKTSIOONID Aluselise ja l. alus hape sool NaOH HCI NaCl + HIC) happelise aine vesi 2 3 H2S04 6 E-120 reaktsioon: tekib 2. aluseline oksiid + hape Mgo + 2HCl MgC12 + alati sool. sool vesi Na20 + H2SOå* Na2S04 + 1-120 3. happcline oksiid + alus —i COZ CaC03 + H20 (Happelise oksiidi sool 4 vesi reageerimisel tekib 2 NaOH + — Nazso, + HIC) oksiidile happe 4. happelinc Okiid aluseline cao + c02 — CaC03 oksiid 6 Nazo moo — 4 Nan, Oksiidi 5. aluseline oksiid + vesi Na20 + H20 2 NaOH
Põhikoolile: Happed, alused ja soolad Happed on ained, mis annavad lahusesse vesinik ioone. Happed koosnevad vesinikioonist e. prootonist ja happejääk-ioonist (Arrheniuse klassikalise definitsiooni järgi). Happejääk ioon on võrdne prootonite arvuga molekulis · HCl - vesinikkloriidhape e. soolhape, oks. aste -1 · H2S - divesiniksulfiidhape, oks. aste -2 · H2SO3 - väävlishape, oks. aste -2 · H2SO4 - väävelhape, oks. aste -2 · H2CO3 - süsihape, oks. aste -2 · H3PO4 - fosforhape (ortofosfor), oks. aste -3
( NaCl - naatriumkloriid) Hüdroksiid anorgaaniline ühend,, mille koostisse kuuluvad hüdroksiidioonid OH- . (LiOH liitiumhüdroksiid) 2. Oksiide saab liigitada: a)aluselised oksiidid(reageerivad hapetega) Li2O liitiumoksiid b)happelised oksiidid(reageerivad alustega) CO2 süsinikdioksiid c)amfoteersed oksiidid - Al2O3 alumiiniumoksiid d)neutraalsed oksiidid - CO süsinikoksiid. 3. a)K2SO3 sool b)Ni lihtaine, metall c)Na2O oksiid d)Cu(OH)2 alus e) HNO3 hape f)S8 lihtaine, mittemetall g) ZnO oksiid h)CaHPO4 sool 4. a)CuOH vask(I)hüdroksiid b)Cl2O7 dikloorheptaoksiid c)HNO2 lämmastikushape d)FeSO4 raud(II)sulfaat e)K2S dikaaliumsulfiid f)CaO kaltsiumoksiid 5. a) hape + alus sool + vesi (neutralisatsioonireaktsioon) Hcl + NaOH NaCl + H2O b)hape + aluseline oksiid sool + vesi 2Hcl + MgO MgCl2 + H2O c) hape + sool uus sool + uus hape H2SO4 + Li2S Li2SO4 + H2S (noolüles)
a. grafiit) · Ei ole head soojusjuhid (v.a. teemant) · Ei ole kõvad (v.a. teemant, räni) · Sulamis- ja keemistemperatuur on madal (v.a. süsinik ja räni) Keemilised omadused · Nii oksüdeerija kui ka redutseerija o F alati liidab elektrone o Metalliga reageerimisel mittemetall alati liidab elektrone o H mittemetalliga reageerimisel alati annab elektrone · Süsinik C vt edasi · Vesinik H o Leidumine Vesi, Maal lihtainena ei leidu o Saamine Elektrolüüs, metall + hape o Füüsikalised omadused Värvitu, lõhnatu, maitsetu, kerge o Keemilised omadused H + metall H on oksüdeerija; H + mittemetall H on redutseerija · Hapnik O o Leidumine Õhk o Saamine Fotosüntees o Füüsikalised omadused Nagu H-l (v.a. kergus)
Oksiidide keemilised omadused · Aluselised oksiidid reageerivad hapetega = sool ja vesi. · Aluselised oksiidid reageerivad veega = leelis. Veega reageerivad ainult aktiivsete metallide oksiidid (IA rühma ja IIA rühma metallid alates Ca) · Aluselised oksiidid reageerivad happeliste oksiididega = sool. · Happelised oksiidid reageerivad veega = oksiidile vastav hape. Veega ei reageeri SiO2. · Happelised oksiidid reageerivad alustega = sool ja vesi. · Happelised oksiidid reageerivad aluseliste oksiididega = sool. Hapete keemilised omadused · Reageerivad metallidega = sool ja vesinik Reag. < h2 · Reageerivad alustega = sool ja vesi · Reageerivad aluseliste oksiididega = sool ja vesi · Reageerivad sooladega = uus sool ja uus hape Reaktsioon toimub siis, kui tekib nõrgem hape või sade
mis tahkes olekus moodustavad niinimetatud metallilise võre, mis annab neile iseloomuliku metallilise läike, hea elektrijuhtivuse ning soojusjuhtivuse ja on ka enamikus hästi sepistatavad. Mittemetallid on suure elektronegatiivsusega elemendid, mis keemilistes reaktsioonides peamiselt liidavad elektrone. Perioodilisustabelis asuvad nad peaalarühmades ülal paremal, k.a. vesinik, mis asub tavaliselt kõige esimese elemendina ülal vasakul. Mittemetallide hulka kuuluvad ka väärisgaasid, kuigi need ei liida elektrone, sest nende väline elektronkiht on maksimaalselt täitunud. Keemilistes reaktsioonides moodustavad nad teiste mittemetallidega tavaliselt kovalentse sideme, metallidega tavaliselt ioonilise sideme. Oksiidid on keemilised ained, mis koosnevad kahest elemendist, millest