CaO- oksiid; SO3- vääveltrioksiid P4O10- tetrafosforheksaoksiid; Fe2O3-diraudtrioksiid H2SO3-väävlishape-hape; H3PO4-fosforhape CuSO4-vask(II)sulfaat- sool; BaCl2-baariumkloriid Ca(NO3)2-kaltsiumnitraat; Na2CO3-naatriumkarbonaat AgNO3-hõbenitraat; Al2(SO3)2-alumiiniumsulfiit Na2S-naatriumsulfiid; K2SiO3-kaaliumsilikaat Mg(OH)2- magneesiumhüdroksiid- alus KOH-kaaliumhüdroksiid ; Fe(OH)3- raud(III)hüdroksiid LiOH- liitiumhüdroksiid Baarium-baariumoksiid- baariumhüdroksiid- baariumnitraat 2Ba+O2->2BaO; BaO+H2O->Ba(OH)2 Ba(OH)2+2HNO3->Ba(NO3)2+2H2O Fosfor-fosfor(V)oksiid-fosforhape-kaltsiumfosfaat 4P+5O2->P4O10; P4O10+6H2O->4H3PO4 2H3PO4+3CaO->Ca3(PO4)2+3H2O Väävel-vääveldioksiid-väävlishape-naatriumsulfit S+O2->SO2; SO2+H2O->H2SO3 H2SO3+2Na->Na2SO3+H2 Vask(II)hüdroksiid-vask(II)oksiid- vask(II)sulfaat-vask Cu(OH)2->CuO+H2O; CuO+H2SO4->CuSO4+H2O CuSO4+Zn->Cu+ZnSO4 Raud(III)hüdroksiid-raud(III)oksiid- raud(III)kloriid- raud(III)hüdroksiid: ...
Laboratoorne töö Metallide keemilised omadused Tallinn 2011 Katse 1 Metallide reageerimine hapete lahustega Katsevahendid: Katseklaas, katseklaasihoidik, HCl, alumiinium, tsink, tina, raud, vask, tikud, piirituslamp. Katsekirjeldus: Valan katseklaasi 1-2 cm³ soolhappe lahjendatud lahust ja lisan sinna sisse erinevaid metalle. Vaatan kuidas erinevad metallid reageerivad. Vaatan, mis aktiivsusega need metallid on. 1. Soolhape + alumiinium / HCl + Al Panin katseklaasi soolhapet ja lisasime sinna alumiiniumtüki. Esialgu reaktsiooni ei toimunud. Soojendasin katseklaasi põletileegil. Reageerimisega läks veidi aega, pärast mida hakkas eralduma veidi vesinikku. Alumiiniumtükk hakkas natukene roostetama, kuid väga märgatavat muutust ei toimunud. Järeldan katsest, et Alumiinium on väheaktiivne metall. Katsetulemus ei ole kooskõlas pingerea asukohaga, kuid tean, et Alumiinium reageerib aeglaselt, sest teda katab õhuke oksii...
.........Soolhape, lämmastikhape, väävelhape....................................................... 2. Kirjuta võrrandid ja tasakaalusta need (6 p) a) Väävelhape + naatriumhüdroksiid .........H2SO4 + 2NaOH — Na2SO4 + 2H2O............................................................. b) Vask(II)oksiid + lämmastikhape .........CuO + 2HNO3 — Cu(NO3)2 + H2O.......................................................... c) Tsink + soolhape .........Zn + 2HCl — ZnCl2 + H2........................................................................... 3. Milline on lilla lakmuse värv happelises keskkonnas ? (1 p) ..........Lilla lakmuse värv happelises keskkonnas on punane............................. 4. Arvuta ränihappe molaarmass (3 p) .......M(H2SiO3) = 1 * 2 + 28 + 16 * 3 = 78 g/mol................................................... 5. Kui palju kaalub 2 mooli ränihapet ? (2 p) .........m(2H2SiO3) = 78 g/mol * 2 = 156 g
Redoksreaktsioonis toimuvad alati korraga oksüdeerumine ja redutseerumine. Oksüdeerumine on elektronide loovutamine (o-a suureneb). Redutseerumine on elektronide liitmine (o-a väheneb). Oksüdeerija on element, mis liidab elektrone (o-a väheneb). Redutseerija on element, mis loovutab elektrone (o-a suureneb). Elektronide üleminekuid näidatakse elektronvõrranditega. Näide: 0 I -I II -I 0 0 +II Zn + 2HCl = ZnCl2 + H2 Redutseerija Zn - 2e ® Zn oksüdeerub +0 Oksüdeerija H + e ® H redutseerub 4.1 Ülesandeid. Kirjuta elektronvõrrandid järgmiste muundumiste kohta: Vesinikiooni redutseerumine vesiniku aatomiks. Raua aatomi oksüdeerumine raud(II)iooniks. Raud(III)iooni redutseerumine raua aatomiks. Naatriumi aatomi oksüdeerumine naatriumiooniks. Alumiiniumi aatomi oksüdeerumine alumiiniumiooniks.
SOOLAD · Soolad koosnevad aluse katioonidest ja happe anioonidest. · Enamik soolasid lahustub vees hästi, 1A ja 2a rühma metallide ja ammooniumisoolad. · Väheaktiivsete metallide soolad lahustuvad vees halvasti. · Soolad on väga värvilised. SOOLADE NIMETAMINE · Soolade nimetamisel tuleb nimetada metalli katioon ja vastav anioon.N:Na2so4-naatriumsulfaat · B-rühma metallide korral tuleb kindlasti märkida ka oksutatsiooniaste N: Feso4 - raud(2)sulfaat SOOLADE SAAMINE · Happe+alus -)Sool + vesi N: HCL + NaOH -) NaCl +H2O · Aktiivne metall +hape -) Sool+Vesinik (1avõi2arühma Metall) N: Ca +2Hcl -) CaCl2 +H2 · Happeline oksiid + alus ja aluseline oksiid +hape -) Sool · Metall + Mittemetall -) Sool N: 2Fe + 3Cl2 -) 2FeCl3 · Aluseline oksiid + happeline oksiid -) Sool +Ves...
o LIHTAINEKS CH4 C + 2H2 o ALKÜÜN + VESINIK C4H10 C4H6 + 2H2 (butüün) CnH2n-2 KONDENSATSIOON VEEAURUGA o SÜSINIKOKSIID/VINGUGAAS CH4 + H2O CO + 3H2 o SÜSINIKDIOKSIID/SÜSIHAPPEGAAS CH4 + 2H2O CO2 + 4H2 ASENDUSREAKTSIOON HALOGEENIDEGA o NÄIDE C4H10 + 2Cl2 C4H8Cl2 + 2HCl (diklorobutaan) C arv saaduses ei muutu H indeksi saadusesse saad, kui lahutad algaine vesiniku indeksist halogeeni kordaja – (H)10- 2(Cl 2) = saaduses C4H8Cl2 Saadusesse C4H8Cl2 läheb algne halogeen koos oma indeksiga, ignoreeri antud hetkel talle antud kordajat o NÄIDE 2, 3 C5H12 + (1)F2 C5H11F + HF (flouropentaan) C9H20 + Br2 C9H19Br + HBr (bromononaan)
Molaarmass: Mr(CaO) = 40 + 16 = 56g/mol Olek: Tahke. Omadused: · Kaltsiumoksiid on sööbiv. · Valge, hallikasvalge, kahvatukollane või kahvatuhall aine. · Kristalne aine. · Lahustub hästi vees. · Ei lendu ning on lõhnatu. · Sulamistemperatuur on 2572 °C. · Keemistemperatuur on 2850 °C. · Kaltsiumoksiid reageerib eksotermiliselt veega, tekib kaltsiumhüdroksiid: CaO + H2O Ca(OH)2 · Kaltsiumoksiid on aluseline oksiid. Ta reageerib happega CaO + 2HCl CaCl2 + H2O ja happelise oksiidiga CaO + SO2 CaSO3 · Normaalsel temperatuuril ja rõhul on kaltsiumoksiid keemiliselt stabiilne. Koostas: Liis Ilves 8. klass
mõõtesilinder, termomeeter, baromeeter. Klassikaliselt saadakse mitmeid gaase laboratooriumis Kippi aparaati kasutades. Kippi aparaat koosneb kolmest klaasnõust CO2 saamiseks pannakse keskmisse nõusse (2) lubjakivitükikesi. Soolhape valatakse ülemisse nõusse, millest see voolab läbi anuma keskel oleva toru alumisse nõusse ja edasi läbi kitsenduse, mis takistab lubjakivitükkide sattumist alumisse nõusse, keskmisse nõusse. Puutudes kokku lubjakiviga, algab CO2 eraldumine CaCO3 + 2HCl → CaCl2 + CO2 + H2O Tekkiv CO2 väljub kraani kaudu. Kui kraan sulgeda, siis CO2 rõhk keskmises nõus tõuseb ja hape surutakse tagasi alumisse ning toru kaudu ka osaliselt ülemisse nõusse. Kui hape on keskmisest nõust välja tõrjutud, reaktsioon lakkab. Puhta CO2 saamiseks tuleks see juhtida veel läbi absorberi(te), mille ülesanne on siduda HCl aurud ja niiskus. Antud töös kasutatakse aja ja reaktiivide kokkuhoiu mõttes süsinikdioksiidi balloonist. Töö käik
b) aluseline oksiid + hape. c) happeline oksiid + 2) Liitainete põlemisel ühinevad tavaliselt kõik oksiidide reageerimisel veega: H2S + SO3 a) metalli reageerimisel veega: H2 + alus. d) a. oksiid + h. oksiid liitaine koostisse kuuluvad elemendid haphikuga. H2SO4. Veega ei reageeri SiO2. Cl2 2HCl 2 Teatud tingimustel toimuvad r.-d: 3) Liitainete lagunemisel: 2) H2S ja Vesinikhalogeniidhapped on b) aluselise oksiidi reageerimisel a) sool + sool mõlemad lähteained lahustuvad vees ja a)hapnikhapete lagunemine: H2SO4 H2O + SO3 vastavate gaasiliste ainete vesilahused. Neid veega: Na2O + H2O 2NaOH. vähemalt 1 saadus ei lahustu. b)aluste lagunemine: (v
Happed. HCl H+ Cl 1 Cl I H2 + Cl2 = 2HCl T kloriidid HBr H+ Br 1 Br I H2 + Br2 = 2HBr K bromiidid HI H+ I 1 I I H2 + I2 = 2Hi K jodiidid HF H+ F 1 F I H2 + F2 = 2HF K floriidid HNO3 H+ NO3 1 N +V T nitraadid HNO2 H+ NO2 1 N +III K nitriit
Hõbedane Läikiv Reageerib kergesti Põleb punase leegiga Avastamine Humphry Davy 1808. aastal. Kaltsiumamalgaani kuumutamine Robert Bunsen 1855 Isotoobid 6 stabiilset isotoopi 40 Ca, 42Ca, 43Ca, 44Ca, 46Ca ja 48Ca 18 ebastabiilset Kus leidub? Looduses ainult CaCO3 Kasutamine Redutseerijana teiste metallide väljaeraldamisel. Sulamite tootmisel Ehituses Juustu tootmisel Ühendid 2HCl + Ca → H2↑+CaCl2- jää eemaldamine, E509 Ca + O2 → CaO- värvid, putukamürk, heitvesi CaO + 3C → CO+CaC2- karbiidlamp, signaalraketid Ca(OH)2 + CO2 → H2O+CaCO3- mört, tsement, Huvitavat Inimese kehakaalust kuni 2% Kaltsium on vajalik vere hüübimiseks Päevas 600-1400 mg Puuduse korral luuhõrenemine Kaltsiumkarbiid Kasutatud kirjandus https://www.mindomo.com/mindmap/kalts
Neutraalsed oksiidid Ei reageeri hapete, vee ega alustega. Hapete keemilised omadused. Happed dissotsieeruvad vesilahustes vesinikioonideks ja happeanioonideks.. Hcl --->H+ + Cl- Mitmeprootonilised happed dissotsieeruvad astmeliselt H2SO4 --->H+ + HSO4- HSO4- <--->H+ + SO4 2- e. H2SO4---> H+ + HSO4- <->2H+ + SO4 2- Reageerivad metallidega ---> Sool ja vesinikioonideks Lahjendatud hapetega reageerivad pingereas H-st vasakul olevad metallid. Zn + 2HCl ---> ZnCl2 + H2 Konsentreeritud H2SO4 ja lahjendatud või konsentreeritud HNO3 puhul on oksüdeerijaks happeanioon, metalli asukoht pingereas pole oluline ja ei eraldu H2 Reageerivad aluseliste oksiididega ---> Sool ja vesi CuO + H2SO4 ---> CuSO4 + H2O Reageerivad alustega ----> Sool ja vesi 2NaOH + H2SO4 ---> Na2SO4 + 2H2O Reageerivad sooladega ---> uus sool ja uus hape Reaktsioon toimub siis, kui saaduseks on nõrgem või lenduvam hape või sade. 2NaCl + H2SO4 ---> Na2SO4 + 2HCl
VII A-rühma elemendid halogeenid Omadused F2 Cl2 Br2 I2 Elektrooniline F +9 2)7) +17 2)8)7) +35 2)8)18)7) +53 2)8)18)18)7) valem Oksüdatsiooniaste +7 ja -1 +7 ja -1 +7 ja -1 +7 ja -1 Füüsikalised 1.gaas 1. gaas 1.vedelik 1. tahke omadused 2.kollakas 2.kollakas 2.pruun 2.tume-mustjas 1.olek roheline gaas roheline 3. lahustub vees, 3.lahustub 2.värv ( kollakas) 3.lahustub vees saame broomivee piiritustes ( tahke 3.lahustuvus 3.lahustumisel aine ei lahustu reageerib veega. vees) 4. kuumutamis...
· 1A ja 2A rühma metall ja OH kõrvuti, on tegemist tugeva alusega N:LiOH · 3A, 4A ja kõik B rühma metall ja OH kõrvuti, on tegemist nõrga alusega N: Cr(OH)3 NEUTRALISATSIOONIREAKTSIOO N · Neutralisatsioonireaktsioon- on hapete ja aluste vaheline reaktsioon. H + O --)H2O · Sama reaktsioon toimub ka aluste ja happeliste oksiidide vahel. N: CaO + 2HCl --) CaCl + H2O PH · PH > 7 aluseline NaOH · PH < 7 happeline HCl · PH = 7 neutraalne H2O Võrrandid · (tugevalt)Aluseline oksiid + vesi --) alus Na2O +H2O --) 2NaOH · (nõrga)aluse sool + leelis --) (tugevalt)aluse sool+ nõrk alus CuSO4 +2NaOH --) NaSO4 + Cu(OH)2 · Leelismetall + vesi --) leelis + vesinik Leelismuldmetall 2Na + 2H2O --) 2NaOH + H2
hüdroksiid). Li2O, K2O, BaO, Na2O, CaO CaO + H2O → Ca(OH)2 - nõrgalt aluselised oksiidid on vähemaktiivsete metallide oksiidid. Ei reageeri veega. CrO, Fe2O3, FeO, NiO, CuO, ZnO b) REAGEERIMINE HAPETEGA - aluseline oksiid + hape= sool+vesi Tugevalt aluseliste oksiidide korral toimub reaktsioon väga energiliselt. Nõrgalt aluselise oksiidide korral vajalik kuumutamine. BaO + 2HCl →BaCl2 + H2O 2. HAPPELISED OKSIIDID a) REAGEERIMINE VEEGA - enamik reageerib veega, moodustades vastava happe. SO2, NO2, CO2, P4O10, SO3 Veega ei reageeri SiO2 (liiva põhiline koostisosa). SO2 + H2O →H2SO3 - REAGEERIMINE ALUSTEGA Happeline oksiid + alus = sool + vesi SO3 + 2 NaOH →Na2SO4 + H2O 3. ALUSELISTE JA HAPPELISTE OKSIIDIDE OMAVAHELINE REAGEERIMINE
I. Oksüdatsiooniaste: 1)lihtaine o.a. = 0 2)liitaines kõigi aatomite o.a.-te summa = 0 3)A-rühmade metallidel tavaliselt püsiv o.a., mis võrdub nende rühma numbriga 4)B-rühmade metallidel o.a. tavaliselt muutuv, sagedasti esineb o.a. II 5)Mittemetallide o.a.-d muutuvad vahemikus ,,rühma nr" (maks) kuni ,,rühma nr 8" (min) 6)Hapnikul alati II, vesinikul alati I II. Anorgaaniliste ainete põhiklassid: Anorgaanilised ained Liitained ehk keemilised ühendid Lihtained Metallid Mittemetallid Oksiidid Happed Alused Soolad 2. Oksiidid ained, mis koosnevad kahest elemendist, millest üks on hapnik V -II N2 O5 a) Saamine: 1) Lihtaine põlem...
Eraldunud vesiniku maht V = | V2 V1 | = 5,25 ml Gaasi rõhk büretis Püld = 101 250 Pa Temperatuur t° = 21° Veeauru osarõhk temperatuuril t° pH2O = 18,7mmHg= 2493,13 Pa Katseandmete töötlus ja tulemuste analüüs Katses leitakse magneesiumi mass reaktsioonis soolhappega eralduva vesiniku mahu põhjal: Mg + 2HCl MgCl2 + H2 P(H2)= 101 250 Pa- 2493,13 Pa=98756,87 Pa V0= ngaas===0,0002124 mol Mg + 2HCl MgCl2 + H2 m(Mg)= 0,0002124*24,3g/mol=5,1628g % Kokkuvõte Katse eesmärgiks oli leida magneesiumi tükikese mass katses eralduva vesiniku hulga järgi. Katse põhjal tuli magneesiumi massiks 5,1628mg. Ebatäpsused võisid tulla katse käigus büretilt ühikute valesti lugemisega või arvutuste tegemise ajal vale ümardamise tulemusena.
seal on OH+ ioonid. Katse 5 CO32 ioone sisaldavale lahusele (1...2 ml) lisada mõni tilk indikaatori fenoolftaleiini lahust. Millise reaktsiooniga (happeline, aluseline) on lahus? Miks? Lisada tilkhaaval 1 M HCl vesilahust. Miks muudab indikaator värvust? Kas soolhappe lisamisel on näha eralduva gaasi mullikesi? Lisan Na2CO3 lahusele fenoolftaleiini. Värvus muutus lillaks, seega pH 9,9 aluseline lahus, kuna seal on OH+ ioonid. Na2CO3 + 2HCl = 2NaCl + CO2 + H20 CO32- + 2H+ = CO2 + H20 Lahus muutus värvusetuks, kuna alusele lisati hapet. pH 8,3 (liikus pH=7 poole). HCl lisamisel eraldusid mulled, mis on CO2. Katse 6 Cu2+ ioone sisaldavale lahusele (1...2 ml) lisada tilkhaaval 6 M NH3 H2O, kuni esialgselt tekkiv sade (mis sade tekkis?) loksutamisel lahustub ja värvus enam ei muutu. Millise värvuse annab lahusele tekkiv kompleksioon [Cu(NH3)4]2+ ? Cu2+ + 4NH3 H2O = [Cu(NH3)4]2+ + 4H2O
( https://www.opiq.ee/kit/76/chapter/3794) ● Madal sulamis- ja keemistemperatuur . ● Hea soojusjuht. ● Ei lahustu vees. ● Läbib kergesti poorseid materjale ning õhukesi metalle. ● Saab hoida klaasnõudes. 6 / 24 Keemilised omadused ● H2 on suhteliset väheaktiivne metall. ● Kuumutamisel reageerib paljude ainetega. ● Reageerides mitemetallidega käitub H2 redutseerijana. H2 + S = H2S H2 + Cl2 = 2HCl ( https://www.opiq.ee/kit/76/chapter/3794 ) 7 / 24 Keemilised omadused ● H2 ja O2 reageerimisel tekib saadusena vesi. 2H2 + O2 = 2H2O (https://www.opiq.ee/kit/76/chapter/3794) ● H2 reageerimisel aktiivsete metaliidega tekib hüdriid* ning H2 on oksüdeerija. H2 + 2Na = 2NaH * vesiniku ja mõne muu keemilise elemendi ühend.
(omadused, leidmine ja kasutamine) (4p) 7. Mis on amfoteersus? (2p) 8. Millised on aldehüüdide ja ketoonide üldised füüsikalised omadused ja füsioloogiline toime? (3p) 9. 0,8 mooli kaltsiumoksiidi pandi reageerima 1,8 mooli soolhappega (HCl). Mitu mooli ja mitu grammi kaltsiumkloriidi tekib? Millist lähteainet ja mitu mooli jääb üle? (5p) CaO + 2HCl CaCl2 + H20 10.Kui suur oli reaktsiooni saagise %, kui 12g kaltsiumhüdroksiidi reageerimisel väävelhappega saadi 15g soola? (5p) H2SO4 + 2KOH K2SO4 + 2H2O Hinded / punktid
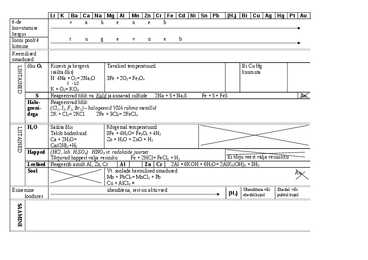
Li K Ba Ca Na Mg Al Mn Zn Cr Fe Cd Ni Sn Pb (H2) Bi Cu Ag Hg Pt Au -de v ä h e n e b loovutamise kergus Iooni poolt t u g e v n e b liitmine Keemilised omadused õhu O2 Kiiresti ja kergesti Tavalisel temperatuuril Bi Cu Hg LIHTAINED (säilta õlis) kuumuta N: 4Na + O2= 2Na2O 3Fe + 2O2= Fe3O4 I -1/2 K + O2= KO2 S Reageerivad kõik va. Kuld ja annavad sulfiide 2Na + S= Na2S Fe + S= FeS Au Halo- Reageerivad kõik geeni- (Cl2, I2, F2, Br2) halogeenid VI...
Tavaline vesinik ehk Raske vesinik ehk Üliraske vesinik ehk Prootium Deuterium Tritium H D T Hapniku kasutamine Kõrge temperatuuriga leek Raketikütuse koostisosa Keemiatööstuses oksüdeerija Meditsiin Vesiniku kasutamine Redutseerija metallide tootmisel maakidest Kütuseelement Vesiniku saamine Laboris Tsingi reageerimisel hapetega Zn + 2HCl ZnCl2 + H2 Tööstuses Vee elektrolüüsil 2H2O 2H2 + O2 Hapniku saamine Laboris Hapnikurikaste ainete lagunemisel 2KMnO4 O2 + K2MnO4+MnO2 Tööstuses Vee elektrolüüsil 2H2O 2H2 + O2 Looduses Fotosünteesil Paukgaas Vesiniku segu hapnikuga on plahvatusohtlik Paukgaas koosneb kahest ruumalaosast vesinikust ja ühes ruumalaosast hapnikust http://www.youtube.com/watch?v =wZ70gBxIrek
Tavaline vesinik ehk Raske vesinik ehk Üliraske vesinik ehk Prootium Deuterium Tritium H D T Hapniku kasutamine Kõrge temperatuuriga leek Raketikütuse koostisosa Keemiatööstuses oksüdeerija Meditsiin Vesiniku kasutamine Redutseerija metallide tootmisel maakidest Kütuseelement Vesiniku saamine Laboris Tsingi reageerimisel hapetega Zn + 2HCl ZnCl2 + H2 Tööstuses Vee elektrolüüsil 2H2O 2H2 + O2 Hapniku saamine Laboris Hapnikurikaste ainete lagunemisel 2KMnO4 O2 + K2MnO4+MnO2 Tööstuses Vee elektrolüüsil 2H2O 2H2 + O2 Looduses Fotosünteesil Paukgaas Vesiniku segu hapnikuga on plahvatusohtlik Paukgaas koosneb kahest ruumalaosast vesinikust ja ühes ruumalaosast hapnikust http://www.youtube.com/watch?v =wZ70gBxIrek
KEEMIA REAAL Happelised oksiidid : Mittemetalli oksiidid Aluselised oksiidid: Metalli oksiidid 1. alus + hape sool + vesi NaOH + HCl NaCl + H2O 2. aluseline oksiid + hape sool + vesi CaO + 2HCl CaCl2 + H2O 3. happeline oksiid + alus sool + vesi Ca(OH)2 + CO2 CaCO3 + H2O 4. happeline oksiid + aluseline oksiid sool CaO + CO2 CaCO3 5. aluseline oksiid + vesi alus Na2O + H2O 2 NaOH CaO + H2O Ca(OH)2 CuO + H2O ei toimu 6. happeline oksiid + vesi hape CO2 + H2O H2CO3
Ca + 2H20 => Ca(OH)2 +H2 Veest tõrjutakse välja vesinik ja moodustub vastav hüdroksiid. Reaktsioon kulg on vähem aktiivsem kui leelismetallidel, sest väliskihi elektronid on tugevamani tuumaga seotud. Alates Ca allapoole jäävate metallide omadused on sarnased ja neid nim. Leelismuldmetallid. Reaktsiooni käigus tekkinud leelised on vees palju vähem lahustuvad kui leelismetallide puhul. Reageerimine hapete lahustega on aktiivsem kui reageerimine veega: Mg + 2HCl => MgCl2 + H2 3. P-metallid ja siirdemetallid: Ei reageeri aktiivselt veega, osa neist (Al, Zn, Fe) võivad kõrgel temperatuuril reageerida veeauruga, tõrjudes välja vesiniku, tekib vastava metalli oksiid: 3Fe + 4H20 => Fe304 + 4H2 Väheaktiivsed metallid ei tõrju veest vesinikku välja ka kõrgel temperatuuril (nt Ni, Pb, Cu, Ag) Tekkinud hüdroksiid ja oksiidid on vees raskesti lahustuvad Paljud p-metallid ja siirdemetallid reageerivad hapete lahustega, tekib vastava metalli sool:
nende kloriidide väga vähesel lahustumisel vees. Kasutatud töövahendid ja kemikaalid Katseklaasid, pipett, keeduklaas, pliit, tsentrifuugi aparaat, Pb(NO3)2 lahus, 2M HCl lahus, konts. HCl lahus, KI lahus, K2CrO4 lahus, 2M NH3 H2O lahus, Hg2(NO3)2 lahus, Esimese rühma katioonide tõestusreaktsioonid. P1.1 Tõestusreaktsioonid Pb2+ -ioonide tõestusreaktsioonid a) Cl -ioonidega moodustub valge pliikloriidi sade: Pb2+ + 2Cl PbCl2 Pb(NO3)2 + 2HCl PbCl2 + 2HNO3 b) I -ioonidega (lisada 1 tilk) moodustub kollane pliijodiidi sade: Pb2+ + 2I PbI2 Pb(NO3)2 + 2KI PbI2 + 2KNO3 Sademe kuumutamisel etaanhappega hapestatud vees ning seejärel jahutades eraldub PbI2 kuldsete lehekestena. c) CrO42 -ioonidega moodustub kollane pliikromaadi sade: Pb2+ + CrO42 PbCrO4 Pb(NO3)2 + K2CrO4 PbCrO4 + K2NO3 Sade lahustub NaOH lahuses moodustades tetrahüdroksüplumbaatiooni, sade kaob: PbCrO4 + 4OH [Pb(OH)4]2 + CrO42
happeline st lahuses on ülekaalus H+ ioonid. Ff lisamisel Na2CO3-le muutus lahus punaseks, pH 9,9; seega on lahuses aluseline keskkond, sest ülekaalus on OH- ioonid. Gaasi teke: Katse 5. CO32 ioone sisaldavale lahusele (1...2 ml) lisada mõni tilk indikaatori fenoolftaleiini lahust. Millise reaktsiooniga (happeline, aluseline) on lahus? Miks? Lisada tilkhaaval 1 M HCl vesilahust. Miks muudab indikaator värvust? Kas soolhappe lisamisel on näha eralduva gaasi mullikesi? Na2CO3 + 2HCl = 2NaCl + CO2 + H20 CO32- + 2H+ = CO2 + H20 Na2CO3 lahus on aluselise reaktsiooniga, sest ff-i lisamisel muutub lahus punaseks. 1 M HCl lisades neutraliseeritakse lahus ja kogu lahus muutub lõpuks happeliseks, indikaatori värvus kaob. Soolhappe lisamisel nägin gaasi mullikesi. Komplekühendi teke: Katse 6. Cu2+ ioone sisaldavale lahusele (1...2 ml) lisada tilkhaaval 6 M NH3 H2O, kuni esialgselt tekkiv sade (mis sade tekkis?) loksutamisel lahustub ja värvus enam ei muutu
1. Vääveldioksiid + vesi SO2 + H2O = H2SO3 2. NAATRIUMOKSIID + VESI Na2O + H2O = 2NaOH 3. VASK(II)OKSIID + VÄÄVELHAPE CuO + H2SO4 = CuSO4 + H2O 4. SÜSINIKDIOKSIID + BAARIUMHÜDROKSIID CO2 + Ba(OH)2 = BrCO3 + H2O 5. KAALIUMOKSIID + VÄÄVELTRIOKSIID K2O + SO3 = K2SO4 6. VÄÄVELTRIOKSIID + VESI SO3 + H2O = H2SO4 7. KAALIUMOKSIID + VESI K2O + H2O = 2KOH 8. RAUD(II)OKSIID + VESINIKKLORIIDHAPE FeO+2HCl = FeCl2 + H2O 9. VÄÄVELDIOKSIID + NAATRIUMHÜDROKSIID SO2 +NaOH = Na2CO3 + H2O 10. NAATRIUMOKSIID + SÜSINIKDIOKSIID Na2O + CO2 = Na2CO3 11. VÄÄVLISHAPE + ALUMIINIUM 3H2SO3 + 2Al = Al2(SO3)3 + H6 12. NAATRIUMOKSIID + LÄMMASTIKHAPE Na2O + 2HNO3 = Na2(NO3)2 + H2O 13. RÄNIHAPE + NAATRIUMHÜDROKSIID H2SiO3 + 2NaOH = Na2SiO2 + (OH)2 + H2 14. VESINIKJODIIDHAPE + KALTSIUMKARBONAAT 2HI + CaCO3 = CaI2 + H2CO3 15. LÄMMASTI...
2Ag+ + 2Cl-→2AgCl↓ Lõpuks lisada katseklaasi veel 1 mL tioatseetamiidi lahust ning soojendada katseklaasi tõmbe all vesivannis kuni sademe värvuse muutuseni. Kuidas muutus sademe ja lahuse värvus pärast TAA lisamist? Lahus muutus mustaks. Kirjeldada reaktsioonivõrrandiga (ioon- ja molekulaarkujul) Ag2S sademe teket. Reaktsioonivõrrandites võib tioatseetamiidi asemel kasutada lihtsalt divesiniksulfiidi H2S. 2AgCl↓ + H2S →Ag2S↓ + 2HCl 2Ag+ +S2- →Ag2S↓ Lähtudes hõbekromaadi, hõbekloriidi ja hõbesulfiidi lahustuvuskorrutiste väärtustest arvutada igal eraldi juhul Ag+-ioonide kontsentratsioon vastava sademe ja selle küllastatud lahuse vahelise tasakaalu korral. Arvutustest lähtudes põhjendada katsetulemusi. Arvutustulemused esitada järgneva tabeli kujul. Sool Värvus Ks [Ag+], mol/L
+metall sool+ metall14. Kuidas saada oksiide, happeid, aluseid, soolasid? Oksiidide saamine: 1) Lihtaine +hapnik oksiid ( 2 Mg + O2 2 MgO ), 2) Liitaine+hapnikoksiid ( C8H18c12O28CO2+9H2O),3)Hüdroksiidaluseline oksiid+vesi ( 2 Fe(OH)3 Fe2O3 + 3 H2O), 4) Soolade lagunemine kuumutamisel ( CaCO3 CaO + CO2) Happete saamine : 1) hape +alus sool +vesi( H2SO4 + 2NaOH Na2SO4 + 2H2O) 2) hape+aluseline oksiidsool + vesi( 2HCl + MgO MgCl2 + H2O), 3) hape+ sooluus hape + uus sool( H2SO4 + Na2S Na2SO4 + H2S), 4) hape+metallsool+ vesinik( 2HCl + Zn ZnCl2 + H2) Aluste saamine: 1) hape +alus sool +vesi( H2SO4 + 2NaOH Na2SO4 + 2H2O),2) alus + happeline oksiid sool+vesi( 2NaOH + CO2 Na2CO3 + H2O) 3) alus + sool uus alus + uus sool (CuCl2 + 2NaOH Cu(OH)2 + 2NaCl), 3) laguneminealuseline oksiid+vesi ( Ca(OH)2 (to) CaO + H2O) Soolade saamine: 1)sool + hape uus hape + uus sool( H2SO4 + Na2S Na2SO4 + H2S),
..2 ml) lisada mõni tilk indikaatori fenoolftaleiini lahust. Millise reaktsiooniga (happeline, aluseline) on lahus? Miks? Lisada tilkhaaval 1 M HCl vesilahust. Miks muudab indikaator värvust? Kas soolhappe lisamisel on näha eralduva gaasi mullikesi? Na2CO3 + fenoolftaleiin roosakas-punane värvus, järelikult pH suurem kui 8,3...9,9. Lahus on aluseline. Lisades HCl lahus muutub värvusetuks, sest lahus muutub neutraalseks. Näha on eralduva gaasi mullikesi(CO2). Na2CO3 + 2HCl CO2 + H2O + 2NaCl CO32+ + 2H+ CO2 + H2O 4. Kompleksühendi teke Katse 6. Cu2+ ioone sisaldavale lahusele (1...2 ml) lisada tilkhaaval 6 M NH3 H2O, kuni esialgselt tekkiv sade (mis sade tekkis?) loksutamisel lahustub ja värvus enam ei muutu. Millise värvuse annab lahusele tekkiv kompleksioon [Cu(NH3)4]2+ ? CuSO4 + 4NH3*H2O [Cu(NH3)4]SO4+ 4H2O annab lahusele tumesinise värvuse, tekib sade. Cu2+ + 4NH3*H2O [Cu(NH3)4]2+ + 4H2O Redoksreaktsioonid 5. Metallid, metallide pingerida
Gaasi teke Katse 5. CO32 ioone sisaldavale lahusele lisada mõni tilk indikaatori fenoolftaleiini lahust. Alguses on Na2CO3 aluseline(indikaator punane), sest CO32- on nõrk happe ioon, aga Na+ on tugev aluseline ioon, aga kui lisada lahusesse HCl, siis muutub lahus neutraalseks(indikaator värvitu), sest Na+ ja Cl- on mõlemad tugevad, kuid eri laenguga ioonid, mis tasakaalustavad teineteist. Lisaks tekivad ka H2O ja CO2, mis on ka mõlemad neutraalsed. Na2CO3 + 2HCl 2NaCl + H2O + CO2 CO32 + 2H+ H2O + CO2 Kommentaar: On näha eralduva CO2 mullikesi. Kompleksühendi teke Katse 6. Cu2+ ioone sisaldavale lahusele lisada tilkhaaval 6 M NH3 H2O, kuni esialgselt tekkiv sade (mis sade tekkis?) loksutamisel lahustub ja värvus enam ei muutu. Millise värvuse annab lahusele tekkiv kompleksioon [Cu(NH3)4]2+? CuSO4 + 4NH4·H2O Cu(NH3)4SO4 + 4H2O Cu2+ + 4NH4·H2O [Cu(NH3)4]2+ + 4 H2O Kommentaar: algselt tekkiv sade oli Cu(OH) 2
Eksperimentaalne töö 2 Metalli massi määramine reaktsioonis eralduva gaasi mahu järgi 1.Töö ülesanne ja eesmärk Gaasiliste ainete mahu mõõtmine, gaaside segud ja gaasi osarõhk, arvutused gaasidega reaktsioonivõrrandi põhjal. 2.Sissejuhatus Teoreetiline osa (definitsioonid, arvutusvalemid) on suuremas jaos toodud 1. eksperimentaalse töö sissejuhatuses. Katses leian magneesiumi massi reaktsioonis soolhappega eralduva vesiniku mahu põhjal Mg + 2HCl MgCl2 + H2 Püld = pH2 + pH2O, millest pH2 = Püld pH2O Püld gaasisegu rõhk süsteemis (büretis), mis võrdub õhurõhuga mõõtmishetkel Selles katses kogutakse eralduv vesinik vee kohale, mistõttu vesinik sisaldab ka veeauru ja vastavalt Daltoni seadusele tuleb vesiniku mahu viimiseks normaaltingimustele kasutada järgmist seost: Veeauru osarõhk sõltuvalt temperatuurist on toodud tööjuhendis olevas tabelis 1.1 t0 = 18,7 mmHg 3
1)Oksüdeerija aine mille osakesed liidavad elektrone ise redutseerides Oksüdeerumine el.loovutamine redoksreakts. sellele vastab o.a suurenemine Elektrolüüs elektroodidel kulgev redoksreakts. mis toimub elektrivoolu läbijuhtimisel lahusest või sulatatud elektrolüüdist Aluminotermia lihtainete enamasti met. Saamine ühenditest alumiiniumiga reutseerimise teel Akumulaator korduvalt kasutatav keemiline vooluallikas, mis on laetav Särdamine metalliühendi üleviimine oksiidiks kuumutamisel õhuhapniku juuresolekul 2)keemiline metalli vahetu keemiline reakts. keskkonnas leiduva oksüdeer. kuivade gaasidega kk. Elektrok metalli kokkupuude elektrolüüdilahusega. Rohkem levinud. 3)muudetakse keemilisel reakts vabanev energia elektrienergiaks. Et elekktri saada tuleb oksüdeerumine ja reduts läbi viia eraldi elektroodidel. Ioonide liikumiseks ühendatakse lahused u-kujulise klaastoru abil, milles on elektrolüüdilahus. Mõlemas lahuses on ...
Mn7++5e Mn2+ 2 N3+-2e N5+ 5 10 II+ V+ II- IV+ II- I+ V+II- I+ VII+ II- II+ V+ II- I+ II- 6. 2Mn(NO3)2 + 5PbO2 + 6HNO3 2HMnO4 + 5Pb(NO3)2 + 2H2O Mn2+-5e Mn7+ 2 Pb4++2e Pb2+ 5 10 III+ I- I+ II- II+ I- 0 I+ I- 7. 2FeCl3 + H2S FeCl2 + S + 2HCl Fe3++e Fe2+ 2 S2-+2e S0 1 2 II+ II- I+ V+ II- I+ I- II+ I- II+ II- 0 I+ II- 8. 3CoS + 2HNO3 + 6HCl 3CoCl2 + 2NO + 3S + 4H2O S2--2e S0 3 N5++3e N2+ 2 6 II+ II- I+ V+ II- I+ I- II+ I- I+ I- 0 I+ II- 9. 3NiS + KClO3 + 6HCl 3NiCl2 + KCl + 3S + 3H2O
6Li + N2 = 2Li3N liitiumnitriid · Kõik reageerivad fosforiga 3Li + P = Li3P liitiumfosfiid · Reageerivad väävliga 2Li + S = Li2S liitiumsulfiid · Reageerivad halogeenidega (7. Rühma elemendid) 2Li + Cl2 = 2LiCl liitiumkloriid · Reageerimine süsinikuga Li + C = Li2C2 liitiumkarbiid Reageerimine liitainetega · Reageerimine veega 2Li + 2H2O = 2LiOH + H2 liitiumhüdroksiid · Reageerimine hapetega 2Li + 2HCl = 2LiCl + H liitiumkloriid · Reageerimine soolavesilahustega Li + CuSO4 = 2Li +2H2O = 2LiOH + H2 2LiOH + CuSO4 = LiSO4 + Cu(OH)2 liitiumsulfaat ja vaskhüdroksiid (mittelahustuv) Leelismetallide kui lihtainete kasutamine Liitium · Vooluallikates (liitiumakud) · Raketikütuste koostises · Sulamitest gaaside sidumiseks Naatrium · Tänavavalgustuslampides · Soojuskandja tuumaenergeetikas
1. Kuidas te määrasite katseliselt NaCl-i sisaldust liiva-soola segus? Keedusoola protsendilise sisalduse leidmiseks lahustatakse kaalutud segu vees ja filtreeritakse. Filtraadi tiheduse kaudu leitakse tabelist NaCl protsendiline sisaldus. 2. Mida väljendab lahuse molaarne kontsentratsioon? Molaarne konsentratsioon väljendab lahustunud aine moolide hulka 1l lahuses. 3. Arvutada KOH lahuse molaarne kontsentratsioon, kui 8 ml selle lahuse neutraliseerimiseks kulus 13 ml 0,1245 M HCl lahust. VHCl C M , HCl C M , KOH VKOH = (13/100 * 0,1245) / (8/100) = 2,02 mol/dm³ 5. Milline töövahend on bürett? Kuidas ja milleks te seda kasutasite? Millise täpsusega tuleb võtta lugem büretilt? Bürett on peenike mõõteskaalaga klaastoru, mille ühes otsas on klaaspalliga kummitoru, mis võimaldab büretist vedelikku tilkhaaval välja lasta. Katsetes kasutakse büretti, et määrata või...
Vesinik Aule Mäemets PA14 Tartu Kutsehariduskeskus Koht perioodilisussüsteemis Vesinik ausb tabelis esimesel kohal Tähis on H Tuumalaeng on 1 Massiarv on 1 Vesinikul on 1 prooton, 1 neutron ja 1elektron Esineb 3 isotoobina: tavaline vesinik, raske vesinik ja üliraske vesinik Omadused (lihtaine) Vesinik koosneb kaheaatomilistest molekulidest Sulamis ja keemis temperatuurid on väga madalad Vesinik on lõhnata, maitseta ja värvusetta Vesinik on kõige kergem gaas Vees väga vähe lahustuv Kergsüttiv Keemilised omadused Suhteliseltväheaktiivne mittemetall Enamikes keemilistes reaktsioonides käitub vesinik redutseerijana, reageerimisel aktiivsete metallidega käitub vesinik oksüdeerujana Molekulaarne vesinik on üsna väheaktiivne Atomaarne vesinik on üsna aktiivne Kus leidub looduses Maal vesiniku eriti ei leidu Vesiniku leidub enamuselt vee koostises, mõnedes mineraalides ja enamustes orgaanilistes ainetes Vesini...
Keemilised omadused Vees lahustuvad soolad esinevad lahustes ioonidena: Na2SO4 2Na+ + SO42- 1. Reageerimine metalliga uus sool + uus metall (metall reageerib ves lahustuva soolaga, kui ta on aktiivsem kui soola koostises olev metall) Fe + CuSO4 FeSO4 + Cu 2. Reageerimine hapetega uus sool + uus hape (toimub vaid siis, kui tekib nõrgem hape) Na2S + H2SO4 Na2SO4 + H2S (kui tekib H2CO3, siis ta laguneb tekkemomendil veeks ja süsinikdioksiidik CaCO3 + 2HCl CaCl2 + H2O + CO2) 3. Reageerimine alustega uus alus + uus sool (lähteained peavad olema vees lahustuvad ja saadustest üks lahustumatu) CuCl2 +2NaOH Cu(OH)2 + 2NaCl 4. Reageerimine sooladega uus sool + uus sool (lähteained peavad olema vees lahustuvad ja saadustest üks lahustumatu) NaCl + AgNO3 AgCl + NaNO3 Soolade saamine 1. hape + metall sool + H2 2. hape + aluseline oksiid sool + H2O 3. hape + alus sool + H2O 4
Kaadmium Füüsikalised omadused Kaadmium (sümbol Cd) on hõbevalge, pehme metall, mis on plastiline ja hea kattevõimega. Kaamdium sulab temperatuuril 321 °C ja keeb temperatuuril 767 °C. Tema tihedus normaaltingimustel on 8,65 g/cm³. Normaaltingimustes on kaadmium tahkes olekus. Paiknemine tabelis Kaadmium (sümbol Cd) on keemiline element järjenumbriga 48. Tema aatommass on 112,41, asub 5.perioodis IIB-rühmas. Kaadmiumil on 5 elektronkihti ja viimasel kihil on 2 elektroni. Avastamine Friedrich Stromeyer avastas kaadmiumi 1817 aastal Saksamaal. Kaadmium on nime saanud vanakreeka mütoloogia tegelase Kadmose järgi, kes oli Liibanoni prints. Samuti öeldakse, et nimetus tuleb kreekakeelsest sõnast kadmeia- tsingimaak (koostiselt ZnO, milles esineb Cd-d) Leidumine Kaadmiumi leidub looduses üldiselt koos tsingiga, kuid on tsingist üle 50% haruldasem. Kaadmium võib leida maagis koos tsingi, plii ja vasega, s...
Metallid Metallide üldised keemilised omadused · reageeri mittemetalliga 1) metall+hapnik->oksiid 2Mg+O2 -> 2MgO 2)halogeen +metall->jodiid,kloriid,floriid 2Al+3J2 ->2AlI3 3)metall+väävel->sulfiid Zn+S->ZnS Fe+S-> FeS · reageerib liirainega 1)veega * IA ja II A Ca-Ba +H2 O->leelis+H2 2K+2H2O->2KOH+H2 *Mg-Fe+H2O->oksiid+H2 *Ni.....+H2O->ei reageeri · metall+lahjendatud hape->sool+H2 reageerivad -H2-ei reageeri Zn+2HCl->ZnCl2+H2 · metall+soolalahus(L)->uus sool +nõrgem metall v.a KnaCaBa Mg+CuSO4->MgSO4+Cu · reageerimine leeliste lahustega amfoteersete metallid Al ja Zn 2Al+2NaOH+6H2O · tugevad oksüdeeruvad happed 1)konts H2SO4 *pingerea algus kuni Mg-ni+k. H2SO4-> sulfaad+H2S+H20 Al ja Fe passive...
HCl vesinikkloriidhape Cl- kloriid ehk soolhape SO3-2 sulfit H2SO3 väävlishape SO4-2 sulfaat H2SO4 väävelhape S-2 sulfiid H2S divesiniksulfiidhape CO3-2 H2CO3 süsihape karbonaat H3PO4 fosforhape PO4-3 fosfaat HNO3 lämmastikhape NO3- nitraat HNO2 lämmastikushape NO2- nitrit 4-tetra; 5-penta; 6-heksa; 7-hepta; 8-okta; 9-nona; 10-deka 1. aluseline oksiid + hape sool + vesi 2. CaO + 2HCl CaCl2 + H2O 3. 4. aluseline oksiid + vesi leelis 5. LiO + H2O 2LiOH 6. 7. happeline oksiid + alus sool + vesi 8. SO2 + 2NaOH Na2SO3 + H2O 9. 10. happeline oksiid + vesi hape 11. P4O10 + 6H2O 4H3PO4 12. 13. aluseline oksiid + happeline oksiid sool 14. CaO + CO2 CaCO3 15. 16. lihtaine + hapnik oksiid 17. C + O2 CO2 18. 19
Zn + CuSO4 ZnSO4 + Cu REAKTSIOONIVÕRRANDITE KOOSTAMINE HAPE + ALUS SOOL + VESI H2SO4 + 2NaOH Na2SO4 + 2H2O + ALUSELINE OKSIID SOOL + VESI 2HCl + MgO MgCl2 + H2O + SOOL UUS SOOL + UUS HAPE H2SO4 + Na2S Na2SO4 + H2S NB! Reaktsioon toimub siis, kui uus tekkiv happe on reageerivast happest nõrgem või lenduvam või kui uus tekkiv sool ei lahustu vees (sade).
Zn + CuSO4 ZnSO4 + Cu REAKTSIOONIVÕRRANDITE KOOSTAMINE HAPE + ALUS SOOL + VESI H2SO4 + 2NaOH Na2SO4 + 2H2O + ALUSELINE OKSIID SOOL + VESI 2HCl + MgO MgCl2 + H2O + SOOL UUS SOOL + UUS HAPE H2SO4 + Na2S Na2SO4 + H2S NB! Reaktsioon toimub siis, kui uus tekkiv happe on reageerivast happest nõrgem või lenduvam või kui uus tekkiv sool ei lahustu vees (sade).
Laboratoorne töö 4 Reaktsioonid elektrolüütide lahustes. Heterogeenne tasakaal 1. Raskelahustuva ühendi sadenemine ja lahustumine Katse 1.1 Valasin katseklaasidesse 1 ml HC ,l NaCl ja CaCl2 lahust ning lisasin igasse katseklaasi 0,1 ml (2 tilka) AgNO3 lahust. Igas katseklaasis tekkis valge sade. Cl- ioonide määramise reaktiiv peab sisaldama Ag + iooni. HCl+ AgNO3=AgCl+ HNO3 NaCl+AgNO3=AgCl+ NaNO3 CaCl2+ 2AgNO3=2AgCl+ Ca(NO3)2 Ks=1,8*10-10 [Ag+]=1,82*10-3 [Cl-]=1,82*10-3 Ks1=[Ag+][Cl-]=3,31*10-5 [Ag+]=2*1,82*10-3 [Cl-]=2*1,82*10-2 Ks2=[Ag+][Cl-]=3,31*10-5 Ks2>Ks Ks1>Ks Järelikult peabki sade tekkima Ks=aAg+ + aCl- a=[A]* aAg+=0,95*0,02=0,019 aCl-=0,95*0,02=0,019 Ks=3,8*10-2 mol/l Katse 1.2 Valasin katseklaasidesse 1 ml H2SO4, Na2SO4, MgSO4, CuSO4 ja Na2S2O3 lahust ning lisasin igasse katseklaasi 0,1 ml (2 tilka) BaCl 2 lahust. Kõigis lahustes peale Na2S2O3 lahuse tekib valge sade. ...
2 Metalli massi määramine reaktsioonis eralduva gaasi mahu järgi Töö eesmärk: Gaasiliste ainete mahu mõõtmine, gaaside segud ja gaasi osarõhk, arvutused gaasidega reaktsioonivõrrandi põhjal. Töövahendid: Seade gaasi mahu mõõtmiseks, väike mõõtesilinder, filterpaber, termomeeter, baromeeter. Kasutatud ained: 10%-ne soolhappelahus, 6,0 mg metallitükk (Mg) Töö käik: Katses leitakse magneesiumi mass reaktsioonis soolhappega eralduva vesiniku mahu põhjal: Mg + 2HCl = MgCl2 + H2 Ettevalmistus: Eemaldada katseklaas ja pesta ning loptutada see hoolikalt destilleeritud veega. Büretid sättida ühele kõrgusele ning kontrollida, et vee nivoo oleks mõlemas büretis silma järgi ühel kõrgusel ja büreti keskel. Vajadusel tuleb lisada või eemaldada büretist vett. Katseklaas ühendda tihedalt korgiga. Seejärel tõsta üks büretiharu teisest 15 cm kõrgemale ning jälgida paar minutit, kas vee nivoo püsib paigal. Kui vee nivoo ei muutunu,
Laboratoorne töö 1 Töö ülesanne ja eesmärk: tõestada katioonide esimese rühma reaktsioone Kasutatud töövahendid: pipett, puhtad katseklaasid Kasutatud ained: 2M HCl, 0,25M KI, 0,2M K2CrO4 Tõestusreaktsioonid Pb2+ -ioonide tõestusreaktsioonid 1) Cl-ioonidega moodustub valge tihe pliikloriidi sade: Pb2+ + 2Cl PbCl2 Pb(NO3)2 + 2HCl PbCl2 + 2HNO3 2) I-ioonidega (lisada 1 tilk) moodustub intensiivne kollane pliijodiidi sade: Pb2+ + 2I PbI2 Pb(NO3)2 + 2KI PbI2 + 2KNO3 Kuumutasin sademe 2M etaanhappega hapestatud vees, seejärel kiiresti jahutasin ning eraldus kuldselt helkiva peenekristalliline PbI2 sade. 3) CrO42-ioonidega moodustub kollane pliikromaadi sade: Pb2+ + CrO42 PbCrO4 Pb(NO3)2 + K2CrO4 PbCrO4 + 2K2NO3 Sade lahustub NaOH lahuses moodustades tetrahüdroksoplumbaatiooni, sade kaob, lahus
keskkond, kuna OH- ioonid on ülekaalus. Al2(SO4)3 metüülpunast lisades muutus lahus punaseks. pH ˂ 4,2 ehk happeline keskkond, kuna H+ ioonid on ülekaalus. Gaasi teke Katse 5. CO32– ioone sisaldavale lahusele (1...2 ml) lisada mõni tilk indikaatori fenoolftaleiini lahust. Millise reaktsiooniga (happeline, aluseline) on lahus? Miks? Lisada tilkhaaval 1 M HCl vesilahust. Miks muudab indikaator värvust? Kas soolhappe lisamisel on näha eralduva gaasi mullikesi? Na2CO3 + 2HCl → 2NaCl + CO2 ↑ + H2O CO32- + 2H+ → CO2 ↑ + H2O Na2CO3 on aluselise reaktsiooniga. Fenoolftaleiini lisamisel muutus laus lillaks. 1M HCl lisades neutraliseeritakse lahus ja happe lisades muutub lahus lõpuks happeliseks, indikaatori värvus kaob. Vähe eraldus gaasi. Kompleksühendi teke Katse 6. Cu2+ ioone sisaldavale lahusele (1...2 ml) lisada tilkhaaval 6 M NH3 ⋅ H2O, kuni esialgselt tekkiv sade (mis sade tekkis?) loksutamisel lahustub ja värvus enam ei muutu
CrO kroom(II)oksiid Struktuurvalemid K2O CaO Fe2O3 PbO2 2 Keemilised omadused a) aluseline oksiid + vesi = ALUS (B rühma metalli oksiidid üldiselt ei reageeri veega) CaO + H2O = Ca(OH)2 [kustutamata lubja ,,kustutamine"] b) aluseline oksiid + hape = SOOL + VESI CaO + 2HCl = CaCl2 + H2O Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O c) aluseline oksiid + happeline oksiid = SOOL K2O + CO2 = K2CO3 d) aluseline oksiid + aluseline oksiid MgO + K2O alus K2O + Fe(OH)3 sool CaO + Na2SO4 metall Saamine: a) otseselt: 2Ca + O2 = 2CaO b) kaudselt: CaCO3 = CaO + CO2 2Fe(OH)3 = Fe2O3 + 3H2O
· Keemilise aktiivsuse tõttu ei leidu neid looduses lihtainena (ehedana), vaid ainult ühendite koostises. Näiteks NaCl kivisool. · Õhus oksüdeeruvad kiiresti, metalli hõbedane pind tuhmub ja seepärast hoitakse neid õli- või petrooleumikihi all. · Reageerivad veega nt. 2Na + 2H2O =2NaOH +H2 Li reageerib veega rahulikult, Na aktiivsemalt, K nii aktiivselt, et süttib vees põlema, Cs plahvatab vees. · Reageerivad happega nt. 2Na + 2HCl =2NaCl+H2 Reageerivad teiste mittemetallidega 2Na + Cl2 =2NaCl Leelismuldmetallid Leelismuldmetallideks nimetatakse aktiivsemaid IIA rühma metalle (alates Ca-st). Ca, Sr, Ba, Ra: nende metallide hüdroksiidid on leelised (st vees lahustuvad hüdroksiidid). I Leelismuldmetallide omadused Nii füüsikaliste kui ka keemiliste omaduste poolest sarnanevad leelismetallidega. Leelismuldmetallid on väga aktiivsed, reageerivad: · veega · hapetega · mittemetallidega