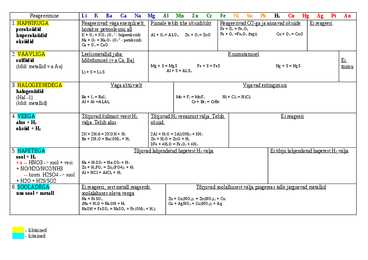
1. Hapete definitsioon happed on ained, mis annavad lahusesse vesinikioone(H+). Happed koosnevad vesinikioonidest ja happeanioonidest. Happeaniooni laeng võrdub vesiniku aatomite arvuga happemolekulis. 2. Hapete valemid ja nimetused, happeanioonide valemid ja nimetused HF vesinikfluoriidhape, F - HCL vesinikkloriidhape(soolhape), Cl - kloriidioon HBr vesinikbromiidhape, Br - bromiidioon HI jodiidhape,I - jodiidioon HNO2 lämmastikkushape,NO2 - nime ei tea HNO3 lämmastikhape,NO3 - nitraatioon H2S divesiniksulfiidhape,S2 - sulfiidioon H2SO3 väävlishpe,SO32 - sulfitioon H2SO4 väävelhape,SO42 - sulfaatioon H2CO3 süsihape,CO32 - karbonaatioon H4SiO4 ortoränihape, SiO44 - silikaatioon H3PO4 fosforhape,PO43 - fosfaatioon HMnO4 permangaanhape,MnO4 Veel anioone - OH - hüdrooksiidioon , HCO3 - vesinikkarbonaatioon 3. Hapete liigitus Tugevad, keskmise tugevusega, nõrgad. 4. Happelised oksiidid ja neile vastavad happed Happ...
docstxt/135879068299.txt
· mitmeprootonilised happed: H2S, H2SO4 , H2SO3, H3PO4, H3PO3, H2CO3, H4SiO4 3. happe tugevuse alusel jagunevad happed koolikeemias kaheks: · tugevad happed (5 tk) alates kõige tugevamast on: H2SO4, HNO3, HI, HBr, HCl · nõrgad happed suvalises järjekorras on: H3PO4, H3PO3, H2SO3, HNO2, H4SiO4, CH3COOH, H2CO3; kõige nõrgem anorgaaniline hape on H2CO3 Nimetatud hapetest on lenduvad happed: HF, HCl, HBr, HI, H2S, CH3COOH Nimetatud hapetest on kergesti lagunevad happed: H2SO3, H2CO3 Nimetatud hapetest on kõik vedelikud, välja arvatud tahke H3PO4 Nimetatud hapetest ei esine puhtal kujul iseseisva ainena, vaid ainult vesilahusena süsihape H2CO3 Nimetatud ainetest on HF, HCl, HBr, HI, H2S gaasid, mis lahustuvad hästi vees, moodustades happe. Nimetatud hapetest puutub inimene tavaelus kokku järgmiselt: · vesinikkloriidhape ehk soolhape on maohape HCl
alus + H2 välja. Tekib alus. oksiid. oksiid + H2 2K + 2H20 = 2KOH + H2 2Al + H2O = 2Al(OH)3 + 3H2 Ba + 2H2O = Ba(OH)2 + H2 Zn + H2O = ZnO + H2 3Fe + 4H2O = Fe3O4 + 4H2 5. HAPETEGA Tõjuvad lahjendatud hapetest H2 välja Ei tõrju lahjendatud hapetest H2 välja sool + H2 v.a -- HNO3 -> sool + vesi Na + H2SO4 = Na2SO4 + H2 + NO/N2O/NO2/NH3 Zn + H3PO4 = Zn3(PO4)2 + H2 Al + HCl = AlCl3 + H2 -- konts. H2SO4 -> sool + H2O + H2S/SO2 6. SOOLADEGA Ei reageeri, sest metall reageerib Tõrjuvad soolalhusest välja pingereas talle järgnevad metallid
lähteainet nimetati tol ajal kaustiliseks soodaks, siis nimetas ta soodast eraldatud metalli sodium'iks. Naatriumi omadused Välimuselt on naatrium hõbevalge metall. Naatrium on pehme, teda saab noaga lõigata. Naatriumi tihedus on 0,97 g/cm3 ja sulamistemperatuur on 98 Celsiust. Ta on keemiliselt väga aktiivne, mistõttu hoitakse teda hapnikukindla kihi all, eemal veest. Naatrium reageerib paljude lihtainete, vee ja hapetega. Hapetest ja veest tõrjub ta välja vesinikku ning tekib vastavalt sool ja hüdroksiid. Suurem osa naatriumi sooli lahustub vees hästi. Omadustelt on naatrium leelismetall. Sellisena on ta oksüdatsiooniaste ühendites 1. Naatriumi reageerimisel hapnikuga tekib kergesti naatriumperoksiid, mitte naatriumoksiid. Naatriumi isotoobid Naatriumil on üks stabiilne isotoop massiarvuga 23. Omadustelt on naatrium leelismetall. Sellisena on ta
– Chuquicamata karjäär. Vask ja tema ühendid on mürgised ! Vaske saadakse ja puhastatakse elektrolüütiliste meetoditega Kasutamine: energeetikaseadmed, elektrijuhtmed, soojusvahetid, müntide metall, Sulamid (pronksid): Cu – Sn tinapronks Cu – Si ränipronks Cu – Zn valgevask Lihtainete omadused Vask reageerib õhuga kõrgemal t°-l (~800°C) Vase alarühma metallid pingereas vesinikust paremal – ei tõrju hapetest välja vesinikku. Oksüdeerivate hapetega reageerivad Cu ja Ag, kuld lahustub vaid kuningvees. Vase reageerimisel lahjendatud lämmastikhape-ga eraldub NO, kontsentreeritud happega NO2. Kontsentreeritud väävelhappega tekib SO2. Leelistega ei reageeri. Vasesoolade lahustel on sinine värvus. Hõbe on keemiline element järjenumbriga 47, metall. Stabiilseid isotoope kaks, nende massiarvud on 107 ja 109. Hõbe on väärismetall. Tihedus on 10,5 g/cm³. Hõbe sulab temperatuuril 960°C
Chuquicamata karjäär. Vask ja tema ühendid on mürgised ! Vaske saadakse ja puhastatakse elektrolüütiliste meetoditega Kasutamine: energeetikaseadmed, elektrijuhtmed, soojusvahetid, müntide metall, Sulamid (pronksid): Cu Sn tinapronks Cu Si ränipronks Cu Zn valgevask Lihtainete omadused Vask reageerib õhuga kõrgemal t°-l (~800°C) Vase alarühma metallid pingereas vesinikust paremal ei tõrju hapetest välja vesinikku. Oksüdeerivate hapetega reageerivad Cu ja Ag, kuld lahustub vaid kuningvees. Vase reageerimisel lahjendatud lämmastikhape-ga eraldub NO, kontsentreeritud happega NO2. Kontsentreeritud väävelhappega tekib SO2. Leelistega ei reageeri. Vasesoolade lahustel on sinine värvus. Hõbe on keemiline element järjenumbriga 47, metall. Stabiilseid isotoope kaks, nende massiarvud on 107 ja 109. Hõbe on väärismetall. Tihedus on 10,5 g/cm³. Hõbe sulab temperatuuril 960°C
korduvatest struktuuriühikutest. Elementaarlüli – polümeeri molekulis korduv struktuuriühik Polümerisatsiooniaste - elementaarlülide arv polümeeri ahelas Liitumispolümerisatsioon – toimub kordsete sidemete arvel (mol liituvad) Polükondensatsioon – selle käigus eraldub mingi madalmolekulaarne aine (tav H20 ) Plastmass – polümeeri ja vajalike lisandite segu Kopolümeer – erinevte lülide kordumine Homopolümeer – samade lülide kordumine Polüester – hüdroksühapetest või dihappest ja dioolist kondensastiooni teel moodustunud polümeer Polüamiid – aminohapetest või dihapetest ja diamiinist kondesatsiooni teel moodustunud polümeer Monosahhariid – polühüdroksükarbonüülühend Disahhariid – sahhariid, mille molekulis on glükosiidsidemega seotud kaks monosahhariidi jääki Polüsahhariid – monosahhariidi(de) jääkidest koosnev polümeer Glükosiidside – nimetus, millega tähistatakse eetrifuntksiooni (hapniksilda) glükosiidi molekulis
MUSTAD SÕSTRAD : Cvitamiini sisaldab must sõstar meie aiamarjade seas kõige rohkem 66 kuni 258 mg 100 grammi marjade kohta Väga palju on Pvitamiini, umbes 1,1 1,2 % Musta sõstra marjad sisaldavad rohkesti kaaliumi, fosfori, magneesiumi, seleeni ning teisi mineraalaineid Veel sisaldavad musta sõstra marjad 7,5 9,1 % suhkruid, 2,5 % orgaanilisi happeid ja 1,5 % pektiini Mustas sõstras on palju suhkruid, kõige rohkem fruktoosi ja glükoosi Orgaanilistest hapetest domineerib sidrunhape MUSTA SÕSTART ON HEA TARVITADA : organismi vastupanuvõime tõstmiseks külmetus ja nakkushaiguste ennetamisel palaviku korral, nahahaiguste korral immuunsüsteemi tugevdamiseks väsimuse korral rauavaegusest tingitud kehvveresuse korral südame rütmihäirete ja kõrgvererõhktõve puhul vere kõrge kolesteroolisisalduse vähendamiseks südameinfarkti ja ajuinsuldi ennetamiseks hingamisteede ja kopsupõletiku ning angiini raviks jne KIRSS :
Nt: H2SO4, HNO3, H2CO3 · Vesinikioonide(H+) ehk prootonite arvu järgi, mida happe molekul saab anda lahuses. Üheprootonihape- hape mille molekul annab lahusesse ainult ühe vesinikiooni. Nt: HNO3, HCl jne. Mitmeprootonihape- hape, mille molekul annab lahusesse kaks või enam vesinikiooni Nt: H2SO4, H2CO3, H3PO4. · Happe tugevuse järgi Tugevad happedon tugevalt happeliste omadustega. Tuntumatest hapetest kuuluvad tugevate hapete hulka vesinikloriidhape, väävelhape ja lämmastikhape. Nõrgad happed on oluliselt nõrgemate happliste omadustega.Enamik tuntud hapetest on nõrgad happed. Nt süsihape, divesinikulfiidhape, fosforhape, ränihape, äädikhape e. etaanhape. ' Hapete saamisvõimalusi · Happe saamine gaasilise vesinikühendi lahustamisel vees · Happe saamine happelise oksiidi reageerimisel veega nt. P4O10 + 6H2O =
Enamik metalle on keemiliselt aktiivsed. Eriti leelismetallid ja leelismuldmetallid, mis kuuluvad perioodilisustabeli kahte vasakpoolsesse rühma, Keemilise inertsuse tõttu on omamoodi erandiks väärismetallid. Metallide keemilist aktiivsust väljendab nn pingerida, ning enamik metalle tõrjuvad lahjendatud hapetest vesinikku välja Liik Esindajad Metallid Alumiinium Kroom Raud Vask Poolmetallid Germaanium Arseen Antimon Telluur Väärisgaasid Heelium Neoon Argoon Radoon Mittemetallid Vesinik Boor Süsinik Lämmastik
on samuti üks igapäevaelus tuntud aine, mida kasutatakse pesupulbris. Naatriumvesinikkarbonaat e. söögisooda on kasutusel saiatoodete valmistamisel.Naatrium leidub organismidest.Välimuselt on naatrium hõbevalge metall. Naatrium on pehme, teda saab noaga lõigata. Naatriumi tihedus on 0,97 g/cm3 ja sulamistemperatuur on 98 Celsiust. Ta on keemiliselt väga aktiivne, mistõttu hoitakse teda hapnikukindla kihi all, eemal veest. Naatrium reageerib paljude lihtainete, vee ja hapetega. Hapetest ja veest tõrjub ta välja vesinikku ning tekib vastavalt sool ja hüdroksiid. Suurem osa naatriumi sooli lahustub vees hästi. vask :Omadustelt on metall. Värvus varieerub punasest kuldkollaseni .Plastiline metall, mida hakati kasutama umbes 10 000 aastat tagasi. Vaske leidub looduses peamiselt ühenditena, näiteks sulfiidina (Cu2S) või rohelise malahhiidina, mis keemiliselt kujutab endast vaskhüdroksiidkarbonaati Cu2(OH)2CO3 ehk CuCO3 x Cu(OH)2. Et
Ioonreakstsioonid lahustes: 1), 2) (SO2, CO2, HCl (kui teine saadus on lahus), H2S), 3)H2O. 2NH4Cl+Ca(OH)2 2NH3+2H2O+CaCl2 Kui mõlemad algained on lahused, siis reaktsioon ei toimu. · Soolad, mis on moodustunud nõrkadest/tugevatest alusest ja hapetest, ei hüdrolüüsu. (CO+H2Oei toimu(neutr. kk), Cu(OH)2 - neutr. sest vees lahustamatu OH-, Al2O3+ H2Oei toimu, sest OH- ei lahustu vees). Näidisül. Vaja on neutraliseerida 0,3 dm3 Ba(OH)2 0,1 M lahust. Mitu g 10%-list HCl lahust selleks kulub? Ba(OH)2+2HClBaCl2+2H2O V(Ba(OH)2)=0,3 dm3 P(HCl)=10% 0,1 M 0,1 mol - 1 dm3 x = 0,03 mol 3 x mol - 0,3 dm n(Ba(OH)2)=0,03 mol n(HCl)=0,06 mol M(HCl)=1+53,5=36,5 g/mol m=n*M=0,06mol*36,5g/mol=2,19g
Keemiliste omaduste poolest kuuluvad leelismetallid kõige aktiivsemate elementide hulka - nad on väga tugevad redutseerijad. Naatriumi omadused Välimuselt on naatrium hõbevalge metall. Naatrium on pehme, teda saab noaga lõigata. Naatriumi tihedus on 0,97 g/cm3 ja sulamistemperatuur on 98 Celsiust. Ta on keemiliselt väga aktiivne, mistõttu hoitakse teda hapnikukindla kihi all, eemal veest. Naatrium reageerib paljude lihtainete, vee ja hapetega. Hapetest ja veest tõrjub ta välja vesinikku ning tekib vastavalt sool ja hüdroksiid. Suurem osa naatriumi sooli lahustub vees hästi. Omadustelt on naatrium leelismetall. Sellisena on ta oksüdatsiooniaste ühendites 1. Naatriumi reageerimisel hapnikuga tekib kergesti naatriumperoksiid, mitte naatriumoksiid. Kaalium ja teised aktiivsemad leelismetallid annavad hapnikuga reageerimisel põhisaadusena hüperoksiid (näiteks KO2) Na+ 02-> Na2O2 - naatriumperoksiid Na+ S-> Na2S Na+ Cl2-> NaCl
raske mürgistuse. Tuleohtlikkus · Tuleohtlikud on peaaegu kõik kergesti lenduvad lahused.Nt eeter,etanool,bensiin ja paljud teised. · Põlema ei sütti vedel lahus vaid lahuse auru ja õhu segu. · Tahked ained on vähem tuleohtlikud. · Plastmassi põlemine võib tekitada rasket mürgistust.( Laguneb polüvinüülkloriid) Söövitav toime. · Söövitava toimega keemiatooded on kontsentreeritud happed ja leelised. · Argielus on kasutatavatest hapetest kõige ohtlikum näiteks äädikhape. · Hapetega töötades on vaja panna kätte kummikindad. Plahvatusohtlikkus · Lõhkeaine koostises on palju hapnikku, mis kuumutamisel kergesti vabaneb. · Selle tulemusena hakkab lõhkeaine väga ruttu põlema ja plahvatab. · Kui näiteks saepuru immutada vedela hapnikuga, siis muutub see tugevajõuliseks lõhkeaineks. Kasutamine · Püssirohtu kasutatakse vähe. (jahimehed,laskesportlased jt)
Lämmastikhape Anett Roosa 9. a Kärdla Ühisgümnaasium Lämmastikhape Lämmastikhape (HNO3) on söövitav värvuseta teravalõhnaline vedelik ning mürgine hape, mis võib põhjustada tõsiseid põletushaavu. Värvuseta või pruun vedelik. Laialt levinud hapetest üks tugevamaid happeid. Iseloomulik terav lämmatav lõhn, mis pisut meenutab kloori lõhna. Kuulub mineraalhapete ja üheprootoniliste hapete hulka. Lämmastikhapet sisaldub ka happevihmades. Kolmemõõtmeline mudel Füüsikalised omadused Molekuli mass: 63,0 amü Sulamistemperatuur: 231,15 K (-42 °C) Keemistemperatuur: 356,15 K (83 °C) Tihedus: 1,522×10³ kg/m³ Lahustuvus: Segunev Ohutus
Omadused Hõbe on hõbevalge värvusega pehme metall. Võrreldes teiste vaserühma metallidega on hõbe vasest pehmem, kuid kullast kõvem. Hõbe on parim soojus- ja elektrijuht. Hõbedal on väga hea peegeldusvõime. Peegli saamiseks sadestatakse klaasile hõbedakiht. Hõbepeeglikiht rakendatakse ka termostes, vähendamaks soojuskadusid kiirgusel. Pehmuse ja plastilisuse tõttu on hõbe hästi töödeldav. Puhtas õhus on hõbe püsiv. Ka ei tõrju ta hapetest välja vesinikku. Hõbe reageerib kontsentreeritud lämmastikhappega: 3Ag + 4HNO3 = 3AgNO3 + NO2 + H2O ja kontsentreeritud väävelhappega 2Ag + 2H2SO4 = Ag2SO4 + SO2 + H2O Neis redoksreaktsioonides hõbe oksüdeerub, lämmastikhape või väävelhape redutseeruvad vastavateks oksiidideks Leidumine Hõbe on looduses vähelevinud element, siiski on seda umbes 20 korda rohkem kui kulda Hõbedat leidub nii ehedalt kui ka ühenditena (Ag2S, AgCl).
leidsin selle elemendi selleks kõige sobilikuma. Selle elemendi kohta leidub infot ning on ka ise endale uusi ning huvitavaid asju teada saada. Välimuselt on naatrium hõbevalge metall. Naatrium on pehme, teda saab noaga lõigata. Naatriumi tihedus on 0,97 g/cm3 ja sulamistemperatuur on 98 Celsiust. Ta on keemiliselt väga aktiivne, mistõttu hoitakse teda hapnikukindla kihi all, eemal veest. Naatrium reageerib paljude lihtainete, vee ja hapetega. Hapetest ja veest tõrjub ta välja vesinikku ning tekib vastavalt sool ja hüdroksiid. Suurem osa naatriumi sooli lahustub vees hästi.Omadustelt on naatrium leelismetall. Sellisena on ta oksüdatsiooniaste ühendites 1. Naatriumi reageerimisel hapnikuga tekib kergesti naatriumperoksiid Naaatriumit leidub praktiliselt kõikides toiduainetes ning naatriumi liigtarbimine võib põhjustada hulle tagajärgesid kuid sellest juba järgnevalt allpool olevas tekstis., mitte naatriumoksiid
Energiat läheb vaja toidu seedimiseks ja omastamiseks, mis on omakorda vajalik kasvamiseks ja kudede uuendamiseks ning kehaliseks ja vaimseks tegevuseks. Toiduenergiat saame toidust ja jookidest. Energiat tuleb toiduga saada täpselt nii palju, kui ära kulutatakse. Toiduenergiat mõõdetakse tavaliselt kilokalorites (kcal). 1 kcal = 4,2kJ Toiduainete energia põhilisteks allikateks on süsivesikud ja rasvad. Energiat saab ka suurel kogusel alkoholist ja orgaanilistest hapetest. Toidud sisaldavad energiat erinevates kogustes: 1 g valke = 4 kcal 1 g rasvu = 9 kcal 1 g süsivesikuid = 4 kcal 1 g absoluutset alkoholi = 7 kcal 1 g orgaanilisi happeid = 3kcal Energiavajadus sõltub: vanusest soost organismi ainevahetuse iseärasusest ja seisukorrast füüsiline aktiivsus Valgud Funktsioonid organismis: vajalikud organismi kasvuks ja ehituseks
Lämmastikhape Lämmastikhape Keemiline valem : HNO3 Lämmastikhape on söövitav värvuseta teravalõhnaline vedelik ning mürgine hape, mis võib põhjustada tõsiseid põletushaavu. Laialt levinud hapetest üks tugevamaid happeid. Iseloomulik terav lämmatav lõhn, mis pisut meenutab kloori lõhna. Füüsikalised omadused 99-protsendilise lämmastikhappe: Tihedus on umbes 1,52 g/cm³ Sulamistemperatuur on umbes -41,7 °C Keemistemperatuur on umbes 84 °C (lämmastikhape lagunemisel eraldub lämmastikdioksiid) Värvus- lämmastikhape ise on värvuseta, on tal enamasti punakaspruunikas või kollakas varjund, sest lagunemisel eraldub
Need on rahvusvahelised ja need peaks ära tundma igaüks. Soovitav on need ära õppida. Neid märgitakse ka tähtedega, tähed on kirjutatud märkide kohale. F-täht tähendab väga tuleohtlik. F+ tähendab aga eriti tuleohtlik. Xn on kahjulik (n on indeks). Xi on lausa ärritav. N on keskkonnaohtlik. T tähistab mürgist asja ja T+ on väga mürgine. C tähendab sööbivat. O on aga oksüdeeruv. E hoopiski plahvatusohtlik. Sööbivad on leelised ja enamik hapetest. Seepärast tuleb vältida isegi väikseid tilkasid nahale ja riietele. Aine sattumisel nahale tuleb saastatud kohta voolava vee all kaua pesta. Sissevõetud mürgiste ainete puhul sõltub esmaabi kasutatud mürkainest. Alati tuleb kohe pöörduda arsti poole. Mürgi eemaldamiseks võib esile kutsuda oksendamist, kuid mitte siis kui on sisse võetud seepi, leeliseid või happeid. Sellisel tuleb kannatanule anda palju piima, soovitav lisada sinna tooreid mune
molekulid Ga2. Madal sulamistemperatuur. Sulatatud Ga ruumala jahtumisel suureneb. Toatemperatuuril on Ga õhus muutumatu, kõrgemal temperatuuril tekib valge digalliumtrioksiid, mis reageerib edasi: 4Ga + 3O2 2Ga2O3 Ga2O3 + 4Ga 3Ga2O Toatemperatuuril või soojendamisel: Halogeenidega GaHal3 Väävliga Ga2S3 Lämmastikuga GaN Fosforiga GaP ...ja teiste mittemetallide ja poolmetallidega Vee suhtes püsiv, redutseerib hapetest vesiniku. Kasutusalad Kvartstermomeetrites temperatuuri mõõtmiseks; Kergsulavate sulamite koostises, mida kasutatakse sulavkaitsmeis ja tulekaitse signalisatsiooniseadmeis; Ga- ühendeid optiliste klaaside saamiseks; Üle 90% kulub pooljuhtmaterjalide valmistamiseks (põhiühend GaAs). Ühendid Ga2(SO4)3 galliumsulfaat valge kristalne aine, lähteaine galliumhüdroksiidi jt ühendite valmistamiseks.
disproportsioneerumisega: 3AuHal → AuHal3 + 2Au 4Au + 8NaCN + 2H2O2 → 4NaOH + 4Na[Au(CN)2] Broomiga reageerib kuld kõrgemal temperatuuril (150 °C) ning kuldtrijodiid on väga ebapüsiv ja laguneb kiiresti. Reageerimine tsüaniididega toimub hapniku osavõtul, soodsamalt vesinikperoksiidi osalusel (saaduseks on naatriumditsüanoauraat): 4Au + 8NaCN + 2H2O2 → 4NaOH + 4Na[Au(CN)2] Seda reaktsiooni tsüaniidiga kasutatakse ka kulla eraldamiseks maagist. Hapetest reageerib kuld ainult kuuma kontsentreeritud seleenhappega: 2Au + 6H2SeO4 → Au2(SeO4)3 + 3H2SeO3 + 3H2O Kulda suudab veel lahustada ka kuningvesi (HNO3/HCl). Kuningvee tekkimisel moodustuvad nitrosüülkloriid ja monokloor. Aktiivne monokloor reageerib kullaga, andeskuldkloriidi: 3HCl + HNO3 → NOCl + 2H2O + 2Cl Au + 3Cl → AuCl3 Lahuse ettevaatlikul soojendamisel tekivad vesiniktetrakloroauriidi kristallid: AuCl3 + HCl → H[AuCl4] http://upload.wikimedia
valem a a Tõrjuvad veest H2 välja, andes hüdroksiidi (vt 3.) Leelis LiOH Liitiumhüdroksiid Li+ Tõrjuvad hapetest vesiniku välja, andes soola Reageerivad lahuses oleva veega. Leelis NaOH Naatriumhüdroksii Na+ d Leelis KOH Kaaliumhüdroksiid K+ Leelis RbOH Rubiidiumhüdroksi Rb+
aastal 1807 Davy avastas elemendi elektrolüüsimeetodiga Davy kasutatud lähteainet nimetati tol ajal kaustiliseks soodaks, siis nimetas ta soodast eraldatud metalli sodium'iks Naatriumi omadused Välimuselt hõbevalge metall Pehme ja seda saab noaga lõigata Tihedus on 0,97 g/cm3 Sulamistemperatuur on 98°C Keemiliselt väga aktiivne, mistõttu hoitakse teda hapnikukindla kihi all, eemal veest. Reageerib paljude lihtainete, vee ja hapetega. Hapetest ja veest tõrjub ta välja vesinikku ning tekib vastavalt sool ja hüdroksiid. Suurem osa naatriumisooli lahustub vees hästi. Naatriumi reaktsioon veega Naatriumi ujumine vees https://www.youtube.com/watch?v=r4CdfaU7Ad4 Naatriumi reaktsioon veega Reaktsiooni tulemus oleneb ainete kogustest Reaktsiooni tagajärjel tekib tuli: https://www.youtube.com/watch?v=EK9XRFbQY0o
ühendid Kuumutamisel reageerib ka teiste mittemetallidega Reageerib lahjendatud hapetega Leelistega ei reageeri Konts. HNO3 toimel passiveerub Sulamid: Ni-Cu; Ni-Cr Alumiinium (Al) el. Nr 13 (3;8;2) aatommass 26,9815 Hõbevalge Tihedus 2,7 g/cm3 Sulamistemp. 660 kraadi C Väga hea korrosioonikindlus Hea elektri- ja soojusjuht, kerge ning äärmiselt plastiline Reageerib paljude lihtainete ja hapetega 2Al + 3I2 = 2AlI3 Hapetest tõrjub ta välja vesinikku ning tekib sool Lahjend, hapetest tõrjub välja vesiniku, leelistega tekivad kompleksühendid 2Al + 6H = 2Al+ 3H2 Külmas konts. Lämmastik- ja väävelhappes passiveerub, kuuma H2SO4 toimerl tekib Al2(SO4)3 ja eraldub SO2 2Al+6HNO3(konts.)= Al2O3 + 6NO2+ 3H2O Reageerib leelistega Sulamid duralumiinium (Al- Cu- Mg Mn) Silumiin (Al- Si) Magneesium (Mg) el. Nr 12 (2:8:2) aatommass 24,312 Tihedus 1,74 g/cm3 Sulamistemp. 650 kraadi C Väga hea korrosioonikindlus Hästi lõiketöödeldav ja keevitatav
Nii avastas Brand fosfori esimese elemendi, mis avastati pärast antiikaega. Kuigi kogused olid enam-vähem õiged (läks vaja 1,1 liitrit uriini, et toota 60 g fosforit), ei olnud vaja lasta uriinil roiskuma minna. Teadlased avastasid hiljem, et värske uriiniga saab toota sama palju fosforit. 2. Kes ja kuidas avastas vesiniku. Kirjutage reaktsiooni võrrandit. Vesiniku avastajaks (1766) loetakse inglise füüsik ja keemik Henry Cavendishi, kes isoleeris metallidest ja hapetest saadud "põleva õhu" (divesiniku) ning kirjeldas ja uuris seda põhjalikult. Vesiniku põlemisel on keemilise reaktsiooni võrrand: 2H2 + O2 = 2H2O 3. Keda peetakse kaasaegse keemia isaks ja miks? Antonie Lavoisier "kaasaegse keemia isa"- olulisemad avastused on seotud põlemisreaktsiooniga>põlemine on ühinemine hapnikuga. Kaasajal on sellest välja arenenud kalorimeetrija, millega mõõdetakse toiduratsiooni kalorite määra. 4
hologrammid. Tehes kogu protseduuri ära ca 4-5 tunniga ning küsides selle eest kõrget hinda. On hea kui klient on kursis, mida antud teenus endast kujutama ja sisaldama peaks, teadma mida ta soovib ning mille eest maksab! Pinnavärv • värvi ei kata läbipaistev lakikiht. Mittemetallik puhtad värvitoonid. Kriimud ja kahjustused tekivad värvi pinnale. Pleegib ja vananeb kiiremini kui lakikihiga kaitstud värvid. On vastuvõtlikum sooladest, hapetest ja UV-kiirgusest tingitud kahjustustele. Hea näide on heleroosaks muutunud punane värv. Hästi oluline on värvi kaitsta Paint Sealanti või vahaga. Pleekinud ja kahjustunud pinnavärv "enne ja pärast" allolevatel piltidel.
sepistada.Raud tõmbub mgneti külge. 3.Keemilised omadused.Keemiliselt puhtas raud on püsiv vee ja õhu suhtes.Tavaline raud(malm,teras) ,mis sisaldab mitmesuguseid lisandeid,korrodeerub niiskes õhus,kattudes keeruka koostisega rauaroostega. Kõrgel temperatuuril oksüdeerub raud õhus või hapnikus triraudtetraoksiidiks(Fe3O4):3Fe+2O2=Fe3O4 Veest aga tõrjub välja vesiniku (700 C) : 3Fe+4H2O=Fe3O4+4H2 Raua asukoht pingereas järeldub et ta on keskmise aktiivsusega metall ning tõrjub hapetest välja vesinikku:................... Kontsentreritud väävelhape ja lämmastikhape oksüdeerivad rauda,seejuures moodustub raua pinnale oksiidikiht,mis väldib metalli kokkupuudet happega.Seepärast kasutatakse kontsentreeritud väävelhappe ja lämmastikhappe säilitamisel ning transportimisel raudtaarat. Raua keemilisi omadusi iseloomustad järgmine skeem. 4.Raua oksiidid-Raua oksüdatsiooniaste on tavaliselt kaks või kolm.Raud (ii) oksiid (FeO) on must kristlane,õhus oksüdeeruv aine
näinud.Kuna uue metalli lähteaineks olid maarjalased (ladina keeles alumen), hakati metalli nimetama alumiiniumiks. Alumiiniumi keemilised omadused Järjenumber on 13 Massiarv on 27 Kõige püsivamates ühendites on o.-a. +3 Alumiiniumi oksiid on amfoteerne oksiid Asub IIIA rühmas ja 3. perioodis Amforteensuse tõttu reageerib leelistega, tõrjub välja vesiniku ja moodustab aluminaate Reageerib paljude lihtainete ja hapetega, hapetest tõrjub vesiniku, tekib sool Reageerides hapnikuga, tekib tema pinnale õhuke ja tihe oksiidikoht Alumiiniumi füüsikalised omadused Hõbevalge värvusega, läikiv Tihedus on 2,7 g/cm³ Sulamistemperatuur on 660 °C Keemistemperatuur 2519 ºC Peegeldab hästi valgust Suhteliselt kerge Hea elektri- ja soojusjuht Hästi töödeldav Pehme ning kergesti kriimustatav Alumiinium Tekkis loodusesse kosmiliste kiirte mõjul
Toidupüramiid Taldrikureegel Click to edit Master text styles Second level Third level Fourth level Fifth level Energia Toiduenergiat mõõdetakse kilodzaulides (kJ), megadzaulides (MJ) või kilokalorites (kcal). 1 kcal= 4,2 kJ ja 1 MJ= 1000 kJ. Toiduenergia põhilisteks allikateks on süsivesikud ja rasvad. Energiat saadakse ka alkoholist ja orgaanilistest hapetest. Energiavajadus sõltub: vanusest soost organismi ainevahetuse iseärasusest ja seisukorrast paljudest väiksematest teguritest kõige enam füüsilisest aktiivsusest Valgud Valgud koosnevad aminohapetest, mis jagatakse omakorda asendamatuteks, mida peab saama toiduga, ja asendatavateks, mida organism suudab ise sünteesida. Erinevad toidud sisaldavad aminohappeid erinevas kombinatsioonis ja koguses. Valkude funktsioonid
vähenemine. Oksüdeerumine-elektronide loovutamine redoksreaktsioonis, sellele vastab elemendi oksüdatsiooniastme suurenemine. Katalüsaator-aine, mis muudab reaktsiooni kiirust, vabanedes reaktsiooni lõpus esialgses koostises ja koguses. Aktiivsed metallid (K-Mg) reag. külma veega, tekivad leelis ja H2. Ca+2H2O=Ca(OH)2+H2. Zn+H2O=ZnO+H2. Väheaktiivsed metallid (alates Ni-st) ei reageeri veega. Vesinikust eespoololevad metallid tõrjuvad hapetest vesiniku välja. Zn+2HCl=ZnCl2+H2. Metall reageerib vees lahustuva soolaga, kui ta on aktiivsem kui soola koostises olev metall. Zn+CuCl 2=ZnCl2+Cu. 2Na+CuCl2+2H2O= Cu(OH)2+2NaCl+H2 2Na+ 2H2O=2NaOH+H2 2NaOH+CuCl 2=Cu(OH)2+2NaCl. Hapnikuga tekivad oksiidid: 2Ca+O2=2CaO. Väävliga tekivad sulfiidid: Ca+S=CaS. EI REAGEERI!: Plii+Vesi, Vask+Magneesiumkloriid, Hõbe+Väävelhape, Vask+Vesi. 0 I+ V+ II- I+ V+ II- IV+ II- I+ II- As + 5HNO3 H3AsO4 + 5NO2 + H2O
37. Kas pingereas paremal pool asuvad metallid on kõige vähema aktiivsemad? 38. Kas metalli asukoht pingereas iseloomustab ka metalli võimet tõrjuda teisi metalle nende ühenditest välja? 39. Kas aktiivsed metallid tõrjuvad veest välja vesinikku? 40. Kas keskmise aktiivsusega metallid tõrjuvad veearust välja vesinikku(kuumutamisel) ? 41. Kas vähemaktiivsed metallid ei reageeri üldse veega? 42. Kas enamus metalle tõrjuvad hapetest välja vesinikku? 43. Kas redoksreaktsioone kasutatakse elektrienergia saamiseks? 44. Kas tsink reageerides vasesoola lahusega oksüdeerub? 45. Kas metalli hävimist ümbritseva keskkonna toimel nimetatakse korrosiooniks? 46. Kas ladina keeles tähendab corrosio puruksnärimist? 47. Kas metallide korrosioon on alati redoksreaktsioon? 48. Kas on võimalusi korrosiooni vastu võitlemiseks? 49. Kas elektrokeemiline kaitse aitab korrosiooni vastu? 50
Kõige raskem metall tihedus normaaltingimustel 13500 kg/m³ Lihtainena hõbevalge läikiv metall Niiskes õhus kattub aegapidi oksiidikilega ja kaotab läike Kergesti sulav Vedelas olekus väga halva elektrijuhtivusega KEEMILISED OMADUSED Perioodi viimane d-element Oksüdatsiooniaste on I või II Enamik ühendeid on vähepüsivad, kuid erakordselt mürgised Asub metallide pingereas vesinikust vasakul ega tõrju seepärast hapetest vesinikku välja Reageerib vaid nende hapetega, mille anioonid on tugevamad oksüdeerijad Reageerib väävli ja joodiga tavalistes tingimustes Lahustab kulda, hõbedat, tsinki, vaske, pliid jt metalle, moodustades amalgaame Õhus on püsiv Õhus kuumutamisel ühineb hapnikuga, andes kollakaspunase värvusega elavhõbeoksiidi HgO, mis veidi kõrgemal temperatuuril laguneb taas lihtaineteks KASUTAMINE
kool Alumiinium Referaat nimi 2011 Alumiiniumist Alumiinium on keemiline element. Alumiinium on hõbevalge metall tihedusega 2,7 g/cm³ ja sulamistemperatuuriga 660 °C. Alumiiniumi keemilise aktiivsuse tõttu teda looduses lihtainena ei esine. Alumiinium reageerib paljude lihtainete ja hapetega. Hapetest tõrjub ta välja vesinikku ning tekib sool. Amfoteersuse tõttu reageerib alumiinium ka leelistega, tõrjudes nende lahustest vesinikku välja ja moodustades aluminaate. Kõigis püsivamates ühendites on alumiiniumi oksüdatsiooniaste +3. Alumiiniumoksiid on amfoteerne oksiid. Alumiiniumi saadakse boksiidist. Alumiiniumi sulatus on üks kõige energiamahukamaid tootmisi. Sellepärast rajati alumiiniumi tootmist tehaseid hüdroenergiajaamade lähedusse.
Alumiiniumi sümbol on Al. Alumiinium on hõbevalge pehme ja plastne hästi elektrit ja soojust juhtiv kergmetall, mida on hõlbus sepitseda ja valtsida. Alumiiniumi järjekorra number on 13. Tal on üks stabiilne looduslik isotoop massiarvuga. Radioaktiivne isotoop massiarvuga 26 tekib looduses kosmiliste kiirte mõjul. Alumiiniumi tihedus on 2.7 Mg/ kuupsentimeetrile. Sulamistemperatuur on alumiiniumil 660´C. Alumiinium reageerib paljude lihtainete ja hapetega. Hapetest tõrjub ta välja vesiniku ning tekib sool. Amfoteeruse tõttu reageerib alumiinium ka leelistega, tõrjudes nende lahustest vesinikku välja ja moodustades aluminaate. Kõigis püsivamates ühendites on alumiiniumi oksüdatsiooniaste +3. Alumiinium oksiid on amfoteeme oksiid. See tähendab,et tal on nii aluselisi kui ka happelisi omadusi. Alumiinium on vee ja õhu toimele vastupidav, sest tema pinnale tekib tihe oksüdatsioonikiht mis takistab alumiiniumi edasist oksüdeerumist.
Võib õhust niiskust koguda ja reageerides õhu CO2 `ga moodustada karbonaate. Vältida kokkupuuded veega (lahustumine on eksotermiline protsess), hapetega, osade metallidega (nt. Al, Mg, Sn, Pb, Zn), orgaaniliste materjalidega (nahk, vill), orgaaniliste halogeenühenditega, nitro- ja kloroorgaaniliste ühenditega, ammooniumsooladega, mõningate plastik- ja kummimaterjalidega. Naatriumoksiid, rektsioonil metallidega H2, reaktsioonil ammooniumsooladega NH3. Hoida eemal hapetest, metallidest, orgaanilistest peroksiididest ja kergeltsüttivatest ainetest. Kasutatud allikad : 1) http://www.ingle.ee/failid/ntqzodk0.doc 2) et.wikipedia.org/wiki/Naatriumhüdroksiid 3) http://www.ktk.ee/index.php? tid=asojJiHdj8ZROzzRxhXusXkKzjsLR88TxkZK6sKOl8&path=dku7uK6ll7 Ol9djRJhk8h 4) www.thermo.com/eThermo/CMA/PDFs/Various/File_2798.pdf 5) www.kemikaal.ee/tooted.php?cat=54 6) tera.chem.ut.ee/~ivo/akpr1/naoh.doc 7) http://et.itpedia.sfilar
Et Davy kasutatud lähteainet nimetati tol ajal kaustiliseks soodaks, siis nimetas ta soodast eraldatud metalli sodium'iks. Naatriumi omadused Välimuselt on naatrium hõbevalge metall. Naatrium on pehme, teda saab noaga lõigata. Naatriumi tihedus on 0,97 g/cm3 ja sulamistemperatuur on 98 Celsiust. Ta on keemiliselt väga aktiivne, mistõttu hoitakse teda hapnikukindla kihi all, eemal veest. Naatrium reageerib paljude lihtainete, vee ja hapetega. Hapetest ja veest tõrjub ta välja vesinikku ning tekib vastavalt sool ja hüdroksiid. Suurem osa naatriumi sooli lahustub vees hästi. Omadustelt on naatrium leelismetall. Sellisena on ta oksüdatsiooniaste ühendites 1. Naatriumi reageerimisel hapnikuga tekib kergestinaatriumperoksiid, mitte naatriumoksiid. Naatriumi kasutamine Naatrium on maakoores neljas kõige levinum metall ja kõige levinum leelismetall. Metallilist
.. tahked. Süsiniku arvu kasvuga muutub molekulmass, tihedus ning kasvab sulamis- ja keemistemperatuur. Tahked alkaanid ei märgu. Vedelad alkaanid on tüüpilised hüdrofoobsed lahustid, mis lahustavad teisi hüdrofoobseid aineid, kuid ei lahusta hüdrofiilseid materjale ega lahustu ise vees. Alkaanide aurud, gaasid, on elusorganismidele ohtlikud ning tugeva narkootilise toimega. On tavalisel temperatuuril oksüdeerijate suhtes üpris püsivad. Alkaanidesse ei toimi ka enamik kontsentreeritud hapetest ega leelistest. Sellised omadused on tingitud C-C ja C-H sideme suurest püsivusest. Reaktsioonide kulgemiseks, st. ainete muundumiseks, on esmalt tarvis enamikel juhtudel lõhkuda sidemed, et võiks toimuda uute sidemete moodustumine. Lõhkumiseks tuleb molekulile anda kuumutamise ja kiirguse abil anda hulk energiat juurde. Madala reaktsioonivõime tõttu ei reageeri alkaanid ka inimorganismis. Seetõttu pole alkaanid ei toitained ega ka eriti mürgised
Omaduse: Hõbe on hõbevalge värvusega pehme metall. Võrreldes teiste vaserühma metallidega on hõbe vasest pehmem, kuid kullast kõvem. Hõbe on parim soojus- ja elektrijuht. Hõbedal on väga hea peegeldusvõime. Peegli saamiseks sadestatakse klaasile hõbedakiht. Hõbepeeglikiht rakendatakse ka termostes, vähendamaks soojuskadusid kiirgusel. Pehmuse ja plastilisuse tõttu on hõbe hästi töödeldav. Puhtas õhus on hõbe püsiv. Ka ei tõrju ta hapetest välja vesinikku. Hõbe reageerib kontsentreeritud lämmastikhappega: 3Ag + 4HNO3 = 3AgNO3 + NO2 + H2O ja kontsentreeritud väävelhappega: 2Ag + 2H2SO4 = Ag2SO4 + SO2 + H2O Neis redoksreaktsioonides hõbe oksüdeerub, lämmastikhape või väävelhape redutseeruvad vastavateks oksiidideks. Hõbeesemed, eriti hõbelusikad, muutuvad aja jooksul tumedaks, kattudes õhus sisalduva vesiniksulfiidi mõjul hõbe sulfiidiga Ag 2S : 4Ag + 2H2S + O2 = 2Ag2S + H2O
Vesinik Nimi Klass Kool Sisukord Elemendi avastamine Koht perioodilusustabelis Vesiniku üldiseloomustus Leidumine looduses Funktsioon inimorganismis Elemendi avastamine Vesiniku avastajaks (1766) loetakse inglise füüsik ja keemik Henry Cavendishi, kes isoleeris metallidest ja hapetest saadud "põleva õhu" (divesiniku) ning kirjeldas ja uuris seda põhjalikult. Elavhõbeda ja happe segus tekkisid väikesed gaasimullid, mille koostist ei õnnestunud tal samastada ühegi tuntud gaasiga. Kuigi ta ekslikult arvas, et vesinik on elavhõbeda (mitte happe) koostisosa, suutis ta selle omadusi hästi kirjeldada. Antoine Laurent de Lavoisier avastas vesiniku 1766 sõltumatult Cavendishist, kui ta tahtis katseliselt näidata, et keemiliste reaktsioonide käigus massi ei kao ega teki
kokku mitu miljonit tonni aastas. Kosmeetikatööstuses, kangaste pehmendajana, plastide lisandina, korrosiooniinhibaatorina jne. Dihapped on looduses üsna levinud. Lihtsaim neist etaandihape ehk oblikhape HOOCCOOH. On mürgine aine mida leidub spinatis, hapuoblikas, rabarbris mitte küll ohtlikes kogustes. Oblikhapperikaste toitude tarvitamine vähendab organismi kaltsiumivarusid ning soodustab neerukivide tekkimist. Küllastumata hapetest on olulisemad küllastumata rasvhapped. Tehnikas on tähtis roll propeenhappel ehk akrüülhappel ja metüülpropeenhappel ehk metakrüülhappel, millest valmistatakse polümeere. Benseenkarboksüülhape ehk bensoehape on lihtsaim aromaatne hape. On valge kristlane aine, mida kasutatakse keemiatööstuses, samuti toiduainetööstuses konservandina (säilitusainena) E210.
HclO = HCl + O siin eraldub aktiivne monohapnik , mis valastab värve ja kasutatakse pleegitusvahendina. Saamine: Cl2 toodetakse sulatatud keedusoolast elektrolüüsimisel : NaCl = Na + Cl K (-) Na + e -> Na A (+) Cl e -> Cl 2Cl = Cl2 Halogeniidid Vesinikhalogeniidid on HF , HCl , HBr , HI. Füüsikalised omadused: Nad on terava lõhnaga mürgised gaasid , lahustuvad hästi vees , andes vesinikhalogeniidhappeid. Tuntum hapetest on vesinikkloriidhape e. Soolhape , mis võib olla kuni 40 %-line. Kontsentreeritud hape ,,Suitseb" õhu käes , sest lahusest eralduv vesinikkloriid lahustub õhuniiskuses ja tekitab nö . suitsu Vesinikfluoriidhape on keskmise tugevusega hape , kuid väga agresiivne , ta söövitab isegi klaasi ja kvartsi. Seda omadust kasutavad klaasikunstnikud klaasnõude kaunistamiseks. Keem. Omadused : Vesinikkloriidhape on tugev hape , ta on täielikult dissotsieerunud
KCl või CaCl2. Seejuures on sulandi temperatuur elektrolüüsiprotsessil 570 580 ºC. Naatriumi omadused: · Välimuselt on naatrium hõbevalge metall. · Naatrium on pehme, teda saab noaga lõigata. · Naatriumi tihedus on 0,97 g/cm3 ja sulamistemperatuur on 98 Celsiust. · Ta on keemiliselt väga aktiivne, mistõttu hoitakse teda hapnikukindla kihi all, eemal veest. · Naatrium reageerib paljude lihtainete, vee ja hapetega. Hapetest ja veest tõrjub ta välja vesinikku ning tekib vastavalt sool ja hüdroksiid. · Suurem osa naatriumi sooli lahustub vees hästi. · Omadustelt on naatrium leelismetall. · Sellisena on ta oksüdatsiooniaste ühendites 1. · Naatriumi reageerimisel hapnikuga tekib kergesti naatriumperoksiid, mitte naatriumoksiid. * Naatriumi avastamine:
Vastavalt süsinikahela pikkusele võivad alkaanid olla nii gaasilised, vedelad kui ka tahkel. Süsinike arv Aine olek 14 Gaasiline 5 - 15 Vedel 16 - ... Tahke 7.Alkaanide keemilised omadused (reag hapnikuga, vastastiktoime veega) Alkaanid on tavalisel temperatuuril oksüdeerijate suhtes üpris püsivad. Alkaanidesse ei toimi ka enamik kontsentreeritud hapetest ega leelised. Alkaanid on väga vähe reaktsioonivõimelised. See tuleneb C C ja C H (-sideme) suurest püsivusest. Selle sideme lõhkumiseks on vaja palju energiat kas tugeva kuumutamise teel või energiarikka kiirguse abil.
6. kergelt süttiv 4 VESINIKU AVASTUS On arvatud, et vesinikku tundis juba Paracelsus, kuid see on vaieldav... Arvatavasti esimesena sai vesinikku Robert Boyle, kes 1671 kirjeldas rauapulbri toimel lahjendatud väävelhappele saadud "kergesti põlevat auru"... Vesiniku avastajaks (1766) loetakse inglise füüsik ja keemik Henry Cavendishi, kes isoleeris metallidest ja hapetest saadud "põleva õhu" (divesiniku) ning kirjeldas ja uuris seda põhjalikult. Elavhõbeda ja happe segus tekkisid väikesed gaasimullid, mille koostist ei õnnestunud tal samastada ühegi tuntud gaasiga. Kuigi ta ekslikult arvas, et vesinik on elavhõbeda (mitte happe) koostisosa, suutis ta selle omadusi hästi kirjeldada... Antoine Laurent de Lavoisier avastas vesiniku 1766 sõltumatult Cavendishist, kui ta tahtis
kullaks, aga hoopis tekkis valge vahane aine, mis helendas pimedas. Nii avastas Brand fosfori – esimese elemendi, mis avastati pärast antiikaega. Kuigi kogused olid enam-vähem õiged (läks vaja 1,1 liitrit uriini, et toota 60 g fosforit), ei olnud vaja lasta uriinil roiskuma minna. 2. Kes ja kuidas avastas vesiniku. Kirjutage reaktsiooni võrrandit. Vesiniku avastas 1766 aastal füüsiku ja keemiku juuurtega inglane Henry Cavendish, kes isoleeris metallidest ja hapetest saadud "põleva õhu" (divesiniku) ning kirjeldas ja uuris seda põhjalikult. Vesiniku põlemisel on keemilise reaktsiooni võrrand: 2H2 + O2 = 2H2O 3. Keda peetakse kaasaegse keemia isaks ja miks? Keemia isaks peetakse Antonie Lavoisier kelle olulisemad avastused on seotud põlemisreaktsiooniga ehk kus põlemine on ühinemine hapnikuga. Kaasajal on sellest välja arenenud kalorimeetrija, millega mõõdetakse toiduratsiooni kalorite määra. 4
Enamik metallidega toimuvaid keemilisi reaktsioone toimub pingerea alusel. Metallide pingerida ( Allpool toodud metallide pingereas on väljatoodud ainult levinumad metallid) Keskmise Aktiivsed metallid Väheaktiivsed metallid aktiivsusega Li K Ba Ca Na Mg Al Zn Cr Fe Ni Sn Pb H Cu Hg Ag Au Tõrjuvad lahjendatud hapetest välja vesiniku (reag. hapetega) Ei tõrju hapetest Mg + H2SO4 MgSO4 + H2 vesinikku välja (ei reageeri hapetega) Reag. veeauruga, Reag. toatemperatuuril tekib oksiid ja veega, tekib alus ja vesinik vesinik Ei reageeri veega 2K + 2H2O 2KOH + H2 Zn+ H2O ZnO+ H2
Alumiinium (Aluminium) on keemiline element järjenumbriga 13. Alumiiniumoksiid on amfoteerne oksiid. Tal on üks stabiilne looduslik isotoop massiarvuga. Radioaktiivne isotoop massiarvuga 26 tekib looduses kosmiliste kiirte mõjul. Alumiinium reageerib paljude lihtainete ja hapetega. Hapetest tõrjub ta välja vesinikku ning tekib sool. Amfoteersuse tõttu reageerib alumiinium ka leelistega, tõrjudes nende lahustest vesinikku välja ja moodustades aluminaate. Kõigis püsivamates ühendites on alumiiniumi oksüdatsiooniaste +3. Alumiiniumi tootmise lähtaineks on boksiid, mille valemit võib avaldada üldkujul AlO * nHO . Kaaliumalumiiniummaarjat kasutatakse juba ammusest ajast riide värvimisel. Avastamise lugu:
- ensüümid - õietolm - süsivesikud - valgud - mikroelemendid - orgaanilised happed - aromaatsed ühendid - mineraalained - vitamiinid - värvained - flavonoidid (taimsed pigmendid) 5 · Valminud mesi sisaldab: 18 22% vett 6 10% sahharoosi 70 80% puu- ja viinamarjasuhkrut 6 Mee koostis · Mesi keeruline bioloogiline saadus koosneb: - suhkrutest - orgaanilistest hapetest - mineraalainetest ja mikroelementidest (K, Na, Ca, Mg, Mn, Cu, Fe, Co, P, Zn, Cl, S, Ni, Cr) - C-, E-, K-, A-, PP- ja B-grupi vitamiinidest 7 · Mesi sisaldab alati õietolmu (1 kuupsentimeeter sisaldab keskmiselt 6000 õietolmutera) · Õietolmurikkam mesi on ka vitamiinirikkam · Õietolmuterade järgi saab kindlaks määrata, millistelt taimedelt nektar on korjatud 8