osmiumi, iriidiumi, pallaadiumi, roodiumi ja ruteeniumi. Ajalooliselt on väärismetallide hulka kuulunud näiteks alumiinium - kuigi ta on kõige levinum metall maakoores, oli teda raske saada puhtal kujul. Seetõttu oli alumiinium 19. sajandi I poolel kallim kui kuld. Kuld: ...on keemiline element järjenumbriga 79. Kullal on üks stabiilne isotoop massiarvuga 197. Keemilistelt omadustelt on kuld väheaktiivne metall. Ei reageeri vee ega hapetega. Kuld on väärismetall. Normaaltingimustel on ta võrdlemisi pehme kollane metall, mille tihedus on 19,7 g/cm³. Kulla sulamistemperatuur on 1064°C. Kuld mineraalina: Kuld on isotroopne kuubilise süngoonia mineraal. Polarisatsioonimikroskoobis on ta maakmineraalile tüüpilisena läbipaistmatu. Lõhenevus ja magnetilisus puuduvad. Kullal on metalliläige. Hõbe: ...on keemiline element järjenumbriga 47, metall. Stabiilseid isotoope on hõbedal kaks, nende massiarvud on 107 ja 109.Hõbe on väärismetall.
pallaadiumi sisaldub vastava väärismetalli sulamis selle tuhande massiosa kohta. Väärismetalli standardproov on käesoleva seadusega lubatud väärismetalli proov. Väärismetalltoode on ese, mis on tervikuna või osaliselt valmistatud ühest või enamast vähemalt väikseima standardprooviga väärismetallist" (Väärismetalltoodete seadus 2003). 1.1. Kuld Kuld on kollane, pehme, kuid raske väärismetall. Kuld koosneb kristallstruktuurist, seega on kristalliline materjal, st siseehituses on aatomid paigutatud kindla korduva korrapärasusega kõikides tasapindades. Looduses leidub kulda ehedal kujul. (Kuld 2006) Kulla sulamistemperatuur on 1064,18 ºC ja tihedus 32 Mg/m3. (Väike Entsüklopeedia 2006). Kuld on normaalolekus inertne materjal, ta ei oksüdeeru hapnikus ega vees, on vastupidav temperatuurimuutustele ja hapetele.
Hõbe (Ag) Helis Lihtsa MJ112 Hõbe Hõbe on keemiline element järjenumbriga 47 Väärismetall Pehme metall, mis peegeledab valgust Sulab temperatuuril 960 0 C Aatomimass ümardatult 108 Hõbe Kasutati vanasti joodisena ning temast tehti peegleid Vähelevinud, kuid 20 korda rohkem kui kulda Leidub nii ehedalt kui ka ühenditena (Ag2S, AgCl) Lisandelemendina leidub hõbedat plii, tsingi ja vasemaagis Omadused Hõbevalge värvusega pehme metall Vasest pehme, kullast kõvem Parim soojus ja elektrijuht Hea peegeldusvõime Hästi töödeldav Valgustundlikkuse tõttu valmistatakse hõbedaühendeist filme ja fotopaberit Väärismetall hõbe on ehete, lauahõbeda, müntide, hambaplommide ja peeglimetal Eesti Vabariigi 10, 100 ja 300kroonised mälestusmündid on vermitud sulamist hõbedaprooviga 925 Hõbedaproov näitab hõbeda massiosade arvu tuhande massiosa hõbedasulami kohta (proov 925 tähendab, et 1000grammis sulamis on 925 g...
Mõnigi nüüdisaja argielu metall (raud, alumiinium) on kunagi olnud väärismetalli seisuses. Tänapäeval loetakse väärismetallideks kulda, hõbedat, plaatinat, pallaadiumi ja nende sulameid. Keemia seisukohalt on väärismetallid ka vask ja elavhõbe. Väärismetallideks loetakse ka plaatinametalle. Plaatinametallid on plaatina ja 5 sellele keemilistelt omadustelt lähedast metalli. Need metallid on iriidium, osmium, palladium, ruteenium ja roodium. 19. Sajandil oli väga kõrge hinnaga väärismetall alumiinium. See oli isegi kullast kallim. Kuigi seda peitub maakoores üsna palju, on seda sealt väga raske kätte saada. [1] Kuld. Kuld on väärismetall nimega aurum, lühendatult Au. Kulla järjekorranumber on 79 ning selle aatommass on 197. Kuld on kollase tooniga, pehme ja raske metall (tihedusega 19 300 kg/m3). Sulab temperatuuril (1064.18 °C). Kuld on ka hea elektrijuht. [2] Kulda leitakse looduses ehedana, nt. mineraal kvartsi pragudes, terakestena kulda sisaldunud
Hõbe Hõbe Hõbe e. Ag, (ladina keeles argentum) Keemiliste elementide perioodilisussüsteemi I rühma element Väärismetall Järjenumber 47 Aatommass 107,8682 Tihedus on 10,5 g/cm³. Hõbe sulab temperatuuril 960°C. Ta kuulub väärismetallide hulka. Hõbe on perioodiliste elementide perioodilisussüsteemi 11. rühm Ühendeis on hõbeda oksüdatsiooniaste I. Omadused Hõbe on hõbevalge värvusega pehme metall. Võrreldes teiste vaserühma metallidega on hõbe vasest pehmem, kuid kullast kõvem. Hõbe on parim soojus- ja elektrijuht. Hõbedal on väga hea peegeldusvõime. Peegli saamiseks sadestatakse klaasile hõbedakiht. Hõbepeeglikiht rakendatakse ka termostes, vähendamaks soojuskadusid kiirgusel. Pehmuse ja plastilisuse tõttu on hõbe hästi töödeldav. Puhtas õhus on hõbe püsiv. Ka ei tõrju ta hapetest välja vesinikku. Hõbe reageerib kontsentreeritud lämmastikhappega: 3Ag + 4HNO3 = 3AgNO3 + NO2 + H2O ja kontsentreeri...
KULD AU & AURUM Keemiline element Kuld on keemiline element, järjenumbriga 79. Kullal on üks stabiilne isotoop massiarvuga197. Keemilistest omadustest on kuld väheaktiivne metall. Ei reageeri vee ega hapetega. Kuld on väärismetall. Normaaltingimustes on ta võrdlemisi pehme kollane metall, mille tihedus on 19,7 g/cm³. Kulla sulamistemperatuur on 1064°C Kuld mineraalina Kuld on isotroopne kuubilise süngoonia mineraal. Polarisatsioonimikroskoobis on ta maakmineraalile tüüpilisena läbipaistmatu. Lõhenevus ja magnetilisus puuduvad. Kullal on metalliläige. Maailma suurimad kullavarud asuvad Lõuna-Aafrika vabariigis Koostis / struktuur Keemiline element kuld (Aurum, Au)kristallstruktuur
• Tina on looduses vähe • Tina sulamistemperatuur on 232 °C. • Tina kasutatakse õhukese kihina terase kaitsmisel . • Tina on pehme metall Plogspot19.11.2015 HÕBE • Hõbe on kõige levinum väärismetall • Maakoores on ta keemiliste elementide levimuselt 65. kohal. • Ehedat hõbedat tunti juba 3000 aastat eKr Egiptuses, Pärsias, Hiinas. • Hõbedast vermitakse münte tehakse kaunistusi, ehteid, kalleid laua- ja kööginõusid. Plogspot19.11.2015 KULD
Viimase 50 aasta jookul on plaatina tootmine muutunud umbes 30 kordseks. Plaatina oli seitsmekümnendail- kaheksakümnendail kullast 1,5 korda kallim. Maakoores on ühe tonni kohta 5mg plaatinat, aga raudmeteoriidis 30g plaatinat. Ehetes kasutatav plaatina on kuue metalli segu. Need metallid on plaatinale väga sarnased ja need olid peaaegu et eristamatud kuni 19. sajandini. Tänapäeval sulatatakse plaatina tihti kokku vase ja titaaniga. Plaatina on ainus väärismetall, mis on allergiat leevendava toimega ja ehetes kasutatakse seda väga puhtalt. Plaatina kasutamises on toimunud suuri muutusi . Alguses piirasid selle kasutust tema kõvadus ja sulamistemperatuur. Plaatinat oli väga raske siis töödelda .Pariisi kauplusevitriinidesse ilmusid plaatinaehted aastal 1776. 19.sajandil olid venemaal käibel 3-, 6-, ja 12- rublased plaatinamündid .Prantsusmaal tehti plaatinast 20- frangilisi münte ja Inglismaal naelsterlingilisi münte, mis kullati üle
Hõbe Keemia referaat Väärismetallid on haruldased metallid, millel on majanduslikult kõrge, suhteliselt stabiilne väärtus. Tänapäeval loetakse väärismetallideks kulda, hõbedat, plaatinat, pallaadiumi ja nende sulameid. Hõbe (Argentum,Ag) Hõbe, Ag, (ladina keeles argentum), keemiliste elementide perioodilisussüsteemi I rühma element, väärismetall; järjenumber 47, aatommass 107,8682. Hõbe on hästi sepistatav metall. Ta kuulub väärismetallide hulka. Arvatavasti seepärast kuulub hõbe elementide hulka, mida inimkond tundma õppis. Vanimad, Indiast leitud hõbeehted ja nõud pärinevad IV-III aastatuhandest enne meie ajaarvamist. Hõbedat kasutati vanasti ka joodisena ning temast tehti peegleid. Hõbe on perioodiliste elementide perioodilisussüsteemi 11. rühma ehk IB-rühma element. Ühendeis on hõbeda oksüdatsiooniaste I. Leidumine: Hõbe on looduses vähelevinud element, siiski on seda umbes...
Kuld (Aurum,Au)on tähtis väärismetall, mida on sajandeid kasutatud rahana, vara säilitajana ja juveelinduses. Looduses esineb kuld väikeste terakeste või kamakatena kivis. Uute kullaleiukohtade avastamine on sageli esile kutsunud nn. kullapalaviku (nt. 1897-1898 Klondikes Alaskal). Omadused Puhas kuld on eredat kollast värvi, mida on ajalooliselt peetud atraktiivseks, lisaks on ta tihe, läikiv ja kõige vormitavam ning plastilisem väärismetall.Kuld on pehme (kõvadus 2,5), raske (tihedus 19 300 kg/m3) metall. Sulab temperatuuril 1337.33 K (1064.18 °C). Hea elektrijuht (eritakistus 2,2·10-8 Wm). Keemiliselt inertne viimane väide aga lakkab olemast õige, kui tegemist on väga väikeste kullaosakestega. Nn. nanokuld on näiteks väga efektiivne vingugaasi (toatemperatuurse) osüdatsiooni katalüsaator . Ajalugu Juba eelajaloolistest aegadest alates on kulda peetud tähtsaimaks metalliks. Egiptuse
perioodini ning tema tähelend lõppes Teise maailmasõjaga, mil ta kuulutati strateegiliseks metalliks ja selle mittesõjaline kasutus keelati. Keeld seostus plaatina ulatusliku kasutusega tööstuses. Plaatina on oluline tooraine autotööstuses, elektroonikas, naftakeemias, aga ka meditsiinis. Igas auto katalüsaator sisaldab plaatinat. Plaatina võlu peitub ta välimuses. Tema välge sära on ainulaadne. Ta on ka kõige kõvem ehetes kasutatav väärismetall ning kaks korda raskem kui 14 karaadine kuld. Plaatina on haruldane väärismetall. Praegu ongi plaatina ehtemetallina kõige otsitum hinnaliste vääriskivide (peamiselt briljantide) raamimisel (peamiselt oma tugevuse ja vastupidavuse pärast).Juveelitööstus kulutab40% maailma plaatinatoodangust. Ühe grammi plaatina saamiseks tuleb mõnigi kord töödelda vagunitäis maaki. Õige oli käibeväljend: üks gramm toodangut üks aasta tööd.
Värvus: Hõbedane (http://www.euyouth.net/projects/keemia/index.php?sisu=elemendid&element=pt) 2. Plaatina Plaatina on keemiliste elementide perioodilisussüsteemi VIII rühma element, selle järjenumber on 78 ning aatommass 195.08. Looduslik plaatina koosneb 5 stabiilsest isotoobist ja radioaktiivsest isotoobist. Plaatina on hõbevalge plastne hästi töödeldav raskemetall. Omadustelt on plaatina plaatinametall ja sellisena väärismetall. Tema tihedus normaaltingimustel on 21,1 g/cm³ ja tema sulamistemperatuur 1768 Celsiuse kraadi. See metall on keemiliselt väheaktiivne, õhus püsiv ning ei reageeri hapetega ega leelislahustega, toatemperatuuril reageerib aeglaselt broomiga, kuningveega moodustab heksaklorophappe H 2 PtCl6 . Kõrgematel temperatuuridel ( üle 400 500 °C ) reageerib halogeenide ja teiste mittemetallidega näiteks fosfori, väävli ja süsinikuga. (Ülo Kaevats, Toomas Varrak, 1994, lk 340)
Plaatina(Pt) Avastuslugu. Tuntud kaugest minevikust. Ameerika asukad töötlesid juba 100 aastat e.m.a. Nimetati platina(hõbedakene) järgi. avastatipeale reisilt saadud kullapesemist, kus eraldati kullast plaatina. arvati, et tänu sellele, et plaatina ja kulla tihedused on lähedased, saab kulda võltsida. Valekulla vältimine. Omadused. Väärismetall Värvus: Hõbedane Tihedus: 21,45 g/cm3 Sulamistemperatuur: 1770 kraadi Keemistemperatuur: 3827 kraadi Prootonite/elektronide arv: 78 Neutronite arv: 117 Kristallide struktuur: Kuupjas Kasutusalad. Leidub looduses ehedalt ja mineraalidena. Ehted(kihlasõrmused) Tooraine autotööstuses, elektroonikas ja ka meditsiinis. Plaatina Aitäh kuulamast! :)
Kuld (Au) Kuld Keemiline element järjenumbriga 79 Kullal on üks stabiilne isotoop massiarvuga 197 Kulla keemilised omadused Väheaktiivne metall Ei reageeri veega Ei reageeri hapetega Kuld metallina Kuld on väärismetall ning kuulub B rühma metallide hulka Kuld normaaltingimustel Pehme kollane metall Tihedus on 19,7 g/cm³ Sulamistemperatuur on 1064°C. Kuld mineraalina On isotroopne kuubilise süngoonia mineraal Polarisatsioonimikroskoobis on ta maakmineraalile tüüpilisena läbipaistmatu Lõhenevus ja magentilisus puuduvad On metalliläige Kulla leiukohad Põhilised kullavarud asuvad Lõuna-Aafrika Vabariigis Kulla kasutusalad
Plaatina domineeris ehtemaailmas kuni Art Deco perioodini ning tema tähelend lõppes Teise maailmasõjaga, mil ta kuulutati strateegiliseks metalliks ja selle mittesõjaline kasutus keelati. Keeld seostus plaatina ulatusliku kasutusega tööstuses. Plaatina on oluline tooraine autotööstuses, elektroonikas, naftakeemias, aga ka meditsiinis. Iga auto katalüsaator sisaldab plaatinat. Plaatina võlu peitub ta välimuses. Tema välge sära on ainulaadne. Ta on ka kõige kõvem ehetes kasutatav väärismetall ning kaks korda raskem kui 14-karaadine kuld. Plaatina on haruldane väärismetall. Praegu ongi plaatina ehtemetallina kõige otsitum hinnaliste vääriskivide (peamiselt briljantide) raamimisel (peamiselt oma tugevuse ja vastupidavuse pärast). Juveelitööstus kulutab 40% maailma plaatinatoodangust. Ühe grammi plaatina saamiseks tuleb mõnigi kord töödelda vagunitäis maaki. Õige oli käibeväljend: üks gramm toodangut üks aasta tööd.
5 Mineraalid Kivimid koosnevad mineraalidest. Mineraal on tahke, anorgaanilise koostisega ja looduslik. Mineraalide teket jaotatakse endogeenseks ja eksogeenseks. Endogeensete mineraalide lähteaineks on magma. Eksogeensete mineraalide tekkele rabenemine, mis küll ei tekita uusi mineraale, kuid peenestades materjali teeb see lihtsamaks keemilise murenemise. Kuld Kuld on tihe, plastne, läikiv ja pehme väärismetall. Kuld esineb looduses mineraalina. Ajalooliselt on väljakujunenud peamiselt kaks kulla funktsiooni: raha ja ehete valmistamise materjal. Ürgajast peale on kuld olnud haruldane ehtemetall mis sümboliseerib rikkust ja selle kaudu ka võimu. Umbes 2500 aastat tagasi hakkas kuld ka kandma raha funktsiooni. Kuld ei lahtu hapnikus ega vees. 2012. aasta seisuga on kokku kaevandatud umbes 171 300 tonni kulda. Väidetavalt peitub enamus Maa kullast tema tuumas. Kuld ei tuhmu kunagi.
Ajaloo ajastud Esiaeg-inimese kujunemine ( ca 700000 a ). Püstine asend ja algelised tööriistad. Ajajooksul tekkis antikuleeritud kõne . Inimese aju areng on tihedas seoses tööriistade kujundamisega . Muinasaeg on kaasaegse inimese tekkest. Muinasaega mahub põllumajanduse tekke , koos sellega vaikne elu viis. Muinasajal levis homosapiens üle maailma. Muinasaeg jaotatakse kolme perioodi vastavalt tööriista materjalile , kivi-pronks ja raud. Muinasaja järel tuli vanaaeg ,-keskaeg ,- uusaeg ja kaasaeg. Inimajalugu teame ajalooallikate järgi . Arheoloogia on kaevur . Arheoloogide leide hoitakse muuseumites, arhiivis, kollektsioonides ja ülikoolides. Antiik äris müüakse vanu asju. Oome ehk tavaelu Tavaelu oli vanal ajal lihtne , lapsed valvasid tuld , emad korjasid marju ja muud söödavat. Mehed käisid jahil loomi küttimas , vahepeal kodustati hundid ja nad hakkasid majade ümbrust kaitsma. Varsti tulid ka tööriistad, siis mõeldi välja lõksud...
Iriidium Lühitutvustus Iriidiumi avastas inglise keemik Smithson Tennant aastal 1803 Iriidium sai oma nime Kreeka jumalate sõnumitooja Irise järgi Ta on üks haruldaseim element, mis maakoores leidub Iriidiumi tähis on Ir, ta asub VIIIB rühmas ning järjekorranumber on 77 Omaduselt on iriidium plaatinametall ja sellisena väärismetall Iriidium Iriidium on hõbedane, kõva ja rabe metall Click to edit Master text styles Sulamistemperatuuriks on 2466 °C Second level Third level ning keemistemperatuuriks 4428 °C Fourth level Tihedus normaaltingimustel on Fifth level 22,65g/cm³ On kõige korrosioonivastaseim metall
Hõbe Sisukord 2. Sisukord 3. Sissejuhatus 4. Leidumine 5., 6.Omadused 7. Kasutatud kirjandus Sissejuhatus Hõbe, Ag, (ladina keeles argentum), keemiliste elementide perioodilisussüsteemi 11. rühma ehk IB rühma element, on väärismetall mille järjenumber 47 ning aatommass 107,8682. Hõbe on värvuselt valge hästi sepistatav metall (kergelt kõvem kui kuld). Ta kuulub väärismetallide hulka. Arvatavasti just tema pehmuse tõttu kuulub hõbe nende elementide hulka, mida inimkond esimestena tundma õppis. Vanimad, Indiast leitud hõbeehted ja nõud pärinevad IV-III aastatuhandest enne meie ajaarvamist. Hõbedat kasutati vanasti ka joodisena ning temast tehti peegleid. Tal on kõige suurem soojus- ja elektrijuhtivus.
Roodium Roodium (kr rhodeios ,,roosa, roosavärviline") on keemiliste elementide perioodilisussüsteemi VIII rühma element, järjenumbriga 45. Roodiumi sümbol on Rh (rhodium). Roodiumi aatommass on 102,9055, aatomiraadius on 135 pikomeetrit Looduslikku roodiumi moodustab stabiilne isotoop 103 45 Rh (massiarvuga 103). Roodium on väärismetall ning plaattinametall (plaattinametallideks nimetatakse ka teisi omadustel plaattinale sarnanevaid elemente: iriidiumi, osmiumi, palladiumi ja ruteeniumi). Perioodilisussüsteemis loetakse teda koos koobalti, iriidiumi ja meitneeriumiga koobaltigruppi (9. gruppi). 103 Roodiumil on kokku 33 isotoopi, kuid looduslik roodium on 100% Rh. Püsivaimad kunstlikud
KULD 7 klass · Keemiline element aurum, Au · Tähtis väärismetall · Keemiline element järjenumbriga 79 · Kullal on üks stabiilne isotoop arvuga 197 · Väheaktiivne metall · Keemiliste elementide perioodilisussüsteemi I rühma element Omadused · Kollane, pehme (kõvadus 2,5) · Raske (tihedus 19 300 kg/m3) · Sulab temperatuuril 1337.33 K (1064.18 °C) · Hea elektrijuht (eritakistus 2,2108 Wm) · Helekollane, läikiv, hästitöödeldav (1 kg kulda saab venitada traadiks, mille pikkus on 3 km) ·
KULLA JÄLG Eneli Uusmets ja Kristin Laas 10.B ÜLDISELT KULLAST tihe, plastne, läikiv ja pehme väärismetall kollakas ja särav puhas kuld ei oksüdeeru hapnikus ega vees kulla keemilise elemendi sümbol on Au ja aatomnumber 79 raha ja ehete valmistamise materjal enamus Maa kullast peitub tema tuumas maailma suurimad kullavarud asuvad Lõuna-Aafrika Vabariigis. KAEVANDAMINE 2012. aasta seisuga on kokku kaevandatud umbes 171 300 tonni kulda Esimene etapp: Kullaotsijad lahustavad setteid kõrgsurvejoaga. Masinad pumpavad muda
Kuld Kuld on keemiline element järjenumbriga 79.Kullal on üks stabiilne isotoop massiarvuga 197.Keemilistelt omadustelt on kuld väheaktiivne metall. Ei reageeri vee ega hapetega.Kuld on väärismetall.Normaaltingimustel on ta võrdlemisi pehme kollane metall, mille tihedus on 19,7 g/cm³. Kulla sulamistemperatuur on 1064°C.Kuld on isotroopne kuubilise süngoonia mineraal. Polarisatsioonimikroskoobis on ta maakmineraalile tüüpilisena läbipaistmatu. Lõhenevus ja magnetilisus puuduvad. Kullal on metalliläige.Maailma suurimad kullavarud asuvad Lõuna-Aafrika Vabariigis. Koostis / struktuur Keemiline element kuld (Aurum, Au), kristallstruktuur tahkkeskendatud kuubiline võre. Omadused
umbes 900 000 tonni. Uuritud varu massiks hinnatakse 150 000 tonni, millest praeguse aastatoodangu (6000-7000 t) korral jätkuks kõigest veerand sajandiks. Juba paljude aastate vältel jääb hõbeda tootmine maha selle metalli tarbimisest, kusjuures vahe kaetakse sekundaarse hõbeda ümbersulatamise ja riikide reservide varal. Seni uuritud varust paikneb kaks kolmandikku Ameerikas ja Austraalias. Varu edasise täiendamise lootusi seostatakse eeskätt Aasiaga. Väärismetall hõbe on ehete, lauahõbeda, müntide, hambaplommide ja peeglimetall. Nüüdisajal on lisandunud suure mahtuvusega hõbetsinkakude ja elektroonikaesemete valmistamine. Eesti Vabariigi 10-, 100- ja 300-kroonised mälestusmündid on vermitud sulamist hõbedaprooviga 925. Hõbedaproov näitab hõbeda massiosade arvu tuhande massiosa hõbedasulami kohta (proov 925 tähendab, et 1000grammis sulamis on 925 grammi hõbedat ja 75 grammi vaske).Hõbedat rakendatakse
tähelend lõppes Teise maailmasõjaga, mil ta kuulutati strateegiliseks metalliks ja selle mittesõjaline kasutus keelati. Keeld seostus plaatina ulatusliku kasutusega tööstuses. Plaatina on oluline tooraine autotööstuses, elektroonikas, naftakeemias, aga ka meditsiinis. Igas auto katalüsaator sisaldab plaatinat. Plaatina võlu peitub ta välimuses. Tema välge sära on ainulaadne. Ta on ka kõige kõvem ehetes kasutatav väärismetall ning kaks korda raskem kui 14 karaadine kuld. 6 Kokkuvõte Plaatina on haruldane väärismetall. Praegu ongi plaatina ehtemetallina kõige otsitum hinnaliste vääriskivide (peamiselt briljantide) raamimisel (peamiselt oma tugevuse ja vastupidavuse pärast).Juveelitööstus kulutab 40% maailma plaatinatoodangust. Ühe grammi
Geograafia kordamine 19.02.10 1. Iseloomusta tootmiskorraldust fordismis ja toyotismis. FORDISM uutele harudele iseloomulik tootmise korraldus, konveieri Kasutuselevõtt, masstootmine, nn. "igaks juhuks tootmine". TOYOTISM paindlik tootmise korraldus, kus töölised lisaks oma tööoperatsiooni täitmisele osalevad ka tootearenduses, tekib meeskonnatöö, kasutatakse rohkeid allhankeid kindlatelt partneritelt, nn. "õigeks ajaks tootmine". Kasutatakse tugitootmise mudelit, st. toodetakse suurtes kogustes, samas tooted on varieeruvad. Jaapani autotootjad kasutavad ka ülikallist robottootmist, et tõsta tootmise kiirust ja kvaliteeti. 2. Võrdle fordismi ja toyotismi. Igaks juhuks Õigeks ajaks tootmine(fordism) tootmine(toyotism) Detailide hankimine ...
elektrokeemiline katmine (värv, õli, passiivne metall, lakk) iseeneslik kaitse (tekib oksiidikiht) 5) Korrosioonitõrje Korrosiooni tõrje roostevaba teras kroomimine katmine inhibiitor korrosiooni aeglustaja (nt NaNO3) 6) Kuidas esinevad looduses: a) aktiivsed metallid; b) vähemaktiivsed metallid; c) väärismetallid aktiivsed metallid looduses ühendite koostises (sooladena) vähemaktiivsed metallid looduses oksiidsed mineraalid väärismetall looduses mineraalidena, lihtainena ehedalt 7) Nimeta kõige levinuimaid metalle looduses levinuimad: Al, Fe, Ca, Na 8) Maavarade kaevandamine metallurgia: Metallide redutseerimine maagist Maagi rikastamine (maak vabastatakse lisanditest, kasutades füüsikaliste omaduste erinevust) särdamine metalli oksiidi redutseerimine metall oksiidse maagi redutseerimine: karbotermia ( Reag. C või reag CO) aluminotermia (reag Al) 9) Keemilised vooluallikad
a maksis maailmaturul unts (31,1 g) kulda 500, unts plaatinat aga 700 dollarit. Aastaks 2000 prognoositi plaatinametallide vajaduseks o Ehetes kasutatav plaatina on tegelikult kuue metalli - plaatina, pallaadiumi, roodiumi, ruteeniumi, iriidiumi ja osmiumi - sulam. Nimatatud metallid on plaatinale kaalult ja koostiselt nii sarnased, et olid pea eristamatud kuni 19. sajandini. Tänapäeval sulatatakse plaatina sageli kokku vase ja titaaniga. See on ainus väärismetall, mida kasutatakse 90-95- protsendilise puhtusega ehetes, mis on allergiat leevendava toimega ja ei määrdu. Plaatinast ehted kannavad märget: 900Pt, 950 Plat või Plat. Kasutusalad o Plaatina kasutamises on aegade vältel toimunud suuri muutusi. Algselt piirasid plaatina kasutust tema kõvadus ja kõrge sulamistemperatuur. Seda ei olnud lihtne olemasolevate tavaliste tehnikatega töödelda. o 1776. a ilmusid Pariisi kauplusevitriinidesse
Plaatina domineeris ehtemaailmas kuni Art Deco perioodini ning tema tähelend lõppes Teise maailmasõjaga, mil ta kuulutati strateegiliseks metalliks ja selle mittesõjaline kasutus keelati. Keeld seostus plaatina ulatusliku kasutusega tööstuses. Plaatina on oluline tooraine autotööstuses, elektroonikas, naftakeemias, aga ka meditsiinis. Iga auto katalüsaator sisaldab plaatina. Plaatina võlu peitub ta välimuses. Tema välge sära on ainulaadne. Ta on ka kõige kõvem ehetes kasutatav väärismetall ning kaks korda raskem kui 14-karaadine kuld. Plaatina on haruldane väärismetall. Praegu ongi plaatina ehtemetallina kõige otsitum hinnaliste vääriskivide (peamiselt briljantide) raamimisel (peamiselt oma tugevuse ja vastupidavuse pärast). Juveelitööstus kulutab 40% maailma plaatinatoodangust. Ühe grammi plaatina saamiseks tuleb mõnigi kord töödelda vagunitäis maaki. Õige oli käibeväljend: üks gramm toodangut – üks aasta tööd.
Hõbe Hõbe (Ag) paikneb perioodilisussüsteemis 1B rühmas, 5 perioodis. aatommass tuumalaeng järjenumber elektrone prootoneid neutroneid 108 amü +47 47 47 47 41 Hõbeda oksüdatsiooniaste on +2. Füüsikalised omadused: Hõbe on hõbvalge värvusega, plasitiline, kege ja hästi sepitstav väärismetall. Ta on parim soojus-ja elektrijuht. Hõbedat iseloomustab ka erakordne peegeldusvõime. Tihedus on 10,5 g/cm³ ning sulamistemperatuur 960°C. Keemilised omadused Hõbe on passiivne metall. Ta ei reageeri veega ega puhta õhuga ning ei tõrju happest välja vesinikku. Hõbe reageerib: · konsentreeritud lämmastikhappega 3Ag + 4HNO3 = 3AgNO3 + NO2 + H2O · kontsentreeritud väävelhappega 2Ag + 2H2SO4 = Ag2SO4 + SO2 + H2O
Hõbe Janno Puusepp Hõbe, Ag, (ladina keeles argentum), keemiliste elementide perioodilisussüsteemi I rühma element, väärismetall; järjenumber 47. Hõbe on hästi sepistatav metall. Ta kuulub väärismetallide hulka. Arvatavasti seepärast kuulub hõbe elementide hulka, mida inimkond tundma õppis. Vanimad, Indiast leitud hõbeehted ja nõud pärinevad IVIII aastatuhandest enne meie ajaarvamist. Hõbedat kasutati vanasti ka joodisena ning temast tehti peegleid. Ajalugu Hõbe on üks vanemaid inimese kasutatavaid metalle, tal oli ja on suur tähtsus. Hõbe on olnud maksevahendiks. Tänapäeval kasutatakse hõbedat moodsas tehnoloogias. Hõbe oli populaarne Pärsias, vanad hõbekaevandused olid Kreekas ja Hispaanias. Hõbedat kaevandasid ka foniiklased, kartaagolased ja hiljem vanad roomlased. Kaevandused olid ka Kesk Euroopas ja LõunaAmeerikas. Hõbedale omistat...
kasutust tema kõvadus ja kõrge sulamistemperatuur. Seda ei olnud lihtne olemasolevate tavaliste tehnikatega töödelda. Enne Teist maailmasõda kulus umbes pool plaatinatoodangust eheteks, nüüd läheb aga 90% toodangust tehniliste vajaduste rahuldamiseks. 19. sajandi viimasel poolel ja 20. sajandi esimesel poolel oli plaatina metall, millest valmistati eriti olulised ehted. Plaatina võlu peitub ta välimuses. Tema välge sära on ainulaadne. Ta on ka kõige kõvem ehetes kasutatav väärismetall ning kaks korda raskem kui 14-karaadine kuld. Plaatina populaarsus on viimastel aastatel kasvanud ning seda kasutatakse kulla asemel kihlasõrmuste valmistamisel, sest selle külm läige toob briljandi ilu kullast paremini esile. Kõige populaarsemad on plaatinast ehted hetkel Jaapanis. Anekdoodid Uusrikas tuleb hambaarsti juurde, avab suu, seal on kunsthambaid kullast, plaatinast, briljantidest. Plommid on safiiridest. "Teil on kõik korras," lausub arst, "mis teil veel vaja on?"
Mis on Kuld? Sünteetilised kulla kristallid. Kuld on keemiline element järjenumbriga 79. Kullal on üks staabiilne isotoop massiarvuga 197. Keemilistelt omadustelt on kuld väheaktiivne metall. Ei reageeri vee ega hapetega. Kuld on väärismetall. Normaaltingimustel on ta võrdlemisi pehme kollane metall, mille tihedus on 19,7 g/cm³. Kulla sulamistemperatu 79 Au 1 196,967 18 32 18 8 Kuld 2 Kuld mineraalina Kuld on isotroopne kuubilise süngoonia mineraal. Polarisatsioonimikroskoobis on ta maakmineraalile tüüpilisena läbipaistmatu. Lõhenevus ja magnetilisus puuduvad. Kullal on metalliläige. Maailma suurimad kullavarud asuvad Lõuna-Aafrika Vabariigis.
Plaatina domineeris ehtemaailmas kuni Art Deco perioodini ning tema tähelend lõppes Teise maailmasõjaga, mil ta kuulutati strateegiliseks metalliks ja selle mittesõjaline kasutus keelati. Keeld seostus plaatina ulatusliku kasutusega tööstuses. Plaatina on oluline tooraine autotööstuses, elektroonikas, naftakeemias, aga ka meditsiinis. Iga auto katalüsaator sisaldab plaatinat. Plaatina võlu peitub ta välimuses. Tema välge sära on ainulaadne. Ta on ka kõige kõvem ehetes kasutatav väärismetall ning kaks korda raskem kui 14-karaadine kuld. Plaatina on haruldane väärismetall. Praegu ongi plaatina ehtemetallina kõige otsitum hinnaliste vääriskivide (peamiselt briljantide) raamimisel (peamiselt oma tugevuse ja vastupidavuse pärast). Juveelitööstus kulutab 40% maailma plaatinatoodangust. Ühe grammi plaatina saamiseks tuleb mõnigi kord töödelda vagunitäis maaki. Õige oli käibeväljend: üks gramm toodangut üks aasta tööd.
Tüüpilised oksüdatsiooniastmed on tal 0, +1, +2, +4 ja harvadel juhtudel ka +6. Kuigi plaatinametallina Pallaadium väga hapetega ei reageeri, on ta plaatinametallidest hapetega kõige reageerivam metall. Kasutusvaldkonnad Enamasti kasutatakse pallaadiumi autotööstuses koatalüsaatorina heitgaaside puhastamiseks. Kunagi kasutati pallaadiumkloriidi ka tuberkuloosiravimina ent vahetati paremate rohtude vastu välja. Pallaadiumit kasutatakse ka ehtetööstuses kuna ta on väärismetall. Pallaadiumi kasutatakse ehtetööstuses sellepärast et tal on loomulik valge läige erinevalt teistest valgetest väärismetallidest millel seda ei ole ning seetõttu puudub ka vajadus seda metalli plaatida mõne teise valgeläikelise metalliga. Plaatina ei tekita ka niipalju allergilisi reaktsioone kui teised ehtemetallid. Pallaadiumi kasutatakse veel ka elektroonikas keraamiliste kondensaatorite elektroodide valmistamisel ja erinevate joodiste koostises. Pallaadium imab
KULD Rahumäe Põhikool. Kelly Värva 8b 22.02.2012 Sisukord: *Kuld *Kulla ajalugu *Kulla kasutusalad KULD Kulla keemilise elemendi järjenumbriks on 79 ning nimetuseks on Au. Tema massiarvuks on ümardatult 197. Keemilistelt omadustelt on kuld vähenegatiivne väärismetall ning ei reageeri vee ja hapetega. Normaaltingimustel on ta võrdlemisi pehme kollane metall, mille sulamistemperatuur on 1064 kraadi. KULLA AJALUGU Kuld oli juba iidsetest aegadest alates tuntud hiinlastele, hindudele ja teistele Aasia rahvastele.Kuld oli hästi tuntud ka muistse Mehhiko elanikel-asteekidele.Puhtast kullast valmistatud kettad olid selle rahva mõnedel suguharudel Päikese sümboliks,mida nad kummardasid. Kulla hinnalisus ja kultuuri ajaloo hilisematel etappidel püüe rikastuda viidi selleni, et hakati ostma meetodeid kulla võltsimiseks.Mõned nendest meeto...
TOLLIMAKS Mis on tollimaks? • Maks, mis lisatakse imporditavatele kaupadele • Sissetoodava kauba koguste piiramine ning eksporditava kauba koguste suurendamine, mõjutades nii nende konkurentsivõimet • Ühekordne, deklareeritav ja määratav maks • Tollimaksumäär on üldjuhul 017% • Tollimaksu suurus sõltub kauba liigist, päritoluriigist ja ka kogusest Mis on tollimaks? • Lisandub ka käibemaks ning aktsiis (alkohol, tubakas, mootorikütus) • 1. mai 2014 • Tollitariifistik TARIC Eesti Tollitariifistik Mida peab arvestama? • Tollimaks lisandub importimisel riikidest, mis ei kuulu Euroopa Liitu • Euroopa Liidu sees tollimakse ei ole ning tollideklaratsiooni ei ole vaja esitada • Käibemaksu tasutakse ka transpordikulult. Mida peab arvestama? • Kui saadetakse midagi kolmanda riigi füüsiliselt isikult füüsilisele isikule mittekaubanduslikul eesmärgil, siis ...
Kuld Kuld on üks esimesi metalle, mida inimene tundma õppis. Seda hinnati aastatuhandeid tagasi. Vanimad kuldesemed pärinevad viiendast aastatuhandest . Vanas Egiptuses kasutati seda metalli ehete, müntide jms valmistamiseks. Kuna kuld on kallis väärismetall, siis seda said lubada endale ainult rikkad valitsejad ehk vaaraod. Peale nende surma balasameeriti neid, nende näole asetati kullast maske ja ka sarkofaagid kaunistati kullast nikerdustega. Kuld on keemiliselt passiivne, ta reageerib ainult väga väheste ainete segudega (nt. kuningveega, mis on lämmastik- ja kloriidhappe segu). Kulla tähiseks on Au, mis tuleb ladinakeelest sõnast aurum. Kuld on kollane, ilus, väga pehme ja plastne raskemetall, mis juhib hästi soojust ja elektrit.
Aurum). Kulda peetakse päikese metalliks. Seda arvatavasti värvuse pärast. Samas ka võimsuse pärast - päike on ju ikkagi võimsaim taevakeha. Samuti on kuld metallide hulgas võimsaim. Omadused Kuld on I perioodi element, mille järjenumber on 79 ja aatommass on 196,9665. Normaaltingimustel on ta võrdlemisi pehme helekollane läikiv metall, mille tihedus on 19,32 g/cm3 ja kõvadus 2,5-3. Lõhenevus ja magnetilisus kullal puuduvad. Ning ta on kõige vormitavam ning plastilisem väärismetall (1g kulda saab venitada traadiks, mille pikkus on 3km). Kulla sulamistemperatuur on 1064,18 °C. Kuld on ka hea elektrijuht ning keemiliselt inertne - viimane väide, aga lakkab olemast õige, kui tegemist on väga väikeste kullaosakestega. Keemilistelt omadustelt on kuld väheaktiivne metall. Kulda nimetatakse metallide kuningaks. Seda seepärast et kuld ei reageeri vee ega hapetega. On olemas vaid üks eriline hapete segu - kuningvesi
KULD (AU) Kuld on tihe, plastne, läikiv ja pehme väärismetall see on nii keemiline element kui ka lihtaine, mis esineb looduses mineraalina. Kulla keemilise elemendisümbol on Au ja aatomnumber 79. Puhas kuld ei oksüdeeru hapnikus ega vees, tänu sellele säilib kulla kollane värvus ja läige. Keemiliselt on kuld 11. (ehk IB) rühma 6. perioodi d bloki element. Normaaltingimustes on kuld üks inertsemaid elemente. Seetõttu esineb kulda tihti puhtal kujul kamakatena, teradena kivides, kulla veenides või jõesettes. Harvem leidub kulda ka ühendites, näiteks telluuriga. KEEMILISED OMADUSED Kuld ei korrodeeru ja sära ei tuhmu ,tänu keemilisele toimele on kuld püsiv, seepärast nimetasid vanaaja õpetlased ja alkeemikud kulda metallide kuningaks. Seetõttu on ka kuld väga sobiv materjal valuuta ja ehete tegemiseks ja teiste reageerivamate metallide...
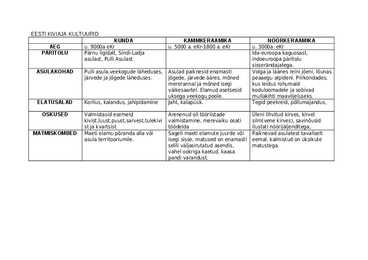
Põhja- skandinaavia eesti mõjud-lihula, martna,kullamaa ELATUSALAD Põllumajandus ja põllumajandus Põlluharimine, põlluharimine Kaubandus, karjakasvatus, karjakasvatus, väärismetall, maaviljelus, käsitöö. TEGEVUSALAD/ Ehted,savinõud, Soorauamaak, Raudesemete Keltide põllud, Linnuste rajamine. OSKUSED kaheväljapõllusüste valmistamine, künnipõllud, Rüüsteretked em, sulatati rauda kvaliteetsed kirved kaheväljasüsteem. meredel,
Riituse liigid religioonifenomenoloogias: Tõrjeriitus kurjade vaimude peletamiseks Väljaajamisriitus (eksortsism eks+ horkizein) seestumus Siirderiitused (initsiatsioon) Kalendririitused Kultus (ld cultus – harimine) – toimingute ehk riituste sooritamine talitustega - austamine - kummardamine - teenimine Ohver (ld offere – annetama) Jaotus tekke alusel: Esimese astme ohver: inimohver Teise astme ohver (asendusohver) (Loom, taim, vääriskivi, väärismetall jne) Kolmanda astme ohver – sümbolohver (Lõhnaaine, lilled, toiduained jne) Neljanda astme ohver - raha Viies - sümboli sümbol ohvriraha - hiinlased) Jaotus liigituse alusel: Anniohver - (ld do ut des - annan, et sa annaksid) Lepitusohver (nt patuoinas) Kommuniooniohver ehk ühendusohver (nt Püha Õhtusöömaaeg) 7. Pühad isikud Šamaan (evengi k – teadja) loodusrahvaste vahendaja siin- ja sealpoolsuse vahel (ld) Pontifex Maximus - Suurim Sillaehitaja, rooma
vähenes, kui on leitud möned rohkete höbeesemete ja relvadega matmispaigad.Hakkasid levima Iiivast kuhjatud kääpad(kääpad sarnanevad kohati kivikalmetega), mille all või sees olid põletusmatused. Aarded ja ohvriannid Keskmisest rauaajast tuntakse nii ehete aardeleide kui ka relvade Vöi tööriistade peitleide. Pronksi kõrval maeti maha ka hõbeaardeid ning esines ka kullatud ja kullast esemeid, mida leiti enamasti põllumaadelt ning kalmetest. Arvatakse, et väärismetall maeti maha sòjaohu korral ning vahel ka ohverdamisel, sest arvati et omanik saab neid kasutada ka surmajärgses elus. Palju on leitud ka odaotsi, mõõga fragmente, võitlusnuge ning tööriistu. Rahutud ajad Linnuste rajamineja relvade arvukus kõneleb rahututest aegadest. Ühelt poolt võisid need olla kohalike ülikute võimuvõitlused. Tollel ajal olid linnused ülikute residentsid ning linnuste kõrval paiknevatesse asulatsesse olid kogunenud käsitöölised. Teiselt
Seotava kaelaräti asemele tuli kitsas lips, milleks kasutati värvilisi materjale. Mehe tualeti juurde kuulusid ehetena ainult lipsunõel, mansetinööbid ja taskukell, mille kett rippus risti üle vesti. Tänavariietuseks olid palitu ja silinderkübar. Naiste rõivad muutusid uuesti toredamaks. Lai krinoliin, mida hakati kandma 19. sajandi 20. aastatel, paisus veelgi kaharamaks. Peokleidid olid avara dekolteega, päevakleidid aga kinnise kaelusega. Palju kanti ehteid, sest väärismetall ja kalliskivid muutusid üheks kapitali paigutamise viisiks. Mood hakkas kiiremini vahelduma. Seda dikteerisid suured moemajad, mille hulgas said juhtivaks Pariisi moekunstnikud ja firmad. REALISTLIK MAALIKUNST Raskem oli JEAN FRANCOIS MILLET [zan fransuaa millee] (1814-1875) saatus. Ka tema asus 1849 aastal Barbizoni, kuid kujutas eelkõige talupoegi, mitte maastikke. Tema kuulsaim töö on "Õhtupalve". Inimeste kujutamises valitsesid aga klassitsismi ajast kindlad skeemi reeglid, mida
õhu käes oksüdeerub ning tuhmistub Reageerimine hapnikuga tº 4Al + 3O2 > 2Al2O3 Reageerimine teiste mittemetallidega tº 2Al + 3Cl2 > AlCl3 tº 2Al + 3S > Al2S3 tº 2Al + N2 > 2AlN Reageerimine sooladega 2Al + 3CuCl2 > 2AlCl3 + 3Cu ALUMINIUMI JA TEMA ÜHENDITE KASUTUSALAD Vanasti oli alumiinium väärismetall, kuna teda osati toota vähe. Seepärast kuni 19. sajandi lõpuni kasutati tänu hõbedale Sarnasusele alumiiniumit erinevate ehete valmistamiseks. Tänapäeval leiab alumiinium rakendust ohtralt igapäevaelus: · hea elekri ja soojusjuhtivuse tõttu elektrijuhtmetes · hea peegeldumisvõime tõttu peeglites ja reflektorites · alumiiniumpulbrit kasutatakse hõbevärvi pigmendina · toiduvalmistamisel kasutatakse palju alumiiniumnõusid
Võru Tarbijate Ühistu Essee Ettevõtte üldine iseloomustus: Nimetus: Võru Tarbijate Ühistu Õigusnorm: Eraõigus Asukoht: Peakontor, Lembitu 1 Kontaktandmed: VTÜ peakontor 7827600 Töötajate arv: 321 Omanike arv: puuduvad Juhatuse liikmete arv: 1 Peamised tegevusalad: Toidu- ja tööstuskaupade jae- ja hulgimüük, alkohol, Väärismetall ja kivid, toitlustus- ja vabaaja teenus, kaubanduslik vahendaja, toodete müük, transport teenused Eesti Vabariigi piires välja arvatud litsentseeritud tegevusalad.1 Missioon Ühistu eesmärgid on liikmete ühise majandustegevuse kaudu toetada ja soodustada oma liikmete majanduslike huve läbi ühise majandustegevuse milles liikmed osalevad: tarbijate või muude hüvede kasutajatena, hankijatena, tööpanuse kaudu, teenuste kasutamise kaudu või mõnel muul sarnasel viisil. Võru Tarbijate Ühistu alla kuuluvad kõik Võru Maakonnas ja linn...
Argentiina Referaat Koostas: 9c klass 2009 a. Riigiasend Argentiina hõlmab enamiku Lõuna-Ameerika lõunaosast, laiudes 3460 km pikkuselt Boliiviast Hoorni neemeni. Ta piirneb Uruguay, Brasiilia, Paraguay,Boliivia ja Tsiiliga.Riigi lääneosas paiknev põhja-lõuna-shiline Andide mäestik moodustab Argentiina ja Tsiili loodusliku piiri.Mäestikust idas laiub maa keskosas viljakas pampa. Argentina on jaotatud 23 provintsiks (provincias; ainsuses: provincia), ja 1 autonoomseks linnaks. Pindala Argentina pindala on 2 766 890 km², sealhulgas vett 1,1%. Ta on maailma riikide seas pindalalt 8. kohal.Argentina pretendeerib lisaks veel 1 000 000 km² alale Antarktikas ja Falklandi saartele. Kliima Riigi kirdeosa asub lähistroopikas.Andide põhjaosa on poolkõrbeline, lõunaosas katab mägesid lumi.Lääneosas laiuvad kõrbelised tasandikud,pampa k...
Vase alarühma metallid pingereas vesinikust paremal – ei tõrju hapetest välja vesinikku. Oksüdeerivate hapetega reageerivad Cu ja Ag, kuld lahustub vaid kuningvees. Vase reageerimisel lahjendatud lämmastikhape-ga eraldub NO, kontsentreeritud happega NO2. Kontsentreeritud väävelhappega tekib SO2. Leelistega ei reageeri. Vasesoolade lahustel on sinine värvus. Hõbe on keemiline element järjenumbriga 47, metall. Stabiilseid isotoope kaks, nende massiarvud on 107 ja 109. Hõbe on väärismetall. Tihedus on 10,5 g/cm³. Hõbe sulab temperatuuril 960°C. Hõbedat leidub ehedalt ja ühenditena (AgCl, Ag 2S), lisanditena plii- ja vasemaakides. Hõbe valge, pehme, plastne metall, hea peegeldusvõimega, parim soojus- ja elektrijuht. Antibakteriaalse toimega. Nii hõbedat kui kulda saadakse maagist tsüaniidmeetodil. Suurimad hõbedakaevandused asuvad Mehhikos, Canningtonis (Austraalias), Dukatis (Venemaal), Peruus ja Alaskal.
Kaitseautomaat Rikkevoolukaitselüliti Liigkoormuskaitse Lühiskaitseseade Termokaitse Kaitsereleed 5. Lisa puuduvad sõnad. Rikkevoolukaitselüliti neutraaljuhi kontakt avaneb tavaliselt viimasene aga sulgub sisselülitamisel esimesena. 6. Hõbe kontaktmaterjali omadused? Plussid Hea elektri- ja soojusjuht Väike kontakttakistus Väikeste voolude puhul kulumiskindel. Odavaim väärismetall kontaktide jaoks Miinused Tundlik väävli suhtes Väike kaarekindlus Saab kasutada väikeste voolude puhul (Kuni 20 amprit) 7. Magnet pehme terase omadused ja kasutusala? Pehmed magnetmaterjalid (raud, pehme teras). Nende materjalidega on võimalik saada suurt magnetvoo tihedust suhteliselt väikese magnetvälja tugevuse juures, kuid seejuures magneetuvad nad kergesti lahti. Pehmeid
Vase alarühma metallid pingereas vesinikust paremal ei tõrju hapetest välja vesinikku. Oksüdeerivate hapetega reageerivad Cu ja Ag, kuld lahustub vaid kuningvees. Vase reageerimisel lahjendatud lämmastikhape-ga eraldub NO, kontsentreeritud happega NO2. Kontsentreeritud väävelhappega tekib SO2. Leelistega ei reageeri. Vasesoolade lahustel on sinine värvus. Hõbe on keemiline element järjenumbriga 47, metall. Stabiilseid isotoope kaks, nende massiarvud on 107 ja 109. Hõbe on väärismetall. Tihedus on 10,5 g/cm³. Hõbe sulab temperatuuril 960°C. Hõbedat leidub ehedalt ja ühenditena (AgCl, Ag2S), lisanditena plii- ja vasemaakides. Hõbe valge, pehme, plastne metall, hea peegeldusvõimega, parim soojus- ja elektrijuht. Antibakteriaalse toimega. Nii hõbedat kui kulda saadakse maagist tsüaniidmeetodil. Suurimad hõbedakaevandused asuvad Mehhikos, Canningtonis (Austraalias), Dukatis (Venemaal), Peruus ja Alaskal.