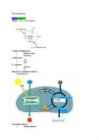
glükogeeni kujul *Palju energiat saadakse 1 glükoosi molekuli täielikul lagundamisel? - Kuni 38 ATP molekuli *Millised etapid on eristatavad glükoosi lagundamisel? - Glükolüüsi , tsitraaditsükli ja hingamisahela reaktsioon *Kus toimub glükolüüs? - Päristuumsete rakkude tsütoplasmavõrgustikus *Mille poolest erineb aeroobne glükolüüs anaeroobsest glükolüüsist? - Aeroobne toimub vaid siis kui on hapnikku, anaeroobne toimub hapniku puudumisel *Mis on käärimise lähteained ja lõpp-produktid? - Lähteaine: glükoos. Lõpp-produktid: piimhape või etanool *Mitu ATP-d moodustub käärimisel? - 2 ATP *Mis on glükolüüsi lähteained ja lõpp-produktid? - lähteained: Glükoos, ensüümid ja hapnik, millest moodustub 2 püroviinamarihapet (CH3COCOOH) ja 4H aatomit. *Mitu ATP-d saadakse glükolüüsil? - 2 ATP-d *Kus toimub tsitraaditsükkel? - toimub mitokondri sisemuses. *Mis on tsitraaditsükli lähteained ja lõpp-produktid
Palju energiat saadakse 1 glükoosi molekuli täielikul lagundamisel?Kuni 38 ATP molekuli Millised etapid on eristatavad glükoosi lagundamisel?Glükolüüsi, tsitraaditsükli ja hingamisahela reaktsioon Kus rakus toimub glükolüüs?Päristuumsete rakkude tsütoplasmavõrgustikus Mille poolest erineb aeroobne glükolüüs anaeroobsest glükolüüsist?Aeroobne toimub vaid siis kui on hapnikku, anaeroobne toimub hapniku puudumisel Mis on käärimise lähteained ja lõpp-produktid?Lähteaine: glükoos. Lõpp-produktid: piimhape või etanool. Mitu ATP-d moodustub käärimisel?Kaks Miks muutuvad treenimata lihased pärast intensiivset kehalist tööd või treeningut valusaks? Lihastesse kuhjuv piimhape ei ole hapniku puudumisel lihasrakkude poolt enam kasutatav ja põhjustab lihaste väsimust, krampe või valu. Selleks, et lihasrakud vabaneksid piimhappest ja lihaste töövõime taastuks, peaks piimhape kanduma verega maksa, kus see muutub
Lk 97- Fotosüntees 1. Nimetage fotosünteesi lähteained ja lõpp-produktid. Lähteained on süsihappegaas ja vesi ( valgusenergia samuti aga seda ei loeta aineks vaid teguriks) ja saaduseks on glükoos, hapnik ja vesi. Võrrand: 6CO2+12H2O= C6H12O6+6O2+6H2O 2. Miks jagatakse fotosüntees valgus- ja pimedusstaadiumiks? Sellepärast et valgusstaadiumi protsessiks on vaja valgusenergiat aga pimedusstaadiumis seda pole vaja. 3. Kuidas kasutatakse fotosünteesi käigus valgusenergiat? Fotosüsteem II toimub vee molekulide lagundamine vee fotooksüdatsioonil ehk vee
CH3CH2CHCH2 CHCH3 CH2CH3 b) OH HOCH2 CHCH3 c) H2N CHCOOH CH3 d) CH3 HOCH2 CCH3 CH3 e) CH3CH2 CHCH3 CI 2. Nimetage see ühend, leia kiraalne tsenter, esitada stereoisomeerid ja määra, kumb neist on S ka kumb R isomeer (5p). CH3CH(OH)CH2CH2OH 3. Nimeta see aine . Kirjuta tema saamise bruttovõrrand, nimeta lähteained, määra reaktsiooni tüüp, leia ja tähista lähteainete reaktsioonitsentrid.( 5p) CH3 H3C CCH2OCH3 CH3 4. Leia ja tähista (+ ja ) reaktsioonitsentrid järgmistes ühendites. Nimeta need ühendid.5p (Nimetatud on need ja reaktsioonitsentrid on ka määratud) CH3 H3C CCH2NH2 CH3 O CH2CH2CH O H3C CNH2 O H2C COH H Br CCH2CH3 CH3 5
Glükoosi lagundamise etapid: 1. Glükolüüs - toimub päristuumse raku tsütoplasmavõrgustikul. 2. Tsitraaditsükkel - toimub mitokondri sisemuses. 3. Hingamisahela reaktsioonid - toimuvad mitokondri harjakeste membraanidel. 31) Mille poolest erineb aeroobne glükolüüs anaeroobsest glükolüüsist? · Aeroobne Hapnikku on piisavalt; rakuhingamine. · Anaeroobne Hapnikku ei jätku; käärimine. 32) Milised on erinevad käärimise lähteained ja lõpp-produktid? · Piimhappekäärimine lähteaine on glükoos. Tekib: piimhape · Alkohol e. etanoolkäärimine lähteaine glükoos. Tekib: CO2 ja etanool. 33) Kuidas organism vabaneb tekkinud piimhappest? Lihastes moodustunud piimhape kandub verega maksa ja lagundatakse seal püroviinamarihappeks, mis liigub edasi tsitraaditsüklisse. Lihaste töövõime taastub. 34) Kirjelda erinevaid ATP saamise viise füüsilisel pingutusel.
organismide elutegevuse käigus tekkinud orgaanilisi ühendeid. EELISED PUUDUSED Saavad kogu energia suunata kasvamisse Sõltuvad otseselt teistest organismidest. ja arenemisse. Saavad energia valgusest - bakterid Saavad energia keemilistest reaktsioonidest - loomad, seened, bakterid Rakuhingamine (millisteks protsessideks jaguneb, millised on lähteained ja saadused (sh ATP hulk), kus rakus toimuvad?) Rakuhingamine on glükoosi lõplik lagundamine hapniku abil, mille tulemusena vabanev energia salvestatakse (ATP), eraldub süsinikdioksiid ja vesi. 6O2 + C6H12O6 = 6CO2 + 6H2O ETAPID 1. Glükolüüs 2. Tsentraaditsükkel 3. Hingamisahela reaktsioonid Lähteained Glükoos C6H12O6 Püruvaat Hapnik O2
· Reageerivad sooladega = uus sool ja uus hape Reaktsioon toimub siis, kui tekib nõrgem hape või sade Kui tekib H2CO3, siis tekkemomendil laguneb ta veeks ja süsinikdioksiidiks · Lagunemine kuumutamisel = happeline oksiid ja vesi Lagunevad ainult hapnikhapped Aluste (hüdroksiidide) keemilised omadused · reageerivad hapetega = sool ja vesi · reageerivad happeliste oksiididega = sool ja vesi · reageerivad sooladega = hüdroksiid ja sool lähteained peavad olema lahustuvad ja saaduses peab tekkima sade · lagunevad kuumutamisel = aluseline oksiid ja vesi ei lagune IA rühma metallide hüdroksiidid soolade keemilised omadused · reageerivad metallidega = sool ja metall metall reageerib vees lahustuva soolaga, kui ta on aktiivsem kui soola koostises olev metall · reageerivad hapetega = sool ja hape reaktsioon toimub siis, kui tekib nõrgem hape või sade · reageerivad alustega = alus ja sool
Katabolism(lagundamine), anabolism(süntees) 8.Kuidas säilitavad organismid oma glükoosivarusid? Organismid säilitavad oma glükoosi varud kas glükogeeni(loomad) või tärklisena(taimed). 9.Palju energiat saadakse 1 glükoosi molekuli täielikul lagundamisel? 38 ATP 10.Millised etapid on eristatavad glükoosi lagundamisel? Glükolüüsi , tsitraaditsükli ja hingamisahela reaktsioon 11.Kus toimub glükolüüs? päristuumsete rakkude tsütoplasmavõrgustikus 12.Mis on glükolüüsi lähteained? Glükoos, ensüümid ja hapnik 13.Mis on glükolüüsi saadused? Püroviinamarihaoe, 2ATP, 2 NADH 14.Kuidas kasutatakse ära eraldunud vesiniku aatomid? Seotakse vesinikukandja NAD-iga, kasutatakse hingamisahelas 15.Mitu ATP-d saadakse glükolüüsil? 2 16.Kus toimub tsitraaditsükkel? Mitokondri maatriksis 17.Mis on tsitraaditsükli lähteained? Apüroviinamarihape, hapnik 18.Mis on tsitraaditsükli produktid? CO2 ja 10NADH2. 19.Mis saab edasi tsitraaditsükli produktidest?
6.Nimeta protsesse, millega kaasneb ATP moodustamine. glükolüüs, hingamisahel, 7.Kuidas võib jaotada metabolismi? assimilatsioon, dissimilatsioon 8.Kuidas säilitavad organismid oma glükoosivarusid? fotosünteesiga 9.Palju energiat saadakse 1 glükoosi molekuli täielikul lagundamisel? 30kJ 10.Millised etapid on eristatavad glükoosi lagundamisel? glükolüüs, tsitraaditsükkel ja hingamisahela reaktsioonid 11.Kus toimub glükolüüs? tsütoplasmas 12.Mis on glükolüüsi lähteained? toitained, polüsahhariidid, glükoos 13.Mis on glükolüüsi saadused? 2 püroviinamarihape, 4 vesinikku, 14.Kuidas kasutatakse ära eraldunud vesiniku aatomid? seostatakse vesinikukandja NAD-iga, mis võimaldav vesiniku aatomeid kasutada hingamisahelas 15.Mitu ATP-d saadakse glükolüüsil? 2 16.Kus toimub tsitraaditsükkel? mitokondris 17.Mis on tsitraaditsükli lähteained? püruviinamarihape, CO2 ja 2H (aktiveeritud äädikhape) 18.Mis on tsitraaditsükli produktid
7. Kirjeldage hingamisahela summaarset võrrandit. V: 12NADH2 molekuli reageerib 6O2 molekuliga ja selle tulemusena eraldub 12NAD molekuli, 12H2O molekuli ja 36ATP molekuli. 8. Võrrelge glükolüüsil,tsitraaditsüklis ja hingamisahelas moodustavaid ATP koguseid. V: 2ATP molekuli moodustub glükolüüsil ja ülejäänud 36 moodustuvad hingamisahela reaktsioonides ja kokku võib vabaneda 38ATP molekuli. LK97 1. Nimetage Fotosünteesi lähteained ja lõpp-produkt V: Lähteained on süsihappegaas ja vesi ja saaduseks on glükoos, hapnik ja vesi. 2. Miks jagatakse fotosüntees valgus-ja pimedusstaadiumiks ? V: Sellepärast et valgusstaadiumi protsessiks on vaja valgusenergiat aga pimedusstaadiumis seda pole vaja. 3. Kuidas kasutatakse fotosünteesi käigus valgusenergiat? V: Fotosüsteem II toimub vee molekulide lagundamine vee fotooksüdatsioonil ehk vee fotolüüsil ja ATP sünteeiks. 4
Kus tsütoplasmavõr mitokonder Mitokondri Lihaskoe rakud toimub? gustik sisemembraani harjakestes Mis Glükoosi algne Püroviinamarihappe NADH2 arvel käärimine toimub? lagundamine edasine lagundamine sünteesitakse ATP molekule Lähteained glükoos Püroviinamarihape O2 PVA Lõpp- Püroviinamarih CO2, H 12NADH2, piimhape/etanool produktid ape, H sünteesitakse 36 ATP-d NAD H-aatomid H aatomid liidetakse NADH2 molekulid liidetakse NADH2le. Tekib 10 vabanevad H NADile, NADH2 aatomitest 2NADH2 kasutatakse ära
+ METALL metallid. Erandiks on k. HNO3, lahj. HNO3 ja k. H2SO4 reageerimine metallidega (ei kehti metallide pingerida, ei eraldu H2, tekib sool, oksiid ja H2O). + HAP.OKSIID = SOOL + H2O = UUS ALUS + UUS SOOL + SOOL NB! Reaktsioon toimub siis, kui mõlemad lähteained on vees ALUS lahustuvad ja vähemalt üks saadustest on vees lahustamatu (sade). + HAPE = SOOL + H2O LAGUNEMINE (t) = ALUSELINE OKSIID + H2O = HAPE HAPPELINE + H2O NB! Ei reageeri SiO2 OKSIID + ALUS = SOOL + H2O (mittemetalli
Valkude lühustamine Nukleiinhapete süntees Rasvade lõhustamine DNA süntees Käärimine Vitamiinide süntees (K, D) GLÜKOLÜÜS TSITRAADITSÜKKEL HINGAMISAHELA Toimumise koht Tsütoplasmavõrgustik Mitokondris maatriks Mitokordri harjakesed Lähteained 1 glükoosi molekul 2 püroviinamarihappe 10 NADH2 molekuli ehk püruvaati 2FADH2 6O2 Saadused 2 püroviinamarihapet 8NADH2 10 NAD 2 NADH2 2FADH2 2 FAD 2ATP 2ATP 32-34 ATP
3. Tekib vees lahustumatu aine (sade) ja vastavad ioonid lahkuvad lahusest. 4. Kui vähemalt üks tingimustest pole täidetud - reaktsioon ei kulge. 5. Tekib nõrk elektrolüüt ja enamus tema koostisse kuuluvatest ioonidest lahkub lahusest molekulidena ( vesi, mõni nõrk hape). Kontrolli, kas 1 lähteainetest on hape Jah - kirjuta võrrandi parem pool Ei - Kontrolli, kas mõlemad lähteained lahustuvad vees Ei , vähemalt üks lähteainetest on vees lahustumatu- reaktsioon ei kulge Jah, mõlemad lähteained on vees lahustuvad - Lõpeta reaktsioonivõrrand ja kontrolli, kas .... Reaktsioon kulgeb, sest tekib 1) ...üks saadustest on vesi või mõni nõrk hape: JAH
8.Kuidas säilitavad organismid oma glükoosivarusid? lihastes ja maksas glükogeeni kujul, taimedel tärklise kujul põhiliselt seemnetes ja mugulates. 9.Palju energiat saadakse 1 glükoosi molekuli täielikul lagundamisel? 1140kJ 10.Millised etapid on eristatavad glükoosi lagundamisel? glükolüüs, tsitraaditsükkel, hingamisahela reaktsioonid, 11.Kus toimub glükolüüs? Glükolüüs toimub päristuumsete rakkude tsütoplasmavõrgustikus 12.Mis on glükolüüsi lähteained? Glükoos, ensüümid ja hapnik 13.Mis on glükolüüsi saadused? 2 püroviinamarihapet (CH3COCOOH) ja 4H aatomit 14.Kuidas kasutatakse ära eraldunud vesiniku aatomid? hingamisahela reaktsioonides 15.Mitu ATP-d saadakse glükolüüsil? 2 ATP-d 16.Kus toimub tsitraaditsükkel? - mitokondris 17.Mis on tsitraaditsükli lähteained? - Glükoos 18.Mis on tsitraaditsükli produktid? - Süsihappe gaas (CO2) ja 8NADH2 19.Mis saab edasi tsitraaditsükli produktidest
Samamoodi avaldub ka reaktsioonientalpia ΔHºreaktsioon= - ΔH1º + 3 ΔH2º + 2 ΔH3º = 2220kJ + 3 · (-394kJ) + 2 · (-572 kJ) = - 106kJ. ______________________________________________________________________________________________ tekkeentalpia Hf – soojusefekt 1 mol aine tekkimisel lihtainest nende standardolekus (tekkereaktsioon – aine tekkimine lihtainetest) reaktsiooni soojusefekt: Hreaktsioon = Hf,j (saadused) – Hf,i (lähteained) standardtingimustes püsivatel lihtainetel tekkeentalpia Hf = 0 eksotermilistes reaktsioonides Hf < 0 . mida suurem on eksotermiline efekt, seda stabiilsem aine on. põlemisentalpia Hc – soojusefekt 1 mol aine täielikul põlemisel / oksüdeerumisel reaktsiooni soojusefekt: HreaktsioonHc,i (lähteained)- Hc,j (saadused) kui kahel ainel on sama aatom molekul, siis suurem põlemisentalpia on sellel ainel, millel
Fotosünteesi tähtsus: · Anorgaanilistest ainetest esmase orgaanilise aine tootmine · Glükoos on põhiline energiaallikas enamikus organismides · Toiduahela esimene lüli · Toit heterotroofidele · Hapnik osaleb hingamisel, osooni tekkel, põlemisel · Süsinku- ja hapnikuringes tähtsal kohal · Fossiilsete kütuste teke Valgusstaadium - toimub ainult valgusenergia mõjul kloroplastides. Lähteained: H2O( ja valgusenergia), saadused: O2 (pimedusstaadiumi protsesside jaoks ATP ja NADPH2)Valgusstaadiumis toimub klorofülli ergastamine. Ergastunud energia arvelt lagundatakse vee molekule ja eraldub gaasiline hapnik. (vaheühendid ja salvestatud ATP energiat kasutatakse pimedusstaadiumis) Pimedusstaadium - ei sõltu valgusest, toimub stroomas. Lähteained: CO2 ja valgusstaadiumis tekkinud ATP ja NADPH2. Saadused: tärklis, varuained, aminohapped, lipiidid
Hape + sool = uus sool + uus hape (uus hape peab nõrgem olema või uus sool mittelahustuv) + metall = sool + vesinik (metall peab aktiivsuse reas vesinikust eespool olema, ära vali HNO3) Alused + hape = sool + vesi + happeline oksiid = sool + vesi * Alus + sool = uus alus + uus sool (lähteained peavad vees lahustuma, vähemalt üks saadustest mitte) t° = aluseline oksiid + vesi (lahustub va. NaOH ,KOH ) Soolad +hape = uus hape + uus sool (uus hape peab olema nõrgem või uus sool lahustumatu) +alus = uus sool + uus alus Sool (mõlemad l-a peavad lahustuma ja üks saadus mittelahustuma)
Heptaan C7H16 Oktaan C8H18 Nonaan C9H20 Dekaan C10H22 Undekaan C11H24 Dodekaan C12 H26 Tridekaan C13H28 Tetradekaan C14H30 Pentadekaan C15H32 Reaktsioonivõrrandis Mittemetallioksiidid + Vesi = Hape Sool + Hape = Uus hapse + Uus sool SiO2 (liiv) veega ei reageeri Tekkiv hape peab olema algsest nõrgem Metallioksiidid + Vesi = Alus Sool + Sool = Sool + Sool Ainult IA/IIA metallid Lähteained peavad vees lahustuma. Üks tekkivatest ainetest peab sadestuma Hape + Alus = Sool + Vesi Metall + Hape = Sool + Vesinik (H2 ) Metall pingereas vesinikust eespool Mittemetallioksiid + Alus = Sool + Vesi Metall + Mittemetall = Sool Metallioksiid + Hape = Sool + Vesi IA/Ca alarühma metallid + Vesi = Alus + H2
või uus sool mittelahustuv) + metall = sool + vesinik (metall peab olema pingereas Hst eespool, v.a. HNO3) ALUSTE REAKTSIOONID + hape = sool + vesi ALUS + happeline oksiid = sool + vesi + sool = uus alus + uus sool (lähteained peavad vees lahustuma ja üks saadus mitte) + laguneb temp. = aluseline oksiid + vesi (v.a. NaOH, KOH) SOOLADE REAKTSIOONID + hape = uus hape + uus sool (uus hape peab olema nõrgem SOOL või uus sool mittelahustuv) + alus = uus alus + uus sool (lähteained peavad vees lahustuma
kulgevad ühes suunas lõpuni. 5. Mis on keemiline tasakaal? · Pöörduva reaktsiooni olek, mille korral päri ja vastassuunaliste reaktsioonide kiirus on võrdsed. 6. Kuidas on võimalik nihutada keemilist tasakaalu: · Kontsentratsiooni abil · Rõhu abil · Temperatuuri abil 7. Mis on eksotermiline ja endotermiline reaktsioon? Kuidas neid määrata reaktsioonide ja soojusefekti järgi? · Eksotermiline lähteained energia eraldub saadused. Ühinemisreaktsioon. (delta H väiksem kui 0 ) · Endotermiline lähteained energia neeldub saadused. Lagunemisreaktsioon. (delta H suurem kui 0 ) 8. Küsimused 1 7 õpikust lk 22 + riigieksamite ülesanded.
Molekulaargeneetika- Teadusharu, mis uurib pärilikkuse seaduspärasusi molekulaarsel tasandil. Pärilikkus- eluslooduse üldine seaduspärasus, mille kohaselt järglased sarnanevad ehituselt ja talitluselt vanematega. 2. Geenist saab tunnus : DNA - > mRNA - > valk. 3. Transkriptsioon ehk RNA süntees. Toimub rakutuumas interfaasi ajal. Ühe DNA lõigu järgi moodustatakse RNA. Tekivad mRNA, tRNA, rRNA. Lähteained on RNA polümeraas, mis keerab lahti ja sünteesib. 4. Translatsioon ehk valgu süntees. Toimub ribosoomides. Lähteained : aminohapped, tRNA molekule, ensüümid ja energiaallikatena ATP-d ja GTP-d. Tekib : valk. 5. Geneetiline kood mRNA molekuli kolme järjestikkuse nukleotiidi vastavus ühele aminohappejäägile valgu molekulis. Koodon mRNA molekuli kolm järjestikkust nukleotiidi.
V:A: FOTOSÜNTEESIJAD( rohelised taimed ja vetikad) H: LOOMAD, SEENED, PROTISTID ja VALDAV OSA BAKTERITEST. 2) Dissimilatsioonijärgud glükoosi täielikul lõhustumisel (aeroobsel glükolüüsil) V: 1) Glükolüüsi reaktsioon 2) Tsitraaditsükli reaktsioon 3) Hingamisahela reaktsioon 3) Piimhappelise käärimise ja etanoolkäärimise saadused Piimhappe: hapupiim, hapukoor, jogurt, keefir, kohupiim,juustud. Etanoolkäärimine: etanool ehk viinapiiritus 4) Rakuhingamise lähteained ja saadused Lähteained: glükoos ja hapnik Saadused: süsihappegaas ja vesi 5) Fotosünteesi lähteained ja saadused Lähteained: süsihappegaas ja vesi Saadused: Glükoos ja hapnik 4.SELGITA 1) Millisel viisil saab ja kasutab energiat autotroofne organism? Heterotroofne organism? V: Organismid kasutavad energiat elutegevuseks ja kudede uuendamiseks. 2) Milline seos on organismides toimuval dissmilatsioonil ja assimilatsioonil? V: 1. seotud ainete kaudu: AS tekivad org
Eraldunud H seotakse hapnikuga ja tekib H2O. vabaneva energia arvel saab 12NADH2 molekuli kohta sünteesida 36ATP molekuli, glükoosimolekuli lõhustamisel saadakse 2ATP molekuli siis lõplikul lagundamisel saab moodustada kuni 38ATP molekuli. 8. Võrrelge glükolüüsil, tsitraaditsüklis ja hingamisahelas moodustuvaid ATP koguseid. Glükolüüsil 2ATP, tsitraaditsüklis 0, Hingamisahelas 36+2ATP FOTOSÜNTEES 1. Nimetage fotosünteesi lähteained ja lõpp-produktid. valgusenergia, CO2, H2O - O2, glükoos 2. Miks jagatakse fotosüntees valgus- ja pimedusstaadiumiks? 3. Kuidas kasutatakse fotosünteesi käigus valgusenergiat? Valgusenergia ergastab klorofülli elektrone selle energia arvel lagundatakse vee molekule ja eraldub gaasiline hapnik. 4. Mis on valgusstaadiumi lähteained ja lõpp-produktid? Lähteained - valgusenergia,H2O Lõpp-produktid - ATP, HADPH2, O2 5
1. Reageerimine metalliga uus sool + uus metall (metall reageerib ves lahustuva soolaga, kui ta on aktiivsem kui soola koostises olev metall) Fe + CuSO4 FeSO4 + Cu 2. Reageerimine hapetega uus sool + uus hape (toimub vaid siis, kui tekib nõrgem hape) Na2S + H2SO4 Na2SO4 + H2S (kui tekib H2CO3, siis ta laguneb tekkemomendil veeks ja süsinikdioksiidik CaCO3 + 2HCl CaCl2 + H2O + CO2) 3. Reageerimine alustega uus alus + uus sool (lähteained peavad olema vees lahustuvad ja saadustest üks lahustumatu) CuCl2 +2NaOH Cu(OH)2 + 2NaCl 4. Reageerimine sooladega uus sool + uus sool (lähteained peavad olema vees lahustuvad ja saadustest üks lahustumatu) NaCl + AgNO3 AgCl + NaNO3 Soolade saamine 1. hape + metall sool + H2 2. hape + aluseline oksiid sool + H2O 3. hape + alus sool + H2O 4. hape + sool sool + hape 5. alus + happeline oksiid sool + H2O 6. alus + sool sool + alus 7
bakterirakul tsütoplasmat. 5. Mis toimub valgus-, mis pimedusstaadiumis? Kus toimuvad? Kuidas valgus- ja pimedusstaadium omavahel seotud on? NADP? FS üldvõrrand. Valgusstaadiumil vajab energiat, toimub kloroplasti tülakoidi membraanis. Valgus ergastab pigmendi molekulid ja neist eralduvat elektronid. Jääkproduktiks O2. 6CO2+12H2O = C6H12O6 + 6O2 + 6H2O Pimedusstaadiumil ei vaja valgust, toimub kloroplasti stroomas. Tsükliline Calvini protsess. Lähteained CO2 ja NADPH-ga kohale toodud H+. Tulemuseks glükoos. 6. FS tähtsus? FS-i mõjutavad tegurid. Anorgaanilistest ainetest esmase orgaanilise aine loomine. Glükoos põhiline energiaallikas. Toiduahela esimene lüli. Lähteaine teiste orgaaniliste ainete sünteesis. Hapnik osaleb hingamisel, osooni tekkel, põlemisel. Süsiniku-ja hapnikuringes tähtsal kohal. Fossiilsete kütuste teke (nafta, kivisüsi, maagaas).
väliskeskkonnaga ja mis võimaldab tal kasvada ja areneda (kõik protsessid). ASSIMILATSIOON- millegi süntees, kus lihtainetest moodustatakse keerulisi ühendeid (süsivesikud ja valgud). Assim. vajab ENERGIAT! DISSIMILATSIOON - millegi lagundamine, kus keerulisted ained muutuvad uuesti lihtaineteks (CO2, H2O jt) . ENERGIA vabaneb! GLÜKOOSI LAGUNDAMINE C6H12O6 + O2 = CO2 + H2O - toimub mitokonderi sees glükoosi lagundamine toimub eri etappides lähteained saadused ATP koht 1). glükolüüs glükoos püroviinamatihape 2 ATP tsütoplasma võrgustik 2). tsitraadi püroviinamarihape CO2 -------- mitokonder tsükkel 3). O2 ja 2 NAD H2O 36 ATP mitokonder hingamisahela reaktsioon
Orgaanilised komposiitmaterjalid Töö pealkiri: Kihiliste plastide valmistamine resoolvaikude baasil Õpperühm: Töö teostaja: KAOB21 Gertrud Arro Õppejõud: Töö Protokoll Protokoll teostatud esitatud: arvestatu Tiia-Maaja Süld : d: Fenoolaldehüüdvaigu saamine ja omadused 1. Resoolvaigu süntees Lähteained: fenool 28,2 g,formaliin 37% 27,25g,NH4OH vesilahus 25%-5% kaalust 1,41g Kasutatavad seadmed ja vahendid: 250ml ümarkolb,tagasivoolu jahuti,mehhaaniline segur,termomeeter,portselan kausike,vaakum kuivatuskapp Töökäik: Resoolvaigu sünteesimiseks kaalutakse ümarkolbi,mis on varustatud termomeetri,jahuti ja seguriga,fenool,formaliin ja ammoniaagivesilahus.Segu soojendatakse 85-90 kraadini kuni algab eksotermiline reaktsioon.Umbes poole
BIO METABOLISM METABOLISM ehk ainevahetus tähendab organismis aset leidvaid sünteesi ja lagundamisprotsess ELUKS ON VAJA ENERGIAT JA SÜSINIKKU lk 811 elusorganismid on võimelised omastama 2te liiki energiat-- valgusen. ja keemilist en. OKSÜDEERUMISE käigus aine koostises olevate aatomite elektonide arv väheneb, aatomitevahelised sidemed lõhutakse ning VABANEB EN. nt: rakuhingamise käigus lagundatakse glükoos CO2ks ja O2 läheb vee koosseisu REDUTSEERUMISE käigus lisandub aatomitesse elektrone (elektronide arv suureneb), tekivad uued aatomitevahelised sidemed ning seeläbi SALEVSTATAKSE EN. nt: fotosünteesis kasutatkse valgusen.t, et CO2st ja H2Ost sünteesida suhkruid ning eraldub O2 C--on võime moodustada pikki ahelaid, mill...
Tasakaalustada ja lõpetada juhendis toodud reaktsioonivõrrandid. Redoksreaktsioonides märkida, milline ühend on öksüdeerija, milline redutseerija. Katseandmete töötlus ja tulemuste analüüs Oksüdatsiooniastmete muutusteta kulgevad reaktsioonid Sademe teke KATSE 1 SO42- ioone sisaldavale lahusele (0,5…1 ml) lisada tilkhaaval Ba 2+ ioone sisaldavat lahust. Na2SO4+ BaCl2=2NaCl +BaSO4 ↓ SO42-+Ba2+=BaSO4 ↓ Lähteained on värvitud; tulemusena tekib valge sade KATSE 2 Al3+ ioone sisaldavale lahusele (0,5…1 ml) lisada 2M NH 3H2O lahust ammoniaagi lõhna püsimajäämiseni Al2(SO4)3 + 6NH3·H2O = 2Al(OH)3↓ + 3(NH4)2SO4 Al3+ + 3OH- = Al(OH)3 Lähteained on värvitud; tulemusena tekib valge sültjas sade. KATSE 3 Pb2+ ioone sisaldavale lahusele (0,5…1ml) lisada CrO 42- ioone sisaldavat lahust Pb(NO3)2 + K2CrO4 = 2KNO3 + PbCrO4↓ Pb2+ + CrO42– =PbCrO4↓
Dissimilatsiooni käigus lõhustatakse orgaanilised ühendid lihtsama ehitusega molekulideks. Nt valk aminohappeks. Dissimilatsiooniga kaasneb energia vabanemine. Makroergiline ühend.. ATP Assimilatsioon on organismi kõik sünteesiprotsessid. Assimilatsiooni käigus moodustuvad lihtsama ehittusega molekulidest keerulisema ehitusega orgaanilised ühendid: sahhariidid, lipiidid, valgud, nukleiinhapped. Assimilatsiooni toimumiseks on vaja enrgiat. Dissi- ja assimialtsiooni Võrdlus. Lähteained. Dissimilatsioon: keerulised orgaanilised ained Assimilatsioon: Anorgaanilised vüi lihtsama ehitusega orgaanilised ained Lõppproduktid: Dissimilatsioon: Anorgaanilised või lihtsama ehitusefa orgaanilised ained. Assimialtsioon: Orgaanilised ained. Energia: Dissimialtsioon: vabaneb Assimilatsioon: Kasutatakse. NÄITED Dissimilatsioon: seedimine, hingamine. Assimilatsioon: fotosünttes, valögusüntees, glükogeeni süntees. Fotosüntees toimub taimede kloroplastides Fotosüntees
Raku hingamine – Glükoosi lagundamine hapniku abil. Selle käigus saavad rakud energiat. Toimub kõikides organismides. *Fotosünteesi käigus tekkinud hapnik pärineb vee molekulidest. Fotosüntees Sümbioos – mõlemad saavad kasu Tülakoid – Kambrike, millel on oma membraan. Fotosünteesi valem: 6CO2+H2O+footonid=C6H12O6+6O2 Fotosünteesi kulg 1. Valgusstaadium toimub tülakoidi membraamis vaja on valgust lähteained: klorofüll, vesi saadused: vesinikioonid, hapnik, ATP 2. Pimedusstaadium toimub stroomas ei vaja valgust lähteained: vesinikioonid, süsihappegaas, ATP saadus: glükoos Orgaanilised ained – pärinevad elusorganismidest Anaorgaanilised ained – mineraalset päritolu ained Fotosüntees – Valgusenergia muundub keemiliseks energiaks.
ALUS + HAPE vaata HAPE + ALUS + HAPPELINE OKSIID SOOL + VESI 2NaOH + CO2 Na2CO3 + H2O + SOOL UUS ALUS + UUS SOOL CuCl2 + 2 NaOH Cu(OH)2 + 2NaCl NB! Reaktsioon toimub siis, kui mõlemad lähteained on vees lahustuvad ja vähemalt üks saadustest on vees lahustumatu (sade). lagunemine (to) ALUSELINE OSKIID + VESI Ca(OH)2 (to) CaO + H2O HAPPELINE + VESI HAPE SO3 + H2O H2SO4
ja saaduste valemid paremale poole võrdusmärki. (Võrdusmärgi asemel võib kasutada ka noolt). Võrrand tuleb tasakaalustada. See tähendab seda, et mingi elemendi aatomeid peab mõlemal pool võrdusmärki olema ühepalju, sest ühegi elemendi aatomid keemilise reaktsiooni käigus ei teki ega kao, samuti ei muutu nad mõne teise elemendi aatomiteks. Tasakaalustamiseks kasutatakse koefitsente, need on arvud, mis kirjutatakse ainete valemite ette. Võrrand näitab, millised olid lähteained ja millised on saadused, kuid ta ei vasta küsimusele, kuidas lähteained saadusteks muutuvad Indeksid näitavad molekuli koostist (kirjutatakse sümboli järele ja alla). Koefitsendid näitavad molekulide arvu kirjutatakse sümboli ette). Tasakaalustamiseks kasutame koefitsente. Indekseid seejuures muuta ei tohi. Koefitsent 1 jäetakse tavaliselt kirjutamata (nagu ka indeks1). Tasakaalustamiseks on mitmeid võimalusi, hea on leida kohe kaks koefitsenti. "Väiksema ühiskordse" meetod.
Aeroobne glükolüüs glükoosi täielik lõhustumine hapniku olemasolul, mis koosneb tsitraaditsüklist ja hingamisahela reaktsioonidest. 13.Nimeta glükoosi lagundamise põhivõrrand ja ained seal võrrandis. Kogu protsessi iseloomustab summaarne võrrand: C6H12O6 + 6O2 6CO2+ 6H2O. Glükoosi lagundamisel eristatakse kolme etappi: glükolüüs, tsitraaditsükkel ja hingamisahela reaktsioonid. (vesinik, süsinik, vesi) 14.Võrdle hingamist ja fotosünteesi. Hingamine · Lähteained: glükoos ja hapnik (orgaanilise aine lagunemine) · Saadused: süsihappegaas ja vesi · Toimumiskoht: mitokonder · Toimumisaeg: pidev Fotosüntees · Lähteained: süsihappegaas ja vesi orgaanilise aine tekkimine) · Saadused: glükoos ja hapnik · Toimumiskoht: kloroplast · Toimumisaeg: valguse käes 15. Mis on käärimine, kes seda teevad jne. Käärimine on teatud tüüpi organismide (bakterite ja pärmseente) ainevahetusprotsess, mis toimub
on võrdsed dünaamiline tasakaal 0 = k1[A]eq k-1[B]eq ehk k1[A]eq = k-1[B]eq [B]eq/[A]eq = k1/k-1 = K K pärisuunalise reaktsiooni tasakaalukonstant Vastasuunalise reaktsiooni tasakaalukonstant on alati pärisuunalise reaktsiooni tasakaalukonstandi pöördväärtuseks Tasakaaluolek valgu seostumine ligandiga k1 E + L EL Tasakaalukonstant K = [produktid]/[lähteained] k-1 Tasakaalukonstant kehtib alati näidatud või nimetatud reaktsiooniskeemi jaoks Pärisuunaline reaktsioon on ühinemisreaktsioon: Kass = k1/k-1 = [EL]/[E] [L] ühik M-1 k1 EL E + L Tasakaalukonstant K = [produktid]/[lähteained] k-1 Pärisuunaline reaktsioon on dissotsiatsioon: Kd = k-1/k1 = [E] [L]/[EL] ühik M Kui [L] = Kd (dissotsiatsioonikonstant), siis on pool valku ligandiga kompleksis
Lihtaine + hapnik = oksiid S + O2 = SO2 kõrgemat temperatuuri mittelahustuv hüdroksiid + temperatuur = Reaktsioon toimub ALATI!!! Zn(OH)2 + to= ZnO + H2O metalli oksiid + vesi Reaktsioon toimub KUI 1)lähteained on Alus + sool = sool + alus NaOH + CuSO4 = Cu(OH)2 + Na2SO4 lahustuvad, 2)üks saadus sadeneb välja Reaktsioon toimub KUI moodustub nõrgem Hape + sool = sool + hape H2SO4 + ZnS= ZnSO4 + H2S hape või gaas või sadeneb sool
H3PO4 Na2SO4 + H2O TEISI VÕIMALUSI SOOLADE SAAMISEKS 1) sool + alus uus sool + uus alus NB! Reaktsioon toimub juhul kui mõlemad lähteained on vees lahustuvad ja vähemalt üks saadustest on vees lahustumatu! CuCl2 + 2NaOH 2NaCl + Cu(OH)2 SOOLAD + H2O 2) sool + hape sool + hape MetxHappeanioony NB! Reaktsioon toimub juhul kui tekib reageerinud happest nõrgem hape või sade.
H3PO4 Na2SO4 + H2O TEISI VÕIMALUSI SOOLADE SAAMISEKS 1) sool + alus uus sool + uus alus NB! Reaktsioon toimub juhul kui mõlemad lähteained on vees lahustuvad ja vähemalt üks saadustest on vees lahustumatu! CuCl2 + 2NaOH 2NaCl + Cu(OH)2 SOOLAD + H2O 2) sool + hape sool + hape MetxHappeanioony NB! Reaktsioon toimub juhul kui tekib reageerinud happest nõrgem hape või sade.
Elektronkatte laeng: Aatom: Aatom koosneb positiivse elektrilaenguga aatomituumast, mida ümbritseb negatiivselt laetud elektronkate ehk elektronkest. Anorgaanilised aineklassid: Alused: aluseid liigitatakse leelisteks ja nõrkadeks alusteks, a) reageerivad happeliste oksiididega- saadused happelisele oksiidile vastav hapesool ja vesi. b) Reageerivad hapetega- saadused sool ja vesi c) Reageerivad sooladega- uus hüdroksiid ja uus sool. !mõlemad lähteained peavad olema vees lahustuvad ja üks saadustest lahustumatu d) Kuumutamisel lagunevad oksiidid- oksiidiks ja veeks va 1A rühma metallide hüdroksiidid. Amfoteersed hüdroksiidid reageerivad nii hapete kui alustega. ALUSTE SAAMINE a) leeliste saamine metall ja vesi- saadused leelis ja vesinik aluseline oksiid ja vesi- hüdroksiid Võrrandid: Mg + H2O -> MgO + H2 P4O10+h2o-> H2PO3 Happed: happeid liigitatakse sooladeks ja hapeteks 1
elementide o-a saab kahaneda. Redutseerijateks on aktiivsed metallid, gaasiline vesinik, süsinikmonooksiid, süsinik (koks) jt ühendid, milles sisalduvate elementide o-a saab kasvada. Kasutatud töövahendid: Katseklaaside komplekt Katseandmed: Oksüdatsiooniastmete muutuseta kulgevad reaktsioonid Sademete teke Katse 1: SO42 ioone sisaldavale lahusele lisada tilkhaaval Ba2+ ioone sisaldavat lahust. Na2SO4 + BaCl2 2NaCl + BaSO4 SO42 + Ba2+ BaSO4 Kommentaar: Lähteained on värvitud, tekib sade valge häguna. Katse 2: Al3+ ioone sisaldavale lahusele lisada 2 M NH3 H2O lahust ammoniaagi lõhna püsimajäämiseni. Al2(SO4)3 + 6NH3·H2O 2Al(OH)3 + 3(NH4)2SO4 2Al3+ + 6NH3·H2O 2Al(OH)3 + 6NH4- Kommentaar: Lähteained on värvitud, tekib piimjas sade. Katse 3: Pb2+ ioone sisaldavale lahusele lisada CrO42 ioone sisaldavat lahust. Pb(NO3)2 + K2CrO4 2KNO3 + PbCrO4 Pb2+ + CrO42 PbCrO4
Saksama on ükss nendest riikidest, kellel puudub oma nafta, sellepärast alutatigi Saksamaal varakult alternatiivkütuste otsinguid. Selle tulemusena arenes mootorkütust tootev tööstusharu eriti kiireti. 4. Nimeta riigid, kus keemiatööstus eriti tugevalt arenenud. Keemiatööstuses on esikohal Ameerika. Teisel kohal on Jaapan. Nendele järgnevad Saksamaa, Prantsusmaa, Suurbritannia ja Itaalia. 5. Põhiorgaanilise tööstuse toorained ja nende kasutamine Täida tabel Lähteained Millest Mida toodetakse? Mida valmistatakse saadakse? saadud ainest? Metaan naftagaas, Metanool, ammoniaak, Lahusti, kütus, maagaas metanaal pleksiklaas, desinfitseeriv vahend Eteen nafta Polüeteen, etüleenoksiid, Antifriiside krakkgaasid, etüülbenseen koostisosa,
6) Aluselised oksiidid on oksiidid, mis reageerivad happega moodustades soola ja H2O 7) Amfoteersed oksiidid on oksiidid, mis reageerivad nii happe kui alusega 8) Inertsed oksiidid on oksiidid, mis ei reageeri happe ega alusega 9) Neutralisatsioonireaktsioon on happe ja aluse vaheline reaktsioon 10) Happe lahuse toimul muutub metüüloranž punaseks, lakmus punaseks 11) Aluse lahuse toimel muutub fenoolftaleiin punaseks, lakmus siniseks 12) Sool reageerib teise soolaga, kui lähteained on vees lahustuvad ja vähemalt üks saadustest mittelahustuv 13) Sool reageerib happega, kui lähtehape on tugevam kui saadud hape 14) Metall reageerib happega, kui üksikmetall asub pingereas enne H2 15) Sool reageerib alusega, kui lähteained on vees lahustuvad ja vähemalt üks saadustest mittelahustuv 16) Metall reageerib soola lahusega, kui üksikmetall on pingereas enne soola koostises olevat metalli
7. Hape + Alus = Sool + Vesi · Reaktsioon toimub alati. 8. Hape + Sool = Uus hape + Uus sool · Reaktsioon toimub siis, kui tekib reageerivast happest nõrgem või lenduvam hape või kui tekib sade. · Kui tekib hape HCO, siis laguneb ta tekkemomendil veeks ja süsinikdioksiidiks. 9. Hape (lagunemine kuumutamisel) = Happeline oksiid + Vesi · Lagunevad ainult hapnikhapped. 10. Alus + Sool = Uus alus + Uus sool · Mõlemad lähteained peavad olema lahustuvad ja saadustes peab olema vähemalt üks lahustumatu. 11. Alus (laguneb kuumutamisel) = Aluseline oksiid + Vesi · Ei lagune IA rühma metallide hüdroksiidid. 12. Sool + Metall = Uus sool + Uus metall · Metall reageerib vees lahustuva soolaga, kui ta on aktiivsem kui soola koostises olev metall. · Metallid, mis reageerivad külma veega (IA ja IIA alates kaltsiumist), ei asenda
2) kemosünteesijad - keemilineenergia (bakterid) Liik: Harilik kuusk, roos Liik: Hobune, lõvi Kõik elu tunnused olemas Kõik elu tunnused olemas Vaja energiat elutegevuseks Vaja energiat elutegevuseks ASSIMILATSIOON DISSIMILATSIOON organismis toimuvad sünteesiprotsessid organismis toimuvad lagundamisprotsessid (tootmine) vaja: lähteained, ensüümid ja energia vaja: lõhustada orgaanilised ühendid lihtsama ehitusega molekulideks saadakse: sahhariidid, lipiidid, valgud, saadakse: energia, mis salvestatakse ATP ja nukleiinhapped soojusena NT: fotosüntees, valkude süntees, DNA süntees NT: glükoosi lagundamine (rakuhingamine) Ülekaalus: lapsel, rasedal, sportlasel
Protsessi Toimumise Lähteained Protsessi nimetus koht saadused Püroviinam GLÜKOLÜÜS Tsüsoplasma glükoos ari- - Hape võrgustikus 2NADH2 TSITRAADITÜK Mitokondri 2 6 CO 2 sisemuses püroviinamar 10 NADH KEL 2 i- hapet 36 ATP HINGAMISAHE Mitokondri 12 NADH2 12 H2O harjakesed 6 O2 12 NAD L
Na2SO4 + H2O TEISI VÕIMALUSI SOOLADE SAAMISEKS 1) sool + alus uus sool + uus alus NB! Reaktsioon toimub juhul kui mõlemad lähteained on vees lahustuvad ja vähemalt üks saadustest on vees lahustumatu! CuCl2 + 2NaOH 2NaCl + Cu(OH)2 SOOLAD + H2O 2) sool + hape sool + hape MetxHappeanioony NB
Fotosüntees FOTOSÜNTEES Valguse - abil - valmistamine I vajalikud tingimused: 1. Valgusenergia 1. Klorofüll II lähteained: 1. CO2 1. H20 III saadused: 1. Glükoos 1. O2 Millisest FS lähteainest tekib 02? · H20 tekib O2 Fotosünteesi tähtsus: 1. Toodab hapniku 2. Toodab toitu 3. Vajalik ka osooni tekkeks
Kõik organismid vajavad elutegevuseks energiat. Vastavalt energia saamise viisile jaotatakse organismid auto- ja heterotroofseteks. 2. Autotroofid sünteesivad ise eluks vajalikud orgaanilised ühendid väliskeskkonnast saadavatest anorgaanilistest ainetest (H2O, CO2), kasutades peamiselt valgusenergiat (fotosüntees) või ka redoksreaktsioonidel vabanevat keemilist energiat. 3. Heteroroofid saavad oma elutegevuseks vajaliku energia ja sünteesiprotsessideks vajalikud lähteained toidus sisalduva orgaanilise aine lagundamisel (glükoosi lagundamine). 4. Fotosüntees tuleusena moodustub glükoos (C6H12O6), jääkprodukt O2 eraldub atmosfääri. Üldvalem: 6CO2 + 12H2O = C6H12O6 + 6O2 + 6H2O 5. Taimedes moodustub glükoosist tärklis või tselluloos. Taimed täiendavaid orgaanilisi aineid väliskeskkonnast juurde ei vaja. 6. Metabolism organismis aset leidvad sünteesi- ja lagundamisprotsessid, mis tagavad tema
AMINOHAPPED ON PALJUDE BIOMOLEKULIDE PREKURSORITEKS AMINOHAPPED JAOTATAKSE · ASENDAMATUD (nn essentsiaalsed): Arg, His, Iie, Leu, Lys, Met, Phe, Thr, Trp, Vai Miks asendamatud? Sest, et imetajatel puudub mõni vastavate metaboolsete radade ensüümidest. · ASENDATAVAD (nn mitte-essentsiaalsed): Ala, Asn, Asp, Cys, Glu, Gln, Gly, Pro, Ser, Tyr AMINOHAPETE BIOSÜNTEESI LÄHTEAINED NB! Enamik organisme (taimed, mikroorganismid) võimelised sünteesima kõiki aminohappeid Sünteesi lähteained Aminohapete arv · -ketohapped -KETOGLUTARAAT 4 OKSALOATSETAAT 6 PÜRUVAAT 3 · 3-fosfoglütseraat 3 · Riboos-5- P 1 · Fosfoenoolpüruvaat + Erütroos- 4- P 3(aromaatsed) NH3 KUI LÄMMASTIKÜHENDITE AINEVAHETUSE LÕPP-PRODUKT · VÄLJUTATAKSE ORGANISMIST