Leelismetallid, naatrium Leelismetallid asuvad IA rühmas. Leelismetallid kui aktiivseimad metallid loovutavad kergesti aatomi väliselt kihilt ainsa elektroni. Kõige tuntumad leelismetallid on kaalium ja naatrium. Veel kuuluvad sinna ka liitium, rubiidium, tseesium, frantsium. Keemiliste omaduste poolest kuuluvad leelismetallid kõige aktiivsemate elementide hulka - nad on väga tugevad redutseerijad. Naatriumi omadused Välimuselt on naatrium hõbevalge metall. Naatrium on pehme, teda saab noaga lõigata. Naatriumi tihedus on 0,97 g/cm3 ja sulamistemperatuur on 98 Celsiust. Ta on keemiliselt väga aktiivne, mistõttu hoitakse teda hapnikukindla kihi all, eemal veest. Naatrium reageerib paljude lihtainete, vee ja hapetega. Hapetest ja veest tõrjub ta välja vesinikku ning tekib vastavalt sool ja hüdroksiid. Suurem osa naatriumi sooli lahustub vees hästi. Omadustelt on naatrium leelismetall. Sellisena on ta oksüdatsiooniaste ühendites 1. Naatriu...
Leelismetallid Li, Na, K, Rb, Cs, Fr Leidumine looduses: · Looduses leidub neid ainult ühenditena. · Põhilielt esinevad kloriididena: naatriumkloriid(merevees,pinnases), kaaliumkloriid(pinnases, taimedes), liitiumkloriid, teised esinevad maakide koostises · Karbonaatidena: Na2CO3 · Sulfaatidena: Na2SO4, K2SO4 · Nitraatide ehk salpeetritena: NaNO3, KNO3 Aatomi ehitus: Na e=11, p1=11, n1=12 Na+11|2)8)1) 1s2 2s2 2p6 3s1 o-a.1 · Leelismetallide aatomid paiknevad kristallvõres suhteliselt hõredalt, see tingib nende väga väikese tiheduse. · Pehmed metallid, kergesti lõigatavad Füüsikalised omadused · Tahkes olekus · Hõbedased, v.a tseesium, mis on kollakat värvi · Tihedus on väike (Liitium, kaalium, naatrium veest kergemad) · Suhteliselt madala keemistemperatuuriga · Head soojus- ja elektrijuhid · Omavad läiget Keemilised omadused · Väga tugevad redutseeriad (loo...
LEELISMETALLID. NAATRIUM 1. Üldiseloomustus · Leelismetallid asuvad IA rühmas. Väliskihi elektronvalem ns1. · Nad on aktiivsed metallid (loovutavad väliskihilt on ainsa elektroni) ja lähevad katioonideks (Na 1e- Na+). · Keemilistelt omadustelt on kõik leelismetallid väga sarnased. · Väike elektronegatiivsus. · Ühendites on iooniline side (NaCl, KOH, Li2SO4). · Looduses esinevad ainult ühenditena (kloriididena, sulfiididena, karbonaatidena jt...). · Kõige levinumad on naatrium ja kaalium. · Ühendid annavad leegis kuumutamisel iseloomuliku värvuse. 2. Leelismetallid lihtainena · Kerged, pehmed, plastilised, madala sulamistemperatuuriga. · Keemiliselt väga aktiivsed (hoitakse petrooleumi või õlikihi all). · Reageerimisel veega moodustavad leelis ja eraldub vesinik (Na + H2O NaOH + H2). · Kõik leelismetallid reageerivad hapnikuga. Liitiumiga tek...
Kordamine üleminekueksamiks: Leelismetallid asuvad IA rühmas (naatrium, kaalium). On aktiivseimad metallid, loovutavad kergesti (võime kasvab ülevalt alla, aatomite mõõtmete kasvu tõttu) väliselt elektronkihilt ainsa elektroni, muutudes väga püsivateks leelismetallide katioonideks laenguga 1+. Väikese elektronegatiivsusega, ühendites on valdavalt iooniline side. Looduses vabalt ei leidu, eelkõige kloriididena. Kõige parem on kindlaks teha kuumutamisel, leegil on iseloomulik värvus. Kerged, pehmed, suhteliselt madala sulamistemperatuuriga. Keemiliselt väga aktiivsed, oksüdeeruvad kiiresti kokkupuutel hapniku (tekib peroksiid, hüperoksiid; need on tugevad oksüdeerijad, süsinikdioksiidiga reageerides eraldavad hapnikku) või veega (moodustavad leelise, tõrjuvad välja vesiniku). Seetõttu hoitakse suletud anumas petrooleumi- või õlikihi all. Nahale tekitavad sügavaid põletushaavu. Naatriumit kasutatakse redutseerijana n...
http://www.abiks.pri.ee LEELISMETALLID Nende aatomite väliskihi elektron valem on ns1. Nendes metallides on metallvõre, mida hoiab koos metalliline side. (Metalliline side on metallioonide ja liikuvate ühistatud elektronide vastastikune tõmbumine metallides) Füüsikalised omadused kerged, pehmed, suhteliselt madala sulamistemp Keemilised omadused: leelismetallid asuvad pingereas vesinikust vasakul ning on kõige aktiivsemad metallid. *Kõik leelismetallid reageerivad veega >> leelis + H2 *Annavad reageerides hapnikuga peroksiidi (Na2O2) või hüperoksiidi (KO2), ainult liitium reageerib ootuspäraselt moodustades oksiidi *Kõik leelismetallid reageerivad lahjendatud hapetege andes soola ja H 2 (2Na + 2HCl =2NaCl + H2 oksüdeerijaks H+ ioon) *Leelismetall reageerib vees lahustuva soolaga kui ta on aktiivsem kui soola koostises olev metall, tekib soo...
Leelismetallid on IA rühma metallid.reag veega tekivad leelised. Vees lahustuv hüdroksiid. Väga söövitav. 2Na+2H2O=2NaOH+H2.. leelismuldmetallid. Ca, Sr, Ba. Levikult maakoores. Al Fe Ca Na K Mg. Ühendid Na+O2=Na2O2.. naatriumperoksiid. K+O2=KO2 kaaliumhüperoksiid. CaO kustutamata lubi. CaCO3 lubjakivi, paekivi = Cao+CO2. CaO+H2O=Ca(OH)2. Lubja kustutamine. Vees vähelahustuv tekib lubjapiim veega segamisel, seismisel lubjavesi. NaOH seebikivi. NaHCO3 söögisooda kasutamine.. taignate kergitamine. Tugeva happe neutraliseerimiseks.Na2CO3 sooda kasutamine. tooraine klaasi valmistamisel, argielus. Na2CO3 pesusooda. NaCL keedusool. Tänu pinnale tekkivale õhukesele, kuid tihedale oksiidikihile on alumiinium väga vastupidav õhu ja vee toime suhtes. Al on raua järel üks enam kasutatavaid metalle. Temast valmistatakse mitmesuguseid tarbeesemeid, kerge metalline on ta hinnatud ehituses. Kasutatakse ka erinevates sulamites, vähemaktiivsete metallid...
Leelis- ja leelismuldmetallid. Leelis- ja leelismuldmetallid: Lühiiseloomustus Lihtaine omadused Leidumine Tuntum ühend ja selle iseloomustus Leidumine organismis Kasutamine Leelismetallid IA rühma metallid Li, Na, K, Rb, Cs, Fr IA rühm => väliskihil 1e => o.a +I Väliskihi elektronvalem ns1 s-metallid Kõige aktiivsemad metallid Rühmas suureneb aktiivsus ülevalt alla Mida suurem aatomiraadius, seda aktiivsem, sest kergem elektrone loovutada Leelismuldmetallid IIA rühma metallid alates kaltsiumist: Ca, Sr, Ba, Ra IIA rühm => väliskihil 2e => o.a +II Väliskihi elektronvalem ns2 s-metallid Aktiivsed metallid Rühmas suureneb aktiivsus ülevalt alla Lihtaine omadused: (leelismetallid) Füüsikalised omadused. Kerged, pehmed, noaga lõigatavad, madal sulamistemperatuur. Hõbevalged. Keemilised omadused. Liikudes rühmas ülalt alla suureneb aatomiraadius, järjest kergemini loovutatakse väliskihi elektron ja metallilised omadused tugevne...
METALLID FÜÜSIKALISED OMADUSED · Plastilised (üks plastilisemaid on kuld). · Head valguse peegeldajad (kõige paremini hõbe, alumiinium ja indium). · Head elektri- ja soojusjuhid (parimad Au, Ag, Cu, Al). · Käega katsudes külmad. · Sulamistemperatuurid on väga erinevad (Hg -39 oC, W 3422 oC). · Värvuselt on enamik metalle hõbevalged, kuid neil võib olla oma iseloomulik helk (Cr sinakas, Bi punakas, Ni - kollakas). Iseloomuliku värvusega on kuld kollane, vask punakas, tseesium kollakas. · Tihedused on väga erinevad. Enamik on veest raskemad välja arvatud leelismetallid liitium (Li) ja naatrium (Na). · Kõvadus on metallidel väga erinev. Leelismetallid (naatrium, kaalium, liitium) on väga pehmed (noaga lõigatavad). Kõige kõvem metall on kroom. Väga kõvad on ka paljude metallide sulamid. METALLILINE SIDE · Enamik metallide väliskih...
Keemia 1.Mõisted! OKSÜDEERIJA- aine, mis seob(liidab) elektrone OKSÜDEERUMINE- elektronide loovutamine reaktsioonis(o.a suureneb) REDUTSEERIJA- aine, mis loovutab(lahutab) elektrone REDUTSEERUMINE- elektronide liitmine reaktsioonis(o.a väheneb) REDOKSREAKTSIOON- reaktsioon, mille köigus elementide o.a muutub 2.Sulamid (mis nad on?, miks valmistatakse?, tähtsamate sulamite koostisosad ja kasutus) SULAM- metallide ( või metalli ja mittemetalli) kokkusulamisel saadud materjal Sulameid valmistatakse, et metallide omadusi paremaks muuta SULAM KOOSTIAINED KASUTAMINE Terased Raud, lisandina süsinik(võivad Tööriistad, sisaldada veel mitmeid metalle masinaosad,seadmed, n. Cr, Ni) ehituskonstruktsioonid Duralumiinium A...
METALLID ÜLDINE ISELOOMUSTUS ·Välisel elektronkihil on enamasti vähe elektrone(1-3) ·Metalliaatomite raadius suht suur. ·Aatomid hoiavad väliskihi elektrone nõrgalt kinni, seega on neil väike elektronegatiivsus. ·Ühendites alati pos. o.a FÜÜSIKALISED OMADUSED ·Elektrijuh., soojusjuh., plastilisus, metalne läige(peegeldusvõime). ·Metallid erinevad teineteisest: 1)tihedus(kerg-, raskemetallid):Li 0,5g/cm3 ; Os 22,6g/cm3 2)Sulamistemp.(kerg-, rasksulavad):Hg -39°C, W 3400°; 3)Kõvadus(kõvad Cr, pehmed leelismet.) 4)Värvus(kollane Au, punane Cu, teised valged,hallid) 5)Magnetiseerivus(Fe,Co,Ni) KEEMILISED OMADUSED ·Metallid on reaktsioonides alati redutseerijad(loovutavad elektrone) ·Reag. veega a)aktiivsed met.(K-Mg) reag. vedela veega; tekivad hüdroksiid ja H2 ( 2Na+2H2O®2NaOH + H2 ) b)keskm aktiivsed met.(Al-Fe) reag. auruga kõrgel temp; tekivad oksiidid ja H2 ( Zn+H2O®ZnO+H2 ) c)väh. akktiivsed met.(Ni-Au) ei reagereeri veega ·Reag. l...
METALLID Metallid on : Berüllium, Magneesium, Alumiinium, Skandium, Titaan, Vanaadium, Kroom, Mangaan, Raud, Koobalt, Nikkel, Vask, Tsink, Gallium, Ütrium, Tsirkoonium, Nioobium, Molübdeen, Tehneetsium, Ruteenium, Roodium, Pallaadium, Hõbe, Kaadmium, Indium, Tina, Hafnium, Tantaal, Volfram, Reenium, Osmium, Iriidium, Plaatina, Kuld, Elavhõbe, Tallium, Plii, Vismut, Poloonium, Rutherfordium, Dubnium, Seaborgium, Bohrium, Hassium, Meitneerium, Darmstadtium ja Röntgeenium. Poolmetallid on : Germaanium, Arseen, Antimon, Telluur ja Astaat. Leelismetallid on : Liitium, Naatrium, Kaalium, Rubiidium, Tseesium ja Frantsium. Leelismuldmetallid on : Kaltsium, Strontsium, Baarium ja Raadium. Sulamistemperatuur metallidel on väga erinevad sulamis temperatuurid. Madalaima sulamistemperatuuriga metall on elavhõbe (-39ºC). Naatrium sulab 98ºC juures, tina sulamistemperatuur on 232ºC. Zn - 420ºC, Al - 660ºC,...
1A Rühma metallide omadused : Hõbe värvus, Kerged, Pehmed, Head soojus-ja elektrijuhid, hoitakse õlis või petrooliumis. leelismetallid tuleneb sellest, et rühma kahe peamise esindaja naatriumi ja kaaliumi hüdroksiidid on iidsest ajast tuntud leeliste nime all. leelismetallide leidumine looduses : Ühenditenam(Nacl,Kcl). Leelismetalle hoitakse õlis või petrooleumis, sest nad on aktiivsed metallid. Süttimisel ei tohi kustuda veega, vaid tuleb takistada hapniku juurdepääs. Leelismetallide Leekreaktsioonid : Li roosa leek, Na kollane leek, K Lilla leek. Na on vajalik soolhappe moodustamiseks maomahlas, osaleb soola ja vee ainevahetuses. K on vajalik südametegevuseks, laiandab veresooni ja alandab vererõhku. Aeroon on alumiiniumi ja Liitiumi sulam, on kerge, tugev ja korrosioonikindel. Kasutatakse lennuki ja autotööstuses. LibBr Meditsiinis, LiCl pürotehnikas, Li2CO3 Meditsiinis, NaCl Toiduainete tööstus, tänavate soolamine,...
Leelised ehk I A rühma metallid Ajalooliselt tuleneb sõna leelismetall sellest, et nende metallide hüdroksiide tunti juba ammu ja neid nimetati leelisteks. Tänapäevane selgitus võiks olla lihtsalt selline, et nende metallide veega reageerimisel tekivad leelised. Leelismetallid on kõige metalsemad elemendid. Aatomi ehituselt kuuluvad nad s-elementide hulka, kuna nende aatomite välisel orbitaalil on üks elektron. Sellest tulenevalt on kõikide leelismetallide aatomite väliskihi elektronvalemiks ns ja oksüdatsiooniastmeks ühendis +I. Kuna leelismetallidel on väliskihis ainult üks elektron, siis seetõttu nad loovutavad selle erakordselt kergesti. Kusjuures mida kaugemal väliselektron aatomituumast asub, seda kergemini see loovutatakse. Just sel põhjusel on leelismetallid väga tugevad redutseerijad ja keemiliste omaduste poolest nad kuuluvad kõige aktiivsemate metallide hulka. Elektroni loovutamise tagajärjel muutuvad leelismetallide aatom...
· Leelis- ja leelismuldmetallid Leelismetallid I Asetus perioodilisussüsteemis ja aatomi ehitus Leelismetallid on IA rühma metallid. Nimetus "leelismetallid" on tuletatud sellest, et nende metallide hüdroksiidid on leelised (st. vees lahustuvad hüdroksiidid). II Leelismetalliühendite kindlakstegemine Leelismetallid ja nende ühendid värvivad leeki. Na-ühendite toimel värvub leek kollaseks, Kühendite toimel violetseks, Li-ühendite toimel punaseks. III Leelismetallide omadused Füüsikalised omadused · kerged · pehmed (saab noaga lõigata) · hõbevalged · madala sulamistemperatuuriga · hea elektri- ja soojusjuhtivusega Keemilised omadused · Keemilise aktiivsuse tõttu ei leidu neid looduses lihtainena (ehedana), vaid ainult ühendite koostises. Näiteks NaCl kivisool. · Õhus oksüdeeruvad kiiresti, metalli hõbedane pind tuhmub ja seepärast hoitakse neid õli- või petrooleumikihi all. · Reageerivad vee...
METALLID FÜÜSIKALISED OMADUSED · Plastilised (üks plastilisemaid on kuld). · Head valguse peegeldajad (kõige paremini hõbe, alumiinium ja indium). · Head elektri- ja soojusjuhid (parimad Au, Ag, Cu, Al). · Käega katsudes külmad. · Sulamistemperatuurid on väga erinevad (Hg -39 oC, W 3422 oC). · Värvuselt on enamik metalle hõbevalged, kuid neil võib olla oma iseloomulik helk (Cr sinakas, Bi punakas, Ni - kollakas). Iseloomuliku värvusega on kuld kollane, vask punakas, tseesium kollakas. · Tihedused on väga erinevad. Enamik on veest raskemad välja arvatud leelismetallid liitium (Li) ja naatrium (Na). · Kõvadus on metallidel väga erinev. Leelismetallid (naatrium, kaalium, liitium) on väga pehmed (noaga lõigatavad). Kõige kõvem metall on kroom. Väga kõvad on ka paljude metallide sulamid. METALLILINE SIDE · Enamik metallide väliskih...
METALLID •Metallide iseloomulikud omadused(metalne läige, hea elektri- ja soojusjuhtivus, plastilisus) on tingitud metallides esinevast metallilisest sidemest. •Parimad elektrijuhid on hõbe, vask ja kuld. Suhteliselt hea elektrijuht on alumiinium. •Suhteliselt madala sulamistemperatuuriga on leelismetallid, neis esineb valdavalt metalliline side. Kõrgeima sulamistemperatuuriga on 5. ja 6.perioodi siirdemetallid(kovalentne side). •Metallide tihedus üldreeglina kasvab rühmas ülevalt alla. Praktikas olulised kergmetallid. Suurima tihedusega on 6.perioodi siirdemetallid. •Magnetilised omadused 1. Ferromagnetilised metallid - raud, koobalt, nikkel ja gadoliinium - magnetiseeruvad juba nõrgas magnetväljas. 2. Paramagnetilised metallid - alumiinium, kroom, titaan - magnetiseeruvad nõrgalt. 3. Diamagnetilised metallid - tina, vask, vismut - ei tõmbu magneti poole, vaid tõukuvad sellest eemale. ...
1.Leelis-, leelismuldmetallide, p-elementide ja d-elementide aatomite ehitus (elektronvalem, elektronskeem), oksüdatsiooniastmed ühendites. *Leelismetallid on 1. A rühm v.a. H. Lihtainena looduses ei leidu. nt. Na +11/2)8)1) *Leelismuldmetallid on 2. A rühm v.a. Be ja Mg.Lihtsainena ei leidu looduses oma aktiivsuse tõttu. nt. Ca +20/2)8)8)2) *P-elemendid- tuntumad plii, alumiinium ja tina. Leidub ainult ühenditena. nt. Al +13/2)8)3) o.-a. võib olla neil +2 või +4. *Siirdemetallid ehk d-elemendid on B rühm, tuntumatest kuuluvad 4. perioodi nt.raud, vask, tsink, nickel, kroom jt. Leidub nii puhtalt kui ka ühenitena. nt. Fe +26/2)8)14)2) 2. Tähtsamate esindajate omadused ( füüsikalised ja keemilised)- Na, K, Ca, Mg, Al, Sn, Pb ja Fe *Na ja K-hõbe valged, hästi pehmed, madala salamis temperatuuriga, veest kergemad, väikse tihedusega, väga head soojus- ja elekrtijuhid. / Üli aktiivsed, nende aktiivsuse tõttu tuleb neid hoida suletud anuma...
Tähtsamad metallid ja nende ühendid. Kõik esimese A rühma metallid on leelismetallid, sest nende hüdroksiidid (NaOH, KOH) on tugevad leelised: süüvitava toimega, Teise A rühma metallidest, alates Kaltsiumist on muldleelised. Ka nende hüdroksiide nimetatakse leelisteks. Kõik b-rühma metallid on siirde e. ülemineku metallideks. Esimese ja teise rühma A rühma metallid on aktiivsed metallid. Sinna kuuluvad leelismetallid jaleelismuld metallid. Kuna nende väliskihil on üks kuni kaks elektroni. Siis need elemendid loovutavad väliskihi elektrone väga aktiivsed metallid. Keskmise aktiivsusega metallid on alates Al kuni Cd. Metallide üldiseloomustus. 1. Metallid paiknevad süsteemis vasakul ja allpool. 2. Metalli aatomite välisel elektron kihil on enamasti vähe elektrone.(1-3(4)) 3. Metalliaatomite raadius on suhteliselt suur. 4. Metalliaatomid hoiavad väliskihielektrone nõrgalt kinni, seega neil on v...
Metallid Metallide üldiseloomustus Hästi töödeldavad, plastilised (va Sb ja Bi) Metalse läikega Suure albeedoga (poleeritult) Head soojusjuhid Head elektrijuhid Pulbrina tuhmhallid või mustad (va Mg, Al, Cu, Au jmt) Füüsikalised omadused · Sulamistemperatuur väga erinevad tavatingimustes tahked (va Hg) leelismetallidel* madal *IA rühma elemendid, mis on nime saanud sellest, et annavad veega reageerides leeliseid Tihedus · > 1 g/cm3 (va Li, Na, K) · on seda väiksem, mida väiksem on metalli aatomi aatommass ja mida suurem on aatomraadius · < 5 g/cm3 kergmetallid (leelismetallid, Ti, Mg, Al) · Ülejäänud raskmetallid Kõvadus Leelismetallid on pehmed ja kergesti lõigatavad Kergesti kriimustuvad Au, Sn, Pb Kõige kõvem Cr Sõltub puhtusest ja eelnevast töötlusest (lisandid suurendavad kõvadust) Metalliline side Elektronkihtide kattumine Elektronide siirdumine teise tuuma mõjualasse Väliskihi ...
Leelis ja leelismuldmetallid 1. Leelis- ja leelismuldmetallide iseloomulikud füüsikalised (kõvadus, sto, tihedus) ja keemilised omadused; Na, K, Mg, Ca levik maakoores ja tähtsus elusloodusele Leelismetallid on IA rühma metallid. Nimetus "leelismetallid" tuleneb sellest, et nimetatud metallide hüdroksiidid on leelised (st. vees lahustuvad hüdroksiidid). Füüsikalised omadused Keemilised omadused · kerged · pehmed (saab noaga lõigata) · Keemilise aktiivsuse tõttu ei · hõbevalged leidu neid looduses lihtainena · madala sulamistemperatuuriga (ehedana), vaid ainult ühendite Li - 454 K koostises. Na 371 K Näiteks ...
Teras on sulam, mille põhikomponent on raud ning mis muude elementide (väävel, fosfor jne) kõrval sisaldab kuni 2,14% süsinikku Vask on punaka värvusega, sepistatav, valtsitav ja traadiks tõmmatav metall. Ta on hea soojus- ja elektrijuht. Kuumutamisel õhus kattub vask musta värvusega vask(II)oksiidi kihiga. Kuivas õhus on vask püsiv. Niiskes õhus tekib vaskesemete pinnale aja jooksul korrosiooniprotsessi tagajärjel pruuni või roheka värvusega paatinakiht. Rohekas paatinakiht, mida mõnikord näeme vanadel vaskesemetel, tekib väga aeglaselt. Kerge saadavus maagist, ja üsna madal sulamistemperatuur lubasid vasel olla üks esimesi inimkonna poolt enimkasutatavaid metalle. Pronksiajal kasutati peamiselt vase ja tina sulamit pronksi, valmistamaks relvi, ehteid, raha jne FÜÜSIKALISED OMADUSED Plastilised (üks plastilisemaid on kuld). Head valguse peegeldajad (kõige paremini hõbe, alumiinium ja indium). Head elektri- ja soojusjuhid (parimad A...
1. Aineklasside määramine 2. Hapete nimetused ja valemid 3. Hapete omadused: reageerimine metallidega, oksiididega, alustega, sooladega. 4. Aluste nimetused ja valemid 5. Aluste omadused: reageerimine oksiididega, alustega, sooladega. 6. Soolade nimetused ja valemid 7. Soolade omadused: reageerimine metallidega, alustega. 8. Molaarmassi arvutamine. 9. Ülesanded( protsent, mass, saagikus) 10. Metallide füüsikalised omadused. 11. Metallide keemilised omadused. 12. Mis on korrosioon ja kuidas selle vastu saab? 13. Leelismetallid ja nende ühendid. 14. Leelismuldmetallid, iseloomustus ja nende ühendid. · Leelismuldmetallid on: Mg, Ca, Be. Looduses neid vabalt ei leidu, need esinevad karbonaatide, sulfaatide ja silikaatidena. Need on väga aktiivsed metallid. Mg- hõbevalge, kergesti sulav. Ca-hõbevalge, veest 1, 5 korda raskem. Ühendid: Kaltsiumoksiid CaO ehk kustutamata lubi. K...
Aatom keemilise elemendi väikseim osake, molekuli koostisosa, koosneb tuumast ja elektronidest Aatomi elektronkate aatomituuma umber tiirlevate elektronide kogum, mis koosneb elektronkihtidest Aatommass aatomi mass aatommassiühikutes Aatomi tuum aatomi keskosake, moodustab põhiosa aatomi massist, koosneb prootonitest ja neutronitest Ainete segu mitme aine segu, mis koosneb erinevate ainete osakestest Alus e. hüdroksiid on aine, mis annab lahusesse hüdroksiidioone (OH-), metalli katioonide+ ühend hüdroksiidiooniga - Aluseline keskkond ülekaalus on hüdrosiidioonid (OH-), pH>7 Aluseline oksiid metallioksiid, hapniku ühend metalliga Anioon negatiivse laenguga ioon Elementide rühm Mendelejevi perioodilisuse tabelis kohakuti üksteise all asuvate elementide rida, rühma elementidel väliskihis rühma numbrile vastav arv elektrone Elementide periood Mendelejevi perioodilisuse tabelis kõrvuti asuvate elemantide rida,...
I A RÜHMA METALLID: nende metallide veega reageerimisel tekivad leelised. Leelismetallid on kõige metalsemad elemendid.mida kaugemal väliselektron aatomituumast asub, seda kergemini see loovutatakse. Leelismetallid on väga tugevad redutseerijad ja keemiliste omaduste poolest kuuluvad kõige aktiivsemate metallide hulka. Ehedalt (lihtainena) neid looduses suure keemilise aktiivsuse tõttu ei leidu!! esineb väga paljude ühendite koosseisus. Füüsikalised omadused: Leelismetallides on kõige puhtamal kujul metalliline side, nad on metalse läikega, enamik neist on hõbevalged metallid, ainult tseesium on kuldkollase värvusega. Nendel on madalamad sulamis- ja keemistemperatuurid, nad on pehmed. Väikese tiheduse tõttu on nad kerged metallid ning hea soojus- ja elektrijuhtivusega. Kui vaadelda füüsikaliste omaduste muutumist rühmas, siis rühmas allapoole liikudes alaneb metallide sulamis- ja keemistemperatuurid, kasvab nende tihedus Keemilised omad...
Leelis ja leelismuld metallid Leelismetallid IA rühm.väliskihi el.valem - ns², oksüd. aste 2. Leelismuldmetallid- IIA rühm(alates Ca) *nendel on omadus anda kuumutamisel leegile isel. värvus. Kuumutamisel ühendid lenduvad,nende aatomid ergastuvad ja üleminekul Madalamasse energiaga olekusse kiirgavad isel, värvusega valgust. Naatrium-kollane K-kahvatulilla Ca-punane Ba-heleroheline Leelis ja leelismuldmetallid (metalliline side) *pehmed ,kergesti lõigatavad *kerged *madal sulamis, temp *hea elektri ja soousjuht. *puhas metallpind on läikiv, hõbevalge värvusega. *reduts. Hapnikuga ja paljude teite metallidega. *reduts, veega mood vastava leelise ja tõrjudes välja happniku. *reduts tormiliselt hapetega,tõrjudes välja vesiniku. *tänavavalgustus Na aurudega täidetud lambid. Oksiidid Valged tahked ainet tugevate aluseliste omadustega. Reag veega mood leelise. Kustutamata lubi kaltsiumoksiid, kasutatakse Gaaside või vedelike kuivam...
Tähtsamaid metalle ja nende ülesanded. 1. Mõisted. a. Leelismetallid – kõige aktiivsemad metallid, mis kuuluvad IA rühma. b. Leelismuldmetallid – metallid, mis kuuluvad IIA rühma. c. Vee karedus – lahustunud kaltsiumi- või magneesiumiühendite sisaldus looduslikus vees. Kui karedust on võimalik kõrvaldada vee kuumutamisel, siis on see mööduv karedus ning kui ka vee kuumutamisel see ei kao, siis on jääv karedus. d. Siirdemetallid – metallid, mis kuuluvad B-rühma. e. P-metallid – metallid, millel on viimasena täitunud p-orbitaal. f. Leelis – hüdroksiid, vees hästi lahustuv tugev alus. 2. Valemid ja kasutusalad. a. Söögisooda - NaHCO3, toidutööstus, meditsiin ja keemialaborid. b. Pesusooda – Na2CO3, pesupulber. c. Seebikivi – NaOH, seebi valmistamine. d. Keedusool – NaCl., meditsiin, seebi- ja teiste pesuainete tootmine. e. Ki...
Metallid Mis on metallid? Enamasti on metallid iseloomuliku läikega tahked ained, mille värvus varieerub tavaliselt terashallist hõbevalgeni. Metallide siledad poleeritud pinnad peegeldavad hästi valgust. Mõned metallid (hõbe, alumiinium)peegeldavad valgust nii hästi, et neid saab kasutada peeglite valmistamiseks.Metallid on enamasti plastilised ning hästi töödeldavad. Kuumutatult saab metalle kergesti valtsida ja venitada ning sepistada nendest vajaliku kujuga esemeid. Üks plastilisemaid metalle on puhas kuld.Metallid on head soojusjuhid. Metallide hea elektrijuhtivus võimaldab nendest valmistada elektrijuhtmeid ja- kontakte. Primad elektrijuhid on hõbe ja vask. Samuti on nad parimad soojusjuhid. Head soojus- ja elektrijuhid on ka alumiinium ja kuld. Füüsikalised omadused Metallide sulamistemperatuurid on väga erinevad. Madalaima sulamistemp. metall on elavhõbe (-39*C). Madal sulamistemp. metal...
Leelismetallid asuvad IA rühmas (naatrium, kaalium). On aktiivseimad metallid, loovutavad kergesti (võime kasvab ülevalt alla, aatomite mõõtmete kasvu tõttu) väliselt elektronkihilt ainsa elektroni, muutudes väga püsivateks leelismetallide katioonideks laenguga 1+. Väikese elektronegatiivsusega, ühendites on valdavalt iooniline side. Looduses vabalt ei leidu, eelkõige kloriididena. Kõige parem on kindlaks teha kuumutamisel, leegil on iseloomulik värvus. Kerged, pehmed, suhteliselt madala sulamistemperatuuriga. Keemiliselt väga aktiivsed, oksüdeeruvad kiiresti kokkupuutel hapniku (tekib peroksiid, hüperoksiid; need on tugevad oksüdeerijad, süsinikdioksiidiga reageerides eraldavad hapnikku) või veega (moodustavad leelise, tõrjuvad välja vesiniku). Seetõttu hoitakse suletud anumas petrooleumi- või õlikihi all. Nahale tekitavad sügavaid põletushaavu. Naatriumit kasutatakse redutseerijana ning välisvalgustites, liitiumit sulamite koostises n...
Anorgaaniline keemia Iseseisev töö 1. Temperatuuri mõju reaktsiooni kiirusele: temperatuuri tõusmisel reaktsiooni kiirus kasvab. See on tingitud asjaolust, et kõrgemal temperatuuril on aineosakestel suurem energia ja liikumiskiirus. Kontsentratsiooni mõju reaktsiooni kiirusele: mida suurem on reageerivate ainete kontsentratsioon, seda intensiivsemalt eraldub vesinikku, s.t seda suurem on reaktsiooni kiirus. Rõhu mõju reaktsiooni kiirusele: gaasiliste ainete puhul rõhu tõstmisel reaktsiooni kiirus suureneb, kuna rõhu tõstmisel suureneb gaasiliste ainete hulk ruumaalaühikus (s.t nende kontsentratsioon). Peensusastme mõju reaktsiooni kiirusele: mida suurem on reageerivate ainete kokkupuutepind, seda suurem on reaktsiooni kiirus. Katalüsaatori mõju reaktsiooni kiirusele: aktivatsioonienergia vähenemine katalüsaatori juuresolekul ongi reaktsiooni kiirenemise...
1. I A RÜHMA METALLID 1.1 I A rühma metallide üldiseloomustus I A rühma metallideks on liitium, naatrium, kaalium, rubiidium, tseesium ja frantsium. I A rühma metalle nimetatakse ka leelismetallideks. Ajalooliselt tuleneb sõna leelismetall sellest, et nende metallide hüdroksiide tunti juba ammu ja neid nimetati leelisteks. Tänapäevane selgitus võiks olla lihtsalt selline, et nende metallide veega reageerimisel tekivad leelised. Leelismetallid on kõige metalsemad elemendid. Aatomi ehituselt kuuluvad nad s-elementide hulka, kuna nende aatomite välisel orbitaalil on üks elekt- 1 ron. Sellest tulenevalt on kõikide leelismetallide aatomite väliskihi elektronvalemiks ns ja oksüdatsiooniastmeks ühendis +I. Kuna leelismetallidel on väliskihis ainult üks elektron, siis seetõttu nad loovutavad selle ...
Kooli nimiGruppNimi Erinevad metallid Berüllium Magneesium Alumiinium Skandium Titaan Vanaadium Kroom Mangaan Raud Koobalt Nikkel Vask Tsink Metallide keemilised omadused Enamik metalle on keemiliselt aktiivsed. Eriti leelismetallid ja leelismuldmetallid, mis kuuluvad perioodilisustabeli kahte vasakpoolsesse rühma, Keemilise inertsuse tõttu on omamoodi erandiks väärismetallid. Metallide keemilist aktiivsust väljendab nn pingerida, ning enamik metalle tõrjuvad lahjendatud hapetest vesinikku välja Liik ...
Metallide asend perioodilisuse süsteemis ja aatomi ehitus Metallideks nimetatakse metallilisi elemente lihtainetena.Metalle iseloomustab metalne läige, nad on head elektri- ja soojusjuhid ( parim hõbe). Suur osa metallidest on plastilised, neid saab sepistada,valtsida, jne.Kõige plastilisem on kuld.Paljude füüsikaliste omaduste poolest erinevad metallid üksteisest oluliselt Kõvadus: Kroomil 9 (Mohsi järgi) ; tseesiumil 0.2 ( pehme vaha) Sulamistemperatuur: -390 elavhõbedal ; 34100 volframil Tihedus: 0.53 g / cm3 liitiumil ; 22,4 - 22,5 g / cm3 osmiumil ja iriidiumil Mendelejevi tabelis paiknevad metallid Perjoodides - eespool ja rühmades - allpool Kõige aktiivsemad metallid on all vasakul (Cs ja praktiliselt mitteeksisteeriv Fr) kõige aktiivsem mittemetall on ülal paremal - fluor Sinisega on ligikaudu kujutatud ala mille "hõlmavad" metallid, kollasega mittemetallid ja poolmetallid. Silmaga on näha, et metallilisi elemente on märgat...
Metallid praktikas Juba keemiliste elementide perioodilisustabelist võib näha,et kõigi tänaseks tuntud elementide hulgas on ülekaalus metallilised elemendid ehk metallid. Sõltuvalt aatomi ehitusest on metallide rühmadel erinevad üldnimetused: leelismetallid, leelismuldmetallid, siirde-ehk üleminekumetallid, latanoidid, aktionoidid.Metalle liigitatakse ka nende väärtuste põhjal. Osad metallid on väärtuslikumad kui teised. Nii nimetatakse kulda, hõbedat ja kõiki kuut plaatinametalli väärismetallideks. Nende hinnalised omadused on äärmine vastupidavus välistingimustele, vastupidavus oksüdeerijate toimele, kõrge sulamistemperatuur ning kena välimus. Looduses leidub metalle nii lihtainena, kui ka liitainete koostises. Kõiki neid käsitletakse mineraalidena, mis on tekkinud maakoores mitmesuguste füüsikalis-keemiliste protsesside tulemusena. Vähem väärtuslikke metalle on looduses rohkem, kui väärismetalle. N...
LEELISED JA LEELISMULDMETALLID Leelismetallid on IA rühma metallid. Väliskihi elektronvalem ns1-s-metallid. Füüsikalised omadused: · Kerged · Pehmed · Kergsulavad Keemilised omadused: · Reag. veega (leelis + H2) 2Na + 2H2O = 2NaOH + H2 · Reag. hapnikuga 4Li + O2 = 2Li2O (oksiid) 2Na + O2 = Na2O2 (peroksiid) K + O2 = KO2 (hüperoskiid) · Leekreaktsioon muudavad leegi värvust. Na-kollane; K-helelilla Leelismetallide saamine ja kasutamine: Na+ ja K+ reguleerivad rakkude veesisaldust, südametegevust. Taimedele vajalikud kaaliumväetised (KCl, puutuhk). Leelismetallide ühendid: NaOH Seebikivi Seebivalmistamisel Na2CO3 (pesu)...
KEEMIA KT II 1. Leelismetallide üldiseloomustus (omadused), leidumine looduses. *On kõige metallilisemad elemendid. *reageerivad aktiivselt hapnikuga ja enamiku teiste *Pehmed, kergesti lõigatavad, mittemetallidega, *kerged (väikese tihedusega) *reageerivad aktiivselt veega, moodustades vastava leelise ja *madala sulamistemperatuuriga, tõrjudes välja vesiniku, *hea elektri- ja soojusjuhtivusega, *reageerivad tormiliselt hapetega, tõrjudes välja vesiniku. *puhas metallipind on läikiv ja valdavalt hõbevalge värvusega, 2. Tähtsamad Na ja K ühendid ning nende kasutamine. Na ühendid.- küpsetusainetes ja ravimites. *NaNO3- naatriumnitraat- kasutatakse väetisena ...
1.Tähtsamad perioodilised seosed aatomite omadustes. Selgitage, kuidas muutuvad aatomiraadius, ionisatsioonienergia, elektronafiinsus, elektronegatiivsus ja polariseeritavus perioodilisustabelis. · Aatomiraadiused vähenevad perioodis vasakult paremale ja rühmas kasvavad ülalt alla. · Esimesed ionisatsioonienergiad I1 kasvavad perioodis vasakult paremale ja rühmas vähenevad ülalt alla. · Elektronafiinsused Ea on suurimad tabeli paremas ülanurgas (fluor, hapnik). · Aatomite elektronegatiivsused kasvavad perioodis vasakult paremale ja rühmas vähenevad ülalt alla. · Aatomite polariseeritavused vähenevad perioodis vasakult paremale ja rühmas kasvavad ülalt alla. Anioonid on polariseeritavamad kui vastavad aatomid tänu oma suuremale raadiusele. Polariseerivad omadused on intensiivsemad väikese raadiusega ioonidel 2.Selgitage inertpaari efekti mõne näite abil. [Omadus moodustada ioone, mille laeng on 2 võrra väiksem valentselektronide ar...
Keemia Perioodilisustabel ja aatom Lahter- Perioodi rühmad- eemiliste elementide perioodilisussüsteem on süsteem, mis jaotab keemilised elemendid nende tuumalaengute järgi rühmadesse ja perioodidesse. Järjekorra number: Keemilise elemendi aatomnumber ehk järjenumber ehk laenguarv on prootonite arv selle elemendi aatomi tuumas. A-rühma numbrist: Kui aktiivne metall on. Perioodi Number: Mitmendas perioodis asub element, Elemendid: 1.Raud : Fe, 2,Vask: Cu, 3,Jood: I, 4,Broom: Br , 5,Tina: Sn , 6,Plii:Pb 7,hõbe: Ag 8, Broom: Br 9, kuld : Au, 10,Elavhõbe : Hg, 11, tsink: Zn, 12,mangaan : Mn, 13 Kroom Cr 14, Baarium: Ba 15,magneesium : Mg 16,naatrium : Na 17,kaalium : K 18,koobalt : Co 19,titann: Ti 20,alumiinum : Al 21,nikkel : Ni 22, Gallium : Ga 23,Iriidium: Ir 24,Plaatina: pt 25,Rubiidium: Rb 26,plii: Pb 27, Indium : In 28,frantsium : Fr 29,Raadium : Ra 30,Vsimut : Bi 31,Tellur : Te 32, flueo : F ...
12. Metallid Metallideks nimetatakse keemilisi elemente, millel on vabu elektrone ja mis tahkes olekus moodustavad nn metallilise võre, mis annab neile iseloomuliku metallilise läike, hea elektrijuhtivuse ning soojusjuhtivuse ja on ka enamasti hästi sepistatavad. Metallide pingereas aktiivsus suureneb, annavad elektrone kergemini, et positiivseid ioone moodustada, roostetavad kergemini, muutuvad tugevamateks redutseerijateks. 13. Materjalide füüsikalised omadused, nimatage ja iseloomustage neid. Tihedus on füüsikaline suurus, mis näitab aine massi ruumalaühikus. Seda tähistatakse reeglina sümboliga ning mõõdetakse ühikutes kg/m3 (SI-süsteemi põhiühik) või g/cm3. Definitsiooni järgi = m/V Sulamistemperatuur ehk sulamispunkt ehk sulamistäpp on aine temperatuur, mille saavutades hakkab aine sulama või tahkuma. Kui aine on tahkes olekus, algab sulamine, kui aine on vedelas olekus, algab tahkumine. Temperatuuri langedes võib siiski e...
12. Metallid Metallideks nimetatakse keemilisi elemente, millel on vabu elektrone ja mis tahkes olekus moodustavad nn metallilise võre, mis annab neile iseloomuliku metallilise läike, hea elektrijuhtivuse ning soojusjuhtivuse ja on ka enamasti hästi sepistatavad. Metallide pingereas aktiivsus suureneb, annavad elektrone kergemini, et positiivseid ioone moodustada, roostetavad kergemini, muutuvad tugevamateks redutseerijateks. 13. Materjalide füüsikalised omadused, nimatage ja iseloomustage neid. Tihedus on füüsikaline suurus, mis näitab aine massi ruumalaühikus. Seda tähistatakse reeglina sümboliga ρ ning mõõdetakse ühikutes kg/m3 (SI-süsteemi põhiühik) või g/cm3. Definitsiooni järgi ῤ = m/V Sulamistemperatuur ehk sulamispunkt ehk sulamistäpp on aine temperatuur, mille saavutades hakkab aine sulama või tahkuma. Kui aine on tahkes olekus, algab sulamine, kui aine on vedelas olekus, algab tahkumine. Temperatuuri langedes võib siiski...
Keemia teooria Metallide iseloomulikud füüsikalised omadused hea elektri- ja soojusjuhtivus plastilisus ja hea sepistatavus metalne läige enamasti hallikas värvus (hõbevalgest terashallini). Metallide iseloomulikud omadused on tingitud metallilisest sidemest: metallides on aatomite väliskihi elektronid muutunud kõigile aatomitele ühiseks. Füüsikalised omadused, mille poolest metallid üksteisest erinevad tihedus (kergmetallid ja raskmetallid) sulamistemperatuur kõvadus (kõige kõvem on Cr ja pehmed on leelismetallid) värvus (Au kollane, Cu punane, ülejäänud valged või hallid) magnetiseeritavus (Fe, Co, Ni) Igapäevasel kasutatakse enamasti väheaktiivseid või keskmise aktiivsusega metalle, kuna aktiivsed metallid reageerivad tugevalt paljude ainetega. Metallide keemilised omadused 1. Reageerimine lahjendatud hapetega (v.a HNO3) ...
Metallid (T) 1. Selgita mõisteid: metallide pingerida, leelismetallid, leelismuldmetallid, siirdemetallid, väärismetallid, oksüdeerumine, redutseerumine, oksüdeerija, redutseerija, maak, maagi rikastamine, särdamine, elektrolüüs, korrosioon, korrosioonitõrje, keemiline vooluallikas, amfoteerne ühend, sulam. 2. Metallide üldised keemilised omadused: · metallid käituvad keemilistes reaktsioonides alati redutseerijana; · metall on keemiliselt seda aktiivsem (seda tugevam redutseerija), mida kergemini tema aatomid loovutavad väliskihi elektrone; · pingerea kasutamine metallide reaktsioonivõime üle otsustamisel. 3. Vastavate reaktsioonivõrrandite koostamine : Metallide reageerimine · mittemetallidega, · lahjendatud hapetega, · soolalahustega, · veega /veeauruga · leelisega 4. Metallide korrosioon: metallide korrodeerumise põhjus, keemilise ja elektrokee...
Metallid Leidumine: 4/5 elementidest on metallid. Enamlevinud on Al, Fe, Ca, Na, K, Mg. Ehedana leidub väheaktiivseid metalle: Cu, Hg, Ag, Au, Pt, enamuses metallidest leiduvad ühenditena maakide koostises. Maagid võivad olla oksiidsed(Fe2O3, Al2O3), sulfiidsed( Cu2S, HgS, FeS2), kloriidsed ( NaCl, KCl), karbonaatsed, ... jt.sooladena. Aatomi ehitus ja paiknemine per. süsteemis: Per. süsteemis- vasakul all; väliskihis 1-3 elektroni, aatomiraadius suhteliselt suur; elektronegatiivsus suhteliselt väike; loovutavad elektrone; on redutseerijad; ühendites omandavad positiivse oksüdatsiooniastme. Metalliline side: Metallioonide ja "vabade elektronide" vaheline side. Füüsikalised omadused: Üldised: hea elektri .ja soojusjuhtivus, metalliline läige, plastilisus. Erinevused: 1. Läige ja peegeldumisvõime (sile poleeritud pind): parimad peegeldusvõimelt hõbe(Ag). alumiinium(Al), kul...
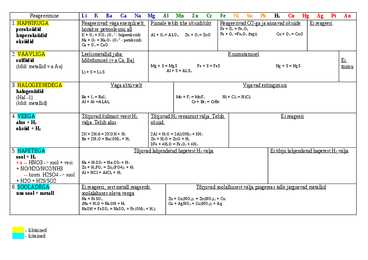
Reageerimine Li K Ba Ca Na Mg Al Mn Zn Cr Fe Ni Sn Pb H2 Cu Hg Ag Pt Au 1. HAPNIKUGA Reageerivad väga energiliselt, Pinnale tekib tihe oksiidikiht Reageerivad O2-ga ja annavad oksiide Ei reageeri peroksiidid hoitakse petrooleumi all Fe + O2 = Fe2O3 hüperoksiidid K + O2 = KO2 (O2-1 - hüperoksiid) Al + O2 = Al2O3 Zn + O2 = ZnO Fe + O2 =Fe3O4 (tagi) Cu + O2 = CuO oksiidid Na + O2 = Na2O2 (O2-2 - peroksiid) Ca + O2 = CaO 2. VÄÄVLIGA Leelismetallid juba Kuumutamisel sulfiidid hõõrdumisel (v.a Ca, Ba) ...
Metallid konspekt Metallide füüsikalised omadused · Läige- metallidel on iseloomulik läige ja peegeldusvõime, mis avaldub pärast metalli poleerimist. Parema peegeldusvõimega on Ag, In, Al, Rh, Pd. Metallide füüsikalised omadused · Värvus- enamik metalle on hõbevalged, Cu- roosakspunane, Au- kollane, Zn-sinakasvalge Metallide füüsikalised omadused · Plastilisus ja haprus- enamik metalle on plastilised, eriti plastiline on Au. Haprad metallid on Sb, Mn, Ru. Metallide füüsikalised omadused · Kõvadus- Leelismetallid, Sn, Pb ja Au on pehmed. Kõige kõvem metall on Cr. Kõvadus sõltub metalli töötlusest ja puhtusest. Metallide füüsikalised omadused · Sulamistemperatuur- selle alusel liigitatakse metallid kerg- ja rasksulavateks metallideks. Piiriks on 1000o C. Kõige madalama sulamistemperatuuriga on Hg (- 38o C ) ja kõrgema sulamistemperatuuriga W (3410o C ). Metallide füüsikalised omadused...
Kordamisküsimused (kasuta vastamisel ka tabeli abi) 1) Selgita mõisteid: leelis: vees hästilahustuv tugev alus (hüdroksiid) redutseerumine: elektronide liitumine redoksreaktsioonis, elemendi o.a- vähenemine sool: kristalne aine, mis koosneb aluse katioonidest ja happe anioonidest redutseerija: aine, mille osakesed loovutavad elektrone, ise oksudeerub oksüdeerumine: elektronide loovutamine redoksreaktsioonis, elemendi o.a- suurenemine leelismuldmetall: IIA rühma elemendid katioon: positiivse laenguga ioon korrosioon: metalli hävimine (oksüdeerumine) keskkonna toimel Metall oksüdeerub keskkonnas oleva oksüdeerija toimel metalliühendiks (loovutab elektrone) oksüdeerija: aine, mille osakesed liidavad el...
Aatomnumber: 19 Aatommass: 39,098 Klassifikatsioon: leelismetallid, s-elemendid Aatomi ehitus: · Elektronvalem: 1s2 2s2p6 3s2p6 4s1 · Elektronskeem: +19|2)8)8)1) · Elektronite arv: 19 · Neutronite arv: 20 · Prootonite arv: 19 · Oksüdatsiooniast(m)e(d) ühendites: 0, I · Kristalli struktuur: ruumikeskne kuubiline Füüsikalised omadused: · Aatommass: 39,098 · Sulamistemperatuur: 63,25 °C · Keemistemperatuur: 759,9 °C · Tihedus: 0,862 g/cm3 · Värvus: hõbevalge · Agregaatolek toatemperatuuril: tahke · Kõvadus Mohsi järgi: 0,4 · Isotoobid: Nukliid Levimus (%) Mass Poolestusaeg 39 K 93,22 38,9637 - 40 K 0,118 39,974 1,28 · 109 aastat 41 K 6,77 40,9618 ...
Kordamisküsimused: Aatomi ehitus ja perioodilisussüsteem 8. klass 1) Mis on aatom ja millest ta koosneb? 2) Mille poolest võivad aatomid üksteisest erineda? 3) Mis on aatommass? 4) Millest koosneb aatomituum ja kui palju on see aatomist väiksem 5) Miks moodustab aatomituum põhilise osa aatomimassist? 6) Mida nimetatakse tuumalaenguks ja põhjenda miks ta on alati positiivne? 7) Iseloomusta elektroni, prootoni, neutroni (kus asub, mis laenguga on, nende mass võrreldes teiste aatomis olevate osakestega jne.) 8) Mida nimetatakse on elektronkihiks, väliseks elektronkihiks, elektronkatteks ja elektronpilveks. 9) Põhjenda, miks on aatom elektriliselt neutraalne? 10) Mida nimetatakse elementaarlaenguks (näited)? 11) Mida nimetatakse elementaarosakesteks (näited)? 12) Selgita mõistet: planetaarne aatomimudel. 13) Milliseid elemente tundsid alkeemikud? 14) Keemilise elemendi mõiste ja mitu neid...
CnH2·+1OH . Metanool(puupiiritus)- CH3OH üks lahustite koostisosi keemiatööstuses, etanoolist välimuselt eristamatu. Etanool (piiritus)C 2H5OH tähtis lahusti ja sünteeside lähteaine, valm eteeni katalüütilisel hüdraatimisel või sahhariidide kääritamisel. Glütseriin- Magus, viskoosne vedelik, seguneb hästi veega, pole mürgine, keemiliselt seotuna kuulub rasvade koostisse, kosmeetikas nahapehmendajana. Puskariõli on destillatsioonijääk etanooli eraldamisel käärimissegust, koosneb kahest pentanooli isomeerist. Põlemine- C2H5OH + 3O2 = 2CO2 + 3H2O. Oksüdeerumine(tekib aldehüüd: CHO)- 2C2H5OH + O2 = 2CH3CHO + 2H2O. Reag. Leelismetallidega(tekivad alkoholaadid)- 2C2H5OH + 2Na = 2C2H5ONa + H2. Alkoholaatide hüdrolüüs- C2H5ONa + H2O = C2H5OH + NaOH. Füüsilised omadused: Lihtsamad suht kõrgete keemistº ja vees hästi lahustuvad, molekulmassi kasvuga ...
Liitium Üldine/aatomi ehitus Lühend: Li Elektronskeem: + 3| 2)1) Aatominumber: 3 Elektronide arv: 3 Aatommass: 6,941 Prootonite arv: 3 Kuuluvus: leelismetallid Neutronide arv: 4 Füüsikalised omadused Liitium see hõbevalge/hallika värvusega suhteliselt pehme leelismetall on kõige väiksema tihedusega metall üldse. Tema tihedus on 0,535 g/cm³, mis teeb liitiumist ka kõige väiksema tihedusega normaaltingimusel tahke aine. Olles erakordselt kerge metall on ta viis korda kergem kui alumiinium ning kaks korda kergem kui vesi. Sellepärast on liitium võimeline ujuma isegi petrooleumis. Tema sulamistemperatuur on 180,54 °C ning keemistemperatuur 1342 °C. Agregaatolek tavatingimustel on tahke. Võrreldes teiste leelismetallidega on liitium väiksema tihedusega ning kõrgema s...
Rubiidium Ettekanne Kristina Hertmann 10K Juhendaja : Anna Perova Üldiseloomustus Aatominumber: 37 Aatomimass: 85,4678 Klassifikatsioon: Leelismetallid, s-elemendid Aatomi ehitus: · Elektronvalem: 1s2 2s2p6 3s2p6d10 4s2p6 5s1 · Elektronskeem: +37|2)8)18)8)1) · Elektronite arv: 37 · Neutronite arv: 48 · Prootonite arv: 37 · Oksüdatsiooniast(m)e(d) ühendites: 0, I · Kristalli struktuur: ruumikeskne kuubiline Avastamine: R.W. Bunsen & G.R. Kirchoff, 1861, Heidelberg, Saksamaa Avastati see mineraal lepidokrokiidist, kasutades spektroskoopi. Nimi rubiidium tuleneb ladina keelsest sõnast "ruber", mis tähendab sügavpunast. Sellist nime põhjustasid rubiidiumi erepunased spektroskoopilised jooned. Leidumine looduses Rubiidiumi (Rb) puudust looduses ei ole. Teda leidub rohkem kui kulda, hõbedat või tina jne. Rubiidium kuulub kohekümne kolme kõige ...