2,70927 0,00798 0,000008676 Töö nr. 6 2,781037 0,008073 0,000008426 2,881955 0,008176 8,0479E-006 FK laboratoorne töö nr.6 y x·y x2 = s PUHTA VEDELIKU KÜLLASTATUD AURURÕHU 17,87525 0,054078 6,4947E-005 MÄÄRAMINE DÜNAAMILISEL MEETODIL Arvutused 1) arvutatakse empiirilise võrrandi logp = A + B*1/T koefitsiendid A ja B a) kui saadud logaritmilise graafiku sirge algordinaat ja tõus, y = -1642,2x + 7,549 A=7,549 B=-1642,2 b) vähimruutude meetodil; x 2y-xyx A=7,549 A= nx 2- ( x )2
Kuna sedimentatsiooni kiirus kahaneb aja jooksul, võetakse esimesed lugemid iga 20 sekundi järel, katse lõpul 10-15 minuti järel. Katse lõpetatakse kui 10 minuti jooksul massi juurdekasv on väiksem kui 2-3mg. Märgitakse üles kaalukausi sukeldussügavus, katseandmed kantakse tabelisse. Katseandmete põhjal joonestatkse graafik P=f(t) ja arvutatakse osakeste integraalne- ja diferentsiaalne jaotuskõver. Teoreetiline põhjendus, valemid: KATSEANDMED JA ARVUTUSED Kaalukausi kaal vees P= 195mg Kaalukausi sukekldussügavus H= 10,3 cm 0,7% suspensioon savipulbrist vett 273 ml ja savipulbrit 1,911g savi = 2,2 g/cm3 Tabel Katseandmed Sademe mass Lugemi Aeg katse Skaala näit P=P'-Po nr algusest t (s) P' (mg) 1. 10 200 5 2. 30 204 9 3
Kuna sedimentatsiooni kiirus kahaneb aja jooksul, võetakse esimesed lugemid iga 20 sekundi järel, katse lõpul 10-15 minuti järel. Katse lõpetatakse kui 10 minuti jooksul massi juurdekasv on väiksem kui 2-3mg. Märgitakse üles kaalukausi sukeldussügavus, katseandmed kantakse tabelisse. Katseandmete põhjal joonestatkse graafik P=f(t) ja arvutatakse osakeste integraalne- ja diferentsiaalne jaotuskõver. Teoreetiline põhjendus, valemid: Katseandmed ja arvutused: Kaaluklaasi kaal vees P0 = 195 mg Kaaluklaasi sukeldussügavus H = 10,3cm=0,103m Lugemi nr Aeg katse algusest t Skaala näit P' Sademe mass P=P'-P0 (mg) (s) 1 10 200 5 2 30 204 4 3 50 208 4
spetsialiseeru otsene näitaja misnäitaja mahunäitaja mahunäitaja Teravilja müügi Segavilja osakaal Segavilja Kasvupind jrk saagikus, kg/ha kogumüügist toodang, kg kokku, ha X1 X2 X3 X4 1 3148,148148148 1 68 000 178,90 2 2238,938053097 0,3082771129 50 600 124,91 3 1700 0,440320407 35 700 376,00 4 3007,692307692 0,0376854187 39 100 763,00 5 2304 0,5555555556 28 800 51,00 6 3098,591549296 0,4973633043 22 000 351,10 7 2000 0,113773135 4 000 26,40 8 1823,529411765 0,5131964809
TTÜ materjaliteaduse instituut Füüsikalise keemia õppetool KYF0080 Füüsikaline ja kolloidkeemia Laboratoorne Töö pealkiri: töö nr: 16 FK Konduktomeetriline tiitrimine Töö teostaja: Õpperühm: Õppejõud: Töö teostatud: Protokoll esitatud: Protokoll K. Lott 14.03.2001 21.03.2011 arvestatud: Töö ülesanne Töös tiitritakse tugeva leelisega kas nõrka ja tugevat hapet või hapete segu. Tiitrimise ekvivalentpunkt määratakse graafiliselt lahuse elektrijuhtivuse mõõtmiste alusel. Töö teoreetilised alused Konduktomeetrilisel tiitrimisel määratakse ekvivalentpunkt elektrijuhtivuse muutuse järgi, mis on tingitud ühtede ioonide asendamisest teistega. Konduktomeetrilisel tiitrimisel määratakse ekvivalentpunkt elektrijuhtivuse muutuse järgi, mis on tingitud ühtede ioonide asendumisest teistega. Soolhappe tiitrimise
Juhtivusnõu loputatakse uuritava lahusega ja seejärel täidetakse sama lahusega nii, et elektroodid oleks kaetud vähemalt 1 cm paksuse lahuse kihiga. Juhtivusnõu asetatakse termostaati ja loksutatakse selles umbes minut püsiva temperatuuri saavutamiseks. Juhtivusmõõtja annab väljundi voltides, mis tuleb teisendada millisiimensiteks arvestusega, et 1 V vastab 5 mS-ile. Katseandmete töötlemine. Kuna uuritav reaktsioon on esimest järku, siis tehakse arvutused vastavalt võrrandile 1 c0 k = ln t c 0 - cx kus k - reaktsiooni kiiruskonstant, co - etaanhappe anhüdriidi algkontsentratsioon, co-cx - etaanhappe anhüdriidi kontsentratsioon ajamomendil t reaktsiooni algusest, cx - ajamomendiks t ärareageerinud anhüdriidi kontsentratsioon, t - aeg reaktsiooni algusest, min.
TTÜ Materjaliteaduse instituut füüsikalise keemia õppetool Töö nr Töö pealkiri 24f Etaanhappe anhüdriidi hüdratatsiooni kiiruse määramine elektrijuhtivuse meetodil Üliõpilase nimi ja eesnimi Õpperühm Reimann Liina KATB41 Töö teostamise Kontrollitud: Arvestatud: kuupäev: 18.03.2015 Töö ülesanne: Lahjendatud vesilahuses kulgeva esimest järku reaktsiooni (CH3CO)2O + H2O = CH3COOH kiiruskonstandi määramine. Reaktsiooni kineetikat uuritakse elektrijuhtivuse mõõtmise teel, mis lubab reaktsiooni pidevalt jälgida proove võtmata. Süsteemi elektrijuhtivus kasvab ajas oluliselt etaanhappe (äädikhappe) moodustumise tõttu. Katse käik. Termostaat reguleeritakse juhendaja poolt antud temperatuurile. Termostaati asetatakse 100-ml kolb dest
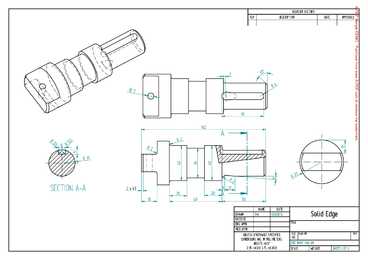
A-PDF Merger DEMO : Purchase from www.A-PDF.com to remove the watermark REVISION HISTORY REV DESCRIPTION DATE APPROVED 2 45 ° R4 O7 48 142 A R0







Kõik kommentaarid