Veredoonorlus Doonorlus on ülimalt oluline tegevus. Inimverd ei suuda miski täielikult asendada. Vere loovutamine on seega ainulaadne ja väga oluline abinõu, mis aitab päästa elusid. Seda nimetatakse veredoonorluseks. Prantsusmaal saab igal aastal vereülekandest abi 500 000 patsienti. Verevõtmise vahendid on steriilsed ja ühekordselt kasutatavad (süstlad, voolikud, kotid). Vereandmisega ei kaasne mingeid riske. Vere loovutamine :re loovutamine: Tegemist on kõige levinuma doonorlusviisiga, mis kestab 45 minutist 1 tunnini. Doonorilt võetakse 450 ml verd. Natuke verd võetakse ka analüüsimiseks ja kontrollimiseks. - Mehed võivad verd anda viis korda, naised aga kolm korda aastas. - Doonoriks võivad olla inimesed vanuses 1865 aastat. Eelmisest vereloovutusest peab olema möödunud vähemalt 8 nädalat. Kes saab/ei saa olla doonor? Kõigepealt tahetakse doonoriks võtta õde või venda ja tõenäosus et ta sobib
1) Selgita mõisteid: leelis: vees hästilahustuv tugev alus (hüdroksiid) redutseerumine: elektronide liitumine redoksreaktsioonis, elemendi o.a- vähenemine sool: kristalne aine, mis koosneb aluse katioonidest ja happe anioonidest redutseerija: aine, mille osakesed loovutavad elektrone, ise oksudeerub oksüdeerumine: elektronide loovutamine redoksreaktsioonis, elemendi o.a- suurenemine leelismuldmetall: IIA rühma elemendid katioon: positiivse laenguga ioon korrosioon: metalli hävimine (oksüdeerumine) keskkonna toimel Metall oksüdeerub keskkonnas oleva oksüdeerija toimel metalliühendiks (loovutab elektrone) oksüdeerija: aine, mille osakesed liidavad elektrone (ise redutseerudes)
endas palju sündmusi, nii häid kui ka halbu. Rootsi ajast on räägitud justkui heast ajast, kuid sellele ei saa minu meelest otseselt vastata. Kui mõisad redukteeriti ehk vabastati riigi kätte läinud mõisade talupojad pärisorjusest, siis vaatamata sellele, et see muutis talupoegade tingimusi teatud määral paremaks, kaasnes sellega ka halba. Kui enne oli talupoegade kohustusteks abiteod, mis olid erinevad hooajalised tööd, rahalised koormised, naturaalandamite loovutamine mõisnikele ja nad olid sunnismaised, siis peale reduktsiooni nende õigusi suurendati. Vaatamata sellele, et alguses said talupojad vakuraamatu abil mõisniku peale kaevata, maksid hiljem mõisnikud riigile selle eest, et nad oleks niiöelda süüst vabad ning seetõttu jäid ka talupjad enamasti süüdlasteks. Seega eksisteeris ka korruptsioon, mis talupoegade suhtes oli väga ebaaus. Suur roll oli usul, nimelt luteri usul. Kõik teised usud ning tõekspidamised olid
Alus: on keemiline aine, mis annab lahusesse hüdroksiidioone. Sool: on kristalne aine, mis koosneb metalli (aluse) katioonidest (näiteks Ca 2+) ja happe anioonidest Indikaator: eriline aine , mis muudab värvust lahusele happe või aluse lisamisel(värvus sõltub pH väärtusest). Keemiline reaktsioon: Aine muundumine teisteks aineteks . Redoksreaktsioon: (ehk redutseerumis.oksüdeerumisreaktsioon) keemiline reaktsioon, millega kaasneb elektronide liitmine ja loovutamine ning elementide oksüdatsiooniastme muutus. Redutseerija: on element, mis redoksreaktsiooni käigus loovutab elektrone(ise oksüdeerub). Oksüdeerija: on aine, mis redoksreaktsiooni käigus liidab endaga elektrone(ise redutseerub). Redutseerumine: elektronide liitumine redoksreaktsioonis, sellele vastab oksüdatsiooniastme vähenemine Oksüdeerumine: elektronide loovutamine redoksreaktsioonis, sellele vastab oksüdatsiooniastme suurenemine
X seminar Isikute vahetumine, isikute paljusus võlasuhtes. Kolmandad isikud võlasuhtes 1. Vald sõlmis ehitusettevõtja U ehitustöövõtulepingu koolimaja laiendamiseks 400 000 euro eest. Lepingus oli klausel, mille kohaselt oli lepingutasu nõude loovutamine keelatud. U oli enne töövõtulepingu sõlmimist tarnija käest omandireservatsiooniga soetanud 150 000 euro eest ehitusmaterjali. Lepingu kohaselt oli ehitusmaterjali ostjal (U) õigus püsivalt ühendada kinnisasjaga vaid juhul, kui sellest tulenevad nõuded loovutatakse tarnijale L. Seepärast oli müügilepingus sätestatud, et materjali püsival ühendamisel võõra kinnisasjaga loetakse kaupade
Oksiid liitaine, mille üks element on hapnik põlemisreaktsioon ühinemisreaktsioon hapnikuga Redoksreaktsioon keemiline reaktsioon, millega kaasneb eletronide liitmine ja loovutamine ning elementide oksüdatsiooniastme muutus. oksüdatsiooniaste arvutuslik suurus, mis näitab elemendi oksüdeerumise astet ühendis. Oksüdeerija aine, mille osakesed liidavad elektrone(ise redutseerudes) redutseerija aine, mille osakesed loovutavad elektrone (ise oksüdeerudes) Redutseerumine elektronide liitmine redoksreaktsioonis. O-A väheneb oksüdeerumine elektronide loovutamine redoksreaktsioonis. O-A suureneb.
Mittekalaletungi lepin 10 aastaks;cSalajane sisu: Ida-Euroopa jagamine Liitlased FRA, ENG, RUS&NSVL(1941) Lääneliitlased GER, ITA, JAP Holokaust (eluta ja elusa looduse täielik hävitamine põletamise teel) Hävitati: juute, slaavlasi, mustlasi Getod; Koonduslaagrid ;Hävituslaagrid (Auschwitz, Treblinka);Meditsiinilised katsed ;Tapmine (vt tabelit lk 100):Gaasikamber:Mahalaskmine Sõja lõpp- sakslaste järk-järguline lüüa saamine : Territooriumite loovutamine (NSVL ja Baltimaad, hiljem Poola ja Balkani poolsaar;:Poolt vahetasid Rumeenia, Bulgaaria, Soome;Normandia dessant ehk Teise rinde avamine (Inglise, Kanada, Usa väed Dwight Eisenhoweri juhtimisel) Sakslased üritasid küll meeleheitlikku vastupanu, kuid see ei aidanud -reaktiivlennukid a) V 1 b) V 2 c) Mobilisatsioon (16-60 eluaastani) Saksamaa kapituleerub 8. mai 1945 - Jaapani lüüsaamine; Territooriumite loovutamine ()
korral jääb osa koormaruumist kasutamata. 5) kauba virnastamine alusel, 6) aluse kaal( tõstuki tõstejõud, riiuli kandevõime, veoviis,aluse tüüp ja kvaliteet) 7) kauba stabiilsus alusel- kaup ei tohi kõikuda ja peab olema kindlalt. 29. Laotöö toimingud ja operatsioonid. Kauba mahalaadimine ja vastuvõtualale paigutamine. Laotöö toimingud on: vastuvõtt, hoiukohtadele paigutamine,siirdamine,komplekteerimine, konsolideerimine, pakkimine,loovutamine,inventeeriine,veokorraldus,töö infosüsteemis ja muu kontoritöö.Kauba vastuvõtt algab mahalaadimisega veovahendilt või veoühikult ning paigutamisega vastuvõtualale. Selleks et saabunud kaup poleks võimalik nõuetekohaselt koguseliselt ja koosseisuliselt üle kontrollida on vaja paigutada kaup vastuvõtualale sorteerituna eraldi erinevate artiklite kaupa. Vastuvõtukontroll järgneb mahalaadimisele. On olemas kaks erinevat vastuvõtmisviisi: tavapärane kontrollimine ja erikontrollimine
obligationes ex contractu lepingust tulenev obligatsioon e võlasuhe obligationes quasi ex contractu nagu lepingust tulenev obligatsioon e võlasuhe negotiorum gestio käsundita asjaajamine bona fides hea usk mala fides pahauskus creditor kreeditor, võlausaldja; õigustatud pool obligatsioonis debitor deebitor, võlgnik; kohustatud pool obligatsioonis novatio uuendus, muutmine; ühe võlaõigusliku suhte asendamine teisega nii, et esimene kaob cessio tsessioon; loovutamine (nõudeõiguse loovutamine uuele kreeditorile, kreeditoride vahetus obligatsioonis) dare ; facere Obligatsiooni objektiks võib olla mitmesugune samme. Roomlastel olid need sammed liigitatud järmiselt: dare midagi andma; facere midagi tegema; praestare solutio täitmine; lahendus; tasumine conditio tingimus; nõue; seisund; olukord vis maior vääramatu jõud mora viivitus, viivitamine; peatus; vaheaeg
arrha käsiraha 35. locatio conductio üür-rent 36. mandatum korraldus, käsund 37. societas seltsinguleping 38. permutatio vahetus 39. obligationes ex contractu lepingust tulenevad obligatsioonid 40. obligationes quasi ex contractu nagu lepingust tulenevad obligatsioonid 41. negotiorum gestio käsundita asjaajamine 42. bona fides hea usk 43. mala fides paha usk 44. creditor võlausaldaja 45. debitor võlgnik 46. novatio uuendus, muutmine 47. cessio loovutamine 1 48. dare andma 49. facere tegema 50. solutio täitmine 51. conditio tingimus 52. vis maior vääramatu jõud 53. mora viivitus 54. res asi 55. dominium omand; omandiõigus 56. proprietas omadn; omandiõigus 57. possessio valdus 58. traditio vormivaba üleandmine 59. res mobiles liikuvad ehk vallasasjad 60. res immobiles liikumatud ehk kinnisasjad 61
Keemia KT kordamine 1. Oksüdeerija aine, mille osakesed liidavad elektrone Redutseerija aine, mille osakesed loovutavad elektrone Redutseerumine elektronide liitmine redoksreaktsioonis , oksüdatsiooniaste väheneb Oksüdeerimine elektronide loovutamine redoksreaktsioonides, oksüdatsiooniaste kasvab Redoksreaktsioon keemiline reaktsioon, millega kaasneb elektronide üleminek ja elementide oksüdatsiooniastme muutust 2. Mõiste kasutamine ja määramine ! 3. Vesiniku saadakse vee elektrolüüsil , vesinukku kogutakse ...... , 4. Vesiniku omadus 5. Veeomadused : värvuseta , lõhnatu , maitseta 6. Lahuse koostise arvutamine , valemite kasutamine .
sellise maksevahendi, võib ta nõuda kohustuse täitmist rahas üksnes juhul, kui maksevahendit ei lunastata. Kui võlausaldajal on õigus keelduda oma kohustuse täitmisest kuni rahalise kohustuse täitmiseni, võib ta keelduda oma kohustuse täitmisest, kuni maksevahend on lunastatud. Rahalise kohustuse täitmisel posti teel loetakse kohustus täidetuks raha võlausaldajale väljamaksmisest alates. 15. Nõude loovutamine. Võlgnikule teatamine. Piirangud nõude loovutamisel. Kohustis ja käsutustehingu eristamine nõude loovutamisel. Võlausaldaja võib oma nõude võlgniku nõusolekust sõltumata anda lepingu alusel tervikuna või osaliselt üle teisele isikule (nõude loovutamine). Nõuet ei või loovutada, kui loovutamine on seadusest tulenevalt keelatud või kui kohustust ei saa selle sisu muutmata täita kellelegi teisele kui senisele võlausaldajale
oksüdeerumine on elektronide loovutamine. oksüdeeruda võivad ained, mille aatomid hoiavad oma väliskihi elektrone nõrgalt kinni. oksüdeeruja redutseerib e liidab elektrone. nt. Cl (Z= 17) +17/ 2) 8) 7), liidab 1 elektroni, (liidab nii palju elektrone, et viimasel el-kihil oleks 8 el.) S (Z= 16) +16/ 2) 8) 6), liidab 2 elektroni. redutseerija oksüdeerub e loovutab elektrone. nt. Na (Z= 11) +11/ 2) 8) 1), loovutab 1 elektroni, (loovutab nii palju elektrone, kui on tal viimasel el-kihil.) Ca (Z= 20) +20/ 2) 8) 8) 2), loovutab 2 elektroni.
reaktsiooni ei toimu. Metallide keemilised omadused Metallide reageerimine sooladega Metalli ja soola vaheline reaktsioon toimub, siis kui eraldi seisev metall on pingereas enne seda metalli, mis on soola koostises. Reaktsiooni ei toimu Metallid kui redutseerijad Oksüdeerumine- Elektronide loovutamine, o.a. Kahaneb. Redutseerija. Redutseerimine- Elektronide liitmine, o.a. Kasvab. Oksüdeerija.
Mõisted: redoksreaktsioon keemiline reaktsioon, milles toimub elektronide üleminek ühtedelt osakestelt teistele; sellega kaasneb elementide o-a muutus redutseerija aine, milles osakesed loovutavad elektrone (ise oksüdeerudes) oksüdeerija aine, milles osakesed liidavad elektrone (ise redutseerudes) oksüdeerumine elektronide loovutamine redoksreaktsioonis, elemendi o-a suurenemine redutseerumine elektronide liitmine redoksreaktsioonis, elemendi o-a vähenemine sulam mitmest metallist või metallist ja mittemetallist koosnev metalliliste omadustega materjal, saadakse koostisainete kokkusulatamisel maak maavara, mida on võimalik kasutada metallide või teiste ainete tootmiseks alumiinotermia maagist metalli kättesaamine aktiivsema metalli abil
PM3A RINGEELUNDKOND Ringeelundkonna moodustavad : süda, veresooned ning nendes ringlev veri. Vereringe jaguneb kaheks: suur vereringe ehk kehavereringe ning väike vereringe ehk kopsuvereringe. SÜDA Suur vereringe algab vasakust südame vatsakesest. Sealt paisatakse hapniku rikas veri aorti. Aordist liigub veri arterite ja arterioolide kaudu kõigi kudedega seotud kapillaaride ehk juussoonte võrgustikku. Seal toimub hapniku loovutamine läbi kapillaaride seinte kudedele ning süsihappegaasi, kusihappe ja teiste ainevahetusjääkide vastuvõtmine. Jääkaineterikas venoosne veri liigub kapillaaride venoossest osast peenikestesse veenulitesse, mis omakorda ühinevad ülemiseks ja alumiseks õõnesveeniks, mis suubuvad südame paremasse kotta. Väike verer inge Väike vereringe algab südame paremast vatsakesest, millest süsihappegaasirikas veri kopsuarterisse surutakse.
Venemaa peamised poliitilised jõud ja nende eesmärgid 1917. Aastal: *Rahva Vabaduspartei (kadetid)-demokraatlik vabariik *Sotsialistid-revolutsionäärid(esseerid)-talurahvas,sotsialistlik riik *Venemaa Sotsiaaldemokraatlik Tööliste Partei(mensevikud)-linnatöölised,haritlased *VSDTP marksistlik suund(bolsevikud)-proletariaadi partei II nõukogude kongressi otsused: *Rahudekreet *Maadekreet *Rahvakomissaride nõukogu Versailles rahulepingu tingimused: *Sõjasüü *Elsass-Lotringi loovutamine *Alade loovutamine uutele riikidele *Sõjaväe suurus kuni 100 000 meest *Laevastiku piiramine *Reparatsioonid *Reini jõe demilitariseeritud tsoon I Maailmasõja tagajärjed: *Suur inimohvrite arv *Kadunud põlvkond *Uute rahvusriikide teke *Jõudude vahekord
res publicae – riigile kuuluvad ehk avalikuks kasutamiseks mõeldud asjad res privatae – eraomanikele kuuluvad asjad res corporales – kehalised asjad res incorporales – kehatud asjad res mancipi – mantsipeeritavad ehk piduliku võõrandamistehingu (mancipatio) teel üleantavad asjad res nec mancipi – mittemantsipeeritavad ehk vormivaba üleandmise (traditio) teel võõrandatavad asjad ex causa- põhjusel, tõttu in iure cessio- omandiõiguse loovutamine kohtus dominium, ii n- omand, omandiõigus usucapio, onis (usucapionis) f- igamine ad inquirendam- otsimiseks
maksevahendi vastuvõtmisest alates. Kui võlausaldajal on õigus keelduda oma kohustuse täitmisest kuni rahalise kohustuse täitmiseni võlgniku poolt ja ta on kohustuse täitmisena vastu võtnud käesoleva paragrahvi lõikes 4 nimetatud maksevahendi, võib ta keelduda oma kohustuse täitmisest, kuni maksevahend on lunastatud. Rahalise kohustuse täitmisel posti teel loetakse kohustus täidetuks raha võlausaldajale väljamaksmisest alates. 15. Nõude loovutamine. Võlgnikule teatamine. Piirangud nõude loovutamisel. Kohustis ja käsutustehingu eristamine nõude loovutamisel. Nõude loovutamine Võlausaldaja võib oma nõude võlgniku nõusolekust sõltumata anda lepingu alusel tervikuna või osaliselt üle teisele isikule (nõude loovutamine). Nõuet ei või loovutada, kui loovutamine on seadusest tulenevalt keelatud või kui kohustust ei saa selle sisu muutmata täita kellelegi teisele kui senisele võlausaldajale.
HNO3 NO3 Nitraat ioon Sool ja nitraat Kui soola koostises on muutuva oksuldatsiooniastmega metall siis öeldakse OKA sisse. (muutuad metallid on : raud, tina, vask, kroom) Mõisted: 1. Aluselised oksiidid Alusele vastav oksiid 2. Anioon Negatiivse laenguga ioon 3.Hape Aine mis annab lahusesse vesinikioone 4.Sool Kristalne aine, mis koosneb (aluse) katioonidest ja (happe) anioonidest 5.Redutseerimine Elektronide liitmine. 6.Oksüdeerimine elektronide loovutamine, sellele vastab elemendi oksüdatsiooni astme suurenemine 7. Leelis Vees lahustuv tugev alus (hüdroksiid) Soolade Füüsikalised Omadused : 1) Tahked 2) Erinev värvus (põhiliselt valge) 3) Vees lahustuv on ka erinev ( vaata lahustuvus tabelist) Soolade Keemilised Omadused : 1. Sool + Alus (mõlemad peavad olema lahustuvad) ja üks saadustest peab olema sade 2. Soolad reageerivad tugevamate hapetega 3. SOOL + HAPE = UUS SOOL + UUS HAPE
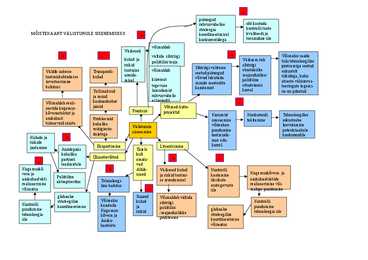
asukohast Probleemid osasaamise tekitamine oskusteabe tulenevaid sääste kohalike võimaluse loovutamine Välisturule müügiesin- puudumine potentsiaalsele sisenemine dajatega tootmisük- konkurendile
Hape aine, mis annab lahusesse vesinikioone Oksiid aine, mis koosneb kahest elemendist, milleks üks on hapnik Alus aine, mis annab lahusesse hüdroksiidioone Sool kristalne aine, mis koosneb katioonidest ja anioonidest Elektrolüütiline dissotsiatsioon ioone sisaldavate lahuste tekkeprotsess elektrolüütide lahustumisel vees Hüdraatumine vee molekulide seostumine ioonidega Hüdrolüüs reageerimine veega Oksüdeerumine(redutseerija) elektronide loovutamine Redutseerumine (oksüdeerija) elektronide liitmine Redoksreaktsioon reaktsioon, mille käigus muutub elementide o.-a Korrosioon metalli hävimine keskkonna mõjul Keemiline vooluallikas e galviaanielement toodetakse energiat..mindfuck (vastupidine elektrolüüsile) Elektrolüüs redoksreaktsioon, mis toimub elektrolüüdi lahuses või sulas elektrolüüdis elektrootide pinnal elektrivoolu toimel Maagi rikastamine lisanditest puhastamine !!! Fe, Cu, Al
osasse investeeritud summa suurusega. EELISED: Piiratud vastutus Piiramatu eluiga Suuremad ressursid Suhteliselt väike nõutav algkapital Suhteliselt kerge juhtida PUUDUSED: Raamatupidamine keerukam Juriidiline abi osaühingu loomisel MTÜ- Mittetulundusühing- eesmärgiks või põhitegevuseks pole kasumi teenimine majandustegevuse kaudu. FAKTOORING - on ostjatelt laekumata arvete loovutamine, et tagada vajalikul hetkel vaba raha. SIHTASUTUS- eraõiguslik juriidiline isik, mida iseloomustab vara valitsemine ja kasutamine põhikirjaliste eesmärkide saavutamiseks. ( Ei teeni tulu ) PIIRATUD VASTUTUS- Aktsiaseltsi eelis, mis paneb aktsinärile vastutuse ettevõtte võlgade eest üksnes aktsiaseltsi investeeritud rahasumma ulatuses. PIIRAMATU VASTUTUS- Nõudmin, et omanik või omanikud vastutaksid täielikult kõikide äritegevuse kahjude ja võlgade eest.
Doonorid- igapäevased kangelased Tänapäeval tänu meditsiini avastustele on võimalik loovutada verd ja anda see kellegile, kes seda väga vajab. Seda üllast inimest, kes verd loovutab nimetatakse doonoriks. Miks vajavad abivajajad sinu verd? Põhjusi on mitu, näiteks kui naine kaotab sünnitusel hulganisti verd. Paljud inimesed arvavad millegi pärast, et vere loovutamine pole vajalik, et küll nad hakkama saavad. See on väga väär mõtlemine. Valus oleks kogeda, kui näiteks sinul oleks peale suurt autoõnnetust suur verekaotus ja sul läheks hädasti vaja verd, aga siis saad teada, et arstidel pole anda piisavalt. Selle pärast nimetaksin ma doonoreid elupäästijateks ehk kangelasteks. Statistika näitab, et Eestis on doonorite arv väike. Verd võib loovutama hakata 18 aastaselt, aga muidugi peab täitma ka paar nõuet, et hoiduda
kasulikum kui abistajale. Selleks, et olla peetud altruistiks, peab toiming olema tahtlik. Kuigi altruist võib omategevuse tulemusena kogeda sisemist rahulolu, mida võib tõlgendada kui teatavat tasu, on tema motiiviks teist aidata. Et vähendada laste käitumises egoistlikke motiive, tuleb nende elu organiseerida nii, et nad tunneksid vajadust teistele head teha. Selleks on altruistlike tegevuste jaoks vaja luua tingimused. Altruistlikud tegevusvormid on: vahetamine, laenamine, jagamine, loovutamine, kinkimine, annetamine. See järjestus kujuneb lapse arengust lähtuvalt just sellises järjekorras. Lapsi ei tohi kunagi sundida altruistlikult tegutsema. Ta ei pruugi selleks veel valmis olla. Tuleb austada lapse soovi valida partnerit. Vahetamine vaatamata sõimeealiste vähesele suhtlemisaktiivsusele, tunnetatakse kaaslase olemasolu ning osatakse kõrvutimängus jälgida kaaslase tegevust. Seetõttu tuleks sõimeeas algust teha mänguasjade lühiajalise vahetamisega. Lapsele tehakse
CO2 jt. (1%). Hapniku saadakse tööstuses põhiliselt vedela õhu fraktsioneerival destilleerimisel, nii tööstuses kui ka laboris vee elektrolüüsil ja laboris hapniku sisaldavate ainete lagundamisel. Hapniku tõestatakse hõõguva pirru viimisega uuritava gaasiga täidetud anumasse. Kuna hapnikus põlevad ained märgatavalt paremini, kui õhus, süttib pird hapniku puhul heleda leegiga põlema. Oksüdeerija on aine, mille osakesed liidavad elektrone. Oksüdeerumine on elektronide loovutamine. Oksiidid on liitained, mis koosnevad kahest elemendist ja millest üks on hapnik (SO 2, Al2O3).Oksüdatsiooniaste on elemendi aatomite laeng ühendis, eeldusel, et ühend on iooniline ja ta näitab elemendi oksüdeerumise astet ühendis. Tähtsamad oksiidid on kaltsiumoksiid e. kustutamata lubi (Tööstuses saadakse põhiliselt lubjakivi lagundamisel kõrgel temperatuuril. Lubjakivi põhikoostisaine CaCO3 laguneb kuumutamisel vastavalt reaktsioonivõrrandile CaCO3CaO+CO2.
Mõisted redoksreaktsioon- keemiline reaktsioon, milles toimub elektronide üleminek ühtedelt osakestelt teistele, toimub elementide o-a muutus. oksüdeerumine- elektronide loovutamine redoksreaktsioonis, sellele vastab elemendi o-a suurenemine. redutseerumine- elektronide liitumine redoksreaktsioonis, sellele vastab elemendi o-a vähenemine. oksüdeerija- aine, mille osakesed liidavad elektrone (ise redutseerudes). redutseerija- aine, mille osakesed loovutavad elektrone (ise oksüdeerudes). korrosioon- metalli hävimine (oksüdeerumine) keskkonna toimel. keemiline ja elektrokeemiline korrosioon- korrosiooni liik, mis toimub juhul, kui kaks metalli
Nt. Reaktsiooni N2 + 3H2 2NH3 (H<0) tasakaal nihkub a) temperatuuri tõstmisel vasakule, alandamisel paremale b) rõhu tõstmisel paremale, alandamisel vasakule c) N2 või H2 kontsentratsiooni suurendamisel paremale, vähendamisel vasakule d) NH3 kontsentratsiooni suurendamisel vasakule, vähendamisel paremale. Redoksprotsessid Redoksreaktsioon reaktsioon, kus toimub üheaegselt nii elektronide liitmine kui ka loovutamine. Redutseerija loovutab elektrone, toimub oksüdeerumine. Oksüdeerija liidab elektrone, toimub redutseerumine. Redutseerumine elektronide liitmine Oksüdeerumine elektronide loovutamine
REDOKSREAKTSIOONID redoksreaktsioon – reaktsioon, milles toimub elektronide üleminek, muutuvad elementide oksüdatsiooniastmed oksüdatsiooniaste – elemendi aatomi tinglik laeng ühendis eeldades ioonilist sidet kõigi aatomite vahel (mitu elektroni aatom saab loovutada või juurde võtta) oksüdeerumine – elektronide loovutamine, redutseerija oksüdatsiooniastme kasv sagedased redutseerijad: H2S, FeSO4, Zn, KI, Na, H2SO3 redustseerumine – elektronide liitmine, oksüdeerija oksüdatsiooniastme kahanemine sagedased oksüdeerijad: O2, KMnO4, Cl2, H2O2, konts. H2SO4 keemiline element saab käituda ainult oksüdeerijana, kui ta on oma kõrgeimas oksüdatsiooniastmes (st see saab ainult kahaneda). nt: F2, O3
3. Ioon aatomite rühmitus, mille laeng on + või Li+ Cl- 4. Puhas aine koosneb ühe aine osakestest destilleeritud vesi 5. Segu koosneb mitme aine osakestest õhk 6. Lihtaine koosneb ühest elemendist Fe 7. Liitaine koosneb mitmest elemendist H20 8. Keemiline element kindla tuumalaenguga aatomite liik Fe 9. Füüsikaline nähtus muutub keha olek, aga uut ainet ei teki autoavarii 10. Keemiline nähtus tekib uus aine küünla põlemine 11. Oksüdeerumine elektronide loovutamine (metall) Mg-2e=Mg2+ 12. Redutseerumine elektronide liitmine (mittemetall) O+2e=O2- 13. Oksudeeruja elektronide liitja (mittemetall) O 14. Redutseerija elektronide loovutaja (metall) Fe 15. Redokreaktsioon reaktsioon, kus muutub oksudatsiooni aste (o.a) H2+O2=H2O 16. Halogeenid VII A rühma elemendid Cl2 17. Väärisgaasid VIII A rühma elemendid He 18. Iooniline side metalli ja mittemetalli vaheline side NaCl 19. Kovalentne side aatomite vaheline side Br ja Br
kasutamise eesmärkidel tingimusel, et selline tegevus ei taotle ärilisi eesmärke. avaldatud teosed – kui on salvestatud arvutisüsteemis Arvutiprogramme Õiguspärasel kasutajal on lubatud: ◦ kopeerida, kohandada, töödelda nendel eesmärkidel, milleks programm omandati, samuti vigade parandamiseks seda võib piirata ◦ varukoopiate tegemine ◦ programmi jälgimine, katsetamine Autorileping ja litsentsileping Varaliste õiguste üleandmine ehk loovutamine Teose kasutamise lubamine All-litsentseerimise õiguste andmine Erinevused ◦ Autorileping hõlmab nii varaliste õiguste üleandmist kui teose kasutusloa (litsentsi) andmist ◦ Litsentsileping käsitab üksnes kasutusluba Lepingute erinevused Autorilepingu võib sõlmida nii olemasoleva teose kasutamiseks kui ka uue teose loomiseks ja kasutamiseks (õiguste jaotamiseks) Litsentsileping käsitab juba eksisteeriva teose kasutusõigusi Autorilepingu sisu
keemia väärisgaaside aatomitle on väliskihise enamasti 8 elektroni ehk, nn elektronkett. Ühiste elektronpaaride moodustamine või elektronide litmine- loovutamine sab toimuda kemilisetes reaktsioonides. Keemiline reaktsioon on protsess milles tekivad või katkevad keemilised sidemed. Keemiliste sidemete tekkel alati eraldub keemiliste sidemete lõhkumiseks tuleb energiat kulutada. Iga süsteem püüab võimaluse korral minna üle kõige madalama energia olekusse nn. Energia miinimumi printsiibile. Rekatsioonil eralduvat või neelduvat energiat nim. Reaktsiooni soojusefektiks ja täh. Sümbol H.
·Jaapaniga sõlmiti rahu ·Ka II MS korral ei suudetud saavutada õiglast maailmakorda ·saavutati võit natsismi üle , kuid kommunistliku diktatuuri mõju kasvas ·NSVL võimu alla jäid Balti riigid moodustus kommunistlik blokk ·Maail lõhestus- Külm Sõda ·Toimus Nürnbergi kohusTulemused: ·Saksa keiser Wilhelm II loobus troonist ·11. nov kirjutasid Antandi ja Saksamaa esindajad alla Compiegne vaherahule ·Saksamaa alistus toimus evakueerimine ja demilitariseerimine, loovutamine suurema osa oma raudtee- veeremisest ·28.juuni 1919 suruti Saksamaale pelae Verssailes rahu ( nõrgestas Saksamaad) ·Võitjad said palju eeliseid ja uusi maid ·Rahulepingutega vähendati kaotatud riiikide territooriumi ning pandi neile ette majanduslikke, poliitilis ja sõjalisi kohustusi. ·Austria-Ungari lagunes ·Tekkisid uued riigid ·venmaast eraldusid mõned riigid ·Saksamaa kaotas osa territooriumist, ka suurriigiseisundi
elektroodidel kulgev redokreaktsioon karbotermia-metalli redutseerimine maagist süsiniku või süsinikoksiidi abil kõrgel temperatuuril keemiline vooluallikas-saade, milles keemilises reaktsioonis vabanev energia muudetakse vahetult elektrienergiaks. korrosioon- metalli hävimine(oksüdeerumine) keskkonna toimel oksüdeerija-aine, mille osakesed liidavad elektrone(ise redutseerudes) oksüdeerumine-elektronide loovutamine redoksreaktsioonis;sellele vastab elemendi oksüdatsiooniastme suurenemine redutseerija-aine, mille osakesed loovutavad elektrone(ise oksüdeerudes) redutseerumine-elektronide liitmine redoksreaktsioonis;sellele vastab elemendi oksüdatsiooniastme vähenemine sulam-mitmest metallist või metallist ja mittemetallist koosnev metalliliste omadustega materjal;saadakse enamasti koostisainete kokkusulatamisel särdamine-kuumutamine õhuhapniku juuresolekul.
· Redoksreaktsioon keemiline reaktsioon, millega kaasneb elektronide üleminek ja elementide oksüdatsiooniastme muutus. · Oksüdatsiooniaste arvutuslik suurus, mis näitab elemendi aatomite oksüdeerumise astet ühendis ; võrdub elemendi aatomi laenguga ühendis eeldusel, et ühend on iooniline. · Asendusreaktsioon reaktsioon, milles üks keemiline element asendab ühendis teise keemilise elemendi. · Oksüdeerumine elektronide loovutamine redoksreaktsioonis. Reaktsioonis o.a väheneb. · Redutseerumine elektronide liitmine redoksreaktsioonis. Reaktsioonis o.a suureneb. Erinevad füüsikalised omadused: Sulamistemperatuur Tihedus Kõvadus Metallide aktiivsuse võrdlus Metallid Reageerimine hapetega Reageerimine veega Aktiivsed metallid Reageerivad väga tormiliselt, Reageerivad väga tormiliselt, Li, Na, K, Ca jt võib toimuda plahvatus
Kordamisteemad laovarude arvestuseks 1.Lao põhilised ülesanded: · Kliendi teenindamine, · Kaitse erakorraliste olukordade vastu, · Silumine ja tasandamine. 2. Ladude tavaliigid: · privaatladu, · avalik ladu · lepinguline ladu. 3. Mis toimub laos? · kauba vastuvõtmine, · ladustamine, komplekteerimi ne, · loovutamine ja lähetamine. 4. Ruumide ja pindade jaotamise põhimõtted. aluseks on laos käsitsetavate kaupade mahud, kaupade ja pakendite füüsikalised omadused ning hoiustamise ja käsitsemise eripära, laos sooritatavad toimingud, kasutatav laotehnoloogia ja laotõstukite tehnilised näitajad. On vaja teha selgeks ladu läbiva kauba koosseis ja hoiustamise ning käsitsemise viisid. Riiulitel ja tugialustel ladustatavad kaubad on võimalik jaotada järgmiselt: · alusekaubad
Redoksreaktsioon-keemiline reaktsioon, milles toimub elektronide üleminek ühtedelt osakestelt teistele, sellega kaasneb elementide okspdstsiooniastme muutus.Fe+S=FeS. Redutseerija-aine, mille osakesed loovutavad elektrone. Li, Na, Mg. Oksüdeerija-aine, mille osakesed liidavad elektrone. H2O2, CrO3. Redutseerumine-elektronide liikumine redoksreaktsioonis, sellele vastab elemendi oksüdatsiooniastme vähenemine. Oksüdeerumine-elektronide loovutamine redoksreaktsioonis, sellele vastab elemendi oksüdatsiooniastme suurenemine. Katalüsaator-aine, mis muudab reaktsiooni kiirust, vabanedes reaktsiooni lõpus esialgses koostises ja koguses. Aktiivsed metallid (K-Mg) reag. külma veega, tekivad leelis ja H2. Ca+2H2O=Ca(OH)2+H2. Zn+H2O=ZnO+H2. Väheaktiivsed metallid (alates Ni-st) ei reageeri veega. Vesinikust eespoololevad metallid tõrjuvad hapetest vesiniku välja. Zn+2HCl=ZnCl2+H2. Metall
Keemia kordamine, metallide omadused Oksüdeerija - aine, mis omastab ehk liidab elektroone / ise redutseerub Redutseerija - aine, mis reedab ehk loovutab elektrone / ise oksüdeerub Oksüdeerumine aine elektronide loovutamine redoksreaktsioonis, sellele vastab elemendi o.a suurenemine Redutseerumine aine elektronide liitmine redoksreaktsioonis, sllele vastab elemendi o.a vähenemine Oksüdatsiooniaste o.a / elemendi aatomite oksüdeerimisist iseloomustav suurus Redoksreaktsioon Reaktsioon, kus kahe aine o.a-d muutuvad / toimub elektronide üleminek ühtedelt osakestest teistele Leelismetall Esimese A-Rühma metallid Leelismuldmetall Teise A-Rühma metallid alatest Ca-st
1. Keemiline side tekib väliskihi elektronide vahel ühe aatomi väliskihielektron(id) ühinevad teise aatomi omadega, nii hakkavadki aatomid teineteise poole tõmbuma 2. a) Elektronide loovutamine või juurdevõtmine (aatomid loovutavad/võtavad juurde niipalju elektrone, kui vaja. Aatomitest tekivad ioonid. Tekib iooniline side) b) Elektronide jagamine omavahel, moodustades ühiseid elektronpaare. Tekib kovalentne side. 3. 2H + O = H2O Energia eraldub. Eksotermiline reaktsioon 4. Keemilise sideme katkemisel energia neeldub. 5. Eksotermiline reaktsioon on reaktsioon kus lähteainete energia on kõrgem saaduste energiast (H < O )
6) muudel seadusega sätestatud juhtudel. 39. Maksumaksjal, kes on tasunud maksuseaduses ettenähtust suurema maksusumma, on õigus kolme aasta jooksul enammakse tekkimise päevast arvates taotleda maksuhaldurilt enammakstud summa tagastamist või tasaarvestamist. 40. Võlausaldaja võib oma nõude võlgniku nõusolekuta anda lepingu alusel tervikuna või osaliselt üle teisele isikule (nõude loovutamine). Nõuet ei või loovutada, kui loovutamine on, kui loovutamine on seadusest tulenevalt keelatud või kui kohustust ei saa selle sisu muutmata täita kellelegi teisele kui senisele võlausaldajale. 41. Kaasaaitamise kohustus: Oluliste asjaoludest teatamine Arvestuse pidamine, dokumentide säilitamine, maksuarvestuse esitamine jne Maksuhalduri tegevuse takistamise keeld 42. Uurimispõhimõte - maksuhalduril on maksude tasumise õigsuse kontrollimise ja maksusumma määramisel kohustus arvestada kõiki asjasse puutuvaid
kindlasse sihtpunkti. Laokulud õigustatud ja efekt saadase eelkõige surte kaubakoguste veokulude säästmisel. Ka Xis kasutame väga palju konsolideerimist, sest poode on palju, kes meilt kaupa tellivad ning kui suunad klapivad, siis kogume kauba kokku ning proovime saata kõik ühe transporldiga, sest see hoiab kõvasti kokku meil veokulusi. Ei kujutaks ettegi, kui peaksime igale firmale või poele saatma eraldi tellimusi, mis vahepeal ei olegi nii suured, et see end ära tasuks. KAUBA LOOVUTAMINE Kauba loovutamine kliendile või veofirma esindajale on vastutusrikas toiming kuna kauba eest läheb loovutamisel üle enamasti selle vastuvõtjale. Loovutamisel ei kontrollita üldjuhul saadetiste koosseisu tooteartilkite järgi. Vastuvõtjale antakse üle pakkeüksused. Vastuvõtja kohus on kontrollida kas pakkeüksuste arv ja ühikud on kooskõlas kauba saatedokumnetidel märgituga, kas saadetis on nõuetekohaselt pakendatud ja kas toodetel või pakenditel pole vigastusi. Minu tööaja
põhjal) Faktooring Millega on tegu? oFaktooring on finantseerimise teenus, mis võimaldab ettevõttel lihtsalt ja kiiresti hankida vajalikku käibekapitali. Faktooring sobib ettevõttele, kelle käibevarast moodustavad olulise osa ostjatelt laekuvad arved. oFaktooring võimaldab Teil pakkuda oma klientidele pikemaid maksetähtaegu. Nii saate vältida 30-, 60- või 90-päevaseid ooteaegu. oFaktooring on ostjatelt laekumata arvete loovutamine, et tagada Teile vajalikul hetkel vaba raha - arvete rahastamine, arvete haldamine ja vajadusel ostjate makseriski maandamine krediidikindlustusega. Faktooring Kuidas toimib? oEttevõte müüb kauba või osutab teenuse faktooringulepingus fikseeritud ostjale. oEttevõte võtab arvele ostja kinnituse. oEttevõte edastab arve panka. Pank võib täiendavalt nõuda enne finantseerimist arvete eelnevat kinnitamist ostja poolt ning kauba liikumist tõendavaid
leping fructus, us m vili, tulu magistratus, us m. magistraat, kõrge riigiametnik metus, us m. kartus, hirm; ähvardus status, us m. seisukord, seisund, olukord usus, us m. kasutamine, tarvitamine; komme ususfructus, us m. kasutusvaldus f acquisitio, onis f. omandamine actio, onis f. hagi, kaebus; tegevus, toiming; kohtupidamine, protsess adoptatio = adoptio, onis f. lapsendamine cessio, onis f. loovutamine, taandumine conditio, onis f. (= condicio) tingimus, nõue conductio, onis f. rentimine, rent constitutio, onis f. (imperaatori) korraldus; määrus datio, onis f. (edasi- v. üle) andmine deminutio, onis f. kaotus; vähendamine, piiramine detentio, onis f. pidamine, käes hoidmine donatio, onis f. kingitus, annetus emancipatio, onis f. isiku vabastamine (v. vabanemine)
14 harj. 3.9 (9,10), lk. 15 harj. 4.1, lk. 2226, lk. 84, 85 harj.5.1. Tuleb teada: 1. Mis on: oksüdatsiooniaste elemendi aatomite oksüdeeruise astet iseloomustav suurus; võrdub aatomi laenguga ühendis redoksreaktsioon keemiline reaktsioon, milles toimub elektronide üleminek ühtedelt osakestelt teistele; sellega kaasneb elementide oksüdatsiooniastme muutus oksüdeerumine elektronide loovutamine redokreaktsioonis; sellele vastab elemendi oksüdatsiooiastme suurenemine redutseerumine elektronide liitumine redoksreaktsioonis; sellele vastab elemendi oksüdatsiooniastme vähenemine oksüdeerija aine, mille osakesed liidavad elektrone redutseerija aine, mille osakesed loovutavad elektrone 2. Kuidas määrata elementide maksimaalset ja minimaalset oksüdatsiooniastet! MAX rühma nr MIN rühma nr miinus 8 (mittemetallid)
2.3. Iga käesoleva Garantii alusel Garantii andja poolt tehtud väljamakse vähendab Garantiisumma suurust väljamakstud summa võrra. 2.4. Garantii andja tasub Garantii saaja poolt nõutud Garantiisumma või selle osa nõudes märgitud pangakontole hiljemalt [päevade arv] päeva jooksul Garantiis nimetatud kirjaliku nõude ja Garantii kohaselt nõutud dokumentide esitamisest arvates. 3. Garantiist tulenevate õiguste loovutamine 3.1. Garantii saajal ei ole lubatud loovutada või muul viisil üle anda osaliselt ega täielikult Garantiist tulenevaid õigusi ilma Garantii andja eelneva kirjaliku nõusolekuta. 4. Garantii kehtivus 4.1. Garantii jõustub alates selle allkirjastamisest Garantii andja poolt ning kehtib kuni [kuupäev]. 4.2. Garantii lõpeb enne Garantii punktis 4.1 sätestatud tähtaega alljärgnevatel juhtudel: 4.2.1
Esimene Maailmasõda lõppes 11. Novembril 1918. Sõda nõudis üle 9 miljoni inimelu. Sõdivatest riigidest tundsid end enam pettetuna ja kaotajatena Saksamaa, Venemaa, Itaalia ja Jaapan. Oli sõja järgne majanduskriis ja inimeste elujärg halvenes. Kas lahendamata jäänud probleemid võis olla põhjus diktatuuride tulekuks? Saksamaa polnud rahul Versailles` rahulepingu tingimustega, sest pidas neid ebaõiglaseks. Pahameelt tekitas ka sakslastega asutatud alade loovutamine naabritele( Alsace- Lorraine'i, Poola alasid jm). Saksamaal puudus põhimõtteliselt tooraine, laevastik ja tööstuspiirkonnad. Itaalia ja Jaapan olid aga kõige vähem rahul kuna nemad jäeti ilma oma territooriumitest ja kolooniatest. Itaallasi ootas tööpuudus ja nälg. Oli sõjajärgne majanduskriis, maailmakaubandus ei taastunud oodatud kiirusega. Kõige keerulisemaks aga kujunesid majandusprobleemid Saksamaal kuna tuli maksta Atlandi riikidele reparatsiooni. Kui Saksamaa ei suutnud 1923
Mittekasutamise õigustatus. varasem ühenduse kaubamärk on selleks kuupäevaks olnud registreeritud vähemalt viis aastat. Selliste tõendite puudumise korral lükatakse vastulause tagasi. Kui varasemat ühenduse kaubamärki on kasutatud vaid osa kaupade või teenuste puhul, mille jaoks see on registreeritud, loetakse see vastulause menetlemisel ainult nende kaupade või teenuste jaoks registreerituks. (Kohtuasjas T-147/03) 5 Autoriõiguse küsimused Autoriõiguste loovutamine. Üheks autoriõiguste üleandmise võimaluseks on varaliste autoriõiguste loovutamine teisele isikule, mis tähendab autori poolt varalistest õigustest loobumist tähtajatult koos isiklike autoriõiguste säilimisega. Autori poolt oma varaliste õiguste üleandmine või loa andmine teose kasutamiseks võib olla piiratud konkreetsete õiguste osas, samuti teose kasutamise eesmärgi, tähtaja, kasutamise territooriumi, ulatuse, viiside ja vahendite osas. Autorile kuulub
11. Keemilised vooluallikad Keemiline vooluallikas on seade, milles muudetakse keemilisel reaktsioonil vabanev energia (nn keemiline energia) vahetult elektrienergiaks. Akud on sellised keemilised vooluallikad, mida saab tühjenemisel uuesti laadida. - Nad on mõeldud korduvaks kasutamiseks. Selleks, et saada redoksreaktsiooni arvel elektrienergiat, tuleb elektronide loovutamine (oksüdeerumine) ja elektronide liitmine (redutseerumine) läbi viia eraldi elektroodidel. Keemilisi vooluallikaid, milles saadakse elektrienergia kütuste oksüdeermisel eralduva energia arvel, nim kütuselementideks. Patareid koosnevad kuivelementidest ja on mõeldud ühekordseks kasutamiseks. Autoaukudes ehk pliiakudes on sees 30% väävelhape ning vahel ka destileeritud vesi ja metallplaadid (osad puhtas Pb ja teised PbO )
Oksiid- liitaine, mis koosneb kahest elemendist ja millest üks on hapnik (o.-a. II). Näiteks: ( Li2O- liitiumoksiid, Na2O- naatriumoksiid, Fe2O3- raud (III) oksiid jne). Hüdroksiid aine, milles metallikatioonid on seotud hüdroksiidioonidega. Näiteks: NaOH, Ca(OH)2. Redutseerija aine, mille osakesed loovutavad elektrone ise oksüdeerudes. Oksüdeerija aine, mille osakesed liidavad elektrone ise redutseerides. Fluor on alati oksüdeerija! Oksüdeerumine- elektronide loovutamine, redoksreaktsioonis vastab sellele elemendi oa suurenemine. Redutseerimine- elektronide liitmine, redoksreaktsioonis vastab sellele elemendi oa vähenemine. Elektrolüütiline dissotsiatsioon- Ainete lagunemine ioonideks lahustumisel polaarses lahustis. (Vaata töövihik lk 24-25). Redoksreaktsioon- keemiline reaktsioon, milles toimub elektronide üleminek ühtedelt osakestelt teistele, sellega kaasneb oa muutus. Ioon- positiivset või negatiivset laengut kandev aatom või aatomite rühmitus
· On mees ja naine, kes virelevad põhjakihis, mees on joodik ja alkoholijahil seikleja, naine vaevleb omaette depressioonis, üks elab mälestustest, teine unistustest. Ja kuskil reaalsuses on nad kahekesi, on mingi nõrk omavaheline side, väike teineteisele toetumine, natuke kindlustunnet, üürike hetk kui kaks südant löövad paar takti üheskoos. Ent kas selline pimedas reaalsuses koperdamine on mingilgi moel lootuseks piisav, kas endast osakese teisele loovutamine või avamine on lõpuks sulle endale midagi väärt? Või lasta kõigel minna, lasta lainetel pea kohal kokku lüüa, lihtsalt kuluda lõpuni. Ei tea. Pea püsti ja edasi? Milleks? Kuhu? On see lõpuks kõike seda väärt? Vastus on kuskil sinu peas. Rubriigid · Eetika, moraal, religioon; · Inimene ja inimsuhted; · Inimene ja ühiskond; · Rahvusvahelised suhted. Minu arvamus Aitäh kuulamast!