Metallide keemilised omadused Metallid reageerivad paljude ainetega, sealhulgas peaaegu kõikide mittemetallidega. Keemilistes reaktsioonides on metallide redutseerijad, mis loovutavad oma viimase kihi elektronid: Me ne- Me+n Parema ülevaate saamiseks paigutatakse metallid aktiivsuse alusel pingeritta. Mida vasemal pingereas metall asub, seda aktiivsem ta keemilistes reaktsioonides on. Kuna enamik keemilisi reaktsioone toimum vesilahustes, siis on pingeritta asetatud ka vesinik. Enamik metallidega toimuvaid keemilisi reaktsioone toimub pingerea alusel. Metallide pingerida ( Allpool toodud metallide pingereas on väljatoodud ainult levinumad metallid) Keskmise Aktiivsed metallid Väheaktiivsed metallid aktiivsusega Li K Ba Ca Na Mg Al Zn Cr Fe Ni Sn Pb H Cu Hg Ag Au Tõrjuvad lahjendatud hapetest välja vesiniku (reag. hapetega) Ei tõrju hapetest
soojuslik) elekter Gaasjahutusega kiire 238 suletud, kiire heelium 850 kõrge U+ 288 & reaktor kohapeal vesinik 2 suletud, 50-150 elekter Pliijahutusega kiire 550- 238 kiire Pb-Bi madal U + regionaaln 300-400 & reaktor 800 e 1200 vesinik
Universum + koosneb põhiliselt varjatud ainest, varjatud aine on kõikjal + areng on igal ajahetkel keskmiselt ühesugune + tugev gravitatsiooni jõud, elektromagnetjõud, nõrk vastastikmõju + inflatsiooniliselt paisuv, paisutajaks terve energia + miski ei välista teiste universumite olemasolu + kärjeline struktuur tekkis 11.miljardit aastat tagasi + tekkis tohutu algplahvatus, Suure Paugu tulemusena + koosneb kolmemõõtmelisest ruumist, on vaadeldav + aeg on ühemõõtmeline + muutub ajas + tekkis 15.miljardit aastat tagasi + varjatud aine põhjustab põhilise gravitatsioonilise tõmbumise + 3 mõõtmelise ruumi tajutab lõputult aga piiridega , ning sisaldab kõiki teada-olevaid galaktikaid ja nende osi + on osa mateeriast + aineosakesed on 4% kogu mateeriast + aineosakesed on kvargid (mis jagunevad) prootonid, neutronid elektronid vesinik kärjeline struktuur
põhineb aineosakeste korduval ümberjaotumisel liikuva ja liikumatu faasi vahel.) 4. Aminohapete stereokeemia suhteline (D/L) ja absoluutne (S/R) konfiguratsioon ja kuidas seda määrata. D,L-nomenklatuur baseerub D- ja L-glütseeraldehüüdi stereokeemial ning R,S-nomenklatuur on ülimuslik, kuna võimaldab ühemõtteliselt nimetada ka kahe kiraalse tsentriga aminohappeid. D/L konfiguratsiooni puhul peab arvestama sellega, et kui keskmise süsiniku juures olev, ühelpool vaid vesinik on üksinda vastu teistele ahela osadele siis on D- ja ühendinimi, kui aga üksik vesinik on teiste ahelaosade sees ja selle süsinikuteises osas olev ühend vastu teistele ahela osadele siis on L- ühend üldjoontes, Teistel juhtudel, erandid on siis kui karbosküülhape osa juures ühendis on ühend D-ühend kui süsinku küljes olev H on väljapoole ja teisel pool olev ahelaosal on vaba elektron üle. R/S puhul vaadatakse kiraalsest tsentrist nõrgima (noorima) grupi suunas
Põhiorgaaniline keemiatööstus Põhiorgaaniline keemiatööstus baseerub lihtsatel lähteainetel (süsivesikud, süsinikoksiidid, vesinik), mida saadakse peamiselt naftast ja looduslikust gaasist. Metaan - maagaasi peamine koostisosa - leidub ka palju naftagaasis - töötlemisel veeauruga temp. 700-900 C ja nikkelkatalüsaatori abil saadakse sünteesigaas - halogeenimisel saadakse triklorometaanja tetraklorometaan - pürolüüsil temp. 1000 C moodustuvad tahm ja vesinik Metanool - kasutatakse lahustina, kütusena, antifriisides, polümetüülmetakrülaadi valmistamiseks ja teiste põhiorgaaniliste sünteeside lähteainena - oksüdeerumisel saadakse metanaal Eteen - saadakse nafta krakkgaasidest, etaanist dehüdrogeenimise teel ja etüünist hüdrogeenimise teel - enamik eteenist läheb polüeteeni tootmiseks ja etüleenoksiidi valmistamiseks - halogeenimisel saadakse lahusti 1,2-dikloroetaan või vinüülkloriid - hüdraatimisel saadakse etanool Etanool
FENOOL EHK HÜDROKSÜBENSEEN Fenooli füüsikalised omadused: värvitu, kristalne, iseloomuliku lõhnaga, toatemperatuuril vees halvasti lahustuv, seguneb veega igas vahekorras alates 70° C, õhuhapniku mõjul muutub tahke fenool kiiresti roosaks. Fenooli keemilised omadused: fenoolile on iseloomulikud nii ühealuseliste alkoholide kui ka areenide üldised omadused: 1. tänu -elektronsüsteemi mõjule on fenooli hüdroksürühma vesinik liikuvam kui tavalisel alkoholil ja ta dissoteerub vesilahuses, muutes keskkonnareaktsiooni + H+ C6 H 5OH C6 H 5O - + H + 2. nii nagu hape, reageerib ta aktiivsete metallidega 2 + 2Na 2 + H 2 2C6 H 5OH + 2 Na 2C6 H 5ONa + H 2 3. reageerib ka hüdroksiididega (peamiselt leelistega) + NaOH + H 2O C6 H 5OH + NaOH C6 H 5ONa + H 2O 4
argooni on kuni 2%, hapnikku 0,3% veeaur Asub Päikesest 1,5 korda kaugemal kui Maa. Marsil on kaks kaaslast: Phobos ja Deimos Click to edit Master text styles Second level Third level Fourth level Fifth level Jupiter Puudub tahke pind. Tuum on kivisest materjalist, peal asub vedel metalliline vesinik. Läbimõõt: 142 984 km (ekvatoriaalne) Temperatuur on 20 000 °C kui pilves on siis 140 °C Mass on 1.8986x1027 kg Atmosfäär on 1000 km paksune, koosneb vesinikust ja heeliumist Jupiter on päikesest umbes viis korda kaugemal kui Maa. Jupiteril on 2006. aasta sügiseks teada 63 kuud. Neli suuremat Io, Europa, Ganymedese ja Callisto avastas Galileo Galilei 1610 Click to edit Master text styles Second level Third level
Järeldan katsest, et Alumiinium on väheaktiivne metall. Katsetulemus ei ole kooskõlas pingerea asukohaga, kuid tean, et Alumiinium reageerib aeglaselt, sest teda katab õhuke oksiidikiht. 6HCl + 2Al 2AlCl + 3H 3 2 2. Soolhape + tsink / HCl + Zn Panin katseklaasi soolhapet ja lisasime sinna tsingi tüki. Reageerimine toimus üldiselt kohe. Kuumutamisel hakkas eralduma veidi suitsu ning kogudes gaasi, mille kohale asetsime põleva tiku, sain teada ka seda, et eraldus vesinik. Järeldan katsest, et tsink on hea aktiivsusega metall, mis on kooskõlas ka metalli asukohaga pingereas. 2HCl + Zn ZnCl + H 2 2 3. Soolhape + tina / HCl + Sn Panin katseklaasi soolhapet ja lisasime sinna tina tüki. Reaktsiooni ei toimunud. Kuumutamisel oli reaktsiooni vaevumärgatav. Katsest Järeldan, et tina on väheaktiivne metall, mis on kooskõlas ka metalli asukohaga pingereas. 4HCl + Sn SnCl4+ 2H 2 4. Soolhape + raud / HCl + Fe
lagundamata ning väljub neerude kaudu kehast. Metanooli kütuseelement 2CH 3 OH +3 O3 4 H 2 O+2 CO2 Keemilise kütuseelementi tööpõhimõte seisneb selles, et vesiniku või vesinikku sisaldavat ainet (vesi, metanool jne.) juhitakse anoodist läbi membraani ja/või elektrolüüdi, mis laseb läbi vaid positiivsed laengud (H+). Negatiivsed ioonid või elektronid juhitakse läbi alalisvooluahela, toites vahetult elektriseadmeid. Katoodi juures saavad kokku vesinik (H+) ja O2 ¿ hapnik ( , mis ühinevad veeks. Metanooli kasutades on lisaks produktiks süsihappegaas. Metanooli kasutamisel on miinuseks see, et osa metanoolist liigub läbi membraani katoodi poole ning selle võrra langeb kütuseelemendi efektiivsus. Samuti on säärases kütuseelemendis kasutatavad materjalid kallid või paljud membraanid on alles arenduse faasis. Hetkel toodab keskmine vesinik-hapnik kütuseelement 1-1,5V voolu 25 kraadi juures.
C6H12O6 -> 2C3H4O3 + 4H 2. Tsitraaditsükkel toimub mitokondris, püruvaadi edasine lagundamine: toimub palju reaktsioone, mille käigus eralduvad järk-järgult CO2 molekulid ja H-ioonid, mis seotakse vesinikukandjatega NAD Kokku tekib 12NADH2 molekuli, mis liiguvad hingamisahela reaktsioonidesse. 3. Hingamisahela reaktsioonid toimub mitokondris. Hingamisahela reaktsioonides vabanevad H-ioonid NADH2 molekulidest. Eraldunud vesinik reageerib molekulaarse hapnikuga ja moodustub H2O. Vabaneva energia arvel saab sünteesida 36 ATP molekuli. 12NADH2 + 6O2 -> 12NAD + 12H2O Rakuhingamise summaarne võrrand: C6H12O6 + 6O2 -> 6O2 + 6H2O
Aatommass(Ar)amü-aatomi mass aatommassiühikutes.Molek ulmass(Mr)-molekuli mass aatommassiühikutes.Li-7,Na-23,Se -79.Lihtaine koosneb ainult ühe ja sama elemendi aatomitest .Lihtainena esinev metall koosneb ainult metallilise elemendi aatomitest.Lihtainena esinev mittemetall koosneb ainult mit temetallilise elemendi aatomitest.O2-hapniku molekuli valem ,N2-lämmastiku molekuli valem.H-üks vesiniku aatom.Arv va lemi ees-kordaja e.koefitsent.2O-kaks hapniku aatomit,2O2 -kaks hapniku molekuli.Lihtained-üksikud aatomid(väärisgaasid -He,Ne,Ar),molekulid(gaasilised-H2,Cl2,F2),kristalsed ained( aatomitest-Si,B.Molekulidest-väävel,fosfor).Liitaine koosne b erinevate elementide aatomitest(vees-elemendid-vesinik,h apnik.Lihtainena-gaasilised,liit.-vedelad).Süsih.-süsinik,hapnik .H2O-2vesinikku,1hapnik.NaCl-naatriumkloriid,Fe2O3-raudoksiid.
ALKOHOLID Alkoholi tunnusrühmaks on OH-rühm - HÜDROKSÜÜLRÜHM. OH ioon on seotud kovalentse sidemega. Alkohol saadakse, kui asendada süsivesiniku (CH) valemis üks vesinik OH rühmaga. Alkoholi nimes on sõna lõpp alati OOL Alkoholi toodetakse teraviljast ja kartulist, suhkrute kääritamisel. Metanool (puupiiritus) (CH3OH) · On vedelik, värvitu, põletava maitsega, mürgine, seguneb hästi veega, keemistemp. 65kraadi, kasutatakse tööstustes lahustina, mootorikütusena ja mitmesuguste ainete valmistamiseks. · Metanooli saadakse metaani(CH4) oksüdeerumisel.
nõrgad happed 4) ehituse järgi mineraalhapped e anorgaanilised happed karboksüülhapped e orgaanilised happed 5) agregaatoleku järgi vedelikud 1 tahked ainult vesilahustes esinevad 3. HAPETE SAAMINE 1) Hapnikhappeid saadakse: oksiid + vesi 2) Divesiniksulfiidhapet ja vesinikhalogeniidhappeid saadakse: Vesinik + lihtaine Sool + tugevam hape 4. HAPETE KEEMILISED OMADUSED Hapete sarnased omadused on tingitud vesinikioonidest. 1) Hape + metall 2) Hape + aluseline oksiid 3) Hape + alus 4) Hape + sool 5) Hapete lagunemine kuumutamisel 2
Metallid: Mittemetallid: Happed: Al-alumiinium Ar-argoon HF-fluoriid-vesinikfluoriidH Ba-baarium B-boor HCl-kloriid-vesinikkloriidH K-kaalium Br-bromiid HBr-bromiid-vesinikbromiidH Ca-kaltsium F-fluor HI-jodiid-vesinikjodiidH Cr-kroom P-fosfor H2S-sulfiid-divesiniksulfiidH Li-liitium He-heelium H2SO4-sulfaat-väävelH Mn-mangaan I-jood H2SO3-sulfit-väävlisH Na-naatrium Cl-kloor HNO3-nitraat-lämmastikH Ni-nikkel N-lämmastik HNO2 -nitrit-lämmastikusH Pt-plaatina Si-räni H3PO4-fosfaat-fosforH Fe-raud C-süsinik H2SiO4-slikaat-räniH Pb-plii H-vesinik H2CO3-karbonaat-süsiH Sr-strontsium S-väävel = CO2+H2O Sn-stannum O-hapnik Zn-tsink Ne-neoon Cu-kuprum Co-koobalt Au-kuld Hg-elavhõbe Ag-hõbe Mg-magneesium
KEEMIA. ALKAANIDE KEEMILISED OMADUSED PÕLEMINE o ALKAAN + HAPNIK -> SÜSIHAPPEGAAS + VESI CH4 + 2O2 CO2 + 2H2O TERMILINE LAGUNEMINE o LIHTAINEKS CH4 C + 2H2 o ALKÜÜN + VESINIK C4H10 C4H6 + 2H2 (butüün) CnH2n-2 KONDENSATSIOON VEEAURUGA o SÜSINIKOKSIID/VINGUGAAS CH4 + H2O CO + 3H2 o SÜSINIKDIOKSIID/SÜSIHAPPEGAAS CH4 + 2H2O CO2 + 4H2 ASENDUSREAKTSIOON HALOGEENIDEGA o NÄIDE C4H10 + 2Cl2 C4H8Cl2 + 2HCl (diklorobutaan) C arv saaduses ei muutu
URAAN CAROLISA HEKTOR 2018 TÄHTSAD FAKTID · Orbitaalperiood: 30589 Maa päev · Päeva pikkus: 17,2 tundi · Läbimõõt: 49 528 km · Raskusjõu tugevus: 8,7 N / kg · Kuude arv: 27 · Uraan teeb tiiru ümber Päikese: 84,3 Maa aastaga ASUKOHT · Seitmes planeet Päikesest eemal · Kaugus päikesest: 2 872 500 000 km KOOSTIS · Vesinik · Heelium · Ammoniaak · Vesi · Metaan Uraani sisemus koosneb peamiselt kivimidest ja jääst. KES AVASTAS? · Avastati William Herscheli poolt 1781 aastal teleskoobi abil KLIIMA Päikesesüsteemi planeetide hulgas kõike madalama temperatuuriga. See võib langeda kuni 49 kelvinini (-224o C) On märgatud kliimamuutuste kasvu. Tuule kiirused võivad ulatuda kuni 250 m/s (900 km/h). URAANI PÖÖRLEMINE PILT URAANIST Tänan kuulamast! KASUTATUD MATERJALID · wikipedia
HF) või gaasid (H2S, NH3, CH4). Mittemetallide ühendid hapnikuga on happelised või neutraalsed oksiidid (SO2, SO3, NO, NO2, CO, CO2, P4O10). VESINIK--HYDROGENIUM--H. 1s 1.Leidumine. Vesinikku leidub looduses peamiselt ühendite koostises (vesi, orgaanilised ühendid). Vabana (H2) esineb ta vulkaaniliste gaaside ja naftagaaside koostises ning tühisel määral atmosfääris (atmosfääri ülemistes kihtides). Kosmoses on vesinik levinumaks elemendiks. Ta moodustab umbes 75% Päikese ja tähtede massist. Looduses esineb kolm vesiniku isotoopi: prootium--H (harilik vesinik), deuteerium 21H ehk D (raskevesinik) ja triitium 31H ehk T (üliraske vesinik). T on radioaktiivne. 2.Saamine. Laboratoorselt saadakse vesinikku: a) tsingi reageerimisel hapetega (asendusreaktsioonil) Kippi aparaadis: Zn+H2SO4=ZnSo4+H2 b) aktiivsete metallide (leelismetallide) ja vee reageerimisel: 2Na+2H2O=2NaOH+H2 c) vee elektrolüüsil:
vesi. · Looduses on levinud kolloidlahused- nt: Biovedelikud, veri, taimemahlad, aerosool. tint Lisaks eristatakse: tardeid, vahtusid ja aerosoole. Tarded on: Sütt, hapupiim, lihased, nahk, makaronid, oad, herned, leib, sai. Iseloomulik on vananemine. Vahud tekivad- gaasi pihustamisel vedelikku nt mannavaht, vahukoor. Aerosoolides on tahke aine pihustatud gaasides. Happed- Ained, mis annavad lahusesse vesinikioone. Esimesel kohal ALATI VESINIK! Liigitatakse kolmel viisil: * Hapnikusisalduse järgi · Prootonite e. vesinike arvu järgi · Happe tugevuse järgi Tugevad happed on lahustes jagunenud täielik ioonideks. Hapete tunnused: Hapu maitse, * söövitav toime
Teemant Süsinik Põrgukivi Hõbenitraat Vesi Divesinikoksiid Väävelvesinik Divesiniksulfiid Vesiklaas Naatriumsilikaat Kvarts Ränidioksiid Apatiit Kaltsiumfosfaat Nuuskpiiritus Ammoniaagi vesilahus Põdrasarvesool Ammooniumkarbonaat Ooleum Vääveltrioksiidi lahus väävelhappes Korund ränidioksiid Smirgel ränidioksiid Triitium Üliraske vesinik Püriit Raud II sulfiid Kassikuld Raud II sulfiid Teras Raua ja süsiniku sulam (C < 2%) Seatina plii
Vee magestamine päästeparvede puhastusvärk. 68. Hinnata ruumi õhus oleva veeauru kontsentratsiooni (anda nii osakeste arvu, kui massi kaudu). Igas kuupmeetris on 9 gr veeauru. Vastus 9 gr/m3 kohta. Osakeste arvu järgi pool mooli 3*10 astmel Lämmastik 23 osakset kuupmeetri kohta. rõhul 100 kPa 69. Miks kurkide soolamisel kurk kaotab kaalust? Vesinik rõhul Osmoosi tõttu läheb vesi välja. Vesinik rõhul 150 kPa 70. Anum on jagatud membraaniga kaheks osaks. 50 kPa Ühel pool membraani on lämmastik rõhul 100 kPa (kilopaskal) ja vesinik rõhul 50 kPa. Teisel pool membraani on vesinik rõhul 150 kPa. Seega gaasi rõhk mõlemal pool membraani on ühesuurune. Membraani avadest mahub läbi vesiniku molekul, kuid lämmastiku molekul läbi ei mahu
Nüüd muutub teine hiidtäht punaseks hiiuks ja temaga kordub sama, kuni lõpuks tiirlevad üksteise ümber 2 läbipõlenud tähte. Hiid täht on tunduvalt suurema raadiuse ja heledusega kui peajada täht, mis on sama pinnatemperatuuriga. Hiidtähtede raadius on tavaliselt 10 kuni 100 korda suurem kui Päikese raadius, mis on 695 500 km. Tähti mis on heledamad kui hiiud kutsutakse superhiidudeks või ülihiidudeks. Tähest saab hiidtäht, kui kogu olemasolev vesinik tähe tuumas on ära kasutatud ning mille tulemusel on täht lahkunud peajadast. Punane hiid On hele hiid täht, mis on väikese või keskmise massiga (0.5 kuni 10 Päikese massi) asudes tähe evolutsiooni hilises staadiumis. On kollakas oranzi kuni punase värvusega, pinna temperatuur on madal 5000K ja vähem. Tuntuimad punased hiiud on Aldebaran (üks tähistaeva kirkamaid tähti, heleduselt 13. asub 65 valgusaasta kaugusel ja on paisunud 38 korda suuremaks kui Päike. Absoluutne
2.1. 1. Nimetage organismide peamisi keemilisi elemente. - Hapnik (O), Süsinik (C), Vesinik (H), Lämmastik (N). 2. Millised keemilised elemendid kuuluvad makroelementide hulka? - Makroelementide hulka kuuluvad veel Fosfor (F), Väävel (S), Kaalium (K), Naatrium (Na), Magneesium (Mg), Kaltsium (Ca) ja Kloor (Cl). 3. Miks vajab organism makroelemente suhteliselt suurtes kogustes? - Sest need moodustavad suure osa organismi koostisest. 4. Millised keemilised elemendid esinevad kõigi orgaaniliste ainete koostises? - O, C, H, N on enamike organismide koostises. 5
Looduslikult tekib eteeni vaid tühisel määral, näiteks puuviljades nende valmimisel. Tööstuslikult saadakse eteeni nafta töötlemisel (krakkimisel) moodustuvatest gaasidest ja teiste maavarade termilisel töötlemisel. Tänapäeval toodetakse eteeni kõrgel temperatuuril etaanist katalüsaatorite (Cr2O3) manulusel. Selle tulemusel moodustub etaanist eteen ja vesinik. Eteeni on lähteaineks halogeenühendite (vinüülkloriidi ja tetrafluoroeteeni) valmistamisel, millest toodetakse teflonkatteid ja plastmaterjale. Eteen leiab rakendust veel taimede kasvuhormoonina, kuna ta kiirendab aed- ja puuviljade valmimist. Terpeenid Beeta-karoteeni molekul on tekkinud kaheksa isopreeni liitumisel. Limoneeni molekul on tekkinud ühe isopreeni liitumisel. Pineeni leidub lehtpuidus. Limoneeni leidub apelsinides. Farneseeni sisaldavad kartulid.
Isotoobi keemilised tähised ja nimetused tulenevad reeglina vastava elemendi nimetusest. Erandiks on vesiniku isotoobid Valem või tähis Nimi Tuuma Tuumas Elekton Keskmine prootoneid neutronei e sisaldus d vesinikus 1 H Prootium Vesinik 1 0 1 99,98% D ehk 2 H Deuteerium Raske vesinik 1 1 1 0.015% T ehk 3H Triitium Üliraske 1 2 1 10-17 % vesinik 4 H 5 H 6 H 7 H Triitium termotuumarelv, vesinikupomm, kui kella osutid helenduvad pimedas rohekalt, siis on
se leegi. Propaan (C3H8) on normaaltingimustes värvitu ja lõhnatu põlevgaas. Propaani ja hapniku segu leegi temperatuur on 2600...2700ºC. Kasutusala: hapniklõikamine, värviliste metallide keevitamine ja jootmine, kuni 6 mm paksuse terase keevitamine, õgvendamine, painutamine, leegiga puhastamine. Vesinik (H2) on normaaltingimustes värvitu ja lõhnatu põlevgaas. Ta on üks kergemaid gaase, õhust 14,5 korda kergem. Teatud vahekordades õhu ja hapnikuga moodustab vesinik plahvatusohtlikke segusid. Seetõttu tuleb keevitustöödel rangelt täita ohutusnõudeid. Keevituskohale toimetatakse vesinik terasballoonides, gaasilises olekus rõhu all. Kasutusala: malmi, alumiiniumi, messini ja kuni 2 mm paksuse terase keevitamine. 6 Keevitusleek Keevitusleek moodustub põlevgaasi ja hapniku põlemisel. Leegi ülesanne on kuumutada ja
tootmine Pärmseened ja mõned bakterid kasutavad etanoolikäärimist. C6H12O6 2CH3CH2OH + 2CO2 (glükoos 2 etanooli + 2 süsihappegaasi) Etanoolkäärimine suhkru lagundamine mikroorganismide toimel Näiteid etanoolkäärimisest: taigna kergitamine, tekkiv alkohol aurustub Tsitraaditsükkel ehk Krebsi tsükkel ensüümide poolt katalüüsitavad reaktsioonid, mille käigus eraldub CO2 ja H aatomid Vahetult enne tsitraaditsüklit eraldub CO2 ning 2H. Vesinik seostatakse NAD molekuliga. Tekib NADH2/2NADH molekuli Püroviinamarihappest moodustunud kahesüsinikuline ühend, atsetüül CoA, siirdub tsitraaditsüklisse Tsitraaditsüklist tulemusena tekib 20 H aatomit, mis seonduvad NAD molekulidega, saadakse kokku 10NADH2 molekuli, mis lähevad edasi hingamisahelasse. Kõik vesiniku aatomid pole pärit algsest glükoosi molekulist, vaid tsüklisse sisenevast veest.
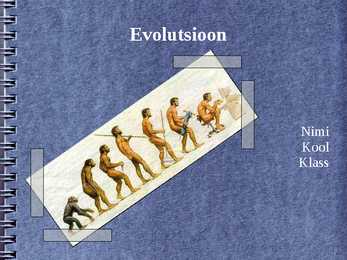
Evolutsioon Nimi Kool Klass Evolutsioon Mis on evolutsioon? Evolutsiooni vormid Füüsikaline evolutsioon Keemiline evolutsioon Bioloogiline evolutsioon Elu areng Maal Evolutsiooni tõendid Mis on evolutsioon Evolutsioon on ladina keelne sõna, mis tähendab lahtirullumist. Evolutsioon on pöördumatu ajalooline areng, järkjärguline mitmekesisemaks ja keerukamaks muutumine. Enamasti peetakse evolutsiooni mõiste kasutamisel silmas elu arengut Maal. Võib eristada nelja evolutsioonivormi: Füüsikaline evolutsioon Keemiline evolutsioon Bioloogiline evolutsioon Sotsiaalne evolutsioon Evolutsiooni vormid Füüsikaline evolutsioon Füüsikaline evolutsioon on ebapüsvate elementaarosakestest raskemate aatomite, tähetede, planeetide ja galaktikate teke ning edasine areng. 15 miljardit aastat tagasi tekkis universum. 5 miljardit aastat...
1. Anorgaanilised ained organismides on vesi, soolade ühendid. 2. Orgaanilised ained organismides on valgud, suhkrud, lipiidid ja nukleiinhapped. 3. Makroelemendid on mittemetallid: süsinik, hapnik, vesinik, lämmastik, fosfor, väävel. Mikroelemendid: raud, tsink, kaltsium, jood, magneesium, fosfor jne. 4. Keemiliste elementide ülesanded organismis: · C (süsinik) moodustab erinevaid molekulaarseid struktuure: lineaarsed (nt. valgud), hargnevad (nt. glükogeen), tsüklilised (nt. steroidhormoonid). · O (hapnik) aeroobsetes organismides oksüdeerija. Hapniku kaasabil lõhustatakse orgaanilised ühendid anorgaanilisteks. Hapniku baasil toodab
Vesinikuühendid mittemetallidega (vesiniku o-a 1). BH3 boraan, SiH4 silaan, AsH3 arsaan, NH3 asaan (trad. ammoniaak), N2H4 diasaan (trad. Hüdrasiin), PH3 fosfaan. Happed: H3BO3 boorhape boraat BO33-; H3AsO4 arseenhape arsenaat AsO43-; HONC fulmiinhape fulminaat ONC-. Madalama o-a korral kasut. -is ja -us liidet, aniooni nimetuse lõpuks on sel juhul -it. Mitu hapet, kus oksüdatsiooniaste on sama, väiksema H ja O meta-, suurema orto-. Hapnikuta hapete vesinik, mittemetall lõpuga -iid hape. Tiohapped tekivad O aatomi asendusel S aatomiga. Oksiidid: Rühma O-O sisaldavad oksiidid on peroksiidid. H2O2 vesinikperoksiidid; Na2O2 naatriumperoksiid; O3- osoniidid; O2- hüperoksiidid. Soolad: Kristallveega soolad hüdraat. Vesiniksoolad aat. Kordinatiivühendid e. Kompleksühendid: S2- tio-, sulfido-, CH3COO- atsetato-, O2- okso-, NH2- amido-, (asanido-), H2O akva-, CO karbonüül-, NH3 ammiin-, H2S sulfaan-.
paleontoloogiliste andmete järgi leitud aegu. Sordi ja tõuaretus- tõestab, et muutuvad aja jooksul. Keemiline evolutsioon- Oparin esitas seisukoga, et elu tekkele eelnes keemiline evolutsioon, mida võimaldasid noore Maa iseärasused. Selles pidi puuduma vaba hapnik, osoonikiht puudus, ürgookean. Atmosfäri läbid ultraviolettkiirgus, radioaktiivsus. Atmosfäär koosnes gaasidest nagu vesinik, lämmastik, ammoniaak, vesiniktsüaniid, metaan, süsinikoksiidid, vesiniksulfiidid ja veeaur. Leidus ka fosfaate. Keemilise evolutsiooni protsessid- 1 aste: bioloogiliste monomeeride teke(aminohapped, lämmastikalused, monosahhariidid, nukleotiidid) 2 aste: bioloogiliste polümeeride teke(polünukleotiidid, polüpeptiidid) 3aste: polümeermolekulide organiseerumine rakutaolisteks süsteemideks-see oli üleminek keemilistelt evolutsioonilt bioloogilisele
Mittemetalliliste elementide elementide maks oa võrdub rühma numbriga n, st väliskihi elektronide arvuga (nagu ka A- rühmade metallilistel elementidel). Minimaalne ehk madalaim oksüdatsiooniaste (kõige negatiivsem) on määratud elektronide arvuga, mida elemendi aatom saab keemilistes reaktsioonides oma väliskihti juurde võtta. Aautom saab väliskihti juurde võtta 8-n elektroni, madalaim oa on seega n-8 (n=rühma number). Erandiks on vesinik, mille aatom saab juurde võtta ainult 1 elektroni. Enamik mittemetallilisi elemente saab moodustada ühendeid ka vahepealsetse oksüdatsiooniastmetes. Paljudel nendest on küllaltki püsib rühma numbrist 2 võrra väiksem oa. Sel juhul on vastava elemendi aatom loovutanud ainult väliskihi p-elektronid, kuid s- alakihi elektronid on jäänud loovutamata. Minim oa esineb ühendites metallidega ja enamikel ühendis vesinikuga (va boor, räni,arseen vesinikust väiksem elektronegatiivsus)
Pindpinevuse tõttu 3) Keemiline- toitained muutuvad keemilise reaktsiooni tagajärel mitte lahustuvateks. Oleneb happelisusest.. 4) Bioloogiline- toitainete ained seotakse, mulla organismide poolt üles ehitamise jaoks 5) Füüsikaliskeemiline- mulla kolloidid seovad Mulla pH. happelisus Lubjatakse Liblikõielised ja kapsad kasutavad palju lupja Vihma veed Happeliste veede kasut. mineraalid Mulla reaktsiooni väljendatakse pH kaudu. Vabade vesinik ioonide 10nend logaritmi pH 3,5- väga happeline pH 3,6-4,5-tugevalt happeline pH 4,5-5,5-mõõdukalt happeline pH 7-neutraalne pH 7,3-leeliseline pH 10- aluseline Soostumine: esineb madalamatel pinnavormidel gleistumine,esimene etapp, liigniiskes anaeroobses õhu hapniku puudumisel mikroorganismid kasutavad mineraal ühendites oleva hapniku. 2valentne raud( Fe 2+)
a) hapetega sool ja vesi. Toimub alati. vesilahustes vesinikioonideks ja happe- oksiididega, tekib sool ja vesi: Reageeriv metall peab olema aktiivsem, kui soola koostises omadused b) veega leelis. Ainult aktiivsete metallide anioonideks. CO2+Ca(OH)2 CaCO3+ 2H2O olev metall. oksiidid. 2) Reageerivad metallidega sool ja vesinik. 2) Reageerivad hapetega sool ja 2) Reageerivad hapetega uus sool ja uus hape. Peab tekkima c) happeliste oksiididega happelisele oksiidile 3) Reageerivad aluseliste oksiididega sool vesi. võetud happest nõrgem või lenduvam hape. vastava happe sool. ja vesi, toimub alati
Keemiline side on mõjujõud elementide aatomite vahel ühendis. Keemilise sideme tekkimisel läheb aatom üle püsivasse olekusseja selle käigus vabaneb energia Keemilise sideme liigid: *Kovalentne side, mis moodustub ühiste elektronipaaride abil välise elektronkihi paardumata elektronide vahel *Iooniline side, moodustub erinimeliselt laetud ioonide vahel *Metalliline side, moodustub metalli attomitest ja elektronidest.tekkiva sidemetüübi üle saab otsustada suhtelise elektronegatiivsuse abil Suhteline elektronegatiivsus iseloomustab elementi aatomivõimet siduda elektrone keemilise sideme moodustumisel Ühikuks on võetud liitiumi aatomi võime siduda endaga elektrone Kovalentne side <1,7< Iooniline side Metallilise sideme korral metallvõre sõlmpunktides asuvad metalli ioonid ja aatomid Nende aatomite ja ioonide vahel liiguvad ühised väliskihi elektronid H-side molekulidevaheline side, mida ei eksisteeri kuskil mujal, saab tekkida ühendites, k...
Keemilised omadused: Metallid jaotuvad aktiivseteks, keskmise aktiivsusega ja mitteaktiivseteks. Metallid on redutseerijad ehk nad loovutavad elektrone. Reageerimine lahjendatud hapetega (v.a HNO3) o Pingereas vesinikust paremal pool olevad metallid ei reageeri lahjendatud hapetega. Ca + HCl CaCl + H2 Reageerimine veega o Aktiivsed metallid (K-Na) reageerivad veega, tekivad hüdroksiid ja vesinik. Na + H2O NaOH + H2 o Keskmise aktiivsusega metallid (Mg-Fe) reageerivad veeauruga, tekivad oksiid ja vesinik. Zn + H2O ZnO + H2 o Väheaktiivsed metallid (Ni-Au) ei reageeri veega. Au + H2O Reageerimine soola lahustega o Metall reageerib vees lahustuva soolaga, kui ta on aktiivsem kui soola koostises olev metall. Fe + CuSO4 FeSO4 + Cu Cu + FeSO4
Arvatakse, et planetesimaalide kokkupõrgete ning kokkusulamiste käigus tekivad protoplaneedid, mille sisemusse koonduvad raskemad elemendid ning väliskihid koosnevad põhiliselt erinevatest gaasidest. Kui tekkiv täht lõpuks süttib, puhutakse tähe ümbrus väga tugeva tähetuule poolt suhteliselt kiiresti gaasist ja väga peenikesest tolmust puhtaks. Ajapikku kaotavad tähele lähimad või väiksema massiga protoplaneedid oma atmosfäärist suure osa kergetest gaasidest (nagu vesinik ja heelium), põhjuseks noore tähe soojendav mõju ning planeetide väike mass, mille tõttu nad ei suuda kiiresti liikuvaid gaasimolekule kinni hoida. Öpik-Oorti pilvega. ... Öpik-Oorti pilv on hüpoteetiline komeetidest koosnev sfääriline pilv umbes
Küllastumata süsivesinikud. II poolaasta tasemetöö kordamiseks Küllastumata süsivesinik- süsiniku aatomite vahel võib esineda kaksik- või kolmiksidet. Alkeen- süsiku aatomite vahel kaksiksidemed een, Eteen C2h4. Alküün- süsiniku aatomite vahel kolmiksidemed üün, Etüün C2H2. Hüdrogeenimine- vesiniku molekuli liitmine keemilise reaktsiooni käigus. Hüdraatimine- keemiline liitumisreaktsioon veega. Nitreerimine- nitrorühma (NO2) viimine orgaanilise ühendi koostisse. Benseeni füs omadused- värvusetu, veest kergem, iseloomuliku lõhnaga vedelik, vees ei lahustu, lahustub bensiinis ja etanoolis. Karbonüülühendid- sisaldavad karbonüülrühma ehk süsinikku, mis on kaksiksidemega seotud hapniku külge. Aldehüüdid- keemilised ühendid, mis sisaldavad põhilise funktsionaalse rühmana aldehüüdrühma (CHO), Pentanaal, aal. Ketoonid- ühendid, milles karbonüülrühm (C=O) on seotud kahe süsiniku aatomiga, propanoon, -oon. Karboksüülhape- happ...
+ sool = + vesi = hape Happeline oksiid + alus = sool + vesi + aluseline oksiid = sool Happed + alus = sool + vesi + aluseline oksiid = sool + vesi Hape + sool = uus sool + uus hape (uus hape peab nõrgem olema või uus sool mittelahustuv) + metall = sool + vesinik (metall peab aktiivsuse reas vesinikust eespool olema, ära vali HNO3) Alused + hape = sool + vesi + happeline oksiid = sool + vesi * Alus + sool = uus alus + uus sool (lähteained peavad vees lahustuma, vähemalt üks saadustest mitte) t° = aluseline oksiid + vesi (lahustub va. NaOH ,KOH )
Reaktsioonivõrrandis Mittemetallioksiidid + Vesi = Hape Sool + Hape = Uus hapse + Uus sool SiO2 (liiv) veega ei reageeri Tekkiv hape peab olema algsest nõrgem Metallioksiidid + Vesi = Alus Sool + Sool = Sool + Sool Ainult IA/IIA metallid Lähteained peavad vees lahustuma. Üks tekkivatest ainetest peab sadestuma Hape + Alus = Sool + Vesi Metall + Hape = Sool + Vesinik (H2 ) Metall pingereas vesinikust eespool Mittemetallioksiid + Alus = Sool + Vesi Metall + Mittemetall = Sool Metallioksiid + Hape = Sool + Vesi IA/Ca alarühma metallid + Vesi = Alus + H2 Metallioksiid + Mittemetallioksiid = Sool Zn/Al/Cr/Fe + Veeaur = Oksiid + H2 Sool + Alus = Alus + Uus sool Metall + Sool = Sool + Metall Lähteained peavad vees lahustuma. Reaktsiooni asuva metall peab olema soola omast
1. C 4 üksiksidet 2. C 1 kaksikside radikaalid 2 üksiksidet 3. C 2 kaksiksidet 4. C 1 kolmikside 1 üksikside lämmastik hapnik vesinik N -III O -II H -I 1. 1. 1. N O H 2. N O 3. N
Sahariidid- ssivesikud,orgaanilised hendid,koostis : ssinik,vesinik,hapnik. Mono-,oligo-,polsahhariidideks. Suhkrud. Monosahariidid: lihtsuhkrud,madamolekulaarsed orgaanilised hendid,ssinike aatomite arv on tavaliselt kolmest kuueni. Olulisemad on riboos ja desoksriboos. Need ribonukleiinhappe rna ja dna koostises. Kuuessinikulistest suhkrutest olumised on: glkoos ja fruktoos. C6H12O6,fotosnteesi abil. Loomad savad aga toidust. 17,6 kJ/g salvestatud energiat saab kasutada elutegevuses. Oligosahhariidid- madalmolekulaarsed orgaanilised hendid, kahe-kolme monosahariidi omavahelisel hinemisel. Maltoos koosenb aga kahest glkoosijgist. Piimas sisaldub laktoos e piimsuhkur, energia saamiseks. Polsahhariidid on krgemolekulaarsed orgaanilised hendid (polmeerid), (monomeerid) monosahariidid? Trklis,tselluoos ja glkogeen. Trklis peamise polsahhariide.keskmiseks 1 miljon molekulmass. Taimed kasutavad trklist energia saamiseks. Lagundavad gl...
KORDAMISLEHT 1. Karboksüülhapped ühendid, mis sisaldavad karboksüülrühma COOH Estrid ained, mis tekivad karboksüülhapete reageerimisel alkoholidega Amiidid karboksüülhappe funktsionaalderivaadid, kus karbonüülrühma kuuluva OH rühma asemel on aminorühm. 3. 1) Happed reageerivad aktiivsete metallidega sool +vesinik. 2) Happed reageerivad metallioksiididega sool+vesi. 3) Happed reageerivad alustega sool+vesi. 4) Happed reageerivad nõrkade hapete sooladega (reeglina karbonaadid ja sulfiidid) sool+uus hape. 5) Happed reageerivad alkoholidega ester+vesi. 4. Metaanhape ehk sipelghape HCOOH terava lõhnaga, ärritava toimega mürgine vedelik, kasutatakse keemiatööstuses. Mesinikud kasutavad kahjuritõrjeks. Sipelghapet leidub kõrvenõgestes ja sipelga mürgis. Ilmutab ka aldehüüdide omadusi. Etaanhape ehk äädikhape CH3COOH kõige tuntum ja kasutatavam karboksüülhape. Pole mürgine. Kasutatakse tööstuses lahustina ning palju...
renaturatsioon on valgustruktuuri taastumine, denaturatsioon on valgustruktuuri muutmine. 4. Nimeta RNA ja DNA ülesanded RNA: informatsiooni kopeerimine ning transportimine informatsiooni realiseerimiseks DNA: päriliku info säilitamine ja selle täpne ülekanne tütarrakkudele 5. Mis on komplementaarsus? 6. Missugust ülesannet täidab transport RNA? transpordib aminohappeid ribosoomidesse 7. Millest koosnevad sahhariidid? süsinik, vesinik, hapnik 8. Milles seisneb vee bioloogiline tähtsus? hoiab ära ülekuumenemise, kindlustab organismide siseelundkondade töö, kaitsefunktsioon (pisarad), hoiab organismisisest temperatuuri, on hea lahusti 9. Mille poolest erinevad RNA ja DNA? DNA's on desoksüribonukleiinhape, koosneb kahest ahelast; RNA's on ribonukleiinhape, koosneb ühest ahelast, puudub biheeliks 10. Joonista DNA ja RNA nim. Osad 11. Mis on rasvad?
Glükoosi lagundamine ja fotosüntees. Glükoosi lagundamisel võime eristada kolme etappi: glükolüüsi, tsitraaditsüklit jahingamisahela reaktsioone. Glükoosi algne lagundamine ehk glükolüüs toimub päristuumsete rakkude tsütoplasmavõrgustikus, tulemusena tekib püroviinamarihappe(CH3COCOOH) eraldub vesinik ja kaasneb 2 ATP süntees. Püroviinamari happe lagundamine jätkub tsitraaditsüklis eraldub 4H aatomit mis seostuvad vesinikandja NAD'iga. Toimub vaid O2 juuresolekul nim aeroobseks. Anaeroobne glükolüüs ehk käärimine lõpeb kas piimhappe või etanooli moodustamisega. (C2H4OHCOOH) Tsitraadi tsükkel, toimub mitokondri sisemuses, lagundatakse püroviinamarihappet. Tsitraaditsükkel koosneb ensüümide poolt katalüüsitavatest reaktsioonidest, mille käigus
N: CaO + 2HCl --) CaCl + H2O PH · PH > 7 aluseline NaOH · PH < 7 happeline HCl · PH = 7 neutraalne H2O Võrrandid · (tugevalt)Aluseline oksiid + vesi --) alus Na2O +H2O --) 2NaOH · (nõrga)aluse sool + leelis --) (tugevalt)aluse sool+ nõrk alus CuSO4 +2NaOH --) NaSO4 + Cu(OH)2 · Leelismetall + vesi --) leelis + vesinik Leelismuldmetall 2Na + 2H2O --) 2NaOH + H2 ALUSTE NIMETAMINE · Kui B-rühma metall siis sulgudesse tuleb öelda oksutatsiooni aste. Cr(OH)3 kroom(3)hüdrooksiid · Kui A-rühma metall siis ütled elemendi nime ja kohe järgi hüdrooksiid NaOH naatriumhüdrooksiid
Nafta Pelgulinna Gümnaasium 11.c klass Sigrid Praats Mis on nafta? · Nafta on maakoorse leiduv peamiselt vedelate süsivesinike segu Nafta keemiline koostis: · süsinik (82...87%) · vesinik (12...15%) · väävl(1,5%) · lämmastik (0,5%) · hapnik (0,5%). Naftat moodustavad ühendid: · Parafiinid(CnH2n+2 ) · Nafteenid(CnH2n ) · Aromaatsed ühendid(CnH2n-6 ) Rafineerimine · Selle käigus puhastatakse nafta väävlist,sest väävel tekitab palju keskkonnaprobleeme. Nafta omadused · On väga tuleohtlik · Erikaal on muutlik, kuid väiksem kui veel · Värvus peaaegu läbipaistvast kuni mustani
keerukamad orgaanilised ühendid. Millerurey eksperiment 1952 sooritatud, avaldatud 1953. aastal Univesity of Chicago H2 CH4 NH3 H2O Saagiks 4 erinevat aminohapet Urey Miller Katseseade Katse UUS analüüs Milleri kunagine õpilane Jeffrey Bada Üle 50 aastat vanad proovid 11 asemel 22 aminohapet Vulkaanilisi aure asendava klaasi tulemused olid parimad Jeffery Bada Elu on siiski pärit maalt Vulkaanipursetes tekkinud vesinik kaob elu tekkeks sobivate tingimuste kujunemiseks atmosfäärist liiga kiiresti. Päike on umbes 30% võrra tuhmim. Tingimused elu tekkeks meie planeedil olid igati sobilikud. Aitäh!
Redoksreaktsioo On reaktsioon mille käigus muutub elementide o-a Oksüdeerija Liidab elektrone, o-a väheneb ja tema redutseerub Redutseerija Annab elektrone ära, o-a suureneb ja tema oksudeerub Elektrolüüs On elektrolüüdide laugunemine alalisvoolu toimel. Kaks elektrolüüdi on panud elektrolüüdide lahusesse ja ühendatud vooluallikaga klemmidega Katiood Negatiivne elektrood, redutseerub Anioon Positiivne elektood, oksüdeerub Elektrolüüdide kasutamine 1.Toodetakse aktiivseid metalle(Na, K, Ca, Mg) 2.Toodetakse kloori, vesinikku ja hapnikku 3.Metalli pinde kaetakse teise metalli kihiga 4.Rafineerimine aine puhastamine ebasoodsatest lisanditest. Keemiline Vooluallikas On seade milles keemilisel reaktsioonil on saadud energia muudetakse elektrienergiaks. Koosneb kahest elektroodist mis on pandud elektrolüüdide lahusesse. Galvaanielement on ühekordne keemiline vooluallikas, aktiivsem metall on aniooniks ja temalt hakkavad el...
aminohappejääkidest. Valke on eelkõige vaja organismide ülesehituseks, kaitseks, ja metabolismi tagamiseks. Lihtvalgud- valgud mis koosnevad vaid aminohapetest, ning on organismile kergesti omandatavad . Näiteks munavalges leiduv albumiin Liitvalgud- valgud , mis koosnevad valgulisest ja mittevalgulisest osast. Näiteks hemoglobiin on rauda sisaldav valk Aminohape- orgaaniline ühend , mis sisaldab karboksüülrühma ja aminorühma. Aminohapped sisaldavad( C.H.N.O.S ehk süsinik,- vesinik,-lämmastik ja hapnik ) Asendamatud aminohapped- aminohapped, mida inimese organism ei suuda ise toota. Täiskasvanud inimesel on neid 8 ja laste puhul 10 Valkude struktuur: 1. Primaarstruktuur- selles on märgitud aminohapete järjestus ( aminohapped on seotud peptiidsidemetega ) 2. Sekundaarstruktuur- moodustub polüpeptiidi keerdumisel alfa heeliksiks. Näiteks küünte ja juuste valgud on sekundaarstruktuuri valgud 3
ühenditest keerukamad ühendid. Milliseid nendest mõistetest ja kus on teile juba räägitud. Olin enne kuulnud selliseid mõisteid nagu rasvad, valgud ja sahhariidid oma erialastes tundides. Kuidas on biokeemia seotud teie õpitav erialaga? Biokeemia on seotud toitumise ja erinavte toiduainetega. Kui ma õpin pagariks, siis on see väga oluline teada, kuidas erinevad toitained kehale mõjuvad. Milliste keemiliste elementideta me hakkama ei saaks? Hapnik, vesinik, magneesium, kaltsium, naatrium, raud, jood. Millistest orgaanilistest ainetest koosneb meie toit (lisa ka antud ainete ülesanded)?