Keemilised elemendid jaotatakse: metallid, mittemetallid ja poolmetallid. 6. Lihtaine- kindlate füüsikaliste ja keemiliste (tihedus, keemis- ja sulamistemp., värvus, kõvadus) omadustega aine mis koosneb ühe ja sama elemendi aatomitest. 7. Liitaine- aine mis koosneb erinevate elementide aatomitest. (nt: vesi koosneb vesinik+ hapnik) Ained võivad olla vedelas, tahkes või gaasilises olekus. 8. Allotroopia- üks ja sama keemiline element võib esineda mitme lihtainena. Nt: süsinik võib esineda nii grafiidi, teemandi, karbüüni kui ka fullereenidena.. Sellist nähtust nim. allotroopiaks. (hapniku allotroopsed teisendid on monohapnik, dihapnik ja trihapnik. 9. Aatomi mass ja aatommass- aatomite mõõtmed ja mass on väga väikesed. Arvutuste hõlbustamiseks kasutatakse suhtarve, kusjuures ühikuks on 1/12 süsiniku aatomi massist. Seda ühikut nim rahvusvaheliseks aatommassiühikuks (1.6*10 astmes-27kg) Aatommass on ühikuta suurus, tegemist on suhtarvudega. 10
maitsestamiseks ja konserveerimiseks. 2) KCl kaaliumkloriid kaaliumväetis 3) ZnCl tsinkkloriid puidu immutusvahend mädanemise vastu 4) CaCl kaltsiumkloriid õhu kuivatamiseks eksikaatoris 5) AgCl hõbekloriid valgustundlikkuse tõttu kasutatakse seda fotopaberite valmistamisel 17 Cl 7 35,453 8 Kloor 2 Süsinik Süsinik asub keemiliste elementide perioodilisustabelis teises perioodis ning IVA rühmas. Süsiniku aatomnumber on 6 ning aatommass on 12,01115. Süsiniku aatomi elektronskeem on C: +6|2)4). Reaktsiooni käigus süsinik ei loovuta elemente ning moodustab neli kovalentset sidet. Süsiniku eripära võrreldes teiste keemiliste elementidega on moodustada arvukalt erinevaid ühendeid. Süsinik on mittemetall. Süsiniku
· Alkaanide omadused · Alkeenide omadused ja saamine · Hüperkonjugatsioon · Alküünide omadused Orgaaniline keemia · Orgaanilise keemia all mõistetakse üldiselt süsinikuühendite keemiat, kuigi täpse piiri tõmbamine on siin raske. Reeglina mõistetakse orgaaniliste ühendite all C, H, O, N ja halogeene sisaldavaid ühendeid. · Elementorgaanilise keemia all mõistetakse selliste ühendite keemiat, kus süsinik on seotud mõne metalli või eelpool nimetamata mittemetalliga. Süsivesinikud · Süsivesinikud on ühendid, mis koosnevad vaid süsiniku- ja vesinikuaatomitest. · Süsivesinikud moodustavad orgaanilise keemia aluse. Vahel ongi orgaaniline keemia defineeritud kui süsivesinike ja nende derivaatide keemia. 1 Süsivesinikud
tõttu. · Peale selle omavad metallid kõrgetel temp. suuri plastseid deformetsioone. · Samas on metallid aga head soojad- ja elektrijuhid (oleneb olukorrast) Metallid jaotatakse mustadeks ja värvilisteks (nt teras ja vask) Tegelikult võiks jaotada ka rauda sisaldavateks ja mittesisaldavateks metallmaterjalideks(nt terased ja malmid ning alumiinium, vask, tsink jne) · Mustad metallide koostis on põhiliselt raud (Fe) ja süsinik (C) mitmesugustes vahekordades. · Lisanditeta raud ehituses ei kasutata ta omadused pole selleks sobivad. Rauale lisatavad elemendid määravad tema omadused ja kasutamisviisid. · Põhimõtteliselt jaotatakse mustad metallid: terasteks ja malmideks. Mustad metallid Malmid. · Süsinikusisaldus malmides 1,7%. Tavaliselt sisaldavad malmid süsinikku 2...4% ja rohkem · Malmid jaotatakse valgeteks ja hallideks malmideks. · Valges malmis e
SÜSÝNÝK Hanna Ulrika Eltmaa, 11B Süsinik kui keemiline element Moodustub kolme heeliumi tuuma ühinemisel Väliskihis neli elektroni Oksüdatsiooniaste saab olla vahemikus 4 kuni +4 4 keemilist sidet kaks stabiilset isotoopi massiarvudega 12 ja 13 10 miljonit erinevat ühendit Taimede, loomade ja inimeste rakud Süsiniku keemilised sidemed Süsivesikud, rasvad, aminohapped Kofeiin Süsinik lihtainena Allotroopia Teemant Grafiit Fullereenid ja nanotorud tuntuim fullereen C60 Süsiniknanotoru Teemant Grafiit Väga kõva materjal · Süsiniku tavatingimustes stabiilseim vorm Juhib hästi soojust ...
Radioaktiivne kiirgus ja selle kasutamise võimalused Radioaktiivne kiirgus ● Tekib looduslikes tingimustes radioaktiivsete elementide ebastabiilsete tuumade lagunemisel ● Samuti kergete tuumade ühinemisel vesinikupommi lõhkemisel ja tähtede termotuumareaktsioonis Radioaktiivsuse liigid Alfakiirgus ● Koosneb kahest osakesest - kahest prootonist ja kahest neutronist koosnevatest heeliumi aatomituumadest ● Rasked, suure laenguga ja aeglased ● Varjendiks piisab paberilehest Radioaktiivsuse liigid Beetakiirgus ● Koosneb beetaosakestest - kas elektronist või positronist ● Läbimisvõime alfaosakestest suurem ● Teisese kiirgusena tekib ka röntgenkiirgus ● Varjestamiseks piisab õhukesest metall-lehest, näiteks alumiiniumilehest. Radioaktiivsuse liigid Gammakiirgus ● Koosneb suure energiaga gammakvantidest ● Inimesele ohtlikuim tänu suurele läbimisvõimele ● Kuna gammakvandil puudub elektrilaeng, siis nad elektromagnetväljas ei pi...
ja maitsetu. Kasutatakse gaasilise kütusena. Segu õhust ja metaanist plahvatab kergesti. Aatomid seotud 4 kovalentse üksiksidemega. C keskel, Hd igas ilmakaares ümber. Metaan on teisisõnu maagaas. Tekib ka orgaanilise aine lagunemisel nt. Prügilates. Metaani põlemine Ch4 + 2 O2 --- Co2 + 2 H2O Mida suurem on oksüdatsiooniastme muutus, seda suurem on kütteväärtus. Selles võrrandis on süsiniku oa muutus 8 ja see on ka maksimaalne. Co ehk süsinik monooksiid ehk vingugaas Mittetäielik põlemine lõpeb vingugaasiga. Süsiniku oksüdatsiooniaste on siin 2. Co saab võimaluse korral oksüdeeruda edasi Co2ks. Co on neutraalne oksiid. Hapete ja alustega ta ei reageeri. Co2 ehk süsinik dioksiid Põlemise lõppsaadus. Võib reageerida veega ja aluseliste oksiidisega. Tekib sool. Co2 ei põle ega toeta põlemist. Co ja Co2 abil saab metallurgias metalle toota Gaasiliste ainete ruumalad ja molaarsuhted langevad kokku!!!
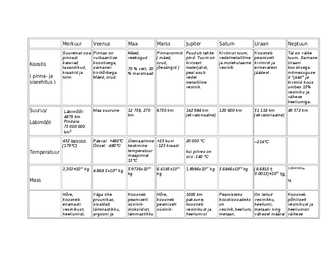
Merkuur Veenus Maa Marss Jupiter Saturn Uraan Neptuun Suuremat osa Pinnas on Mäed, Pinnavormid Puudub tahke Kivimist tuum; Koosneb Tal on väike pinnast vulkaanilise veekogud ( mäed, pind. Tuum on vedelmetalliline peamiselt tuum. Sarnane Koostis katavad koostisega, orud, kivisest ja molekulaarne kivimist ja Uraani tasandikud, sarnanev 70 % vett, 30 jõesängid ) materjalist, vesinik. erinevatest koostisega: kraatrid ja kivikõrbega. % maismaad peal asub jäädest mitmesuguse ( pinna- ja tolm Mäed, orud. vedel ...
Looduses võivad mittemetallid esineda mitmete allotroopidena ehk esineda mitme lihtainena. Paljud mittemetallid on halvad elektrija soojusjuhid. Lihtainetes on aatomite vahel kovalentne side ehk ühiste elektronpaaride vahendusel aatomite vahel moodustuv keemiline side. Metallidega reageerimisel toimivad mittemetallid oksüdeerijana. Mittemetallid ja nende ühendid looduses ning kasutusest keskkonda sattumisel · Süsinik. Süsinikku on elusa looduse peamine koostisosa, omandatakse taimede poolt fotosünteesiprotssesis. Süsinikku leidub looduses nii ehedalt (grafiidina, teemandina) kui ühenditena nagu näiteks: lubjakivi, marmor, kriit, dolomiit, sooda. Süsinkurikkad on ka orgaanilised kütused: biomass turvas pruunsüsi kivisüsi antratsiit 50% C 55% 65% 6873% 79% C
VASTAN KÜSIMUSTELE ÕP LK 25 1) NIMETAGE ORGANISMIDE PEAMISI KEEMILISI ELEMENTE? V: Organismide peamised keemilised ühendid on hapnik (O), süsinik (C), vesinik (H) ja lämmastik. 2) MILLISED KEEMILISED ELEMENDID KUULUVAD MAKROELEMENTIDE HULKA? V: Makroelementide hulka kuuluvad fosfor (F), väävel (S), kaalium (K), naatrium (Na), Magneesium (Mg), kaltsium (Ca) ja kloor (Cl). 3) MIKS VAJAB ORGANISM MAKROELEMENTE SUHTELISELT SUURTES KOGUSTES? V: Organism vajab mikroelemente suhteliselt suurtes kogustes seetõttu, et need moodustavad suure osa organismi koostisest. 4) MILLISED KEEMILISED ELEMENDID ESINEVAD KÕIGI ORGAANILISTE
Viis naftasaadust: bensiin, diislikütus, määrdeõlid, masuut, bituumen. Mitu sidet on tavaliselt süsiniku, hapniku, lämmastiku ja vesiniku aatomil? Süsinik: 4 sidet (4 üksiksidet, 1 kaksiksideme ja 2 üksiksidet, 2 kaksiksidet, 1 üksik- ja 1 kolmiksideme. Hapnik: 2 sidet ( 2 üksiksidet, 1 kaksikside). Lämmastik: 3 sidet (3 üksiksidet, 1 kaksik- ja 1 üksikside, 1 kolmikside). Vesinik: 1 side Miks on süsinikuühendeid palju rohkem kui teiste elementide ühendeid? Süsinik asub perioodilisustabelis oma perioodi keskel. Moodustab sidemeid mitmesuguste teiste aatomitega, ka süsiniku aatomitega. Süsiniku aatomid võivad olla mitmesugustes olekutes. Etanool: C2H5OH Vänge lõhnaga, läbipaistev, lahustub vees hästi, alkohoolsete jookide tootmiseks, ravimite tootmiseks, ilutööstuses. Etaanhape: CHCOOH ehk äädikhape. Hapuka maitse ja lõhnaga söövitav vedelik, mis seguneb veega. Lahja lahusena kasutatakse toitude maitsestamiseks ja marineerimiseks.
1. Millistest keemilistest elementidest koosnevad peamiselt orgaanilised ained? Orgaanilised ained koosnevad alati süsinikust(C), sageli ka vesinikust(H), hapnikust(O), lämmastikust(N) ja ka väävlist(S), halogeenidest ja metallidest. 2. Miks on orgaaniliste ainete hulk väga suur? Sest süsinik on võimeline moodustama väga pikki ja keerulisi ahelaid(hargnenud, tsükliline ja normaal- ehk lineaarahel); süsinik moodustab 4 püsivat kovalentset sidet; C moodustab nii üksik-, kaksik- kui kolmiksidemeid. 3. Mitu kovalentset sidet on võimelised moodustama järgmised keemilised elemendid: C, H, N, O? C- 4 sidet; N- 3 sidet; O- 2 sidet; H- 1 side 4. Selgita ja oska koostada: 1. Summaarne valem - nt C₃H₈O; näitab, millised ained on valemis 2. Lihtsustatud struktuurivalem - nt CH₃CH₂CH₂OH; näitab ära aatomite rühmad 3
kriniaarireaktiivi liitumine karbonüülühendile ja ammiini liitumine karbonüülühendile. Karbonüülühend võis olla kas aldehüüd või ketoon. 3. Aldoolreaktsioonid Tähelepanu pöörata karbohappelistele vesinikele, ketoenoolsele tautomeeriale, karbaniooni teke Kõige lihtsamat tüüpi aldoolkondensatsioon kui juba seda teada, siis on väga hea (kus üheltpoolt karbanioon ja teisteltpoolt karbonüülrühma süsinik kui elektrofiil annavad sideme moodustub süsinik süsinik sideme) Tekivad aldoolid (aldehüüdi ja alkoholrühma sisaldavad ühendid) ja võib tekkida ka krotoonne produkt - peame teadma mis see on Ei tule : reaktsioone mis toimuvad alfa vesinike juures või alfa süsinike juures neid alküülimisi ja mida iganes. Ei tule ka kondensatsioone estritega. 4. Karboksüülühendite reaktsioonid teine suurem teema. anhüdriidid halogenanhüdriidid
Vee jahutuskiirus tagab martensiidi tekke, õli ja õhk mitte neis tekivad erinevad ferriidi ja tsementiidi segud. Süsinik ei jõua polümorfsel muutusel eralduda, üleküllastunud tardlahus a-rauas ehk martensiit. Süsiniku üleküllus deformeerib kristallstruktuuri ja kuupvõre muutub tetragonaalvõreks. Tekivad sisepinged, mis teevad materjali kõvemaks ja hapramaks (ei saaks kasutada enamikus rakendustes). Kriitilisest aeglasemalt jahutades austeniidist ferriidi tekkimisel eraldub süsinik, millest moodustuvad karbiidid. Tegemist on alaeutektoidterasega, seega peaks kõvadus olema 60+ HRC. Isegi õhus jahutades jäävad materjali sisepinged. Seepärast tuleb kasutada lõõmutamist, et vähendada maksimaalselt sisepingeid. Õhus jahutatud materjalid on veel plastselt töödeldavad, kuna ta läheb põhimõtteliselt algolekusse tagasi. Möötetulemused, mis on õli ja õhu kohta, on tõenäoliselt ebatäpsed, sest kõvadus jääb samasse suurusjärku.
· Millisel juhul lämmastik oksüdeerub, millisel juhul redutseerub, millisel juhul pole tegemist redoksreaktsiooniga? NH3 N3- NO3- NO2 N2 NO NO3- NH4+ ÜLESANDED · Kirjuta reaktsioonivõrrand, kus... Hapnik oleks oksüdeerija Broom oleks oksüdeerija Lämmastik oleks redutseerija Vesinik oleks oksüdeerija Vesinik oleks redutseerija ÜLESANDED · Kirjuta kolme süsinikühendi valem, kus... Süsinik saab olla vaid redutseerija Süsinik saab olla vaid oksüdeerija Süsinik saab olla nii oksüdeerija kui redutseerija ÜLESANDED · Kuidas võivad redoksreaktsioonides käituda järgmised osakesed? N3- SO32- S NO3- Cl- ClIII Süsinik CH4-s PH3 S2- BrVII HNO3 HNO2 ÜLESANDED · Kirjuta skeemile vastavad reaktsioonivõrrandid: C CH4 CO CO2 H2CO3
Orgaaniliste ainete koostis: 1)Makroelemendid(palju): C (süsinik) O(hapnik) H(vesinik) P(fosfor energia salvestamine, ATP oragnismi energiaühik) S(väävel) N(lämmastik aminohapped, ehk valgud) 2)Mikroelemendid(vähe): Fe(raud- hemoglabiini koostises, hapniku transport kehas) Mg(magneesium) Ca(caltsium) J(jood) Anorgaanilised ained: 1 ) Vesi : thermoregulatsioon, ainete lahustamine, rakusisene rõhk turgor, jääkide eemaldamine, ainete transport Sahhariidid (süsivesikud) 1) Monosahhariidid koosnevad 3-6 C(süsinik) Alati suhkrud ja magusa maitsega! Riboos ja desoksüriboos nukleiinhapete koostises, ehk märksõna DNA Nt: glükoos ja fruktoos 2)Oligosahhariidid koosnevad 2-3 MONOsahhariidist nt: Laktoos (piimas sisalduv suhkur) 3)Polüsahhariidid koosnevad paljudest MONOsahhariididest EI OLE suhkrud Nt: Kitiin(koorikloomade kooriku koostis), Tselluloos(taimede koostises) Tärklis energiavaru allikas taimedel Glükogeen ene...
1. Võrdle elus- ja eluta looduse keemilist koostist. -Elusloodus: H-vesinik N-lämmastik O-hapnik P-fosfor C-süsinik S-väävel -Elutaloodus: Fe-raud O-hapnik Si-räni Mg-magneesium S-väävel Ni-nikkel Ca-kaltsium Al-alumiinium 2. Nimeta 6 tähtsamat makroelementi biomolekulides. -VESINIK -SÜSINIK -LÄMMASTIK -HAPNIK -FOSFOR -VÄÄVEL 3. Mikroelementide ülesanded organismis. -KALTSIUM-Osaleb vere hüübimisel ja lihaste kokkutõmbumisel. -RAUD-Kuulub vere punaliblede koosseisu ja osaleb hapniku trantspordis. -FLUOR-Kaitsebhambaemaili ja soodustab kaltsiumi ladestumist hammastesse. -JOOD-Osaleb kilpnäärme töös ja kilpnäärmehormoonide ja valkude sünteesis. -NAATRIUM JA KAALIUM-Osaleb ainete trantspordis rakku ja rakust välja ning närviimpulsside töös. -MAGNEESIUM-Kuulub klorofülli koostisesse. 4. Vee omadused, vee ülesanded rakkudes ja organismis. -Vesi tagab rakkude siserõhu. -Vesi osaleb keemilistes reaktsioonides. -Vett on vaja organismide paljun...
Organismide koostis Keemiline koostis · ained · keemilised elemendid Anorgaanilised Orgaanilised Mineraalained Süsinik, vesinik, hapnik Hapnik CHO, Sellest moodustab peamiselt vesi. 1. Anorg. Vesi- lahusti reagtsioonid- oksuteerumine(hingamine) 2. Kaalium-naatriumioonid- närviimpulss- 3. Kaltsium- luude tugevus- haprus- 4. Magneesium- DNA ja RNA 5. Raud- Punaliblede koostisosa- Hemoklobliin- higamisel vajalik hapniku siduja 6. Anioonid- Karbonaat- hingamise läbi viiad 7. joodid- kilpnääre 8. orgaanilised ained- süsinik, vesinik, hapnik 1. Sahariidid
mittemetalle? · Nende ehitusest tulenevalt ükski mittemetall ei ole hea elektri- ega soojusjuht (välja arvatud süsiniku allotroop grafiit). Sellest tulenevalt koosnevad elektri- ja soojusisolatsiooni materjalid mittemetallidest. Lisa! · Kui metallid olid enamasti tahked ained, siis mittemetallid on enamasti gaasid (hapnik, vesinik, lämmastik, fluor, heelium jne) või ka vedelikud (broom) ja tahked ained (väävel, süsinik, räni, jood jne). · Kuigi mittemetallilisi elemente on võrreldes metallidega vähe, on nende omadused väga erinevad ja üldistada on raske. Eelnevale võib lisada veel, et mittemetallilised elemendid võivad esineda mitme lihtainena. Sellist nähtust nimetatakse ALLOTROOPIAKS ja neid erinevaid lihtaineid nimetatakse ALLOTROOPSETEKS TEISENDITEKS. ALLOTROOPIA: · Allotroopia on nähtus, mis seisneb selles, et sama keemiline element võib esineda mitme
*Mustade metallide koostis on põhiliselt raud(fe) js süsinik(c)mitmesugustest vahekordades. *Lisandite rauda ehituses ei kasutata ta omadused pole selleks sobivad.Rauale lisatavad lisandid määravad tema omadused ja kasutamisviisi. *Põhimõtteliselt jaotatakse mustad metallid:terasteks ja malmideks. *Süsiniku sisaldus malmides C 1,7%Tavaliselt sisaldavad malmid süsiniku 2...4% ja rohkem. *malmid jaotatakse valgeteks ja hallideks malmideks. *valges malmis ehk toormalmis sisalduv süsinik on seotud raudkarbiidist Fe3C(tsementiit) *malm on habras,väikse tõmbetugevusega,aga suure kulumiskindlusega.vähe löögi kindlust. *tempermalm saadakse valgest malmist mida kuumutatakse850C juures.sellise protsessi tulemusena suureneb malmi löögikindlus ja plastsus. *hallmalm evalumalmis esineb süsinik vaba grafiidi lehekestena see muudab malmi pehmeks ja kergemini töödeldavaks. *omaduselt on hallmalm jäik ja suure survetugevusega
Lk 25-Üldine keemiline koostis 1. Nimetage organismide peamisi keemilisi elemente. Hapnik (O), Süsinik (C), Vesinik (H), Lämmastik (N). 2. Millised keemilised elemendid kuuluvad makroelementide hulka? Makroelementide hulka kuuluvad veel Fosfor (F), Väävel (S), Kaalium (K), Naatrium (Na), Magneesium (Mg), Kaltsium (Ca) ja Kloor (Cl). 3. Miks vajab organism makroelemente suhteliselt suurtes kogustes? Sest need moodustavad suure osa organismi koostisest. 4. Millised keemilised elemendid esinevad kõigi orgaaniliste ainete koostises? O;C;H;N on enamike organismide koostises.
Kihtide vaheline kaugus on suurem kui vahemaa kuusnurga süsiniku aautmote vahel, see töttu on grafiit pehme. Kasutamine: pliiatsisüdamikud, elektroodid (?) Fullereenid koosnevad kerakujulistest ainult süsinikku sisaldavatest molekulidest. Süsi ja tahm Aktiivsüsi saadakse kui puidusöest juhitakse läbi veeauru, see suurendab sõe poorsust ja võimet siduda mitmeid aineid Kasutatakse: meditsiinis, sõjaväes Tahm on kõigep uhtam süsinik ja koosneb grafiidi kristallidest Kasutus: trükivärvid, llõhkeained, kummitööstus Süsiniku tähtsamad ühendid Vingugaas tekib kütuse mitte täielikul põlemisel 2c + o2 = 2co Füüsiline: värvuseta, lõhnata, mürgine gaas Tekitab peavalu, oksendamist, pea ringlemist Vingugaas reageerib veresoleva hemoglobiiniga, tekib mürgine ühend, mis takistab hapnikukandumist organismi Esmaabi vingu mürgituse puhul: värske õhk, nuuskpiiritus, kange tee
Orgaanilised ained jaotatakse: 1)Mitte tsükliline Ahel on sirge ch3 ch2 ch2 ch3 Ahel on hargnenud ch 3 ch / ch3 ch3 2) tsükliline ch 2 ruuduna Valents näitab mitu keemilist sidet võib antud aatomil olla. Süsinik on nelja valentne. Hapnik on kolmevalentne Lämmastik on kolmevalentne Vesinik on ühevalentne Lihtsustatud struktuur valem: ch3 ch2 ch2 ch3 Molekul valem C4H10 Alkaanid on orgaanilised ained, kus süsinik aatomite vahel on üksiksidemed. Alkaanidel on nimetuses lõppliide aan. 1 meta 2 eta 3 propa 4 buta 5 penta Alkaanide esindajad Metaan CH4 - Soogaas, maagaas, kaevandusgaas Kasutatakse majapidamis gaasina Nafta on süsivesinike segu. Naftast toodetakse: bensiini, petrooliumi, kütteõli, diislit Parafiinid on tahked alkaanid, kus süsinike arv on üle 20. Valmistatakse: küünlad, parafiinmähised OA Leidmine orgaanilistes ainetes
Lähtuvalt kasutusalast on tegemist süsiniktööriistaterasega. 3. Antud terase korral on võimalik poollõõmutus ning peale seda on struktuuriosad terajad sferoidaalsed tsementiidiosakesed. 4. Tegemist on termotöödeldava terasega ning antud terase tüüpiline termotöötlus on poolkarastus. 5. Antud terase karastustemperatuur on 757 C- 777 C, sest kui kõrgemat temperatuuri kasutada, siis muutub teras hapramaks, süsinik põleb välja ning saadava terase kõvadus väheneb. Peale karastamist on terase struktuuris martensiit ning tsementiit ning kõvadus HRC-s on 65+ . 6. Noolutustemperatuurid 200-250 C ning seda noolutust nimetataks madalnoolutuseks. Noolutatud terase struktuuriosadest tekib juurde tsementiit ja kõvadus on 67 HRC. 7. Antud noolutatud terase kõvadus ja tugevus on suur ning säilub enam vähem sana suurena kuid antud teras muutub noolutamise käigus sitkemaks. Malmid 8
Orgaaniline keemia Süsinikuühendite keemia põhineb süsinikuaatomi võimel moodustada piki ahelaid kovalentsete sidemetega. Süsinikuahel võib olla lineaarne, hargnenud, tsükliline. c-c-c-c-c (lineaarne) c c-c-c-c (hargnenud) c c c c (tsükliline) c c c Kehtib HONC reegel, mis ütleb et vesinik saab moodustada ühe kovalentse sideme,hapnik 2, lämmastik 3 ja süsinik 4. ALKAANID (süsivesinikud) Süsiniku ja vesiniku ühendid; küllastunud ühendid e. Süsinikuaatomite vahel on ainult üksik sidemed. -aan (peaahela lõpp) -üül (kõrvalrühm) 1-met 6-heks 2-et 7-hept 3-prop 8-okt 4-but 9-non 5-pent 10-dek Isomeerid Nähtus ,kus sama elementkoostisega ainetel on erinev struktuur ja seetõttu ka erinevad omadused. Süsinikuoksüdatsioonide määramine C oksüdatsiooni astmete summa C keskmine=
Esinevad nii gaasi, vedeliku kui ka tahkisena. Nad on suure elektronegatiivsusega elemendid, mis keemilistes reaktsioonides peamiselt liidavad elektrone. Mittemetallid on kõik p- elemendid, mis pole metallid ega poolmetallid. Neid on kokku 22. Tavaliselt on välisel elektronkihil võrdlemisi palju elektrone, tavaliselt 4-8. Tahked mittemetallid on haprad ja ei ole sepistatavad, samuti puudub neil metalne läige (v.a jood). Mittemetallideks on näiteks vesinik, hapnik, boor, süsinik, lämmastik, fluor, räni,fosfor, väävel, kloor, selen, broom ja jood. Neid iseloomustab peamiselt see, et perioodilisustabelis asuvad nad pea-alarühmades ülal paremal, k.a. vesinik, mis asub kõige esimese elemendina ülal vasakul. Traditsiooniliselt VIIIA rühma elemente ehk väärisgaase mittemetallideks ei loeta, kuivõrd neile pole iseloomulik keemilistesse reaktsioonidesse astuda. Keemilistes reaktsioonides moodustavad nad teiste
1. karboksüülhapete ja nende soolade nimetused ja struktuurid Nt. 5-kloro-4-metüülpentaanhape, propaandihape kaltsiumpropanaat [(CH3CH2COO)2Ca], magneesiumpentanaat, kaalimpentaandiaat 2. karboksüülhapete füüsikalised omadused (lahustuvus praktilise ül-na e millise aine lahustuvus on kõige suurem ja kõige väiksem) Mida rohkem OH, seda paremini lahustuv. Mida rohkem hargnemisi, seda paremini lahustuv. Mida rohkem süsinikke (süsinik-süsinik), halvemini lahustuv. 3. saamine Tv 9.3 D-F sipelg- ehk metaanh., oblik- ehk etaandih., palderjan- ehk pentaanh. (...+O2...+H2O) äädik- ehk etaanh., või- ehk butaanh., merevaik- ehk butaandih. (...+O2...) 4. keemilised omadused (happelisus) tv 9.3 G,H metall + hapesool + H2 KUI on H2-st eespool sool + hapesool + hape KUI tekib nõrgem hape/sadeneb vahetusr. metallioksiid + hapesool + H2O ALATI ...
Esinevad nii gaasi, vedeliku kui ka tahkisena. Nad on suure elektronegatiivsusega elemendid, mis keemilistes reaktsioonides peamiselt liidavad elektrone. Mittemetallid on kõik p-elemendid, mis pole metallid ega poolmetallid. Neid on kokku 22. Tavaliselt on välisel elektronkihil võrdlemisi palju elektrone tavaliselt 4-8. Tahked mittemetallid on haprad ja ei ole sepistatavad, samuti puudub neil metalne läige (v.a jood). Mittemetallideks on näiteks vesinik, hapnik, boor, süsinik, lämmastik, fluor, räni, fosfor, väävel, kloor, selen, broom ja jood. Neid iseloomustab peamiselt see, et perioodilisustabelis asuvad nad pea-alarühmades ülal paremal, k.a. vesinik, mis asub kõige esimese elemendina ülal vasakul. Traditsiooniliselt VIIIA rühma elemente ehk väärisgaase mittemetallideks ei loeta, kuivõrd neile pole iseloomulik keemilistesse reaktsioonidesse astuda. Keemilistes reaktsioonides moodustavad nad teiste mittemetallidega
vitamiin, kuid ta ei ole värviline.Karoteen annab porgandile iseloomuliku värvuse.Looduslik kautsuk sisaldab samuti 1.alkeen-küllastumata süsivesinikud,mille molekulides on süsinik kaksiksidemeid, kuna kaksiksidemed on seal üksteisest aatomite vahel kaksikside.Alküünid-küllastumata lahutatud,siis sel põhjusel on kautsuk ka värvusetu.5.Alkeenide süsisvesinik,mille molekulides on süsinik aatomite vahel füüsikalised omadused. Alkeenide füüsikalised omadused nende kolmikside.-side-P-orbitaali katuumisel tekkinud ühise homoloogilises reas muutuvad samamoodi nagu ka
Struktuur on üldmõiste, mis on määratletud kui süsteemi elementide seostus ehk organiseerimisviis. Isomeerid ühesuguse elementkoostise ja molekulmassiga, kuid eriva struktuuriga ained. Hüdrofoobsus veelembus, ühendi võime vastastikmõjuks veega. Hüdrofiilsus veetõrjuvus, ühendi võimetus vastikmõjuks veega. Radikaal osake, millel on paardumata elektron. Pürolüüs aine muundumine kõrge temperatuuri toimel. 2. Tetraeedriline süsinik, ruumilisus Tetraeedriline süsinik on süsiniku aatom, mille kovalentsed sidemed on suunatud tetraeedri tippudesse. Lk.16 3. H, O, N, C valentsolekud , süsinikahela võimalikud kujud (hargnemata e. lineaarne, hargnenud, tsükliline) Lk.17 4. Aine koostise ja struktuuri kujutamine erinevatel viisidel (summaarne valem, lihtsustatud struktuurvalem, tasapinnaline e klassikaline struktuurvalem, molekuli graafiline kujutis) Lk.19 5
liikudes purustab katsekeha ja tõuseb veel ülejäänud energia viral teatud kõrgusele.h purustamiseks tehtud töö leitakse valemiga g vasara kaal l pendli pikkus A töö A = G*l (H-h)[J] KCv = A/S J/m2 Terased teraseks nim raua ja süsiniku sulamit milles on kuni 2,14% süsiniku:Keemilise koostise järgi võib teraseid liigitada süsinikterasteks ja lekerterasteks.Kasutusotstarbe järgi võib teraseid liigitada tööriista ja konstruktsiooniterasteks. Süsinik konstruktsiooniteras Süsinik konstruktsiooniterased jagunevad tava sys kons.terasteks ja kvaliteet sys kons. Terasteks.Standardiga GOCT 380 88 toodetakse järgmisi marke tava sys kons. Teraseid.Ct,O,Ct1,Ct2,Ct3,Ct4,Ct5,Ct6.Arv materjali margis iseloomustab teatavaid mehaanilisi omadusi.Taandamisastme järgi toodetaks selles terasegruppis nii keevaid (vene P), poolrahulike (Vene PC) ja rahulike teraseid (vene CP)
Praeguseks on välja töötatud ja katsetatud enam kui paarikümmet erinevat vanuse määramise viisi. Tähtsaim nendest on radioaktiivse süsiniku meetod. Radioaktiivne süsinik tekib maa atmosfääri ülemistes kihtides, kus kosmilise kiirguse neutronid ,,löövad" lämmastiku aatomist välja prootoni ehk vesiniku aatomi tuuma. Selle reageerimisel hapnikuga moodustub süsihappegaas, milles tavalise süsiniku aatomi (massiarv 12) asemel on radioaktiivne süsinik (massiarv 14). See seguneb atmosfääri alumistes kihtides tavalise süsihappegaasiga ja osaleb koos sellega süsinikuringes - taimedes tekib päikeseenergia toimel orgaaniline aine (fotosüntees), mis satub kõigisse taimtoidulistesse ja edasi juba nendest toituvaisse organismidesse. Selgroogsete puhul ladestub süsinik peamiselt luudes, kasvavates puudes aga selle viimase aasta kasvukihis, nn. aastarõngas. Sisemistesse kihtidesse seda enam ei satu.
IUPAC'i nomenklatuur- Rahvusvaheline Puhta Keemia ja Rakenduskeemia Liit, kõige tähtsam keemikute rahvusvaheline organisatsioon. asendusnomenklatuur + nt- orgaaniliste ühendite nimetamise moodus, mis lähtub tüviühendist ning käsitleb nimetatavat ühendit kui tüviühendi asendusderivaati funktsionaalnomenklatuur + nt orgaaniliste ühendite nimetamise moodus, mille järgi ühendiklassi nimetus koostatakse tüvistruktuuri nimetusest ja sellele järgnevast ühendiklassi kirjeldavast liitest osalaeng- , erinev ioonlaengust. Kasutatakse orgaanilises keemias, kuna elektronpilt on tõmmatud elektronegatiivsema elemendi poole elektrofiil ühend või osake, millel on elektrofiilne tsenter nukleofiil- ühend või osake, millel on nukleofiilne tsenter reaktsioonitsenter- aatom või aatomite rühm, mis osaleb ning muundub reaktsiooni käigus lahkuv rühm- rühm, mis tõrjutakse välja asendusreaktsioonid asendiisomeeria- tuleneb funktsionaalsele rühmade erisugusest ...
1. Suhkrute lühiiseloomustus Suhkrud e süsivesikud- orgaanilised ühendid, mille koostisesse kuuluvad süsinik, vesinik ja hapnik. Suhkruid jagatakse 3 rühma: 1)Monosahhariidid e lihtsuhkrud (üks tsükkel)- kõige lihtsamad süsivesikud, mis koosnevad 3-6 süsinikuaatomist. Tähtsamad neist on: · 5-süsinikuga e pentoosid i. riboos (C5H10O5)- kuulub RNA (nukleotiidi) koostisesse. ii. desoksüriboos (C5H10O4)- kuulub DNA (nukleotiidi) koostisesse. · 6-süsinikuga e heksoosid i. glükoos e viinamarjasuhkur (C6H12O6)- tähtis energiallikas. Taimedes
Alkaanid võivad olla vedelad, tahked või gaasilised. Alkaanid on hübrofoobsed ehk vett tõrjuvad. Inimestele ja loomadele mõjuvad alkaanide gaasid narkootiliselt. o-a leidmine süsinikul: Iga side H-ga vähendab C o-a 1 võrra ja iga side O, N, halogeeni jne suurendab süsiniku o-a 1 võrra. Vastavalt sellele mitmekordne side on o-a muutub. Kui element pole C-ga otseses kontaktis, siis ta oa-d ei muuda. Mõisted: Valents näitab mitu sidet võib antud aatomil olla. Tetraeedriline süsinik nelja üksiksidemega süsinik Hargnev ahel süsinikahel hargneb mitmeks ja on seotud naabersüsinikega Hargnemata ahel süsinikuahel on ühe pika ahelana Tsükliline ühend suletud süsinikahel Alkaanid orgaanilised ühendid, kus süsinike vahel on kovalentne üksiksida Isomeer ühesuguse elementkoostise ja molekulmassiga, kuid erineva struktuuriga ained Hüdrofoobsus vett tõrjuvad Oksüdeerumine kõik orgaanilised ained on redutseerijad st. nad võivad
OKSIIDID-liitained,mis koosnevad kahest ALUSED e. HÜDROKSIIDID- ainest(neist 1 on hapnik.o-a. -2.) liitained, mis koosnevad Na2O-naatriumoksiid metallkatioonist ja ühest või mitmest MgO-magneesiumoksiid OH- anioonist CaO-kaltsiumoksiid Mg(OH)2-magneesiumhüdroksiid Fe2O3-raud(3)oksiid Fe(OH)3-raud(3)hüdroksiid Cu2O-vask(1)oksiid NaOH-naatriumhüdroksiid N2O5-dilämmastikpentaoksiid KOH-kaaliumhüdroksiid P2O5-difosforpentaoksiid Ba(OH)2-baariumhüdroksiid CO-süsinik(2)oksiid Ca(OH)3-kaltsiumhüdroksiid N2O3-dilämmastiktrioksiid LiOH-liitiumhüdroksiid Mn2O7-mangaan(3)oksiid ...
teiste aatomite elektronide osavõtul. Süsiniku aatomil on nüüd väga püsiv kaheksast elektronist koosnev teine ehk viimane elektronkiht. Süsiniku aatom molekulis Orgaanilistes ühendites on süsinikul alati neli sidet, hapnikul kaks, lämmastikul kolm ja vesinikul üks side. Süsiniku aatomi olekud molekulis: Hapniku aatomi olekud molekulis: Lämmastiku aatomi olekud molekulis: Tetraeedriline süsinik Nelja üksiksidemega süsinik on tetraeedriline kõigis ühendites. Sidemetevaheline nurk on umbes 109. Omavahel võib olla seotud mitu tetraeedrilist süsinikku ning tekib süsinikuahel. Süsinikuahel võib olla hargnemata, hargnenud või tsükliline. Valemid ja struktuurivalemid Summaarne valem Lihtsustatud struktuurivalem Klassikaline ehk tasapinnaline struktuurivalem Ruumiline struktuurivalem Graafiline kujutis Orgaaniliste ainete oksüdeerumine
Kõrgahju kõige ülemises osas on temperatuur kõige madalam ning seda nimetatakse soojendustsooniks. Mida allapoole liikuda, seda kõrgemaks temperatuur muutub. Ahju keskosas toimub raua järk-järguline redutseerumine nn käsnrauaks ning ahju allosas toimub raua rikastamine süsinikuga, mille tulemusel raua sulamistemperatuur alaneb ja toimubki raua sulatamine ning eraldub kolde allosast sulamalm. Selline malm sisaldab rauda, milles on lahustunud raudkarbiid (Fe3C), süsinik, räni jt. lisaaineid. Kõrgahju keskosas toimub ka aheraine muutumine räbuks (räbusti - lubjakivi) toimel. Räbusse lähevad peale kaltsiumoksiidi ja ränidioksiidi ka kütuse (koksi) tuhk ning magneesiumoksiid, mis ei redutseerunud. Seda tekkinud räbu kasutatakse tsemendi ja räbutelliste tootmiseks. Terast toodetakse tavaliselt malmist ja samades tehastes konverterites või martäänahjudes (kõrge temperatuuriga ahjud, kust puhutakse õhku läbi).
Maa atmosfäär koosneb lämmastikust ja hapnikust. Levinud ühendid on H2O, SiO2 ja CO2. Elusorganismides esinevad orgaanilised ained koosnevad süsinikust, vesinikust ja hapnikust. Fossiilsed kütused sisaldavad peamiselt süsinikku või orgaanilisi aineid. Vääriskivid koosnevad peamiselt mittemetallilistest elementidest: teemat süsinikust, mäekristall/ametüst ränidioksiidist. Esimesed mittemetallid, mida inimene tundma õppis olid süsinik ja väävel. Süsinik tekkis söe kujul puude põletamisel Süsiniku kaks rolli: põlemisel saadakse vajalik kõrge temperatuur ja ühtlasi võtab ta otseselt osa reaktsioonist süsinik redutseerib metalliühendist puhta metalli. Alguses saadi sedasi vaske, hilje tina pliid ja rauda. Väävliga puututi kokku vulkaanilistes piirkondades, kus seda leidub sageli ehedal kujul. Seostati tulega. Arseen avastati 13 saj, fosfor 17 saj. Mittemetalliliste elementide aatomiehituse iseärasused. Põhilised iseärasused:
Rakkudes hapnik(igasuguseks elutegevuseks, ainevahetuseks), süsinik (kehas orgaaniliste ühendite koostises), vesinik(biomolekulide ehitusüksus) fosfor-DNA oluline ühend. Kaalium ja naatrium osalevad närviimpulsi muudustumises. Vesi on organismis hea lahusti, osaleb enamikus keemilistes reaktsioonides, aitab säilitada organismis püsivat temperatuuri. Org ained organismis: sahhariidid, lipiidid, valgud, nukleiinhapped. Põhilised ensüümid, vimaniinid, hormoonid. Monosahhariidid e lihtsuhkrud on madalmolekulaarsed. C arv aatomi molekulis on 3-6
Mina ja rasvad Rasvad on glütseriini ehk propaantriooli ja kõrgemate karboksüülhapete (rasvhapete) estrid, mille olek toatemperatuuril on tahke. Elusorganismid kasutavad rasvades valdavalt paarisarvu süsinikega (kuni 20) rasvhappeid. Kõrgemate karboksüülhapete estrid, mille olek toatemperatuuril on vedel, on õlid. Rasvhapped on kas 16 või 18 süsinikulised, ning kas tegemist on õlide või tahkete rasvadega vaadatakse kordseid sidemeid. Kui rasvhappes esineb kordne süsinik-süsinik side siis on tegemist õliga. Rasvade põhiülesandeks on energia katmine ning säilitamine, nad on ka asendamatute polüküllastamata rasvhapete ja rasvlahustuvate vitamiinide allikas. Fosfatiidid kuuluvad kõikide kudede ja rakkude koostisesse, suuremal hulgal on neid närvikoes ja ajurakkudes. Rasvad võtavad osa kasvuprotsesside ja muu elutegevuse reguleerimisest. Uuemad soovitused pakuvad rasvade osatähtsuseks toiduenergiast 30 %. Sel...
c. 150 ameerika dollari võrra d. 200 ameerika dollari võrra Küsimus 2 Komposiitmaterjalide liigitus sarruse keemilise koostise alusel: a. orgaanilised b. anorgaanilised c. looduslikud d. sünteetilised kombineeritud Küsimus 3 Komposiitmaterjalide liigitus sarruse ehituse alusel: a. osakearmeeritud b. kiudarmeeritud c. struktuursed d. kombineeritud Küsimus 4 Milline kiu tüüp on aromaatsel baasil? a. boor b. aramiid c. klaas d. süsinik Küsimus 5 Sarrusena vill on: a. süntetiline dispergeeritud faas b. looduslik dispergeeritud faas c. anorgaaniline dispergeeritud faas Küsimus 6 Lennuki massi vähendamine 10 kg võrra säästab kuus a. 348 liitrit kütust b. 3477 liitrit kütust c. 16688 liitrit kütust d. 41720 liitrit kütust Küsimus 7 Millal alustati melamiinkilede valmistamist? a. 1935 b. 1945 c. 1955 Küsimus 8
Millise OA-ga on kõige enam a) Oksüdeerunud süsinik +4 (CO2) b) Redutseerunud süsinik -4 (CH4) Mis moodustub orgaanilise aine täielikul põlemisel? CO2+H2O Mis on pürolüüs? Aine lagunemine kõrge temperatuuri toimel Millal tekib põlemisel tahm? Kui põlemine on mittetäielik või pürolüüsiprotsessis Isomeeria On nähtus, kus ühenditel on ühesugune koostis kuid erinev struktuur ja sellest
Rasvad ehk lipiidid Rasvad on glütseriini ehk propaantriooli ja kõrgemate karboksüülhapete estrid, mille olek toatemperatuuril on tahke. Kõrgemate karboksüülhapete estrid, mille olek toatemperatuuril on vedel, on õlid. Rasvhapped on kas 16 või 18 süsinikulised, ning kas tegemist on õlide või tahkete rasvadega vaadatakse kordseid sidemeid. Kui rasvhappes esineb kordne süsinik-süsinik side, siis on tegemist õliga. Lipiidid koosnevad alkoholist ja rasvhappejäägist. Lipiidid on veest kergemad ja hüdrofoobsed. Lipiidid jagunevad kolmeks: lihtlipiidid, liitlipiidid ja tsüklilised lipiidid. Lihtlipiidid jagunevad omakorda: vedelad rasvad ehk õlid, tahked rasvad ehk loomsed rasvad ning vahad. Liitlipiidid ehk fosfolipiidid - üks rasvhappejääk on asendunud fosfaatrühmaga, kuuluvad rakumembraani koostisesse. Tsüklilised lipiidid on steroidid, kolesteriidid, hormoonid ja toidulipiidid. Ra...
Millise OA-ga on kõige enam a) Oksüdeerunud süsinik +4 (CO2) b) Redutseerunud süsinik -4 (CH4) Mis moodustub orgaanilise aine täielikul põlemisel? CO2+H2O Mis on pürolüüs? Aine lagunemine kõrge temperatuuri toimel Millal tekib põlemisel tahm? Kui põlemine on mittetäielik või pürolüüsiprotsessis Isomeeria On nähtus, kus ühenditel on ühesugune koostis kuid erinev struktuur ja sellest
siduv reeglite kogum 6. homoloogiline rida rida , mille kõrvuti seisvad liikmed erinevad teineteisest rühma CH2 võrra homoloog homoloogilise rea liige 7. tüviühend pikim süsivesinikahel alküülrühm alkaanidest tuletatud asendusrühmad 8. sigma side kovalentne side, mida moodustuvate elektronide pild asub aatomeid ühendaval ühel sirgel tetraeedriline süsinik nelja üksiksidemega süsinik 9. parafiinid tahked alkaanid või nende segud hüdrofoobsed ained ained, millel puudub veega vastastikmõju, puudub võime moodustada vesiniksidemeid, veega ei märgu ja vees ei lahustu hüdrofiilsed ained ehk vee-lembelised on ained, millel esineb vastastikmõju veega, esineb võime moodustada vesiniksidemeid, nad on vees märguvad ja lahustuvad. 10. Täielik põlemine toimub piisava hapnikukoguse (õhu) olemasolul. Selle käigus
Riina Tamm Teemant imepäraste omadustega süsinik Referaat 2010 SISUKORD Sisukord...................................................................................................................................... 2 sissejuhatus..................................................................................................................................3 1. Teemandi üldiseloomustus..........................................................
reeglite kogum 6. homoloogiline rida rida , mille kõrvuti seisvad liikmed erinevad teineteisest rühma CH2 võrra homoloog homoloogilise rea liige 7. tüviühend pikim süsivesinikahel alküülrühm alkaanidest tuletatud asendusrühmad 8. sigma side kovalentne side, mida moodustuvate elektronide pild asub aatomeid ühendaval ühel sirgel tetraeedriline süsinik nelja üksiksidemega süsinik 9. parafiinid tahked alkaanid või nende segud hüdrofoobsed ained ained, millel puudub veega vastastikmõju, puudub võime moodustada vesiniksidemeid, veega ei märgu ja vees ei lahustu hüdrofiilsed ained ehk vee-lembelised on ained, millel esineb vastastikmõju veega, esineb võime moodustada vesiniksidemeid, nad on vees märguvad ja lahustuvad. 10. Täielik põlemine toimub piisava hapnikukoguse (õhu) olemasolul. Selle käigus tekivad
10. Aldoolreaktsioonid Karbonüülrühma -vesinike happelisus Karbonüülühendite teiseks oluliseks iseloomuks on karbonüülrühmaga külgnevate süsinikuaatomite juures olevate vesinike happelisus. Selliseid vesinikuaatomeid nimetatakse -vesinikeks. O H O R C C C R H Karbonüülrühma -vesinike happelisuse põhjused on lihtsad. Karbonüülrühm on tugev elektronaktseptoorne rühm ja kui karbonüülühendist eraldub -prooton, siis tekkinud anioon on resonantsi poolt stabiliseeritud. Aniooni negatiivne laeng on delokaliseerunud. .. - .. .. - :O H :B :O :O : -.. C C C C C C + H B A B Resonantsi po...
Mittet. 2C+O2>CO(sees) 3.Järgnvlt on antud. 3.1(A)täielik B(mittetäielik) 3. Sest vingugaas on väga mürgine,ja takistab põlemist(on raske) 4.Kuidas kustutada...? 1)takistada hapniku juurdepääsu. Nt:riidetükk,vesi,vaht 2)Lõhkeainega(nafta tulekahjud,võtab kogu hapniku ära) 5.Mis juthub põlemisel kui O2?Tuli kustub või muutub väikseks,tekib vingugaas 6.Mis on tahm?Puhas süsinik 7.Mida kujutab endast see suits...?Süsinik 8.Mis on kütuse kütteväärtus?Soojushulk mis eraldub 1kg kütuse täielikul põlemisel (bensiin,petroolium,nafta) 9.Järgnevalt on toodud glükoos 'leegita põlemise'reaktsioon... C6H12O6(glükoos)+602(hapnik)[lähtained]>6CO2(süsihappeg)+6H2O(vesi) [saadused] 9.1Energia eraldub 9.2Toimub põlemine kuid leeki pole näha 10.Mida nim. Fotokeemiliseks reaktsiooniks?Reaktsioon mille kutsub esile valgus (fotosüntees)11.Kas fotokeem. Reakts