Sideme tüüp Aineosakesed kristall Tugevus Omadused võre tüüp Aatomid, aatomvõre Tugev kovalentne Kõrge sulamis-ja keemis side temp, ei lahustu vees,ei juhi elektrit,kõva ,rabe Mittepolaarne hea soojusjuht. kovalente side Molekulid,molekulvõre Tugev kovalentne Gaasiline,vedel või tahke side, vahel on nõrk ,oleku määrab vastastikune molekulmassi tõmbejõud suurus.Madal sulamis ja keemistemp. Ei lahustu ...
Variant 1 1) Keemilise sideme tekkimisel püüavad aatomid (elektronide liitmisel või loovutamisel) saavutada endale 8 või 2 elektronilise väliskihi. 2) PK sideme korral on elektronpaar nihutatud suurema elektronegatiivsusega aatomi poole. 3) Dipoolid on poolustega molekulid, kus molekuli 2 poolt on erineva laenguga. (Dipoolsed molekulid saavad tekkida kuna aatomine elektronegatiivsused erinevad.) 4)Metallilises sidemes osalevad osakesed: metallikatioonid, metalliaatomid ja elektrongaas. 5) Ioonilise sidemega ained on haprad, sest kristalli mõjutamisel satuvad kohakuti samanimelised ioonid, mis tõukuvad. Kristall puruneb. 6) Molekulide vaheline side on vesinikside. 7) Vesiniksideme korral peab molekulis esinema H aatom ja teise aatomina kas F, O, N või S. 8) Elektroneatiivsus on suurus, mis iseloomustab ELEMENDI AATOMI VÕIMET SIDUDA ENDAGA ELEKTRONE. Variant 2 1) PK side esineb selliste aatomite vahel, mille elektronegatiivsuse vahe on 0...
............. 4 1.2 Lapse äravõtmine vanemalt .................................................................................... 4 1.3 Linna-/ vallavalitsuse kohustused ............................................................................. 5 2. VANEMA ÕIGUSTE ÄRAVÕTMINE............................................................................... 5 2.1 Vanema õiguste äravõtmise tagajärjed ja taastamine............................................... 5 3. PEREKONNA SIDEMETE SÄILITAMINE....................................................................... 6 4. LASTE ERALDAMINE PEREKONNAST EESTIS AASTATEL 2000 2007...................6 Tabel 1............................................................................................................................ 6 Tabel 2............................................................................................................................ 6 Tabel 3.............................................
Kontrolltöö Keemiline side 1. Täida lüngad. o ...................... side moodustub metalli ja mittemetalli vahel. o Metallide vahel moodustub ....................... side, seega mittemetallide vahel aga ........................ side. o ..................side on alati täiendavaks sidemeks, mis esineb molekulide vahel. 2. Määra polaarsus. Polaarne märgi P-ga ja mittepolaarne MP-ga. o O=O o O=C=O o HOH o O=S=O o Cl Cl H | o HCH | H 3. Täida tabel. Elemendid Ioonide valemid Ioonide arvude suhe Aine valem K+ I - 1:1 Na ja P ...
Kordamine. KEEMILINE ELEMENT- ühesuguste tuumalaengutega aatomite liik. ALLOTROOPIA- nähtus, kus 1 keemiline element võib esineda mitme lihtainena. O2-dihapnik, O3- trihapnik(ehk osoon) ISOTOOP- ühesuguste tuumalaenguga, erineva massiarvuga osakesed. 1. AINE KLASSID: a. Lihtained- (400),koosnevad ühe elemendi aatomitest.: · mittemetallid(19)- S, P, O2, Cl2 jne · poolmetallid e. metallid(15)- Ge, As, Sb, Te, At jne · metallid (90); Al, Au, jne b. Liitained- koosnevad mitme elemendi aatomitest: 1. Oksiidid- on ained, mis koosnevad kahest elemendist, millest üks on hapnik (oksüdatsiooniaste -II). Oksiid on hapnik (o.-a. II) ja mingi teise keemilise elemendi ühend. a. Aluselised oksiidid oksiidid, mis reageerivad hapetega, moodustades soola ja vee. Aluseliste oksiidide hulka kuulub...
(naatriumsulfaatvesi 1/10)? Lahendus: M( Na2SO4* 10H2O)= 322 g/mol n( Na2SO4* 10H2O)= 48,3 g MNa= 2*23 g/mol= 46 g/mol n= m/M= 48,3/ 322= 0,15 mol kui naatriumi on selles aines 46 g/mol, siis järelikult on ilma naatriumita soola 322 g/mol- 46 g/mol= 276 g/mol n= m/M= 48,3 / 276 = 0,175 mooli on ülejäänud soolas kui pole naatriumit ja naatriumi ioonide arvu saame kui 0,175- 0,15= 0,025 mol Vastus: Naatriumi ioonide arv on 0,025 mol 3. Määra keemiliste sidemete tüüp järgmistes ühendites CO2 mittepol. kovalentne KCl iooniline H2 mittepol. kovalentne NaF iooniline side Cl2 mittepol. kovalentne CH3Cl mittepol. kovalentne NH3 kovalentne polaarne HCl kovalentne polaarne K2O iooniline SiH4 kovalentne polaarne S8 mittepol. kovalentne Li metalliline H2O kovalentne polaarne CaF2 iooniline Metall + mittemetall = kovalentne polaarne Aktiivne metall + aktiivne metall = iooniline Metall lihtainena = mittepol. kovalentne
Mis on sulamine? Sulamine on aine üleminek tahkest olekust vedelasse olekusse. 2. Mida nimetatakse sulamistemperatuuriks? Temperatuuri, mille juures aine sulab, nimetatakse selle aine sulamistemperatuuriks. 3. Kirjelda aine sulamist. Lõhutakse aineosakeste korrapärane asetus Suureneb siseenergia potentsiaalne komponent Aine temperatuur ei muutu, sest kogu juurde saadud soojussiseenergia kulub molekulidevaheliste sidemete lõhkumiseks. 4. Mis on tahkumine? Tahkumine on aine muutumine vedelast ainest tahkesse olekusse. 5. Kirjelda aine tahkumist. Aineosakesed võtavad sellele ainele omase vastastikkuse asendi Vabaneb soojushulk Aine temperatuur ei muutu, sest kogu äraantud soojusenergia kulub molekulidevaheliste sidemete moodustamiseks. 6. Mida näitab sulamissoojus? Sulamissoojus näitab, kui suur soojushulk kulub/eemaldub 1 kg sulamiseks või tahkumiseks.
Füüsika Keemiline side - seob aatomeid molekulideks ja kristallideks Keemilise sideme liigid: · Kovalentne side ühtlustunud elektronpaaride vahendusel · Iooniline side positiivsete ja negatiivsete ioonide vahel Keemiliste sidemete tekkimine tekib aatomite ,,annetamise" või ,,ühistamise" teel Kristallvõre aatomid/ioonid on paigutatud korrapäraselt ruumvõresse Võredefekt: · Üksikud aatomid või ioonid paiknevad vales kohas · Mõned võresõlmed on vakantsed (tühjad) · Kristalli on lisatud teisi keemilisi elemente · Terasele lisati Cr ja Ni - roostevaba teras Keelutsoon on energiatsoon, millele vastav energiavahemik on elektronidele laineomaduste tõttu keelatud
vahel. tõmbejõuga aatomi negatiivseid poole osalaenguid (mittemetalsema elemendi aatomi poole) 1) Keemilise sideme mõiste, moodustumise viisid, miks on keemiliste sidemete teke aatomite või ioonide vahele energeetiliselt kasulik? Keemiline side on aatomite ja ioonide vaheline side, mis seob aatomid molekuliks ja ioonid kristallideks. Moodustub kahel viisil: 1. Elektronide üleminekul ühelt aatomilt teisele 2. Ühiste elektronpaaride tekke kaudu 2) Mõisted: Elektronoktett- aatomi väliskihil on 8 elektroni. Termokeemilised võrrandid- reaktsioonivõrrand, mis sisaldab ka reaktsiooni soojusefekti väärtust.
vahel. tõmbejõuga aatomi negatiivseid poole osalaenguid (mittemetalsema elemendi aatomi poole) 1) Keemilise sideme mõiste, moodustumise viisid, miks on keemiliste sidemete teke aatomite või ioonide vahele energeetiliselt kasulik? Keemiline side on aatomite ja ioonide vaheline side, mis seob aatomid molekuliks ja ioonid kristallideks. Moodustub kahel viisil: 1. Elektronide üleminekul ühelt aatomilt teisele 2. Ühiste elektronpaaride tekke kaudu 2) Mõisted: Elektronoktett- aatomi väliskihil on 8 elektroni. Termokeemilised võrrandid- reaktsioonivõrrand, mis sisaldab ka reaktsiooni soojusefekti väärtust.
KORDAMISKÜSIMUSED 10.KL. KEEMILISED REAKTSIOONID (õpik lk.68-98) 1. Selgita mõisted: aktiveerimisenergia, keemiline reaktsioon, eksotermiline reaktsioon, endotermiline reaktsioon. 2. Miks vahel keemilises reaktsioonis reaktsioonisegu soojeneb, vahel jahtub? Selgita keem. sidemete tekke ja katkemisega. 3. Soojusefekt ühinemis- ja lagunemisreaktsioonides. 4. Mida näitab keemilise reaktsiooni kiirus? 5. Kuidas on võimalik keemilise reaktsiooni kiirust muuta? Põhjenda. 6. Mis on katalüsaator, katalüüs, inhibiitor, ensüüm? Mis põhimõttel katalüsaator reaktsiooni kiirendab? 7. Mis on pöörduv reaktsioon? Mis on keemiline tasakaal? Näide võrrandina. 8. Kus on tasakaal kasulik? 9. Le Chatelier printsiip
TARTU ÜLIKOOL Pärnu kolledz Ettevõtluse osakond TURISMITRENDID Referaat Juhendaja: Pärnu 2013 SISUKORD 2 SISSEJUHATUS Turism on kasvanud üheks populaarseimaks puhkuse veetmise viisiks tänapäeval. Turism mõjutab ka tänu oma tugevate sidemete tõttu teise majandusharudega kogu majandust ning suurendab ka nõudlust erinevate toodete ja teenuste peale, mis kuuluvad teistesse elu valdkondadesse. Antud referaadi eesmärgiks on erinevat kirjandust uurides koostada ülevaade tursimi üldistest asjaoludest ja ka trendidest selle valdkonnas. Töös antakse ülevaade turismi liigitusest, erinevatest turismi vormidest ja ka turismitrendidest. Uurimisülesanded, millele vastust otsitakse, on järgmised:
KT nr 5 mõisted. Polümeerid. Sahhariidid. Valgud Polümeer – on ained, mille molekulid koosnevad kovalentse sidemeega seotud korduvatest struktuuriühikutest. Elementaarlüli – polümeeri molekulis korduv struktuuriühik Polümerisatsiooniaste - elementaarlülide arv polümeeri ahelas Liitumispolümerisatsioon – toimub kordsete sidemete arvel (mol liituvad) Polükondensatsioon – selle käigus eraldub mingi madalmolekulaarne aine (tav H20 ) Plastmass – polümeeri ja vajalike lisandite segu Kopolümeer – erinevte lülide kordumine Homopolümeer – samade lülide kordumine Polüester – hüdroksühapetest või dihappest ja dioolist kondensastiooni teel moodustunud polümeer Polüamiid – aminohapetest või dihapetest ja diamiinist kondesatsiooni teel moodustunud polümeer
aatomi ehitusest.Süsiniku sümbol on C, tema aatomi tuumas on 6 prootonit ja 6 neutronit.Tema elektronkatte moodustavad 6 elektroni, mis on jaotunud 2 elektronkihile ja väliskihil on neist 4 elektroni.Süsiniku aatom võib moodustada 2 või 4 keemilist sidet.Süsiniku aatom molekulis: Orgaanilistes ühendites on süsinikul alati neli sidet.Teiste ,,orgaaniliste" elementide-lämmastiku ja hapniku tüüpilised sidemete arvud on kolm ja kaks.Arvestades tähtsamate elementide tüüpilist sidemete arvu-vesinikul 1, hapnikul 2,lämmastikul 3,süsinikul 4.Tetraeedriline süsinik: Süsinik võib olla seotud nelja ühesuguse aatomiga ja nelja erineva aatomiga.Seega süsiniku aatom on olekus neli üksiksidet.Kõige lihtsam molekul on metaani(CH4)molekul. C ja H aatomid seotud sigma sidemetega.Süsinik moodustab erineva kujuga ahelaid:hargnemata ahel,hargnev ahel, tsükliline e. kinnine ahel
hallutsinatsioonid (6.8%). 10% pöördumatuid muutusi organismis. 15-12% surm veri niivõrd paks et süda ei suuda tagada normaalset vereringet. HO2 Hüdrofiilsus ainete omadus lahustuda vees (lahustuva aine ja veemolekulide vaheline tugev vastasmõju) Hüdrofoobsus ainete omadus mitte lahustuda vees Hüdratatsioon keemilise ühendi füüsikaline või keemiline liitumine veega Dehüdratatsioon veekaotus Hüdrolüüs keemiliste sidemete lõhkumine vee molekulide toimel (keerulistest ühenditest lihtsamate saamiseks Vee dissotsiatsioon ehk vee dissotsieerumine - vee molekuli lõhkumine ioonideks H2O H+ + OH OH hüdroksüülioon - H vesinikioon + ÜLESANDED ORGANISMIS · Rakkude sisekeskkond (vett 70-95%) ja rakuvaheruum · Lahustumine ja elektrolüütiline dissotsatsioon, ensüümreaktsioonid
Ained liigitatakse molekulaarseteks ja mittemolekulaarseteks aineteks. Keemilist sidet mis moodustub ühiste elektronpaaride abil nim kovalentseks sidemeks. Elektronnegatiivsus on aatomi võime siduda elektrone Keemiline reakt. on protsess, milles tekivad keemilised sidemed. Keemiliste sidemete tekkel energia alati eraldub, keemiliste sidemete lõhkumiseks tuleb energiat kulutada. Reaktsioonil eralduvat või neelduvat energiat nim reaktsiooni soojusefektiks. Reakts võrrandeid milles on märgitud reaktsioonis eralduv või neelduv soojushulk, nim. termokeemilisteks võrranditeks. Eksotermilistes reaktsioonides energia eraldub, endotermilistes reaktsioonides energia neeldub. Väärisgaaside aatomite väliselektronkiht on elektronidega täidetud ja seetõttu kõige püsivamas olekus
Keemia kontrolltöö Keemiline side Energia muutus keemilistes reaktsioonides Keemiline side aatomite- või ioonidevaheline vastastikmõju, mis seob nad molekuliks või kristalliks. Vääriskaaside aatomite väliskiht on täielikult elektronidega täitunud. ( Elektronktett ) Keemiline reaktsioon protsess, milles tekivad ja/või katkevad keemilised sidemed. Keemiliste sidemete tekkel energia alati eraldub, keemiliste sidemete lõhkumisel tuleb energiat kulutada. Lähteainetes olevate keemiliste sidemete katkemisel energia neeldub, uute keemiliste sidemete tekkimisel energia eraldub. Termokeemiline võrrand reaktsioonivõrrand, milles on märgitud ka reaktsioonis eralduv või neelduv soojushulk. Eksotermilistes reaktsioonides energia eraldub H < 0 ( saaduste energia on madalam kui lähteainetel ).
ORGAANILISE KEEMIA KT Teab keemia pohimoisteid ja definitsioone: aatomiorbitaal; molekulaarorbitaal; keemiline side; Suudab maarata molekulides olevate aatomite (C, O, N, H) hubridisatsiooniastet ja sidemete vahelisi nurki; suudab kirjeldada aatomiorbitaalidest -ja -sidemete tekkimist, sidemete geomeetriat ja elektronide paigutust keemilistes sidemetes; suudab esitada mittepolaarse- ja polaarse resonantsi resonants- piirstruktuure. Kontrolltoo on arvestatud, kui oigeid nimetusi on vahemalt 51%. Hinde ,,5" saab vahemalt 91% soorituse korral. · Aatomiorbitaal piirkond, kus elektronpilv asub; orbitaalide asukohad soltuvad osakese energiast (mida suurem energia, seda kaugemal); orbitaalide osakesed on kvanditud
kattumisel. Kovalentse sideme põhiomadused: küllastatavus, suunalisus, polaarsus ja polariseeritavus. Doonor-aktseptormehhanism kovalentse sideme tekkel: doonor - aatom, mis annab sideme moodustamiseks kaheelektronilise orbitaali; aktseptor aatom, mis annab sideme moodustamiseks tühja orbitaali. · Kovalentse sideme küllastatavus Küllastatavus üks aatom saab moodustada vaid teatud piiratud arvu kovalentseid sidemeid; valents aatomi poolt moodustatud kovalentsete sidemete arv antud ühendis (molekulis); maksimaalne kovalents maksimaalne kovalentsete sidemete arv, mida antud elemendi aatom saab (põhimõtteliselt) moodustada. · Kovalentse sideme suunalisus Kovalentse sideme peamised tüübid: side orbitaalid kattuvad ühes ruumiosas, tuumi ühendava sirge suunal; - side kattumine toimub kahes ruumiosas kahel pool tuumi ühendavat sirget; sideme kordsus kahe aatomi vaheliste kovalentsete sidemete arv.
kattumisel. Kovalentse sideme põhiomadused: küllastatavus, suunalisus, polaarsus ja polariseeritavus. Doonor-aktseptormehhanism kovalentse sideme tekkel: doonor - aatom, mis annab sideme moodustamiseks kaheelektronilise orbitaali; aktseptor – aatom, mis annab sideme moodustamiseks tühja orbitaali. • Kovalentse sideme küllastatavus Küllastatavus – üks aatom saab moodustada vaid teatud piiratud arvu kovalentseid sidemeid; valents – aatomi poolt moodustatud kovalentsete sidemete arv antud ühendis (molekulis); maksimaalne kovalents – maksimaalne kovalentsete sidemete arv, mida antud elemendi aatom saab (põhimõtteliselt) moodustada. • Kovalentse sideme suunalisus Kovalentse sideme peamised tüübid: σ– side – orbitaalid kattuvad ühes ruumiosas, tuumi ühendava sirge suunal; π- side – kattumine toimub kahes ruumiosas – kahel pool tuumi ühendavat sirget; sideme kordsus – kahe aatomi vaheliste kovalentsete sidemete arv.
- Ioonilised ained vee molekulid rebivad ioonid kristallist välja. - Molekulaarsed ained vee molekulide mõjul lahustuva aine molekulid. Polariseeruvad ja lagunevad ioonideks. · Kristallvõre või molekuli lõhkumisel kulub energiat, ioonide hüdraatumisel vabaneb energia. 1) Kristallvõre lõhkumine kulub energiat (energia neeldub) endotermiline 2) Sidemete moodustumine vabade ioonide ja vee molekulide vahel hüdraatumine (energia vabaneb) eksotermiline > - lahus, endo, tahked soolad < - TH, TA, gaasid · Soojusefektid lahustumisel: - hüdraatumine sidemete teke energia eraldub to tõuseb - kristalli lagunemine sidemete lõhkumine energia neeldub t o tõuseb - enamiku soolade lahustumine on endotermiline, sest ülekaalus on energia neeldumine kristalli lagunemisel.
ENERGIA.. ERALDUMISEGA KULGEVATEL REAKTSIOONIDEL ON SUUR TÄHTSUS. SUUR OSA KÜTUSTE PÕLEMISEL SAADAVAST SOOJUSENERGIAST MUUDETAKSE SOOJUSJAAMADES ELEKTRIENERGIAKS, AUTOMOOTORIS AGA AUTO KINEETILISEKS ENERGIAKS. ENERGIA ERALDAMISEGA KULGEVAD REAKTSIOONID ON VAJALIKUD KA ELUSORGANISMIDE ELUTEGEVUSEKS. MILLEST ON TINGITUD REAKTSIOONIDE SOOJUSEFEKT KEEMILISTES REAKTSIOONIDES TEKIVAD LÄHTEAINETEST JA SAADUSTEST. KEEMILISTE SIDEMETE TEKKIMISEL LÄHEVAD OSAKESE PÜSIVAMASSE OLEKUSSE, MILLES NENDE KEEMILINE ENERGIA ON VÄIKSEM. KEEMILISTE SIDEMETE TEKKIMISEL ENERGIA NEELDUB. ÜHINEMISREAKTSIOON ÜHINEMISREAKTSIOONIS ENERGIA ENAMASTI ERALDUB, SEST REAGEERIVATE AINETE OSAKESTE VAHEL TEKIVAD KEEMILISED SIDEMED. NÄIDE: FE + S FES KA NEUTRALISATSIOONIREAKTSIOON ON ÜHINEMISREAKTSIOON. KOKKUVÕTTEKS REAKTSIOONI SOOJUSEFEKT- SAADUSTE JA LÄHTEAINETE
nt 3H2 + N2 2NH3 3) Mis toimub keemiliste sidemetega reaktsiooni käigus? Keemilistes reaktsioonides ja/või katkevad keemilised sidemed. Aatomitevahelisi keemilisi sidemeid moodustavad elektronid paiknevad ümber, st et ühed sidemed katkevad ja uued sidemed moodustuvad. Keemilise sideme tekkel lähevad aineosakesed püsivamasse, madalama energiaga olekusse, seetõttu keemiliste sidemete tekkel energia eraldub. Keemiliste sidemete lõhkumiseks on vaja kulutada energiat, st teha tööd, sest aineosakesed tuleb viia ebapüsivamasse, kõrgema energiaga olekusse, seetõttu keemiliste sidemete katkemisel energia alati eraldub. 4) Millisel juhul keemiline reaktsioon saab üldse toimuda? Keemiline reaktsioon saab toimuda vaid siis, kui ained omavahel puutuvad kokku ja oma omaduste poolest reageerimiseks sobivad. 5) Mis on aktiveerimisenergia? Selle seos reaktsiooni kulgemisega.
Matemaatiliselt kirjeldab elektronpilve Schrödingeri võrrand: hy=ey Orbitaali saab kirjeldada lainevõrrandiga = peakvantarv n (orbitaali kaugus tuumast, n-le vastab n2 orbitaali), orbitaankvantarv l (orbitaali kuju, igale l-le vastab alakiht, s=0), magnetkvantarv m (orbitaalide asend üksteise suhtes, 0, +-1..+-l). Elektronpaar vastasmärgiliste spinnidega elektonid Elektronvalem elektronide paigutus energia järgi aatomis MO-meetod keemiliste sidemete tekkimine lähtudes kvantmehaanika seadustest. Lõdvendav, mittesiduv, siduv Orbitaal piirkond, kus elektron(paar) saab aatomis või molekulis asuda Kvant energiaportsjon, et elektron saaks orbitaale vahetada Van der Waalsi raadius molekuli elektronpilvede poolt hõivatud piirkonna raadius s-orbitaalid ''ots-otsaga'', p-orbitaalid ''külg-küljega'' Lewis'e valem .. Kekule valem F formaalne laeng = ve valentselektronide arv se pool siduvate el.arvust mse mittesiduvate el. Arv
1)iooniline 2) mittepolaarne kovalentne 3)Polaarne kovalentne 4) mittepolaarne kovalentne 5) iooniline 6)polaarne kovalentne Kujuta struktuurvalemite abil vesiniksidemete teket kolme molekuli vahel. Kuidas mõjutavad molekulidevahelised vesiniksidemed aine keemistemperatuuri? Põhjendus. Vastus : molekulidevahelised vesiniksidemed tõstavad aine keemistemperatuuri. Põhjus selles, et tekkinud sidemete lõhkumiseks läheb vaja rohkem energiat, seega tõuseb ka keemistemperatuur. JOONIS ÜLESANNETE LÕPUS Kui suur ruumala on normaaltingimustel 20 moolil lämmastikul ? n=20 mol Vastus: 20 mooli lämmastiku ruumala normaaltingimustel on Kui suur mass on 280 vesinikul? 280
Keemilistes reaktsioonides tekivad ühtedest ainetestreaktsiooni lähteainetest teised ained reaktsiooni saadused Kuidas keemilised reaktsioonid toimuvad? + N2 + 3H2 2NH3 Kuidas keemilised reaktsioonid toimuvad? · Selleks, et keemilised reaktsioonid toimuksid on vaja aktiivsete (energiarikaste) osakeste kokkupõrkeid · Selle tulemusena toimub aatomitevaheliste keemiliste sidemete tekkimine ja katkemine · Keemiliste sidemete lõhkumiseks kulutatakse energiat · Keemiliste sidemete tekkimisel eraldub energiat ja osakesed lähevad püsivamasse olekusse Keemilised reaktsioonid võivad toimuda erineva kiirusega Kui kiiresti toimub see Kui kiire on nafta tekkimine reaktsioon? maapõue sügavuses? Mis on keemilise reaktsiooni kiirus? kindlal ajahetkel toimuvate aktiivsete osakeste kokkupõrgete arv
KEEMILINE SIDE
Keemiline side esineb + ja ioonide vahel kristallides.
· Sidemete tekkimisel vabaneb energia. (eksotermiline protsess)
- eraldub energiat (H
Ioonkristall kristall, mis koosneb vastaslaenguga ioonidest. Molekulaarne aine Molekulidest koosnev aine. Mittemolekulaarne aine Väga suurest hulgast aatomitest või ioonidest, mis on omavahel seotud keemiliste sidemetega. Molekule nendes ainetes ei esine. Küsimused : Selgitage, miks aatomid ei esine üksikult, vaid ühinevad molekulideks ja kristallideks. Aatomid ei esine üksikult sellepärast, et keemilise sidemete moodustamisel lähevad aatomid üle püsivamasse olekusse, kus nende energia on väiksem. Aatom püüdleb alati põhioleku poole. Selgitage kovalentse sideme teket ja ioonilise sideme teket. Kovalentne side moodustub aatomite vahel ühe või mitme ühise elektronpaari abil. Kovalentse sideme tekkeks peavad aatomid sattuma teineteisele nii lähedale, et nende elektroide orbitaalid osaliselt kattuvad. Mittepolaarse kovalentse sideme korral on ühine elektronpaar jaotunud võrdselt mõlema
0,140 7,1429 0,00850 292 604 0,210 4,7619 0,00885 292 604 0,300 3,3333 0,00875 284 244 0,500 2,0000 0,00875 284 244 Jooniselt näeme, et , seega: Seega molekuli pindala adsorptsioonikihis on: Leitud tulemust võrdlen pikkusega, mis on arvutatud sidemete keskmiste pikkuste alusel: Katsevea arvutus Oma arvutustes leidsin ma, et katses adsorptsioonikihi paksus oli m, mis on suhteliselt erinev sidemete keskmiste pikkuste alusel arvutatud molekuli pikkusega, milleks on m. Nende kahe tulemuse erinevus on: Seega leitud adsorptsioonikihi paksus on sidemete keskmiste pikkuste alusel arvutatud molekuli pikkusest poole võrra suurem. Järeldused tööst ja hinnang tulemusele
Soojenduse eesmärgiks on treeningtulemuste parandamine ja vigastuste vältimine. Kui sa treenid suurte lihasgruppidega, tõuseb kehatemperatuur. Lihased kannavad soojuse verre,mis omakorda soojendavad kogu keha. Keha temperatuur võib korraliku soojendusega tõusta kuni 40 kraadini.Lihastes võib temperatuur ulatuda kuni 42 kraadini. Uuringud on näidanud,et hea soojendus tagab paremad treeningtulemused.Soojenduse tulemusena tekkiv kehatemperatuuri tõus vähendab nii lihaste kui ka sidemete ja kõõluste vigastuste ohtu,kuna „külmad“ lihased ja sidekoed on vigastustele väga vastuvõtlikud. Suurendab oksühemoglobiini degradatsiooni.Keemilise kompleksi hapnik + hemoglobiin lõhustamine tähendab seda, et hapniku vabanemine verest ja toimetamine töötavatele lihastele on tõsisema intensiivsuse ajaks efektiivistunud. Suurendab verevoolu/juurdevoolu töötavates lihastes.Mida suurem on verevool töötavatesse treeningul põhikoormust kandvatesse lihastesse, seda efektiivsem
Abs. jäik keha- 2 punkti vaheline kaugus kehas ei muutu Descarte võttis kasutusele koordinaatteljestiku, taustsüsteemi uurimiseks Elastne keha- välisjõudude mõjul keha kuju muutub Ekvivalentsed jõusüsteemid- jõusüsteemid, millel sama mõju vaadeldavale kehale. Kas siis seisab paigal või hakkab liikuma sama kiirendusega Hõõrdetegur- iseloomustab pinna karedust Fh=fN Jõud- kehade vastastikune mõju(otsene/kaudne) Jõu rööpküliku aksioom- 2 ühte punkti rakendatud jõudu võib asendada 1 jõuga, mis rakendatud samasse punkti Tasakaalus olevaks jõusüsteemiks nim jõusüsteemi, mis mõjutades paigalseisvale kehale ei kutsu esile selle liikumist Jõumoment punkti suhtes- vektor, mis võrdub jõu rakenduspunkti kohavektori ja jõuvektori vektorkorrutisega. Jõupaarimoment- vabavektor, risti jõupaari tasandiga ja seda võib lugeda lahendatuks ükskõik mis punkti antud kehal. R=Ruutj. F12+ F22+2 F1F2 cosa Jõusüsteemide tasakaal- R=Fi=0 Mo=Mo(Fi)=0 Koonduv jõusüs...
Abs. jäik keha- 2 punkti vaheline kaugus kehas ei muutu Descarte võttis kasutusele koordinaatteljestiku, taustsüsteemi uurimiseks Elastne keha- välisjõudude mõjul keha kuju muutub Ekvivalentsed jõusüsteemid- jõusüsteemid, millel sama mõju vaadeldavale kehale. Kas siis seisab paigal või hakkab liikuma sama kiirendusega Hõõrdetegur- iseloomustab pinna karedust Fh=fN Jõud- kehade vastastikune mõju(otsene/kaudne) Jõu rööpküliku aksioom- 2 ühte punkti rakendatud jõudu võib asendada 1 jõuga, mis rakendatud samasse punkti Tasakaalus olevaks jõusüsteemiks nim jõusüsteemi, mis mõjutades paigalseisvale kehale ei kutsu esile selle liikumist Jõumoment punkti suhtes- vektor, mis võrdub jõu rakenduspunkti kohavektori ja jõuvektori vektorkorrutisega. Jõupaarimoment- vabavektor, risti jõupaari tasandiga ja seda võib lugeda lahendatuks ükskõik mis punkti antud kehal. R=Ruutj. F12+ F22+2 F1F2 cosa Jõusüsteemide tasakaal- R=Fi=0 Mo=Mo(Fi)=0 Koonduv jõusüs...
toimub reaktsioon.(peenestamine) o Segamine-Aine segamisel hakkavad osakesed rohkem põrkuma ja reaktsioon kulgeb kiiremini. o Temperatuur-Osakeste liikumine temperatuuri tõstmisel suureneb ja reaktsioon toimub kiiremini. Energia muutumine reaktsioonides Mõisted o Reaktsiooni soojusefekt-Saaduste ja lähteainete energiante vahe. o Ühinemisreaktsioonid-Enamasti eksotermilised, ülekaalus on energia eraldumine sidemete tekkimisel. o Lagunemisreaktsioonid-Enamasti endotermilised, ülekaalus energia neeldumine sidemete katkemisel. Teooria o Keemiliste sidemete lõhkumiseks on vaja teha tööd, energia neeldub. o Energia eraldub tavaliselt soojusena, aga paljudel juhtudel ka valgusena. o Majade kütmine. o Soojusenergia muudetakse soojuselektrijaamades elektrienergiaks. Kütused Mõisted o Kütused-Parim energia salvestamise ja kasutamise võimalus.
Kovalentne side teeb sobivaks "elumolekulid" H, O, C ja N, sest neid iseloomustab võime moodustada kovalentseid sidemeid elektronpaari jagamise teel. C-C sidemel on 4 erinevat ehituse varianti biomolekulides lineaarne alifaatne (ilus sirge ahelake), tsükliline (ahelast tekkinud on süsinikuring), hargnenud (ahela küljes palju harusid) ja planaarne (mingi pundar aatomeid ahela otsas) Põhimõtteliselt kõik rakus toimuvad reaktsioonid on kovalentsete sidemete katkemised või tekked: funktsionaalrühmade ülekanne oksüdeerumine C-C sidemete teke või katkemine funktsionaalsete rühmade ümberpaigutumine molekulide kondenseerumine (- vesi) Sidemeenergia Sideme energia ehk kovalentse sideme tugevus on pöördvõrdeline seda moodustavate aatomite massidega, seetõttu ongi H, O, C ja N-i vahelised sidemed kõige tugevamad. Tuleks meeles pidada nelja järgneva sidemete energia:
sidemes. Polaarne side- elek paar küll ühine kuid ei jaotu tuumade väljas ühtlaselt. Iooniline side-laeg on täielikult ühel elem. Dipoolmoment- iseloomustab sideme ioonilisuse mahtu, mis on arvuliselt võrdne elementaarlaengu sajakordse väärtusega. Induktsioon-elektronegatiivse aatomi mõju edasikandumine piki sigmasidet. Isoeerija- sama mol mass ja valem erinev struktuur. Asendisomeer-erinevad paigutuse poolest. Radikaalne reaktsioon- toimub sümmeetriline sidemete katkemine(homolüütiline prot)ja moodustumine (homogeenne protsess). Polaarne reakts-mittesümmeetriline sidemete katkemine (heterolüütiline) ja tekkimine (heterogeenne). BRONSTEDI def: Hape-aine mis loovutab prootoneid.saab neg laengu muutub konj alusex Alus-aine mis seob prootoneid. LEWISE def: Hape-aine mis on võimeline liitma el paari. Alus-aine mis on võimeline looutama elek paari, ühendid millel vaba elek paar. Keemilise sideme polariseeritavus-
kaksikside süsiniku aatomite vahel. Alküünid on küllastumata süsivesinikud, mille molekulides esineb kovalentne kolmikside. Alküünide tähtsamaks esindajaks on etüün ehk atsetüleen HCCH. küllastunud ühend (e. alkaan) - C aatomite vahel on ainult ühekordsed sidemed, kõik vabad sidemed on küllastunud H-ga küllastumata ühend - süsivesinik, mis sisaldab kordseid sidemeid. Kaksikside on keemiline side, kus on ühinenud kaks elektronpaari.Kaksikside kuulub kovalentsete sidemete hulka. Kolmikside on keemiline side, kus on ühinenud kolm elektronpaari.Kolmikside kuulub kovalentsete sidemete hulka. Alküülimine on alküülrühmaga asenduse teostamine. Fenoolid (ka hüdroksüareenid) on aromaatsed ühendid, milles üks või mitu benseenituuma kuuluvat süsinikuaatomit on seotud hüdroksüülrühmaga. Hüdraatimine on keemiline liitumisreaktsioon veega. Dehüdrogeenimine on vesiniku eraldumine keemilise reaktsiooni käigus.
painutusvenitusharjutused ja hiljem juba funktsionaalseid harjutusi. Mida tuleks meeles pidada ! · Neil, kes on juba varem on sidemeid vigastanud, ei teki järgmistel kordadel nii suurt turset, kui esimesel korral. · Esmakordselt hüppeliigest vigastades tuleb olla eriti ettevaatlik kahe esimese kuu jooksul, et mitte korduvalt hüppeliigest vigastada. · Spetsiaalselt ettevalmistaval treeningperioodil tehtavad hüppeliigeste eriharjutused vähendavad vigastuste arvu. · Sidemete taastumisel on kasulik ravivõimlemine. · Haigele jalale tuleb anda rahu! Tugiside Kasutatud materjal : http://woman.delfi.ee/talje/trenn/article.php?id=14994500 http://www.inimene.ee/pages.php3/17080202 http://www.kliinikum.ee/ortopeedia/taagepera/I.pdf http://anklefoot.com/images/_borders/mall101.gif http://www.drgregmorris.com/drawings/ankle/ankle1.gif
Reageerivate ainete kontsentratsioon mida kõrgem on lähteainete konsentratsioon, seda kiirem on reaktsioon. Temperatuur mida kõrgem on temperatuur, seda suurem on aineosakeste energia. Katalüsaator aine, mis kiirendab reaktsiooni, kuid säilib reaktsiooni lõppedes samas koguses ja koostises. Ekso ja endotermilised reaktsioonid ·Eksotermilise reaktsiooni korral vabaneb soojus, kuid endotermilise korral neeldub. ·Eksotermilise reaktsiooni korral kulub lähteainete sidemete lõhkumiseks vähem energiat, kui saadusel sidemete tekkimisel vabaneb. · Keemiliste sidemete tekkimisel energia eraldub ning katkemisel energia neeldub Kütused ja kütteväärtused ·Energia salvestamise võimalused: mehaaniline- salvestatud suurde hoorattasse, mis pöörleb, Elektrienergia- kondensaator, Soojusenergia- väikesteks kogusteks termonõu ·Kütus- peamiselt süsinikühend, mille põlemisel vabaneb palju soojusenergiat
·Sideme pikkus Morse kõver näitab potentsiaalse energia sõltuvust aatomite vahelisest kaugusest Toodud näide kirjeldab H2 molekuli moodustumist kahest H aatomist H-H sideme pikkus 74 pm ja sideme energia 436 kJ/mol Mõningate keemiliste sidemete keskmised energiad Elektromagnetilise kiirguse spekter ja sideme energia E = h = hc-1 1 eV mol-1 = 96000 J mol-1 ehk ca 100 kJ/mol Elektromagnetilise kiirguse spekter ja sideme energia Pigmentide konjugeeritud kaksiksidemete süsteemid neelavad kiirgust nähtavas spektriosas Silmanägemises on oluline valguse poolt indutseeritud retinaali isomerisatsioon Keemilise sideme mudelid ühise elektronpaari mudel · G.N Lewis 1916
Keemiline reaktsioon on protsess, milles tekivad ja/või katkevad keemilised sidemed. KEEMILINE SIDE-jõud mis hoiab koos molekule. Keemiliste sidemete tekkel energia alati eraldub, keemiliste sidemete lõhkumiseks tuleb energiat kulutada. EKSOTERMILISTES reaktsioonides energia eraldub H<0(ühinemisreaktsioon), endotermilistes re.. neeldub(lagunemisreaktsioon). Suurus H näitab reaktsiooni saaduste ja lähtainete energiaTE vahet(reaktsioonil eralduvat või neelduvat energiat nim. Reaktsiooni soojusefektiks) VESINIKSIDE-on molekulide vaheline keemiline side
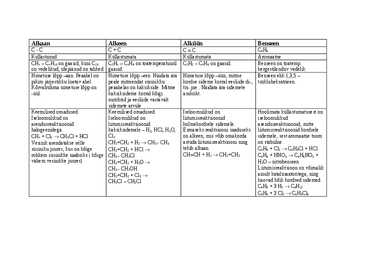
on vedelikud, ülejäänud on tahked gaasid. kergestilenduv vedelik Nimetuse lõpp aan. Peaahel on Nimetuse lõpp een. Näidata ära Nimetuse lõpp üün, mitme Benseen ehk 1,3,5 pikim järjestikku loetav ahel. peale mitmendat süsinikku kordse sideme korral eesliide di-, tsükloheksatrieen. Kõrvalrühma nimetuse lõpp on peaahelas on kaksikside. Mitme tri- jne.. Näidata ära sidemete -üül. kaksiksideme korral kõigi asukoht. numbrid ja eesliide vastavalt sidemete arvule Keemilised omadused: Keemilised omadused: Iseloomulikud on Hoolimata küllastumatusest on Iseloomulikud on Iseloomulikud on liitumisreaktsioonid iseloomulikud
1- mõisted Eksotermiline reaktsioon energia eraldumisega kulgev keemiline reaktsioon. Endotermiline reaktsioon energia neeldumisega kulgev reaktsioon. Keemiliste sidemete tekkel energia alati eraldub, keemiliste sidemete lõhkumiseks tuleb alati kulutada energiat. Kui saaduste energia on madalam kui lähtainetel on reaktsioon eksotermiline(energia eraldub) Kui saaduste energia on kõrgem kui lähtainetel, on reaktsioon endotermiline(energia neeldub) kovalentne side aatomivaheline keemiline side, mis tekib ühiste elektronpaaride moodustumisel. polaarne kovalentne side - kovalentne side erineva elektronegatiivsusega aatomite vahel, sidet moodustavatel aatomitel tekivad seejuures erinimelised osalaengud.
Oligomeerse valgu mõiste- On valgud mis koosnevad rohkem kui ühest polüpeptiid ahelast. 2. Valkude arhitektuur - konfiguratsiooni ja konformatsiooni mõisted, kolme(nelja) struktuuritaseme iseloomustus ja kirjeldus. Primaarstruktuuri mõiste ja ise-loomustus. Konfiguratsioon- On valgu struktuuri muutumine lõhkudes olemasolevad kovalentsed sidemed ja luua nendest uued Konformatsiooni - valgu kolmemõõtmelise struktuuri muutumist ilma kovalentsete sidemete lõhkumiseta nimetatakse valgu konformatsiooniks. Mis tuleneb vabast rotatsioonist ümber C-C sideme. Nelja struktuuritaseme iseloomustus ja kirjeldus- 1)Primaarstruktuur- On valgu kõige algelisem struktuur mis näitab aminohapete järjestus valgus esinevad ainult kovalentsed sidemed (peptiid- ja disulfiidsidemed) 2)Sekundaarstruktuur- Vesiniksidemete tekkimise tõttu valk saab kolmemõõtmelise struktturi kas a- heeliksi või B-struktuuri(volditud ahel).
Alus on aine, mis annab lahusesse hüdroksiidioone Tugev elektrolüüt on aine, mis esineb vesilahuses ainult ioonidena Nõrk elektrolüüt on aine, mis esineb vesilahuses ioonide ja molekulidena Redutseerimine on protsess, milles liidetakse elektrone Oksüdeerumine on protses, milles loovutatakse elektrone Valgud on polüpeptiidid Rasvad on triglütseriinid/ester Seep on rasvhappe sool Bensiin on süsivesinike segu Sahhariidid on polühüdroksükarbonüülühendid Keemilistes sidemete tekkel energia eraldub Pöörduva reaktsiooni tasakaal nihkub lähteainete lisamisel saaduste suunas Reaktsiooni kiirus lähteainete kontsentratsiooni suurendamisel kasvab Tahke joodi (I) aurustumisel katkeb molekulidevaheline side Allotroobid on lihtaine teisendid, mis erinevad 1teisest struktuuri või aatomite arvude poolest molekulis Isomeerid on liitaine teisendid, mis erinevad stuktuuri ja seetõttu ka omaduste poolest Isotoobid on elemendi teisendid, mis erinevad 1teisest neutronide arvu
Laiemas mõttes arvatakse alkaanide alla ka tsükloalkaanid, mis ei sisalda mitmiksidemeid, kuid sisaldavad tsükleid.Laiemas mõttes mõistetuna võivad alkaanid olla lineaarsed (üldvalem CnH2n+2) või tsüklilised (üldvalem C nH2n, n>2) .ALKAANIDE KEEMILISED OMADUSEDKuna alkaanid kuuluvad küllastunud süsivesinike alla, siis saavad nende keemilised reaktsioonid kulgeda ainult läbi olemasolevate sidemete katkemise ja uute tekkimise. Sidet süsiniku ja vesiniku (CH) ning süsiniku ja süsiniku (CC) vahel loetakse mittepolaarseks. Nende sidemete katkemisel jagatakse sidemel olev elektronpaar võrdselt. Üksiku paardumata elektroniga osakest nimetatakse radikaaliks. Radikaalideks lagunemist nimetatakse radikaalseks dissotsiatsiooniks ja nende radikaalide ühinemist radikaalseks rekombinatsiooniks
energia mis eraldub on keemiline energia mis eraldub soojuse, valguse või elektrina Keemiline energia soojus/ valgus/ elekter energia nivoo tähis on H aktiveerimis energia barjäär - energia mis on vajalik, et alustada reaktsiooni. Et alustada reaktsiooni peab kõigepealt ületama energia barjääri, mis omakorda nõuab energiat ning on igal reaktsioonil erinev. Peamiselt valitsevad 2 protsessi: 1) Keemiliste sidemete katkemine - energiat neeldub, on endotermiline 2) Keemiliste sidemete moodustumine - energiat eraldub, on eksotermiline Toimub see reaktsioon, millel on absoluutväärtus suurem Nt: söe põlemine C + O CO ühinemis oksüdeerumisreaktsioonid Kulgevad eksotermiliselt. Eksotermilises reaktsioonis neeldub lähteainetes olnud sidemete katkemisel vähem energiat kui eraldub saadustest olevate sidemete moodustumisel. Nt: elektrolüüs 2HO 2H + O
piiritus,co2,ATP(2),etanoolkäärimine-teostavad pärmseened ja mõned bakterid, moodustub 2 etanooli, ATP(2)autotroofid-org. Kes valmistavad ise anor-st ainetest org. Aineid, valgusenergia või keemiliste reaktsioonide energia arvel.,heterotroofidkasutavad oma aine- ja energiavajaduse rahuldamiseks väliskeskkonnast saadavaid valmis orgaanilisi aineid, Fotosüntees:assimilatsiooniprotsess, mille käigus salvestatakse valgusenergia orgaaniliste ühendite keemiliste sidemete energiaks.toimub taime rohelistes osades, mida vaja-valgusen. Co2,vesi,klorofüll,mis tekib-hapnik,tähtsus-ainuke looduses toimuv protsess, mille käigus muundatakse valgusen. Keemiliste sidemete energiaks, fotosüntees tagab süsiniku ja hapniku ringe,glükolüüs-süsinik on pärit mitokondri sisemusest,vesinik-mitokondri harjakeste membraanidest,hapnik-raku tsütoplasmavõrgustikust,valgusfaas-klorofülli ergastunud
Mõisted: 1) Elektrolüüt aine, mis lahustumisel või sulamisel jaguneb täielikult või osaliselt ioonideks ja juhib elektrit. 2) Elektrolüütiline dissotsiatsioon aine jagunemine lahustumisel ioonideks. 3) Mitteelekrolüüt aine, mis vesilahuses ei jagune ioonideks ja mille lahus ei juhi elektrit. 4) Hüdraatumine e. hüdratsioon - lahustunud aineosakeste seostumine vee molekulideda. 5) Endotermiline sidemete lõhkumiseks tuleb kulutada energiat. 6) Eksotermiline sidemete tekkel alati energia eraldub. Ainete jagunemine: I Happed jagunevad - positiivseteks vesinikioonideks ja negatiivseteks happeanioonideks. HCl -> H + Cl H3PO4 -> 3H + PO4 II Alused jagunevad positiivseteks metalliioonideks ja negatiivseteks hüdroksiidioonideks. NaOH -> Na + OH Al(OH)3 -> Al + 3OH
keskkonda. 10. Millised on 4 interkulturaalse pädevuse staadiumit (Gudykunsti järgi)? 1. Teadvustamata pädevuse puudumine 2. Teadvustatud pädevuse puudumine 3. Teadvustatud pädevus 4. Teadvustamata pädevus Eesmärgiks on see, et interkulturaalne pädevus muutuks loomulikuks. 11. Akulturatsioonistrateegiad John Berry järgi (kaks dimensiooni, vastavalt neli strateegiat). 1. Kui omaenese eripära/identiteedi hoidmine ja domineeriva kultuuriga sidemete hoidmine on tähtsad, siis toimub integratsioon. 2. Kui omaenese kultuurilise eripära/ identiteedi hoidmine pole tähtis, aga domineeriva kultuuriga sidemete hoidmine on tähtis, siis on tegu assimilatsiooniga. 3. Kui domineeriva kultuuriga sidemete hoidmine pole tähtis, aga omaenese kultuurilise eripära/identiteedi hoidmine on tähtis, siis toimub eraldumine. 4. Kui ei omaenese kultuurilise eripära/identiteedi hoidmine ega ka domineeriva
1.SÜSINIKU ASEND, EHITUS, SIDEMED, MAKSIMAALNE JA MINIMAALNE OKSÜDATSIOONI ASTE. 2.SÜSINIK LOODUSES: a)lihtainena-teemant, grafiit, kivisüsi, koks, pruunsüsi, antratsiit. B)LIITAINENA-NAFTA, MAAGAAS, KARBONAADID, CO2 3.TEEMANT: koostis-tahke, C leidumine-vähe, L-Ameerikas, Aafrikas, I-Venemaal ehitus-korrapärane, sidemete tugevus-tugevad soojus ja elektrijuhtivus-ei juhi elektrit, juhib soojust hinnalisus-väga kallis sulamine-üle 3000kraadiC värvus-läbipaistvast mustani kasutamine-briljandid, lõiketerad 4.GRAFIIT: koostis-tahke, C leidumine-palju ehitus-korrapärane sidemete tugevus-nõrgad soojus ja elektrijuhtivus-juhib elektrit ei juhi soojust hinnalisus-odavam sulamine-üle 3000krradiC värvus-hallikas must kasutamine-pliiatsi südamikud, raketidüüs 5