(sulamistemp, keemistemp, lahustuvus vees) lähtuvalt süsinike arvust ja hargnevusest) Näide: a) kumb lahustub vees paremini- kas propanool või metanool? Põhjenda b) kummal keeb kõrgemal temperatuuril- kas etanool või butanool? Põhjenda. 4) Kuidas tõestada, et alkohol on nõrga happe omadustega? 5) Alkoholide keemilised omadused. Näide: Kirjuta reaktsioonivõrrandid ja anna saadustele nimetused a) etanooli põlemine b) metanool + kaltsium c) propanooli põlemine 6) Metanool (igapäeva nimetus, saamine, füüsikalised omadused, toime organismile, kuidas ravitakse metanooli mürgitust, metanooli kasutamine) 7) Etanool (saamine, füüsikalised omadused, kasutamine) 8) Millest oleneb etanooli imendumise kiirus organismi? 9) Joobeastmed 10) Millised reaktsioonid toimuvad organismis, kui inimene on tarbinud etanooli? 11) Etaan-1,2-diool (valem, füüsikalised omadused, kasutamine)
Ehk osake, millel on üksik paardumata elektron. Pürolüüs Aine lagunemine kõrge temperatuuri toimel. Püsolüüsi tulemusena tekib väga erinevaid aineid. Orgaaniliste ainete kuumutamisel õhu juurdepääsuta saadakse mitmeid lenduvaid aineid, sh veeauru. Tihti või täheldada aine söestumist, polümeersete ainete teket ja teisi kõrvalprotsesse. Pürolüüsiprotsess on ka tahkete kütuste nt põlevkivi utmine. Täielik põlemine - toimub piisava hapnikuhulga olemasolul. Hapniku puudujäägi korral pole põlemine täielik. Füüsikalised omadused Vastavalt süsinikahela pikkusele ja selle ehitusele on alkaanid gaasilised, vedelad või tahked. Vedelas või tahkes olekus on nad veest kergemad. Alkaanid on veel peaaegu lahustumatud. Alkaanid on hüdrofoobsed ehk vett-tõrjuvad. Alkaani molekulidel ei teki vastastikmõju vee molekulidega ning alkaanid ei segune veega ega märgu. Füsioloogilised omadused
Alkaanide omadused: Põlemine[(CH4+2O2->2CO2+H2O) II- 27513 III-24385 IV-64106] Halogeenimine[Cl2F2 Br2 I2] (CH4+Cl2->CH3Cl+ HCl)Saamine küllastumata ühenditest Füüsikalised omadused:ei lahustu vees, veest kergemad, vesiniksidemed puuduvad, C1-C4=gaasid, -14=vedelad, 15- =tahked, lõhnatu, värvitu(mitte kõik), mürgised, mõjub knsile, kergesti lenduvad. Alkeenide omadused: Põlemine[C2H4+ 302->2O2+2O2 2 C5H10+ O2- >10CO2+10H20]Hüdrogeenimine (H2 liitmine) Halogeenimine(VIIA rühma liitmine) Vesinikhalogeenimine(HF,HBr,HI,HCl) Vee liitmine Ei lahustu vees, veest kergemad. Alkoholid, aldeh. Ketoonid.Füsioloogilised omad:narkootilise toimega, kahjustab knsi, ald. Mürgisemad kui ketoonid, nahale sattudes tekitavad põletikke, organismist eraldub aeglaselt. Metanaal e. formaldehüüd.terava lõhnaga, mürgine gaas. Lahustub vees, metaani vesilahus-formaliin, kas. Desinfitseerimisvahendina, säilitatakse preparaate.Eta...
Graafiline kujutis Orgaaniliste ainete oksüdeerumine Süsiniku oksüdatsiooniaste (o.-a.) võib olla ühendites IV kuni IV. Ühes molekulis võib olla erineva o.-a.-ga süsiniku aatomeid. Mida madalam on süsiniku o.-a. (mida rohkem on temaga seotud vesiniku aatomeid), seda rohkem eraldub oksüdeerumisel energiat. Järelikult on orgaanilised ained energiaallikad. Nende põlemisel või plahvatamisel, aga ka elusorganismides oksüdeerumisel eraldub energiat, mis lõpuks muutub soojuseks. Põlemine ja bioloogiline oksüdeerumine on reaktsioonide poolest erinevad, kuid lõpptulemused on samad (eraldub CO2 ja veeaur). Eralduv energia kasutatakse looduses organismide elutegevuse tagamiseks, inimtegevuses aga masinate käivitamiseks. Kütuste puhul arvutatakse kütteväärtust, toit- ja toiduainete puhul toiteväärtust ehk kalorsust. Oksüdeerumisprotsessid (hingamine, põlemine jne) kulgevad erineva kiirusega ja tavaliselt aeglaselt. Protsesse on võimalik kiirendada katalüsaatori abil
valgusena. Kui lõke põleb, toimub keemiline reaktsioon. Selle tunnuseks on ainete muundumine. Kui puuhalud põlevad siis nad muutuvad tuhaks ja eraldub suits ning veeaur. Kui hapniku on vähe, sisaldavad saadused mürgist vingugaasi süsinikdioksiidi (CO 2) ja tahma, mis on üks süsiniku esinemisvormidest. Kui lõkkes kütus põleb, siis lagunevad tema molekulid aatomiteks, mis ühinedes hapnikuga moodustavad teistsuguseid molekule. Kui põlemine on täielik, siis on saadusteks gaasiline süsinikdioksiid (CO2) ja veeaur (H2O). Kui hapniku on vähe, sisaldavad saadused mürgist vingugaasi süsinikdioksiidi (CO2) ja tahma, mis on üks süsiniku esinemisvormidest. Keemias nimetatakse põlemiseks kiirelt kulgevat oksüdatsiooniprotsessi, mille käigus aine ühineb hapnikuga. Hapnik käitub oksüdeerijana ja redutseerub ning põlev aine käitub redutseerijana ning oksüdeerub. Põlemisele iseloomulik reaktsiooon:
................... 12. Kui kustutatud lubjale lisada ........................., muutub ta ........................... , ................................. vedelikuks, mida nimetatakse .................................... 13. Seismisel .......................... lubjaosakesed ........................... ja sette peale jääb puhas ............................... 14. Vastavad valemid ja keemilised reaktsioonid on järgmised : Lubjakivi: ...................... Põlemine: ............................................................ Põletatud lubi : ................................................................ Kustutamine: ................................................................. Kustutatud lubi: .............................................................. Lubja karboniseerumine: ................................................... RISTSÕNA 1 2 3 4 5 6 7
Millise OA-ga on kõige enam a) Oksüdeerunud süsinik +4 (CO2) b) Redutseerunud süsinik -4 (CH4) Mis moodustub orgaanilise aine täielikul põlemisel? CO2+H2O Mis on pürolüüs? Aine lagunemine kõrge temperatuuri toimel Millal tekib põlemisel tahm? Kui põlemine on mittetäielik või pürolüüsiprotsessis Isomeeria On nähtus, kus ühenditel on ühesugune koostis kuid erinev struktuur ja sellest tulenevalt erinevad omadused Isomeerid On ühendid, millel on ühesugune koostis, kuid erinev struktuur ja erinevad omadused Ch3-Ch2-OH (C2H6O) Etanool, piiritus, vesilahuses viin, 78kraadi juures
Päikese vanus on 4,57 miljardit aastat. Päikese läbimõõt on 1,392 miljonit kilomeetrit ja mass 1,9891×1030 kg Päikese pinnatemperatuur on 5778 K, kuid märksa kuumemad on Päikese kroon kuni 1,8 miljonit K ja tuum umbes 15,7 miljonit K. Päike koosneb peamiselt vesinikust (73,46% massi järgi) ja heeliumist (24,85% massi järgi), kõiki ülejäänud elemente on 1,67% massi järgi PÄIKE 1. gaasipilve kokkutõmbumine 2. vesiniku põlemine heeliumiks 3. heeliumi põlemine süsinikuks. Selle tagajärjel muutub Päike punaseks hiiuks. 4. Päikene heidab ära oma atmosfääri, tõmbub kokku valgeks kääbuseks ja hakkab aeglaselt jahtuma. PÄIKESE STAADIUMID TÄNAN KUULAMAST
röövlinnud, näiteks valgepeamerikotkad, mõõkvaalad või merilõvid ning surevad omakorda mürgitusse. Nii jätkub nafta tõttu mereloomade toiduahela saastumine. Kõige populaarsem nafta saadus on bensiin ja petrooleum. Maailma teedel liigub igapäevaselt 555 miljonit liiklusvahendit, neile lisandub igal aastal autotehastest 40 miljonit autot. Enamus autosid töötab kas bensiini või diisli peal, mis on nafta saadused. Kui auto mootoris toimuks täielik põlemine, ei tekiks palju ohtlikke jääge, kuid seda ei juhtu peaaegu kunagi. Näiteks tekitab seesama mittetäielik põlemine kasvuhoonegaase, mis põhjustavad muutusi maakera atmosfääris ning mõjutab kliimat, muutes ilmastiku soojemaks. Ning kui kliima soojeneb, põhjustab see omakorda igikeltsa sulamist, mis asub poolustel. See omakorda viib suurte uputusteni ning katastroofideni. Nafta on kasutusel paljudel aladel, eriti keemiatööstuses ning kütusetööstuses, kuid kauaks seda jätkub
Millise OA-ga on kõige enam a) Oksüdeerunud süsinik +4 (CO2) b) Redutseerunud süsinik -4 (CH4) Mis moodustub orgaanilise aine täielikul põlemisel? CO2+H2O Mis on pürolüüs? Aine lagunemine kõrge temperatuuri toimel Millal tekib põlemisel tahm? Kui põlemine on mittetäielik või pürolüüsiprotsessis Isomeeria On nähtus, kus ühenditel on ühesugune koostis kuid erinev struktuur ja sellest tulenevalt erinevad omadused Isomeerid On ühendid, millel on ühesugune koostis, kuid erinev struktuur ja erinevad omadused Ch3-Ch2-OH (C2H6O) Etanool, piiritus, vesilahuses viin, 78kraadi juures
Aatomimudel Aine massi jäävuse Anioon Aatomituum seadus Asendusreaktsioon Aatomnumber Aine omadused Aurustumine Destillatsioon Koefitsient ehk Prooton Destillaat kordaja Puhas aine Elektrijuhtivus Kolb Põlemine Elektron Kondensatsioon Põleti Elektronskeem Kontsentratsioon Reaktsioonivõrrand Elektronkate Korrosioon Redoksreaktsioon Elektronkiht Kuumutamine Redutseerija Elemendi järjenumber Lagunemisrektsioon Segu Filtrimine Lahus Setitamine Filtraat Lahustumine Soojusjuhtivus Fotosüntees Lahuse massiprotsent Sool
Amiini reageerimine : hape R - NH2 + HCl R NH3 Cl vesi R NH2 + H2O R NH3 OH alkeen(-een)-süsinikuvahelise kaksiksidemega ühendid n : CH2 = CH CH3 (propeen) alküün(-üün)-süsinikuvahelise kolmiksidemega ühendid n : CH C CH3 (propüün) keemilised omadused 1 reageerimine halogeeniga ( VIIA2 ) 2 reageerimine vesinikhalogeeniga ( H VII A ) 3 reageerimine veega e. hüdraatimine ( H2O ) 4 reageerimine vesinikuga e. hüdrogeenimine | üüneen | eenaan | ( H2 ) 5 põlemine ( een/üün + O2 CO2 + H2O ) 6 polümerisatsioon kaksiksidemed katkevad ja tekivad ühesugustest Areenid Benseen-lihtsalim aromaatne süsivesinik C6H6 -NO2 nitro F: vedelikud/kristallid,ei lahustu vees,lahustuvad eetrites,lahustavad vaiku/rasvu Fülog: narkootilised,mürgised,suur sissehingamine-krambid, närvisüsteem,maks,vereloomeelundid,nahka ärritavad K: oksüdeerumine,põlemine(1alküülimine,2halogeenimine,3nitreerumine) 1 C6H6 + RCl C6H5R + HCl (C6H6 + R VIIa C6H5R + H VIIa)
Anorgaaniline: Keemiline side-iooniline side NaCl, Sulamistemp- üle 350 o, Keemistemp üle 750o, Lahustuvus a)vees-hea, b)orgaanilistes ainetes halb, süttivus-enamasti ei sütti, Elektrijuhtivus- enamasti juhivad. Orgaaniline: Keemiline side- enamasti kovalentne side CH 4-metaan, Sulamistemp alla 350o, Keemistemp alla 750o, l ahustuvus a)vees- enamasti halb, b) Orga. Ainetes hea, süttivus enamasti süttivad, Elektrijuhtvus- enamasti ei juhi. Isomeeria: On nähtus kus ainetel n ühesugune element koostis ja molekulmass, kuid erinev struktuur ja seetõttu ka erinevad omadused. Valents olek: -C- Neli üksiksidet, -C= 2 üksiksidet 1 kaksik side, =C= 2 kaksikside, -C= 1 üksikside ja 1 kolmikside Valentsolekud:Lämmastik(N): -N-, -N=, N=, Hapnik(O): -O-, O=, Vesinik(H): H- Valents: Näitab mitu kovalentset sidet võib antud aatom moodustada. Orgaaniliste ühendites süsiniku valents on alati 4. Molekulvalem: Näitab aine koostist kui palju ja milliste ele...
Litosfäär- on maakera suhteliselt jäik väline kest, mis koosneb maakoorest ja vahevöö ülemisest osast Pedosfäär- e.mullastik, mis hõlmab maakoore pindmist kihti, kus toimuvad mullatekkeprotsessid Hüdrosfäär- osa maast, mis on täidetud veega Atmosfäär- e. õhkkond. Maa sfäär, Maad ümbritsev õhukiht Biosfäär-maa funktsionaalne sfäär, mis koosneb Maa sfääride nendest osadest, kus elavad organismid, Litosfäär- 50-200km-maakoor ja vahevöö ülemine osa. Muutused on aeglased, toimuvad kivimite ringe ja ainevahetus teiste sfääridega. Litos. pinnal areneb muld ja kujun. Taimestik. Pedosf- mõnest cm-10m. Täielikult biosfääri osa- Ilma elustikuta muldi ei kujune. Muutused on kiiremad kui litos. Hüdros. Maa vesikeskkond-. Litost. Väiksema tihedusega ja vesi on liikuvam kui kivimid. Seetõttu toim. ka muutused kiiremini. Vee liikumine moodustab osa veeringest, millega seotult kulgevad ka teised aineringid. Ilma veeta poleks eeldusi taimede, loomade mul...
Q= lambda * m 11. Mida näitab sulamissoojus? Soojushulk, mis on vajalik ühe kg aine sulatamiseks tema sulamistemperatuuril. J/kg 12. Aurumine ja kondenseerumine ( mõisted, arvutusvalem ) Üleminek mis olekust mis olekusse? Q= L*m 13. Mida näitab aurumissoojus ( keemissoojus ) ? Soojushulk, mis on vajalik 1kg aine aurustamiseks jääval temperatuuril. Kui jäävad temp-ks on keemistemperatuur, siis on L ka keemissoojus. J/ks 14. Põlemine ( mõiste, valem ) Põlemine on oksüdatsiooniprotsess. Q=km 15. Mida näitab kütteväärtus? Soojushulk, mis vabaneb 1kg kütuse täielikul põlemisel. 16. Termodünaamika I seadus ( sõnastus, valem ) Süsteemile antud soojushulga arvel suureneb tema siseenergia ning süsteem teeb pärisjõudude ületamiseks tööd. Q=delta U+A 17. Termodünaamika II seadus ( vali üks sõnastus ) Pole võimalik masin, mis töötaks ainult teise keha arvelt. 18. Pööratav protsess ( mõiste, näide ) Protsess, mida saab tagasi pöörata
1. Mõisted Süsteem-omavahel seotud objektide terviklik kogum, nt. auto=süsteem, automootor=alamsüsteem Litosfäär-on maakera suhteliselt jäik väline kivimiline kest, mis koosneb maakoorest ja vahevöö ülemisest osast. Litosfäär ulatub 50-200 km-ni. Muutused toimuvad aeglaselt, see on jäik ja püsiv. Kuid seal siiski toimub kivimite ringe ja ainevahetus teiste sfääridega. Litosfääri pinnal areneb muld ja kujuneb taimestik. Seal on ka fosiilkütused ja teised maavarad. Pedosfäär-ehk mullastik hõlmab maakoore pindmise kihi, milles mikroobid, seened ja taimed sünteesivad ja muundavad orgaanilist ainet. Mulla mineraalne osa pärineb litosfäärist. Pedosfäär on täielikult biosfääri osa ilma elustikuta muldi ei kujune. Muutused toimuvad kiiremini kui litosfääris. Ulatub 1cm 10m-ni. Hüdrosfäär-hõlmab Maa mineraalidega keemiliselt sidumata vee: maailmamere, järvede, jõgede, soode, mulla-, põhja-, atmosfääri- ja listikuvee. Hüdrosfäär on litosf...
Kosjalkäigul saadakse korvi ning kirikukoolis karistab neid õpetaja nende kõvade peade pärast. Vennad lõhuvad akna ning põgenevad. See tekitab kirikuisas palju pahameelt. Lisaks sellele tekib vendadel enne kooli minekut ka kaklus Toukola küla noortega ning sõnelus "Rajamäe rügemendiga". Nad pilkavad neid ning ning saadavad nende kaudu kihelkonna praostile inetu sõnumi. Oma laiskuse ja tülinormisega saavad vennad endale külas palju vaenlasi. Jukola talu sauna maha põlemine ning Mäkelä toodud sõnum inimeste vihast, viib vennad otsusele oma talu rendile anda ning minna metsa elama. 2. Koostage 1 venna karakteristika. Eero oli Jukola talu pesamuna. Ta oli väga terava keelega ning ninatark. Kuid kõigist vendadset oli ta kõige õpivõimekam. Ta oli ainus, kes suutis lugemise selgeks saada. Vennad aga arvasid, et Eero on liiga ärahellitatud ning tihtilugu suskisid nad teda lühikese kasvu pärast. Kuid Eero ei olnud kitsi vastu torkama
Keemilised reaktsioonid Keemiline reaktsioon ja reaksiooni võrrand: Ühe või mitme aine (lähteaine) muundumist teisteks aineteks (saadusteks) nimetatakse keemiliseks reaktsiooniks. Keemilisel reaktsioonil moodustunud ained erinevad lähteainetest koostise ja omaduste poolest. Keemilise reaktsiooni ülesmärkimiseks kasutatakse reaktsioonivõrrandit. Tekkereaktsiooniks nimetatakse ühendi tekkimist vastavatest lihtainetest. Keemilises reaktsioonis muutuvad molekulid, kuid aatomite liik ja arv ei muutu. Reaktsioonis osalevate ainete massi- ja ruumala suhted: Keemilise reaktsiooni võrrand on matemaatiline võrrand. Reaktsioonivõrrand väljendab reaktsioonis osalevate ainete moolide suhet. Reaktsioonivõrrand näitab reaktsioonis osalevate ainete massivahekorda. Lähteainete kogumass on võrdne saaduste massiga. n = m/M Kui reaktsioonist võtavad osa gaasilised ained, saame reaktsioonivõrrandist arvutada ka reageerivate gaaside või gaasiliste reakts...
33. Termodünaamilise keha drosseldamise olemus. Drosseldamist iseloomustav skeem. Voolava vedeliku, gaasi, auru jne. rõhu vähendamine takistuse ehk drosseli abil. Mida suurem on takistus seda suurem on rõhulang. Drosseldamisel juga kiireneb. Joonis TV ja vihikus. 37. Otto ringprotsess pv ja Ts diagrammil koos seletusega. Mootori surveastme mõiste. 1) 1.-2. Küttesegu isoentroopne komplimeerimine silindris 2) 2. Segu süütamine 3) 2.-3. Isohoorne põlemine 4) 3.-4. Gaaside adiabaatiline paisumine (lükkavad silindrit) 5) 4.-1. Soojuse isohoorne eemaldamine mootori silindrist. Paisumistöö komplimeerimistöö = kasulik töö Üheks põhiliseks karakteristikuks sisepõlemismootoritel on surveaste, mis väljendab silindri kogumahu(V1) ja põlemiskambri mahu (V2) suhet = (V1 / V2 ) . Autodel kuni 10 38. Diseli ringprotsess pv ja Ts diagrammil koos seletusega. 1) 1.-2. Siin komplimeeritakse õhk. 2) 2
33. Termodünaamilise keha drosseldamise olemus. Drosseldamist iseloomustav skeem. Voolava vedeliku, gaasi, auru jne. rõhu vähendamine takistuse ehk drosseli abil. Mida suurem on takistus seda suurem on rõhulang. Drosseldamisel juga kiireneb. Joonis TV ja vihikus. 37. Otto ringprotsess pv ja Ts diagrammil koos seletusega. Mootori surveastme mõiste. 1) 1.-2. Küttesegu isoentroopne komplimeerimine silindris 2) 2. Segu süütamine 3) 2.-3. Isohoorne põlemine 4) 3.-4. Gaaside adiabaatiline paisumine (lükkavad silindrit) 5) 4.-1. Soojuse isohoorne eemaldamine mootori silindrist. Paisumistöö komplimeerimistöö = kasulik töö Üheks põhiliseks karakteristikuks sisepõlemismootoritel on surveaste, mis väljendab silindri kogumahu(V1) ja põlemiskambri mahu (V2) suhet (V1 / V2 ) . Autodel kuni 10 38. Diseli ringprotsess pv ja Ts diagrammil koos seletusega. 1) 1.-2. Siin komplimeeritakse õhk. 2) 2
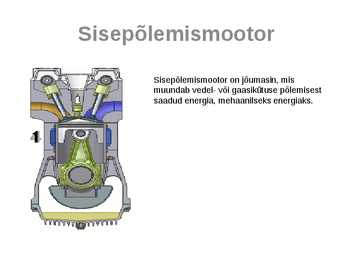
1. Gaaside , võrreldes vedelate ainetega , annavad ennast kokku suruda . 2. Gaasid kokkusurumisel kuumenevad . 3. Gaasid põlemisel , see tähendab kuumenemisel , paisuvad . Autodel kasutatakse valdavalt sisepõlemismootoreid . See on soojusjõumasin , kus põletatakse kütust ; bensiini , diiselkütet , parafiini , gaasi , piiritust , taimeõli jne . Kütuse põlemisel silindris muudetakse kütuse olev keemiline energia mehaaniliseks tööks . Põlemine on keemiline reaktsioon , kus kütuses olevad aineosakesed ühinevad õhuhapnikuga . Mootoreid iseloomustavad põhinäitajad .. Kolvi ülemine ja alumine surnud seis ( üss ja ass ) : need on kolvi liikumistee piirasendid silindris . Kolvi käik : kolvi teekonna pikkus silindris ülemise ja alumise surnud seisu vahel . Põlemiskambri maht : ruumala , mis jääb pealepoole kolbi , kui kolb on ülemise surnud seisus . Silindri töömaht : ruumala , mis jääb silindris ülemise ja alumise surnud
ja karjääridest välja pumbata 1015 tonni vett. Põlevkivikaevanduste kuivendamise ning suurte reostuskollete pikaajalise koosmõju tulemusel on aga tõsiselt kahjustada saanud ülemised põhjaveekihid. Põletamisel eraldub õhku suures koguses süsinikdioksiidi, vääveldioksiidi ja lendub orgaanilisi ühendeid ning raskmetalle. Põlevkivi tuhk on kõrge leelisusega ning ohustab ümbritsevat keskkonda. 2012 aasta juuli kuus avastati Kohtla-Järve poolkoksimäe põlemine. See põlemine on kestnud tegelikult juba aastakümmneid, ning jätkub ka praegu. Selle kustutamine on väga kallis.
Tahked kütused ja gaaskütused 1. Mis on kütus ja mis eesmärgil teda kasutatakse? Mis tingimusi peavad kütuseks kasutatavad ained täitma? Kütus e kütteaine on süsivesinikke sisaldav põlevaine, mida kasutatakse soojusenergia saamiseks või keemiatööstuse toorainena. 2. Kuidas liigitatakse kütuseid? (agregaatolekult, päritolult) a)tahke, vedel, gaasiline b) looduslik, tehislik 3. Mis on kütuste põletamise eesmärk? Mis tingimused peavad olema täidetud, et põlemine toimuks? (tule tetraeeder) Kütuseid, nii tahkeid kui vedelaid, põletatakse energia saamise eesmärgil. Oxygen hapnik, heat kuumus, fuel kütus, chain reaction ahelreaktsioon. 4. Missugusel viisil võib põlemisprotsess toimuda? leegitsemine, hõõgumine, plahvatus 5. Kirjelda põlemissaadusi, kui kütus koosneb süsinikust, vesinikust, lämmastikust, väävlist ja mineraalsooladest. (täielik ja mittetäielik põlemine) Kütuse täielikul
3. millised tegurid ja kuidas mõjutavad kristalsete ainete lahustuvust vees? 4. millised tegurid ja kuidas mõjutavad keemiliste reaksioonide kiirust? 5. elektrolüütiline dissotsiatsioon? Näide 6. millised iseloomulikud ioonid tekivad hüdroksiidide ehk aluste dissotsiatsioonil vesilahuses? Milline on sellise lahuse pH 7. millised iseloomulikud ioonid tekivad hapete dissotsiatsioonil vesilahuses? Milline on sellise lahuse pH? 8. katalüsaatorid 9. mis on põlemine? Kuidas toimub tahkete, vedelate ja gaasiliste ainete põlemine? Millised tingimused on vajalikud, millised produktid tekivad? 10. milliseid aineid nim. isomeerideks? Mis on sama, mis on erinev? Vastused 1. seitsmenda rühma elementidel on aatomivälises elektronkihis 7 elektroni ja kuna ta tahab 8 kokku saada võtab 1 juurde ja kuna elektroni laeng on negatiivne, tekib anioon. 2. energia jäävuse seadus energia ei teki ega kao kuid võib muunduda ühest
Nende struktuurvalemeid võib kirjutada, kujutades tsükleid hulknurkadena. Kõigil tsükloalkaanidel võib olla mitmesuguseid alküülderivaate (molekulide koosseisus on ka sirge ahelaga osi). Neid loetakse aga ikkagi tsükliliste ühendite hulka kuuluvateks. Tsükloalkaanide omadused on küllalt lähedased alkaanide omadustega. Need ühendid on hüdrofoobsed, neist koosnevad materjalid põlevad hõlpsalt ning annavad asendusreaktsioone. Põhiliseks leidumisallikaks on nafta. Täielik põlemine: CH4 + 1,5O2 CO2 + 2H2O Mittetäielik põlemine: 2CH4 + 3O2 CO2 + 4H2O + C Halogeenidega (VIIA): CH4 + Br2 CH3Br + HBr Vesinikhalogeenidega: CH4 + HBr CH3Br + H2 Oksüdeeerumine: 2CH4 + O2 2CH3OH Homoloogiline rida: 1. metaan CH4 2. etaan C2H6 3. propaan C3H8 4. butaan C4H10 5. pentaan C5H12 6. heksaan C6H14 7. heptaan C7H16 8. oktaan C8H18 9. nonaan C9H20 10. dekaan C10H22
1.2 Nimetamine. (vt töölehtedelt) 1.3 Saamine. a) primaarsete alkoholide oksüdatsioonil (O2, KMnO4) 2 R-CH2-OH + O2 2 R-CHO + 2 H2O Näide: CH3-CH2-CH2-OH + O2 kirjuta ise edasi 1.4 Keem. omadused. a) oksüdatsioon (tekib karboksüülhape, uus aineklass); kõrgel temperatuuril põlevad, tekitades CO2 ja H2O. 2 R-CHO + O2 2 R-COOH R-COOH - karboksüülhape ! CH3-CHO + Ag2O CH3-COOH + 2 Ag (hõbepeeglireaktsioon) R-CHO + 2 Cu(OH)2 R-COOH + 2 CuOH + H2O R-COOH + Cu2O +2 H2O b) põlemine (kõrgel temperatuuril) R-CHO + O2 CO2 + H2O (põlemine) c) reageerimine alkoholidega (I etapis tekib nn poolatsetaal, mis täiendava alkoholi lisamisel ja sellega reageerides tekitab nn atsetaali) I etapp R-C+HO- + R`-O-H+ R-CH(-O-R`(-OH) (kohustuslik on vaid see) II etapp R-C+H(-O-R`,-O-H+) + R`-O-H+ R-CH(-O-R`)2 + H2O ! Reaktsioon toimub nii, et omavahel ühinevad reagendid nende reaktsioonitsentrite kaudu ,,+" ja ,,-,, laengut kandvad aatomid. 1.5 Füsioloogiline toime. (vt õpikust)
Aineklass Nimetuste süsteem Füüsikalised omadused Keemilised omadused Leidumine/kasutamine alkaan Järelliide –aan Hüdrofoobsed. 1) Täielik põlemine kiire oksüdatsioon Maagaas (CH4) CnH2n+2 C1-C4 –gaasiline Süsinikahela pikenedes C6H12 + 8O2 → 5CO2 + 6H2O Nafta (vedelate alkaanide segu C5-C8 –vedel tihedus, st°,kt°suurenevad. 2) Oksüdeerumine halogeeniga Parafiin (tahke-te alkaanide segu) Nt
Vabade elektronide suunatud liikumine metallis on elektrivool. Selle põhjustab elektrijõud. 28.Missugused kehad omavad kineetilist energiat? Kineetilist energiat omavad liikuvad kehad, millel on võime teha tööd. 29.Millest sõltub kineetilise energia väärtus? Energia on võrdne suurima tööga, mida keha võib teha. 30. Mis on erisoojus? Erisoojus on aine soojuslikke omadusi iseloomustav füüsikaline suurus. 31. Mis on kondenseerumine? Kondenseerumine on aurumise pöördnähtus 32.Mis on põlemine? Põlemine on keemiline reaktsioon, millest eraldub soojust ja valgust. 33. Mis on kütteväärtus? Kütteväärtus on soojushulk, mis vabaneb 1kg kütuse täielikul põlemisel. 34.Nimeta fotosünteesi toimumise tingimused. Fotosünteesi toimumise tingimused on: Valgus ja rohelised taimed. 35.Millest saadakse tuumaenergiat? Tuumaenergiat saadakse kergete tuumade ühinemisel või raskete tuumade lagunemisel. 36.Nimeta tuumaenergia plussid ja miinused.
Katse ,,Põlemine" Katse vahendid: küünal, metallese, tikud Katsekäik: 1.Panen küünla põlema. 2.Asetan leegi sisse metallese. 3.Jälgin toimuvaid muutusi ja kirjeldan need. Kirjeldus: Kui ma panin metallese leeki metallese hakkas minema mustaks. Kuigi oli ka tunda soojust (metalleses hoides). Järeldus: Metallist tehtud esed annavad soojust hästi üle. Pildid: enne-ajal-pärast
Keemilised vooluallikad Keemilised vooluallikad on vooluallikad, millega saadakse elektrivoolu redoksreaktsioonide kulgemisel vabaneva energia arvel. Elektrienergia saamiseks kulutatakse elektrokeemiliselt aktiivseid aineid aineid, mis astuvad redoksreaktsioonidesse elektroodidel, liites või loovutades seejuures elektrone. Keemiliste vooluallikate tähtsaimad iseloomustussuurused on elektromotoorjõu, tööpinge, mahutavus (vooluallikast saadav elektrihulk) ja tööiga. Nad jagunevad 3 rühma: galvaanielementideks, akudeks ja kütuselementideks, kuigi kahel viimasel on sarnasusi galvaanielementidega. Galvaanelemendid Galvaanielemendid on keemilised vooluallikad, milles on elektrienergia saamiseks võimalik ainult ühekordne elektrokeemiliselt aktiivsete ainete kasutamine, sest nende ainete läbireageerimise järel muutub galvaanielement vooluallikana kasutamiskõlbmatuks.Tänapäeval on galvaanielementidest kasutusel põhiliselt kuivelemendid, mill...
surnud seisus nimetatakse põlemiskambri mahuks. Töömahu ja põlemiskambri mahu summat nimetatakse üldmahuks. Mitmesilindriliste mootori kõigi silindrite töömahtude summat nimetatakse mootori töömahuks. Väiksematel mootoritel tähistatakse töömahtu kuupsentimeetrites, suurematel mootoritel liitrites. Surveaste on parameeter, mis iseloomustab sisepõlemismootori (kolbmootori) maksimaalse ja minimaalse põlemiskambri mahu suhet. Silinder - Silinder moodustab ruumi, kus toimub küttesegu põlemine ja soojusenergia muundamine mehaaniliseks tööks. Kolb - Kolb on silindris tihedalt liikuv vahesein. Mootori töötamisel sooritab kolb silindris sirgjooneliselt edasi- tagasi liikumist. Keps - kujutab endast kangi mis seob kolvi edasi tagasi liikumise väntvõlli pöörlevaks liikumiseks ja vastupidi, olenevalt sellest, mis sugune neist on liikumise allikas. Väntvõll - koosneb poolitatud võllist, mis on üheks tervikuks liidetud neid ühendava vända kaudu.
elektriseeruvuse kuivas õhus. Mõõdupüsivus on parem, kui viskoosil. Saab kedrata väga peeneid kiude, mis tunduvad pehmetena ja on siidja mati läikega. Viskoosist kergem, kuulub keskmise raskusega kiudude hulka. Põleb ühtlaselt ja lõhnab äädika järgi. Talub viskoosist paremini päikesevalgust ning see ei aldistu hallituse ja kahjuriputukate poolt tekitavatele kahjustustele. Põleb kiiresti suure leegiga, leegist eemaldamisel põlemine jätkub, üüdikhappe lõhn. Antimikroobne atsetaatkiud tuli müügile 1994. aastal, seda kiudu kasutatakse rõivaste ja kodutekstiili materjalina, aga samuti haiglatekstiilides. Modaal(MD) Modaalkiu ristlõikepind on ümaravõitu ja kiupind on sile. Modaal on suure tõmbetugevusega ja kõrge märgmooduliga hüdraattsellulooskiud. Tema märgtugevus on viskoosist oluliselt suurem. Koostiselt on puhas tselluloos. Modaal on kiud, millest on kõrvaldatud viskoosi puudused
Põlemine võib mõnikord toimuda ilma leegita, seda nimetatakse hõõgumiseks. Hõõgumisel eraldub samuti soojust, valgust ning põlemissaadusi, mille hulgas on ka süsihappegaas ja vesi. Kui süsi, turvasd või riie hõõgub, siis ta tegelikult põleb. Üks põlemise eriliikidest on plahvatus. Ülikiire põlemisprotsessi korral, nt gaasisegus ei jõua eralduv soojus hajuda ning põlemiskohas tõuseb temperatuur järsult väga kõrgele. Plahvatuse purustavat toimet põhjustavad tekkiv kõrge rõhk ning sellega kaasnev lööklaine.
tekib olukord kus järjest rohkem päikesekiirgust peegeldub maale tagasi ning seega tõuseb ka temperatuur. Selle tulemusena hakkab sulama jää poolustel ja veetase tõuseb, samuti mõjuvad klimaatilised muutused elusloodusele. Kasvuhoone efekt oli ka peamine põhjus Kyoto Lepingu allakirjutamisel. Osooniaugud Teadlastele on alati olnud mureks, kuidas peatada osooniaugu suurenemist. Osooniauk asub Antarktise kohal. Osooniauke tekitavad freoonid ja nafta, kivisöe ja maagaasi põlemine. Osooniaugu laienemist soodustab ka vihmametsade põlemine. Kui osooniaugu laienemine jätkub sama hooga, siis 2030. aastaks on kliima soojenenud 5 kraadi võrra ja veetase on 166 cm võrra kõrgem. Kui ultraviolettkiired pääsevad läbi osooniaugu, siis taimede kasv aeglustub ja see tähendab hapniku vähenemist, mille järel tuhanded inimesed võivad surra hapnikupuudusesse.
Seetõttu suureneb ka keha siseenergia.Kui soojusvahetuse käigus keha annab ära mingi soojushulga,siis tema siseen.väheneb.Töö gaasi paisumisel: Gaasidega võrreldes paisuvad vadelikud ja tahked ained suhteliselt vähe.Paisudes avaldavad nad küll väga suurt rõhku,mis võib aga masina konstruktsioonile isegi ohtlikuks osutuda.Pealegi on soojushulga kiire üleandmine vedelikule või tahkele ainele raskendatud.Kui gaasis saavutatakse see erinevate gaaside reageerimise teel(bensiiniaurude põlemine õhu juuresolekul),sis vedelike ja tahkete ainete korral pole võimalik sarnast protsessi rakendada.Nii jääbki praktikas ainsaks võimaluseks kasutada töötava kehana mingit gaasikogust. A=P V Teoreeetiliselt on võimalik kõige suurem soojushulk saada,kui kasutada isotermilist paisumist.Sel teel saaksime kogu soojushulga tööks muuta.Kahjuks pole praktikas võimalik.Q=A(kogu juurdeantav soojushulk läheb paisumistööks). Miks kasutatakse gaasi: Gaasidega
n-alkaanide (C16 C40) segu. 2.Keemilised omadused. Alkaanid on tavatingimustel madala reageerimisvõimega, kuna nende molekulides paiknevad üksiksidemed on tugevad ja püsivad. · Reaktsioonivõime tõtstmiseks tuleb kasutada katalüsaatorit või kuumutada. · Alkaanid ei reageeri toatemperatuuril isegi konsentreeritud hapetega ja leelistega. a) Täielik põlemine ehk kiire oksüdatsioon CH4 + 2O2 CO2 + 2H20 b) Mittetäielik põlemine ehk aeglane oksüdatsioon C5H12 + 5O2 2CO2 + 6H2O + C (tahm) c) Oksüdeerumine alkoholis 2C2H6 + O2 2C2H5OH d) Pürolüüs (krakkimine) Aine lagundamine kõrge temperatuuri või katalüsaatorite toimel, mille
Füsioloogilised omadused: *Kuigi alkaanide reaktsioonivõime on tagasihoidlik, tuleb meeles pidada, et alkaanide aurud ja gaasilised alkaanid avaldavad inimesele ja loomadele tugevat narkootilist toimet.Nad kahjustavad kesknärvisüsteemi ning suurte koguste sissehingamine võib olla surmav. *Nahale võivad alkaanid toimida ärritavalt. Tahked alkaanid aga organismi ei tungi ja on seepärast ohutud (nt parafiin, mis leiab rakendust ka meditsiinis). Keemilised omadused: . 1. Põlemine. Kõik alkaanid põlevad. Madalamad alkaanid põlevad vähemärgatava, kahvatu leegiga ja põlemissaadusteks on süsinikdioksiid ning veeaur : CH 4 + 2O2 CO2 + 2H2O - õhuga segatuna moodustavad nad äärmiselt plahvatava segu. 2. Oksüdeerijate toime. Tavalisel temperatuuril nad oksüdeerijate KMnO 4, K2Cr2O7 toimel ei reageeri. 3. Termiline püsivus.Kõrgel temperatuuril alkaanid lagunevad. Millised reaktsioonisaadused tekivad oleneb t-st, reaktsiooni ajast ja katalüsaatoritest. 4
21 79 100 ( 16.4 2.5) 1 4.179 Katse nr 2 arvutus 21 2 18 21 79 100 ( 18 3) 2 7 6 5 TULEMUSED JA JÄRELDUSED Esimese katse liigõhutegur: α1=4,179 Teise katse liigõhtutegur: α2=7 Mida suurem on maagaasi kogus, seda ebatäiuslikum on põlemine ning tekib rohkem CO. Liigõhutegur näitab kui palju hapnikku oli liiast. Mida suurem liigõhu tegur, seda väiksemad on CO2 ja CO ppm näidud. Põlemine tuleks reguleerida selle järgi, et liigõhu tegur oleks võimalikult väike, samas ei tohi CO liiga kõrge olla. Esimeses katses oli maagaasikulu suurem kui teises. 7 LISA 1 – KATSEANDMETE TABEL
tetraeedriline süsinik nelja üksiksidemega süsinik 9. parafiinid tahked alkaanid või nende segud hüdrofoobsed ained ained, millel puudub veega vastastikmõju, puudub võime moodustada vesiniksidemeid, veega ei märgu ja vees ei lahustu hüdrofiilsed ained ehk vee-lembelised on ained, millel esineb vastastikmõju veega, esineb võime moodustada vesiniksidemeid, nad on vees märguvad ja lahustuvad. 10. Täielik põlemine toimub piisava hapnikukoguse (õhu) olemasolul. Selle käigus tekivad alati süsinikdioksiid ja veeaur mittetäielik põlemine põlevad need ained, milles on süsinikusisaldus vesinikusisaldusega võrreldes suhteliselt suur. Võivad moodustuda süsinikdioksiidi ja veeauru kõrval veel mitmeid orgaanilisi ühendeid, süsinikoksiid ja süsi. Pürolüüs orgaaniliste ainete lagunemine kõrgel temperatuuril, mida
Hiiuna kaotab ta intensiivse tähetuulega umbes 30% oma massist. Pärast heeliumi ammendumist tuumas jätkuvad termotuumareaktsioonid tuuma ümbritsevas kihis. Kõrge temperatuuriga tuum koosneb selleks ajaks peamiselt hapnikust ja süsinikust. Seejärel jätkub tähe evolutsioon sarnaselt punase hiiu evolutsioonile, ent kõrgema pinnatemperatuuriga. ( Dspace.utlib.ee, 2012) Tuuma surutakse kokku, kuni temperatuur on piisav, et algaks süsiniku põlemine. See protsess jätkub, järgmistes faasides neooni, hapniku, räni põlemisega. Tähe elu lõpufaasis toimub tähes sibulasarnase kihistumisega kihtpõlemine. Igas kihis toimub erinev termotuumaprotsess, välimises vesiniku põlemine, järgmises heeliumi põlemine. Viimasesse faasi on täht jõudnud siis, kui sünteesiprotsessid jõuavad raua tootmiseni. Tähe läbimõõt väga suur ja täht muutub ebastabiilseks, sest ta ei jõua oma välimisi kihte enam hoida.Äkitselt paiskab täht oma
tetraeedriline süsinik nelja üksiksidemega süsinik 9. parafiinid tahked alkaanid või nende segud hüdrofoobsed ained ained, millel puudub veega vastastikmõju, puudub võime moodustada vesiniksidemeid, veega ei märgu ja vees ei lahustu hüdrofiilsed ained ehk vee-lembelised on ained, millel esineb vastastikmõju veega, esineb võime moodustada vesiniksidemeid, nad on vees märguvad ja lahustuvad. 10. Täielik põlemine toimub piisava hapnikukoguse (õhu) olemasolul. Selle käigus tekivad alati süsinikdioksiid ja veeaur mittetäielik põlemine põlevad need ained, milles on süsinikusisaldus vesinikusisaldusega võrreldes suhteliselt suur. Võivad moodustuda süsinikdioksiidi ja veeauru kõrval veel mitmeid orgaanilisi ühendeid, süsinikoksiid ja süsi. Pürolüüs orgaaniliste ainete lagunemine kõrgel temperatuuril, mida rakendatakse nafta,
N +7 | 2) 5) H +1 | 1)
Ehitus
2p 1s
2s
polaarne kovalentne side
1) värvuseta
Füüsikalised 2) iseloomuliku terava lõhnaga (nuuskpiiritus)
omadused
3) mürgine
4) õhust kergem (M=17g/mol)
5) lahustub hästi vees, moodustades ammoniaakhüdraadi
NH3 + H2O NH4 + OH
1) põlemine (võib ka süttida)
Keemilised 4NH3 + 3O2 6H2O + 2N2
omadused
2) katalüütiline oksüdeerumine (Plaatinaga)
4NH3 + 5O2 6H2O + 4NO
3) reageerimine hapetega
2NH3 + H2SO (NH4)2SO4
NH3 + HCl NH4Cl
1) N2 + 3H2 2NH3
Saamine eksotermiline reaktsioon (H
Oksüdatsioon on keemiline protsess, mille käigus aine loovutab elektrone ehk oksüdeerub. Oksüdeerumine toimub redoksreaktsioonis ning aine, mille korral toimub oksüdeerumine, on redutseerija. Oksüdeerumise vastandprotsess on redutseerumine ehk reduktsioon. Tüüpiline oksüdatsiooniprotsess on põlemine, mille käigus põlev aine oksüdeerub. Keemiline aine on aine, mille molekulidel on ühesugune koostis ja struktuur. Redoksreaktsioon on keemiline reaktsioon, mille käigus aatom liidab või loovutab elektrone. Elektronide liikumise tõttu muutub ka aatomi oksüdatsiooniaste. Reduktsioon ehk redutseerumine on redoksreaktsiooni käigus oksüdeerijaga toimuv protsess, mis seisneb selles, et ta liidab endaga elektrone Redutseerija on keemias element, mis redoksreaktsiooni käigus
tasakaalus. Inimese mõju süsinikuringele Inimesel on väga suur ökoloogiline jalajälg Bensiini, Diisli põletamisel tuuakse süsinikuringesse süsinikku juurde. Taimestunud alade vähendamise kaudu vähendatakse süsiniku fotosünteetilise protsesside voogu. Kuivendamise ja muldade õhustamise kaudu suurentatakse orgaanilise aine mineraliseerumist ja süsihappegaasi eraldumist õhkkonda. Süsiniku põlemine Süsinik põleb ilma lõhnata Süsinik on mürgine Süsisnik on värvitu Süsinik on maitsetu Süsinik on igal pool meie ümber Aitäh kuulamast !
on hegnoskoopne, mida rohkem OH rühmi või mida lühem ahel, seda paremini lahustub vees.. Ühe ja kahe hüdroksüülrühmaga alkoholid on suuremal või väiksemal määral mürgised, mõned on narkootilise toimega. (http://www.miksike.ee/documents/main/referaadid/susivesinikud_maarjakager.htm; puudub konkreetne autor (G. Naan - peatoimetaja), ENE 2, Tallinn, kirjastus "Valgus") 3.2 Keemilised omdused Etanooli keemilised omadused on põlemine (täielik põlemine), reageerimine leelismetallidega, dehüdraatimine, oksüdeerumine aldehüüdiks ja karboksüülhappeks, redutseerumine alkaaniks, reageerimine karboksüülhapetega (tekib ester ja vesi), reageerib aldehüüdidega (tekivad poolatsetaalid ja alkoholi liia korral poolatsetaalist atsetaalid), reageerib vesinikhalogeniididega. 1) Põlemine (täielik põlemine): C2H5OH + 3O2 = 2CO2 + 3H2O 2) reaktsioon leelismetallidega: 2C2H5OH + 2Nagm = 2C2H5ONa + H2
20) Njuutoni 3 seadus. Newtoni esimene seadus ehk inertsiseadus väidab, et keha liigub ühtlaselt sirgjooneliselt või seisab paigal, kui talle mõjuvate jõudude resultant võrdub nulliga. Newtoni teine seadus väidab, et kehale mõjuv resultantjõud on võrdne keha massi ja kiirenduse korrutisega. Newtoni kolmas seadus väidab, et kaks keha mõjutavad teineteist jõududega, mis on suuruselt võrdsed ja suunalt vastupidised. 21) Põlemine kui protsess. C+O2=CO2 Põlemine on ainete ühinemine hapnikuga. Põlemise tulemusena tekivad uued ained. Põlemisel eraldub soojust.
1 kg vee kondenseerumisel eraldub 2 300 000 J soojust/energiat. 10 Kütuste energia Mida sa tead aine ehitus? Molekulid koosnevad aatomitest. Iga molekuli võime jagada aatomiteks. Molekulide jagamisel aatomiteks tuleb ületada aatomite vastastikused tõmbejõud, st tuleb teha tööd, kulutada energiat. Aatomite ühinemisel molekulideks aga vabaneb energiat. Põlemine on kiirelt toimuv oksüdatsioon. 11 Kütuste energia Kütuste kasutamine põhineb asjaolul, et aatomite/ ioonide ühinemisel molekulideks vabaneb energiat. Tavaline kütus sisaldab süsinikku. Põlemisel ühinevad süsiniku aatomid hapniku aatomitega. Ühinemisel tekib süsihappegaasi molekul, kusjuures vabaneb soojust/energiat. Mida madalam on süsiniku oksüdatsiooniaste, seda rohkem energiat põlemisel vabaneb. Kütust on mitut liiki:
1 ANORGAANILISTE AINETE PÕHIKLASSID Keemilised ained jaotatakse: lihtained (koosnevad ühe elemendi aatomitest) -metallid näiteks: vask - Cu, alumiinium - Al -mittemetallid näiteks: hapnik - O2, grafiit - C liitained (koosnevad mitme elemendi aatomitest) Olulisemad anorgaaniliste liitainete klassid on: -oksiidid näiteks: CO2, CaO, H2O -happed näiteks: HCl, H2SO4 -alused näiteks: NaOH, Ca(OH)2 -soolad näiteks: NaCl, K2SO4 OKSIIDID Oksiidid on liitained, mis koosnevad kahest elemendist, millest üks on hapnik (O). Oksiidid võivad tekkida: 1. Liht- või liitainete reageerimisel hapnikuga (oksüdeerumisel). Kiiret oksüdeerumist nimetatakse põlemiseks. C + O2 CO2 (põlemine) S + O2 SO2 (põlemine) 4Fe + 3O2 2Fe2O3 (aeglane oksüdeerumine, roostetamine) 2. Hapnikku sisaldavate ainete lagunemisel. CaCO3 CaO + CO2 (...
1 kg vee aurustumiseks on vaja 2 300 000 J soojust/energiat. 1 kg vee kondenseerumisel eraldub 2 300 000 J soojust/energiat. 10 Kütuste energia Mida sa tead aine ehitus? Molekulid koosnevad aatomitest. Iga molekuli võime jagada aatomiteks. Molekulide jagamisel aatomiteks tuleb ületada aatomite vastastikused tõmbejõud, st tuleb teha tööd, kulutada energiat. Aatomite ühinemisel molekulideks aga vabaneb energiat. Põlemine on kiirelt toimuv oksüdatsioon. 11 Kütuste energia Kütuste kasutamine põhineb asjaolul, et aatomite/ ioonide ühinemisel molekulideks vabaneb energiat. Tavaline kütus sisaldab süsinikku. Põlemisel ühinevad süsiniku aatomid hapniku aatomitega. Ühinemisel tekib süsihappegaasi molekul, kusjuures vabaneb soojust/energiat. Mida madalam on süsiniku oksüdatsiooniaste, seda rohkem energiat põlemisel vabaneb. Kütust on mitut liiki:
Gustavus II Avastused Leiutas esimese õhu pumba Uuris vaakumit 1663 leiutas ta kui nähtust esimese elektri Uuris õhu rolli generaatori põlemises ja Mis tootis hingamises staatilist elektrit, pöörleva väävli palli hõõrdumisel Avastused 1673 avastas, et väävli palli hõõrdumisel see hakkab hõõguma Ta avastas, et gaasi Õppis keskkonnas astronoomiat põlemine Ennustas, et tekkitab komeedi sadu suuremat valgust pole juhuslik. ja on säästlikum. (Säästulamp) Tänan kuulamast