Potentsiaalseid lasteaialapsi 88 88 88 88 88 88 88 Turuosa % 10% 15% 15% 20% 20% 20% 20% Potentsiaalseid pöördujaid perioodis 8,8 13,1 13,1 17,5 17,5 17,5 17,5 Keskmine laekumine kliendilt ** 372 372 372 372 372 372 372 Laekumine perioodis 3 255 4 883 4 883 6 510 6 510 6 510 6 510 KOV tegevustoetuse määr *** 400 400 400 400 400 400 400 KOV tegevustoetus perioodis 10 500 15 750 15 750 21 000 21 000 21 000 21 000 * Regioon on ……………. ..linnaosa ** 124 € kuus *** 400 € kuus lapse kohta Allikas: autori koostatud
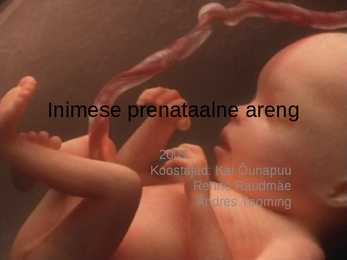
Inimese prenataalne areng 2009 Koostajad: Kai Õunapuu Renno Raudmäe Andres Tooming Sissejuhatuseks · Prenataalne areng on lapse arenguperiood,mis on vanuses 0-9.kuud Prenataalset arengut saab vaadelda kolmes perioodis · Eostumisperiood · Embrüonaalperiood · Looteperiood Eostomisperiood · Kestab 2 nädalat alates viljastumise hetkest Embrüonaalperiood · Kestab 3. nädalast kuni 8. nädala lõpuni · hakkavad kujunema süda, kehaosad (jalad, käed, silmad, kõrvad) Looteperiood · Kestab 9.nädalast kuni sünnini · Lühidalt on 9.nädalat pärast munaraku 12.Nädalane viljastumist loode embrüol olemas kõik organid ja
a) Vees lahustuvad Ei lahustu b) Orgaanilistes ühendites Enamasti ei lahustu Enamasti lahustuvad (bensiin, alkohol) süttivus Ei sütti Süttivad Elektrijuhtivus Juhivad Ei juhi Anorgaaniliste ja orgaaniliste ainete võrdlus 2.) süsiniku aatomi ehitus ja valentsmudelid süsinik paineb 1. Perioodis ja 4A rühmas 6 p+= 6 anorgaanilistes ainetes on süsinik posiiivne, no= 12-6=6 orgaanilises negatiivne. 12 e-= 6 süsiniku valents ALATI 4 süsiniku võrdlus Anorgaanillistes ühendites Orgaanilistes ühendites Oksüdatsiooniaste +2 kuni +4 Valents alati -4
Lämmastik on keemiline element järjenumbriga 7. 14prootonit ja elektroni, ja 7 neutronit. Väliskihis 5 elektroni.Asub teises A rühmas teises perioodis.( ruutskeem : 1s2 2s2 5p3) Lämmastik on mittemetall. Tavatingimustes on lämmastik värvitu ja lõhnatu gaas.Kõrgema rõhu all mõjub lämmastik iseenesest narkootiliselt, seda ka piisava hulga hapniku juuresolekul.Ühendites on lämmastiku oksüdatsiooniaste 3 KUNI +5. Lämmastiku oksiidid: NO-värvuseta mürgine gaas, vees praktiliselt ei lahustu, veega ei reageeri.N20-(nitro)- nõrga meeldiva lõhnaga värvuseta gaas, mis väiksemates kogustes sissehingamisel põhjustab elevust
Jood Jood on keemiline element järjenumbriga 53. Tal on üks stabiilne isotoop massiarvuga 127. Jood on halogeen. Ta moodustab kaheaatomilisi lihtaine molekule. Asub VII A rühmas, 5. perioodis Lihtainena väga mürgine Normaaltingimustes esineb jood tumepruunide kristallidena, mis sulavad temperatuuril 113°C ja keevad temperatuuril 184°C, moodustades lillaka auru. Jood on keemiliselt aktiivne, kuigi teistest halogeenidest vähem aktiivne. Elusorganismidele mõjub enamasti kahjulikult. Joodi tähtsus organismis Jood on kilpnäärme hormooni kohustuslik koostisosa. Joodi vähesus organismis põhjustab erinevaid haigusi. Joodi puudus võib kaasa tuua raseduse katkemise, lastel
RAUD VIII B rühmas ja 4. perioodis 26 prootonit ja elektroni ning 30 neutronit Fe : +26/2)8)14)2) Tihedusega 7,87 g/cm3 Sulamistemperatuur on 1539 °C Toodangult esikohal Kõige kättesaadavam metall Leidumine Üks levinumaid metalle Maal Sisalduselt maakoores neljandal kohal Rauarikkad planeedid on Merkuur ja Marss Meteotiidid, magmakivimid Savides, liivades ja kivimites Vere koostises Must rauamaak Magnetiit ehk magnetrauamaak Fe3O4 Raudmusta värvi Tugeva magnetilise omadusega Kõige puhtam ja rauarikkam rauamaak Kasutusel magnetravis Eestis leidub Jõhvi lähedal Korrosioon Raua puuduseks on intensiivne roostetamine Korrosioon ehk metalli hävimine ümbritseva keskkona toimel Eemaldada saab fosforhappega Ennetada saab pinda värviga või tsingiga kattes -kaetakse korrosioonikindlama metalliga Isoleeritakse ümbritsev...
1.Tähtsamad perioodilised seosed aatomite omadustes. Selgitage, kuidas muutuvad aatomiraadius, ionisatsioonienergia, elektronafiinsus, elektronegatiivsus ja polariseeritavus perioodilisustabelis. · Aatomiraadiused vähenevad perioodis vasakult paremale ja rühmas kasvavad ülalt alla. · Esimesed ionisatsioonienergiad I1 kasvavad perioodis vasakult paremale ja rühmas vähenevad ülalt alla. · Elektronafiinsused Ea on suurimad tabeli paremas ülanurgas (fluor, hapnik). · Aatomite elektronegatiivsused kasvavad perioodis vasakult paremale ja rühmas vähenevad ülalt alla. · Aatomite polariseeritavused vähenevad perioodis vasakult paremale ja rühmas kasvavad ülalt alla. Anioonid on polariseeritavamad kui vastavad aatomid tänu oma suuremale raadiusele.
Kui periood algab kohe peale koma, on see puhtperioodiline murd, nt. = 0,(2) 9 5 Kui periood ei alga kohe peale koma, on see segaperioodiline murd, nt. = 12 0,41(6) Perioodilise kümnendmurru saab teisendada harilikuks murruks. Puhtperioodilise murru korral paneme perioodis oleva arvu lugejasse ning nimetajasse paneme nii mitu üheksat kui mitu arvu on perioodis. Üks kõik millise murru korral paneme koma taga oleva arvu lugejasse ja lahutame sellest mitteperioodis oleva arvu. Nimetajasse paneme üheksa ja nii mitu nulli kui on mitteperioodis olevaid numbreid, -1 null. Ratsionaalarvude hulk Q Täisarvude hulga ja murdarvude hulga ühend on ratsionaalarvude hulk (v.a. mitteperioodilised lõpmatud kümnendmurrud).
kunstinikud huvitatud liikumise kujutamisest. Tihti kujutati üht ja sama objekti üheaegselt erinevatel ajahetkedel. Heaks näiteks on Giacomo Balla ''Koera ja keti dünaamika''. Teise moodusena lõhuti nähtav maailm geomeetrilisteks kildudeks,millest loodi lõikuvate pindade ja joontega dünaamiline kompsitsioon. Pilt pidi mõjuma rahutu ja liikuvana. Sageli kasutati erksaid värve ja teravaid värvi kontraste. Näiteks vasakul on Gino Severini ''Sea=Dancer''. Hilisemas perioodis kujutasid futuristlikud kunstnikud kõike nö lenduri vaatepunktis ehk aeropiltidena. Näiteks Gino severini ''Soomusrong lahingus''. Veel tuntuid teoseid Üleval: Luigi Russolo ''Automobile at speed''. Paremal: Giacomo Balla ''Lamp ja kuu'' Kasutasin : http://et.wikipedia.org/wiki/Futurism http://www.paideyg.ee/kunstiajalugu/kunstilugu/mode http://hatfuturismo.blogspot.com/2008/05/principais-p
Vask Vask (cuprum) on keemiline element järjenumbriga 29. Vase aatommass on 63,54. Ta asub IB rühmas ning 4. perioodis. Vase elektronskeem on: 2) 8) 18) 1). Sulamistemperatuur on tal 1083 Celsiuse kraadi.Vase värvus ulatub punasest kuldkollaseni. Juhib hästi elektrit ja soojust. Kuivas õhus on vask püsiv, niiskes õhus tekib aga vase peale ajapikku pruunikas paatina kiht. Vask ise on plastiline metall, mida hakati kasutama umbes 10000 aastat tagasi. Vask oli üks esimesi inimkonna poolt kasutatavaid metalle, kerge saadavuse ja madala sulamistemperatuuri tõttu
Arrheniuse võrrand k = A · e-EA/RT ; (k kiiruskonstant, R universaalne gaasikonstant 8,314 kJ/k·mol, A nn sagedusfaktor, mis iseloom molekulide kokkupõrgete sagedust, EA aktivatsioonienergia kJ/mol).Aktivatsioonienergiat on võimalik vähendada ensüümide ja katalüsaatoritega, kokku puute pinna suurendamisega .ionisatsioonienergia energia, mis kulub kõige nõrgemini seotud elektroni eemaldamiseks aatomist või ioonist.. Kasvab perioodis vasakult paremale ja rühmas alt üles.Elektronafiinsus energia, mis kulub või eraldub, kui aatom (ioon) liidab enesega elektroni. Kasvab perioods vasakult paremale ja rühmas alt üles.Galvaanielement seadis, milles rediksreaktsioonide tulemusena vabaneva energia arvel tekib elektrivool keemiline energia muundub elektrienergiaks.
Magneesium Sisukord · Mis on magneesium · Kus seda leidub · Milleks on see vajalik · Magneesiumi puudus · Magneesium ja inimene · Tänan kuulamast Mis on magneesium · Magneesium on keemiline element järjenumbriga 12. · Magneesium asub kolmandas perioodis. Kus seda leidub · Magneesium on litofiilne element, mis kontsentreerub Maa vahevöösse ja maakoorde. · Maal ei leidu teda looduses vabalt, vaid ainult ühendite koosseisus oksüdeerituna. · Magneesium kuulub ligikaudu 200 mineraali koostisesse. Milleks on see vajalik · Magneesiumi leidub kõigis organismides. · Taimede klorofülli koostises oleva magneesiumi üldhulka hinnatakse 100 miljardile tonnile. Klorofüll sisaldab ligikaudu 2% magneesiumi.
Argoon Helen Lajal Põhiline info Argoon on.. Kolm stabiilset isotoopi ➔ Väärisgaas Ar36, Ar38, Ar40 ➔ Järjenumbriga 18Aatommass on ~ ➔ VIIIA rühmas 402 1s 2s2 2p6 3s2 3p6 ➔ 3. perioodis Tähis on Ar. Põhiline info Sulamistemperat -189,4°C Prootonite uur ja -185,87°C elektrontie Keemistemperatu arv - 18 Kristallvõre ur on Neutronite kuubiline. arv - 22 Pilt on Wikipediast. Avastamine Henry Cavendish algselt kahtlustas argooni olemasolu õhus. (1785)
keskpunkti ühendav raadius. Ringjoonelise liikumine kiirused:*joonkiirus- ringliikumisel läbitud teepikkuse ja liikumisaja suhe.*nurkkiirus- pöördenurga ja liikumisaja suhe. Võnkumine- keha liikumine kordub teatud ajavahemikes * vabavõnkumine-toimub süsteemisiseste jõudude mõjul. *sundvõnkumine-toimub välise perioodilise jõu mõjul. Periood- aeg ühe võnke tegemiseks, ei sõltu massise ega amplituudist. Sõltub kiirendusest ja pendli pikkusest. Sagedus-võngete kiirus perioodis. Resonants- amplituudi järsk kasv. Laine- võnkumise levimine ruumis. Ristlaine-ainet edasi ei kanta, keskkond saab ainult häiritud, võnkumine toimub risti laine levimissuunaga. Pikilaine- võnkumine toimub piki laine levimissuunda. Lainepikkus- kahe lähima samas faasis võnkuva punkti vaheline kaugus. Periood- aeg, mille jooksul levin laine lainepikkuse kaugusele. Lainete interferents-lainete liitumine, liituda saavad ainult ühesuguse lainepikkusega lained. Lainete
rasva olema). Psüühika ja käitumise omapära (retseporitega avaldatakse teatud piirkonnale mõju). Sugunäärmete eemaldamine, mitte väljakujunemine vm ei võimalda sekundaarsetel tunnustel välja areneda. (Kastraatlauljad- Farinelli testised eemaldatud enne suguküpseks saamist; haaremi valvurid eunuhhid? arenevad naiselikud tunnused rasv ladestub rindade, puusade piirkonda, hääl peenikeseks, habe ei kasva.) Suguhormoonid mõjutavad tsüklit reproduktiivses perioodis. Naissuguhormoonidel mõjud suuremad Östrogeenide ja gestageenide toimed (FAILID ÕISIST!!!!!!!!!!! Östrogeenid ja gestageenid) Endomeetrium emaka limaskest, soodustavad kasvu, toimub östrogeenide mõju all. Müomeetrium lihaskest, östrogeenide stimuleeriv mõju
Se-seleen Rinaldo Must 11L Ehitus ja asetus PS-s ● Seleen on keemiline element järjenumbriga 34, mittemetall ● Asub 4. perioodis ja VIA rühmas ● Aatommass on 78,96 ● Aatomis on 34 prootonit, 34 elektroni ja 45 neutronit “Tuntuim fullereen C60” Michael Ströck, CC BY-SA 3.0 Füüsikalised omadused ● Pooljuhtiv tahke aine ● Tihedus 4,8 g/cm³ ● Keemistemperatuur: 685°C ● Sulamistemperatuur 170-217°C ● Vees ei lahustu Tähtsamad ühendid ja kasutusalad ● SeO2 ● SeO3 ● H2SeO3 ● Ag2Se3 ● Na2Se3 ● Se2Cl2 Elemendi tähtsus bioelemendina
vajavad funktsioneerimiseks kolesterooli naistel emakas, rinnanäärmetes, neerudes, südames raseduse ajal ka platsentas Mõju sünnitusele Laps surub emakakaelale signaal ajju oksütotsiini emakalihaste kokkutõmbed. Stimuleerib prostaglandiinide vallandumist vereringesse, mis tugevdavad emakalihaste kontraktsiooni. See protsees hoogustub sünnitustegevuse käigus, muutudes aina jõulisemaks ja lõpeb lapse sündimisega. Mõju sünnitusjärgses perioodis Piima eritamise refleks Sünnitusjärgne emaka kokkutõmbumine Piima eritamise refleks Kui oksütotsüün voolab rindade veresoontesse, sunnib see alveoole kokku tõmbuma, piim pigistatakse piimajuhade kaudu siinustesse ja edasi välja nibudesse. Võib olla valulik Aktiveerub, kui laps nutab Sünnijärgsed emaka kokkutõmbed emakas tõmbub kokku väheneb verejooks sarnane menstruaalvaluga valuvaigistamiseks võib kasutada Ibuprofeeni ja Paracetamooli
Lämmastik (N) Aatomi ehitus Lämmastik on keemiline element järjenumbriga 7. Lämmastik asub perioodilisussüsteemi V A rühmas ja 2. perioodis. Lihtaine omaduses Lämmastik on mittemetall, lõhnata, värvita, maitseta, õhust natuke kergem gaasiline aine, vees väga vähe lahustuv, aatommass on 14.01, ei ole mürgine, vedeldub temperatuuril -195. Kerge rõhu all avaldub lämmastikul narkootiline toime. Leidumine Lämmastikku esineb nii ehedalt kui ühendis. Ehedalt: 78% maa atmosfäärist on lämmastik. Ühenditena: valkudes, mineraalidena, tsiili salpeeter (NaNO3). Tähtsamad ühendid 1
Cl2+2Na=2NaCl (naatriumkloriid) S+2Na=Na2S (naatriumsulfiid) O2+2Zn=2ZnO (tsinkoksiid) MITTEMETALL+MITTEMETALL=KOVALENTSE SIDEMEGA ÜHEND 2H2+O2=2H2O H2+S=H2S (divesiniksulfiid) Si+O2=SiO2 (ränidioksiid) H2+Cl2=2HCl (vesinikkloriid) S+O2=SO2 (vääveldioksiid) Mittemetallid võivad olla nii oksüdeerujad kui ka redutseerijad, eelistatud oksüdeerijad. 5.2 VESINIK JA HAPNIK-TÄHTSAMAD MITTEMETALLE 5.2.1. Üldiseloomustus *Vesinik on perioodilisustabelis esimene element. Asub esimeses perioodis ja alakihis on üks elektron. Loovutab ühe elektroni ja tekib H+ Lihtainena on vesinik gaasiline, esineb H2-na. On levinud eelkõige ühendites. H: +1| 1) 1 element perioodilisussüsteemis, paikneb I ja/või VII rühmas Molekuli valem H2; H:H H-H *On 3 isotoopi: H-prootium D-deuteerium, raskevesinik T-triitium, üliraske vesinik(radioaktiivne) *Levimus: Kosmoses levinum element ( -75% päikese massist) Maal H2O-na , orgaaniliste ainete koostiselement.
kruusamäe.2010artikkel. 4) http://et.wikipedia.org/wiki/Kasutaja:Kruusam %C3%A4gi/Keemilised_elemendid Süsiniku toime.09.11.10 5) http://www.obs.ee/~jaak/loengud/teine/yksteist/kakskymmend1.html#sysinik Süsiniku kasutamine tööstuses ja majanduses.09.11.10 6) http://www.kl.ttu.ee/atrik/ope/kky3153/loeng101.pdf Süsiniku üldine iseloomustus Süsinik asub elementide perioodilisuse tabelis teises perioodis, seega on tema elektronkate kahekihiline. Süsiniku aatominumber on 6, ümardatud suhteline aatomimass 12. Sellele vastavalt on tuumas on 12 nukleoni A=N+Z, millest neutronite arv , N=A-Z, 12-6=6 ja prootonite arv on samuti 6. Kuuest elektronist kaks paiknevad esimesel elektronkihil ja 4 teisel .
Metallide tugevus kasvab ülevalt alla ja vasakult paremale.Aatomiraadius kasvab rühmas ülevalt alla,sest kihtide arv kasvab e.metalli tugevus kasvab,sest kergem ära anda elektrone tuumast kaugemal.Kui elektronkihtide arv jääb samaks,tuumalaeng kasvab perioodis vasakult paremale ja aatomi raadius väheneb.Mida väiksem raadius,seda tugevamad mittemetalli omadused(lihtne juurde võtta).Mida suurem raadius,seda tugevamad on metallilised omadused(elektrone ära anda).Metallilised-suhteliselt väike väliskihi elektronide arv;suhteliselt suur aatomiraadius;aatomid alati loovutavad elektrone(on redutseerijad- võtavad juurde).Mittemetallilised-suhteliselt suur väliskihi elektronide arv;suhteliselt väike
pole teada. Tõenäoliselt kasutas esmakordselt seda nime Paracelsus, Sveitsis sündinud sakslasest keemik, kes kasutas sõna ,,Zincum" 16. sajandil. See sõna tähendab saksa keeles ilmselt ,,hamba-sarnanast, teravaotsalist või sakilist osa", ja kuna tsingi metalli kristallid on okka-sarnased, siis näib selle päritolu üsna usaldustäratav. Ehitus ja asend perioodilisussüsteemis · Tsink sümbol: Zn · Asub 4 perioodis II B rühmas · keemiline element järjenumbriga 30, metall. · Tal on 4 stabiilset isotoopi massiarvudega 64, 66, 67 ja 68. Omadused, kasutamine ja tähtsus · Keskmise reageerimisvõimega · sinakashall metall · tuhmub niiske õhu käes ja põleb õhus ereda, sinakas-rohelise leegiga · tihedus 7,14 g/cm³. · sulamistemperatuur 419°C · keemistemperatuur on 907°C. · Tsinki kasutatakse terase galvaniseerimiseks, et korrosiooni ära hoida
Süsinik Asetus perioodilisussüsteemis Süsinik asub IVA rühmas Süsiniku aatomnumber on 6(aatomituumas on 6 prootonit) Elektrone on samuti kuus ning need asuvad kahel elektronkihil Süsinik asub teises perioodis Süsinik looduses Süsinikku leidub liht- ja liitainena Lihtainena esineb ta näiteks teemandi ja grafiidina Looduses esineb arvukalt süsinikuühendeid Õhus leidub süsinikku süsinikdioksiidina Kuulub organismide koostisse. Sealseid süsinikuühendeid nim. orgaanilisteks ühenditeks Süsinik lihtaine ja liitainena. Allotroopia Lihtainena esineb süsinik vaid teemandi ja grafiidina Teemant- särav ja hinnaline vääriskivi. Lihvituna nim. briljandiks.
3. Keemistemp. Üle 750 kraadi alla 750 kraadi 4. Lahustuvus a)vees hästi halvasti b)orgaanilistes ainetes halvasti hästi 5. Süttivus halvasti süttivad 6. Elektrijuhtivus enamasti juhivad enamasti ei juhi Süsiniku aatomi ehitus: Asub II perioodis. IV A rühmas. Prootonite arv 6. Neutronite arv 6. Elektronide arv 6. Elektronskeem: C:+6 l 2)4) Isomeeria mõiste: On nähtus kus ainetel on ühesugune elementkoostis ja molekulaarmass, kuid erinev struktuur ja selle tõttu erinevad omadused. Valents: Näitab mitu kovalentset sidet võib antud aatom moodustada. Anorgaanilistes ühendites on süsiniku o.a. Aste II; IV Orgaanilistes ühendites on süsiniku o.a. Aste alati IV
Mode of birth and women's psychological and physical wellbeing in the postnatal period Ingrid J Rowlands and Maggie Redshaw Aljona Ostapjuk Tallinn 2013 Tagaplaan Füüsilised ja vaimsed probleemid pärast sünnitamist on ühised paljudele naistele. Need probleemid võivad väga negatiivselt ja pikaajaliselt mõjutada naise igapäevast elu postnataalses perioodis. Sünnitamisviis võib olla väga tihedalt seotud taastumisega pärast sünnitamist. Meetodid Osavõtjad 10 000 küsimustikku 5 332 vastati (53%) Ankeeti küsimusi gruppeerimine psühholoogilised sümptomid posttraumaatilise stressi sümptomid keha muutused sünnitamisega seotud sümptomid imetamise probleemid äge väsimus Vastused 10., 60. ja 90. päeval pärast sünnitamist Statistiline analüüs Tulemused Kõige rohkem sümptomeid oli naistel 10
MÕISTED: Naturaalarv arve 0,1,2,.... nimetatakse naturaalarvudeks. Naturaalarvude hulga tähis on . Täisarv - arve ... -2; -1; 0; 1; 2... nimetatakse täisarvudeks. Täisarvude hulga tähis on Ratsionaalarv- on murdavaldis, mille lugeja ja nimetaja on täisarvud, kusjuures nimetaja ei ole 0. Ratsionaalarvude hulga tähis on . Irratsionaalarv on mitteperioodilised lõpmatud kümnendumurrud. Irratsionaalarvude hulga tähis on . Reaalarv lõpmatu kümnendmurd, mis ei lõpe 9-ga perioodis. Ratsionaalarvude hulga tähis on Ratsionaalarvude hulgas kehtivad järgmised tehete põhiomadused: Kommutatiivsus: a + b = b + a ab=ba Assotsiatiivsus: (a + b) + c = a + (b + c) a(bc)=(ab)c Korrutamise distributiivsus: a(b + c)= ab + ac Arvuhulka nimetatakse kinniseks mingi tehte suhtes, kui selle hulga iga kahe arvu korral kuulub samasse hulka ka vaadeldava tehte tulemus. Arvuhulka nimetatakse tihedaks, kui iga tema kahe erineva arvu vahel leidub veel sama hulga arve
Raud Raud (Ferrum) on keemiline element järjenumbriga 26. Raud asub perioodilisussüsteemi VIII B rühmas ja 4. perioodis. Raud avastati 3500 aastat ekr, egiptlaste poolt meteoriidi seest Rauaühenditel on tähtis roll elusorganismide eluprotsessides. Veres sisalduv hapnikku transportiv hemoglobiin näiteks sisaldab rauda ja raud on vajalik ka vereloomeks. Raud asub perioodilisusüteemis VIII rühma kõrvalalarühmas. Raua aatomi järjenumbrist on 26 ja täisarvuni ümardatud aatommassist 56 järeldub, et raua aatomi tuumas on 26 prootonit, ja 30 neutronit
pälvivaks elavhõbedaühendiks oli erkpunase värvusega mineraal kinaver (tõlkes draakoni veri) , mida tunti ja 2) 8) 18) 32) 12) 6) kasutati Vanas Kreekas ja Rooma riigis. Juba eelajaloolisel ajal joonistati sellega Elavhõbe asub II B perioodis, 6. rühmas. koopa ja hauakambrite seintele. Plinius Elavhõbe on metallidest ainus metall, mis nimetas elavhõbedat elavaks hõbedaks, toatemperatuuril on vedel. Elavhõbe on Aristoteles aga vedelaks hõbedaks. hõbevalget värvi. Elavhõbe on raskeim Alkeemikud tundsid elavhõbedat planeet vedelik, ületades vee tiheduse 13,6 Merkuuri järgi merkuuriumi nime all, sest kordselt
lihaste hüpoplaasia ja hüpotoonia ning teised defektid nagu näiteks lühikesed iseloomuliku asetusega sõrmed. Väga oluliseks tunnuseks on ka embrüonaalse arengu mahajäämus, mistõttu ajaliselt sündinud lastel on ebanormaalselt väike sünnikaal. Vastsündinud on nõrgad ja loiud, nende imemisrefleks on puudulik ja hääl nõrk. Vastsündinute füüsiline ja vaimne areng on peetunud ja elujõuetus süveneb kiiresti sünnijärgses perioodis. Levinumad sümptomid: Väike kasv Longus ülemised silmalaud Söötmis-/söömisraskused Kokku kasvanud/väändunud Hingamisraskused sõrmed Arengupeetus Väljaarenemata Vaimne väärareng pöidlad/sõrmeküüned Eraldumata munandid poisslastel Kodarluu puudumine Suurem muhk kuklal või peas 2.-3. varba kokkukasvamine
Nimed on tuletatud linna järgi. (2) Joseph Black Sotimaal avastas magneesiumi, kui eraldi elemendi 1755. Sir Humphry Davy isoleerise 1808.a elektrolüütilisel teel puhast magneesiumi metalli. Antoine Alexandre Brutus Bussy eraldas 1831 magneesiumi sidusal kujul. (4) 4 2. Aatomi ehitus 2.1 Asend perioodtabelis Magneesium asub keemiliste elementide periodilisustabelis kolmandas perioodis, IIA rühmas. IIA rühmas asuvad leelismuldmetallid. Ühes perioodis asuvatel ainetel on sarnased omadused. Lisaks Magneesiumile kuuluvad sinna berülleum, kaltsium, strontsium, baarium ja raadium. Magneesiumi järjekorra number on 12. (4) 2.2 Aatomi ehitus ja Elektronskeem Elektron skeem +12| 2) 8) 2) Paiknevus perioodilisuse tabelis: 3 periood, 2A rühm. Magneesium on keemiline element järjenumbriga 12. (2) Elektronvalem: 1s2 2s2p6 3s2 Elektrone: 12 Prootoneid: 12
metioniini ja tsüstiini ning B2-vitamiini ja insuliini koostisse. Keskmisest enam on väävlit juustes, karvades, küüntes, sarvedes ja sulgedes. Inimene sisaldab kokku ligikaudu 140 g väävlit. Väävlirikkamad toiduained on teravili, herned, oad ja kapsas. Gaasilised väävliühendid on inimesele sissehingamisel mürgised. N Lämmastiku järje- ehk aatomnumber on 7, ta kuulub perioodilisustabeli VA rühma elementide hulka, asudes 2. perioodis. Lämmastiku aatomis on 7 prootonit, 7 elektroni ja 7 neutronit. Lämmastiku aatomi väliskihis on viis elektroni ning lämmastiku aatomid võivad elektrone nii liita kui ka loovutada. Seetõttu on lämmastiku oksüdatsiooniaste ühendites 3 kuni +5. elektronskeem: N: +7| 2) 5) elektronvalem: 1s2 2s2p3 levik looduses Lämmastik on õhu peamine koostisosa , õhus on lämmastikku ligikaudu 78% ja 21 % hapnikku.
Perioodilisussüsteem s (leelis ja leelismuldmetallid), d (siirdeelemendid e üleminekumetallid), p (mittemetallid (väärisgaasid)) ja f (lantanoidid ja aktinoidid) elemendid; Aatomite raadiused kasvavad rühmas ülevalt alla, perioodis vähenevad vasakult paremale, diagonaalne sarnasus; Katioonide raadiused väiksemad kui vastaval aatomil ja anioonidel raadiused suuremad, kui vastaval aatomil. Aatomi või iooni ionisatsioonienergia energia, mis kulub kõige nõrgemini seotud elektroni eemaldamiseks aatomist või ioonist. Ionisatsioonienergiad vähenevad koos aatomi (iooni) raadiuse kasvuga. Kasvab perioodis vasakult paremale ja rühmas alt üles.
Raud Raud Raud e. Ferrum on keemiline element järjenumbriga 26. Raud asub perioodilisussüsteemi VIII B rühmas ja 4. perioodis. Tal on neli stabiilset isotoopi massiarvudega 54, 56, 57 ja 58. Omadustelt on raud metall Normaaltingimustel on raud tahke aine tihedusega 7,87 g/cm3 Sulamistemperatuur 1811 K (1538 °C) Hõbevalge metall Raua puuduseks on ta intensiivne roostetamine Füüsikalised ja keemilised omadused Raud on hõbevalge keskmise kõvadusega metall. Lisandid muudavad raua kõvemaks. Raua tihedus on 7874 kg/m3 ja sulamistemperatuur 1539 kraadi.
Keemia iseseisev töö VASK Vask e. cuprum; tähis Cu on keemiline element järjenumbriga 29. Vase tihedus 8,9 g/cm³. Vask asub IB rühmas ning 4. perioodis. Sulamistemperatuur on 1083 °C Vask on plastiline metall. Seda hakati kasutama umbes 10 000 aastat tagasi. Omadused Punakas-kollaka värvusega metall. Tihedus 8920 kg/m3. Hea elektri- ja soojusjuht. Sulamistemperatuur 1084.62 °C. Välistingimustes tekib vase pinnale aja jooksul rohekas kattekiht (paatina), mis kujutab endast erinevate vase hüdraatsoolade segu (sulfaat, karbonaadid).
com/061df3285410ee245e91679590feb5f0 $ Perioodilisusssteemi lhike variant. - https://gyazo.com/61ff73e2324c00c6935556df33f8b20b $ Perioodilisusssteemi poolpikk variant. -https://gyazo.com/408dcbe5cf61b3be91b2d20a83590f1d $ Elementide omaduste muutmine rhmas? -Rhmas (levalt allla) kasvab elektronkihtide arv aatomi ja aatomiraadius suureneb. Metallilised omadused tugevnevad ja mittemetallilised omadused nrgenevad. $ Elementide omaduste muutmine rhmas? $ Elementide omaduste muutmine perioodis? -Vasakult paremale elementide tuumalaeng kasvab, kuid elektronkihtide arv aatomites seejuures ei muutu.
JOOD JOOd · Sümbol: I · Perioodilisestabelis asub VIIA rühmas ja 5. perioodis · Halogeene mittemetall, moodustab kaheaatomilisi lihtaine molekule · Oksüdatsiooniast(m)e(d) ühendites: -I...VII · Üks stabiilne isotoop masssiarvuga 127 · Aatommass: 126,90447 aatommassiühikut Joodi aatomi ehitus · Tuumalaeng: 53 · Aatomis: 53 elektroni, 53 prootoni ja 74 neutroni · Elektronvalem: 1s22s22p63s23p64s23d104p65s24d105p5 · Elektronskeem: +53|2)8)18)18)7) Füüsikalised omadused ·
Hõbe Hõbe (Ag) paikneb perioodilisussüsteemis 1B rühmas, 5 perioodis. aatommass tuumalaeng järjenumber elektrone prootoneid neutroneid 108 amü +47 47 47 47 41 Hõbeda oksüdatsiooniaste on +2. Füüsikalised omadused: Hõbe on hõbvalge värvusega, plasitiline, kege ja hästi sepitstav väärismetall. Ta on parim soojus-ja elektrijuht. Hõbedat iseloomustab ka erakordne peegeldusvõime. Tihedus on 10,5 g/cm³ ning sulamistemperatuur 960°C. Keemilised omadused
Kaadmium Füüsikalised omadused Kaadmium (sümbol Cd) on hõbevalge, pehme metall, mis on plastiline ja hea kattevõimega. Kaamdium sulab temperatuuril 321 °C ja keeb temperatuuril 767 °C. Tema tihedus normaaltingimustel on 8,65 g/cm³. Normaaltingimustes on kaadmium tahkes olekus. Paiknemine tabelis Kaadmium (sümbol Cd) on keemiline element järjenumbriga 48. Tema aatommass on 112,41, asub 5.perioodis IIB-rühmas. Kaadmiumil on 5 elektronkihti ja viimasel kihil on 2 elektroni. Avastamine Friedrich Stromeyer avastas kaadmiumi 1817 aastal Saksamaal. Kaadmium on nime saanud vanakreeka mütoloogia tegelase Kadmose järgi, kes oli Liibanoni prints. Samuti öeldakse, et nimetus tuleb kreekakeelsest sõnast kadmeia- tsingimaak (koostiselt ZnO, milles esineb Cd-d) Leidumine Kaadmiumi leidub looduses üldiselt koos tsingiga, kuid on tsingist üle 50% haruldasem. Kaadmium võib leida maagis koos tsingi, plii ja vasega, s...
Alumiinium * Hõbevalge läikiv metall, mis kuulub kergmetallide hulka. * Tuntud oma kerge kaalu poolest. * Tihedus on 2,7 g/cm³ ja sulamistemperatuur 660 ºC , keema läheb see 2519 ºC juures. * Väga hea elektri- ja soojusjuht. * Alumiiniumi ümbersulatamisel selle omadused ei muutu, olenemata ümbersulatamise kordadest. Asukoht perioodilisussüsteemis * Asub perioodilisussüsteemis 3. perioodis ja IIIA rühmas (alumiiniumi aatomil on 3 elektronkihti ja viimasel kihil on 3 elektroni). * Järjekorra number on 13 * Aatommassi number on 26,981 Leidumine looduses * Erinevate mineraalidena moodustab alumiinium umbes 8% maakoorest ehk selle toormaterjali varud on peaaegu piiramatud. * Ainult hapnikku ja räni on maakoores rohkem,kui alumiiniumi * 100kg pinnases on keskmiselt 7kg alumiiniumi * Alumiiniumi ühendeid on ka meie toidus ja joogis.
Raud Aatomi ehitus Raud (Ferrum) on keemiline element järjenumbriga 26. Raud asub perioodilisussüsteemi VIII B rühmas ja 4. perioodis. Fe : +26/2)8)14)2) Lihtaine omadused ·Omadustelt on raud metall. ·Tihedus 7,87 g/cm3. ·Raua sulamistemperatuur on 1539°C. ·Raud on plastiline. ·Raud on hõbevalge. ·Raud on keskmise kõvadusega metall. Leidumine Raud on looduses laialt levinud element, olles sisalduselt maakoores neljandal kohal. Raud on ka kosmoses levinud element. Meie Päikesesüsteemi planeetidest on rauarikkamad Merkuur ja Marss. Tähtsamaid ühendeid
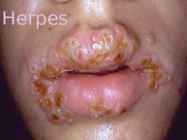
asuvate lümfisõlmede suurenemine. Ravi Huule ja suguelundite ohatist ravitakse viirusevastaste ravimitega - levinum on atsükloviir. Atsükloviiri on saadaval kreemina, tablettidena ja süstitava vormina. Sõltuvalt haiguse raskusest valitakse ravimvorm: huuleohatise puhul piisab tavaliselt kreemist, tablette kasutatakse väga tihti korduva ohatise ning nõrgestatud immuunsüsteemiga haigete puhul. Kuna herpesehaige on Ennetamine nakkav ka mittelööbivas perioodis, on oluline seksuaalvahekordade ajal kasutada kondoomi. Huuleohatise teket aitab vältida tableti ennetav manustamine esimeste haigusnähtude ilmnemisel - tavaliselt punetus ja kihelus Kasutatud kirjandus http://et.wikipedia.org/wiki/Herpes http://static.inimene.ee/index.php?disea se=g&sisu=disease&did=76 http://www.ohatis.ee http://www.derma.ee/articles.php?id=173 http://www.derma.ee/articles.php?id=66 http://whatisherpes.net/wp-content/uploads/
Näitab elektronide jaotust orbitaalidel 8) Mis on elektronvalem? Elektronvalem näitab elektronide jaotust kihtidel ja alakihtidel 9) Mis on elektronskeem? On aatomi elektronkatte ehitust väljendav skeem, mis näitab elektronide arvu elektronkihtides. 10) Osata kirjutada elemendi aatomi kohta elektronskeemi, ruutskeemi, elektronvalemit 11) Mis on a) periood b) rühm? a)horisontaane elementide rida b)vertikaalne elementide rida 12) Metallilisuse, elektronegatiivsuse muutumine perioodis ja rühmas. 13) Mis on a) s-element b) p-element? a) (IA ja IIA) rühma elemendid ja heelium, mille väliselektronkihi konfiguratsioon on s1 või s². b) (IIIA kuni VIIIA) rühma elemendid (välja arvatud heelium), mille väliselektronkihi konfiguratsioon on s²p1, s²p², s²p³, s²p4, s²p5 või s²p6. 14) Osata leida elemendi maksimaalset o-a, sellest tulenevalt kirjutada oksiidi valemit ja happe/aluse valemit. Maksimaalne o-a võrdub rühmanumbriga
prognoosid (kvartalite lõikes, vt lisa 3) ja bilansi prognoosid (kvartalite lõikes, vt lisa 4). 28 LISA 1 Laenugraafik Põhivara arvestus I - 2007 II - 2007 III - 2007 IV - 2007 I - 2008 II - 2008 III- 2008 IV- 2008 I- 2009 Soetusväärtus per. alguses 0 616 000 616 000 616 000 616 000 616 000 616 000 616 000 616 000 soetused perioodis 616 000 Võõrandamised perioodis Soetusväärtus per.lõpus 616 000 616 000 616 000 616 000 616 000 616 000 616 000 616 000 616 000 Kulumi määr perioodis % 5% 5% 5% 5% 5% 5% 5% 5% 5% Akumuleeritud kulum 15400 61 600 107 800 154 000 200 200 246 400 292 600 338 800 385 000
Õenduslugu ja õendusplaan õdede II kursusel kirurgilise haige õenduse õppepraktikal Sissejuhatus Oma kirurgia praktikat ma läbisin Kõrvakliinikus Kõrvakliiniku-kirugia osakonnas. Osakonnas oli minu juhendajaks Kaire Kärne ja koolipoolne juhendaja oli Helme Toss. Oma õendusloo patsiendiks ma valisin 34 aastase meesterahva. Valisin selle patsiendi, sest ta oli juba mõned päevad postoperatiivses perioodis ja pidi veel jääma mõneks ajaks haiglasse. Osakonnas, kus ma olin on väga raske valida sellist patsiendi, keda sul oleks võimalik jälgida pre ja postoperatiivses perioodis piisavalt aega, et sa saaks jälgida muutumisi tema tervislikus seisundis, kuna patsiendid pärast operatsiooni lähevad tavaliselt samal või järgmisel päeval juba koju. Samas ma olin praktikal kümme päeva ja ei saanud loota, et selle aja jooksul tuleb mingi patsient, kes jääb kauemaks ajaks haiglasse
alakiht rohkem. Igas alakihis on kindel arv orbitaale. Orbitaal ruumiosa, kus elektroni leidumise tõenäosus on väga suur. salakihis on 1 orbitaal, palakihis on 3 orbitaali, dalakihis on 5 orbitaali jne. Üks orbitaal mahutab kuni kaks elektroni ehk ühe elektronipaari. 2. Aatomi ehituse seos perioodilisustabeliga Aatomiraadius suureneb rühmas ülevalt alla, sest kasvab elektronkihtide arv. Aatomiraadius väheneb Arühmades perioodis vasakult paremale, sest suureneb tuumalaeng ja seega tuuma mõju elektronegatiivsuse ja mittemetallilisuse kasv elektronkattele. Keemilistes reaktsioonides on: metallidele omane elektrone loovutada, mittemetallidele elektrone pigem liita. 3. Elementide sümbolid Elementidele antakse ka kindel keemiline sümbol,
Metallid. Perioodis vasakul pool paiknevatel elementidel esinevad metallilised omadused, paremale poole liikudes muutuvad elemendid järjest vähem metallilisteks. Metallideside esineb metalliiooni ja poolvaba elektroni vahel. Metalle iseloomustab läige, hea elektri- ja soojusjuhtivus, plastilisus, metalliline side ja hea mehhaaniline töödeldavus.
Aatomi ehitus ja perioodilisussüsteem 1. Aatom on aineosake, mis koosneb aatomituumast ja elektronidest. Aatomi mudelid: 1) Dalton; 2) Thomson; 3)Rutherford; 4) Bohr; 5)kvantteooria. Aatomi koostisosad: tuum, elektronkate, prooton, neutron. 2. Keemiline element on teatud kindel aatomite liik. Selle massiarv A=p+n 3. Isotoobid on sama keemilise elemendi aatomid, mis erinevad üksteisest neutronite arvu poolest. 3 vesiniku isotoopi: 1) tavaline vesinik H; 2)raske vesinik H; 3) üliraske vesinik H. 4. Bohri järgi on elektronkatte ehitus kihiti. Elektronide arv elektronkihil 2n . 5. Tänapäeva mudeli järgi ei paikne kihiti vaid moodustub energiatasemete järgi elektronpilv- s.o. negatiivsete laengute pilv. Orbitaal on ruumi osa aatomis, kus elektroni leidumise tõenäosus on kõige suurem.s-kera, p-hantel 6. Elektronkihtides alakihid : I kiht 1s (saab olla 2 elektroni) II kiht 2s 2p ...
Alumiinium Paiknemine tabelis Alumiinium on keemiline element järjenumbriga 13, mis asub perioodilisussüsteemis 3. perioodis ja III A rühmas. Seega on alumiiniumi aatomil 3 elektronkihti ning viimasel elektronkihil asub 3 elektroni. Kõigis püsivamates ühendites on alumiiniumi oksüdatsiooniaste +3. Avastamine Alumiiniumi avastas väljapaistev Saksa keemik Friedrich Wöhler, kes tegi 15 aastat katseid peale seda kui ta 1827.aastal sai enda valdusesse metalli, mida mitte keegi ei olnud kunagi näinud. Leidumine/saamine Alumiiniumit lihtainena looduses ei esine, kuna ta on keemiliselt nii aktiivne. Maakoores on ta siiski üks levinumaid elemente. Alumiiniumi saadakse boksiidist ning alumiiniumi sulatus on üks kõige energiamahukamaid tootmisi. Kasutamine Ehedalt ja kergsulamitena kasutatakse seda ehitusmaterjalina, elektrijuhtmetena ning valgu...
Alguses Corot käis Lycée Pierre Corneille koolis. See on kool , mis asub linnas nimega Rouen Prantsusmaal. Ta lahkus sealt, kuna olid raskused ja läks edasi internaatkooli. Isa tahtis, et ta tegeleks äriga, aga Camille oli pühendanud ennast kunstile. Aastatel 1825-1828 viibis Corot Itaalias, kus ta sai veel väga palju informatsiooni maalikunsti kohta. 19.saj keskel oli Corot Barbidzoni kooli parim maalikunstnik. Oma töödes sai ta innovatsiooni impressionismist. Varasemas perioodis maalis ta traditsiooniliselt ja kitsalt. Maalis väga täpselt, selgete kontuuridega, pintsli töö oli üsna peenike. Hiljem tema meetodid muutusid : avardas kujundite varjundeid, andes piltidele sügavama sisu. 20.a. hiljem tema maalimismaneer hakkas väljenduma luules ja müsteeriumis, millega andis impressionistlikuma pildi. 1860ndatel hakkas Corot huvituma fotograafiast. Tehes pilte iseendast ja konsulteerides teiste kuulsate fotograafidega.
2) Neutron- Laeng 0, mass 1, tähis n , elektron- laeng -1, mass 0,0005, tähis e , prooton- laeng +1, mass 1, tähis b 3) Perioodi nr näitab elektrokihtide arvu, Rühma nr näitab väliskihi elektronide arvu, Aatomi nr näitab prootonite,elektronite, ja tuuma laengut 5) Peamised elemendid: Õhus- lämmastik,hapnik, Vees- hapnik,vesinik, Inimeses- hapnik,süsinik,vesinik, Maakoores- hapnik, alumiinium,räni , Universumis- vesinik, heelium 6) Kuidas muutuvad metallilised omadused rühmas ja perioodis ? Rühmas- ülevalt alla tugenevas, Perioodi: vasakult paremale nõrgenevad 7) Mitu rühma ja perioodi on tabelis ? 7 perioodi, 18 rühma 9) Elektroniskeemi koostamine aatomi kohta ? 10) Mis on isotoobid ? Isotoob on ühe ja sama keemlise elemendi aatomeid, mis erinevad neutronite arvu poolet tuumas. 11) Mis on elektronoktett ? 8 elektroniga väliskiht, mis esineb väärisgaasides 12) Mis on väärisgaasid, metallid ja mittemetallid ja kus kohas tabelis asuvad