Kasvuhooneefekt tekib, kui CO2 kontsentratsioon õhus pidevalt tõuseb (tööstus) ning taimed ei jõua seda ära tarbida. CO2 koguneb atmosfääri, kus takistab soojuse tagasikiirgumist maalt. Toimub kliima soojenemine ja liustike sulamine. Osoon (O3) on hapnik, mille molekul koosneb kolmest aatomist. Ta moodustab atmosfääris kaitsekihi UV-kiirte eest. Aerosoolide pidev kasutamine paiskab atmosfääri freoone, mis hävitavad ning lõhuvad osoonikihti. Tehase korstendest atmosfääri paiskuvad oksiidid SO2, SO3, NO2 moodustavad veeauruga ühinedes happe (SO2+H2O->H2SO3), mis sajavad vihmaveena alla (vihmavesi on happeline, PH väike). Happevihmad muudavad põllud happeliseks ja hävitavad loodust. Keskkonna saastumist on võimalik vähendada, kui juurutada kinnise tsükliga tootmist (selline tootmine võib olla peaaegu jäätmevaba), muuta tootmisjäägid ohutuks (põletada kütuseid, mis ei sisalda süsinikku) ning kasutada tuule- päikese-, hüdro- ning ka tuumaenergiat
Halogeenide saamine Halogeenide oksüdeerivad omadused nõrgenevad rühmas ülevalt alla . Iga aktiivsem halogeen võib vähem aktiivsema halogeeni ühendist välja tõrjuda. Kloor on oksüdeerija. Na + H2S04 Kloori kasutusalad Tekstiili-ja paberitööstuses kasutatakse seda pleegitajana, veepuhastusjaamades klooritakse joogivett, et hävitada pisikuid. Keemiatööstuses rakendatakse kloori orgaaniliste ühendite, vesinikkloriidhappe ja kloriidide tootmisel. Kloori oksiidid on happelised . Ta on normaalsetel tingimustel rohekaskollane gaas. Hüpokloorishape Kloori o.-a. on seal 1 . Väga nõrk hape, ebapüsiv, teda saadakse klooriveest, väga tugev oksüdeerija . Lagunemisel tekib vesinikkloriid ja atomaarne hapnik . ( HClO). Kasutatakse pleegitamiseks paberi-ja tekstiilitööstuses . Kloorlubi Saadakse kloori juhtimisel lubjavette. Tahke kloorlubi on valge või hallikasvalge aine, millel on iseloomulik terav kloorilõhn .Kasutatakse pleegitamiseks
Karboksüülhapped Screen clipping taken: 4.03.2011 9:06 Sisaldavad karboksüülrühma HCOOH -metaanhape(sipelghape) CH3COOH - etaanhape CH3CH3COOH - propaanhape · Neil on kõik hapetele iseloomulikud omadused o Hapu o Söövitav o Annavad lahusesse H+ ioone o Lakmus ->punaseks; MO->punaseks o Reageerivad leelistega, metallidega, endast nõrgemate sooladega · Keemilised omadused: o Reageerimine metallidega(mida aktiivsem metall, seda paremini reageerib) o Reageerimine metallioksiididega (aluselised oksiidid) o Reageerimine alustega o Nõrgemate hapete sooladega(karbonaadid, sulfaadid) o Vesinikuga -> aldehüüd + H2O (redutseerumine) Füüsikalised omadused · Molekulid moodustavad tugevaid vesiniksidemeid · Suhteliselt kõrge sulmas ja keemistemperatuuriga · Lühikese süsinikuahelaga (mida lühem ahel, seda paremi...
ALUMIINIUM Lisette Põld Mis on alumiinium? • Alumiinium on keemiline element järjenumbriga 13. • Tema keemiline lühend on Al. • Alumiinium on hõbevalge, pehme, plastne metall. • Alumiinium on kolmas kõige levinum element maakoores. • Alumiiniumi kõrge keemilise aktiivsuse tõttu ei leidu teda puhtal kujul. • Alumiinium on keemiliste elementide perioodilisussüsteemi III rühma element. • Järjenumber on 13. • Aatommass 26,98154. • Sulamistemperatuur on 660˚C. • Keemistemperatuur 2060˚C. Füüsikalised omadused • Alumiinium on suhteliselt pehme, vastupidav, kerge, plastne ja hästi sepistatav metall. • Värvus varieerub hõbedasest hallini. • Süttib raskelt. • Hea nähtava valguse ja infrapunakiirguse peegeldaja • Alumiinium on väga hea soojus- ja elektrijuht. Keemilised omadused • Alumiinium peab korrosioonile hästi vastu. • Korrosioonikaitse tõttu on alumiinium üks väheseid me...
LAHUSTUVUS https://m.youtube.com/watch?v=gcxU2uXeh0c Aine lahustuvus näitab, mitu grammi aineid saab lahustada 100 grammis vees. Paljudes lahustes on lahustiks vesi. On aineid, mis lahustuvad vees väga vähe, neid võib lugeda vees peaaegu lahustumatuteks. Sellised ained on näiteks: paljud soolad, hüdroksiidid, oksiidid ja suurem osa orgaanilisi aineid. Paljud ained lahustuvad vees hästi, näiteks: HCl, NaOH, H3PO4, sahharoos jne. Küllastumata lahus- lahus, milles antud tingimustel saab veel ainet lahustada. Küllastunud lahus- lahus, milles lahustatud aine sisaldus (antud tingimustel) on maksimaalne. Hästi lahustuvad ained- lahustuvus üle 1g/100g H²O. Vähe lahustavad ained- lahustuvus 0,1-1g/100g H²O Praktiliselt mitte lahustuvad- lahustuvus alla 0,1g/100g H²O
Keemia Perioodilisustabel ja aatom Lahter- Perioodi rühmad- eemiliste elementide perioodilisussüsteem on süsteem, mis jaotab keemilised elemendid nende tuumalaengute järgi rühmadesse ja perioodidesse. Järjekorra number: Keemilise elemendi aatomnumber ehk järjenumber ehk laenguarv on prootonite arv selle elemendi aatomi tuumas. A-rühma numbrist: Kui aktiivne metall on. Perioodi Number: Mitmendas perioodis asub element, Elemendid: 1.Raud : Fe, 2,Vask: Cu, 3,Jood: I, 4,Broom: Br , 5,Tina: Sn , 6,Plii:Pb 7,hõbe: Ag 8, Broom: Br 9, kuld : Au, 10,Elavhõbe : Hg, 11, tsink: Zn, 12,mangaan : Mn, 13 Kroom Cr 14, Baarium: Ba 15,magneesium : Mg 16,naatrium : Na 17,kaalium : K 18,koobalt : Co 19,titann: Ti 20,alumiinum : Al 21,nikkel : Ni 22, Gallium : Ga 23,Iriidium: Ir 24,Plaatina: pt 25,Rubiidium: Rb 26,plii: Pb 27, Indium : In 28,frantsium : Fr 29,Raadium : Ra 30,Vsimut : Bi 31,Tellur : Te 32, flueo : F ...
AINEKLASSID JA NENDE SAAMISVÕIMALUSED Klass Nimetus Saamine OKSIIDID K2O kaaliumoksiid 1.Oksüdeerumisel: CO2 süsinikdioksiid Metall + hapnik = metallioksiid (aluseline oksiid) Fe2O3 raud(III)oksiid või diraudtrioksiid 2Ca+O2=2CaO Mittemetall+hapnik=mittemetallioksiid (happeline oksiid) C+O2=CO2 2
Mannerjää hakkab sulama ja ookeni tase tõuseb. · Aerosoolballoonide massilise kasutamise tulemusena on · atmosfääri sattunud feroone, mille tulemusel laguneb atmosfääri ülemistes osades osoon ning tekivad osooniaugud. · Osooniaukude piirkonnas on väga tugev ultravioletkiirgus ja ohtlik päevitada, kuna võib põhjustada nahavähki. · Mõned atmosfääri kogunevad gaasid on otseselt ohtlikud nt. SO ja NO . Need on 2 2 happelised oksiidid ja muudavad tavalised sademed happesademeteks. · Atmosfääri saastab ka tolm, mis on tekkinud inimtegevuse tagajärjel. · Atmosfääri saastab ka väga ohtlikku radioaktiivset tolmu. Vee saastumine · Tööstuslikud heitveed võivad sisaldada raskemetallide ühendeid ja mitmesuguseid mürgiseid orgaanilisi ühendeid. · Õlireostust tekitab nii tööstus kui ka transport. · Olmereostuse tulemusena satub vette hulgaliselt orgaanilisi ühendeid. · Sademetega jõavad
OKSIIDID Oksiid aine, mis koosneb kahest elemendist, millest üks on hapnik. Aluseline oksiid aluseliste omadustega, reageerib hapetega. Happeline oksiid happeliste omadustega, reageerib alustega. Oksiidide saamine: *Põlemise teel: C+O2 CO2 2Ca+O2 2CaO *Kuumutamise teel: 2Cu+O2 2CuO HAPPED Hape aine, mis annab vesilahusesse vesinikioone. Liigitamine: Hapnikusis Prootonite Tugevuse järgi alduse järgi arvu järgi Hapnikhappe Hapnikut Üheprootonilis Mitmeprootonilis Tugevad Nõrgad d a ed happed ed happed happed happed happed Sisaldavad Ei Sisaldab ainult Sisaldab mitut Vesinikkloriid Süsihape ühe sisalda ühte vesinikiooni. , , elemendina hapnikku vesinikiooni. vesinikbromii fosforhap hapnikku. . ...
DIMDI klassifitseerimist üle soovitatava kontsentratsiooni on ärritav Linalool lõhnastatud hügieenitooted ja puhastusvahendite sh seebid, pesemis-, sampoonid ja vedelikud Kahjuritõrjetes võib põhjustada allergilisi reaktsioone nagu ekseemi tundlikel inimestel Teadlased väidavad et see leevandab stressi Muud ohtlikud kemikaalid Paret-polümeer Xn ohtlik keskkonnale R22 vältida sissehingamist Amiinid, alküüldimetüül, oksiidid Xi ärritavad N keskkonnaohtlik Etanool F tuleohtlik R11 väga tuleohtlik Alküül Xi - ärritav Ohtlikud kemikaalid R38 on halb silmadele ja nahale R41 esineb silmade kahjustamise tõsine oht R50 aga väga mürgine veeorganismidele. NB! Need pole märgitud pakendil, vaid leiab internetist ohutuskaardilt. Kahjulikkus Poisslastel võib tekitada tulevikus viljakuse probleeme Püsib nõudel 30 pesukorda, mis tähendab, et
olema Fifth le · Väävel ei reageeri kulla, plaatina, joodi, lämmastiku ja väärisgaasidega. · Väävli stabiilsemad oksüdatsiooniastmed on -2, 0, 4 ja 6 · Väävli oksiidid on happelised. · Väävli vesinikühendeist tähtsaim on divesiniksulfiid, mis on nõrk hape ja redutseerivate omadustega. Kus leidub? Väävel esineb looduses nii ehedal kujul kui ka ühendite koostises. Ehedat väävlit võib esineda näiteks vulkaanilistes piirkondades. Mida tehakse väävliga? Väävlit kasutatakse põhiliselt väävelhappe tootmiseks, mida omakorda kasutatakse põhiliselt akudes.
Aanorgaanilis Valgus- ja ilmastikukindlad, leelistes lahustumatud, hea kattevõimega looduslikud värvained: ooker, ed värvid Saadakse savidest, maakidest ja kivimitest nende mehaanilisel töötlemisel. Sünteetilised anorgaanilised värvid: tsinkvalge, titaanvalge, kunstlik ultramariin jt. Saadakse anorgaa füüsikaliste ja keemiliste protseduuride tulemusel. Keemiliselt koostiselt peamiselt soolad ja oksiidid. Orgaanilised Elusloodusest või organismidelt pärineva aine töötlemisel saadud värvaine. värvid Kattevärv Värv, mis katab pinna enamasti läbipaistmatult: guass, tempera, õlivärv. Lasuurvärv Läbipaistva kihina pinda kattev vähese pigmendi sisaldusega värv. Akrüülvärv Akrüül on sünteetiline plastvärv, mis võeti kasutusele 1960. aastatel. Akrüülvärv on vesivärv, mida saab veega lahjendada, kuid
· Keemistemperatuur: 184,35 °C · Tihedus: 4,93 g/cm3 · Värvus : joodi värvus on kas metallse läikega must või violetne. Gaasilises olekus on jood lilla · Kõvadus: puhtal kujul on jood väga kõva kristallne aine Keemilised omadused · Oksiidi tüüp: tugevhappeline · Kuumutamisel tekivad toksilised aurud · Jood on tugev oksüdeerija · Elektronegatiivsus: 2.66 · Ühendid: Oksiidid: I2O4; I2O5 ;I4O9 Kloriidid: ICl; (ICl3)2 Fluoriidid: IF; IF3; IF5; IF7 Bromiidid: IBr Kasutamine · Tööstuses: tsrkooniumi ja titaani jodiidrafeerimisel ja katalüsaatorina orgaanilises sünteesis · Keemilises analüüsis: jodomeetrias · Meditsiinis: antitüreoidse vahendi, antiseptikuna ja radioaktiivsuse vastu ·
· Levinuim keemiline element maakoores-ligikaudu 45%. · Leidub vees ja õhus. · Looduses leidub vähesel määral ka hapniku teist allotroopi-osooni. · Maad ümbritsev hõre osoonikiht takistab elusloodust ohustava lühilainelise ultraviolettkiirguse jõudmist maapinnani. Keemilised omadused · Molekulaarne hapnik on tavatingimustes vähe aktiivne, kuumutamisel aga aktiivne. · Tugev oksüdeerija · Paljud ained põlead hapnikus tekivad oksiidid. Hapnik Kasutatud materjalid · http://et.wikipedia.org/wiki/Esileht · https://www.google.com/imghp?hl=et&gws_rd=ssl AITÄH VAATAMAST!
Teiseks rauadepooks on hemosideriin. (25% kokku). Transferiini abil kantakse raud vabanemiskohtadest maksa, põrna ja luuüdisse. Fe leidub ka lihastes, nahas ja küüntes ning kuulub juustevärvi määravate pigmentide koostisesse. Rauapuudusel areneb kehvveresus, mida nüüdisajal leevendatakse rauapreparaatidega: orgaaniliste hapete soolade, FeSO4 või redutseeritud rauaga. Hemoglobiinis on peamine Fe kogus. Inimene saab toiduga keskmiselt 6-40 mg Fe päevas. 1. tähtsamad kroomi oksiidid - värvus, lahustumine, valemid jt omadused Oksiidides on kroomi oksüdatsiooniaste II kuni VI. Tähtsamad oksiidid on Cr2O3, CrO2, CrO3. Cr2O3 kroom(III)oksiid on roheline värvusega korundi tüüpi kristallvõrega, suure kõvadusega ja vees praktiliselt lahustumatu tahkis. Keemiliselt inertne: ei reageeri toatemperatuuril hapete ega leelistega. Kroom(III)oksiid tekib Cr põlemisel hapnikus; laboris saadakse ammooniumdikromaadi lagundamisel soojendamisega:
koostise ja kasutusalade järgi Tehniokeraamika jaguneb: · Oksiidikeraamika · Mitteoksiidikeraamika · Segakeraamika. Kasutusalade järgi jaguneb aga: · Konstruktsioonikeraamika · Tööriistakeraamika · Elektrokeraamika 2.1 Oksiidikeraamika Oksiidkeraamika aluseks on oksiidid, mis esinevad looduses puhtal kujul või saadakse metallide kuumutamisel õhus vôi hapnikus. Oksiidid on kõrge sulamistemperatuuriga tehnokeraamikas kasutatakse kõige rohkem: Al2O3, MgO, ZrO2 , SiO2 , TiO2. 2.2 Mitteoksiidikeraamika 4 Mitteoksiidkeraamika aluseks on puhtad karbiidid,nitriidid, boriidid ja silitsiidid.
KEEMILISE REAKTSIOONI KIIRUS JA TASAKAAL TASAKAAL Temp tõstmisel – endo (∆H>0 ) suunas > Temp alandamisel – ekso (∆H<0) suunas < Tahke aine kogus või peenestamine, segamine ja katalüsaatori kasutamine EI MÕJUTA TASAKAALU, vaid kiirust ! Pöörduv reaktsioon ei saa kunagi otsa ! KIIRUS Kui reaktsioonis kõik gaasid, kiirus ei muutu ANORGAANILISTE AINETE PÕHIKLASSID Anorgaanilised ained – Lihtained → Metallid Mittemetallid Liitained → Oksiidid Happed Alused Soolad Oksiidid on ained, mis koosnevad kahest elemendist, millest 1 on Hapnik. Liigitatakse keemiliste omaduste põhjal: aluselised, happelised, amfoteersed, neutraalsed HCl CH₃COOH Happed on ained, mis annavad vesilahusesse vesinikioone. Hapete liigitamine vesinikuaatomite arvu järgi 1. Üheprootonilised HCl HNO₃ 2. Mitmeprootonilised H₂SO₄ H₃PO₄ Tugevad happed Keskmised Nõrgad happed
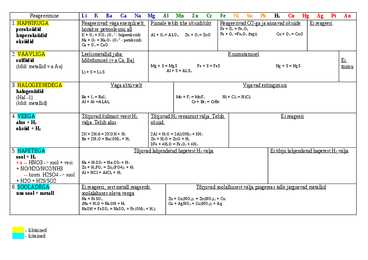
1. HAPNIKUGA Reageerivad väga energiliselt, Pinnale tekib tihe oksiidikiht Reageerivad O2-ga ja annavad oksiide Ei reageeri peroksiidid hoitakse petrooleumi all Fe + O2 = Fe2O3 hüperoksiidid K + O2 = KO2 (O2-1 - hüperoksiid) Al + O2 = Al2O3 Zn + O2 = ZnO Fe + O2 =Fe3O4 (tagi) Cu + O2 = CuO oksiidid Na + O2 = Na2O2 (O2-2 - peroksiid) Ca + O2 = CaO 2. VÄÄVLIGA Leelismetallid juba Kuumutamisel sulfiidid hõõrdumisel (v.a Ca, Ba) Ei (kõik metallid v
V: Fe3O4 ja Al2O3 põlemisel eralduval soojusel, raidrööbaste liitmisel. 22) Laserkeevitust iseloomustab: V: Väikesed toote deformatsioonid, min terade kasv, suur keevituskiirus. 34) Jootmisel hinnatakse liitepinde märgumist joodisega märgumisnurgaga, räbusti kasutamise eesmärk on: V: mitte mõjutada märgumisnurka, taandada oksiidikelmet. 35) Sulatuspõkk-keevituse eeliseks takistuspõkk-keevituse ees on: V: toote suurem ristlõige, liitepinnad suletakse ja oksiidid paisutatakse. 38) Laserlõikamisega saadud toorikut iseloomustab: V: kitsas lõiketsoon (0,1-0,6 mm), täpsed toorikud, suur lõikekiirus. 40) Metallide keevitavuse hindamisel tuleb arvesse võtta: V: konstruktiivseid ja ekspluatatsiooninõudeid liidete.... I)Plasmakeevitust otskaarega iseloomustab: V: suur keevituskiirus, kitsas termomõju tsoon. II) Elekterkontaktkeevituse protsessid kuuluvad: V: termomeehaaniliste protsesside hulka.
hüdrosfääris ja ja maitsetu gaas, Vees on vesiniksidemed. Kasutatakse atmosfääris. väikseima karetikütustes, metallurgias, molekulimassiga keemiatööstustes. kõigist gaasidest. 2 Hapnik O2 Leidub õhus. Ta on värvitu ja Kõige tähtsamad on oksiidid. Ja väga suur lõhnatu. tähtsus on eluslooduses (hingamine). 3 Halogeenid Suure keemilise Halogeenid on tugevad Tähtsamad ühendid: fluor, kroom. aktiivsuse tõttu leidub oksüdeerijad. Kasutatakse tuumakütuse puhastamiseks. Cl2,F2,Br2,J2 neid looduses vaid ühendite koosseisus.
2.Metallilisus: Elektronide loovutamise võime. Mida paremini ta seda teeb, seda metallim ta on. Mida kaugemal on elektron tuumast, seda aktiivsem ta on ning metallilisus kasvab. Aatomi raadius on tuuma kaugus viimasest elektronkihist. Rühma number näitas väliskihi elektronide arvu. Perioodi number näitas Arühma metallide elektronkihtide arvu. Metallilisus on suurem seal, kus on väliskihil vähem elektrone. Etanool Ch3Ch2OH Metallide keemilised omadused: 1) metall+hapnik Tekivad oksiidid!!! 2) metall+hape -- sool+ H2 Nt: Zn+HCl --- ZnCl2 + H2 NB! On redoks! Metallid reageerivad hapetele vastavalt pingereale. K, Ba, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Ni, Sn, Pb reageerivad tavaliste hapetega. Cu, Hg, Ag, Pt, Au ei reageeri hapetega. 3) metall+vesi --- hüdroksiid/oskiid+ H2 Veega reageerivad toatemperatuuril Li, Ba, Ca, Na, Mg Veega reageerivad kuumutamisel Al, Mn, Zn, Cr, Fe Nt: Na+H-OH --- NaOH+H2 Nt: Zn+H2O ---kuumutamine--- Zn(OH)2 + H2 Zn(OH)2 --- ZnO+H2O
Samuti annab see neile nõrgalt hapuka maitse. Pudeli avamisel eraldub süsihappegaas kihisedes limonaadist. Süsihape on ebapüsiv ja laguneb küllalt kiiresti jälle süsinikoksiidiks ja veeks. Suure rõhu all lahustub süsinikoksiid vees küllalt hästi. Süsinikoksiidi molekulid moodustuvad veemolekulidega reageerimisel süsihappe. Süsihape on väga nõrk hape. Ainult üsna väike osa laguneb lahuses ioonideks. Happelised oksiidid Oksiidi reageerimisel veega on võimalik saada veel mitmeid teisi hapnikhappeid. Nt. väävlishape ja süsihape. Mõned happed on ebapüsivad ja võivad kergesti (eriti kuumutamisel) uuesti laguneda oksiidiks ja veeks. Nt. süsihape ja väävlishape. Hapetele vastavaid oksiide nim. happelisteks oksiidideks. Enamik happelisi oksiide on mittemetallidoksiidid.
Oksiidid on liitained, mis koosnevad kahest elemendist, millest üks on hapnik. Oksüdatsiooniaste näitab liidetud või laenatud elektronide arvu. Reeglid: Lihtaine oa = alati 0 Hapniku oa ühendis on alati II A-rühmade metallid on kindlalt oa-d, mis võrduvad rühma numbriga (elektronide arv väliskihis = rühma numbriga). Oa määramine ühendis (hapniku või vesiniku kaudu) (akna meetodiga). Õhu koostis: õhk on gaaside segu; kõige enam leidub õhus lämmastikku (78%); teine peamine õhu koostisosa on hapnik (21%) kõigist õhus esinevatest gaasiliste ainete osakestest on hapniku molekulid; kõik ülejäänud õhus leiduvad gaasilised ained argoon, süsihappegaas (0,03%), veeaur ja veel mõned moodustavad kokku vaid umbes 1% õhu koostisest. Puhas õhk on läbipaistev, värvuseta, maitseta ja lõhnata. Järelikult on niisuguste omadustega ka õhu peamised koostisained hapnik ja lämmastik. Eluslooduse jaoks on õhu tähtsaim koostisosa hapnik. See koosneb kaheaat...
HAPNIK Sissejuhatus Hapniku keemiline sümbol on O Keemiline element järjenumbriga 8 Hapnik on keemiliselt aktiivne mittemetall Tal on kaks levinud allotroopset vormi: dihapnik ehk lihtsalt hapnik (O2) ja trihapnik ehk osoon (O3). Hapnik Hapnik on üks tähtsamaid bioelemente Levinuim keemiline element maakoores, moodusades ligi poole selle massist (~45%) Leidub looduses lihtainena kui ka paljude ühenditena (mitmesugused oksiidid) Füüsikalised omadused Lõhnata, maitseta, värvusetu gaas Vees suhteliselt vähe lahustuv Keemistemperatuur -183 C Keemilised omadused Keemilistes reaktsioonides käitub oksüdeerijana Moodustab enamasti ühendid oksüdatsiooniastmes II Suhteliselt vähe aktiivne Elektronegatiivsuselt teine element fluori järel Kuumutamisel muutub hapnik oluliselt aktiivsemaks Palju ained põlevad hapnikus heleda leegiga Hapnik looduses (O2) Tekkinud peamiselt fotosünteesi tulemusena Elusorganismide tähtsaim energiaallikas Atoma...
Hapnik Hapnik on üks levinumaid ja olulisemaid keemilisi elemente Maal ning moodustab ligi poole selle massist. Teda leidub maakoores, vees, õhus ja elavates organismides kõikidest elementidest kõige rohkem. Hapnikku leidub looduses nii lihtainena kui ka paljude ühenditena (mitmesugused oksiidid ja paljud teised ühendid. Hapniku keemiline sümbol on O ja asub perioodilisustabeli 2. Perioodi VI rühmas. See on lõhnata, maitseta ja värvuseta gaas. See on vees suhteliselt väha lahustuv ja keemistemperatuur on 183°C. Keemilistes reaktsioonides käitub hapnik oksüdeerijana (v.a fluori suhtes). Molekulaarne hapnik on tavatingimustes suhteliselt väheaktiivne. Hapniku molekulide vähene aktiivsus on tingitud sellest, et aatomitevaheline side molekulis on väga tugev
Teke · Keskkonna saastumine happeliste oksiididega Äike Suured põlengud Vulkaanipursked Fossiilsete kütuste põletamine · Transport · Tööstus · Olme Detsember 2005 2 Teke Detsember 2005 3 Happesademete teke üldine skeem Detsember 2005 4 Reageerimine veeauruga · Happelised oksiidid reageerivad atmosfääris veeauruga: SO2+H2O ->H2SO3 SO3+H2O->H2SO4 2NO+H2O->HNO3+HNO2 · Tagajärg: happesademed Vihm Lumi Detsember 2005 5 Gaaside päritolu Detsember 2005 6 Happesademete riskifaktor Euroopas Detsember 2005 7 Hapestumine Euroopas · Esimesena täheldasid hapestumise märke rootslased oma maa lõunapiirkonnas · Tänaseks on Rootsis ligi 4000 järve, milles
läbipuhkumisel. Kasutatakse: mürkaaside sidumiseks, seedehäirete ja toidumürgituse puhul. Metaan: lihtsam süsiniku ühend(4kovalentset sidet); maagaasi peamine koostisosa; süsinik on ühendis kõige redutseerunud olekus; omadused: värvuseta, lõhnatu, maitsetu, õhus kergem, vees vähelahustuv gaas. Põlemine:põleb hästi; õhu segus metaan süttib ja plahvatab kergesti. Süsiniku oksiidid: süsihappegaas Co_2 ja Vingugaas Co Süsinikdioksiid: Leidumine: õhus u. 0.03 mahuprotsent; tekib hingamisel, põlemisel, tööstuslikes protsessides. Omadused: värvuseta, lõhnatu, hapuka maitsega gaas, lahustub vees, ei põle. Kasutamine: mitmetes eluvaldkondades nt. Külmutus seadetes. Süsinikoksiid: omadused: lõhnatu, maitsetu, värvuseta, väga mürgine. Saamine: tekib süsiniku põlemisel hapnikupuudusel; kui hapniku järkub põleb Co edasi Co_2-ks.
Toorium sadestub välja lahenduse hüdroksiid ja eemaldatakse. Happeliste filtraate osaliselt neutraliseeritud koos seebikivi pH 3-4. Toorium sadestub välja lahenduse hüdroksiid ja eemaldatakse. Pärast seda lahust töödeldakse ammooniumoksalaadi konverteerimiseks haruldaste muldmetallide oma lahustumatud oksalaadid. Pärast seda lahust töödeldakse ammooniumoksalaadi konverteerimiseks haruldaste muldmetallide oma lahustumatud oksalaadid. Oksalaadid ümber oksiidid poolt anniilimine. Oksalaadid ümber oksiidid poolt anniilimine. Oksiidid lahustatakse lämmastikhappe mis välistab üks peamisi komponente, tseerium, kelle oksiidi lahustu HNO 3. Oksiidid lahustatakse lämmastikhappe mis välistab Üks peamisi Komponente, tseerium, Kelle oksiidi lahustu HNO 3. Terbium on eraldatud, nagu kahekordne sool ammooniumnitraadi kristalliseerimisest. [6] Terbium kohta Eraldatud, Nauvo kahekordne Sool ammooniumnitraadi kristalliseerimisest. [6] Kõige
Raud kui keskmiselt aktiivne metall reageerib hästi lahjendatud hapetega. (Miksike, 2007) Fe + 2HCl = FeCl2 + H2 Kontsentreeritud väävel - ja lämmastikhappega raud ei reageeri. Nende toimel tekib metalli pinnale väga tihe oksiidikiht ja reaktsioon edasi ei lähe. Niisugust nähtust nimetatakse metalli passiveerumiseks. Sel põhjusel võib kontsentreeritud väävel ja lämmastikhapet transportida raudanumates. (Miksike, 2007) Raua oksiidid veega praktiliselt ei reageeri. Seetõttu tema hüdroksiide saadakse kaudsetel meetoditel, näiteks vastava soola reageerimisel leelisega. (Miksike, 2007) Rauamaagid on: · pruun ja punane rauamaak Fe2O3; · must rauamaak e. magnetiit Fe3O4. (Vikipeedia, 2007b). 5 Tähtsamad ühendid: · Fe(HCO)3 - vees (katlakivi pruun värvus); · Oksiidid Fe3O4 magnetilised omadused
Leekide värvused: Ca- telliskivi punane, Sr- punane, Ba- kollakasroheline Füüsikalised omadused: värvuselt hõbevalged või hallikasvalged. neil on kõrgemad sulamis- ja keemistemperatuurid, suurem tihedus ja kõvadus. pehmed, suhteliselt kergesti lõigatavad, hea elektri- ja soojusjuhtivusega. Keemilised omadused: keemiliselt aktiivsed, keemiline aktiivsus suureneb rühmas ülevalt alla. Hapnikuga reageerimisel süttivad metallid heleda leegiga põlema ja tekivad vastava metalli oksiidid. Reageerimisel happega tekib vastava metalli sool ja eraldub vesinik. Leelismuldmetallid reageerivad veega ning saadusteks on vastava metalli hüdroksiid ja vesinik BERÜLLIUM: on kergete, korrosioonikindlate ja heade mehhaaniliste omadustega sulamite komponent. Berülliumsulamitest tehtud detailid ja seadmed taluvad suurepäraselt koormust ja on kulumiskindlad
alus + sool =>> sool + alus I mõlemad lahustuvad, II üks lahutumatu sool + metall =>> metall + sool sool lahutuv, I metall aktiivsem II metllist sool + sool =>> sool + sool I mõlemad lahutuvad, II üks lahutumatu alus.oks + hap.oks =>> sool alati metall + mittemetall =>> sool ??? alus.oks + vesi ainult IA ja IIA (alates Ca) metallide oksiidid hap.oks. + vesi ei reageeri SiO2.
· Aatommass: 24,305 · Sulamistemperatuur: 648,8 °C · Keemistemperatuur: 1090 °C · Tihedus: 1,738 g/cm3 · Värvus: hõbevalge · Agregaatolek toatemperatuuril: tahke · Kõvadus Mohsi järgi: 2 Keemilised omadused: · Elektronegatiivsus Paulingu järgi: 1,31 · Oksiidi tüüp: tugevaluseline · Ühendid: Fluoriidid: MgF2 Kloriidid: MgCl2 Bromiidid: MgBr2 · 6H2O, MgBr2 Jodiidid: MgI2 Hüdriidid: MgH2 Oksiidid: MgO, MgO2 Sulfiidid: MgS Seleniidid: MgSe Telluriidid: MgTe Nitriidid: Mg3N2 Elemendi, ühendite kasutusalad: · signaalraketid · valuveljed, lennukidetailid · tulekindlad tellised · pigmendid, täiteained Magneesium on väga kerge metall. Magneesium on pehme ja peab vähe vastu. seetõttu tuleb tema kasutamine kõne alla ainult sulamitena. Need on samuti kerged, kuid heade mehaaniliste omadustega
42 K 0 41,963 12,36 tundi 43 K 0 43 22,3 tundi Keemilised omadused: · Elektronegatiivsus Paulingu järgi: 0,82 · Oksiidi tüüp: tugevaluseline · Ühendid: Fluoriidid: KF Kloriidid: KCl Bromiidid: KBr Jodiidid: KI Hüdriidid: KH Oksiidid: KO2, K2O, K2O2 Sulfiidid: K2S Seleniidid: K2Se Telluriidid: K2Te Nitriidid: - Avastaja(d), avastamisaeg, - koht: Sir Humphrey Davy, 1807, London, Suurbritannia Lihtaine saamine: Kaaliumit saadakse sulatatud KOH elektrolüüsil: 4KOH 4K (katoodil) + 2H2O + O2 (anoodil) Nüüdisajal toodetakse kaaliumi metalse naatriumi ja kaaliumkloriidi sulandist 850 ºC juures: Na + KCl NaCl + K
oksiidile vastava happe 4. happeline oksiid + CaO + CO2 CaCO3 sool!) aluseline oksiid sool 6 Na2O + P4O10 4 Na3PO4 Oksiidi 5. aluseline oksiid + vesi Na2O + H2O 2 NaOH reageerimine alus CaO + H2O Ca(OH)2 veega. Reageerivad vaid IA ja IIA al CuO + H2O ei toimu Ca-st metallide oksiidid Aluselise oksiidi 6. happeline oksiid + vesi CO2 + H2O H2CO3 korral tekib alus, hape SO2 + H2O H2SO3 happelise korral SiO2, mis on liiva põhi- SO3 + H2O H2SO4 komponent, ei reageeri veega! hape. N2O5 + H2O 2 HNO3 P4O10 + 6 H2O 4 H3PO4 SiO2 + H2O ei toimu
a. K2SO4, c. P4, e. Ca(HCO3)2, g. H2TeO4, b. Mn(OH)4, d. CrO, f. Sr, h. N2O. 6. Andke nimetused järgmistele ainetele: a. Sn(OH)4, c. I2O7, e. CuSO3, b. Ni2(SO4)3, d. HNO2, f. FeS. 7. Millised järgmised väited on õiged, millised valed? Vale väide parandage eitust kasutamata. a. Kõik aluselised oksiidid reageerivad veega, moodustades aluseid. b. Enamus happelisi oksiide reageerib veega, moodustades happeid. c. Soolad on liitained, milles metalli anioonid on seotud happekatioonidega. d. Igale hapnikhappele vastab happeline oksiid. e. Igale hüdroksiidile vastab happeline oksiid. f. Leeliseid saadakse vastava aluse reageerimisel veega. g. Leeliseid saadakse vastava metalli reageerimisel veega. h
KT ,,Aine ehitus" kordamisküsimused/teemad. Õpikust lk 8-66, näidisülesanded töölehelt Selgita mõisteid: · Aatomorbitaal - aatomi osa, milles elektroni leidmise tõenäosus on kõige suurem. · Elektronegatiivsus - keemilist elementi iseloomustav suhtarv, mis arvestab aatomi võimet tõmmata · eksotermiline reaktsioon soojuse(energia) vabanemisega toimuv reaktsioon · endotermiline reaktsioon soojuse(energia) neeldumisega toimuv reaktsioon · kovalentne side aatomite vahel ühiste elektronpaaride kaudu moodustunud keemiline side · kovalentne mittepolaarne side side, milles mõlemad aatomid mõjutavad ühist elektronpaari võrdse jõuga · kovalentne polaarne side aatomeid siduv ühine elektronpaar on enam kui ühe aatomi valduses ja molekulide osadel on erinimelised osalaengud · iooniline side ioonide vahel tekkinud keemiline side metalliline side, · molekulaarne aine osakeste vahel olevad nõrgad molekulidevaheli...
vasakult paremale. Keemiline aktiivsus. Metallidel muutub keemiline aktiivsus rühmas ülevalt alla, mittemetallidel vastupidi. See on seotud elementide metallisuse ja mittemetallilisusega. Metallilised-mittemetallilised omadused. Rühmas ülevalt alla tuuma ja väliselektronkihi vaheline külgetõmme nõrgeneb ning väliskihi elektron võib kergemini eralduda. Metallilisus suureneb rühmas ülevalt alla, mittemetallilisus vastupidi. Aktiivsete metalliliste elementide oksiidid on tugevalt aluseliste omadustega, vähemaktiivsete metalliliste elementide oksiidid on enamasti nõrgalt aluseliste omadustega. Mittemetalliliste elementide oksiidid on enamasti happeliste omadustega (v.a üksikud erandid). Elementide metalliliste omaduste nõrgenedes ja mittemetalliliste omaduste tugevnedes oksiidide aluselised omadused nõrgenevad ja happelised omadused tugevnevad. Mida enam vasakul metall pingereas asub, seda:
Siirdemetallide hulka kuuluvad kõik väärismetallid. Õhu ja vee suhtes enamasti vastupidavad. · Kõige enam kasutatakse praktikas rauda. Niklit ja kroomi kasutatakse paljude sulamite koostises. Kroomi kasutatakse laevatööstuses. Vaske kasutatakse peamiselt elektrijuhtmetes. · Oksiidid; valged ZnO ja TiO ,roheline Cr O , punased Cu O ja HgO, mustad CuO ja MnO . Mitmeid neist kasutatakse värvipigmentidena. Raua oksiidid ooker on kollakas ja rauamennik punakas. Rauatagi Fe O on magneetiliste omadustega. Raud(II) sooladest tähtsaim on raud(II)sulfaat FeSO mis tahkel kujul esineb roheka kristallhüdraadina FeSO x7H O mida nimetatakse raudvitrioliks ja kasutatakse taimede kaitsmiseks mürgina. Raud(III)sooladest on tähtsaim raud(III)kloriid DeCl selle lahuseid kasutatakse vask-trükiplaatide töötlemisel.
reageeri veega, reaktsiooni ei toimu) NT: CO2 + H2O = H2CO3 (tegemist on oksiidi ja vee reaktsiooniga, kuna ühendis on vaid kaks elementi, millest üks on hapnik (O). See oksiid on happeline, kuna C on mittemetall. Veega reageerides moodustab happeline oksiid vastava happe, tekib süsihape) NT: SiO2 + H2O = ei reageeri (tegemist on erandiga, mida peate teadma. SiO 2 on liiv ja see ei reageeri ka rannas veega (muidu poleks meil ju liivarandu)) Reageerivad oksiidid 1. Vaata, kas mõlemad on oksiidid 2. Oksiidide reageerimisel tekib sool, mis koosneb aluselise oksiidi metallist ja happelisest oksiidist tekkinud anioonist (vaata lahustuvustabelis anioonide tulpa. Kui sarnaseid anioone on mitu, siis esialgsele ühendile tuleb ainult üks hapnik juurde (Nt SO 2 muutub SO32- ja SO3 muutub SO42-). 3. Esimesena kirjutatakse alati metall ja teisena anioon.
Värvilt suurtes Sinakas kogustes sinakas väikestes kogustes lõhnatu Terav lõhn Lahustub Ei lahustu vees vähesel määral vees Keemist.-183C Keemist.-111 mürgine Keemilised omadused: · O3 on keemiliselt aktiivsem kui O2; ta laguneb O2 ja O(monohapnik on hästi aktiivne) · Mõlemad reageerivad liht ja liitainetega; toimub põlemine ja saaduseks on oksiidid Kasutamine: · O3: veepuhastusjaamades(tapab baktereid) · O2: Põlemisreaktsiooni läbiviimiseks e. Energia tootmiseks ; nt:meditsiinis Halogeenid Floor,Kloor,Broom,Jood Lihtainena 2 aatomilised molekulid( F2;Cl2;Br2;I2) Kõigil on oksüdatsiooniaste -1, ülejäänutel 2;5;7... v.a F Füüsikalised omadused: · F(kollakas) · Cl(rohekas kollane) · Br(Vedelik ja aur pruunid) · I(hallikas, must; metallse läikega; aur on aga lillakas)
RAUD-(Üldine keemia.H.Karik) 1.Leidumine looduses. Ehedalt leidub rauda Maale langenud meteoriitides.Maakoores leidub rauda ainult ühudnditena.Rauaühendeid,mida kasutatakse raua tootmiseks,nimetatakse rauamaakideks.Tähtsamad neist on järgmised. Magnetiit ehk magnetrauamaak(Fe3O4) on must kristalane magnetiline ühend.Rikkalikud magnetiitilademed esinevad Kurski oblastis.Punased ja pruunid rauamaagi põhikomponendiks on raud(III)-oksiid ehk sideriit(FeCo3) on hallia värvusega maak.Rauamaakide töötlemisel saadakse malmi,see on rauasulam milles on üle 2% süsiniku ning lisandina väävlit,räni,fosforit jt. elemente. 2.Füüsikalised omadused. Raud on läikiv hallikasvalge metall,tihedusega 7,86*10 3 kg/m3 ja sulamistemperatuuriga 1540 C.Raud on plastiline,mis võimaldab teda valtsida ja sepistada.Raud tõmbub mgneti külge. 3.Keemilised omadused.Keemiliselt puhtas raud on püsiv vee ja õhu suhtes.Tavaline raud(malm,teras) ,mis sisaldab mitmesuguseid ...
(mittemetalli + ALUS vaata ALUS + HAPPELINE OKSIID oksiid) + ALUSELINE OSKIID SOOL SO2 + Na2O Na2SO3 ALUSELINE + VESI LEELIS Li2O + H2O 2LiOH OKSIID NB! Reageerivad ainult IA ja IIA(alates Ca) metallide oksiidid. (metalli oksiid) + HAPE vaata HAPE + ALUSELINE OKSIID + HAPPELINE OKSIID vaata HAPPELINE OKSIID + ALUSELINE OKSIID METALL + HAPNIK OKSIID 4Fe + 3O2 2Fe2O3
Lepidoliit sisaldab rubiidiumi 1,5% ja see on tuntud kaubanuslik element. Rubiidiumi üheks leiukohaks on Bernici järv Kanadas. Füüsikalised omadused: · Aatommass: 85,4678 · Sulamistemperatuur: 38,89 °C · Keemistemperatuur: 686 °C · Tihedus: 1,532 g/cm3 · Värvus: hõbevalge · Agregaatolek toatemperatuuril: tahke Keemilised omadused: · Elektronegatiivsus Paulingu järgi: 0,82 · Oksiidi tüüp: tugevaluseline Ühendid: Fluoriidid: RbF Oksiidid: Rb2O, RbO2, Rb2O2 Kloriidid: RbCl Sulfiidid: Rb2S Kodiidid: RbI Telluriidid: Rb2Te Hüdriidid: HRb Nitriidid: - Saamine: Rubiidium saadakse metalse naatriumi ja rubiidiumkloriidi sulandist: Na + RbCl Rb + NaCl Rb lendub auruna, mis metalse rubiidiumi saamiseks kondenseeritakse. Rubiidiumi ei ole võimalik saada rubiidiumkloriidi elektrlüüsil, sest Rb lahustub sulas rubiidiumkloriidis. Kasutamine · fotoelemendid · gaaside neelaja vaakumtorus
Jäätmete probleemid- rahvastiku arvu suurenemine, tarbimise ja tootmise suurenemine. Tagajärjed: linnade ümber tekivad prügimäed, igal aastal kantakse ookeanisse 6,5 milj tonni prahti, pinnas, vesi ja õhk saastuvad. Lahendus: prügimäe alla kavandatav ala katta vastava kattega, prügilast eralduvat vett suunata kanalisatsiooni, ohtlikud jäätmed viia selleks ettenähtud kohtadesse, prügi sorteerimine. Happevihmad Tekkepõhjused: kütuste põlemisel atmosfääri sattuvad happelised oksiidid ühinevad veeauruga ja tekivad happelised reaktsiooniga sademed. Tagajärjed: okaspuude kahjustamine, kiireneb keemiline murenemine, veekogude vesi muutub happeliseks, veeorganismid võivad hukkuda, inimestel võivad tekkida hingamisteede haigused. Lahendused: Õhu saaste vähemine, alternatiivse energia kasutamine. Rahvastiku kasv Põhjused: suremuse langus Tagajärjed: Vasus, nälg, suureneb tarbimine ja tootmine. Lahendus: pere planeerimine, abielu ea tõstmine. Magevee varude puudus
Korrosiooni vormid Elektrokeemiline korrosioon Mikroobide korrosioon Kõrgetemperatuuriline korrosioon Materjalide pulbristumine Korrosioon mittemetallides Elektrokeemiline korrosioon Juhtub juhul kui keemiliselt aktiivne ja vähemaktiivne metall satuvad omavahel kontakti ning toimub elektronide kandumine nõrgemale Protsess kiirendab aktiivse metalli korrosiooni Vähem aktiivse korrodeerumine aeglustub või üldse peatub Tekivad enamjaolt aktiivsema metalli oksiidid või soolad Järgnev pilt iseloomustab hästi elektrokeemilist korrosiooni. Vaskplaadist on läbilöödud raudneet. Raua ja vase vahel on otsene kontakt. Nende pinnale kondenseerub õhuniiskus ning moodustub Fe-Cu galvaanipaar ning järgneb elektrokeemiline korrosioon. Raud on pingereas aktiivsem ja seetõttu korrodeerub see kiiremini. Mikroobide korrosioon Korrosioon, mis on tekitatud või kiirendatud mikroorganismide poolt
Aatommass: 126,9045 Sulamistemperatuur: 113,5 °C Keemistemperatuur: 184,35 °C Tihedus: 4,93 g/cm3 Värvus: metalse läikega Olek toatemperatuuril: tahke Elektronegatiivsus Paulingu järgi: 2,66 Oksiidi tüüp: tugevhappeline Ühendid: Fluoriidid: IF, IF3, IF5, IF7 Kloriidid: ICl, (ICl3) 2 Bromiidid: IBr Oksiidid: I2O4, I2O5, I4O9 Tahkel joodil on omadus kuumutamisel sublimeeruda, see tähendab aurustuda ilma, et vahepeal tekiks vedelat olekut. Aurude jahtumisel moodustuvad uuesti tahke aine kristallid. Antiseptikuna meditsiinis Kilpnäärme diagnostikas Orgaaniliste ja anorgaaniliste joodiühendite saamiseks. Katalüsaatoritena Looma ja linnutoidu lisanditena Värvainete ja pigmentide koostuses Halogeenlampides Keedusoola lisandis
on Me + ZH+ + = MeZ+ + Z/2 H2 (2Na + 2H+ = 2Na+ + H2) Väärismetallid hapetega ei reageeri Kui happe anioon on tugev oksüdeerija ( HNO3 ja kange H2SO4) siis pingerida ei saa kasutada, sest toimuv reaktsioon ei ole asendusreaktsioon Ag + 2HNO3 = AgNO3 + NO2 + H2O Metall + vesi Väga aktiivsed metallid tõrjuvad vesiniku veest välja. Alguses tekib oksiid, kuid nende metallide oksiidid reageerivad veega ja reaalseks saaduseks on hüdroksiid (leelis) Ca + 2H2O = Ca(OH)2 + H2 Keskmise aktiivsusega metallide oksiidid veega ei reageeri ja reaktsiooni saaduseks on oksiid.reaktsioon kulgeb kõrgel temperatuuril. eriti vastupidava oksiidse kile tõttu on Al ja Cr praktiliselt püsivad ka veeaurus .Näiteks3Fe + 4H2O = Fe3O4 + 4H2 Nendes reaktsioonides on oksüdeerijaks samuti vesinikioon Väheaktiivsed- ja väärismetallid veega ei reageeri Metall + soola vesilahus
Aktiivsed metallid (K-Mg) reag. külma veega, tekivad leelis ja H2. Ca+2H2O=Ca(OH)2+H2. Zn+H2O=ZnO+H2. Väheaktiivsed metallid (alates Ni-st) ei reageeri veega. Vesinikust eespoololevad metallid tõrjuvad hapetest vesiniku välja. Zn+2HCl=ZnCl2+H2. Metall reageerib vees lahustuva soolaga, kui ta on aktiivsem kui soola koostises olev metall. Zn+CuCl 2=ZnCl2+Cu. 2Na+CuCl2+2H2O= Cu(OH)2+2NaCl+H2 2Na+ 2H2O=2NaOH+H2 2NaOH+CuCl 2=Cu(OH)2+2NaCl. Hapnikuga tekivad oksiidid: 2Ca+O2=2CaO. Väävliga tekivad sulfiidid: Ca+S=CaS. EI REAGEERI!: Plii+Vesi, Vask+Magneesiumkloriid, Hõbe+Väävelhape, Vask+Vesi. 0 I+ V+ II- I+ V+ II- IV+ II- I+ II- As + 5HNO3 H3AsO4 + 5NO2 + H2O As0 5e As5+ 1 N5+ +e N4+ 5 0 I+ V+ II- I+V+II- II+II- I+II- 3Sb + 5HNO3 3HSbO3 + 5NO + H2O 0 5+ Sb 5e Sb 3 N5++3e N2+ 5 0 I+V+II- IV+II- II+II- I+II- 3C + 4HNO3 3CO2 + 4NO + 2H2O C0 4e C4+ 3
on fosfori allotroopne vorm, väliselt vaha meenutav poolläbipaistev tahke aine. Sulab 44o Celsiuse juures. Kergel soojendamisel või hõõrumisel süttib kergesti. Põlemisel annab kuni 800kraadise temperatuuri. Sattudes põlevana inimese nahale, tekitab valge fosfor väga sügavaid ja ohtlikke põletushaavu. Verre ja seedimisteedesse sattudes mõjub valge fosfor kange mürgina. Fosfori stabiilseim oksüdatsiooniaste on +5. Teised olulisemad oksüdatsiooniastmed on +3 ja 3. Fosfori oksiidid on happelised. Fosfori vesinikühendid, fosfaanid ehk fosfiinid, on tugevad redutseerijad. Elektronvalem: 1s2 2s2p6 3s2p3 Elektronskeem: +15|2)8)5) Elektronite arv: 15 Neutronite arv: 16 Prootonite arv: 15 Aatommass: 30,97376 Sulamistemperatuur: 44,1 °C Keemistemperatuur: 277 °C Tihedus: 1,82 g/cm3 Värvus: värvusetu / punane / hõbevalge Avastaja(d), avastamisaeg, - koht: Hennig Brand, 1669, Hamburg, Saksamaa Kasutatud kirjandus http://et.wikipedia