raud(III)hüdroksiid HAPPED on liitained, mis koosnevad vesinikust ja happeanioonist. HAPE = H+ + happeanioon- (vt. tabelist) N. HCl vesinikkloriidhape H2S - divesiniksulfiidhape H2SO4 - väävelhape Soolad on liitained, mis koosnevad metallist ja happeanioonist. SOOL = metall+ + happeanioon- (vt. tabel) N. NaCl naatriumkloriid K2CO3 kaaliumkarbonaat Ba3(PO4)2 - baariumfosfaat Anorgaaniliste ainete klassid oksiidid, hüdroksiidid, happed, soolad OKSIIDID on liitained, mis koosnevad kahest elemendist, millest üks on hapnik. OKSIID = element+ + hapnik2- N. NaO naatriumoksiid CaO kaltsiumoksiid Al2O3 alumiiniumoksiid N2O5 dilämmastikpentaoksiid HÜDROKSIIDID on liitained, mis koosnevad metallist ja hüdroksiidrühmast OH- HÜDROKSIID = metall+ + OH- N. KOH kaaliumhüdroksiid Ba(OH)2 baariumhüdroksiid Fe(OH)3 raud(III)hüdroksiid
Anorgaania. Oksiidid on ühendid, mis koosnevad kahest elemendist, millest üks on hapnik. Oksiide saadakse põletamisel * Mg + O2 - 2MgO * ja lihtainete *metall ja mittemetall* omavahelisel reaktsioonil *4Fe +3O2 2Fe3O3* Oksiide liigitatakse happelisteks oksiidideks, aluselisteks oksiidideks, anforteerseteks oksiidideks ja neutraalseteks oksiidideks. Happelised oksiidid siia kuuluvad enamasti mittemetalli oksiidid ja kõrge o.-a. Metalli oksiidid. *CO2; NO2; P4O10; CrO3; Mn2O7* Aluselised oksiidid siia kuuluvad enamasti metalli oksiidid. *Na2O;FeO* Amfoteersed oksiidid siia kuuluvad Al2O3; ZnO; Fe2O3; Gr2O3 Neutraalsed oksiidid siia kuuluvad mittemetallid *CO; NO; N20* Oksiidide keemilised omadused. 1. Happelised oksiidid reageerivad veega *CO2 + H2O H2CO3* 2. Happelised oksiidid reageerivad aluseliste oksiididega *CO2 + Na2O Na2CO3* 3
Keemia: oksiidid, alused, soolad, happed. 1. Oksiidid Koostis: koosnevad kahest elemendist, üks on hapnik. AlO3; CaO Nimetused: a. metallioksiidide puhul märgitakse esikohale metalli nimi, tesele kohale oksiid, vahele metalli o-a, kui o-a on muutuv. Fe2O3 raud(III)oksiid b. mittemetallide puhul kasutatakse eesliiteid. CO2 süsinikdioksiid, P2O5 difosfor- pentaoksiid. Saamine: 1.lihtainete ühinemine hapnikuga: C + O2 => CO2 2. liitainete põlemine: CH4 + 202 => CO2 + 2H2O 3. liitainete lagunemine: CaCO3 => CaO + CO2
raud(III)hüdroksiid HAPPED on liitained, mis koosnevad vesinikust ja happeanioonist. HAPE = H+ + happeanioon- (vt. tabelist) N. HCl – vesinikkloriidhape H2S - divesiniksulfiidhape H2SO4 - väävelhape Soolad on liitained, mis koosnevad metallist ja happeanioonist. SOOL = metall+ + happeanioon- (vt. tabel) N. NaCl – naatriumkloriid K2CO3 – kaaliumkarbonaat Ba3(PO4)2 - baariumfosfaat Anorgaaniliste ainete klassid – oksiidid, hüdroksiidid, happed, soolad OKSIIDID on liitained, mis koosnevad kahest elemendist, millest üks on hapnik. OKSIID = element+ + hapnik2- N. NaO – naatriumoksiid CaO – kaltsiumoksiid Al 2O3 – alumiiniumoksiid N2O5 – dilämmastikpentaoksiid HÜDROKSIIDID on liitained, mis koosnevad metallist ja hüdroksiidrühmast OH - HÜDROKSIID = metall+ + OH- N. KOH – kaaliumhüdroksiid Ba(OH)2 – baariumhüdroksiid Fe(OH)3 – raud(III)hüdroksiid
Ainete valemid. Oksiidid ja nende saamine. Vesi ja lahused KORDAMINE KONTROLLTÖÖKS I. Arvutusülesanded III. Kas järgmised ained on oksiidid? Miks/miks mitte? Tase 1 Kui tegemist on oksiidiga, siis nimeta ta (ja kirjuta valem, Mitu grammi vett on vaja lisada 30 g äädikhappele, et saada 12%-line lahus? kui pole antud)! Tase 2 vesi PE 2006. 0,32 kg viinamarjamahla sisaldab süsihappegaas 46,5 g süsivesikuid ja 0,6 g valku
Millest on tingitud vee karbonaatne karedus? mööduv. Ca- ja Mg vesinikkarbonaadi esinemine Kuidas seda kõrvaldada? vee kuumutamisel, kuumutamisel vesinikkarbonaadid lahustuvad ning tekkinud raskestilahustuvad karbonaadid sadestuvad põhja (katlakivi) Millest on tingitud vee mittekarbonaatne karedus? jääv. vees lahustunud Ca- ja Mg kloriidid, sulfaadid Kuidas seda kõrvaldada? vee pikemaajalisel keetmisel, vee destilleerimisel, kasutada vee pehmendajaid ioniitide abil Nimeta veekaredusest tingitud kahjulikke tagajärgi. rikuvad kuumutusnõusid, boilereid, torude ummistusi Milliseid metalle nimetatakse leelismetallideks? I A rühma metallid. on kõige metallilisemad elemendid, oksüdats aste on 1 ja väliskihi el valem on ns1 Iseloomusta neid lühidalt(füüsikalised omadused). Füüsikalised omadused - On pehmed, kergesti lõigatavad, madala sulamistemp, head soojus- ja elektrijuhid, keemilised omadused - reageerivad hapniku ja teiste mittemetallide...
Anorgaaniliste ainete põhiklassid 1. Oksiidid Oksiidid on liitained, mis koosnevad kahest elemendist, millest üks on alati hapnik. Metalli oksiidid Mittemetalli oksiidid (aluseline oksiid) (happeline oksiid) ZnO CO2 Fe2O3 SO3 Na2O Eesliited: 2 di; 3 tri; 4 tetra; 5 penta; 6 heksa; 7 hepta; 8 okta; 9 nona; 10 deka SO3 vääveltrioksiid Ag2O dihõbeoksiid Nimetused: IV -II SO2 väävel(IV)oksiid III -II N2O3 lämmastik(III)oksiid Arseen(IV)oksiid IV -II Ar2O4 ArO2 Püsiva oksüdatsiooni astmega metallide oksiididel oksüdatsiooniastet ei märgita
10 A,C Ülesanded- oksiidide nimetused, saamisreaktsioonid 1. Anna nimetused mittemetallioksiididele, kasutades arvsõnalisi eesliiteid! 1) CO2 6) SO3 2) N2O dil'mmastikoksiid 7) N2O5 dil'mmastik 3) P4O10 8) SiO2 ränidioksiid 4) Cl2O7 dikloor 5) B2O3 diboortrioksiid 2. Anna nimetused aktiivsete metallide oksiididele 1) K2O 2) CaO 3) Al2O3 4) Rb2O 5)MgO kaaliumIIoksiid 3. Anna nimetused , kasutades metalli o.-a (B-rühmade metallid, Sn, Pb), määrates selle aine valemi järgi! 1) Fe2O3 2) ZnO 3) Cu2O 4) Cr2O7 5) MnO2 6) PbO 4. Koosta oksiidide valemid nimetuste järgi! 1) dikloorpentaoksiid 2) süsinikmonooksiid 3)vääveldioksiid 4) strontsiumoksiid 5) nikkel(IV)oksiid 6)titaan(II)oksiid 5. Lõpeta ...
+ ALUS = SOOL + H2O +AL. OKSIID = SOOL + H2O = UUS SOOL + UUS HAPE + SOOL NB! Reaktsioon toimub siis, kui tekkiv hape on reageerivast HAPE happest nõrgem või kui uus tekkiv sool ei lahustu vees (sade). = SOOL + H2 NB! Reageerivad pingereas vesinikust vasakul paiknevad + METALL metallid. Erandiks on k. HNO3, lahj. HNO3 ja k. H2SO4 reageerimine metallidega (ei kehti metallide pingerida, ei eraldu H2, tekib sool, oksiid ja H2O). + HAP.OKSIID = SOOL + H2O =...
Aineklassid Mõisted: 1) Oksiidid on liitained, mis koosnevad kahest elemendist, millest üks on hapnik 2) Happed on liitained, mis koosnevad happevesinikust ja happeanioonist 3) Alused on liitained, mis koosnevad metallikatioonist ja hüdroksiidioonist 4) Soolad on liitained, mis koosnevad metallikatioonist ja happeanioonist 5) Leelised on vees lahustuvad tugevad alused 6) Aluselised oksiidid on oksiidid, mis reageerivad happega moodustades soola ja H2O 7) Amfoteersed oksiidid on oksiidid, mis reageerivad nii happe kui alusega 8) Inertsed oksiidid on oksiidid, mis ei reageeri happe ega alusega 9) Neutralisatsioonireaktsioon on happe ja aluse vaheline reaktsioon 10) Happe lahuse toimul muutub metüüloranž punaseks, lakmus punaseks 11) Aluse lahuse toimel muutub fenoolftaleiin punaseks, lakmus siniseks
MISTED - keemiline reaktsioon- ainete muundumine teisteks aineteks. - keemiline element- kindla tuumalaenguga aatomite liik. - aatom- livike aineosake, koosneb tuumast ja elektronidest. - ioon- aatom vi aatomite rhmitus, millel on positiivne vi negatiivne laeng. - molekul- aine vikseim osake, koosneb omavehel kovalentse sidemega seotud aatomidest. - keemiline side- aatomite- vi ioonidevaheline vastasmju, mis seob nad molekuliks vi kristalliks. - lihtaine- aine, mis koosneb ainukt he keemilise elemendi aatomidest. - liitaine- keemiline hend; aine mis koosneb mitme erineva keemilise elemendi aatomidest. - metall- lihtaine, millel on metallidele iseloomulikud omadused(hea elektri- ja soojusjuhtivus,iseloomulik lige jm). - mittemetall- lihtaine, millel puuduvad metallidele iseloomulikud omadused. - oksiid- hapniku ja mingi teise keemilise elemendi hend. - hape- aine, mis annab lahusesse vesinikioone. - alus- aine, mis annab lahusesse hdrok...
Keemia oksiid koosneb kahest elemendist, millest üks on hapnik Aluselised oksiidid on aluseliste omadustega, reageerivad hapetega Happelised oksiidid- on happeliste omadustega, reageerivad alustega Tugeval aluseliste oksiidide - reageerimisel veega tekivad tugevad alused ehk leelised. Enamiku happeliste oksiidide reageerimisel veega tekib vastav hape. Veega ei reageeri nõrgalt aluselised ning ka mõned happelised oksiidid nt SiO2 Oksiidide põhilised saamisvõimalused : 1. vastavate lihtainete reageerimine hapnikuga, 2. suhteliselt ebapüsivate hapnikku sisaldavate ühendite lagunemine Aluselised oksiidid on metall oksiidid(ainult I ja II A rühma metallid reageerivad veega) ja happelised oksiid on mittemetal oksiid. SO2 ja CO2 saamise võimalused: Põlemine,hingamine Hape aine, mis annab lahusesse vesinikioone Hape molekulid jagunevad lahuses vesinikioonideks ja happe anioonideks
1. OKSIIDID 2) dilämmastiktrioksiid N2O3 1.1. Oksiidide koostis ja vääveldioksiid SO2 nimetused dikloorheptaoksiid Cl2O7 A. Määra elementide tetrafosfordekaoksiid P4O10 oksüdatsiooniastmed ja kirjuta nende süsinikoksiid CO nimetused (elemendi taga sulgudes on tema oksüdatsiooniaste) 1) Li2 ( I ) O ( -II ) liitiumoksiid Mg ( II ) O ( -II ) magneesiumoksiid Fe2 ( III ) O ( -II ) raud(III)oksiid Pb ( II ) O ( -II ) plii(II)oksiid Cr ( VI ) O3 ( -II ) kroom(VI)oksiid 2) N( IV ) O3 ( -II ) - lämmastikdioksiid Cl2 ( I ) O ( -II ) diklooroksiid P4 ( III ) O6 ( -II ) tetrafosforheksaoksiid I2 ( V ) O5 ( -II ) dijoodpentaoksiid S ( VI ) O3 ( -II ) vääveltrioksiid B. Koosta oksiidide valemid. (Mä...
OKSIIDID Oksüdatsiooniastme arvutamine: Hapnik liidab reageerimisel teiste ainetega oma aatomite väliskihile juurde 2 elektroni. Kui eeldame, et saadusena tekib iooniline ühend, on hapniku ioonide ehk oksiidioonide laeng selles ühendis -2. Elemendi aatomite laengut ühendis, eeldusel, et ühend on iooniline, nimetatakse elemendi oksüdatsiooni astmeks. Elemendi oksüdatsiooniaste märgitakse valemis tavaliselt rooma numbriga vastava elemendi sümboli kohale. Negatiivse oksüdatsiooni astme korral kirjutatakse numbri ette miinus märk. Kui on aga positiivne siis plussi reeglina ei kirjutata. II -II NÄITEKS: Mg O Oksüdatsiooniaste näitab elemendi oksüdeerimise astet ühendis. Mida suurem on oksüdeerimisaste on seda rohkem on elemendi aatom loovutanud elektrone teise elemendi aatomile. Mida negatiivsem seda rohkem on võtnud endale. Ühendis on kõigi aatomit...
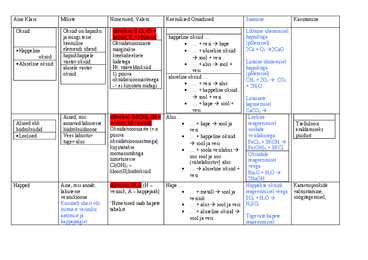
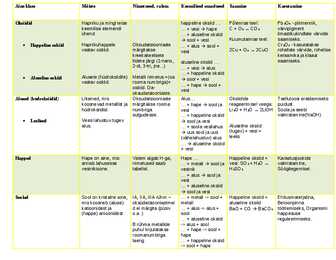
Aine Klass Mõiste Nimetused, Valem Keemilised Omadused Saamine Kasutamine Oksiid Oksiid on hapniku üldvalem: E2On (O = Lihtaine ühenemisel ja mingi teise hapnik, E = element) happeline oksiid ... hapnikuga keemilise Oksüdatsiooniaste · ... + vesi hape (põlemisel) · Happeline elemendi ühend märgitakse · ... + aluseline oksiid 2Ca + O2 2CaO oksiid hapnikhappele kreekakeelsete sool + vesi · Aluseline oksiid vastav oksiid liidetega Liitaine ühinemisel · ... + alus sool ...
Oksiidid Oksiidid koosnavad kahest elemendist, millest üks on hapnik. Liigitus: Metallioksiidid Mi ttemetallioksiidid Aluselised oksiidid Amfoteersed oksiidid Happelised oksiidid Neutraalsed oksiidid K2O, CaO, MgO, Al2O3, ZnO, Cr2O3 SO2, SO3, CO2, P4O10, NO2, NO, N2O, CO Na2O, FeO, BaO N2O5, N2O3, SiO2,(CrO3, Mn2O7) Keemilised omadused: Saamin e: I Aluseline oksiid+ HAPE = sool+ vesi 1.)Lihtainete põlemisel Aluseline oksiid+HAPPELINE
a) Laenguga aatomid b) Nt: Cl-2, Al1. c) Tekivad siis, kui 1 aatom annab teisele oma väliskihi elektrone või võtab nii, et kokku oleks väliskihil 8. 11. Liht ja liitained. Näited: a) Ca2- lihtaine. b) KMnO3- Liitaine. 12. Reaktsioonivõrrandid ja nende tasakaalustamine. Al + O2 = AlO 2Al + O2 = 2AlO 13. Hapnikuühendid- Oksiidide nimed, valemite koostamine, o, - a määramine, õhu koostis, oksüdeerumine, tuntumad oksiidid, arvutused reaktsioonivõrrandi põhjal. a) Kui metallil erinevad oksüdatsiooniastmed Fe2O3 Alumiinium (3) Oksiid, MgO b) Kui elemendi ühendites on vaid 1 oksüdatsiooniaste (1,2,3A rühm), Siis oksüdatsiooniastet ei märgita. Li2O- Liitiumoksiid. c) Mittemetallokiidide korral kasutame eesliidet. 2 di- 3 tri- 4 tetra- 5 penta- 6 heksa- 7 hepta- 8 okta- 9 nona-
Aine klass Mõiste Nimetused, valem Keemilised omadused Saamine Kasutamine Oksiidid Hapniku ja mingi teise happeline oksiid ... Põlemise teel: PbO - pliimennik, keemilise elemendi ... + vesi hape C + O CO värvipigment ühend ... + aluseline oksiid ilmastikukindlate värvide sool + vesi Kuumutamise teel: saamiseks. · Happeline oskiid Hapnikuhappele Oksudatsiooniaste ... + alus sool + CrO - kasutatakse vastav oskiid. märgitakse vesi ...
Alumiiniumoksid Al2O3- on polümeerse struktuuriga valge kristalne aine. See on äärmiselt inertne aine mis on väga vastupidav veetoimele ja praktiliselt ei reageeri ka hapete ning leeliste lahjendatud lahustega. Üks enam tuntud alumiiniumoksiidi teisendeid looduses on korund. Erakordselt kõva ainena kasutatakse peeneteralist korundo ehk smirglit lihvimispulbrite, puhastuspastade jms koostises läipaistvad suured korundikristalid on hinnalised vääriskivid. Lisandite tõttu on nad sageli värvilised. Punaseid korunde nimetatakse rubiinideks, siniseid ja kollaseid safiirideks. Al(OH)3 temp. Al2O3+H2O Normaaltingimustel sulab alumiiniumoksiid temperatuuril 2054°C ja keeb temperatuuril 2980°C. Plii(II)oksiid PbO2-Üks tähtsamaid pliiühendeid, tumeda (pruunikas, must) värvusega väga tugevate oksüdeerivate omadustega. Teda kasutatakse põhiliselt elektroodimaterjalina pliiakudes. Kõik plii lahustuvad ühendid on tugevalt mürgised. Pb3O4-plii(II) j...
OKSIIDID Metallioksiidid: nimetus à metalli nimi (vajadusel oksüdatsiooniaste)oksiid Mittemetallioksiidid : tavaliselt on molekulaarse ehitusega ja nimetus reagee Metallioksiidid on ioonilised ained ja molekule pole moodustatakse eesliidete abil (mono, di ,tri, tetra, penta, heksa, hepta, okta, rimine Näiteks CaO kaltsiumoksiid Fe2O3 raud(III)oksiid e. diraudtrioksiid nona ,deka)
Aineklassid Lihtained: Metallid (Na, Zn, Fe, Cu...) Mittemetallid (C, Si, B, O2, H2, N2, F2, Cl2...) Liitained Oksiidid koosnevad kahest elemendist, millest üks on hapnik o.a-ga –II; Na2O, CO, Cl2O3... o Keemiliste omaduste järgi Aluselised oksiidid – peamiselt metallioksiidid (eriti madalamas o.a-s); reageerivad hapetega; Na2O, CaO, BaO Happelised oksiidid – peamiselt mittemetallioksiidid; reageerivad alustega; SiO2, SO3, CO2 Amfoteersed – võivad reageerida nii hapete kui alustega; Al2O3, ZnO Neutraalsed – ei astu tavaliselt keemilisse reaktsiooni; NO, N2O, CO Nimetused oksiididele:
metalli oksiidi nimetamine: metall (metalli o.a.) OKSIID (erandid: IA IIA IIIA ja IIB) c) Oksiidide saamise reaktsioonid metall + hapnik -> metallioksiid mittemetall + hapnik -> mittemetallioksiid (lihtainetena kirjutatakse mittemetallidest alati indeksiga kaks järgmisi: H2, O2, N2, Cl2, F2, Br2, I2, teistel indeksit ei panda, nt: S, P, Si) d) Oksiidide reageerimine veega aluseline oksiid (metalli oksiid) + vesi -> leelis (millised aluselised oksiidid reageerivad veega ja millised mitte?) IA IIA reageerivad veega Näide: CaO + H2O Ca (OH)2 happeline oksiid(mittemetalli oksiid) + vesi-> hape (ainukesed erandid NO, CO ja SiO2, nemad veega ei reageeri) Näide: SO3 + H2O H2SO4 2. Happed a) Nende valemite ära tundmine, peab seostama nimetust ja valemit Hapnikuta happed ja hapnikuga happed b) Hapete nimetamine peab olema selge (vaata tabelit lk 106) c) Hapete saamise reaktsioonid happeline oksiid + vesi -> hape Näide: H2 + Br2 --> 2 HBr
Keemia eksamiks. 1. Mis on oksiidid ? Liitained, mis koosnevad kahest elemendist , millest üks on hapnik . Aluselised oksiidid: Amfoteerne oksiid: NaO naatriumoksiid ZnO; Al2O3 Fe2O3 raud 3 oksiid Al2O3 alumiinimumoksiid MgO magneesiumoksiid Cu2O vask 1 oksiid Happelised oksiidid: Neutraalne oksiid: N2O5 dilämmastikpentaoksiid N2O; CO SO3 vääveltrioksiid Süsinikdioksiid CO2 tetrafosfordekaoksiid- P4O10 Mis on alused? Ained, mille vesi lahustes esinevad hudroksiidioonid. Mis on happed ? Liitained, mis koosnevad ühest või mitmest vesiniku aatomist ja happeanioonidest. Mis on soolad ? Liitained, milles metalli katioon on seotud happeaninoonidega Happed: Happenimetus - Happevalem Soolanimetus
Anorgaaniliste ainete põhiklassid 12.klass Jaguneb Lihtained: Liitained: Metallid Happed Mittemetallid Alused Soolad Oksiidid Happed Koosnevad vesinikioonist ja happejääkioonist Happed on ained, mis annavad lahusesse prootoneid või vesinikioone. Jaotatakse: Tugevuse Vesiniku arvu Hapnnikusisalduse järgi Tugevuse järgi Tugevad happed näiteks: HCI; HF; HNO3;H2SO4 Keskmised happed näide: H3PO4 Nõrgad happed näiteks: H2CO3; H2S Vesiniku arvu järgi Üheprootonilised happed- happed milles on ainult üks vesinikioon.
saastamine, naiteks heiteid õhku mootorist ja heitvesi reisilaevadest. Naiteks Läänemeremaad on juhtitavad osalejad laevanduses. Mõned näited: Taanis registreeritud laevadel on 10 protsenti kõigist maailma kaubandusest, Baltimeres on üks kõige rohkem paroomid. Lisaks heitkoguste, laevandus kahjustab keskkonda igasuguseid jäätmetega, reovee merre heidetud. Et piirata laevanduse reostust , alates aastast 2015 kehtestati uued reegleid, nõudes, et laevad, vähendavad nende väävli oksiidid 1st protsendi lubatud täna kuni 0,1%. Lähiaastatel eeldatav kehtestamine regulaator seoses heitkogustega lämmastikoksiidide. Need nõuded sunnivad laevaomanikele kasutada kallimad kütuse tuubid. Üks lahendus on üleminek vähem saastavate kütuse, naiteks veeldatud maagaasi ( ). Laevadelt pärit heitkoguseid, mis kasutavad veeldatud maagaasi, praktiliselt ei sisalda mingit väävli ja lämmastiku, sisaldavad vähem süsinikdioksiidi, vähendades sellega kokku heitkoguseid ligikaudu 15%.
Keemiliselt väga püsiv, nõrk elektrolüüt, happeliste ja aluseliste omadustega => reageerib mõlemat tüüpi oksiididega: Li2O + H2O => 2LiOH SO2 + H20 => H2SO3 Aktiivsete metallide suhtes käitub oksüdeerijana, eraldub vesinik. 2. Vesinkperoksiid (H202) Ebapüsiv, esineb ainult lahusena vees. Tugev oksüdeerija, kasutatakse pleegitamisel. 2-3% (kanged) lahused võivad nahale tekitada söövitushaavu. Päikese valguse käes laguned kiiresti, eraldub monohapnik: H2O2 => H2O + O 3. Oksiidid: Aktiiveste metallide oksiidid on aluselised, reageerimisel veega tekivad leelised. Vähemaktiivsete metallide oksiidid on vähem aluselised ei reageeri veega, võivad reageerida hapete lahustega, osa neist on amfoteersed, võivad reageerida leelistega. Enamiku mittemetallide oksiidid on happelised, veega reageerides moodustavad vastavaid happeid, erandiks on SiO2, mis on polümeerse struktuuriga ja vees praktiliselt ei lahustu, vastav hape on H2SiO3.
Aineklassid Oksiidid: Nimetused: Metallioksiidid kasutatakse o.a.-sid. Kui metall asud1A 2A 3A rühmas siis o.a.-d ei öelda Mittemetalli oksiiditel kasutatakse eesliiteid. 1-mono 2-di 3-tri 4-tetra 5-penta 6-heksa 7-hepta 8-okta 9-nona 10-deka Aluselised oksiidid on oksiidid, mis reageerivad hapetega, moodustades soola ja vee. Hapetega reageerivad Veega reageerivad Happeliste oksiididega reageerivad Happelised oksiidid on oksiidid, mis reageerivad alustega, moodustades soola ja vee. Alustega reageerib Veega reageerib Aluseliste oksiididega reageerib. Amfoteersed oksiidid - On oksiidid, mis võivad reageerida nii hapeet kui ka alustega( kuid reaalselt astuvad reaktsioonidesse vaid ekstreemsetes tingimustes) ; ei reageeri veega. Tähtsamad: Al2O3 , ZnO , Cr2O3 Kui on mitu erinevat metalli seotud happejäägiga siis neid üheneid nimetati kompleks ühendiks.
Fosfor-P (kr.k. phosphoros valguskandja) FOSFOR Keemiline sümbol: P Järjekorra nr. : 15 Massiarv: 30,9738 Allotroobid: valge, punane ja must fosfor Stabiilseim o.-a. : +5, lisaks ka +3 ja -3 Valge fosfor helendub Leidumine looduses ja saamine Leidub ainult ühenditena fosfaadid ja apatiidid Põhiosaks kaltsiumfosfaat Ca3(PO4)2 apatiit fosforiit Allotroopia Erinevad üksteisest tunduvalt Üle 10 erineva allotroobi Tähtsaid allotroope on kolm VALGE FOSFOR tetraeedrilised molekulid P4 alles 1000oC juures molekul laguneb PUNANE FOSFOR Pikad ahelakujulised molekulid Tuntud 7 erinevatvormi Levinuim amorfne punane fosfor MUST FOSFOR Kõige püsivam ja vähemaktiivsem Vähelevinud Saadakse valge fosfori kuumutamisel kõrgel temperatuuril OMADUSED Valge fosfor Keemiliselt väga aktiivne Õhus kergesti isesüttiv Pimedas helenduv Säilitatakse ja lõigatakse veekihi all Küüsl...
Oksiidid. · Oksiidid on liitained, mis koosnevad kahest elemendist, millest üks on hapnik. · Oksiidid on elemendi ühendid hapnikuga. · Oksiide liigitatakse: 1. happelised S03 3. amfoteersed Al203 2. aluselised K20 4. inertsed (neutraalsed) CO · Oksiididele nimetuste andmine: 1. IA, IIA ja IIIA rühma metalli oksiididele nimetuse annan järgmiselt: Nimetan metalli ja lisan sõna oksiid K20 - kaaliumoksiid 2. Mittemetallioksiidide nimetused annan eesliidetega:
Seosed anorgaaniliste ainete põhiklasside vahel 1. Kontrolli, kas oskad selgitada küsimustes toodud mõisteid ja teema teoreetilist tausta. 2. Kuidas liigitatakse oksiide keemiliste omaduste järgi? Tooge näited (kirjutage nii valem kui ka nimetus).--------1)aluselised oksiidid: CaO-kaltsiumoksiid 2)happelised oksiidid: SO₂- vääveldioksiid 3)amfoteersed oksiidid: Al₂O₃- alumiiniumoksiid 4)neutraalsed oksiidid: CO-vingugaas 3. Kuidas liigitatakse happeid a. vesiniku sisalduse, ------- Üheprootonilised: HBr-vesinikbromiidhape; Mitmeprootonilised happed: H₂SO₄-väävelhape b. hapniku sisalduse,--------hapnikhapped: H₂SO₄- väävelhape; Hapnikuta happed: HCl-vesinikkloriidhape c. tugevuse järgi?-------tugevad happed: HCl-vesinikkloriidhape; Nõrgad happed: H₂CO₃-süsihape Tooge igal juhul näited (kirjutage nii valem kui ka nimetus). 4
Leelis ja leelismuld metallid Leelismetallid IA rühm.väliskihi el.valem - ns², oksüd. aste 2. Leelismuldmetallid- IIA rühm(alates Ca) *nendel on omadus anda kuumutamisel leegile isel. värvus. Kuumutamisel ühendid lenduvad,nende aatomid ergastuvad ja üleminekul Madalamasse energiaga olekusse kiirgavad isel, värvusega valgust. Naatrium-kollane K-kahvatulilla Ca-punane Ba-heleroheline Leelis ja leelismuldmetallid (metalliline side) *pehmed ,kergesti lõigatavad *kerged *madal sulamis, temp *hea elektri ja soousjuht. *puhas metallpind on läikiv, hõbevalge värvusega. *reduts. Hapnikuga ja paljude teite metallidega. *reduts, veega mood vastava leelise ja tõrjudes välja happniku. *reduts tormiliselt hapetega,tõrjudes välja vesiniku. *tänavavalgustus Na aurudega täidetud lambid. Oksiidid Valged tahked ainet tugevate aluseliste omadustega. Reag veega mood leelise. Kustutamata lubi kaltsiumoksiid, kasutatakse Gaaside või vedelike kuivam...
(Happelise oksiidi sool 4 vesi reageerimisel tekib 2 NaOH + — Nazso, + HIC) oksiidile happe 4. happelinc Okiid aluseline cao + c02 — CaC03 oksiid 6 Nazo moo — 4 Nan, Oksiidi 5. aluseline oksiid + vesi Na20 + H20 2 NaOH reageerimine alus reageerivad vaid ja al CaO Ca-st oksiidid Cuo + H20 ei toimu Alusclise oksiidi 6. happcline oksiid + vesi —i C02* H20 — korral tekib alus, happelise korral hape. hape H2CO, soa + H.O H2S03 SO, + H20 HaS04 N20i+ H20 2 HN03
Oksiidid - ained, mis koosnevad kahest elemendist, millest üks osa on hapnik (oa II) Aluselised, amforteersed oksiidid on mittemolekulaarsed. Happelised, neutraalsed oksiidid aga molekulaarsed. Amfoteersed oksiidid oksiidid, millel võivad avalduda nii happelised kui ka aluselised omadused. Vähemaktiivsed metallid on need. Tavaliselt on o-a III, ehk alumiinium, raud, kroom, tsink (ZnO). Amfoteersed hüdroksiidid on vees lahustumatud, ehk veega nad ei reageeri. Neutraalsed oksiidid ei reageeri hapete, leeliste ega veega. Neutraalsed oksiidid on CO, NO, N2O. Hape aine, mis vesilahuses jaguneb vesinikioonides ja happe anioonideks. Happeid saab liigitada: 1) hapnikusisaldus (O või ei ole O) 2) prootonite arvu järgi (mitu H molekuli on [H; H2; H3]) 3) happe tugevuse järgi. Tugevad: väävelhape, lämmastikhape, soolhape, vesinikbromiidhape, vesinikjodiidhape Keskmised: fosforhape, väävlishape, vesinikfluoriidhape
Oksiidide keemilised omadused · Aluselised oksiidid reageerivad hapetega = sool ja vesi. · Aluselised oksiidid reageerivad veega = leelis. Veega reageerivad ainult aktiivsete metallide oksiidid (IA rühma ja IIA rühma metallid alates Ca) · Aluselised oksiidid reageerivad happeliste oksiididega = sool. · Happelised oksiidid reageerivad veega = oksiidile vastav hape. Veega ei reageeri SiO2. · Happelised oksiidid reageerivad alustega = sool ja vesi. · Happelised oksiidid reageerivad aluseliste oksiididega = sool. Hapete keemilised omadused · Reageerivad metallidega = sool ja vesinik Reag. < h2 · Reageerivad alustega = sool ja vesi · Reageerivad aluseliste oksiididega = sool ja vesi · Reageerivad sooladega = uus sool ja uus hape Reaktsioon toimub siis, kui tekib nõrgem hape või sade Kui tekib H2CO3, siis tekkemomendil laguneb ta veeks ja süsinikdioksiidiks · Lagunemine kuumutamisel = happeline oksiid ja vesi
: · mittemetallid(19)- S, P, O2, Cl2 jne · poolmetallid e. metallid(15)- Ge, As, Sb, Te, At jne · metallid (90); Al, Au, jne b. Liitained- koosnevad mitme elemendi aatomitest: 1. Oksiidid- on ained, mis koosnevad kahest elemendist, millest üks on hapnik (oksüdatsiooniaste -II). Oksiid on hapnik (o.-a. II) ja mingi teise keemilise elemendi ühend. a. Aluselised oksiidid oksiidid, mis reageerivad hapetega, moodustades soola ja vee. Aluseliste oksiidide hulka kuulub enamik metallioksiide (nt. CaO, Na 2O, FeO jt.). b. Happelised oksiidid oksiidid, mis reageerivad alustega, moodustades soola ja vee. Happeliste oksiidide hulka kuulub enamik mittemetallioksiid (nt. CO 2, SO2, SO3) c
Kordamisküsimused kontrolltööks nr.2. Teema: Aineklassid 1. Mis on oksiidid, hüdroksiidid (alused), happed, soolad? Oksiidid-ained,mis koosnevad kahest elemendist,millest üks on hapnik.Oksiide liigitatakse keemiliste omaduste põhjal( aluselised,happelised,amfoteersed,neutraalsed) Hüdroksiidid(alused)-on ained,mis annavad lahusesse hüdroksiidioone.Tüüpilised alused on hüdroksiidid. Happed-on ained,mis annavad lahusesse vesinikioone.Happed koosnevad vesinikioonidest ja happeanioonidest. Soolad-on kristalsed ained,mis koosnevad katioonidest ja anioonidest. 2
Aineklassid Sisukord Aineklassid Oksiidid Happed Alused Soolad Tuntumad ained Millest saab mis? Aineklassid Hape Oksiidid (happeline, aluseline) Sool Alus Oksiidid Oksiid on kahes elemendist koosnev ühend, millest üks on hapnik. Oksiidid jagunevad Happeline oksiid Aluseline oksiid Hapetele vastavaid oksiide Aluseline oksiid on alusele nimetatakse happelisteks (hüdroksiidile) vastav oksiid. oksiidideks. Enamasti on Happelised oksiidid mitte- metallioksiid. Oksiide nimetatakse a)Oksüdatsiooniastme kaudu b)Eesliidete järgi Haped Haped on liitained, mis annavad lahusesse. vesinikioone.
Anorgaanilised ained oksiidid hüdroksiidid happed soolad Oksiidid Oksiidid liitained, mis koosnevad kahest elemendist, millest üks on hapnik koostise järgi liigitatakse oksiide · metallioksiidideks (FeO, Al2O3) · mittemetallioksiidideks ( CO2, P2O5) omaduste järgi liigitatakse oksiide · happelisteks (SO2, CO2, P4O10 jne.) · aluselisteks (Na2O, Fe2O3, MgO jne.) · amfoteerseteks (Al2O3,ZnO) Aluselised oksiidid on moodustunud metalliaatomitest ja hapniku aatomitest Reageerivad hapetega moodustades soola ja vee Nimetuste andmisel lisatakse metalli nimetusele sõna "oksiid", muutuva o.a.ga metalli puhul näidatakse sulgudes metalli o.a. või kasutatakse eesliiteid, näiteks: · Na2O naatriumoksiid · FeO raud(II)oksiid · Fe2O3 raud(III)oksiid ehk diraudtrioksiid Happelised oksiidid on enamasti mittemetallioksiidid.
OKSIIDID - Ühendid, mis koosnevad kahest elemendist, millest üks on hapnik Oksiide saadakse: Lihtainete vaheline reaktsioon 2Mg + O2 -> 2MgO CH4 + 2O2->CO2 + 2H2O Hüdroksiidide ja karbonaatide kuumutamisel MgCO3 --to> MgO + Co2 OKSIIDIDE LIIGITUS - Oksiide saab liigitada aluselisteks, happelisteks ja amfoteerseteks ning neutraalseteks oksiidideks (happelisust, ega aluselisust üldse ei avaldu) ALUSELINE OKSIID - Oksiid, mis reageerib hapega NB! Kõik aluselised oksiidid on mittemolekulaarsed. Tugevalt aluselised oksiidid reageerivad aktiivselt veega, nõrgalt aluselised oksiidid veega ei reageeri. HAPPELINE OKSIID - Oksiid, mis reageerib alusega Suurem osa tuntumaid happelisi oksiide on molekulaarsed, kuid nende seas on ka mittemolekulaarseid aineid(nt SiO2 ja CrO3). Happeline oksiid + alus = sool + vesi SO2 + 2NaOH -> Na2SO3 + H2O Happeline oksiid + vesi = vastav hape P4O10 + H2O -> 4H3PO4
Proovi KT Nimi: Sinu punktid /10p Kuupäev: 1. Mis on oksiidid? (1p) 2. Lõpeta lause: happeline oksiid + alus = . (0,5p) 3. Mis tingimustel reageerivad veega aluselised oksiidid? (alati/ainult tugevad/ainult nõrgad/mitte üldse) (0,5p) 4. Mis on keemiline sool? (1p) 5. Millised on happelised oksiidid? (1p) 6. Nimeta järgmised ühendid. (3p) a. Na2O b. MgSO3 c. HNO3 7. Lõpeta ja tasakaalusta reaktsioonid (3p) a. H2SO4 + MgO → b. Vesinikkloriidhape + naatriumhüdroksiid → c. Kaalium → kaaliumoksiid Boonus: (1,5p)
4)B-rühmade metallidel o.a. tavaliselt muutuv, sagedasti esineb o.a. II 5)Mittemetallide o.a.-d muutuvad vahemikus ,,rühma nr" (maks) kuni ,,rühma nr 8" (min) 6)Hapnikul alati II, vesinikul alati I II. Anorgaaniliste ainete põhiklassid: Anorgaanilised ained Liitained ehk keemilised ühendid Lihtained Metallid Mittemetallid Oksiidid Happed Alused Soolad 2. Oksiidid ained, mis koosnevad kahest elemendist, millest üks on hapnik V -II N2 O5 a) Saamine: 1) Lihtaine põlemisel (2H2 + O2 2H2O) 2) Liitaine põlemisel (CH4 + O2 CO2 + H2O) 3) Liitainete lagunemine (CaCO3 CaO + CO2) b) Aluselised oksiidid (AlOks) oksiidid, mis reageerivad hapetega, moodustades soola ja vee
Harjuta ( oksiidi valemi koostamiseks kasuta aatomi väliskihi elektronide arvu, vaadates tabelist A-rühma nr- sellest tulenes elemendi aatomi oksüdatsiooniaste ühendis) S+O2-> P+O2-> 2. Orgaanilised ained oksüdeeruvad (põlemine, hingamine) süsihappegaasiks ja veeks CH4+ 2O2->CO2+2H2O metaani ehk maagaasi põlemine C6H12O6+6O2->6CO2+6H2O hingamine, glükoosi oksüdatsioon rakkudes Harjuta C3H8+O2-> 3. Happelised oksiidid (mittemetallide oksiidid) reageerivad veega ja tekib hape. SO2, SO3 ja NO2 põhjustavad orgaaniliste kütuste põlemisjääkidena happesademeid. SO2+H2O->H2SO3 SO3+H2O->H2SO4 NO2+H2O-> HNO2+HNO3 Harjuta (vaata tabelist happejääke, et moodustada hapete valemid; elemendi oksüdatsiooniaste oksiidis ja happes on ühesuurune) CO2+H2O->…………….. süsihape P2O5+H2O->…………………fosforhape N2O5+H2O->……………….
Hape -aine, mis annab lahusesse vesinikioone. (H2SO4 - väävelhape) Sool kristalne aine, mis koosneb (aluse)katioonist ja (happe)anioonist. ( NaCl - naatriumkloriid) Hüdroksiid anorgaaniline ühend,, mille koostisse kuuluvad hüdroksiidioonid OH- . (LiOH liitiumhüdroksiid) 2. Oksiide saab liigitada: a)aluselised oksiidid(reageerivad hapetega) Li2O liitiumoksiid b)happelised oksiidid(reageerivad alustega) CO2 süsinikdioksiid c)amfoteersed oksiidid - Al2O3 alumiiniumoksiid d)neutraalsed oksiidid - CO süsinikoksiid. 3. a)K2SO3 sool b)Ni lihtaine, metall c)Na2O oksiid d)Cu(OH)2 alus e) HNO3 hape f)S8 lihtaine, mittemetall g) ZnO oksiid h)CaHPO4 sool 4. a)CuOH vask(I)hüdroksiid b)Cl2O7 dikloorheptaoksiid c)HNO2 lämmastikushape d)FeSO4 raud(II)sulfaat e)K2S dikaaliumsulfiid f)CaO kaltsiumoksiid 5. a) hape + alus sool + vesi (neutralisatsioonireaktsioon) Hcl + NaOH NaCl + H2O
Harjuta ( oksiidi valemi koostamiseks kasuta aatomi väliskihi elektronide arvu, vaadates tabelist A-rühma nr- sellest tulenes elemendi aatomi oksüdatsiooniaste ühendis) S+O2-> P+O2-> 2. Orgaanilised ained oksüdeeruvad (põlemine, hingamine) süsihappegaasiks ja veeks CH4+ 2O2->CO2+2H2O metaani ehk maagaasi põlemine C6H12O6+6O2->6CO2+6H2O hingamine, glükoosi oksüdatsioon rakkudes Harjuta C3H8+O2-> 3. Happelised oksiidid (mittemetallide oksiidid) reageerivad veega ja tekib hape. SO2, SO3 ja NO2 põhjustavad orgaaniliste kütuste põlemisjääkidena happesademeid. SO2+H2O->H2SO3 SO3+H2O->H2SO4 NO2+H2O-> HNO2+HNO3 Harjuta (vaata tabelist happejääke, et moodustada hapete valemid; elemendi oksüdatsiooniaste oksiidis ja happes on ühesuurune) CO2+H2O->................. süsihape P2O5+H2O->.....................fosforhape N2O5+H2O->...................
Keemia kordamisküsimused 9.klassile 1.Aineklassid ja nendevahelised seosed OKSIIDID-koosnevad kahest elemendist, millest üks on hapnik (O). Oksiidide liigitus:1) Aluselised oksiidid-metalli oksiidid: # tugevalt aluselised, ( leelis ja leelismuld metallid IA ja IIA alates Ca metallide oksiidid) # nõrgalt aluselised oksiidid- vähem aktiivsete metallide oksiidid. 2) Happelised oksiidid-mitte metallide oksiidid. Keemilised omadused: happeline oksiid + vesi = vastavhape ! Veega ei reageeri SiO N: dilämmastikpentaoksiid + vesi happeline oksiid + alus = sool +vesi HAPPED-ained, mis annavad lahusesse vesinikioone. Hapete liigitus erinevate tunnuste järgi:1) Hapniku sisalduse järgi: # hapniku mittesisaldavad happed N: # hapnikhapped N: 2) Prootonite arvu järgi: # üheprootonilised happed N: # mitmeprootonilised happed N: 3) Tugevuse järgi: #
Keemia kordamisküsimused 9.klassile põhikool 1.Aineklassid ja nendevahelised seosed OKSIIDID-koosnevad kahest elemendist, millest üks on hapnik (O). Oksiidide liigitus:1) Aluselised oksiidid-metalli oksiidid: # tugevalt aluselised, ( leelis ja leelismuld metallid IA ja IIA alates Ca metallide oksiidid) # nõrgalt aluselised oksiidid- vähem aktiivsete metallide oksiidid. 2) Happelised oksiidid-mitte metallide oksiidid. Keemilised omadused: happeline oksiid + vesi = vastavhape ! Veega ei reageeri SiO N: dilämmastikpentaoksiid + vesi happeline oksiid + alus = sool +vesi HAPPED-ained, mis annavad lahusesse vesinikioone. Hapete liigitus erinevate tunnuste järgi:1) Hapniku sisalduse järgi: # hapniku mittesisaldavad happed N: # hapnikhapped N: 2) Prootonite arvu järgi: # üheprootonilised happed N: # mitmeprootonilised happed N: 3) Tugevuse järgi: #
HSO + NaO NaSO + HO 3) Hape + metall sool + vesinik HNO + Na NaNO + H 4) Hape + sool hape + sool CaCO + HCl CaCl + HCO Tingimused: *Tekib nõrgem või lenduvam hape *Tekib sade Oksiidid Oksiidid koosnevad mittemetallist või metallist ja hapnikust (O). Jagunevad samuti kaheks: 1) Aluselised oksiidid: metall + O 2) Happelised oksiidid: mittemetall + O Nimetamine: Happelised: Aluselised: 2 di Kui metall on 1., 2. või 3. A rühmas, siis 3 tri metalli nimi + ,,oksiid" 4 tetra 5 penta Kui metall asub mujal, siis 6 heksa metalli nimi(metalli oksüdatsiooniaste) + ,,oksiid" 7 hepta 8 okta 9 nona 10 deka Reaktsioonivõrandid:
koostise püsivuse seadus, ruumalaliste suhete seadus,Avogadro seadus. 5. Keemiline side, sideme pikkus. Keemilise sideme tüübid: Kovalentne side (polaarne ja mittepolaarne), iooniline, metalliline, vesinikside ja doonor- aktseptorside). Aine omaduste sõltuvus keemilise sideme tüübist. 6. Ainete liigitus: Liht- ja liitained. Anorgaaniliste ühendite põhiklassid: Oksiidid ja nende liigitus. Happelised oksiidid, happevihmad. Happed ja nende liigitus, pH lahustes. 7. Hüdroksiidid, nende liigitus ja keemilised omadused. Soolad, liigitus ja keemilised omadused. Anorgaaniliste ühendite nomenklatuur. 8. Protsentarvutuse põhitüübid: lahjendamine, kontsentreerimine, tihedus. 9. Elementide keemia: IA rühma elemendid, levik looduses, ühendite
OKSIID- hapniku ja mingi teise keemilise elemendi ühend 1A, 2A ja 3A rühmas nimetuses metalli nimi+oksiid B rühmas või teistes A rühmades nimetuses metalli nimi (rooma nr metalli o-a) +oksiid Mittemetallioksiid nimetuses eesliited 2-di 3-tri 4-tetra 5-penta 6-heksa 7- hepta 8-okta 9-nona 10- deka Happelised oksiidid (mittemetallioksiid)- SO2-vääveldioksiid CO2- süsinikdioksiid Aluselised oksiidid (enamasti metalloksiidid) Tugevalt aluselised (IA;Ca, Sr, Ba, Ra) Reageeriva veega ja tekib vastav alus - K2O-kaaliumoksiid Nõrgalt aluselised (enamik ülejäänud metallidega) Veega ei reageeri, vastavad alused lagunevad kuumutamisel oksiidideks – Fe(OH)3=Fe2+H2O Amfoteersed oksiidid (osa metallioksiide) – ZnO-tsinkoksiid ja Al2O3- alumiiniumoksiid Ei reageeri veega, vaid hapete ja alustega Inertsed ehk neutraalsed oksiidid (osa mittemetallioksiide)