hemoglobiiniga . Veri kaotab hapniku sidumise ja edasikandmise võime ning inimene võib lämbuda. 15. Süsinikoksiidi tekkimine( võrrand ) 2C+O22CO 16. Süsinikoksiidi omadused ja tekkimine . ( 3 võrranidt) CO2 on 1) Värvitu 2) Nõrga hapuka lõhna ja maitsega 3) Vees hästi lahustuv 4) Õhust 1.5 korda suurema tihedusega gaas CO2 on süsiniku tähtsaim oksiid,mis tekib süsiniku ja igasuguste süsinikuühendite põlemisel hapniku külluses. C+O2CO2 CH4+2O2CO2+2H2O CO2 tekib ka karbonaatide lagunemisel kõrgel temperatuuril . CaCO3CaO+CO2 17. Mis tekib süsinikoksiidi lahustamisel vees ? CO2 on happeline oksiid. Selles lahustumisel vees tekib nõrk ja ebapüsiv süsihape H2CO3 (võrrand) CO2+H2O H2CO3
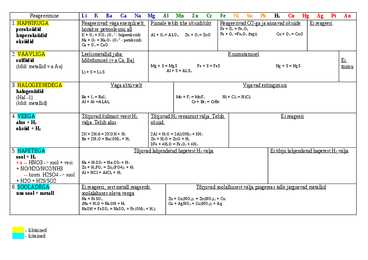
halogeniidid (Hal -1) Ba + I2 = BaI2 Mn + F2 = MnF2 Ni + Cl2 = NiCl2 (kõik metallid) Al + At =Al3At3 Cr + Br2 = CrBr 4. VEEGA Tõrjuvad külmast veest H2 Tõrjuvad H2 veeaurust välja. Tekib Ei reageeri alus + H2 välja. Tekib alus. oksiid. oksiid + H2 2K + 2H20 = 2KOH + H2 2Al + H2O = 2Al(OH)3 + 3H2 Ba + 2H2O = Ba(OH)2 + H2 Zn + H2O = ZnO + H2 3Fe + 4H2O = Fe3O4 + 4H2 5. HAPETEGA Tõjuvad lahjendatud hapetest H2 välja Ei tõrju lahjendatud hapetest H2 välja sool + H2 v
Fosfor-P (kr.k. phosphoros valguskandja) FOSFOR Keemiline sümbol: P Järjekorra nr. : 15 Massiarv: 30,9738 Allotroobid: valge, punane ja must fosfor Stabiilseim o.-a. : +5, lisaks ka +3 ja -3 Valge fosfor helendub Leidumine looduses ja saamine Leidub ainult ühenditena fosfaadid ja apatiidid Põhiosaks kaltsiumfosfaat Ca3(PO4)2 apatiit fosforiit Allotroopia Erinevad üksteisest tunduvalt Üle 10 erineva allotroobi Tähtsaid allotroope on kolm VALGE FOSFOR tetraeedrilised molekulid P4 alles 1000oC juures molekul laguneb PUNANE FOSFOR Pikad ahelakujulised molekulid Tuntud 7 erinevatvormi Levinuim amorfne punane fosfor MUST FOSFOR Kõige püsivam ja vähemaktiivsem Vähelevinud Saadakse valge fosfori kuumutamisel kõrgel temperatuuril OMADUSED Valge fosfor Keemiliselt väga aktiivne Õhus kergesti isesüttiv Pimedas helenduv Säilitatakse ja lõigatakse veekihi all Küüsl...
Cr-Kroom Kelli Hinn 11.L Ehitus ja asetus PS-s Keemiliste elementide perioodilisuse süsteemi VI rühma element. Järjenumber on 24 Aatommass 51,996 24 prootonit ja elektroni , 28 neutronit ning 4 elektronkihti, mis jagunevad +24 2)8)13)1) „Chrom“, Tomihahndorf, CC0 Füüsikalised omadused Tihedus 7,14 g/cm3 Sulamistemperatuur 1857oC Keemistemperatuur 2482 oC Metalläige Hea elektri- ja soojusjuhtivus Hõbevalge, sinika helgiga Lõhnatu ja maitsetu Tähtsamad ühendid ja kasutusalad kroom (III)oksiid Cr2O3 -kasutatakse telliste vooderdiseks tööstuslikes kõrgtemperatuuriahjudes ja metallide, sulamite ja keemiliste ühendite valmistamiseks. kaalium(III)sulfaatdodekahüdraat KCr(SO4)2.12H2O kroom(VI)oksiid CrO3 -metallviimistlusel ja katalüsaatorina. kroom(VI)hape H2CrO4 dikroom(VI)hape H2Cr2O7 kromaadid- metallpindade töö...
Ühinemisreaktsioonis liituvad omavahel kaks (või ka enam) ainet, moodustades uue aine. Sellega kaasneb enamasti energia eraldumine. Lagunemisreaktsioonis üks aine laguneb kaheks (või enamaks) aineks enamasti aine kuumitamisel Neutralisatsioonireaktsioon on happe ja aluse vaheline reaktsioon, kus saaduseks on sool ja vesi, sellega kaasneb soojuse eraldumine. 7. Reaktsioonivõrrandite kirjutamine. Ühinemisreaktsioon: metalli oksiid + vesi => hüdroksiid NB: Lagunemisreaktsioon: alus => oksiid + vesi Neutralisatsioonireaktsioon: alus + hape => sool + vesi 8. Mis on lahuse pH ja mida see näitab? pH on eriline suurus, mis iseloomustab lahuse aluselisust ja happelisust. 9. Nimeta indikaatoreid ja nende värvuseid happelises ja aluselises keskkonnas. lakmuselahus (lilla)- happelises keskkonnas punane, aluselises keskkonnas sinine.
jaotunud nimetatakse ebaühtlasteks sulamiteks (malm).9. Elavhõbedasulameid nimetatakse amalgaamideks.10.kõige enam kasutatakse edutseerijana süsinikku,süsinikoksiidi.11.Malm on habras ja raskesti töödeldav.Malmist tehakse nt kütteradiaatoreid,pliidiraudu jm.Teras on malmiga võrreldes oluliselt paremini töödeldav ja mehhaaniliselt vastupidavam.Ka teras sisaldab süsinikku,kuid vähem kui malm kuni2%.12.särdamine ehk kuumutamine. Sulfiid oksudeerub, tekib vastava metalli oksiid ja eladub SO2- 2PbS+3O2--2PbO+2SO2.13.maagi tööt. Etapid: maak-rikastatud maak-metalli oksiid- metall.Rikastamine,säradmine(ülevalO2), redutseerimine ül redutseerija.14:Üks tähtsamid eeliseid on see, et metallid on kergesti töödeldavad, nad on plastilised.15.Korrosioonitõrje võimalused:a.metalli isoleerimine väliskeskkonnast kaitsekihiga,b.metalli kaitsmine emaili-,värvi-või lakikihi abil,c.metallin kaitsmine korrosioonikindlamast metallist kaitsekihiga.16.metalli korrosiooni
spiraalsed antiferromagnetic riik, kus kõik aatomi hetk eriti basaal Lennuk Kiht on paralleelsed ja suunatud kindlaksmääratud nurga hetked kõrval kihid. See ebatavaline antiferromagnetism muundub korrastamata (paramagnetilise) riigi-230 K. Keemiline Kõige tavalisem Valence seisundi terbium on 3, nagu Tb 2 O 3. Kõige tavalisem Valence seisundi terbium 3., Nauvo Tb 2 O 3. 4 olek on tuntud TBO 2 ja TbF 4. [5] [6] Terbium põleb kergesti moodustada segatud terbium (III, IV) oksiid: 4 olek kohta Tuntud TBO 2 ja TbF 4. [5] [6] Terbium põleb kergesti moodustada segatud terbium (III, IV) oksiid: 8 Tb + 7 O 2 2 TB 4 O 7 8 Tb + 7 O 2 2 TB 4 O 7 Lahuses, terbium moodustab ainult trivalentset ioone. Lahuses, terbium moodustab Ainult trivalentset ioone. Terbium on üsna electropositive ja reageerib aeglaselt külma veega ja väga kiiresti, kuuma vett vormi terbium hüdroksiid: Terbium kohta üsna electropositive ja
Cr2O3 kasutatakse rohelise värvipigmenina ja poleerpulbrite koostisosana. CrO3 [kroom(VI)oksiid] on punakas-oranz niiskust imav tahke aine. Ta on väga tugev oksüdeerija CrO3 on happeliste omadustega ning selle veega reageerimisel tekib kroom- või dikroomhape. CrO3 kasutatakse m CrO3 e elektrokeemilisel kroomimisel. Orgaaniliste ainete kokkupuutel CrO3-ga need süttivad põle CrO3 eetõttu on CrO3 ka väga sööbiv nahale, sellest tekivad haavandid. CrO [kroom(II)oksiid] on aluseline oksiid. Ta on must tugev redutseerija. CrO reageerib ainult hapetega. CrO2 (kroomdioksiid) on segaoksiid. Seda kasutakse magnetofoni- ja videolintide valmistamiseks. Kroom(VI)oksiidile vastavad happed on kroomhape (H2CrO4) ja dikroomhape(H2Cr2O7). Hapete soolad on kromaadid ja dikromaadid. Kromaadid on püsivad leelilises keskkonnas. Nad on tugevad oksüdeerijad. Kromaate kasutatakse nahatööstuses,korrosioonitõrjeks ja puidu konservandina(muudavad puidu püsivaks
3) alus.oksiid + hape = sool + vesi MgO + 2HCl = MgCl2 + H2O 4) hap.oksiid + alus = sool + vesi SO3 + Ca(OH)2 = CaSO4 + H2O 5) hap.oksiid + alus.oksiid = sool CaO + CO2 = CaCO3 6) alus.oksiid alus hap.oksiid hape Li2O + H2O = 2LiOH N2O5 + H2O = 2HNO3 IV REAGEERIMINE VEEGA aktiivsed metallid reageerimisel tekib hüdrokiidioon + H2 kekmiseaktiivsusega metallid reageerimisel tekib oksiid + H2 väheaktiivsed metallid ei reageeri veega V REAGEERIMINE HAPPEGA pingereas vesinikust paremal olevad metallid ei reageeri happega(v.a. HNO3) VI REAGEERIMINE SOOLADEGA metall reageerib vees lahustuva soolaga, kui on aktiivsem, kui soolas olev metall. m N V n= = = M N A Vm n moolide arv [mol] m aine mass [g] M aine molaarmass [g/mol] N osakeste arv [molekuli; aatomit jne
Kasutamine: *Teemantit: ehtetööstuses ja tehnoloogias, lõiketeradel *Sütt: kütusena (kivisöe, koksina) *Grafiit: elektroodina, kirjutusvahendina *Aktiivsütt: söetablett=adsorbent, söefilter Adsorbent-seob pinnaga Absorbent-seob sisse CO ehk vingugaas ehk süsinikoksiid Füüsikalised omadused:Värvitu, lõhnatu, õhuga u. ühe raskusega, vees lahustumatu, mürgine Keemilised omadused:*põleb 2CO+O2 > 2CO2 *reageerib metallioksiididega Fe2O3+3CO > 2Fe + 3CO2*neutraalne oksiid st. Reageerides veega ei moodusta hapet Kasutamine: metallide tootmisel e. metallurgias, väetiste tootmisel CO2 ehk süsihappegaas ehk süsinikdioksiid Füüsikalised omadused: Värvitu, lõhnatu, õhust poolteist korda raskem, tahkub -40kraadi juures, ei oma vedelat olekut, tahket CO2 nim. kuivaks jääks, vees vähesel määral lahustuv, lämmatav. Keemilised omadused: *happeline oksiid, millele vastab süsihape, vähesel määral gaseeritud jookides
10%-list lahust kasut. Meditsiinis , vedelat ammoniaaki kasutatakse külmikutes. Saamine: 1. Laboris saadakse ammooniumsoolast ja Ca- hüdroksiidist 2 NH4Cl + Ca(OH)2 -> 2 NH3 + 2 H2O + CaCl2 Tööstuses vesinikust ja lämmastikust t, rõhu ja katalüsaatori abil N2 + 3 H2 -> 2 NH3 Lämmastikoksiidid N2O Dilämmastikoksiid ( naerugaas ) nõrga meeldiva lõhnaga narkootilise toimega gaas. Ta on neutraalne oksiid NO Lämmastikoksiid on värvuseta mürgine gaas. Ta on ka neutraalne oksiid. Reageerib hapnikuga 2 NO2 + O2 -> 2NO2 Lämmastikdioksiid. NO2 lämmastikdioksiid on punakaspruun terava lõhnaga väga mürgine gaas. Reageerib veega NO2 + H2O -> HNO3 + HNO2 NO2 on tugev oksüdeerija . Paljud ained tema atmosfääris süttivad ( väävel , fosfor jt ) Ammooniumsoolad Saamine: ammoniaak + hape NH3 + HCl -> NH4Cl
jagunenud ioonideks happe molekule Väga aktiivsed ja sööbiva toimega jagunenud ioonideks H Cl H2 S H2 SO4 H2 CO3 H NO3 H3 PO4 CH3COOH Hapete saamine Enamik mittemetallioksiididest reageerib veega, andes happe HAPPELINE OKSIID + VESI HAPNIKHAPE Happeline oksiid VIoksiid, millele vastabVIkindel hape, S enamasti O3 + H2O H2 S O4 mittemetallioksiid SIVO2 + H2O H2 SIVO3 Happed reageerivad metallidega eraldub vesinik ja tekib sool METALL + HAPE SOOL + VESINIK 2Al + 6HCl 2AlIIICl3- + 3H2 2Al + 3H2SO4 Al 2III (SO4)3II- + 3H2 Cu + HCl reaktsiooni ei toimu, sest ... Cu + HCl reaktsiooni ei toimu,
CaO ehk kustutamata lubi Kaltsiumoksiid (keemiline valem CaO; triviaalnimetused kustutamata lubi, põletatud lubi) on laialdaselt kasutatav keemiline aine, kaltsiumi oksiid. Toidulisandina (happesuse regulaator) on aine koodiks E529. Füüsikalised omadused Kaltsiumoksiid on valge, hallikasvalge, kahvatukollane või kahvatuhall aine. Tööstuslikult toodetud kaltsiumoksiidil on rauasisalduse tõttu kollakas või pruunikas varjund. Kaltsiumioksiid on kristalne aine (kõva teraline mass või pulber). Struktuur on tahkkesendatud kuubiline. Molaarmass on 56,08 g/mol. Normaaltingimustel on ta tahke, sulamistemperatuur on 2572 °C (2845 K). Keemistemperatuur on
Na2S + 2HCl = 2NaCl + H2S Kui tekib sadenev sool, siis ei pea tekkiv hape olema nõrgem ega lenduvam. 4)sool + SOOL = uus sool + uus sool(üks ) (reageerivad soolad peavad olema vees lahustuvad) NaCl + AgNO3 = NaNO3 + AgCl 5) karbonaadid ja nitraadid lagunevad kuumutamisel CaCO3 = CaO + CO2 2NaNO3 = 2NaNO2 + O2 2Zn(NO3)2 = 2ZnO + 4NO2 + O2 2AgNO3 = 2Ag + 2NO2 + O2 Soolade saamine 1) Hape + metall =sool+H2 2) Hape+aluseline oksiid =sool+H2O 3) Hape + alus =sool+H2O 4) Hape + sool =sool+hape 5) Alus+happeline oksiid =sool+H2O 6) Alus+sool =sool+alus 7) Sool+metall =sool+metall 8) Sool+sool =sool+sool 9) Alusel.oksiid+happel.oksiid =sool 10) Metall + mittemetall =sool Soolade rahvapäraseid nimetusi · NaCl - keedusool · CaCO3 lubjakivi, marmor, kriit · NaHCO3 - söögisooda
Raud ehk Fe Aatomi ehitus: 26 Fe: 1s22s22p63s23p64s23d6 Fe oksuüdatsiooniaste ühendites on: II sel juhul loovutab raua aatom 2 elektroni väliskohi s-orbitaailt III-sel juhul loovutab raua aatom 2 elektroni väliskihi s-orbitaalilt ja 1 elektori 3d- orbitaalit Raua püsivam oksüdatsiooniaste on III, ebapüsivam II Levik looduses Kõigist melementidest on Fe levikult 4. Kohal, metallidest aga 2. Kohal Puhast (ehedat) rauda leidub looduses väga harva. Fe-aatom kuulub hemoglobiini koostisse. Hemoglobiin on valk, mis transpordib vere punalibledes hapnikku ja süsihappegaasi. Raua ühendid Fe2O3 raud(III)oksiid, pruun või punane rauamaak e. Hematiit. Hematiiti kasutatakse raua tootmiseks. Punase värvusega raud(III)oksiidi rauamennikut kasutataksekeedu- ehk rootsi värvides pigmendina (värvimullana). ...
jagunenud ioonideks happe molekule Väga aktiivsed ja sööbiva toimega jagunenud ioonideks H Cl H2 S H2 SO4 H2 CO3 H NO3 H3 PO4 CH3COOH Hapete saamine Enamik mittemetallioksiididest reageerib veega, andes happe HAPPELINE OKSIID + VESI HAPNIKHAPE Happeline oksiid VIoksiid, millele vastabVIkindel hape, S enamasti O3 + H2O H2 S O4 mittemetallioksiid SIVO2 + H2O H2 SIVO3 Happed reageerivad metallidega eraldub vesinik ja tekib sool METALL + HAPE SOOL + VESINIK 2Al + 6HCl 2AlIIICl3- + 3H2 2Al + 3H2SO4 Al 2III (SO4)3II- + 3H2 Cu + HCl reaktsiooni ei toimu, sest ... Cu + HCl reaktsiooni ei toimu,
üldarvu suhe. Mittepolaarne aine mittepolaarsetest molekulidest koosnev aine. Polaarne aine polaarsetest molekulidest koosnev aine. Iooniline aine ioonilise kristallivõrega aine, milles osakesed on seostunud ioonilise sidemega. Elektrolüüdi lahus juhib elektrivoolu. Lahuse elektrijuhtivus Hape keemiline aine, mis vesilahustes dissotsieerudes annab lahusesse vesinikioone ehk loovutab vesinikioone ekh prootoneid. Happeline oksiid hapnikhappele vastav oksiid, mis reageerib alustega. Tugev hape hape, mis dissotsieerub vees täielikult (HI; HClO4; HBr; HCl; H2SO4; HNO3). Nõrk hape hape, mis ei lahustu vees täielikult (H2CO3; H2S; H3PO4; HNO2; CH3COOH). Alus keemiline aine, mis vesilahustes dissotsieerudes annab lahusesse hüdroksiidioone; seob vesinikioone ehk prootoneid. Aluseline oksiid hüdroksiidile vastav oksiid, mis reageerib hapetega. Leelis vees hästilahustuv tugev alus (hüdroksiid): NaOH; KOH; Ca(OH)2; Ba(OH)2.
57) Elektrolüüt - aine,mis lahustumisel või sulamisel jaguneb täielikult või osaliselt ioonideks ja juhib elektrit. 58) Dissotsiatsioonimäär - on keemias dissotsieerunud molekulide arvu ja molekulide üldarvu suhe. 59) Polaarne aine - polaarsetest molekulidest koosnev aine. 60) Iooniline aine - ioonilise kristallvõrega aine, milles osakesed on seostunud ioonilise sidemega. 61) Hape - on aine, mis annab lahusesse vesinikioone. 62) Happeline oksiid - hapnikhappele vastav oksiid, reageerib alustega. 63) Tugev hape - on hape, mis dissotsieerub vees täielikult. 64) *Tuntuimad tugevad happed: HI, HClO4 , HBr, HCl , H2SO4 , HNO3. 65) Nõrk hape - on hape, mis ei lahustu vees täielikult. 66) Alus - aine, mis annab lahusesse hüdroksiidioone. 67) Aluseline oksiid - hüdroksiidile vastav oksiid, reageerib hapetega. 68) Leelis - vees hästi lahustuv tugev alus.1A ja 2A rühma elemendid.
55)Elektrolüüt on aine, mille vesilahus juhib elektrit. 56)Dissotsiatsioonimäär näitab lahuses olevat vahekorda ioonide ja molekulide vahel. 57) Mittepolaarsed ained omavad mittepolaarset kovalentset sidet. 58) Polaarsed ained omavad polaarset kovalentset sidet (näiteks H2O) 59)Ioonilised ained omavad ioonilist sidet. (näiteks NaCl) 60)Lahuse elektrijuhtivus on võime juhtida elektrit. 61)Hape on aine, mis annab lahusesse vesinikioone. 62)Happeline oksiid ehk mittemetallioksiid koosneb mittemetallist ja hapnikust.(NO) 63) Tugev happe lahuses on peamiselt vesinikioonid ja happeanioonid. Happe molekule seal praktiliselt pole . (HNO3, HCl, H2SO4) 64)Nõrk happe lahuses on ülekaalus happe molekulid ja väga vähe on vesinikioone ja happeanione.(H 2CO3, H2SO3, H2S) 65)Alus on aine, mis annab lahusesse hüdroksiidioone. 66)Aluseline oksiid ehk metallioksiid koosneb metallist ja hapnikust (CaO) 67)Leelis on vees lahustuv alus.
ALUMIINIUM GEIR RINDLA 2010 Alumiiniumi avastamine 1827. aastal sai saksa keemik Friedrich Wöhler metalli, mida keegi polnud kunagi näinud.Kuna uue metalli lähteaineks olid maarjalased (ladina keeles alumen), hakati metalli nimetama alumiiniumiks. Alumiiniumi keemilised omadused Järjenumber on 13 Massiarv on 27 Kõige püsivamates ühendites on o.-a. +3 Alumiiniumi oksiid on amfoteerne oksiid Asub IIIA rühmas ja 3. perioodis Amforteensuse tõttu reageerib leelistega, tõrjub välja vesiniku ja moodustab aluminaate Reageerib paljude lihtainete ja hapetega, hapetest tõrjub vesiniku, tekib sool Reageerides hapnikuga, tekib tema pinnale õhuke ja tihe oksiidikoht Alumiiniumi füüsikalised omadused Hõbevalge värvusega, läikiv Tihedus on 2,7 g/cm³ Sulamistemperatuur on 660 °C Keemistemperatuur 2519 ºC Peegeldab hästi valgust
Saamine Vesinik + mittemetall (halogeenid . väävel,...) 1a ja 2a rühma metal(metallioksiid) + vesi Metall + mittemetall 2 Fe + 3 Cl2 = 2 FeCl3 H2 + Cl2 = 2 HCl Ca + 2 H2O = Ca(OH)2 + H2 Metall + Hape (pingerida) Ca + 2 HCl = CaCl2 + H2 Vesi + happeline (enamasti mittemetalli) oksiid Na2O + 2 H2O = 2 NaOH Metall + soolalahus (pingerida) Fe + CuCl2 = CuCl2 + Fe H2O + SO3 = H2SO4 ei reageeri SiO2 Vees lahustumatuid hüdroksiide saadakse Alus + hape NaOH +HCl = NaCl + H2O Nõrga happe sool + tugev hape nõrga aluse sool + leelis Sool + Hape ( kui tekib kas: sade, gaas või nõrgem hape)
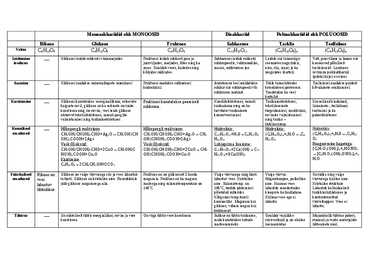
Monosahhariidid ehk MONOOSID Disahhariid Polüsahhariidid ehk POLÜOOSID Riboos Glükoos Fruktoos Sahharoos Tärklis Tselluloos Valem C5H10O5 C6H12O6 C6H12O6 C12H22O11 (C6H10O5)n (C6H10O5)n Leidumine Glükoosi leidub rohkesti viinamarjades Fruktoosi leidub rohkesti puu-ja Sahharoosi leidub rohkesti Leidub siis taimeriigis Vatt, puuvillane ja linane riie looduses juurviljades, marjades, õites ning ka suhkrupeedis, vahtrama...
KEEMIA Aatom-aineosake mis koosneb aatomituumast ja elektronidest;molekuli koostisosa Alus-aine mis annab lahusesse hüdroksiidioone Aluseline oksiid-hüdroksiid millel avalduvad nii alulised kui ka happelised omadused Anioon-neg. Laenguga aatom või aatomite rühmitus Elektronegatiivsus-suurus mis iseloomustab keemilise elemendi aatomi võimet keemilise sideme moodustamisel tõmmata enda poole ühist elektronpaari Elektronskeem-aatomi elektronkatte ehitust kirjeldav skeem mis näitab elektronide arvu elektronkihtides Hape-aine mis annab lahusesse vesinikioone Hapnikhape-hapniku sisaldav mineraalaine Hüdrooksiid-anorgaaniline ühen mille koostisesse kuuluvad hüdrooksiidioonid OH- või hüdroksiidrühmad OH Hüdrolüüs-aine keemiline reaktsioon veega:soola hürdolüüs on neutralisatsioonireaktsiooni pöördereaktsioon Ioon-laenguga aatom või aatomi rühmitus Iooni laeng-iooni positiivsete või negatiivsete elementa...
temperatuuril ei sütti. Kõige madalamal temperatuuril süttib süsi ja kõige kõrgemal temperatuuril teemant. Reaktsioon kulgeb sõltuvalt hapniku hulgast kahel eri viisil. Piisava hapniku hulga korral tekib süsiniku ja hapniku vahelise reaktsiooni tulemusena süsinikdioksiidHapniku vajakul tekib süsinikoksiid. Hapniku vajakul tekib süsinikoksiid A. Hapnikuga reageerimine (põlemine) süsinik on redutseerija. i. Täielik põlemine- tekib OKSIID, kus süsiniku aatomil ei ole maksimaalne osküdatsiooniaste. C + O2 C O2 Mittetäielik põlemine- tekib OKSIID, kus süsiniku aatomil ei ole maksimaalne oksüdatsiooniaste -II 2C + O2 2CIV O Vesinikuga reageermine- süsinik on oksüdeerija C + 2H2 C H4 II -II - IV I 2 Reageerimine
Radioaktiivne isotoop massiarvuga 26 tekib looduses kosmiliste kiirte mõjul. Alumiiniumi tihedus on 2.7 Mg/ kuupsentimeetrile. Sulamistemperatuur on alumiiniumil 660´C. Alumiinium reageerib paljude lihtainete ja hapetega. Hapetest tõrjub ta välja vesiniku ning tekib sool. Amfoteeruse tõttu reageerib alumiinium ka leelistega, tõrjudes nende lahustest vesinikku välja ja moodustades aluminaate. Kõigis püsivamates ühendites on alumiiniumi oksüdatsiooniaste +3. Alumiinium oksiid on amfoteeme oksiid. See tähendab,et tal on nii aluselisi kui ka happelisi omadusi. Alumiinium on vee ja õhu toimele vastupidav, sest tema pinnale tekib tihe oksüdatsioonikiht mis takistab alumiiniumi edasist oksüdeerumist. Alumiiniumi tootmine: Alumiiniumi tema kõrge aktiivsuse tõttu looduslikult teda ei leidu. Maakoore koostises on ta massi järgi hapniku ja räni järel kolmandal kohal. Alumiiniumi sisaldavad paljud kivimid ja mineraalid,
1. mangaani tähtsamad oksiidid, valem, värvus, lahustuvus vees, leelistes, hapetes jt omadused. Tuntakse järgnevaid stabiilseid mangaanoksiide: MnO (hallikas-roheline), Mn2O3 (pruunikas-must), MnO2 (pruunikas-must), Mn3O4 (pruunikas-must), Mn2O7 (rohekas või pruunikas vedelik). Leiduvad looduses mineraalidena v.a viimane neist. MnO2 ehk mangaandioksiid on praktikas tähtsaim mangaani oksiid ja levinuim Mn ühend looduses. MnO2 on tugev oksüdeerija, mis juba nõrgal kuumutamisel vesiniku atmosfääris redutseerub: MnO2 + H2 MnO + H2O. MnO2 oksüdeerib ka ammoniaaki: 6MnO2 + 2NH3 3Mn2O3 + N2 + 3H2O. MnO2 on amfoteerne oksiid. Sulatamisel leelistega õhuhapniku juuresolekul moodustuvad manganaadid(VI): 2MnO2 + 4KOH + O2 2K2MnO4 + H2O
12. CO2 ehk süsihappegaas ja CO ehk vingugaas on süsiniku oksiidid. CO on vees vähelahustuv värvuseta ja lõhnata väga mürgine gaas, mille sissehingamine võib lõppeda surmaga. CO kuulub neutraalsete oksiidide hulka, millele ei vasta hapet ega alust. CO2 on värvuseta õhust raskem gaas, mis tekib süsiniku ja enamiku orgaaniliste ühendite täielikul põlemisel. Süsihappegaasi tekib ka hingamisel, kõdunemisel, tööstusprotsessides. CO2 on happeline oksiid, reageerimisel veega moodustab ta ebapüsiva süsihappe. 13. . 14. . 15. Metallid on värvuselt hallikad, nad on tahked kõvad ained (erandid Hg, Au, Cu), kerge või raske kaaluga, sepistatavad, läikega ained. Metallid sulavad üpris madalatel või kõrgetel temperatuuridel, paljud metallid juhivad hästi soojust ja elektrit. 16. Metall+hapnik→oksiid Nt: Na+O2→Na2O 4Fe+3O2→2Fe2O3 Metall+mittemetall→sool Nt: Ca+Cl2→CaCl2 Zn+S→ZnS 17. Metall+hape
1-3 põhiliselt. Elektronide loovutamine ja liitmine: loovutavad kergesti elektrone: Me - ne => M n+ Võivad loovutada ka eelviimase kihi elektrone rühmanumbri järgi. Praktiliselt elektronide liitmist ei ole, tekivad alati positiivsed ioonid. 2. Keemilised omadused: 1. Metallide reageerimine lihtainetega (mittemetallidega) · Metallid reageerivad enamiku mittemetallidega kuumutamisel, sealjuures moodustuvad nn binaarsed ühendid, mille nime lõpus on alati -iid. O oksiid, N nitriid, Cl kloriid, C carbiid. · Aktiivsemate mittemetallidega (Cl) reageerivad kõik metallid, hapniku ja väävliga ei reageeri mõned metallid (pingerea lõpus), neid nim väärismetallideks. · Aktiivsemad metallid võivad põleda hapnikus ja klooris. · Võrrandid: Mg+O2 => 2MgO; 2Al + 3S = Al2S3 · Need protsessid on redoksreaktsioonid ( ainete o.-a muutub) · Metallide reageerimisel mittemetallidega metall oksüdeerub ja mittemetall redutseerub.
Keemia arvestuse kokkuvõte Aineosakesed- aatom,molekul,ioon. * keemiline element: kindla tuuma laenguga aatomite liik. * aatom: keemilise elemendi väiksem osake, molekuli koostisosa * molekulaarne aine: aine väiksem osake, koosneb aatomitest * molekul: koosneb omavahel seostunud aatomitest. Molekulideks liitumisel lähevad aatomid üle püsivasse olekusse, kus nende energia on madalam. * molekuli valem: näitab, millistest aatomitest molekul koosneb. * indeks: näitab sama elemendi aatomite arvu molekulis. * ioon: laenguga aatom (aatomite rühm) - positiivne ioon e. katioon tekib kui aatom loovutab väliskihilt elektrone - negatiivne ioon e. anioon tekib kui aatom liidab väliskihile elektrone * tihedus: ühikulise ruumalaga ainekoguse mass, põhi ühik kg/m kuubis. Ioonsed ained on tahked ained. Koosnevad kristallidest. Osad lahustuvad vees, osad mitte. Valemi kirjutamisel eespool on katioon, tagapool anioonid. La...
tugevate hapetega: S + O2 _ SO2 Na2SO3 + H2SO4 _ Na2SO4 + SO2 + H2O . SO2 on terava lõhnaga värvuseta mürgine gaas, mida mürgisuse tõttu kasutatakse keldrite, ladude jt hoidlate desinfitseerimiseks (mikroorganismide hävitamiseks). Põhiosa vääveldioksiidist kulub väävelhappe tootmiseks. Lisaks kasutatakse teda veel ka pleegitamisvahendina tekstiili- ja paberitööstuses, sest ta lagundab paljusid värvaineid..SO2 on happeline oksiid, kuna tema reageerimisel veega tekib väävlishape. Leelistega annab ta sulfiteid 2NaOH + SO2 _ Na2SO3 + H2O SO3- vääveltrioksiid ehk väävel(VI)oksiid, SO3 moodustub vääveldioksiidi oksüdeerumisel õhuhapniku toimel 2SO2 + O2 _ 2SO3SO3 on tavatingimustel kergesti lenduv vedelik. SO3 on väga tugev oksüdeerija, milles temaga kokkupuutel võivad paljud orgaanilised ained süttida. Tugeva happelise oksiidina ta reageerib veega SO3 + H2O _ H2SO4
7. Oksiidide lühiülevaade H2O – väga polaarne, hea lahusti, üsna püsiv, nõrk elektrolüüt H2O2 – vesinikperoksiid, ebapüsiv, pleegitav, söövitav P4O10 – püsivaim fosforoksiid, valge, tahke aine, happeline, gaasisegude kuivatamiseks SO2 – mürgine gaas, happevihmades 2SO 2 + O2 → 2SO3 + H2O → H2SO4 SO3 – lenduv vedelik, põleb, reageerib veega H2O + SO3 → H2SO4 NO – neutraalne oksiid, läbipaistev, mürgine, veega ei reageeri 2NO + O 2 → 2NO2 NO2 - punakas, mürgine gaas, reageerib veega 2NO2 + H2O → HNO3 + HNO2 N2O – naerugaas, neutraalne oksiid CO – vinngugaas, lõhnatu, värvitu, väga mürgine, neutaalne oksiid -> vees hapet ega alust ei moodusta CO2 – süsihappegaas, õhust raskem, värvitu, tekib täielikul põlemisel, õhus 0,03%, kuiv jää - tulekustutites
NH3Cl(t) -> NH3(g) + HCl (g) Lämmastiku hapnikuühendeid Lämmastikuoksiid NO on värvuseta mürgine gaas,mis vees praktiliselt ei lahustu ega veega ei reageeri 2NO+O2 -> 2NO2 Lämmastikdioksiid NO2 on punakaspruuni värvuse ja terava lõhnaga väga mürgine gaas. Lämmastikdioksiidis on lämmastiku o-a IV . Reageerimisel veega moodustav ta kaks hapet lämmastikhape ja lämmastikushappe : 2NO2 +H2O - > HNO3+HNO2 Dilämmastikoksiid N2O on neutraalne oksiid (nagu ka NO) . Ta on nõrga meeldiva lõhnaga värvuseta gaas, mis väiksemates kogustes sissehingamisel põhjustab elevust ( naerugaas ) suuremas hulgas tekitab aga narkoosi . NB! LÄMMASTIKHAPE POLE MITTE AINULT TUGEV HAPE,VAID ON KA VÄGA TUGEV OKSÜDEERIJA,SEEPÄRAST TULEB TEMA KASUTAMISEL HOOLIKALT JÄLGIDA OHUTUSNÕUDEID. Lämmastikhappe soolad - nitraadid lahustuvad vees hästi. Leelismetallide nitraatide kuumutamisel tekib vastav nitrit ( lämmastikushappe sool ) ja eraldub hapnik :
Titaan-Ti Avastamine: Titaani avastas 1791. aastal inglise keemik W. Gregor. Titaan on keemiliste elementide perioodilisussüsteemi IV rühma element. Titaani lühendiks on Ti ja kreeka keelne nimetus on Titanium. Tema järjekorra number on 22 ja aatommass on 47, 88. Looduslik titaan koosneb viiest stabiilsest isotoobist, mille massiarvud on 46 & 50. Titaan on hõbevalge, plastne, tugev ja korrosioonikindel metall. Ta on keskmise aktiivsusega metall. Tema sulamistemperatuur on 1668 kraadi C, keemistemperatuur on 3287 kraadi C ja tihedus 4,505 Mg/m3. Õhu toimel titaan ei oksüdeeru, sest tiheda ja vastupidava oksiidikihi tekkimise tõttu ta passiveerub. Kuumutamisel reageerib titaan halogeenide, vesiniku ja süsinikuga. Kasutamine: Titaan ja titaani sisaldavad sulamid on väga kuumus- ja korrosioonikindlad. Neid tarvitatakse konstruktsioonimaterjalina raketi- ja lennutööstuses, laevaehituses. Lisaks sellele kasut...
· baariumhüdroksiid Ba(OH)2 · kaaliumhüdroksiid KOH · mangaan(II)hüdroksiid Mn(OH)2 · liitiumhüdroksiid LiOH Aluste keemilised omadused: · Kõik alused reag. hapetega, tekib sool ja vesi: KOH+HCl=KCl+H2O · Kõik alused reag.happeliste oksiididega, tekib sool ja vesi: Ca(OH)2+CO2=CaCO3+H2O · Leelis reag.vees lahustuva soolaga,kui vähemalt üks saadustest on sade () Ba(OH)2+CuCl2 =BaCl2 +Cu(OH)2 () · Vees lahustumatud alused lagunevad kuumutamisel, tekib oksiid ja vesi Cu(OH)2 () = CuO + H2O Aluste saamine Leeliste saamine: · Leelis-või leelismuldmetalli reag. veega, tekib leelis ja vesinik 2 Na + 2 H2O = 2 NaOH + H2 · Tugevalt aluselise oksiidi reag. veega Na2O + H2O = 2 NaOH Lahustumatute aluste saamine: Vastava vees lahustuva soola reag. leelisega: CuCl2+2KOH=Cu(OH)2 +2KCl Lõpetage reaktsiooniõrrandid, mis toimuvad: 1) Raud(III)hüdroksiid+süsihape 2) Vääveldioksiid+kaltsiumhüdroksiid
tinatamisel, elektrolüüt süsinik-tsinkelemendis, meditsiinis rögalahtisti . NH4NO3 (ammooniumnitraat) väetis ja lõhkeaine komponent (NH4)2CO3 (ammooniumkarbonaat ehk põrdasarvesool) kasutatakse kondiitritööstuses kergitusainena taignas. Kuumutamisel ta laguneb, eraldades gaasilisi aineid, mis kergitavad küpsevat tainast // (NH4)2CO3 2NH3 + CO2 + H2O N2O - dilämmastikoksiid ehk lämmastik(I)oksiid ehk naerugaas Ta on värvuseta, neutraalne oksiid, nõrga meeldiva lõhnaga, vees lahustuv narkootilise toimega gaas. Väiksemates kogustes sissehingamisel põhjustab ta elevust ja lõbusat meeleolu. Suuremates kogustes kutsub ta esile valutunde kaotamise ja narkootilise une. Sel põhjusel on teda kasutatud ka lühiajalistel operatsioonidel ja sünnitustel valuvaigistamisel. Dilämmastikoksiidi saadakse NH4NO3 nõrgal kuumutamisel, kuid tekkiv N2O ei ole püsiv, sest ta laguneb kergesti lämmastikuks ja hapnikuks.
· Põhiosa tööstuslikult toodetavast lämmastikust kulubki ammoniaagi tootmiseks. · Lihtainena kasutatakse elektripirnides, vältimaks hõõgniidi läbipõlemist. · Vadelana kastutatakse aineta jahutamisel väga madala temperatuurini. · Oluline tooraine nitraatide ja teiste ainete saamisel, · Väetiste koostises Lämmastiku hapnikühendid Lämmastikoksiid · Värvuseta · Mürgine gaas · Vees praktiliselt lahusumatu · Ei reageeri veega · Neutraalne oksiid · Võib tekkida vastavate lihtainete omavahelisel reageerimisel väga kõrgel temperatuuril N2 + O2 2NO · Tööstuses saadakse NH3 katalüütilisel oksüdeerimisel 4NH3 + 5O2 4NO + 6H2O Lämmastikdioksiid · Punakaspruuni värvi · Terava lõhnaga · Väga mürgine gaas · Veega reageerides moodustab kaks hapet: 2NO2 + H2O HNO3 + HNO2 · Tugev oksüdeerija · Paljud ained võivad kokkupuutel atmosfääris põleda(fosfor, väävel)
b)IA
rühma või IIA(al.Ca)metallioksiidide reag.veega nt.CaO+H2O->Ca(OH)
Ca laeng on 2.
2 Ei tule H2-te.2)Raskl.aluste saamine:neid aluseid saadakse k
audsel meetodil,kui vastava metalli sool pannakse reag.leelisega.nt.2A
lCl3(sool)+3Ca(OH)2->2Al(OH)3down+3CaCl2.Keemilised omad:1)Alused
reag.hapetega ja saadusteks tekivad sool ja vesi(see on neut.reak.)alus+
hape->sool+vesi.Nt.Ca(OH)2+2HMnO4->Ca(MnO4)2+2H2O.2)Raskl
.alused lagunevad kuumutamisel,saadusteks on oksiid ja vesi nt.Cu(OH)
t'
2- ->CuO+H2O.Indik.-värvained,millel on erinevates keskkondades eri
nev värvus.Aluste indik.on lakmus-sinine,metü-oranz,fflillakasp.,univers
aalindik-rohekas.pH näitab vesinikioonide konsentratsiooni lahuses.Hap
peline keskkond pH<7,H+>OH-(H3PO4).Aluseline pH>7,H+
Räni on keemiline element järjenumbriga 14, mittemetall. Sümbol: Si (silicium) Aatommass on 28,086 Stabiilseid isotoope on 3, massiarvudega 28, 29 ja 30. Lihtainena on ta kerge tumehall metalse läikega kristalne aine. · Füs om: Sulamistemperatuur: 1417 ºC · Tihedus : 2330 kg/m³ Räni oksüdatsiooniaste ühendeis on valdavalt +4. Peamine oksiid on ränidioksiid. Räni ühendid vesinikuga,( silaanid,) on tugevad redutseerijad. Räni on pooljuht, mille elektrilised omadused sõltuvad väga tugevasti lisanditest. Räni kuulub silikaatide ja ränidioksiidi koostisse ning on telliste, tulekindlate materjalide, klaasi, portselani, tsemendi ja teiste materjalide koostisosa. Räni saamine Kuigi räni on maakoores hapniku järel kõige levinum element, puhtal kujul teda looduses ei esine
2) metallid reageerivad hapetega, tekib vastava metalli sool ja eraldub vesinik Fe + H2SO4 = FeSO4 + H2 Mg + 2HCl = MgCl2 + H2 3) aktiivsed metallid reageerivad veega (aktiivsuse tabeli punane ja roheline ei reageeri) 4) aktiivsed metallid( IA rühm + Ca, Sr, Ba) reageerivad veega moodustades tavatingimustel leelise ja vesiniku 5) keskmise aktivsusega metallid reageerivad kõrgel temperatuuril veeaurudega, saadusteks on vastava metalli oksiid ja vesinik 3Fe + 4H20 t Fe3O4 + 4H2 Zn + H2O t ZnO + H2 Metallidele iseoomuikud tunnused : Läige, sepistatavus, hea elektrijuhtivud, tihedus tavaiselt üle 1g/cm3, hallikas värvus 6) näide elektroonskeemist Al+13|2)8)3) 7) metallilised omdused rühmas ülevalt alla kasvavad sest et kihtide arv kasvab ja aatomi raadius kasvab 8) perioodis metallilised omadused vasakut paremale nüõrgenevad, sest et kasvab tummalaeng 9) A)kuidas reageerivad Na, Zn, Cu hapnikuga
Olustvere Teenindus- ja Maamajanduskool Loodusmajandus I Talvi Põldma LEESLISELISED AINED Referaat Olustvere 2010 Sisukord Alused Nimetuste määramine Liigitamine Saamine Keemilised omadused Kaltsiumhüdroksiid Kasutatud kirjandus Alused Alused ehk hüdroksiidid on ained, mis reageerivad hapetega ja annavad soola ja vee. (Tegelikult ei ole "alus" ja "hüdroksiid" kattuvad mõisted.) Alused koosnevad metallioonist ja hüdroksiidioonist. Alused on ained, mis liidavad prootoni (H+). Hüdroksiidid koosnevad metalliioonidest ja hüdroksiidioonidest (OH-). Hüdroksiidiooni laeng on -1, seega peab metalliioonide arv valemis olema alati 1 ja hüdroksiidioonide arv võrdub metalli ioonilaengu või oksüdatsiooniastmega. Kõikide hüdroksiidide valemid avalduvad kujul Men+(OH)n - n . Nimetuste määramine Kui metal...
Aine, mis annab lahusesse hüdroksiidioone OH-. Alused on näiteks: (NaOH, LiOH jne). Leelis- vees hästilahustuv tugev alus (Ca(OH)2, KOH JNE) Üldjuhul Ia rühm kaltsiumist alla poole. Sool- kristalne aine, mis koosneb aluse katioonidest ja happe aniooonidest. Näiteks: ( ZnCl2, ZnSo4, NaCl jne) Oksiid- liitaine, mis koosneb kahest elemendist ja millest üks on hapnik (o.-a. II). Näiteks: ( Li2O- liitiumoksiid, Na2O- naatriumoksiid, Fe2O3- raud (III) oksiid jne). Hüdroksiid aine, milles metallikatioonid on seotud hüdroksiidioonidega. Näiteks: NaOH, Ca(OH)2. Redutseerija aine, mille osakesed loovutavad elektrone ise oksüdeerudes. Oksüdeerija aine, mille osakesed liidavad elektrone ise redutseerides. Fluor on alati oksüdeerija! Oksüdeerumine- elektronide loovutamine, redoksreaktsioonis vastab sellele elemendi oa suurenemine. Redutseerimine- elektronide liitmine, redoksreaktsioonis vastab sellele elemendi oa vähenemine.
Metall + hapnik = (Na + O2 Na2O) Metall + mittemetall = (Väärisgaasidega ei reageeri, sest neil on oktett!) Metall + vesi = [Li Mg (Toa temp = Leelis + H.); Al Fe (kuum. = oksiid + H)] Metall + hape = Sool + vesinik (Pingerida - H) Metall + sool = (Pingerida üksikmetall ja soolas olev metall )
Keemilised omadused o Ammoniumisoolad on nõrga aluse soolad, mis reageerivad kergesti tugevate o Reageerib O2-ga katalüsaatori juuresolekul aluste ehk leelistega o 2S+3O22SO3 o 2NH4Cl+Ca(OH)2CaCl2+2H2O+2NH3| o On happeline oksiid, seega reageerib alustega ja aluseliste oksiididega o Amooniumsoolad kuumutamisel o SO2+2NaOHNa2SO3+H2O o NH4ClNH3+HCl Kasutatakse kasvuhoonete desifitseerimiseks Kasutamine: pesuvahendites, külmutusseadmetes ja jahutusvedelikes, nuuskpiiritus,
· Kasutamine: Alumiiniumist valmistatakse kõiksugu tarbeesemeid, kerge hea töötlemis omadustega metallina on ta hinnatud materjal ehituses. Tina kasutatakse tinatatud plekkist konservkarpide valmistamisel. Pliid kasutatakse autoakude(pliiakude) valmistamisel. Veel kasutatakse pliid näiteks elektrikaablite kaitsetorude valmistamisel. Pliid kasutakse tuumakiirgust takistavate kaitseekraanide valmistamisel(näiteks tuumaelektrijaamades) · Ühendid: Alumiinium oksiid Al O rhk korund. Peeneteraline korund ehk smirgel on kasutuses lihvimispulbri, puhastuspastade jms koostises. Läbipaistvad suured korundi kristallid on vääriskivid. Neis on lisandeid seega on nad värvilised. Punane korund =rubiin, sinine/kollane korund=safiir. Alumiinium hüdroksiid Al(OH) tegelikult polümeerne keeruka struktuuriga muutuva koostisega aine, mida väljendab tinglik valem Al O x nH O Alumiiniumi soolad
tugevamini tuuma poole, aatomi raadius väheneb ning väliskihi elektrone hoitakse aatomis tugevamini kinni. See tähendab, et metallilised omadused nõrgenevad. 3. Metallide keemilised omadused Metallide aatomid keemilistes reaktsioonides VAID loovutavad elektrone. Seepärast suureneb nende oksüdatsiooniaste ning nad on redutseerijad, reageerides oksüdeerijatega. Redutseerija oksüdeerus tema oksüdatsiooniaste kasvas. 3.1 Reageerimine hapnikuga: metall + hapnik oksiid IA, IIA ja Al oksüdatsiooniaste ühendis on võrdne rühmanumbriga, tsingil II, hõbedal I, raual II või III, vasel eelistatult II (aga ka I). II -II III -II 2Ca + O2 2CaO 4Al + 3O2 2Al2O3 Raud roostetab niiskes õhus: III -II 4Fe + 3O2 2Fe2O3
perioodis. Elektronvalem on 1s22s22p63s23p2. · Väga väheaktiivne mitemetall. On ka poolmetallidele iseloomulige omadusi (väga oluline pooljuht elektroonikas). · Moodustab väga palju polümeraalseid ühendeid. · Väga oluline osa eluta looduses (SiO2 põhiline liiva koostisosa). 2. Ühendid · Ränidioksiid (SiO2) polümeerne struktuur. Liiva peamine koostisosa. Looduses esineb ta kvartsina (mäekristall), mis on poolvääriskivi. Happeline oksiid. Veega ei reageeri. · Ränihape (H2SiO3) hästi nõrk hape. Seismisel tekib silikageel. · Silikaadid on ränihappe soolad. Vees väga vähe lahustuvad. · Klaas silikaatse koostisega tehismaterjal. Saadakse enamasti sooda, lubjakivi ja SiO2 (klaasiliiv) kokkosulatamisel. Omaduste parandamiseks võidakse lisada ka veel teisi elemente. Klaas on keemiliselt väga vastupidav. · Klaasile plii- või baariumoksiidi lisamisel saame kristallklaasi. Võrreldes
Anioonid Katioonid Li OH¯ Na Cl¯ K Br¯ NH I¯ Mg² S ²¯ Ca² SO³¯ Ba² CO²¯ Al³ SiO²¯ Pb² SiO¯ Fe² Fe³ Cu³ Ag Zn² OKSIID HAPPE HÜDROKSIID SOOL Suvaline aine + hapnik Vesinikioon + OH¯ + metalli o.a Metall + CaO ; AlO ;PO happeanioon sulgudes happeanioon HNO ; HSO ; Ca(OH) ; Al(OH) ; Ca(NO) ; HPO NaOH Al(SO) ; NaPO
KEEMIA MÕISTED AATOM neutraalne osake, mis koosneb aatomtuumast ja elektronkattest ELEKTRONSKEEM näitab elektronide paigutust elektronkihtidel KEEMILINE ELEMENT ühesuguse tuumalaenguga aatomite liik IOON laetud aatom KATIOON positiivselt laetud ioon ANIOON negatiivselt laetud ioon O-A arvutuslik suurus, mis näitab elemendi oksüdeerumise astet ühendis LIHTAINE koosneb ainult ühe elemendi aatomitest LIITAINE koosneb vähemalt kahe erineva elemendi aatomitest MOLEKULAARSED AINED soolad, metallid, alused, aktiivsete metallide oksiidid MITTEMOLEKULAARSED AINED happed, orgaanilised ained, vedelikud, gaasid KEEMILINE SIDE jõud või mõju, mis seob aatomid molekuliks või aatomid ja ioonid kristalliks KOVALNTNE SIDE ühiste elektronpaaride abil tekkiv keemiline side (mittemetallid) METALLILINE SIDE keemiline side metallides, tekib metalliaatomite vahel ühiste väliskihielektronide abil IOONILINE SIDE erinimeliste laeng...
Ainete triviaalnimetused. CO2 süsinikdioksiid ehk süsihappegaas CO- süsinikmonooksiid ehk vingugaas NH3 ammoniaak, mille vesilahus NH3•H2O (ammoniaakhüdraat- ammooniumhüdroksiid) – nuuskpiiritus. Fe2O3 – raud(III)oksiid – rooste, punane ja pruun rauamaak, rauamennik, ooker, muumia. Fe3O4 – magnetiit, must rauamaak CaO – kaltsiumoksiid, kustutamata lubi. Veega reageerimine lubja kustutamine. Ca(OH)2 – kustutatud lubi /lubimört/ lubjavesi Al2O3 – alumiiniumoksiid – Boksiit, korund, safiir, rubiin CaCO3 – kaltsiumkarbonaat – lubjakivi, kriit, paekivi, marmor, munakoore koostises CaSO4• 2H2O – kaltsiumhüdraat ehk/ kaltsiumsulfaat korda 2 vett – kips, ilma veeta põletatud kips NaCl – naatriumkloriid – keedusool NaOH – naatriumhüdroksiid – seebikivi Na2CO3 – naatriumkarbonaat – pesusooda NaHCO3 – naatriumvesinikkarbonaat – söögisooda HCl – vesinikkloriidhape – soolhape/maohape NH4HCO3 – ammooniumvesinikkarbonaat – põdrasarveso...
lahusena on ta nuuskpiiritus, mis mõjub ergutavalt.Õhus leidub lämmastikku vabal kujul, kuid lämmastiku molekulid on passiivsed, ja ühendeid on väga raske saada. Ammoniaagi saamismeetodid väljatöötamine lahendas lämmastiku sidumise probleemi. Vees lahustumisel ammoniaagi molekulid hüdraatuvad ning tekib Ammoniaakhüdraa on ebapüsiv ja laguneb kergesti gaasiliseks ammoniaagiks ja veeks.NH3 + H2O çèNH3*H2O N2O dilämmastikoksiid ehk naerugaas. Ta on värvuseta, neutraalne oksiid, nõrga meeldiva lõhnaga, vees lahustuv narkootilise toimega gaas. Sissehingamisel väheses koguses põhjustab elevust ja lõbusat meeleolu. Suuremates kogustes kutsub esile valutunde kaotamise ja narkootilise une, sel põhjusel kasutatakse operatsioonide ja sünnitusel valuvaigistina.Dilämmastikoksiidi saadakse NH4NO3 nõrgal kuumutamisel, kuid tekkiv N2O ei ole püsiv, sest ta laguneb kergesti lämmastikuks ja hapnikuks. NH4NO3 N2O + 2H2O 2N2O 2N2 + O2