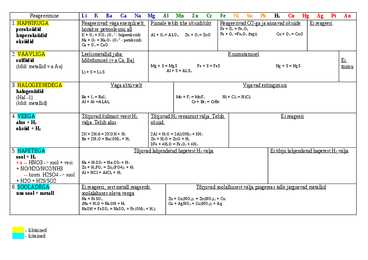
Mõnede rühmade puhul kasutatakse rühma üldnimetusi, näiteks leelismetallide rühm (IA), halogeenide rühm (VIIA), väärisgaaside rühm (VIIIA). Keemiliste elementide perioodilisustabel koosneb metallidest ja mittemetallidest. Mittemetallide hulka kuuluvad ka väärisgaasid. Tabeli enamuse moodustavad metallid, vähem on mittemetalle. Metallid (nt. Na, K, Ca) paiknevad tabelis vasakul, paremal on mittemetallid (nt. P, S, C).Paremal, kõige ääres on väärisgaasid (nt. He, Ne, Ar). Metallid on enamasti iseloomuliku läikega tahked ained, mille värvus varieerub tavaliselt terashallist hõbevalgeni. Metallide siledad poleeritud pinnad peegeldavad hästi valgust. Metallid on enamasti plastilised ja hästi töödeldavad. Metallid on ka head soojus-ja elektrijuhid. Metallide sulamistemperatuurid on väga erinevad. Enamik metalle on veest raskemad. Metalli tihedus on seda väiksem, mida väiksem on selle aatommass ja suurem aatomiraadius
hapnik (O) (OH) happejääk Mittemetalli oksiidid ·NaOH ·HCl -vesinikkloriidhape ehk ·NaCl-naatriumklorii CO - süsinikdioksiid ·Ca(OH) soolhape keedusool NO - NB!Muutuva o.-a. ·HBr -vesinikbromiidhape ·NaBr- naatriumbrom dilämmastiktrioksiid metallid ·HF -vesinikfloriidhape ·NaF - naatriumfluor PO - Cr(OH) ·HS - divesiniksulfiid ·NaS - naatriumsulf tetrafosfortekaoksiid -kroom(3)hüdr. ·HSO ·NaSO-naatriumsu Metallioksiidid CuOH-vask(1)hüdr. ·HSO ·NaSO-naatriumsu ·A-rühma metallid Liigid : ·HCO - süsihape ·NaCO -
asendata teise materjaliga. Metalli erinevus võib tuleneda koostis osadest, kaalust, tugevusest jne. See omakorda tingib metalli hinna variatsioonid. · Roostevaba teras/metall. · Titaanium.Erisulamid. · Allumiinium/duraallumiinium. · Valgevask, vask, pronks (teised kokkusulatatud vasest metallid). · Raud/plekk/malm (must metall,gabariit). · Tehniline hõbe/hõbe. · Plaatina, kuld (väärtuslikud metallid). Need on kõige tuntumad värvilised metallid, mustad metallid ja väärtuslikud metallid. Mis tooteid saab pakkuda firma, mis teenused saab osutada ja kas nende järgi on Eesti turul nõudmist? vanametalli kokkuost ostuosakondades vanametalli äravedu kliendi territooriumilt (tõste- ja transpordi teenus) konteinerite vahetusteenus tõstukauto teenus metallkonstruktsioonide demonteerimine ning lammutustööd vagunite laadimine kaalumisteenus
või moodustub nõrk elektrolüüt. Metallid käituvad keemilistes reaktsioonides alati redutseerijana. Tüüpiliste(a rühm) metalliliste elementide oa ühendites võrdub enamasti rühma nr. Redoks reaks. Võrdub oksüdeerija poolt liidetud elektronide arv alati redutseerija poolt loovutatud elektronide arvuga. Metalli reageerimisel hapete lahustega on redutseerijaks metall ja oksüdeerijaks happe vesinik ioonid. Metallide pingereas on metallid reastatud redutseerivate omaduste nõrgenemise suunas. See rida peegeldab metallide võimet loovutada elektrone vesilahuses kulgevates reaktsioonides. Metallid mis asuvad pingereas vesinikust vasakul, on võimelised hapete lahustest vesinikku välja tõrjuma. Metallis, mis aga paremal, hapete lahustest vesinikku välja ei tõrju. Metalli reageerimisel veega on red metalli oks vesi.
Aineklasside dissotseerumine: 1) Soolad NaCl Na+ + Cl 2) Alused KOH K+ + OH Mg(OH)2 OH + MgOH+ 2OH + Mg2+ 3) Happed HCl H+ + Cl H2SO4 H+ + HSO4 2H + SO42 METALLIDE KEEMILISED OMADUSED 1) REAGEERIMINE LIHTAINETEGA (mittemetallid) 4Al + 3O2 2Al2O3 3Fe + 2O2 Fe3O4 2) REAGEERIMINE VEEGA NB! Toimub pingerea alusel · Väga aktiivsed metallid reageerides veega, annavad saadustesse leelis + H2 2Na + 2H2O 2NaOH + H2 · Keskmise aktiivsusega metallid reageerivad kõrgel temperatuuril veeauruga oksiid + H2 Zn + H2O ZnO + H2 · Väheaktiivsed metallid ei reageeri veega 3) REAGEERIMINE HAPETEGA NB! Toimub pingerea alusel · Metallid mis asuvad pingereas vesinikust vasakul
Tallinna Polütehnikum Materjaliõpetus Õppematerjalide mapp Rühm: Nimi: 2010/2011 Sissejuhatus Tehnikas kasutatakse loetelu: 1. Tahkeid ehk õhumaterjale(metallid, tehnoplastid jne.) 2. Vedelaid (õhk, õli, mitmesugused lahustid) 3. Gaasilised (looduslikud: õhk, keemilised gaasid nagu vesinik- kasutatakse isolaatorina, jahutina). Tahkeid materjalid liigitatakse siseehituse järgi: 1. metallid (kristallilise siseehitusena) 1.1 metallid- mustad metallid ehk raudsüsinik sulamid(terased, malmid, elektrotehniline raud) 1.2 värvilised metallid (vask, alumiinium, hõbe, kuld, plaatina)- kasutatakse elektroonikas puhtal kujul. 1.3 värviliste metallide sulamid(pronks, messing)- kasutatakse põhiliselt tehnikas. Vase ja nikkli sulamid- suure eritakistusega, küttekehadeks 2. Mitte- metalsed materjalid (looduslikud või tehis ehk sünteetilised) 2.1 keraamilised materjalid (klaas, portselanid, kivimid jne) 2
esinevas kristallis. Metallis paiknevad aatomid kindla seaduspärasuse järgi, moodustades korrapärase kristallivõre. Selline aatomite paigutus vastab aatomite omavahelise mõju minimaalselebenergiale (aatomite ideaalsele paigutusele). 2. Teiste metallide mõju terase omadustele. Tabelist 3. Kumm ja kummidetailide tootmine. Pilet nr.3 1.Metall mittemetall. Metallid ja sulamid Metallid on ained, millel on tahkes olekus iseloomulik läige, hea elektri- ja soojusjuhtivus ning tavaliselt ka hea mehaaniline töödeldavus, suur plastsus ja elastsus. Metallide omadused on seletatavad aatomi tuumaga nõrgalt seotud vabade elektronide (valentselektronide) olemasoluga nende kristallivõre aatomite välimises elektronkihis. Metallid loovutavad kergesti väliskihi
Korrosioon Korrosiooniks nim metallide ja nende sulamite hävimist ümbritseva keskkonna keemilise, elektrokeemilise või biokeemilise toime tõttu. Korrosiooni tulemusena metallid purunevad kas osaliselt või täielikult muutudes kasutamiskõlbmatuteks. Korrosioonile alluvad kõik metallid ja sulamid ning muutuvad tagasi esialgseteks ühenditeks millest neid saadi. Keemiline korrosioon esineb siis, kui metallid puutuvad kokku keemiliselt agressiivsete ainetega. Keemiline korrosioon tekib: · sisepõlemismootorite detailidel, · elektrisoojendite kütteelementidel, · summutites, heitgaaside torustikes jm Seda põhjustavad mitmesugused gaasid. Keemiliselt aktiivsed ja korrosiooni põhjustavad vedelikud on: · kõik naftasaadused, · kemikaalide vesilahused, · mineraalväetiste lahused (samuti tahked väetised), · vasksulfaat jms
4.1. Põllumajandus 15 4.2. Metsandus 17 4.3. Info ja sidetehnoloogia 18 4.4. Kalandus 19 4.5. Töötlev tööstus 20 4.5.1.Tselluloos ja paber 20 4.5.2. Keemiatooted 20 4.5.3. Metallid 20 4.5.4. Keskkonnakaitse 20 4.6. Meretööstus 22 4.6.1. Spetsialiseeritud laevatehased 22 4.6.2. Kaasaegsed laeva ja kalapüügiseadmed 22 4.6.2. Akvakultuuriseaded 22 4.7. Maavarad 23 4.7.1
Markus Põder MATERJALID AUTOEHITUSES REFERAAT Õppeaines: TEHNOMATERJALID Mehaanikateaduskond Õpperühm: MI 21 Juhendaja: lektor Annika Koitmäe Tallinn 2014 SISUKORD Sissejuhatus ..........................................................................................................................................4 1. Mustad metallid ............................................................................................................................5 1.1. Teras ...................................................................................................................................5 1.1.1 Roostevaba teras ................................................................................................................5 1.1.2 Terase kasutusalad autoehituses [5] ..............
Üks levinumaid metalli saamise meetod on karbotermia metalli saamie metalliühendi redutseerimisel süsiniku või süsinikoksiidiga kõrgel temperatuuril. Kasutatakse ka redutseerimist aktiivsema metalliga, näiteks alumiinimuiga (aluminotermia) Miks suurem osa metalle esineb looduses ainult ühenditena? Milliste ühenditena? Sest et metallid on aktiivsed ja hakkavad reageerima ja pikaajalistes looduslikes keemilistes protsessides moodustavad metallid selliseid ühendeid, mis on kõige püsivamad. Metallid esinevad looduses peamiselt sooladena. Vähemaktiivsed metallid esinevad peamiselt oksiidsete või sulfiidsete mineraalidena. Mis on elektrolüüs? Milleks seda kasutatakse? Elektrolüüs on redoksreaktsioon, mis toimub elektrolüüdilahuses või sulas elektrolüüdis, elektroodide pinnal. See reaktsioon toimub elektrivoolu toimel ja selles muundub elektrienergia keemiliseks energiaks. Aktiivsemate
· POOLA Kaubavahetus · Poola on Eesti suurim väliskaubanduspartner Kesk- Euroopa riikide hulgas, olles Eesti väliskaubanduspartnerite hulgas juba aastaid 7. positsioonil. · 2012. aastal oli Eesti-Poola kaubavahetuse maht 1,029 mld eurot (3,9% kogukäibest), eksport 176,901 mln, import 852,673 mln, saldo -675,773 mln. 2011. aastaga võrreldes kahanes käive 0,9%. POOLA Peamised ekspordiartiklid 2012. aastal · Masinad ja seadmed - 27,6% · Metallid ja metalltooted - 19,0% · Puit ja puittooted - 11,1% · Transpordivahendid 9,0% Peamised impordiartiklid 2011. aastal · Masinad ja seadmed - 35,0% · Metallid ja metalltooted - 11,3% · Keemiatooted - 10,0% SLOVAKKIA Kaubavahetus · Eesti ja Slovakkia kaubavahetus on seni olnud suhteliselt tagasihoidlik. · 2012. aastal oli Slovakkia Eestile 27. kaubanduspartner kaubavahetuse kogukäibega 116,4 mln eurot. · Eksport Slovakkiasse moodustas 2012
· Ioonvõre-võrest moodustavate osakeste (ioonide )vahel on tugev iooniline side,mistõttu ained on tahked ning kõrge sulamistemp ja keemistemp,haprad · Aatomvõre-moodustavate osakeste vahel on tugev kovalentne side,mistõttu ained on tahked ning kõrge salamis-ja keemistemp. · Metallivõre-moodustavate osakeste(metalliioonide) vahel on metalliline side,mille vahel liiguvad vabad elektronid,mistõttu metallid on head elektri ja soosjusjuhid ning plastilised · Kovalentne side-on ühiste elektronpaaride abil tekkinud side.esineb aatomite vahel molekulides · Valents-näitab ühe aatomi poolt moodustatud kovalentse sidemete arvu · Struktuurvalem-näitab aine ehitust · Mittepolaarne kovalentne side-tekib ühe ja sama mittemetallilise elemendi aatomite vahel · Polaarne kovalentne-tekib erinevate mittemetalliliste elementide aatomite vahel
Kuna elektronid suudavad soojusliikuvusest omandada piisavalt energiat, et hüpata üle keelutsooni ja muutuda vabaks. 2. Miks on dielektrikud läbipaistvad? Dielektrikud on läbipaistvad, järelikult ei neela valguskvante (metallid ja pooljuhid neelavad) Ei neela valguskvante sest, nähtava footoni energia kvandid on E=1.8- 3.1eV, Elektronide ergastumiseks on vaja 5-10 eV 3. Dielektrikud on läbipaistvad, ei neela valguskvante. Metallid ja pooljuhid neelavad valguskvante seega on läbipaistmatud. Dielektrikutes on keelutsoon lai (5-10eV), soojusenergiast ei piisa juhtivuselektronide tekitamiseks. Tavatemperatuuridel ergastab soojusliikumine pooljuhtides elektrone üle kitsa (1eV) keelutsooni kõrgemasse tsooni juhtivustsooni, jättes valentstsooni auke. Kuna metallides on kõrgeim hõivatud energiatsoon ainult osaliselt elektronidega asustatud, on nad head soojusjuhid. 4
ületa 106 m. Elektrijuhtide kohta öeldakse, et nad juhivad elektrit ehk neil on hea elektrijuhtivus. Materjali, mis elektrit ei juhi, nimetatakse isolaatoriks. Kui elektrilised potentsiaalid juhi eri punktides on erinevad, siis vastavalt Ohmi seadusele läbib juhti elektrivool. Juhtide elektrijuhtivust iseloomustatakse tavaliselt eritakistusega. Mida väiksem on eritakistus, seda paremini juht elektrit juhib. Paljud elektrijuhid on metallid, kuid on ka mittemetallilisi elektrijuhte. Metallid on elektronjuhtivusega elektrijuhid. Nende juhtivus tuleneb metalliaatomite elektronkatte väliskihi elektronide ehk valentselektronide nõrgas t sidemest aatomituumaga. Kõik metallid on keemilised elemendid, mis asuvad Mendelejevi tabelis boori ja polooniumit ühendavast diagonaalist vasakul. Neil on väliskihis alla nelja elektroni ning nad on valmis neid ära andma, et saavutada stabiilsemat olekut. Elektrone saab
oksiidid Na + O2 = Na2O2 (O2-2 - peroksiid) Ca + O2 = CaO 2. VÄÄVLIGA Leelismetallid juba Kuumutamisel sulfiidid hõõrdumisel (v.a Ca, Ba) Ei (kõik metallid v.a Au) Mg + S = MgS Fe + S = FeS Hg + S = HgS toimu Li + S = Li2S Al + S = Al2S3 3. HALOGEENIDEGA Väga aktiivselt Vajavad eritingimusi halogeniidid
Kristallivõret kooshoidvatest sidemetest lähtuvalt eristatakse kolme liiki keemilisi ühendeid: elektrokeemilised ühendid, sisendusfaasid ja elektronühendid. Keemilisi ühendeid moodustavatest komponentidest lähtudes eristatakse oksiide, intermetalliide, karbiide, nitriide ja boriide. 7. Missugust struktuuri nimetatakse tekstuuriks? 8. Missuguse struktuuriga sulamid on hästi survetöödeldavad? Hästi survetöödeldavad on ühefaasilised struktuurid (puhtad metallid, tardlahuse struktuuriga sulamid), sest nad on väikese tugevusega ja kõvadusega ning suure plastsusega. 9. Missuguse struktuuriga sulamid on hästi valatavad? Parimate valuomadustega sulamid on eutektse koostisega või eutektkoostisele ligilähedase koostisega sulamid, seda tänu madalale sulamistemperatuurile ja heale vedelvoolavusele. (kahefaasilise struktuuriga sulamid) 10. Missuguse struktuuriga metallid ja sulamid on väikese tugevuse ning kõvadusega, kuid suure plastsusega?
Keemia põhimõisted (aine, materjal, valem, reaktsioonivõrrand). Ainete klassifikatsioon, Loengud: 12 loengut (iga nädal A V-103) tähistamine ja iseloomustamine (sertifitseerimine). Materjalide Praktikumid: 6 praktilist tööd (üle nädala) loodusteaduste maja 4. oamdused, klassifikatsioon; metallid, keraamika, polümeerid, korrus; komposiidid, kõrgtehnoloogilised ja nanomaterjalid. Harjutustunnid: 4 (üle 2 nädala). 2. Gaasid. Gaasiliste ainete põhiomadused, gaaside segud, veeaur, aururõhk. Gaaside põhiseadused. Reaalsed gaasid, atmosfäär. Mõnede
b)keskm aktiivsed met.(Al-Fe) reag. auruga kõrgel temp; tekivad oksiidid ja H2 ( Zn+H2O®ZnO+H2 ) c)väh. akktiivsed met.(Ni-Au) ei reagereeri veega ·Reag. lah. hapetega a)vesinikust vasakul olevad met.; tekivad sool ja H2 ( Zn+2HCl®ZnCl2+H2 ) b)vesinikust paremal olevad met. ei reag. lah. hapetega ·Reag. soola lahustega(reag. vees lahustuva soolaga, kui ta on aktiivsem kui soola koostises olev metall; tekivad sool ja met.) Fe+CuSO2®FeSO4+Cu Met. mis reag. külma veega(IA ja IIA metallid alates Ca), ei asenda soola koostises vähem aktiivseid met. vaid reag. veega ja tekkinud leelis võib reag. soolaga- Na+CuCl2 1) 2Na+2NaOH+H2 2) 2NaOH+CuCl2®Cu(OH)2+ 2NaCl Summaarselt: 2Na+CuCl2+H2O®Cu(OH)2+2NaCl+H2 ·Reag. mittemet.(peaaegu kõik met. reag. mittemet. 2K+Cl2®2KCl) SAAMINE ·Maagid on kivimid, mis sisaldavad tootmisväärses koguses metallide looduslikke ühendeid. 1. Maagi rikastamine (lisanditest puhastamine) 2. Metalli redutseerimine maagist a) koksiga (kõige odavam)
Kõige levinumaks leelismetalliks ongi naatrium, sest ta on elementide levikult maakoores kuuendal kohal, kuid metallide levikult merevees lausa esikohal. Loomulikult on viimane tingitud sellest, et meredes ja ookeanides sisaldub ohtralt naatriumi tuntumat ühendit naatriumkloriidi. Lihtainena saadakse leelismetalle neile vastavate soolade või leeliste elektrolüüsil sulatatud olekus. Leelismetallide füüsikalised omadused Leelismetallid on lihtainena kõige tüüpilisemad metallid. Leelismetallide elementide aatomitel on 1 2 6 väline (s ) ja eelviimaste elektronkihtide (s p ) konfiguratsioon ehk elektronide arv ja paigutus orbitaalidel (v.a. Li) ühesugune. Sel põhjusel on nende elementide ja ka lihtainete omadused ligikaudselt ühesugused. Leelismetallides on kõige puhtamal kujul metalliline side, nad on metalse läikega, enamik neist on hõbevalged metallid, ainult tseesium on kuldkollase värvusega. Nendel on
H2SO4 + Zn à ZnSO4 + H2 Cu + HCl reaktsiooni ei toimu Hapete reageerimisel metallidega tuleb arvestada metalli asendit aktiivsuse reas ja happe iseloomu. Li K Ca Na Mg Al Zn Cr Fe Ni Sn Pb H Cu Hg Ag Pt Au Metallide aktiivsuse rida (pingerida) algab aktiivsete metallidega, rea lõpus on väheaktiivsed metallid. Aktiivsuse reas vesinikust vasakul paiknevad metallid tõrjuvad lahjendatud hapetest vesiniku välja, paremal olevad metallid aga ei tõrju. Tugevad happed (konts. H2SO4 ja mistahes kontsentratsiooniga HNO3) reageerivad ka mõnede pingereas vesinikust paremal olevate metallidega, kuid antud reaktsioonides vesinikku ei eraldu. Cu + 4HNO3 (konts) à Cu(NO3)2 + 2NO2 + 2H2O
optimaalselt ja seal on temperatuur kõige kõrgem, leeki ümbritseb vaevu nähtav kollakas osa. Täieliku põlemise saadused on süsihappegaas ja veeaur, kuid mittetäielikul on ka palju teisi aineid, nagu näiteks tahm, alkaanid ja polütsüklilised süsivesikud. 3 Höögumine tekib kõrge sulamistemperatuuriga ainete ja metallide puhul. Madalama sulamistemperatuuriga metallid võivad sulada või isegi keema minna. Höögvel olev materjal on kergest töödeldav ja elastne. Höögvel oleva materjali temperatuuri saab hinnata höögumise värvuse järgi. Mida erksam ja heledam punane seda kõrgem on temperatuur, kui temperatuur kerkib üle tuhande kraadi muutub höögumine valgemaks. Leekreaktsioon ehk leegi värvumisreaktsioon, selle reaktsiooni abil saab kindlaks määrata metalli või aine millega on tegemist, kuna erinevad metallid põlevad erineva värvusega
METALLIDE BIOTOIME ÜLDISELOOMUSTUS MIHKEL TAMMIK HOLGER KOPPEL 10.A BIOTOIME ON Metallide bioloogilised funktsioonid organismis. Bioorgaaniline keemia. Biometalle aatomitena inimese organismis ei leidu, Sest lihtainena on paljud metallid vähepüsivaid ning rohkem on tuntud nende ühendid. Biokeemilised protsessid. Toidust, joogiveest, sissehingatava õhust ja ümbritsevast keskkonnast. 1. MESO- E. MAKROBIOMETALLID · Katioonid Ca2+, Na+, K+, Mg2+ · Täidavad biofunktsioone valdavalt ioonsel kujul. · Neid leidub organismis 0,......% 2. MIKRO- E. MIKROBIOMETALLID · Fe, Sn, Cr, Ni, V, Co, Mn, Zn Cu · Eri organismides on neid erinev hulk. · Neid leidub organismis 0,00..% TÄHTSAIMAD METALLID INIMKAHAS · Kaltsium 1
SISUKORD Sissejuhatus............................................................................................................................................3 1. Millest Sõltub Metallide Kasutamine ?.............................................................................................4 1.1 Metallid minu ümber ja kodus ..........................................................................................................5 1.1.1 Raud ( Fe ).......................................................................................................................................5 1.1.2 Naatrium ( Na )...............................................................................................................................5 1.1.3 Kuld ( Au ) ja hõbe ( Ag )..................................
Korrosioon on raua roostetamine, vase kattumine paatinakihiga, alumiiniumi tuhmumine, hõbeda tumenemine jne. Korrosioon kujutab endast redoksprotsessi, mille käigus metalli aatomid oksüdeeruvad. Korrosioon sõltub keskkonnast (õhus, vees, pinnases), mõjuteguritest (mehaaniline pinge vedrudes, koormust kandvad terastrossid), temperatuurist (kõrgemal temperatuuril korrosioon kiireneb), radioaktiivsest kiirgusest jm. Korrosiooni tulemusena metallid purunevad kas osaliselt või täielikult muutudes kasutamiskõlbmatuteks. Korrosioonile alluvad kõik metallid ja sulamid ning muutuvad tagasi esialgseteks ühenditeks millest neid saadi. Keemiline korrosioon esineb siis, kui metallid puutuvad kokku keemiliselt agressiivsete ainetega. Keemiline korrosioon tekib sisepõlemismootorite detailidel, elektrisoojendite kütteelementidel, summutites, heitgaasidetorustikes ja muud mitmesugused gaasid
Eriotstarbelisi materjale kasutatakse vastavalt kasutusvaldkonna nõudmistele. Näiteks elektrotehnikas elektrimasinate, aparaatide ning muude seadmete tootmiseks kasutatavatel materjalidel peavad olema teatud elektrilised ja magnetilised omadused. Neid nimetatakse elektrimaterjalideks. Materjalide klassifikatsioon Elektrimaterjalid liigitatakse vastavalt nende elektrilistele ja magnetilistele omadustele: Juhid (juhtmed, poolid, kontaktide) kõik metallid, kasutatakse metalle, millel on: väike elektriline eritakistus, küllaldane mehaaniline vastupidavus, vajalikud füüsikalis-keemilised omadused (korrosioonikindlus, kuumuskindlus vm). Dielektrikud (isolatsioon, isolaatorid) Kasutatakse tahkeid, vedelaid ja gaasilisi. Dielektrikul peab olema: suur elektriline eritakistus, läbilöögi kindlus, vajalikud mehaanilised omadused, kindlad füüsikalis-keemilised omadused.
Värvus: enamik metalle on hõbevalged ja terashallid. Teistsuguse värvusega on kuld(kollane) ja vask(punane). Plastilisus: enamik metalle on plastilised: välisjõudude mõjul võib muuta nende kuju ja see kuju säilib ka pärast jõu mõju lakkamist. Plastilisuse tõttu saab neid sepistada, valtsida õhukesteks lehtedeks ja tõmmata traadiks. Elektri-ja soojusjuhtivus: suhteliselt vabade elektronide olemasolu tõttu on metallid head elektri-ja soojusjuhid. Kõvadus: metallid on erineva kõvadusega. Kõige kõvem metall on kroom, millega võib lõigata isegi klaasi. Ka volfram ja mangaan on kõvad metallid. Leelismetallid kaalium ja naatrium on niivõrd pehmed, et neid saab noaga lõigata. Tihedus: enamik metalle on veest raskemad. Erandiks on osa leelismetalle( Li, Na, K). Sulamistemperatuur: kõik metallid peale elavhõbeda on tavatingimustes tahked. Elavhõbeda sulamistemperatuur on -38,9°C, kõige kõrgema sulamistemperatuuriga metallil volframil aga 3410°C.
NB! Reaktsioon toimub siis, kui uus tekkiv happe on reageerivast happest nõrgem või lenduvam või kui uus tekkiv sool ei lahustu vees (sade). + METALL SOOL + VESINIK 2HCl + Zn ZnCl2 + H2 NB! Reageerivad pingereas vesinikust vasakul paiknevad metallid. Erandiks on k. HNO3, lahj. HNO3 ja k. H2SO4 reageerimine metallidega (ei kehti pingerida ning ei eraldu vesinikku). ALUS + HAPE vaata HAPE + ALUS + HAPPELINE OKSIID SOOL + VESI 2NaOH + CO2 Na2CO3 + H2O
pruunid roostelaigud. Aeglasemalt tuhmub läikiv vasepind. Korrosiooni puhul mõjutab metalli ümbritsev keskkond keemiliselt. Mis on korrosioon? - See nimetus tuleneb ladinakeelsest sõnast corrodere, mis tähendab puruks närimist. Seega korrosioon on metallide hävimine ümbritseva keskkonna toimel. Keemia keeles öelduna oksüdeeruvad metalli aatomid ümbritseva väliskeskkonna (õhk, vesi, erinevad gaasid, lahused jne.) toimel. Korrosioon on redoksprotsess, kus metallid on redutseerijad ise oksüdeerudes. Igapäevaelus näeme korrosiooni enamasti raudesemete roostetami- sena, aga ka vask- ja hõbeesemete tuhmumisena. Too konkreetseid näiteid oma kodusest elust erinevate metallide korrosioonist. Raua korrosioon Korrosiooni iseloomu järgi võime jagada korrosiooniprotsessi kaheks: 1. Keemiline korrosioon, mis toimub kuivades gaasides või vedelikes, mis ei juhi elektrivoolu, seega mitteelektrolüütides. Näiteks raua ühinemine
Erinevaid materjaide grupid (metallid, plastid, keraamika) erinevad üksteisest eelkõige tiheduse (roo) poolest, mille ühik on mahuühikumass, kg/m3. Plastide tihedus on vahemikus 1000-2000kg/m3, keraamikal 1500-2500, metallidel 1700-22000kg/m3 piires. Temperatuuri, mil materjal läheb üle tardolekust vedelasse, nimetatakse sulamistemperatuuriks (Ts). Korrosiooniks nimetatakse materjali ja keskkonna (õhk, gaasid, vesi, kemikaalid) vahelist reaktsiooni, milles materjal hävib. 8. Kuidas saab metallid liigitada lähtuvalt füüsikalistest omadustest (näited). Tihedus Tiheduseks nimetatakse metalli ühe mahuühiku massi. Metallid liigitatakse tihedusest lähtuvalt: kergmetallid ja -sulamid: tihedus on alla 5000 kg/m3 (Mg, Al, Ti jt.) keskmetallid ja -sulamid: tihedus 5000...10 000 kg/m3 (Fe, Cu) raskmetallid ja -sulamid: tihedus ületab 10 000 kg/m3 (Pt, W, Mo, Pb, jt.) Tehnikas kasutatavaist metallidest kergeim on magneesium, raskeim aga plaatina. Näiteid metallide tihedusest:
hüdroksiidid. Amfoteersed hüdroksiidid reageerivad nii hapete kui alustega. ALUSTE SAAMINE a) leeliste saamine metall ja vesi- saadused leelis ja vesinik aluseline oksiid ja vesi- hüdroksiid Võrrandid: Mg + H2O -> MgO + H2 P4O10+h2o-> H2PO3 Happed: happeid liigitatakse sooladeks ja hapeteks 1. Reageerivad metallidega -> sool ja vesinik Lahjendatud hapetega reageerivad pingereas vesinikust eespool olevad metallid. Vesinikust paremal pool olevad metallid ei reageeri., 2. reageerivad aluseliste oksiididega -> sool ja vesi 3. reageerivad alustega -> sool ja vesi 4. reageerivad sooladega -> uus sool ja uus hape Reaktsioon toimub vaid juhul kui tekin oluliselt nõrgem või lenduvam hape, või kui tekib sade. 5. lagunevad kuumutamisel -> vastav oksiid ja vesi kuumuyamisel lagunevad hapnikhapped HAPETE SAAMINE: Hapnikhapped saadakse vastavate happeliste oksiidide reageerimisel veega va ränihape
Eriala Metall materjalid *Metallmaterjale kasutatakse nende tugevuse,elastsuse keevitavuse pärast. *Metallide puuduseks on nende korrodeerumise keskonna mõjutuste tõttu. *Samas on metallid aga head sooja ja elektrijuhid. Metallid jaotatakse mustadeks ja värvilisteks(nt:teras ja vask) Tegelikult võiks jaotada ka rauda sisaldavateks ja mittesisaldavateks(nt:terased ja malmid ning vask,tsink jne. *Mustade metallide koostis on põhiliselt raud(fe) js süsinik(c)mitmesugustest vahekordades. *Lisandite rauda ehituses ei kasutata ta omadused pole selleks sobivad.Rauale lisatavad lisandid määravad tema omadused ja kasutamisviisi. *Põhimõtteliselt jaotatakse mustad metallid:terasteks ja malmideks.
6 heksa 2 di 7 hepta 3 tri 8 okta 4 tetra 9 nona 5 penta 10 deka Oksiidid • vääveltrioksiid SO3 • difosforpentaoksiid P2O5 • süsinikmonooksiid CO • Magneesiumoksiid MgO • Triraudtetraoksiid Fe3O4 Mittemetallid • Indeksid Risti Ette Indeksi Nimi (Di, Tri) lk 2 • dikloorpentaoksiid Cl2O5 • seleentrioksiid SeO3 • vääveltrioksiid SO3 • vääveldioksiid SO2 A-Rühma Metallid • Risti Alla Indeks, Lõppu Oksiid (di, tri) Ei kirjuta • Magneesiumoksiid MgO • Kaltsiumoksiid CaO • Alumiiniumoksiid Al2O3 B-Rühma Metallid • Indeks risti alla keskele kesmine indeks rooma numbriga • Plii(II)oksiid PbO • Tina(IV)oksiid SnO2 • Plii(IV)oksiid PbO2 • Kroom(III)oksiid Cr2O3 Harjutus • Kirjuta oksiidide valem • Liitiumoksiid- • Vääveltrioksiid- • Cl2O- • Lämmastikdioksiid-
Fe+S=FeS. Redutseerija-aine, mille osakesed loovutavad elektrone. Li, Na, Mg. Oksüdeerija-aine, mille osakesed liidavad elektrone. H2O2, CrO3. Redutseerumine-elektronide liikumine redoksreaktsioonis, sellele vastab elemendi oksüdatsiooniastme vähenemine. Oksüdeerumine-elektronide loovutamine redoksreaktsioonis, sellele vastab elemendi oksüdatsiooniastme suurenemine. Katalüsaator-aine, mis muudab reaktsiooni kiirust, vabanedes reaktsiooni lõpus esialgses koostises ja koguses. Aktiivsed metallid (K-Mg) reag. külma veega, tekivad leelis ja H2. Ca+2H2O=Ca(OH)2+H2. Zn+H2O=ZnO+H2. Väheaktiivsed metallid (alates Ni-st) ei reageeri veega. Vesinikust eespoololevad metallid tõrjuvad hapetest vesiniku välja. Zn+2HCl=ZnCl2+H2. Metall reageerib vees lahustuva soolaga, kui ta on aktiivsem kui soola koostises olev metall. Zn+CuCl 2=ZnCl2+Cu. 2Na+CuCl2+2H2O= Cu(OH)2+2NaCl+H2 2Na+ 2H2O=2NaOH+H2 2NaOH+CuCl 2=Cu(OH)2+2NaCl. Hapnikuga tekivad oksiidid: 2Ca+O2=2CaO.
Korrosioon-metallide hävimine ümbritseva keskkonna toimel. Redoksprotsess,milles metallid oksüdeeruvad ümritsevas keskkonnas Leiduvate oksüdeerijate toimel. Keemiline korrusioon- metalli vahetu keemiline reaksioon keskkonnas leiduva oksüdeerijaga.nt.metalli reag .(hapnik,kloor) või (bensiin,õli). Intensiivsemalt toimub kõrgemal temp. Elektrokeemiline korrusioon-toimub ka tavatingimustes.Toimub, kui metal Puutub kokku elektrolüüdilahusega. Elektrokeemiline reaks. Kulgeb kahe omava hel seotud reaktsioonina,mis vqivad toimuda metalli erinevatel pinnaosadel.
8. Molaarmassi arvutamine. 9. Ülesanded( protsent, mass, saagikus) 10. Metallide füüsikalised omadused. 11. Metallide keemilised omadused. 12. Mis on korrosioon ja kuidas selle vastu saab? 13. Leelismetallid ja nende ühendid. 14. Leelismuldmetallid, iseloomustus ja nende ühendid. · Leelismuldmetallid on: Mg, Ca, Be. Looduses neid vabalt ei leidu, need esinevad karbonaatide, sulfaatide ja silikaatidena. Need on väga aktiivsed metallid. Mg- hõbevalge, kergesti sulav. Ca-hõbevalge, veest 1, 5 korda raskem. Ühendid: Kaltsiumoksiid CaO ehk kustutamata lubi. Kaltsiumsulfaat CaS04 ehk kips. Ehitusmaterjal, lahaste koostises. Kaltsiumkarbonaat CaCO3 ehk lubjakivi (paas, marmor, kriit) · Leelismetallid on: Na, K, Li. On aktiivsed metallid, esinevad looduses ühenditena. LM on pehmed, kerged, madala sulamistemp. Ühendid: Naatriumkloriid NaCl ehk keedusool.
.. 3) Sulam- aine, mis on saadud kahe või enama komponendi kokkusulatamise- või paagutamise teel. 4) 5) Tardlahus- sulaolekust moodustunud faasid, kus üks komponentidest (lahustajakomponent) säilitab oma kristallivõre, teise (lahustunud) komponendi aatomid paigutuvad lahustajakomponendi kristallivõresse. 6) Keemiline ühend on keemiline aine, mis koosneb kahest või enamast erinevast keemilisest elemendist 7) 8) Hästi survetöödeldavad on ühefaasilised struktuurid (puhtad metallid, tardlahuse struktuuriga sulamid), sest nad on väikese tugevusega ja kõvadusega ning suure plastsusega. 9) Parimate valuomadustega sulamid on eutektse või eutektkoostisele ligilähedase koostisega sulamid tänu madalale sulamistemperatuurile ja heale vedelvoolavusele (Kahefaasilise struktuuriga sulamid) 10) Puhtad metallid, tardlahuse struktuuriga sulamid on väikese tugevusega ja kõvadusega ning suure plastsusega
ümbrusest, mis kutsub materjalis esile mõõdetava muutuse. Metallide korrosioon on metallide oksüdeerumine, mille tulemusena võivad metallisse tekkida augud või metallikihid lahti tulla. Raua korrosiooni nimetatakse roostetamiseks. Tugeva korrosiooni puhul võib materjal lakata täitmast funktsiooni, milleks ta on mõeldud. Igapäevaelus näeme korrosiooni enamasti raudesemete roostetamisena, aga ka vask- ja hõbeesemete tuhmumisena. Mõned metallid, näiteks alumiinium, võivad moodustada korrosiooni takistava oksiidikihi. Korrosiooni takistamiseks kasutatakse mitmesuguseid korrosioonikaitse meetmeid. Keemias käsitletakse korrosioonina metallide hävimist ümbritseva keskkonna (õhk, vesi, erinevad gaasid, lahused jne.) toimel. Korrosioon on redoksprotsess, mille käigus metallide aatomid oksüdeeruvad ja muutuvad ioonideks Meditsiinis nimetatakse korrosiooniks kudede hävimist põletuse või söövituse tagajärjel.
Aktiivse metalli, näiteks tsingi, kristallvrest väljuvad katioonid ja siirduvad lahusesse. Elektronid jäävad metalli ja annavad sellele negatiivse laengu. Metallide reastamisel standardpotentsiaali E° väärtuse järgi saadakse metallide pingerida, mis iseloomustab metallide keemilist aktiivsust: 1. Mida negatiivsem on antud metalli standardpotentsiaal, seda aktiivsem on ta keemiliselt ning seda tugevamad on tema taandavad omadused. 2. Iga metall trjub pingereas temale järgnevad metallid nende soolade vesilahustest välja. 3. Metallid, mille standardpotentsiaal on negatiivne, trjuvad lahjendatud hapetest välja gaasilises ve.. Keemilised vooluallikad: Keemilised vooluallikad on galvaanielemendid, mida kasutatakse elektrivoolu saamiseks. Akuks nimetatakse korduvat laadimist ja tühjenemist võimaldavat galvaanielementi. Galvaanielemendid. Galvaanielemendiks nimetatakse seadeldist, milles keemilise reaktsiooni energia muudetakse elektrienergiaks
aatomid. Sisestussulami tekkimiseks peavad sisestunud metalli või mittemetalli aatomid olema tunduvalt väiksemad põhimetalli aatomitest, et nad mahuksid kristallvõre tühimikesse. Selliste sulamite teke on iseloomulik raua, kroomi, või mangaani sulamite puhul. Sisestussulamiteks on terased, milles süsiniku aatomid on raua kristallvõre tühimikes. Nad on heade mehaanilise-tehnoloogiliste omadustega ja head elektrijuhid. Sulami tekkimisel võivad sulatatud metallid omavahel reageerida, moodustades metallide vahel keemilisi ühendeid, mida nimetatakse intermetalseteks ühenditeks. Intermetalseid sulameid iseloomustab tugevus, kõvadus, kuid vähene elektrijuhtivus.Intermetalsete ühentide sulamistemperatuur võib olla madalam või kõrgem lähtemetallidest. Nad erinevad asendussulamitest, sest viimastel on asenduvate aatomite paigutus korrapäratu, intermetalsetel ühenditel on aga korrapärane ja aatomite vahekord täisarvkordne. Seepärast
........................................................... 13 2 Sissejuhatus Suur Järvistu (ingl. Great Lakes või Laurentian Great Lakes) on Põhja-Ameerikas USA- Kanada piiril asuv mageveejärvede süsteem, mis sisaldab umbes 18% Maailma mageda pinnavett. Need järved peaaegu kogu oma eksisteerimise ajal mängivad tähtsat rolli elavate seal inimeste elus, olles tohutult rikkadeks erinevate ressurssidega nagu toit, metallid ja soola. Inimese tegevuste tõttu on nad praegu ohustatud ja see provleem äratab tähelepanu avaliku ja teadusliku seltskondade poolt. 3 1. Suure Järvistu üldiseloomustus Suureks Järvistuseks peetakse 5 suurimat järve: Ülemjärv, Huroni, Erie, Michigani ja Ontario järved (1). 1.1. Geograafiline asukoht Suur Järvistu vesikond asub Põhja-Ameerika idapool, USA ja Kanada territooriumitel. See
tahkkesendatuks ja temperatuuril 1392 °C tagasi ruumkesendatuks. Metall mittemetall Metallid on ained, millel on tahkes olekus iseloomulik läige, hea elektri ja soojusjuhtivus ning tavaliselt ka hea mehaaniline töödeldavus, suur plastsus ja elastsus. Metallide omadused on seletatavad aatomi tuumaga nõrgalt seotud vabade elektronide (valentselektronide) olemasoluga nende kristallivõre aatomite välimises elektronkihis. Metallid loovutavad kergesti väliskihi elektrone, mis on omakorda mõjutatavad välise elektriväljaga, andes korrapärase elektronide voolu ja hea elektrijuhtivuse. Metallide hulka kuulub keemilistest elementidest 80%, kusjuures kõik metallid peale
KEEMIA KT Mõisted 1) Redutseerija on aine, mille osakesed loovutavad elektrone (ise oksüdeerudes). On metall. (KATOOD) 2) Oksüdeerija on aine, mille osakesed liidavad elektrone (ise redutseerudes). (ANOOD) 3) Metallid on kergesti töödeldavad, nad on plastilised. 4) Elektrolüüs on elektrivoolu toimel aine saamine. Aine lagundamine elektrivoolu toimel. Elektrolüüsi korral toimuvad redutseerumine ja oksüdeerumine eraldi elektroodidel. Elektroodi, millel toimub redutseerumine, nimetatakse katoodiks, elektroodi, millel toimub oksüdeerumine, nimetatakse anoodiks. 5) 6) Maagi rikastamine: rikastamisel eraldatakse maagist suurem osa kõrvalainetest
Pentaan C5H12 Heksaan C6H14 Heptaan C7H16 Oktaan C8H18 Nonaan C9H20 Dekaan C10H22 Undekaan C11H24 Dodekaan C12 H26 Tridekaan C13H28 Tetradekaan C14H30 Pentadekaan C15H32 Reaktsioonivõrrandis Mittemetallioksiidid + Vesi = Hape Sool + Hape = Uus hapse + Uus sool SiO2 (liiv) veega ei reageeri Tekkiv hape peab olema algsest nõrgem Metallioksiidid + Vesi = Alus Sool + Sool = Sool + Sool Ainult IA/IIA metallid Lähteained peavad vees lahustuma. Üks tekkivatest ainetest peab sadestuma Hape + Alus = Sool + Vesi Metall + Hape = Sool + Vesinik (H2 ) Metall pingereas vesinikust eespool Mittemetallioksiid + Alus = Sool + Vesi Metall + Mittemetall = Sool Metallioksiid + Hape = Sool + Vesi IA/Ca alarühma metallid + Vesi = Alus + H2
Metallid redutseerijana: · võivad elektrone ainult loovutada, (vt D, käituvad alati reaktsioonides redutseerijana · metallide keemilist aktiivsust reaktsioonides veega või vesilahustega iseloomustab metallide pingerida. 4.Metallide füüsikalised omadused ja nende võrdlus mittemetallide omadustega. Neil on iseäralik läige, peegeldusvõime. Eriti hästi peegeldavad valgust Ag; Al; In. Mg; Al; Au; Cu; omavad pulbrina läiget, ülejäänud metallid on pulbrina hallid või mustad. Juhivad hästi soojust ja elektrit. Metallid on plastilised see on omadus muuta välisjõu mõjul kuju ja jõu lakkamisel see kuju säilitada. Kuna metalli kuju saab muuta , saab metalli sepitseda, valtsida jne. Hästi sepitsetav on N: kuld. 5.Metallide keemilised omadused: metallide reageerimine hapniku, väävli, kloori, lahjendatud hapete, leeliste, soolade vesilahustega ja veega Näited.
SISUKORD Tunnused Tahked ained Difusioon Soojusjuhtivus Sisehõõrdumine Tahkiste liigid Kristallide struktuur Metallid TUNNUSED: Tahkete ainete kuju ja ruumala säilib Tõmbe- ja tõukejõud molekulide vahel on väga suured Molekulide paigutus tahkistes korrapärane Amorfsetes molekulide paigutus korrapäratu Korrastatus tahkistes- kaugkorrastus Korrastatus amorfsetes- lähikorrastus TAHKED AINED TAHKISED AMORFSED (kivi, kristallid jne) (plastiliin, pigi) Difusioon Difusioon Soojusjuhtivus Soojusjuhtivus Sisehõõrdumine Sisehõõrdumine
Siirdemetallid Siirdemetallid Teisisõnu d-elemendid Perioodilisustabeli B-rühma metallid Kõvad metallid Kõrge sulamistemperatuur Värvus hõbevalgest terashallini Nt raud, vask, tsink Raud Tähtsaim siirdemetall 4.perioodi VIII B-rühmas Põhilised oksüdatsiooniastmed II ja III Suhteliselt õhuke metall Korrodeerumisel vees või niiskes keskonnas tekib raua pinnale kohev, poorne, punakaspruun roostekoht Kõrgemal temperatuuril raud põleb Organismis vajalik hemoglobiini ja punaste vereliblede tootmiseks Sulamistemperatuur 1 538 °C Vask Kaks stabiilset isotoopi
REAGEERIMISED 1. Aluseline oksiid + Vesi = Leelis · Reageerivad ainult aktiivsed metallid, IA ja IIA alates kaltsiumist. 2. Aluseline oksiid + Hape = Sool + Vesi · Reaktsioon toimub alati. 3. Aluseline oksiid + Happeline oksiid = Sool (happelisele oksiidile vastava happe sool) · Reaktsioon toimub alati. 4. Happeline oksiid + Vesi = Oksiidile vastav hape · Veega ei reageeri SiO 5. Happeline oksiid + Alus = Sool (happelisele oksiidile vastava happe sool) + Vesi · Reaktsioon toimub alati
Mõisted: Laeng-iseloomustab keha aktiivsust elektri-ja magnetnähtuvustes. Laengud looduses-positiivsed(prootonid)negatiivsed(elektronid) Elementaarlaeng-vähim võimalik laengu väärtus Juhid-kõik metallid,neil on vabu elektrone ja sp.juh.hästi voolu. Pooljuhid-elektrijuhtivuselt metallide ja isolaatorite vahepeal, nad ei juhi voolu nii hästi nagu metallid ega ole päris isolaatorid. Dielektrikud-isolaatorid ehk mittejuhid ei juhi voolu-kumm,klaas. Coulombi seadus-2 laengut mõjutavad teineteist jõuga,mis on võrdeline nende laengute korrutisega ja pöördvõrdeline nende laengutevahelise kauguse ruuduga. Punktlaengud-laetud keha,mille mõõtmeid võib mitte arvestada. Erinimelised tõmbuvad,samanimelised tõukuvad. Dielektriline läbitavus näitab mitu korda on antud keskkonnas laengute vastastikune mõju väiksem võrreldes vaakumiga.
(Metalli aktiivsus ) Reaktsioonisaaduse koostis sõltub metallist, happe kontsentratsioonist (tingimused) Mida lahjem on lämmastikhape ja mida aktiivsem on metall, seda rohkem redutseerub NO3 ioon Peale lämmastikühendite tekib reaktsioonis vastava metalli nitraat, gaas ja vees Väheaktiivsete metallide (Cu, Ag, Hg) reageerimisel kontsentreeritud HNO3-ga tekib No2, lahjendatud HNO3-ga NO. Tugevasti lahjendatud HNO3-ga (~1,3%) väheaktiivsed metallid ei reageeri Pingerea keskel seisvate metallide (näit. Zn) reageerimisel kontsentreeritud HNO3-ga on põhisaaduseks NO2. Zn reageerimisel lahjendatud HNO3-ga sõltuvalt happe kontsentratsioonist võivad tekkida NO, N2O, N2 või nende gaaside segu. Tugevasti lahjendatud HNO3 puhul on põhisaaduseks NH4NO3 Fe, Co, Ni, Cr, Al pinnal tekib kontsentreeritud HNO3 toimel toatemperatuuril oksiidne kaitsekiht ja nad passiveeruvad