happelised - enamasti mittemetalli oksiidid (B met max o- MgBr2 + 2KOH - Mg(OH)2 + 2KBr astmega) · täielik ioonvõrrand amfoteersed - nii aluselised kui happelised Al2O3, Zn Mg + 2Br + 2K + 2OH - Mg(OH)2 + 2K + 2Br neutraalsed - ei al ega hap, NO, CO, N2O Mg + 2OH Mg(OH)2 Oksiidide saamine Soolade saamine · Lihtaine + O2 oksiid · Lihtainetevaheline reaktsioon · Ml hüdroksiidi lagunemine 2Al + 3Cl 2AlCl3 Fe(OH)3 Fe2O3+ H2O · Alus + hape sool + vesi · Karbonaadi lagunemine CaCO3 CaO + CO2 2LiOH + H2SO4 Li2SO4 + 2H2O · Aluseline oksiid + hape sool + vesi
lidumine looduses ja üldiseloomustus Iseloomustus: on mittemetall. Lämmastik (ladina keeles nitrogenium; tähis N) on keemiline element järjenumbriga 7.Tal on kaks stabiilset isotoopi massiarvudega 14 ja 15.Ta moodustab kaheaatomilisi lihtaine molekule, mis on keemiliselt väga püsivad. Tavatingimustes on lämmastik värvitu, lõhnatu ja maitsetu gaas. Kondenseerub -196C värvituks vedelikusk Lämmastik on suurim üksik koostisosa Maa atmosfääri (~75%). See on loodud tuumasünteesi protsessiga tähtedes, Molekulaarne lämmastik ja lämmastiku ühendid on avastatud tähtedevaheline kosmose astronoomide kasutades Far Ultraviolet Spectroscopic Explorer. Molekulaarne lämmastik on
F2+H2O=2HF+O (muutub vedelikuks) Keemilised: *Põleb ,reageerib O2-ga,leek on nähtamatu(helesinine) *H ja O2 segu on plahvatusohtlik. ¤2H2 + O2= 2H2O ¤H2+F2=2HF *Reageerib väävli ja N-ga kuumutamisel,reageerib vähe aktiivse metallidega. 3H2+N2=2NH3 *Metallide reageerimiseks happega ja elektrolüüsiga ,saadakse vesiniku. *Tööstulikult saadakse vesinikku metaani lagundamisel.(O2 ei tohi ligi pääseda) HAPNIK: Allotroop-Sama keemilise elemendi erinevakoostisega lihtaine.(O2 , O3) Füüsikalised omadused: O2 *Värvitu,suurtes koguses on sinine *Lõhnatu *Toetab eluprotsessi,puhtal kujul mürgine. *Keemistemp. -183kraadi. O3 *sinine *vastik lõhn *mürgine(inimestele, bakteritele) *keemistemp. -112 kraadi. Keemilised omadused:
Oksiidid on liitained, mis koosnevad kahest elemendist, millest üks on hapnik. Oksüdatsiooniaste näitab liidetud või laenatud elektronide arvu. Reeglid: Lihtaine oa = alati 0 Hapniku oa ühendis on alati II A-rühmade metallid on kindlalt oa-d, mis võrduvad rühma numbriga (elektronide arv väliskihis = rühma numbriga). Oa määramine ühendis (hapniku või vesiniku kaudu) (akna meetodiga). Õhu koostis: õhk on gaaside segu; kõige enam leidub õhus lämmastikku (78%); teine peamine õhu koostisosa on hapnik (21%) kõigist õhus esinevatest gaasiliste ainete osakestest on hapniku molekulid; kõik ülejäänud õhus leiduvad gaasilised ained argoon, süsihappegaas (0,03%), veeaur ja veel mõned moodustavad kokku vaid umbes 1% õhu koostisest. Puhas õhk on läbipaistev, värvuseta, maitseta ja lõhnata. Järelikult on niisuguste omadustega ka õhu peamised koostisained hapnik ja lämmastik. Eluslooduse jaoks on õhu tähtsaim koostisosa hapnik. See koosneb kaheaat...
ühised elektronpaarid iooniline side - mittemetalliliste ja metalliliste ainete vahel esinev side, kus aatomid loovutavad ja liidavad elektrone molekulaarne aine - aine, mis koosneb molekulidest (kovalentne side) mittemolekulaarne aine - aine, mis koosneb ioonidest või kristallidest (iooniline side) molekulvalem - valem, mis näitab molekuli koostist: keemiliste elementide sümboleid ja alaindekseid (aatomite arvu molekulis) lihtaine - aine, mis koosneb vaid ühe keemilise elemendi aatomitest liitaine - aine, mis koosneb kahest või enamast keemilise elemendi aatomitest puhas aine - liht- või liitaine, mis koosneb ühesugustest aineosakestest ainete segu - segu, mis koosneb vähemalt kahe erineva aine osakestest ning tihti on võimalik segust puhtaid aineid eraldada Tuntumad molekulid Lämmastik (moodustab 78% õhust) - N2
HALOGEEN ID TOOMAS RÜÜTEL 11.KLASS TEXT MIS NEED ON? ▸ Halogeenid on VII A rühma elemendid.(F, Cl, Br, I, At) ▸ Nimetus ,,Halogeen” on tulnud kreeka keelest. See tähendab ,,soola moodustajat” ▸ Looduses halogeen lihtainena ei leidu. FLUOR(F) ▸ Fluor on keemiline element järjenumbriga 9. ▸ Floral on üks stabiilne isotoop massiarvuga 19. ▸ See on normaaltingimustel kollakas gaas. ▸ Fluor moodustab kaheaatomilisi lihtaine molekule. ▸ Reageerib ägedalt paljude liht- ja liitainetega. ▸ Inimorganismile mõjub söövitavalt. ▸ See on kõige elektronegatiivsem element ja hologeenidest on kõige elektronegatiivsem. ▸ Universumis on Fluor üsna levinud element, Maal on ta levikult 17. ja maakoores 13. kohal. ▸ Fluori saadakse vedela vesinikfluoriidi ja kaaliumfluoriidi elektrolüüsil 100 kraadi juures. ▸ Fluori kasutatakse fluorsüsinike(nagu nt. plastmass)
Koostaja: Juhendaja: jood Jood on keemiline element järjenumbriga 53. Tal on stabiilne isotoop massiarvuga 127. Joodi täpne aatommass on 126,90447 aatommassiühikut. Jood on halogeen. Jood moodustab kaheaatomilisi lihtaine molekule. Normaaltingimustes esineb jood tumepruunide kristallidena, mis sulavad temperatuuril 113 °C ja keevad temperatuuril 184 °C. Joodi aur on lillaka värvusega . Tal puudub vedel olek. Jood on keemiliselt aktiivne, kuigi teistest halogeenidest vähem aktiivsem. Ta juhib elektrit, ja on läikega Joodi kasutatakse meditsiinis. joodi saab kindlaks teha tärklisega, pannes tärklise peale joodi muutub see sinakaslillaks . Inimorganismis võib leiduda joodi kilpnäärmest.
omadustega. Happeliste oksiidide reageerimine veega Enamik happelisi oksiide reageerib veega, moodustades vastava happe. Osa nõrgalt happelisi oksiide ei reageeri veega. Tuntumaid nendest on SiO2. TV lk 18 G Vesi H2O · Vesi on väga erandlike omadustega oksiid. · Ta on mittemetallioksiid, kuid võib reageerida nii aluseliste kui happeliste oksiididega, seega... Oksiidide saamine · Paljusi oksiide võib saada vastava lihtaine reageerimisel hapnikuga (enamasti põlemine). · Vähemaktiivsed lihtained reageerivad hapnikuga suhteliselt aeglaselt ja leegita. · Nt Na + O Ülesanded TV lk 19 ül 5.3. A (1), B (1), C (1) Järgmise tunni tunnikontroll "Oksiidid" · Oksiidi mõiste · Oksiidide nimetamine · Oksiidi valemi koostamine · Oksiidide liigitamine · Kirjuta ja tasakaalusta reaktsioonivõrrand oksiidi reageerimisel veega.
Samuti on raud Maa koostises üks levinuimatest elementidest. Referaadi eesmärgiks on saada rohkem teada rauast. Ülesanneteks on uurida, millised on raua omadused ja millised on tema sulamid. Töö koosneb ühest peatükist, milles räägitakse rauast üldiselt, selle omadustest ja selle kahest sulamist. 3 1. RAUD Raud on lihtaine ning ehedalt leidub rauda ainult meteoriitide koostises ja ka paljude ühendite koostises. Näiteks: vees, liivas, savides, mineraalides, taimedes, inimese veres, maasikates ja nõgestes. (Protonizer, 2007) Raua järjenumber on 26. Raud asub Perioodilisussüsteemi VIII B rühmas ja 4. perioodis. See on kõige levinum element Maa koostises ning levimuselt maakoores teine metall alumiiniumi järel. Raual on neli stabiilset isotoopi massiarvudega 54, 56, 57 ja 58. (Vikipeedia, 2007b)
sisepõlemismootori klapid, silindrid, kolvid) elektrokeemiline korrosioon: On seotud galvaaniaelementide tekkimisega (juhib elektrit), toimub kui kaks erinevat metalli on kontaktis elektrolüüdi lahusega bioloogiline korrosioon: Biokorrosioon tekib bakterite, seente ja vetikate poolt eritatavate ainete toimel (nt rauabakterid ja väävlibakterid) metall: lihtaine, millel on metallidele iseloomulikud omadused, keemilistes reaktsioonides käitub redutseerijana. maak: kivim või mineraal, mis on mingi lihtaine saamisel tooraineks aluminotermia: metallide saamine ühendist alumiiniumiga redutseerimise teel karbotermia: metalli redutseerimine maagist süsiniku või süsinikoksiidi abil kõrgel temperatuuril
süsinikuühendeid oluliselt rohkem kui kõiki teisi ühendeid kokku. Süsinikuühendid on eluslooduse aluseks ja nende uurimisega tegeleb orgaaniline keemia. Kuigi süsinik ei kuulu levinumate elementide hulka maakoores ( ta moodustab u. 0,1 % maakoore massist) on ta eluslooduse põhiline koostiselement. Süsinik võib moodustada mitmeid erineva ehitusega allotroopseid teisendeid.Tuntumad nendest on teemant ja grafiit. Teemant on korrapärase ehitusega ja ta on kõige kõvem lihtaine. Teemantnuge,-puure jt. tööriistu kasutatakse mitmesuguste kõvade ainete töötlemisel ( klaasi lõikamisel ). Läbipaistvad suured teemandikristallid on hinnalised vääriskivid. Lihvitud teemante kutsutakse briljantideks. Grafiit on tumehall, metallidele iseloomuliku läikega kristalne aine. Ta on üsna pehme ja muutub lõhenedes kihtidideks. Selle omaduse tõttu kasutatakse grafiiti pliiatsi südamike ja määrdeainete valmistamiseks. Kuigi grafiit on mittemetall juhib ta hästi elektrit.
Elektrokeemiliseks-toimumise tingimuseks on metalli kokkupuude elektrolüüdilahusega. Soodustavad tingimused: Metalli iseloom, välistingimused, metall, mis sisaldab lisandina vähemaktiivseid lisandeid korrodeerub kiiremini kui puhas metall, lahuses esinevad lisandid. Kaitsevõimalused: Metalli kaitsmine emaili-,värvi-lakikihi abil, metalli kaitsmine korrosioonikindlamast metallist kaitsekihiga. Maak-kivim või mineraal, mis on mingi lihtaine saamisel tooraineks. Maagi rikastamine-rikastamisel eraldatakse maagist suurem osa kõrvalainetest. Maagis sisalduvate ainete üksteisest eraldamine kasut. Enamasti ära nende ainete füüsikaliste omaduste erinevust. Metalli saamise 4 võimalust maagist: redutseerimine süsiniku või süsisinikoksiidiga, redutseerimine alumiiniumiga, rikastamine, särdamine. Sulam Koosneb: 1.metall+metall, 2.metall+mittemetall Eelised võrreldes lihtmetalliga: Madalam sulamistemperatuur kui seda moodus
Kiviõli 1 Keskkool Kätlin Palm 7b Fluor Kiviõli 2006 Mis on fluor? · Fluor on keemiline element järjenumbriga 9. · Fluor on helekollase värvusega, õhust veidi raskem, terava lõhnaga väga mürgine gaas. · Ta moodustab kaheaatomilisi lihtaine molekule. · Ta reageerib ägedalt paljude liht- ja liitainetega. · Ta on keemiliselt kõige aktiivsem mittemetall. · Toatemperatuuril ühineb fluor plahvatuse saatel õhus leiduva -vesinikuga, mille tulemusel tekib vesinikfluoriid HF. Viimase sooli nimetatakse fluoriidideks (metalli ja fluori ühendid). · Kokkupuutel fluoriga ained süttivad. Isegi vesi süttib fluoris põlema, mille tulemusel tekib hapnik. See on äärmiselt ebatavaline reaktsioon:
Liitium Liitium on hõb e v al g e ja erak ord s e lt kerg e m etal, mis sulab temp e r aturril 180°C. Ta on kõrge väiksema tihedusega metal ja üldse kõige väiksema tihedusega normaaltingimusel tahke lihtaine: tema tihedus on 0,535g/cm³. Liitium on esikohal metallide hulgas kerguse poolest. Ta on viis korda kergem kui alumiinium ja kaks korda kergem kui vesi. Seepärast ujub liitium mitte ainult veepinnal vaid isegi petrooleumis. Liitium on leelismetall. Keemiliselt on ta väga aktiivne. Kõigis ühendites on liitiumi oksüdatsiooniaste 1. Liitium reageerib aeglaselt õhuga ja tõrjub veest vesinikku välja, moodustades hüdroksiid. Erinevalt
Aatomnumber: 19 Aatommass: 39,098 Klassifikatsioon: leelismetallid, s-elemendid Aatomi ehitus: · Elektronvalem: 1s2 2s2p6 3s2p6 4s1 · Elektronskeem: +19|2)8)8)1) · Elektronite arv: 19 · Neutronite arv: 20 · Prootonite arv: 19 · Oksüdatsiooniast(m)e(d) ühendites: 0, I · Kristalli struktuur: ruumikeskne kuubiline Füüsikalised omadused: · Aatommass: 39,098 · Sulamistemperatuur: 63,25 °C · Keemistemperatuur: 759,9 °C · Tihedus: 0,862 g/cm3 · Värvus: hõbevalge · Agregaatolek toatemperatuuril: tahke · Kõvadus Mohsi järgi: 0,4 · Isotoobid: Nukliid Levimus (%) Mass Poolestusaeg 39 K 93,22 38,9637 - 40 K 0,118 39,974 1,28 · 109 aastat 41 K 6,77 40,9618 ...
Glkoos ehk viinamarjasuhkur-on monosahhariid,mis kuulub disahhariidide sahharoosi ja laktoosi koostisse. Fruktoos-on ks monosahhariididest. Trklis-on taimedes olev polsahhariid. Tselluloos-polsahhariid. Anioon-neg. laenguga ioon. Katioon-pos. laenguga ioon. Elektron-neg. laenguga aatomi koostisosa. Prooton-pos. laenguga tuumaosake. Hape-aine,mille vesilahuses on lekaalus vesinikioonid vrreldes hdroksiidioonidega. Oksiid-elemendi hend laenguga. Eksotermiline reaktsioon-on keemiline reaktsioon,mille kigus eraldub soojust. Endotermiline reaktsioon-on keemiline reaktsioon,mille kigus neeldub soojust. Ensmid- on bioloogilised katalsaatorid. Katalsaator-on aine,mis muudab reaktsiooni kiirust,kuid vabaneb prast reaktsiooni lppu endises koguses. Indeks-on aine valemis esinev number,mis nitab antud elemendi aatomite arvu valemis. Sulam-on kahe vi enama metalli vi metalli ja mittemetalli kokku sulatamisel saadud aine. Korrosioon-metallide hvinemi...
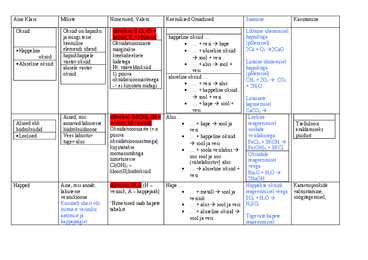
Aine Klass Mõiste Nimetused, Valem Keemilised Omadused Saamine Kasutamine Oksiid Oksiid on hapniku üldvalem: E2On (O = Lihtaine ühenemisel ja mingi teise hapnik, E = element) happeline oksiid ... hapnikuga keemilise Oksüdatsiooniaste · ... + vesi hape (põlemisel) · Happeline elemendi ühend märgitakse · ... + aluseline oksiid 2Ca + O2 2CaO oksiid hapnikhappele kreekakeelsete sool + vesi
· Pürometallurgilised meetodid · Hüdrometallurgilised meetodid · Elekrtometallurgilised meetodid Tavaliselt ei ole metallid lisanditest täiesti puhtad, vajadusel neid puhastatakse, kuid üldiselt on täiesti puhta metalli saamine väga kallis. Seda tehakse vaid haruldaste ja väga väärtuslike metallide puhul. Enamasti ei ole aga metalli absoluutne puhtus vajalik, sest põhiliselt kasutatakse argielus metallide sulameid. Sulam saadakse vähemalt kahe lihtaine sulatatult segamisel. Tavaliselt on sulami koostiseks metallid, kuid esineb ka mittemetalle. Väga levinud on süsiniku sisaldus rauasulamites. Näiteks teras ja malm. 3 Pürometallurgilised meetodid Pürometallurgia on vanim metallurgiaharu. Pürometallurgia maake redutseeritakse kõrgel temperatuuril, redutseerijate järgi jaotatakse sedasi: karbotermia, vesiniku kasutamine ja metallotermia. Redutseerijana käsutatakse süsinikku, süsinikoksiidi, vesinikku, alumiiniumi, jt.
Kuna nende molekulide vahel on suhteliselt nõrgad molekulidevahelised jõud, siis on halogeenidel madalad keemistemperatuurid. Kõik halogeenid, eriti fluor ja kloor on lihtainena tugevalt mürgised. Halogeeniaurud on terava lõhnaga ja kahjustavad hingamisteid. Seetõttu tuleb kõik halogeenidega tehtavad katsed sooritada töötava tõmbega tõmbekapis. 3 2 Halogeenide omadused Halogee Lihtaine Värvus Olek Omadused Lisa n valem Õhust raskem, terava Ainus lihtaine millega vesinik lõhnaga, väga mürgine, kõige reageerib toatemperatuuril Fluor F Kahvatu Gaasiline aktiivsem mittemetall ilma täiendavate tingimusteta,
Mittemetallid Mis on mittemetall? · Nimigi ütleb - ei ole metall. Täpsemalt, mittemetall on lihtaine, millel ei ole metallidele iseloomulikke omadusi, nende väliselektronkihis on tavaliselt 4-8 elektroni. Aga miks erinevad mittemetallid metallidest? · Peamine põhjus on nende ehitus, kus kõik aatomid on omavahel ühendatud (ei jää sellist vaba ruumi nagu metalli kristallis, kus elektronid saaksid vabalt liikuda). Mis siis iseloomustab mittemetalle? · Nende ehitusest tulenevalt ükski mittemetall ei ole hea elektri- ega soojusjuht
mittemetallilised omadused, rühmades ülevalt alla tugevnevad metallilised omadused ja nõrgenevad mittemetallilised omadused. 3. Elementide sümbolid Elementidele antakse ka kindel keemiline sümbol, mis põhineb elemendi ladinakeelsel nimetusel. Keemilised sümbolid võimaldavad keemikute suhtlemist hoolimata keelte erinevustest. 4. Lihtained, liitained, metallid, mittemetallid, oksiidid, happed, alused, soolad Lihtaine on keemiline aine, milles esinevad ainult ühe elemendi aatomid. Lihtaine on näiteks kolmeaatomiline osoon (O3). Liitaine on keemiline ühend, milles esinevad kahe või enama keemilise elemendi aatomid. Liitained on näiteks vesi (H2O), keedusool (NaCl) ja süsihappegaas (CO2). Metallideks nimetatakse keemilisi elemente, millel on vabu elektrone ja
Vahevöö ülaosas asub mõnesaja km paksune plastiline astenosfäär, kus tekib basaltne magma. Maakoort koos astenosfääri peale jääva vahevöö osaga nimetatakse litosfääriks (O, Si, Fe, Mg, Ca, Al, K, Na). Maa tuum jaguneb vedelaks välis- ja tahkeks sisetuumaks. Vahevöös tekivad kivimainesse soojuslikud konvektsioonivoolud (võrreldav vee liikumisega soojenevas anumas). Mineraal (3600 eri liiki) on looduslik tahke lihtaine või keemiline ühend, mis esineb iseloomuliku kuju ja kindla struktuuriga kristallina (grafiit, teemant). Mineraalid tekivad looduses aine tahkestumise e. kristalliseerumise või temperatuuri ja rõhu suurenemise e. ümberkristalliseerumise käigus nii tahketest ainetest kui vedelikest. Kivim on mineraalide tugevalt kokku tsementeerunud kogum, jagunedes tard- e. magma- (tekivad süvakoore ja vahevöö ülessulamisel tekkinud magma
MÕISTED: aluminotermia-lihtaine(enamasti metallide) saamine ühenditest alumiiniumiga redutseerimise teel elektrolüüs-elektsivoolu läbijuhtimisel lahustest või sulatatud elektrolüüdist elektroodidel kulgev redokreaktsioon karbotermia-metalli redutseerimine maagist süsiniku või süsinikoksiidi abil kõrgel temperatuuril keemiline vooluallikas-saade, milles keemilises reaktsioonis vabanev energia muudetakse vahetult elektrienergiaks. korrosioon- metalli hävimine(oksüdeerumine) keskkonna toimel oksüdeerija-aine, mille osakesed liidavad elektrone(ise redutseerudes) oksüdeerumine-elektronide loovutamine redoksreaktsioonis;sellele vastab elemendi oksüdatsiooniastme suurenemine redutseerija-aine, mille osakesed loovutavad elektrone(ise oksüdeerudes) redutseerumine-elektronide liitmine redoksreaktsioonis;sellele vastab elemendi oksüdatsiooniastme vähenemine sulam-mitmest metallist või metallist ja mittemetallist koosnev metalliliste omadustega ...
Aatomituum koosneb prootonitest ja neutronitest Massiarv Prootonite (Z) ja neutronite (N) koguarv tuumas. Tahistatakse tahega A. Aatommassi ummardatud arv. Isotoop Uhe ja sama keemilise elemendi teisendid, millel on aatomituumas uhesugune arv 235 238 prootoneid, kuid erinev arv neutroneid. Naiteks 92U ja 92U . Uhe ja sama keemilise elemendi isotoopidel on suhteliselt sarnased omadused. Keemiline element Liit- voi lihtaine koostisosa (aatom), mis pole keemiliselt lagundatav. 118 keemilist elementi. Iga elemendi aatomil on oma aatomnumber ja tuumalaeng. Tuumajõud Nukleone hoiavad tuumas koos tugeva vastastikmoju joud (tuumajõud), mis ei lase nukleonidel eemalduda kaugemale kui moni fermi (1 f = 10-15 m) ega laheneda alla uhe fermi Uhed tugevamad joud looduses, mida tuntakse. Vaikese mojuraadiusega (tuuma labimoot). Tuumajoud seob nukleonid tuumas uhtseks ehk hoiab tuumaosakesed koos.. Massidefekt
Aatomvõre-kristallivõre,kus võre sõlmpunktides asuvad aatomid. Atomaarne aine-lihtaine,mis koosneb omavahel seostumata üksikaatomitest. Binaarne ühend-ühend,mis koosneb kahe elemendi aatomitest(H2O.NaCl) Dihapnik-hapniku levinuim ja püsivaim allotroop,koosneb kaheaatomilistest molekulidest Ekso-soojuse eraldumisega kulgev keemiline reaktsioon Endo--soojuse neeldumisega kulgev keemiline reaktsioon Elektroneg-suurus,mis iseloomustab keemilise elemendi aatomi võimet keemilise sideme moodustumisel tõmmata enda poole ühist elektronpaari. Elektronskeem-aatomi elektronkatte ehitust kirjeldav skeem,mis näitab elektronide arvu elektronkihtides Na +11|2)8)1) Elektronvalem-aatomi elektronstruktuuri kirjeldav ülskirjutus,mis näitab elektronide jaotumist kihtidesse ja alakihtidesse.Na 1s22s22p63s1 Grafiit-süsiniku kihilise ehitusega allotroop,hea elektrijuht Iooniline aine-ioonilise kristallivõrega aine,mis tekib vastasmärgiliste laengutega ioonide ...
Lämmastik 1)Aatomi ja molekuli ehitus: N: +7| 2) 5) Lämmastiku järje- ehk aatomnumber on 7, ta kuulub perioodilisustabeli VA rühma elementide hulka, asudes 2. perioodis. Lämmastiku aatomis on 7 prootonit, 7 elektroni ja 7 neutronit. Lämmastiku aatomi väliskihis on viis elektroni ning lämmastiku aatomid võivad elektrone nii liita kui ka loovutada. Seetõttu on lämmastiku oksüdatsiooniaste ühendites 3 kuni +5. 2)Lihtaine omadused 2.1)Füüsikalised omadused: · terava lõhnaga · värvuseta · gaas · õhust ~2 korda kergem · vees väga hästi lahustuv · veeldub 33oC juures NB! 25% line lahus võib põhjustada hingamislihaste krampi ja silma sattudes pimedaks jäämise. 2.2)Keemilised omadused: Lämmastik on väga püsiv, sest molekulis on tal aatomite vahel tugev kolmikside NºN , mistõttu ta onkeemiliselt väheaktiivne.Lämmastik reageerib kõrgel temperatuuril, mil side ...
KEEMIA Aatom-aineosake mis koosneb aatomituumast ja elektronidest;molekuli koostisosa Alus-aine mis annab lahusesse hüdroksiidioone Aluseline oksiid-hüdroksiid millel avalduvad nii alulised kui ka happelised omadused Anioon-neg. Laenguga aatom või aatomite rühmitus Elektronegatiivsus-suurus mis iseloomustab keemilise elemendi aatomi võimet keemilise sideme moodustamisel tõmmata enda poole ühist elektronpaari Elektronskeem-aatomi elektronkatte ehitust kirjeldav skeem mis näitab elektronide arvu elektronkihtides Hape-aine mis annab lahusesse vesinikioone Hapnikhape-hapniku sisaldav mineraalaine Hüdrooksiid-anorgaaniline ühen mille koostisesse kuuluvad hüdrooksiidioonid OH- või hüdroksiidrühmad OH Hüdrolüüs-aine keemiline reaktsioon veega:soola hürdolüüs on neutralisatsioonireaktsiooni pöördereaktsioon Ioon-laenguga aatom või aatomi rühmitus Iooni laeng-iooni positiivsete või negatiivsete elementa...
Ehitusmaterjalid Looduslikud ehitusmaterjalid Paas Graniit Savi Liiv Looduslikud ehitusmaterjalid Mineraal on looduslik, enam-vähem kindla koostisega keemiline ühend, mõnel juhul ka lihtaine. Mineraalid on enamasti tahked. Kivimid koosnevad ühest või sagedamini mitmest mineraalist, mis võivad kivimi koostises olla nähtavad eraldi terakeste või kristallidena. Eestis on looduslikest kivimitest ehitusmaterjalidena tähtsaimad paas ja graniit ning need mõlemad on laialt levinud. Paas Pae peamiseks koostisosaks on kaltsiumkarbonaat (CaCO3). Paas on värvuselt hallikas, ei ole väga kõva - laguneb kergesti kihtideks ja teda on lihtne töödelda (raiuda ja saagida)
Mõisted:Laam-litosfääri plokk,mis triivib astenosfääri.Mineraal-looduslik tahke lihtaine või keemiline ühend millel on iseloomulik kristallstruktuur.Kivim-loodusliku tekkega mineraalide tsemsnteerunud mass.Tardkivim-nii maakooress kui ka maapinnal magmast tardunud kivim.Settekivim-teke algab maapinnal murenenud kivimitest pärit pudeda kruusa,liiva,savi jt setete kuhjumisega,kivimiks saab sete alles kivistudes.Moondekivimid-maakoores kõrgenenud rõhu ja temperatuuri(200-650C)tingimustes moondunud kivimid.Maak-majanduslikku huvi pakkuvad kivimid ja mineraalid
Mittemetallid ja nende omadused Mis on mittemetall? - Nimigi ütleb - ei ole metall. Täpsemalt, mittemetall on lihtaine, millel ei ole ______________metallidele iseloomulikke omadusi; nende väliselektronkihis on tavaliselt 4- _8___ elektroni. Mis siis iseloomustab mittemetalle? Nende ehitusest tulenevalt ükski mittemetall ei ole hea _elektri ega soojusjuht________ (välja arvatud süsiniku allotroop grafiit). Sellest tulenevalt koosnevad elektri- ja soojusisolatsiooni materjalid mittemetallidest Kui metallid olid enamasti tahked ained, siis mittemetallid on enamasti _____gaasid_____ (hapnik, vesinik,
sisaladavaid soolasid mineraaljärvedes, soolaallikates ja jõgedes. KLOORI SAAMINE · Tööstuslikult saadakse tänapäeval kloori NaCl lahuse elektrolüüsil. 2NaCl + 2H2O --------® 2NaOH + H2 + Cl2 · Laboratooriumis peamiselt vesinikkloriidhappest oksüdaeerijate toimel 4HCl + MnO = MnCl2 +Cl2 + 2H2O AJALUGU · Kloori nimetus tuleb kreekakeelsest sõnast chloros, mis tähendab tõlkes kahvaturohelist. · Kloori kui lihtaine avastas 1774. aastal Rootsis teadlane Carl Wilhelm Scheele, kui ta kuumutas keedusoola ja väävelhappe segu mineraal pürolusiidiga. · 1810.a tõestas H. Davy tõestas, et tegu oli lihtainega (Cl) ja pani sellele nime. · Kloor oli ka esimene gaas, mida kasutati sõjanduses. 1915. aprill vabastas Saksa armee prantslaste, kanadalaste ja aafriklaste poole 180 tonni kloori gaasi. Kannatada sai umbes 20 000 inimest. 5000 neist suri ning paljud jäid eluks ajaks vigaseks.
....................................................................6 Kasutatud kirjandus.....................................................................................................................9 2 Jood Jood on keemiline element järjenumbriga 53.Tal on üks stabiilne isotoop massiarvuga 127.Jood on halogeen. Ta moodustab kaheaatomilisi lihtaine molekule. Normaaltingimustes esineb jood tumepruunide kristallidena, mis sulavad temperatuuril 113°C ja keevad temperatuuril 184°C, moodustades lillaka auru. Jood on keemiliselt aktiivne, kuigi teistest halogeenidest vähem aktiivne. Elusorganismidele mõjub enamasti kahjulikult. Jood organismis on lokaliseerunud kilpnäärmesse, kus ta on vajalik kilpnäärme hormoonide sünteesiks ja kilpnäärme normaalseks talitluseks. Kilpnäärme hormoonid mõjutavad tugevasti
Omadused Omadus Hg Sulamistemp, -38,9 Keemistemp, 356,6 Tihedus, kg/m3 (25) 13540 Eritakistus, m 95,8 Maailmatoodang, tonni 4 aastas Elavhõbe on kuivas õhus toatemperatuuril täisti püsiv. Sellel elementidel on mitmeid omadusi, mille poolest ta erineb oma, 12. rühma elementidest, nt. lihtaine aur koosneb peaaegu täielikult üksikutest Hg aatomitest, lihtaine anomaalselt madal sulamis- ja keemistemperatuur ning väike elektrijuhtivus. Elavhõbe on ainus toatemperatuuril vedel metall. Toodang ja kasutamine Enamik tänapäeval toodetavast elavhõbedast saadakse pürometallurgiliselt maakide ja kontsentraatide särdamisel 700-800 juures. Hg eraldub auruna, mis puhastatakse elektrofiltrites tolmust ja kondenseeritakse. Peamised kasutusalad on järgmised:
Kordamisküsimused II Keemiline side 1. Mis on : · Lihtaine aine, mis koosneb ainult ühe keemilise elemendi aatomitest. · Liitaine keemiline aine, mis koosneb mitme erineva keemilise elemendi aatomitest. · Molekul koosneb aatomitest. · Molekulaarne aine · Mittemolekulaarne aine molekulidest koosnev aine. · Keemiline side aatomite või ioonide vaheline side molekulaarses aines.
8d klassi KT kordamisküsimused 1. Mõisted Keemiline element- on kindla tuumalaenguga aatomite liik Aatom- üliväike aineosake, koosneb tuumast ja elektronidest Molekul- koosneb keemilise elemendi aatomist !! lk 57 Liitaine- liitained koosnevad erinevate elementide aatomitest Lihtaine- on aine, mis koosneb ainult ühe keemilise elemendi aatomist Iooniline side- erinimeliste laengutega ioonide vaheline keemiline side Iooniline aine- metall loovutab mittemetallile elektrone, viimasesse kihti tuleb 8 elektroni Katioon- positiivse laenguga ioon Anioon- negatiivse laenguga ioon Kovalentne side- aatomite vaheline keemiline side, mis tekib ühiste elektronipaaride moodustamisel Molekulaarne aine- on molekulidest koosnev keemiline aine Elektronkiht- elektronkatte osa, koosneb tuumast teatud kaugusel tiirlevatest elektronidest Rühm- perioodilisustabelis kõrvuti asuvate elementide rida, mille moodustavad samasuguse väliskihi elektronide ar...
Laam - litosfääri plokk, mis triivib astenosfääril. Mineraal - looduslik tahke lihtaine või keemiline ühend, millel on iseloomulik kristallstruktuur. Kivim - mineraalidega tugevalt kokku tsementeerunud kogu, mis looduses esineb kivimites. Jaotus tekke järgi: tard, sette, moond. Tardkivimid - on kivimid, mis tekivad magma tardumisel maakoores või maapinnal. Settekivimid - on kivim, mis on tekkinud lahustest väljasadestumise teel või murenemissaaduste ja organismide jäänuste ladestumisel ja kivistumisel. Moondekivim - on kõrge rõhu ja temp tingimustes moondunud kivim.
Nimetustes kasutatvad kreekakeelsed arvsõnad Tähtsamad o.-a. lihtainete oksüdatsiooni aste on null 2 - di 5 - penta 8 - okta liitainetes on kõigi aatomite oksüdatsiooniastmete summa null 3 - tri 6 -heksa 9 - nona IA ja IIA ja rühm metallid võrdne rühma numbriga 4 - tetra 7- hepta 10-deka B-rühma metallidel on tavaliselt muutuvad oksüdatsiooniastmed kindel O -II muutuv Fe II ja III H I Cu I ja II F -I Sn II ja IV ...
Lämmastik ja tema ühendid Lämmastik Ladina keeles nitrogenium Tähis N Keemiline element järjenumbriga 7 Kaks stabiilset isotoopi Lämmastik on mittemetall Moodustab püsivaid kaheaatomilisi lihtaine molekule Ühendites on lämmastiku oksüdatsiooniaste 3 kuni +5 On õhu peamine koostisosa 78% Omadused Tavatingimustes on värvitu ja lõhnatu gaas kondenseerub temperatuuril 196° C värvituks vedelikuks moodustab 78 protsenti Maa atmosfäärist aeroobsed organismid ei saa lämmastikku hingamiseks kasutada suuremas kontsentratsioonis lämmatava toimega Kõrgema rõhu all mõjub narkootiliselt Väga kõrgel temperatuuril(üle 3000 OC) reageerib lämmastik : hapnikuga:
perioodideks. Elementide järjekorra tabelis määrab aatomnumber. Elemendi kuuluvuse perioodi määrab elektronkihtide arv ja kuuluvuse rühma elektronide arv väliselektronkihis (õieti valentselektronide arv). Keemiliste omaduste alusel rühmitatakse elemente metallideks, poolmetallideks, mittemetallideks, leelismetallideks, leelismuldmetallideks, halogeenideks, väärisgaasideks, lantanoidideks, aktinoidideks. 6. Metallid ja mittemetallid mittemetall on lihtaine, millel ei ole metallidele iseloomulikke omadusi; nende väliselektronkihis on tavaliselt 4-8 elektroni. Aga miks erinevad mittemetallid metallidest? Peamine põhjus on nende ehitus, kus kõik aatomid on omavahel ühendatud (ei jää sellist vaba ruumi nagu metalli kristallis, kus elektronid saaksid vabalt liikuda. Nende ehitusest tulenevalt ükski mittemetall ei ole hea elektri- ega soojusjuht. Metallideks nimetatakse keemilisi elemente, millel on vabu elektrone ja mis
Litosfäär Maa siseehitus Sisetuum Välistuum Vahevöö (astenosfäär) Maakoor (ookeaniline ja mandriline) Koostiselemendid Mineraal Looduslik tahke lihtaine või keemiline ühend, mis esineb iseloomuliku kuju ja kindla struktuuriga kristallina. 3600 liiki Püriit FeS2 Opaal Teemant Kivim Mineraalide tugevalt kokku tsementeeritud kogum Tard, sette ja moondekivimid Tardkivim Maa süvakoore ja vahevöö kivimite ülessulamisel tekkinud tulivedelast magmast kristalliseerumisel (nt. graniit, basalt). Settekivim Maapinnal murenenud kivimitest pärit pudeda kruusa, liiva, savi jt
maadest, näiteks Horvaatiast (800 000), Kreekast (600 000), Itaaliast (600 000) ja Poolast (200 000). Loodusvarad Austraalias leiduvad loodusvarad: boksiit, süsi, rauamaak, alumiiniumoksiid, kuld, vask, valgetina, hõbe, uraan, nikkel, volfram, mineraalliivad, tina, tsink, teemandid, pruunsüsi, nafta ja maagaas. Boksiit on settekivim, mis koosneb peamiselt alumiiniumoksiidist ja alumiiniumhüdroksiidist. Boksiit on peamine alumiiniumimaak. Süsi on süsiniku aatomitest koosnev lihtaine, mis moodustab looduses mitmeid modifikatsioone. Rauamaak on kivim või mineraal, mis sisaldab piisavalt rauda ning on piisavalt hõlpsalt ligipääsetav, et tema kaevandamine oleks majanduslikult tasuv. Pruunsüsi on pruunika värvusega kaustobioliit. Pruunsüsi tekib kivisöega sarnaselt, kuid enamasti väiksemal mattumissügavusel. Sarnaselt kivisöele kuulub pruunsüsi fossiilsete kütuste hulka ning on tähtis maavara. Pruunsöe kütteväärtus on kivisöe omast väiksem.
sünonüümsed) või orgaanilises keemias levinud hüdroksüülrühma nimetuse segiajamisest hüdroksiidiooniga. Ülesanne 1. Tuli ja vesi Kõnekeeles peetakse vett tule vastandiks, mis tule kustutab. Ometigi ei ole see keemia seisukohalt alati tõene. 1) Milliseid põlevaid aineid/ainete segusid siit nimekirjast ei tohi veega kustutada? Põhjendage valikut! a) toiduõli b) puit c) magneesium d) paber e) puuvill Gaasiline lihtaine X reageerib veeauruga põledes. Moodustub gaasidest A ja B koosnev segu. Kahest elemendist koosnev gaas A sisaldab 5,04% vesinikku ja gaas B tihedus õhu suhtes on ligikaudu 1,1 (õhu molaarmass on 29 g/mol). 2) Leidke ainete X, A ja B valemid ning kirjutage gaasi X veeauruga reageerimise võrrand. Vesi saab toimida ka katalüsaatorina, mis süütab tule. Tilga vee lisamisel reageerib metalli Y pulber tahke lihtainega C, kerkib ere leek ja eraldub lilla aur. Tekivad ühend D, mille
Geograafia kordamine 1) Maa siseehitus: Maa koosneb maakoorest (tahke, tard-, moonde- ja settekivimid), vahevööst (tahke ja plastiline) ja tuumast (tahke). 2) Mandriline ja ookeaniline maakoor Mandriline: vana (1,5 mld), paks (40 km), väiksema rihedusega, ei sukeldu, tekib pidevalt juurde, graniidikihiga. Ookeaniline: noor (200 mln), õhuke (7 km), tihe, sukeldub, hävineb ja uueneb, basaldikihiga. 3) Mineraalid, kivimid, maagid. Mineraal – looduslik tahke lihtaine, kindla kuju ja struktuuriga kristall, ligi 3600 liiki, tekivad tahkestumise käigus. Kivim – mineraalide tugevalt kokkutsementeerunud kogum. Tard-, moonde- ja settekivimid. Nt graniit, basalt. Maak – majanduslik kasu ja võimalus kasutada inimesel oma hüvedeks. 4) Kivimiringe Magma: kristalliseerumisel tardkivim. Tardkivim: murenedes setted, soojuse ja rõhu toimel moondekivim. Moondekivim: sulades magma.
1.Millest koosneb puhas õhk? Puhas õhk koosneb hapnikust, argoonist, süsihappegaasist ja lämmastikust 2.Millised on puhta vee omadused? Puhas vesi on maitsetu, lõhnatu, värvitu, läbipaistev. 3.Nimeta vee puhastamise meetodid. Vee puhastamise meetodid on filtrimine, sadestamine ja destilleerimine. 4.Mis on molekul ning millest see koosneb? Molekul on üliväike aineosake, mis koosneb aatomitest. 5.Mille poolest erineb liitaine lihtainest? Liitaine koosneb mitme elemendi aatomitest, kuid lihtaine ühest elemendist. 6.Mida näitab molekulivalem? Molekulivalem näitab aine koostist. Nt. H2O, CO2 7.Mis on mehaaniline liikumine? Mehaaniline liikumine on keha asukoha muutus teiste kehade suhtes. 8.Mida nimetatakse soojus liikumiseks? Soojus liikumiseks nimetatakse aineosakeste liikumist. 9.Mida näitab kiirus? Kiirus näitab, kui suure teepikkuse läbib keha ajaühikus. 10.Mis on mitteühtlane liikumine? Mitteühtlane liikumine on ebaühtlase kiirusega liikumine. 11.Mida nimetatakse jõuks
II -II IV -II CaO kaltsiumoksiid SO2 vääveldioksiid III -II V -II Al2O3 alumiiniumoksiid P4O10 tetrafosfordekaoksiid Aga: II -II FeO raud(II)oksiid III -II Fe2O3 raud(III)oksiid OKSIIDIDE SAAMINE Oksiide saadakse peamiselt põlemisreaktsioonides on ju põlemine eelkõige reageerimine hapnikuga. Iseloomulik on reaktsioon: LIHTAINE + HAPNIK OKSIID Kui elemendil on ühendis kindel oksüdatsiooniaste (IA, IIA, Al), on lihtne võrrandit ka kirjutada (koostame tekkiva oksiidi valemi oksüdatsiooniastmete abil)! · naatriumi reageerimine hapnikuga: I -II 4 Na + O2 2 Na2O · vesiniku reageerimine hapnikuga (paukgaas, kütus): I -II 2 H2 + O2 2 H2O
Tartu 2014 0 Sisukord Sissejuhatus Füüsilised omadused ja aatomi ehitus Füüsilised omadused Aatomi ehitus Leidumine looduses Isotoobid Keemilised omadused ja reaktsioonid Ühendeid ja nende kasutamine Füsioloogiline toime Huvitavaid fakte Mida andis mulle referaadi koostamine? Kasutatud materjal 1 Sissejuhatus Kuld on tihe, plastne, läikiv ja pehme väärismetall; see on nii keemiline element kui ka lihtaine, mis esineb looduses mineraalina. Kulla keemilise elemendi sümbol on Au ja aatomnumber 79. Kuld asub IB rühmas Levimiselt looduses on kuld haruldane metall. Ometi on see kollane metall kõigile tuntud ja teatud. Ajalooliselt on väljakujunenud peamiselt kaks kulla funktsiooni. Alates ürgajast on kuld olnud ehtemetall ja kuna seda leidub looduses harva, siis sümboliseerib kuld rikkust ja selle kaudu ka võimu. Kulla ladinakeelne nimetus aurum , mis tähendab koidusära. Eesti sõna kuld
Referaat Naatrium Steve Mägi A-08 Pärnumaa Kutsehariduskeskus 08.12.08 Pärnu 2008 Sisukord: Naatriumi referaat Naatriumi omadused: ............................................................................ 4 Füüsikalised ja keemilised omadused:........................................................................................7 Kasutatud kirjandus:................................................................................................................... 8 Naatriumi kohta tutvustus: Na Naatrium -metall Aatomnumber: 11 Aatommass: 22,989 Klassifikatsioon: leelismetallid, s-elemendid Aatomi ehitus: Elektronvalem: 1s2 2s2p6 3s1 Elektronskeem: +11|2)8)1) Elektronite arv: 11 Neutronite arv: 12 Prootonite arv: 11 Oksüdatsiooniast(m)e(d) ühendites: -I, 0, I Krista...
vahevöö: kuni 2900 km, kivimeteoriitide sarnased kivimid astenosfäär: vahevöö ülaosas mõnesaja km paksune, plastiline, vahevöö kivimite mõningase ülessulamise piirkond litosfäär: maakoor+astenosfääri peale jääv vahevöö maa tuum: nikkelraua koostis 2900-6400 km, vedel välistuum, tahke sisetuum Maa dünaamiline magnetväli: vahevöös, kergemad kivimite massid pealepoole, raskemad allapoole Litosfäär koosneb O Si Fe Mg Ca Al K ja Na Mineraal looduslik tahke lihtaine või keemiline ühend, iseloomulik kuju ja kindla sturktuuriga kristall, enamus räni ja hapniku baasil. Tekivad gaaside ja vedelike tahkestumisel looduses. Ümberkristalliseerumine: kõrge rõhk+temp -> aine kristallsturktuur muutub Kivim-mineraalide kokku tsementeerunud kogum Kivimite jagamine tekkeviisi järgi: 1) tard- ehk magmakivimid: Maa süvakoore ja vahevöö kivimite ülessulamisel tekkinud vedelast magmast tahknemisel (süvakivimid-magmakivimid).
järgneb metalli tootmine ja selle lõplik puhastamine. Tavaliselt ei ole metallid lisanditest täiesti puhtad, vajadusel neid puhastatakse. Üldiselt on täiesti puhta metalli saamine väga kallis ja seda tehakse vaid haruldaste ja väga väärtuslike metallide puhul. Enamasti ei ole aga metalli absoluutne puhtus vajalik, sest põhiliselt käsutatakse argielus metallide sulameid. Sulam saadakse vähemalt kahe lihtaine sulatatult segamisel. Enamasti on sulami komponentideks metallid, kuid esineb ka mittemetalle. Väga levinud on süsiniku sisaldus rauasulamites (teras, malm). Ning mis kõige olulisem metalli tootmine toimub elektrienergia abil.Metalli tootmine ei ole küll pikk protsess, aga samas suhteliselt keeruline, aga meie tänapäeva elus on metall üheks oluliseimaks vahendiks meie tavaelus. Alumiiniumi tehased ehitatakse kohtadesse kus on elektrienergia odav ning tarneaine on läheduses
Kuid siiski kõik metallid ei põle erinevate värvustega, aga näiteks: Na muudab leegi kollaseks, K; Rb; Cs lillaks, Li; Sr karmiinpunaseks, Ca tellispunaseks, Ba; Cu; B; Tl roheliseks ja Pb; Sn; Sb; As -valkjassiniseks. Leekreaktsiooni tegemiseks kasutatakse põletit või piirituslampi. Leekreaktsioon on väga tundlik ja leeki ei tohi sattuda ükski muu aine kui katsetatakse. Kõik peab olema väga puhas ja ka aine peab olema lihtaine sest muidu võib reaktsioon kohe rikutud olla. Naatriumi tuvastamiseks on vaja väga vähe naatriumit et leegi värv muutuks, seda kasutas ära kunagi prof. R. Bunsen. Kuna higis on naatriumi siis eritus seda õpikutele. Bunsen lasi üliõpilastel oma raamatuga leegi juures lehvitada ja kui leek muutus kollaseks lasi ta õpilase eksamile. Kõik ained põlevad ka erineva temperatuuriga. Kõige kõrgem põlemistemperatuur on tsüaanil reageerimisel osooniga C2N2 + O3.