· Happeline lahus lahus, mille pH < 7 (vesinikioonide sisaldus lahuses ületab hüdroksiidioonide sisalduse) · Aluseline lahus lahus, mille pH > 7 (hüdroksiidioonide sisaldus lahuses ületab vesinikioonide sisalduse) · Neutraalne lahus lahus, mille pH = 7 (vesinik ja hüdroksiidioonide sisaldus lahuses on võrdne) · Leelis vees hästi lahustuvad tugevad alused. 2) Kirjuta järgmiste aluste, hapete ja oksiidide valemid. - Alumiiniumoksiid Al+32O2-3 - raud(III)oksiid Fe3+2O2-3 - Lämmastikhape HNO3 - väävelhape H2SO4 - 2+ Vask(II)hüdroksiid Cu (OH) 2 - - kaaliumhüdroksiid K+OH-
Keemia Kontrolltöö Alused 1. Mis on alused, millest tulenevad nende ühised omadused? Alused on ained, mis annavad vesilahusesse hüdroksiidioone. Nende ühised omadused tulenevad hüdroksiididest. 2. Mida peaks tegema, kui leelist on sattunud naha peale? Tuleks kiiresti veega üle pesta, vajadusel tuleks loputada kahjustatud koht lahjendatud äädikhappe lahusega ning seejärel uuesti veega. 3. Aluste jaotus + näited. Tugevad alused ehk leelised - nende molekulid jagunevad vesilahuses täielikult ioonideks. 1A rühm, 2A alates Ca (Ca, Sr, Ba). N2iteks: Li, Na, K, Rb, Cs, Ca, Sr, Ba Nõrgad alused ehk vees praktiliselt mittelahustuvad alused. Ülejäänud metallid. N2iteks: Ni, Fe, Cu, Zn, Al, Ag, Ru, Rh 4. Hüdroksiidide nimetuste ja valemite koostamine. 1A, 2A, 3A - metall + hüdroksiid Ülejäänud metallid - metall(o.a)hüdroksiid Näiteks: ...
KEEMIA MÕISTED AATOM neutraalne osake, mis koosneb aatomtuumast ja elektronkattest ELEKTRONSKEEM näitab elektronide paigutust elektronkihtidel KEEMILINE ELEMENT ühesuguse tuumalaenguga aatomite liik IOON laetud aatom KATIOON positiivselt laetud ioon ANIOON negatiivselt laetud ioon O-A arvutuslik suurus, mis näitab elemendi oksüdeerumise astet ühendis LIHTAINE koosneb ainult ühe elemendi aatomitest LIITAINE koosneb vähemalt kahe erineva elemendi aatomitest MOLEKULAARSED AINED soolad, metallid, alused, aktiivsete metallide oksiidid MITTEMOLEKULAARSED AINED happed, orgaanilised ained, vedelikud, gaasid KEEMILINE SIDE jõud või mõju, mis seob aatomid molekuliks või aatomid ja ioonid kristalliks KOVALNTNE SIDE ühiste elektronpaaride abil tekkiv keemiline side (mittemetallid) METALLILINE SIDE keemiline side metallides, tekib metalliaatomite vahel ühiste väliskihielektronide abil IOONILINE SIDE erinimeliste laeng...
OSKIID NB! Ei reageeri SiO2. (mittemetalli + ALUS vaata ALUS + HAPPELINE OKSIID oksiid) + ALUSELINE OSKIID SOOL SO2 + Na2O Na2SO3 ALUSELINE + VESI LEELIS Li2O + H2O 2LiOH OKSIID NB! Reageerivad ainult IA ja IIA(alates Ca) metallide oksiidid. (metalli oksiid) + HAPE vaata HAPE + ALUSELINE OKSIID + HAPPELINE OKSIID vaata HAPPELINE OKSIID + ALUSELINE OKSIID
1.Milliseid ohutus nõudeid on vaja järgida? a)Leelis -ja leelis muld metallide kasutamisel.Kanda kummikindaid ja prille Laboris tuleb hoida petrooliumi või õli kihi all.Lõikamisel tuleb kanda kindaid ja kasutada kummikindaid. b)Leeliste kasutamisel-tugeva söövitava toimega Kasutada kaitse vahendeid .Tuleb vältida nahale sattumist.Kahjustatud kohta pesta veega. 2.Mis on kare vesi? Vees lahustunud kaltsiumi ja magneesiumi soolad põhjustavad vee karedust 3.Mööduvkaredus-Ca(HCO3)2,Mg(HCO3)2 kõrvaldatakse kuumutamisel.kuumutamisel
Rakendus: suhkru tootmine suhkrupeedist Avastati Šotimaal Pehme, kerge OMADUSED Neis esineb puhtaimal kujul metalliline side Pehmed, kergesti lõigatavad Suhteliselt kerged, väike tihedus Suht. madal sulamistemperatuur Hea elektri- ja soojusjuhtivusega Läikiv, hõbevalge värvus Reageerivad aktiivselt hapniku ja enamiku teiste mittemetallidega Reag. aktiivselt veega, moodustub vastav leelis ja vesinik Reag. tormiliselt hapetega, tõrjudes välja vesiniku VÄRVUSED Ba- roheline Strontsium- punane Kaltsium- oranzikas punane
3. Metallide reageerimine veega Metalli reageerimisel veega on redutseerijaks metall ja oksüdeerijaks vesi. Metallid, mis asuvad pingereas vesinikust vasakul, tõrjuvad hapete lashustest välja vesinikku. Tavatingimustes reageerivad aktiivselt veega ainult leelis- ja leelismuldmetallid (vähesel määral ka magneesium), tõrjudes veest välja vesinikku. Saadusena tekib metalli hüdroksiid leelis. Keskmise aktiivsusega metallid (alumiiniumist rauani) reageerivad kuumutamisel veeauruga, tõrjudes välja vesinikku. Seejuures tekib metalli oksiid. Rauast vähem aktiivsed metallid veega ei reageei. 4. Metallide reageerimine soolade lahustega Iga metall on tugevam redutseerija, kui temast metallide pingereas paremal asubad metallid. Metallid tõrjuvad endast nõrgemate redutseerivate omadustega (metallide pingereas endast paremal
Leelis-ja leelismuldmetallide oksiidid · Valged tahked ained, millel on tugevalt aluselised omadused. · Reageerivad väga aktiivselt veega ja sellest moodustub ka vastav leelis. · Kõige tuntum ja tähtsam nendest on kaltsiumoksiid ehk kustutamata lubi. · Reageerib energiliselt veega, moodustades kaltsiumhüdrooksiidi ehk kustutatud lubja. Reaktsioonis eraldub nii palju soojust, et lahus võib kuumeneda lausa keemiseni. · Imab ka aktiivselt niiskust, muutudes valgeks kohevaks hüdrooksiidimassiks. Tänu sellele saab teda kasutada ka gaaside ja vadelike kuivatamisel. · Reageerib nii hapete kui ka happeliste oksiididega (tugevalt aluseline oksiid) Hüdroksiidid
11. Alus (laguneb kuumutamisel) = Aluseline oksiid + Vesi · Ei lagune IA rühma metallide hüdroksiidid. 12. Sool + Metall = Uus sool + Uus metall · Metall reageerib vees lahustuva soolaga, kui ta on aktiivsem kui soola koostises olev metall. · Metallid, mis reageerivad külma veega (IA ja IIA alates kaltsiumist), ei asenda soola koostises vähem aktiivseid metalle, vaid reageerivad veega. Tekkinud leelis võib reageerida soolaga (kui tekib sade). 13. Sool + Sool = Uus sool + Uus sool · Mõlemad lähteained peavad olema lahustuvad ja vähemalt üks saadustest peab olema mittelahustuv/lahustumatu. TUNTUMATE HAPETE JA ANIOONIDE NIMETUSED JA VALEMID Happe nimetus Happe valem Aniooni nimetus Aniooni valem Vesinikflouriidhape HF Fluoriid F Vesinikkloriid hape e
Metall + hapnik = (Na + O2 Na2O) Metall + mittemetall = (Väärisgaasidega ei reageeri, sest neil on oktett!) Metall + vesi = [Li Mg (Toa temp = Leelis + H.); Al Fe (kuum. = oksiid + H)] Metall + hape = Sool + vesinik (Pingerida - H) Metall + sool = (Pingerida üksikmetall ja soolas olev metall )
väheaktiivne Au- pehme metall, tihe, plastne, läikiv ja pehme väärismetall. Rahandus, ehted 9. Leelismetali oksiidid on valged tahked ained, millel on tugeval aluselised omadused. Reageerivad väga aktiivselt veega. Siirdemetallide hüdroksiidid on erineva värvusega, vees praktiliselt lahustumatud tahked ained. Neid on võimalik saada kautselt. Nõrkade aluseliste omadustega. Mõned on amfoteersed, kkumutades moodustavad oksiidid. Leelis hüdroksiidid on tugevad alused, valged kristalsed ained. Lahustuvad hästi vees. Kuumutamisel lagunevad vastavaks oksiidiks ja veeks Leelis soolad on kõrge sulamist, kõvad, kuid haprad, valged ja tugevad elektrolüüdid. Vees hästilahustuvad Siirdemetallide oksiidid on vees praktiliselt lahustumatud tahked ained, erineva värvusega. Nõrgalt aluselised omadused, reageerivad hapetega. 10. Aine on aluseline kui on nõrk hape, reageerib veega.
Kordamisküsimused (kasuta vastamisel ka tabeli abi) 1) Selgita mõisteid: leelis: vees hästilahustuv tugev alus (hüdroksiid) redutseerumine: elektronide liitumine redoksreaktsioonis, elemendi o.a- vähenemine sool: kristalne aine, mis koosneb aluse katioonidest ja happe anioonidest redutseerija: aine, mille osakesed loovutavad elektrone, ise oksudeerub oksüdeerumine: elektronide loovutamine redoksreaktsioonis, elemendi o.a- suurenemine
ravimseepidele mitmesuguseid ravimeid. Seebi kvaliteet oleneb valmistamiseks kasutatavatest rasvainetest ja lisanditest.[5] Roheline seep ehk kaaliumiseep valmistatakse rasva kaaliumhüdroksiidiga. Värvuselt on ta rohekas või pruunikas. Roheline seep on salvitaoline mass, mis vees hästi lahustub. Ta vahutab hästi ning on tugeva desinfitseeriva toimega, kuid võib õrnemat nahka, eriti lastel, ärritada ja isegi rikkuda.[5] Normaalse nahaga inimesele sobib seep, milles leelis on väikses ülekaalus. Kuiva nahaga inimesele on sobivam seep, milles on rohkem rasva ja millele on lisatud lanoliini või spermatseeti. Lasteseepidele lisatakse lanoliini ja boorhapet. [5] Õrna ja kuiva nahaga inimestel ei ole soovitav end liiga sageli seebiga pesta, sest siis eemaldatakse täiesti naharasu ja võib tekkida nahapõletik, mis avaldub naha kiheluse, punetuse ja kestendusena.[5] 7
tegelikult: Cl2 + 2e- 2Cl-. · Metallide reageerimine mittemetallidega on ühinemisreaktsioon. · Endotermiline reaktsioon soojust neeldub. · Eksotermiline reaktsioon soojust eraldub (metallide reageerimine mittemetallidega). 2. Metallide reageerimine vee ja hapete ning leeliste lahustega. · IA leelismetallid, IIA leelismuldmetallid (Ca ja sellele järgnevad elemendid). Edaspidi kokkuvõetult leelismetallid. · Leelismetall + vesi leelis + H2 (leelismetallid IA ja IIA v.a. Mg ja Be) · Leelismetall + hape(lahus) sool + H2 (võib plahvatada) · Siirdemetall (p-metall) + vesi aktiivselt ei reageeri. Osa (Fe, Al, Zn) reageerib kõrgemal temperatuuril. Tekib oksiid ja H2. · Metall + leelis uus hüdroksiid + H2 (enamik metalle ei reageeri) või kompleksühend. N: 2Al + 2NaOH + 6H2O 2Na[Al(OH)4] + 3H2 3. Metallide aktiivsuse rida.
tegelikult: Cl2 + 2e- 2Cl-. · Metallide reageerimine mittemetallidega on ühinemisreaktsioon. · Endotermiline reaktsioon soojust neeldub. · Eksotermiline reaktsioon soojust eraldub (metallide reageerimine mittemetallidega). 2. Metallide reageerimine vee ja hapete ning leeliste lahustega. · IA leelismetallid, IIA leelismuldmetallid (Ca ja sellele järgnevad elemendid). Edaspidi kokkuvõetult leelismetallid. · Leelismetall + vesi leelis + H2 (leelismetallid IA ja IIA v.a. Mg ja Be) · Leelismetall + hape(lahus) sool + H2 (võib plahvatada) · Siirdemetall (p-metall) + vesi aktiivselt ei reageeri. Osa (Fe, Al, Zn) reageerib kõrgemal temperatuuril. Tekib oksiid ja H2. · Metall + leelis uus hüdroksiid + H2 (enamik metalle ei reageeri) või kompleksühend. N: 2Al + 2NaOH + 6H2O 2Na[Al(OH)4] + 3H2 3. Metallide aktiivsuse rida.
siis tuleb märkida selle aine valemi taha nool alla. 4) Kõik toimuvad reaktsioonivõrrandid tuleb tasakaalustada. 5) Kui reaktsiooni ei toimu, siis tuleb sõnadega märkida põhjendus, miks antud reaktsioon ei toimu. Aluseliste oksiidide keemilised omadused 1) aluseline oksiid + hape sool + vesi II -II + - 2+ - III -II + 2- 3+ 2- CuO + 2HCl CuCl2 + H2O Al2O3 + 3H2SO4 Al2(SO4)3 + 3H2O 2) aluseline oksiid + vesi leelis Veega reageerivad ainult aktiivsete metallide oksiidid (I A rühma metalli oksiidid ja II A rühma alates kaltsiumist metallide oksiidid) II -II 2+ - I -II + - CaO + H2O Ca(OH)2 Na2O + H2O 2NaOH 3) aluseline oksiid + happeline oksiid sool II -II 2+ 2- I -II + 3- BaO + CO2 BaCO3 6Cs2O + P4O10 4Cs3PO4 Happeliste oksiidide keemilised omadused 1) happeline oksiid + alus sool + vesi + - + 2- 2+ - 2+ 3- SO3 + 2NaOH Na2SO4 + H2O P4O10 + 6Ca(OH)2 2Ca3(PO4)2 + 6H2O
1. ALUSED on ained, mis annavad lahusesse hüdroksiidioone 2. Tüüpilised alused on hüdroksiidid, mis koosnevad metalliioonidest ja hüdroksiidioonidest 3. ALUSTE LIIGITAMINE 1) Vees lahustuvad hüdroksiidid 2) Vees praktiliselt lahustumatud hüdroksiidid 3) Teised alused 4. ALUSTE SAAMINE 1) Leeliseid saadakse: metall + vesi 2) Leeliseid saadakse: aluseline oksiid + vesi 3) Lahustumatuid hüdroksiide saadakse: sool + leelis 5. ALUSTE KEEMILISED OMADUSED Aluste sarnased omadused on tingitud hüdroksiidioonidest 1) Alus + happeline oksiid 2) Alus + hape 1 3) Alus + sool 4) Aluste lagunemine kuumutamisel 5) Amfoteerne hüdroksiid + hape 6) Amfoteerne hüdroksiid + alus 2
MgO) 2) Mittemetallioksiidid gaasid, vedelikud või tahked ained (SO2, CO2, P4O10 N2O5) Oksiidide saamine: 1) Lagunemisreaktsioonil CaCO3 = CaO + CO2 Rasklahustuvate hüdroksiidide lagunemisel Cu(OH)2 = CuO + H2O 2) Oksüdeerimisel e. hapnikuga reageerimisel 4Al + 3O2 = 2Al2O3 C + O2 = CO2 Keemilised omadused: 1) Metallioksiidid a) Leelismetalli oksiid reageerib aktiivselt veega, tekib leelis CaO + H2O = Ca(OH)2 b) Reageerib happelise oksiidiga, tekib sool CaO + CO2 = CaCO3 c) Reageerib happega, tekib sool ja vesi CaO + H2CO3 = CaCO3 + H2O 2) Mittemetallioksiidid a) Reageerib veega, tekib hape CO2 + H2O = H2CO3 b) Reageerib aluselise oksiidiga, tekib sool CO2 + CaO = CaCO3 c) Reageerib alusega, tekib sool ja vesi CO2 + Ca(OH)2 = CaCO3 + H2O
Elektrofiili ehk elektrofiilse tsentri tunneme ära positiivse laengu/osalaengu ja vaba orbitaali järgi. Nukleofiili ehk nukleofiilse tsentri tunneme ära negatiivse laengu/osalaengu ja vaba elektronpaari järgi. Nukleofiil ühineb elektrofiiliga. Halogeenühenditega toimub nukleofiilne asendusreaktsioon st ründavaks osakeseks on tugevam nukleofiil, reaktsioonitsentriks on halogeenühendi elektrofiilsustsenter, lahkuv rühm eraldub halogeenühendist halogeniidioonina. 1. halogeenühend + leelis = alkohol + metallihalogeniid 2. halogeenühend + alkoholaat = eeter + metallihalogeniid 3. halogeenühend + tsüaniid = nitriil + metallihalogeniid
Metallide pingereas on metallid reastatud redutseerivate omaduste nõrgenemise suunas. See rida peegeldab metallide võimet loovutada elektrone vesilahuses kulgevates reaktsioonides. Metallid mis asuvad pingereas vesinikust vasakul, on võimelised hapete lahustest vesinikku välja tõrjuma. Metallis, mis aga paremal, hapete lahustest vesinikku välja ei tõrju. Metalli reageerimisel veega on red metalli oks vesi. Tavatingimustes reageerivad aktiivselt veega ainult leelis ja leelismuld metalli, tõrjudes veest välja vesinikku, saadusena tekkiv leelis. Keskmise akt. Metallid al kuni fe reageerivad kuumutamisel veeauruga, tõrjudes välja vesiniku. Tekib metalli oksiid. Rauast vähem aktiivsed pingereas ei reageeri veega. Keemililse rektsiooni kiirust mõõdetakse lähteaine või saaduse kontsentratsiooni muutusega ajaühikus. Reaktsiooni kiirus kasvab lähteainete kontsentratsiooni suurendamisel
puhtad metallid . Reaktsiooni käigus jääb energiat üle ja neid keemilisi reaktsioone , kus energia vabaneb nimetatakse eksotermilisteks reaktsioonideks . 17. Metallide põhilised oksüdatsiooni astmed ühendites . I , II ja osaliselt III Arühma metallide oksüdatsiooni aste = rühma nr . IV A rühma ja edasi maksimaalne oksüdatsiooni aste = rühma nr . Brühmades maksimaalne oksüdatsiooni aste = rühma nr . Püsivad ühendid on oksüdatsiooni astmega +II ja +III . 18. Kuidas reageerivad leelis ja leelismuldmetallid veega ? Mis tekib ? Leelismetallid ( I Arühmas ) : Li , Na , K , Rb , Cs , Fr . Leelismuldmetallid ( II Arühmas ) : Ca , Sr , Ba , Ra . 19. Kuidas reageerivad keskmise aktiivsusega metallid veega ? Reageerivad veega kuumutades metalli või kuumutades vett ( tulise ülekuumenenud veeauruga ) . 20. Millised metallid ei reageeri veega ? Vähe aktiivsed metallid . 21. Mis on redutseerijaks / oksüdeeriaks metallide reageerimisel veega? Redutseerijaks metallid
1. Metall + mittemetall sool NB! H2CO3 2Na + S Na2S H2O + CO2 2. Metall + hape sool + H2 Zn + 2HCl ZnCl2 + H2 3. Metall + sool uus metall + uus sool Fe + CuSO4 Cu + FeSO4 4. Alus + hape sool + vesi NaOH + HCl NaCl + H2O 5.Alus + happeline oksiid sool + vesi 2NaOH + SO2 Na2SO3 + H2O 6.Hape + aluseline oksiid sool + vesi 2HCl + CuO CuCl2 + H2O 7.Happeline oksiid + aluseline oksiid sool CaO + CO2 CaCO3 8. Alus(leelis) + sool uus alus + uus sool CuSO4 + NaOH Cu(OH)2 + Na2SO4 9. Hape + sool uus hape + uus sool H2SO4 + BaCl2 HCl + BaSO4 10. Sool + sool uus sool + uus sool K2SO4 + BaCl2 KCl + BaSO4
aox+hape=sool+vesi aox+vesi=leelis(1,2arühm) aox+hox=sool hox+alus=sool+vesi hox+vesi=hape neut ox:NO,N2O,CO ei reag. aluse, hape, soolaga. Hape+metal=sool +H2 (vesinikust vasakul) Hape+ aox=sool+vesi Hape+alus=sool+vesi Hape+sool=hape+sool(kuitekib nõrgem hape v sade) Alus+hox=sool+vesi Alus+hape=sool+vesi Alus+sool=alus+sool(mõlem. Lah+lah=sade) Sool+met=sool+met(met aktiivsem) Sool+hape=sool+hape(kui tekib nõrgem hape v sade) Sool+alus=sool+alus (mõlem. Lah+lah=sade) Sool+sool=sool+sool(mõlem. Lah+lah=sade) Aox = aluseline oksiid Hox= happeline oksiid
OKSIIDIDE REAGEERIMINE VEEGA NB! Lõpeta näidete eeskujul punktides I. ja II reaktsioonivõrrandid. I. aluseline oksiid + vesi alus Veega reageerivad ainult IA ja IIA metallide al Ca-st oksiidid, tekib tugev alus ehk leelis. (Meenutame: olid ju leelised IA ja IIA al Ca-st metallide hüdroksiidid.) Na2O + H2O 2 NaOH CaO + H2O K2O + H2O Fe2O3 + H2O II. Happeline oksiid + vesi hape Happelise oksiidi reageerimisel veega tekib oksiidile vastav hape. (Meenutame: oksiidide ja hapete vastavused on põhikoolis pähe õpitud, tuleb korrata!) Oksiid Hape CO2 H2CO3 SO2 H2SO3 SO3 H2SO4 SiO2 H2SiO3 N2O5 HNO3 P4O10 H3PO4 H2O + CO2 H2CO3 SO2 + H2O P4O10 + H2O SO3 + H2O
Keemia · Väävel (S) Madal sulamistemperatuur Kergesti peenestatav Vees praktiliselt lahustumatu Lahustub hästi vähepolaarse ainetes orgaanilistes lahustes Üldjuhul S8 ja pulbrina Keemilised omadused: 1. Oksüdeerijana käitub väävel metallide ja endast vähemaktiivsete mittemettallide suhtes. 2. Saadus suldiif 3. Leelis + leelis muldmettallid reag. Toa temp. 4. Enamiku mettalidega reag. Alles kuumutamisel 5. Vesiniku juhtimine keemiseni kuumutamisel väävlisse tekib H2S 6. Redutseerijana käitub aktiivsemate mettalidegamoodustades tugeva ühendi. S+ H2 = H2S S+ Fe = FeS S+ HNO3(konts) = H2SO4 S+ O2 =SO2 · Sulfiidid Divesiniksülfiid (H2S) Väga mürgine, Õhust raskem gaas värvusetu H2S juhtimine vette moodustub nõrk hape H2S + (1 mol) NaOH =NaHS
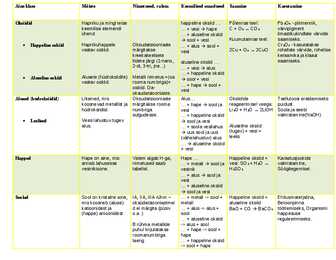
Keemilised 1) Aluselised Oksiidid reageerivad: 1) Hapete molekulid dissotsieeruvad 1) Reageerivad happeliste 1) Reageerivad metallidega uus sool ja uus metall. a) hapetega sool ja vesi. Toimub alati. vesilahustes vesinikioonideks ja happe- oksiididega, tekib sool ja vesi: Reageeriv metall peab olema aktiivsem, kui soola koostises omadused b) veega leelis. Ainult aktiivsete metallide anioonideks. CO2+Ca(OH)2 CaCO3+ 2H2O olev metall. oksiidid. 2) Reageerivad metallidega sool ja vesinik. 2) Reageerivad hapetega sool ja 2) Reageerivad hapetega uus sool ja uus hape. Peab tekkima c) happeliste oksiididega happelisele oksiidile 3) Reageerivad aluseliste oksiididega sool vesi
ELEKTROLÜÜDID JA MITTEELEKTROLÜÜDID Elektrolüüdid ained, mis vesilahuses/sulaolekus lagunevad täielikult/osaliselt ioonideks juhivad elektrivoolu Nt NaCl-lahus (füsioloogiline lahus tilgutites), kraanivesi, leelis- ja leelismuldmetallide hüdroksiidid, happed (HCl,H3PO4). Sisaldavad ioone ka tahkes olekus, kuid soolad ei juhi tahkena voolu (ioonid ei suuda tugeva sideme tõttu kristallvõrest väljuda). Elektrolüütiline dissotsiatsioon elektrolüütide lahutumisega kaasnev aine osaline/täielik lahustumine ioonideks Astmeline dissaotsiatsioon järkjärguline, iseloomulik nt mitme OH rühmaga alustele Dissotsiatsiooni määr ntb, kui suur osa lahustunud aine molekulidest on dissotseerunud ioonideks suureneb tempo tõstmisel Jaotus: · Tugevad(täielikult ioonideks) tugevad happed, leelised, soolad. Ka pmst lahustumatud soolad annavad lahusesse vähesel määral ioone=tugevad dissotsiatsiooni määr üle 30% · Nõrgad(os...
Reaktsioonid Oksiidid + vesi = leelis Aluseline oksiid + hape = sool + vesi + sool = + vesi = hape Happeline oksiid + alus = sool + vesi + aluseline oksiid = sool Happed + alus = sool + vesi + aluseline oksiid = sool + vesi Hape + sool = uus sool + uus hape (uus hape peab nõrgem olema või uus sool mittelahustuv)
päikesekiirgusele (kiire soojenemine). · Põhjuseks on ka telliste kehv kvaliteet, seda selgitab ka osaline lagunemine. Telliseid on põletatud madalamal temperatuuril ja pole toimunud paakumist, sellest ka osade telliste suurem poorsus ja veeimavus. · Valged laigud on põhjustatud ilmselt auru difusioonist läbi seinte, sellega on kristalliseerunud välja soolad, mis võivad sisalduvad savis (SO42- ) · Teine põhjus valgetele laikudele võib olla leelis ja leelismuldmetallide suur sisaldus savis, millest tellised on valmistatud. Põletamisel tekivad tellise pinnale valged laigud. Korrosiooni eemaldamine · Telliste pinnatöötlus katetega, mis vähendaksid lahtist poorsust ja sellega suurendaksid siis ka külmakindlust. · Katta maja fassaad osaliselt või terviklikult uute fassaadimaterjalidega koos lisasoojustusega. · Valgeid laike peaks saama eemaldada soolhappe lahusega
LEELISED JA LEELISMULDMETALLID Leelismetallid on IA rühma metallid. Väliskihi elektronvalem ns1-s-metallid. Füüsikalised omadused: · Kerged · Pehmed · Kergsulavad Keemilised omadused: · Reag. veega (leelis + H2) 2Na + 2H2O = 2NaOH + H2 · Reag. hapnikuga 4Li + O2 = 2Li2O (oksiid) 2Na + O2 = Na2O2 (peroksiid) K + O2 = KO2 (hüperoskiid) · Leekreaktsioon muudavad leegi värvust. Na-kollane; K-helelilla Leelismetallide saamine ja kasutamine: Na+ ja K+ reguleerivad rakkude veesisaldust, südametegevust. Taimedele vajalikud kaaliumväetised (KCl, puutuhk). Leelismetallide ühendid: NaOH Seebikivi Seebivalmistamisel Na2CO3 (pesu)...
( kestab umbes 20 min) ● koorest puhastatud palgid tükeldatakse saepuruks ● saepuru pestakse veega läbi ● siis asetatakse puru suurtesse tünnidesse, kus kuumutatakse 158 C juures läbi ● tekib tumepruun mass ● tumepruun mass keedetakse ja eraldatakse aur ● lisatakse paksendaja ● tekib helepruun kuiv mass ● kuivale helepruunile massile lisatakse vesi ja leelis, mis seda valgendab ja tekib valge pasta ● pastast eraldatakse vesi, masinaga mis pöörleb 1060 meetrit sekundis ja tekib niiske paberimass ● mass pressitakse lapikuks ja rullitakse metallist varda ümber ● rull kaalub 35 tonni ● suured rullid lõigatakse väiksemaks ning saadetakse edasi paberi lõikusesse ● tehases valmib ühe minuti jooksul 55000 paberilehte1 1 https://www.youtube.com/watch?v=1f_iPltxygs (21.05.2017)
OKA sisse. (muutuad metallid on : raud, tina, vask, kroom) Mõisted: 1. Aluselised oksiidid Alusele vastav oksiid 2. Anioon Negatiivse laenguga ioon 3.Hape Aine mis annab lahusesse vesinikioone 4.Sool Kristalne aine, mis koosneb (aluse) katioonidest ja (happe) anioonidest 5.Redutseerimine Elektronide liitmine. 6.Oksüdeerimine elektronide loovutamine, sellele vastab elemendi oksüdatsiooni astme suurenemine 7. Leelis Vees lahustuv tugev alus (hüdroksiid) Soolade Füüsikalised Omadused : 1) Tahked 2) Erinev värvus (põhiliselt valge) 3) Vees lahustuv on ka erinev ( vaata lahustuvus tabelist) Soolade Keemilised Omadused : 1. Sool + Alus (mõlemad peavad olema lahustuvad) ja üks saadustest peab olema sade 2. Soolad reageerivad tugevamate hapetega 3. SOOL + HAPE = UUS SOOL + UUS HAPE vana hape on tugevam ja uus nõrgem ;) TUGEVAD HAPPED ON : H2SO4 kõige tugevam HCL HNO3
Keemia. OKSIID- aine, mis koosneb 2-st elemendist, millest üks on hapnik. HAPE- koosneb vesinikust ja happejäägist. ALUS- koosnevad metallist ja OH rühmast. SOOL- aluse katioonist+ ja happe anioonidest- Elektrolüüt- vesilahuses või sulatatud olekus osaliselt või täielikult ioonideks.(happed alused soolad) Elektrolüütiline dissotsiatsioon- aine jagunemine ioonideks. Hüdraatumine on lahustunud aine osakeste seostumine vee molekulidega. Mitte elektrolüüt- ained, mis neutr. molekulidena lahuses. Ioonsed ained on tugevad elektrolüüdid.(sool leelis) Molaarne kontsentratsioon. väljendab moolide arvu 1 liitris. Tugevad happed lahustuvad täielikult ioonideks. Tugevad happed aktiivsed ja ohtlikud. Elektrol. dis. on happe ja vee molekuli vaheline keem. reakts., milles tekivad hüdrooniumioonid ja happe anioonid. Tugevate hapete elektrol. dis. lahuses on täielik. Nõrkadel pöörduv. Mitmeprooton. ainete dis. on astmeline. Nõrgad alused lahustuvad vähe...
ULTIMATE KEEMIA REAKTSIOONIDE TABEL. (anorgaaniline) OKSIIDIDE REAKTSIOONID + vesi = leelis (reag. IA ja IIA metallidega) Aluseline oksiid + hape = sool + vesi (metallioksiidid) + happeline oksiid = sool + vesi = hape (reag. CO2, SO2, SO3, N2O3, P4O10) Happeline oksiid + alus = sool + vesi (mittemetallioksiid) + aluseline oksiid = sool HAPETE REAKTSIOONID + alus = sool + vesi
hüdroksiidioonidest (OH-). Liigitus · LEELISED - vees lahustuvad hüdroksiidid Mendelejev tabeli I a & II a rühma elementide ühendid. · VEES PRAKTILISELT MITTELAHUSTUVAD ALUSED Kõikide ülejäänute metalli elementide ühendid. Hüdroksiidide keemilised omadused · Kõik hüdroksiidid reag. hapetega. Tulemus: sool ja vesi: KOH+HCl=KCl+H2O · Reag happeliste oksiididega. Tulemus: Sool ja vesi: Ca(OH)2+CO2=CaCO3+H2O · Leelis reag. vees lahustuva soolaga, kui vähemalt üks saadustest on sade () Ba(OH)2+CuCl2 =BaCl2 +Cu(OH)2 () KUUMUTAMINE · Leelised on kuumutamisele vastupidavad. Väga kõrgel temperatuuril lagunevad vaid IIa rühma metallielementide ühendid. · Vees mittelahustuvad hüdroksiidid lagunevad kuumutamisel veeks ja oksiidiks. Puhka veidi. Saamine · Leeliseid saab: Vee reageerimisel metalli või metalli oksiidiga. · 1) Ca + H2O = Ca(OH)2 + H2
Anni Petron 11.m Estrid Estrid on karboksüülhapete funktsionaalderivaadid, milles on karboksüülhappe –OH rühm asendatud –OR rühmaga. (R tähistab süsiniku ahelat) Nende üldvalemiks on R–COO–R. Estreid on võimalik saada happest ja alkoholist tugeva happe juuresolekul. Sellist reaktsiooni nimetatakse esterdamiseks. Estrite nimetused tekivad sarnaselt karboksüülhappe soolade nimetustega. Esimene osa nimest tuleb alkoholist ning teine vastavast karboksüülhappest Nt etaanhapeetüületanaat Estrid on vedelad või tahked ained. Enamasti meeldiva puuvilja lõhnaga. Need on läbipaistvad ning vees halvasti lahustuvad. Estrid ise ei ole mürgised, kuid estrite lagunemisel võivad tekkida väga mürgised ühendid. Estreid leidub eeterlike õlidena taimedes (nt: sidrunikoores). Veel on nendeks looduslikud rasvad (nt: vaalarasv) ja v...
Nimetuste andmise võimalusi anorgaanilises keemias Katrin Soika Nimetuste andmine 1) Muutumatu oksüdatsiooniastmega metalliühendi (IA-IIIA) korral: oksiid metalli nimetus hüdroksiid happejäägi nim I A rühm NT: Na2O naatriumoksiid Al(OH)3 alumiinium hüdroksiid 2) Muutuva oksüdatsiooniastmega metalliühendi nimetamine oksiid metalli metalli o.-a. hüdroksiid nimetus rooma numbriga happejäägi nim B rühm 2+ I NT: Ag2O hõbe(I)oksiid CuSO4 vask (II)sulfaat 3) Mittemetallioksiidide nimetamine arvsõna mittemetalli nim ...
http://www.abiks.pri.ee 1. Mõisted Alus -ained, mis annavad lahusesse hüdroksiidioone. Hüdroksiidid koosnevad metallianioonidest ja hüdroksiidioonidest Aluseline oks. -oksiid, mis reageerib happega, moodustades soola ja vee CaO, Na2O Amfoteer. Oks -oksiid, mis võib reageerida nii happe kui ka alusega, ei reageeri veega Al2O3 ja ZnO Amfoteerne -hüdroksiidi võime reageerida kas aluse või happega hüdroksiid Astmeline -aineosakeste lagunemine väiksemateks osadeks dissotsiatsioon Dissotsiatsiooni määr -näitab, kui suur osa lahustunud aine molekulidest on jagunenud ioonideks Elekrolüütilie (iooniline) -ioone sisaldavate lahuste tekkimine elektrolüütide lahustumisel dissotsiatsioon Elektr...
veega. Kätele sattunud alust ei tehta kahjutuks mõne tugeva happe abil, kuna ka happed on tervisele ohtlikud. Alus on aine, mis annab lahusesse hüdroksiidioone. Kõik alustele iseloomulikud omadused, nagu sööbiv toime, võime muuta indikaatorite värvust ning libedus on tingitud nende lahuses esinevatest hüdroksiidioonidest. Leelised on vees lahustuvad söövitava toimega tugevad alused, mis muudavad indikaatorite värvust. Naatriumhüdroksiid (NaOH) on tugev leelis. Ta on valge tahke aine, mis lahustub väga hästi vees, eraldades seejuures palju soojust. Samuti seob ta õhu käes seismisel õhuniiskust. Aluselisteks oksiidideks nimetatakse metallioksiide, mis vastavad mingile alusele (metalli oksüdatsiooniaste on sama). Ba(OH)2 -> BaO . Osa metallioksiide reageerib veega, osa mitte. Reageerivad aktiivsete metallide oksiidid. Hüdroksiidid jagunevad kuumutamisel aluseks ja veeks. Lagunemisreaktsioonis jaguneb aine
Oksiidide keemilised omadused · Aluselised oksiidid reageerivad hapetega = sool ja vesi. · Aluselised oksiidid reageerivad veega = leelis. Veega reageerivad ainult aktiivsete metallide oksiidid (IA rühma ja IIA rühma metallid alates Ca) · Aluselised oksiidid reageerivad happeliste oksiididega = sool. · Happelised oksiidid reageerivad veega = oksiidile vastav hape. Veega ei reageeri SiO2. · Happelised oksiidid reageerivad alustega = sool ja vesi. · Happelised oksiidid reageerivad aluseliste oksiididega = sool. Hapete keemilised omadused · Reageerivad metallidega = sool ja vesinik Reag. < h2
Keemia Mõisted: Hape Hape on keemiline aine, mis annab lahusesse vesinikioone. [HNO3, H2S, H2SO3] Alus Alus on keemiline aine, annab lahusesse hüdroksiidioone. [NaOH, Ca(OH)2] Oksiid Hapniku ja mingi teise keemilise elemendi ühend. [Li2O, SO3] Sool Soolad on kristalsed ained, mis koosnevad aluse katioonidest (näiteks Ca2+) ja happe anioonidest (näiteks SO42-). [K2S04, Na2CO3] Aluseline oksiid Alusele (hüdroksiidile) vastav oksiid. Aluselised oksiidid on oksiidid, mis reageerivad hapetega, moodustades soola ja vee. [CaO, BaO] Happeline oksiid Hapnikhappele vastav oksiid. Happelised oksiidid võivad reageerida aluse, aluselise oksiidiga või veega. [SO3, CO3] Leelis Vees lahustuv tugev alus (hüdroksiid). [KOH, NaOH] Valemite koostamine: Alumiiniumsulfiid - Karbonaatioon - Naatriumsulfit - Kaaliumoksiid - Raud (II) hüdroksiid - Vask (II) katioon Leia aineklass ja nimetus: ...
16 S 32,064 6 8 VÄÄVEL 2 Leidumine Esineb looduses ehedalt või sulfiidi ja sulfaadi koostises. Kohati asuvad S- lademed maapinna lähedal (Itaalia) või sadadade meetrite sügavusel (USA) Vulkaanigaasides on alati S- ühendeid ja pursetes eraldub väävlit, seega leidub teda ehedal kujul vulkaanide jalamil. S on mitme aminohappe koostiselement ning kuulub valkude koostisse. Suhteliselt S- rikkad on juuksed, karvad ja linnusuled. S kuulub elemendina kivisöe, põlevkivi, nafta jt fossiilsete kütuste koostisse. Inimene sisaldab kokku ligikaudu 140 g väävlit Väävlirikkamad toiduained on kaer, rukis, tatar, herned, oad ja kapsas Omadused. Väävel on keemiline element järjenumbriga 16 Mittemetall Tavatingimustes rabe kollane, rohekas, punakas kristalne aine. Elektrit mittejuhtiv , halb soojusjuht. Kristalne väävel vees ei lahustu. Keemil...
a LiOH) Cu(OH)2 CuO + H2O 3. Hapete lagunemisel H2CO3 CO2 + H2O 4. Soolade lagunemisel CaCO3 CaO + CO2 5. Liitainete põlemise CH4 + 2O2 CO2 + 2H2O Liigitus: · Aluselised oksiidid- enamus metalli oksiide Jagunevad: Tugevalt aluselised IA rühma metalli oksiidid ja IIA rühma metalli oksiidid alates Ca. Reageerivad: happega sool + vesi Veega leelis Nõrgalt aluselised oksiidid Ei reageeri veega! Reageerivad: happega Happelise oksiidiga sool Li2O + SO2 Li2SO3 · Happelised oksiidid- Enamus mittemetallioksiide. Happelised on ka metallioksiidid, milles metallil on kõrgeim o.a Nt CrO3 Enamik neist on molekulaarsed ained. Erandid: CrO3 ja SiO2 Reageerivad: alusega sool + H2O
Looduses levinuim metall. (kööginüud, pakkefoolium, elektrijuhtmed) Al2O3 alumiiniumoksiid, väga kõva, hinnatud vääriskivid nagu punane rubiin, sinine ja kollane safiir. CO2 süsihappegaas, karastusjoogid, gaasiline, ei põle, ei ole mürgine, lahustub vees, tekib põlemisel. SiO2 liiv, tahke, mittelahustuv, tehakse klaasi, valge kvarts. CaO kustutamata lubi, ehituses. HCl vesinikkloriidhape e. soolhape, rugev hape, neutraliseeridakse soolaga. NaOH subikivi, leelis, süüvitab, seep, tahke, valge, pH>7. Ca(OH)2 kustutatud lubi, leelis, ehitusmaterjalid, söövitav. NaCl keedusool, tahke lahustub vees, sälitusaine, kasutatakse toitude maitsestamiseks. CaCO3 lubjakivi, marmor, peakivi, kriit, valge. CH4 metaan, HCOOH metaanhape e. sipelghape. C2H5OH etanool e. piiritus, värvitu, põletava maitsega ja terava lõhnaga, lahustub vees, tekitab joovet, tehakse
KORDAMISKÜSIMUSED: I A rühma metallid 1)Selgita mõisteid: *Leelismetall I A rühma metallid. Neid nimetatakse leelismetallideks asjaolu tõttu, et nende vette asetades annavad nad saadusena leelise. *Aktiivne metall leelis ja leelismuldmetallid, metallid mis loovutavad kergelt elektrone *Leekreaktsioon reaktsioon, mille käigus on võimalik leelismetalle kindlaks teha leegi värvuse põhjal. *Leelis tugev alus, I ja II A rühma, alates Ca'st metallide hüdroksiidid *Seebikivi naatriumhüdroksiidi rahvapärane nimetus, sest naatriumihüdroksiidist ja rasvadest on võimalik keeta seepi. Valge värvusega vees hästi lahustuv, tahke kristalne ja väga sööbivate omadustega aine.
CH3C (N-metüületaanamiid); CH3C (N,N-dimetüületaanamiid) 3. Reaktsioonivõrrandid Kondensatsioonireaktsioon estri või amiidi tekkereaktsioon. tekib suurem molekul ja eraldub vesi. Pöördreaktsiooniks on hüdrolüüs, mille käigus suur molekul reageerib veega ja laguneb kaheks väiksemaks molekuliks. Hüdrolüüsi võib kiirendada katolüsaatoriga (hape või alus). Estrid: hape + alkohol ester + vesi ester + vesi karboksüülhape + alkohol ester + leelis karboksüülhappe sool + alkohol Amiidid: hape + NH3 amiid + vesi amiid + vesi karboksüülhape + NH4 amiid + leelis karboksüülhappe sool + NH3 Rasvad: glütserool + karboksüülhape(3) rasv + vesi Rasva hürdolüüs: tekkinud rasv + NaOH/KOH - seep
Alkohol- aine, mille molekuli süsiniku aatomi juures asuv vesinik on asendatud OH-rühmaga. Nimed liide- ool. CH3(OH)-metanool CH3(CH3)CH2CH2(OH)-propaan 1,2diool Omadused: osaleb hästi H-sidemete moodustamisel; võib veega teha H-sideme;hea vees lahustuvus;(lühike C- ahel)on ka hüdrofoobsed funktsionaalsedrühmad ja osalaengud- R-O-H Eeter-orgaaniline ühend üldvalemiga R-O-R Nimed- liide-eeter CH3CH2OCH2CH3-dietüüleeter CH3OCH2CH3-etüülmetüüleeter Omadused:eetri molekulid ei saa omavahel H-sidemeid moodustada;on lenduvad;veega ei anna tugevaid H- sidemeid, ei lahustu vees;heaks lahustiks organilistele ainetele funktsionaalsedrühmad ja osalaengud- R-O-R Amiin- lammastikühend,on alus ja nukleofiil; NH2 Nimed- liited: amino- ja amiin.NH3-ammoniaak (CH3)2NH-dimetüülamiin/diaminometanool Omadused- lämmastikul asuv nukleofiilsustsentner võtab osa H-sideme tekkest;lühikese C-ahelaga lahustuvad vees hästi;omavahelised H-sidemed on nõrgad kui a...
Seepide molekulid · Käitub vee pinnal nagu kahepaikne. · Veelembene "pea" sukeldub vette, püüab lahustuda vees. · Pikk vett- tõrjuv "süsivesiniksaba" aga jääb veest välja. Seebivesi · On libe. · On aluseline keskkond, sest seep reageerib veega. Millega pesta? · Linast ja puuvillast materjali võib pesta tugevasti aluseliste pesuainetega. · Villaseid esemeid ja naturaalseid age mitte. · Vill ja siid on koostiselt valkained , leelis lõhub selle struktuuri. Pesupulber Tide · Sünteetiline pesuaine Pesemistoime · Ensüümid - lagundavad valgulist mustust · Fosfaadid pehmendavad vett, tekitavad aluselise keskkonna. · Silikaadid Pehmendavad vett, tekitavad aluselise keskkonna,viivad mustuseosakesed emulsiooniks, kaitsevad metalli korrosiooni eest Puhastusvahendid · Puhastusvahendite koostis sõltub otstarbest milliste pindade puhastamiseks nad on ette nähtud.
· Leelised Vees lahustuv tugev sool ja vesi alus. ... + soola vesilahus Aluseline oksiid uus sool ja uus (tugev) + vesi = (vähelahustuv) alus leelis ... aluseline oksiid + vesi Happed Hape on aine, mis Valem algab H-ga, Hape ... Happeline oksiid + Karastusjookide annab lahusesse nimetused saab ... + metall sool ja vesi: SO + HO valmistamine,
Keemia igapäevaelus ja tööstuses. 1.Lubja tootmine. Keemiliselt näeb protsess välja järgmine: CaCo3 CaO Ca(OH)2. Lupja toodetakse paekivist ehk lubjakivist, põletades seda lubjapõletusahjus mitmeid ööpäevi järjest üle 1000° C temperatuuri juures. Tulemuseks on põletatud ehk kustutamata lubi, mis veega ägedalt reageerib ja annab kustutatud lubja. Sellest valmistatakse lubimört, mida kasutatakse ehitusel. Lubimört kuivab aja jooksul, reageerib õhus oleva süsihappegaasiga ja muutub uuesti keemiliselt paekivi sarnaseks ühendiks, kuid on paekivist poorsem ja mehaaniliselt mitte nii tugev. CaCo3 ehk kaltsiumkarbonaat on põletamata lubi. Seda sisaldavad näiteks kriidid, luud, munakoored, tigude ja karpide kojad ning ka looduslikud pärlid. Kaltsiumkarbonaat on tundlik hapete suhtes, seepärast happevihmad kahjustavad pikkamööda paekivist kui ka marmorist ehitisi ja skulptuure. Lubjakivi on tööstuses tähtis, s...