keskkonna saastumine väetistega, loomastike ja taimestike liigilise koosseisu muutumine ja liikide hävimine, haiguste levik. 7. Keskkonnaprobleemid Eestis. Põlevkivi kaevandamine ja põletamine, liigne metsade raie, õhusaastumine, veereostus, jäätmete teke ja ladustamine, läänemere reostumine, jõgede ja järvede eutrfeerumine, pinnase erosioon. 8. Vee omadused. Läbipaistev, värvusetu vedelik, parim lahusti. Polaarne molekul, moodustab vesiniksidemeid. 9. Kuidas saab hinnata hüdrofoobsust? Pikk süsinike ahel, ei lahustu vees. Aine jaotumine kahefaasilises süsteemis- oktanool- vesi. 10. Puhta aine ja segu erinevust. Puhas aine on kindla koostisega aine, koosneb ainult ühe aine osakestest. Segu koosneb aga mitmest erinevast ainest, seega koosneb erinevate ainete osakestest. 11. Vee peamised kvaliteedi näitajad. Hägusus, lõhn, maitse, värvus, elektrijuhtivus 12
18.Nimeta erinevaid steroide ja nende ülesandeid – Suguhormoonid – vastutavad rakkude eest, soole iseloomulik kehakuju. Kolesterool – raku membraani ehituses. 19.Mis haigus on ateroskleroos? – Veresoonte lupjumine. 20.Lipiidide funktsioonid organismis? – Energiarikas varuaine, temperatuur regulaarne loomadel. Kaitse – taimelehti kattev vahakiht takistab vee liigset aurumist. Varuaine – taimede rasvaarud asuvad õlidena seemnetes ja viljades. Lahusti – d vitamiin on rasvlahustuv aine, mida meie nahk sünteesib piisava päikesevalguse korral. Mees ja naissuguhormoonid on lipiidse ehitusega. 21.Kuidas on omavahel seotud aminohapped ja valgud? – Valgud koosnevad aminohapetest, aminohapete vahel on peptiisid. 22.– 23.Nimeta erinevaid valgustrukstuure, oska neid eristada joonise alusel, too näiteid. – 2 järku: tekib polupeptiidi keerdumisel kruvikujulseks heeliksiks
TAIMEDE ELUPROTSESSID: 1. Fotosünteesivad 2. Hingavad 3. Paljunevad 4. Kasvavad 5. Transpiratsioon ehk vee aurustumine MÕISTEID: Plasmolüüs- raku sisu, protoplasti kokkutõmbumisena avalduv nähtus, mis on tingitud hüpertoonilise lahuse toimel vee väljaimemisest rakus Hüpertooniline lahus- Antud lahusest kõrgema kontsentratsiooniga lahus Hüpotooniline lahus- Antud lahusest madalama kontsentratsiooniga lahus Osmoos- Nähtus, kus lahusti molekulid liiguvad läbi poolläbipaistva membraani suurema kontsentratsiooniga lahuse suunas. Pungumine- Suguta paljunemise viis, kus tütarorganism jääb mõneks ajaks emasorganismi külge ÜLEVAADE BOTAANIKA AJALOOST Carl Linne Töötas välja kahesõnalise nimetamisviisi ehk binaarse nomenklatuuri Kirjeldas väga palju taimeliike ja süstematiseeris need Theophrastus Botaanika rajaja Hakkas taimeriike kirjeldama ja uurima Robert Hooke Leiutas 1
Anorgaaniliste ainete põhiosa mood. vesi. Orgaanilistest ainetest on rakkudes kõige rohkem: valke. Enim levinud valgud: LIPIIDID(rasvad, õlid & vahad) SAHHARIIDID( glükoos, tärklis, tselluloos). DNA- pärilikkuse kandja. RNA- molekulidel on oluline roll päriliku inf. avaldumises. VESI: täidab rakus erin. funkt.- hea lahusti & osaleb enamikus keem. reaktsioonides. Peamised ORGAANILISED ained on: süsivesikud, lipiidid, valgud Ja nukleiinhapped. BIOMOLEKULID: sahhariidid, lipiidid, valgud, nukleiinhapped BIOAKTIIVSED AINED: ensüümid, vitamiinid, hormoonid, antibiootikumid SAHHARIIDID ehk SÜSIVESIKUD on orgaanilised ühendid, mille Koostises esinevad süsinik, vesinik ja hapnik. / täidvad organismis: 1.transpordifunktsiooni, 2. ehituslikku f., 3. kaitse f., 4. energeetilist funktsiooni.
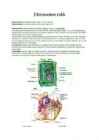
LOOMARAKK RAKUMEBRAAN: ümbritseb rakku, andes rakule kuju · Ühendab rake kudedeks · Kautseb rake Ehitus : fosfolipiidne kaksikkiht, mille sisse sukelduvad valud ja kolesterool Läbi selle toimub ainete trantsport : Aktiivne: enamik molecule on nii suured, et sellleks on vaja lisaenergiat või ainet muuta Passiivne : ained saavad ilma lisapingutuseta liikuda, läbi poori ( O2 ; CO2; H2O ) Difusioon läbimine (gaasiliste aineosakseste liikumine) Osmoos lahusti liigub (lahjemalt kangema lahuse suunas) RAKUTUUM : tavaliselt raku keskel ; seal asuvad kromosoomid, mis kannavad pärilikku infot; kromosoomid on näha raku jagunemisel Tähtsus : · Juhib raku elutegevust · Sisaldab pärilikku infot · Reguleerib rakus toimuvaid protsesse · Tuumakestas toimub ribosoomide moodustamien jar RNA süntees TSÜTOPLASMA : poolvedel aine, mis täidab kogu raku ruumi Tähtsus:
Magusad ained, morsid. Antidiureetiline hormoon väljutatakse hüptalamuse kaudu? ADH o Isotooniline lahus selle osmootne rõhk on võrdne organismi sisese osmoose rõhuga, nt 0,93%line naatriumkloriidlahus o Hüpotooniline lahus selle osmootne rõhk on madalam organismi sisest osmoosest rõhust, nt vesi, seda süstida ei tohi, vesi hakkab minema punaliblede sisse, hakkab pihta osmoos lahusti ühesuunaline muutumine madalama rõhuga keskkonnas kõrgema suunas, punalibles kõrgem osm.rõhk. o Hüpertooniline lahus selle osmootne rõhk on kõrgen kui vereplasmas. Hakkab vedelik punalibledest minema välja vereplasmasse. 3. Organismi talitluse regulatsiooni põhiprintsiibid. Toimib regulaarsete süsteemide kaudu. Närvisüsteem ja humoraalne süsteem (sisesekretoolne süsteem). See töötab, reguleerib veres ringlevate ainete abil. Suurema
Tiitrimismeetodid · otsene tiitrimine · tagasitiitriminekui reaktsioon analüüdi ja titrandi vahel on aeglane või titrant pole püsiv; · kaudne tiitriminekui titrant ei reageeri analüüsitava ainega. Standardlahused · standardlahuste kontsentratsiooni määramise meetodid · otsene meetod · standardiseerimise meetod abi standardlahus Standardlahuste kontsentratsiooni väljendamise viisid · molaarsus - cM (M) · normaalsus - cN (N) · protsent- % · ppm, ppb, ppt · lahustunud aine ja lahusti ruumalade suhe (näiteks 1:4 HCl) · p funktsioonid pH, pX Gravimeetriline tiitrimeetria · Olemus Mõõdetakse tiitrimiseks kulunud titrandi massi · Eelised - suurem kiirus, mugavus; - pole vaja kalibreerida klaasnõusid; - pole vaja arvestada temperatuuri muutusi; - kaalumine on täpsem kui ruumala mõõtmine; - kergelt automatiseeritav. Vesilahuste keemia · Vesilahuste keemiline koostis · Elektrolüüdid - ühendid mis lahustudes vees moodustavad ioone AaBb -> aAb+ + bBa-
petrooleetrit, segasin. Filtrisin ekstrakti klaaslehtriga ja läbi paberfiltri 100 ml mensuuri. - Kordasin protsessi kuni kuni ekstrakt oli läbipaistev (muidu kollane). Ühendasin saadud ekstraktiportsjonid. - Määrasin ekstrakti üldmahu (23,5 ml). 2. Kasutades spektrofotomeetrit mõõtsin uuritava lahuse neeldumisspektrid (aparaat muutis sujuvalt lainepikkuseid vahemikus 350 600 nm), võrduslahuseks puhas lahusti (petrooleeter). Võrdlesin saadud tulemusi laborimaterjalidega, sain tulemuseks, et minu proov (porgand) sisaldas -karoteeni. ABS nm 0,922 424,0 nm 1,207 449,0 nm 1,070 476,0 nm 3. Karoteeni kvalitatiivne määramine: kasutan optilist tihedust mis on mõõdetud
segude lahutamine komponentideks. plaadile vävained: esimene täpp 1 x Black B, teine täpp 2 x Black GSP ja kolmas täpp 1 x Black GSP. Seejärel asetatakse plaat klaasnõusse, kuhu on eelnevalt lisatud eluent 80%-line 2-propanool- vesi, vahekorras Töövahendid: Värvained, värvainete lahusti 75% etanool, eluent: 80 4:1 (40 ml + 10 ml). Klaasinõus jälgitakse eluendi tõusmist %-line 2-propanool-vesi, õhukesekihi plaat (silikageel 60 lõpujooneni, mis asub plaadi stardijoonest 70 mm kõrgusel. Plaat alumiiniumfoolium, tootjafirma MERCK), põleti, klaastoru, viil, eemaldati anumast, kui eluent oli jõudnud 68 mm kõrgusele. Plaat joonlaud, harilik pliiats, suletav klaasnõu, filterpaber
37)Elektrolüüs aine lagunemine ioonideks, kui temast elektrit läbi juhtida. 38) Korrosioon on metalli iseeneslik hävimine ümbritseva keskkonna mõjul. 39)Lahus on ühtlane segu, mis koosneb lahustist ja lahustunud ainest. 40)Lahusti on aine, milles lahustunud aine on jaotunud ühtlaselt. 41)Lahustunud aine on aine, mis asub lahuses pihustunult. 42)Lahustuvus on suurim aine kogus, mis võib lahustuda kindlas lahusti koguses. 43)Disahhariid- kahest monosahhariidist tekkinud sahhariid 44)Lahustumise soojusefekt on lahustumisega kaasnev soojusefekt, mis koosneb kristallivõre lagunemissoojusest(selle arvel lahus jahtub) ja hüdraatumissoojusest(selle arvel lahus soojeneb). 45) Küllastunud lahus on lahus, milles antud tingimustel enam ainet ei lahustu. 46) Küllastumata lahus on lahus, milles antud tingimustel võib veel ainet lahustada. 47)Kristallhüdraat on kristallilises olekus olevad hüdraadid
ANNA NIMETUS CH3 CH CH2 CH2 CH3 ALKOHOLID Alkoholid on orgaanilised ühendid mille molekulis asuvad hüdroüksüül rühmad. Nimetuse tunnuseks on ool. Alkoholid tekivad kui alkaani molekulis asendada 1 või mitu vesiniku aatomit hüdroksüül rühmaga. · Metanool metüülalkoholid rahvakeeles puu piiritus, füüsikalised omadused: värvusetta, iseloomuliku alkoholi lõhnaga vedelik, ülimürgine, põleb, on väga hea lahusti.Süütevedelik,kütus. Lahusti kasutamine, puhastusvahendid, kütuse lisandid. · Etanool etüülalkoholid Värvusetu, iseloomuliku alkoholi lõhnaga vedelik, põleb , kõige vähem mürgisem alkohol, 200gr puhast. Segu mis koosneb 96-98% etanoolist, ja 2-4% veest nimetatakse piirituseks. Hüdroskoopne imab vett endasse. Defitseerija, konvenseerija. Väga hea lahusti, tema kasutus alad on laialdased. Mootori kütus , kütuse lisandid. Süütevedelik. Termomeeter
kilpnäärme haigus - struuma Väikelaste kasv ja vaimne areng aeglustub, juuste, küünte, naha seisund. Vee tähtsus organismis : - Suure soojusmahtuvuse ( hoiab organismisisest püsivat temperatuuri ) - Hoiab ära ülekuumenemise ( loomad higistavas, taimedel toimub transpiratsioon õhulõhede kaudu) - Kindlustab organismide ringeelundkondade töö (veri , lümf ) - Kaitsefunktsioon nt pisarad, liigesed, sülg, loode areneb vesikeskkonnas. - Hea lahusti vees lahustub rohkem aineid, kui üheski teises lahustis. - Hüdrofiilsed ained - Lahustuvad vees, glükoos ja koodusool - Hüdrofoobsed - Ei lahusti rasvad ja õlid - Osaleb paljudes keemilistes reaktsioonides ( lähteainena nt fotosünteesil, lõpp-produktina - Kindlustab rakkude ja kudede mahtuvuse tagab siserõhu ehk turgori. - Organismis veesisalduse ja rakkude siserõhu vähenemisel taimed vajuvad lonti. 31.01
18.Polümeermaterjalid põhitüübid (tabel konspektis lk10) 1)Plastid kompaktplastid, kiled, vahtplastid, komposiidid 2)Kiud *Sünteetilised(tekstiil, koord, polüester, polüamiid) *Modifitseeritud tselluloos (tekstiil) *Looduslik(puuvill,siid, vill) 3)Elastomeerid *Sünteetilised (alkadieenid(auto rehv), polüuretaanid, polüsiloksaanid) *Looduslikud (Hevea brasiliensis) 4)Adhesiivid, pinnakatted, sideained liimid, lakid, värvid, sideained 19.Liimikihi dubleerimine Liim ja lahusti pannakse paberile, lahusti aurub ning siis pannakse paber liimikihiga vahule (nt PU-vaht). Seejärel paber eemaldatakse ja PU-vaht fikseeritakse. See ongi liimikihi dubleerimine 20.Toote plakeerimine See tähendab mingi toote, nt pleki, traadi, torude jt metalltoodete katmist teise metalli või sulami kihiga rakendades valtsimist, valamist keevitamist või pealesulatamist 21. Mis on termoplast? Mis on reaktoplast?
aterogeensete ja kaitsvate lipoproteiinid e vahel 1.3.1 Rasvapleki proov LIPIIDIDE ÜHINE OMADUS: lahustuvus orgaanilistes lahustites. Lipiidi sisaldav lahus tuleb kanda paberile; lahusti aurustub. Oluline on, et järeldusi saab teha kuiva prooviga paberit uurides, sest niiske paberi läbipaistvus on suurenenud ka lipiide mittesisaldavate lahuste korral Lahus sisaldab lipiide, kui: · Paberile moodustub rasvaplekk, millest paberi läbipaistvus suureneb · Vastu valgust vaadates on rasvaplekk muust paberist heledam · Pimeda poole vaadates on rasvaplekk muust paberist tumedam TÖÖ KÄIK: 1
Rõhk oluliselt mõju ei avalda. Lahustus suureneb temperatuuri tõustes, kui lahustumisprotsess on endotermiline. Väheneb temperatuuri tõustes, kui lahustumisprotsess on eksotermiline. Lahustumise temperatuurisõltuvus väljendab lahustuvuse muutumist temperatuuri muutmisel. Sellistes lahustes (nt NaCl lahus) on küllastunud vedelike aururõhk väiksem kui nt puhta vee kohal. Kinnises süsteemis lahutsunud ainete osakesed jäävad vedelikku, auruvad lahusti molekulid. Avatud süsteemis lahustunud ainete osakesed jäävad alles, muu aurustub. Lahusti molekulid, mis on lahusti pinnal, difundeeruvad lahustist välja ja hajuvad ümbritsevasse gaasilisse keskkonda (lendumine). Kui lahus sisaldab tahkeid, mittelenduvaid aineid, nt keedusoola lahus, siis lendub vesi. Vedelik vedelikus: sarnased vedelikud (vesi, etanool) lahustuvad teineteises igas vahekorras. Temperatuuri tõusuga suureneb vedelike vastastikune lahustumine
Täidab mitmesuguseid funksioone: 1) Ta on hea lahtusti ja osaleb enamikes keemilistes reaktsioonides (fotosünteesi lähteaine; hingamise lõpp-produkt). 2) Transpordifunktsioon – kindlustab organismide siseelundkondade töö 3) Kaitsefunktsioon – pisarad, sülg, loode 4) Tagab siserõhu rakkudes (selle vähenedes tekivad kortsud) 5) Suure soojusmahtuvusega – aitab säilitada organismisisest püsivat temperatuuri. Vesi lahustina Vesi on polaarne lahusti. Vesi on lahusti ka endale, sest vees osa H2O molekule lõhutakse ja tekivad H+ ja OH- aatomid. Lahusti – keskkond, kus midagi lahustuma hakkab. Diffusioon – lahustunud osakeste liikumine madalama kontsentratsiooni suunas. Osmoos – kui lahustunud osake ei saa liikuda läbi membraani, liigub lahus selleks, et ainete konsentratsioonid võrdsed oleks Osmolaarsus – lahustunud osakeste arv lahustis. Reguleerib lahusti liikumist rakkudest piiritletud ruumis. Hüdrofoobne – vett hülgav
sajandini ja mis kandis alkeemia nime. Nimetus alkeemia tuleneb vanaegiptuse sõnast chemi, mida tõlgendatakse erinevate autorite poolt isemoodi. Keemia tähendavat musta maad või musta maagiat (maagide ja nõidade käsitööd) või metallide sulatamise kunsti. Araablased lisasid eesliite al- ja nii kujuneski sõna "alkeemia." Alkeemikute põhieesmärkideks oli filosoofilise ehk tarkade kivi, elueliksiiri ja universaalse lahusti ehk alkagesti leidmine. Filosoofiline kivi tähendas seda, et selle abil loodeti väheväärtuslikest metallidest saada väärtuslikke metalle nagu näiteks kulda. Elueliksiiri abil loodeti ravida kõiki haigusi ja pikendada eluiga või tagada hoopis igavese elu. Universaalne lahusti aga tähendas seda, et selle lahustiga sai lahustada kõiki aineid ja seetõttu teha kõiki katseid kõikide ainetega. Üle 2000 aasta taguse Egiptuse võimsus oli seotud just metallide tootmisega, eriti
polarisatsioonitasapinda. Eripöörang on arvutuslik suurus, mis väljendab monokroomse valguse pöördenurga muutust, kui see on läbinud teepikkuse 1 dm keskkonnas (s.o. lahusekihi paksus), mis sisaldab optiliselt aktiivset ainet kontsentratsioonis 1 g/ml. Mida suurem eripöörang, seda optiliselt aktiivsem on aine. Eripöörang alati määratakse ja kõik pöördenurga muutused määratakse temperatuuril 20oC ja lainepikkusel (Na-lainepikkus) 589,3 nm. Alati märgitakse ära ka lahusti [] = (a*100)/(l*c), kus alfa- mõõdetud pöördenurk l lahusekihi paksus (dm) c lahuse kontsentr. (gr/100ml lahuse) vedelike jaoks : [] = /l*p kus p vedeliku tihedus (gr/1ml) kontsentratsiooni leidmine: c = ( *100)/([]*l) Valgus, mis näiteks päikeselt tuleb, on polariseerimata. Valgus võngub täiesti suvalistes tasandites. Kui
Kordasin sama ka pesuveega. NaCl täielikuks väljapesemiseks filtri pooridest täitsin filtr i destilleeritud veega. 1 Valasin lahuse keeduklaasist mõõtesilindrisse ja lisasin destilleeritud vett, et lahust saaks 250 cm3 . Mõõtsin segatud lahuse tiheduse areomeetriga. Katseandmed Mass segu C = 7,03 g Ruumala lahus = 250 ml = 0,25 l Mass lahusti (vesi) = 119 ml Lahuse tihedus = 1017 kg/m3 = 1,017 g/cm3 Mõõdetud tihedusest väiksem tihedus tabelist = 1,0161 g/cm3 Mõõdetud tihedusest suurem tihedus tabelist = 1,0197 g/cm3 Massiprotsent, mis vastab tihedusele ρ1 = 2,50 % Massiprotsent, mis vastab tihedusele ρ2 = 3,00 % Katseandmete töötlus ja tulemuste analüüs NaCl protsendiline sisaldus lahuses: 𝐶%2 − 𝐶%1 0,5%
Biokeemia eksamiks kordamine 1) Selleks, et tagada vajalike rasvhapete piisav saamine, peab toit sisaldama nii loomset kui ka taimset rasva. 2) Ööpäevasest energiavajadusest peaksid valgud täitma: 10-15% 3) Ööpäevasest energiavajadusest peaksid süsivesikud katma: 55-60%. 4) Mitu % inimese ööpäevasest vajadusest peavad täitma lipiidid? 26-30% 5) Vee saamine ja eritumine organismis peaksid olema tasakaalus: õige/vale 6) Katabolism on (dissimilatsioon ehk lagundav ainevahetus ) on organismis hapniku kaasabil toimuv keemiline protsess, ainevahetuse osa, milles keerulisematest ainetest tekivad lihtsamad ja milles vabaneb energiat. 7) Inimorganismis olev vesi jaguneb võrdselt erinevate ruumide: õige/vale 8) Palaviku korral on organismi veevajadus suurenenud: õige/vale 9) Altsidoos on vere pH tõus: õige/vale 10) Põhibioelemendid on: Vesinik (H), süsinik (C), hapnik (O), lämmastik (N), fosfor (P), väävel (S). 11) Lihtvalke v...
KASUTUSVALDKONNAD · Vesinik on tähtis tooraine nii keemiatööstuses... · eelkõige ammoniaagi tootmiseks · Osaleb orgaanilises sünteesis · Redutseerijana metallide saamisel · ...kui ka energeetikas. · Vesiniku põlemisel eraldub palju energiat, mistõttu on vesinik hea raketikütus ja sobiv redutseerija vooluallikates. · Ta on kerge · Teda on lihtne salvestada. VESINIKU ÜHENDID · Levinuim ja tähtsaim ühend on vesi. · Keemia tööstuses tähtsaim lahusti. · Looduses oluline organismide elutegeuvses. · Kuulub ka hapete, enamiku orgaaniliste ainete jpt väga tähtsate ainete koostisesse. · Olulist rakendust on leidnud ka hübriidid. · Kasutatakse redutseerijana keemilistes vooluallikates ja orgaanilises sünteesis. VESINIKU ÜHENDID · Puhta volframi saamiseks kasutatakse vesinikku. WO3 + 3H2 = W + 3H2O METALLIOKSIIDI JA VESINIKU REAKTSIOON
Pinotsütoos selle käigus omastab rakk vedelikus lahustunud aineid. Mõned ained (vesi, gaasid, etanool) liiguvad läbi membraani difusiooni ja osmoosi teel (imbuvad) see ongi passiivne transport. Osa rakumembraani koostisse kuuluvatest valkudest on varustatud kanalikesega, mille kaudu toimub väiksemate molekulide liikumine kui selleks ei kulutata täiendavat energiat, siis on ka see passiivne transport. Osmoos lahusti molekulide difusioon läbi poolläbilaskva membraani madalama kontsentratsiooniga keskkonnast kõrgema kontsentratsiooniga lahuse suunas. Raku infovahetus väliskeskkonnaga: Retseptorvalgud seovad rakku ümbritsevast keskkonnast erinevaid molekule (nt hormoone) ja vallandavad seejärel mitmesuguseid biokeemilisis reaktsioone, mille tulemusena muutub raku sisetalitlus vastavalt väliskeskkonna muutustele. Igas eukarüootsel rakul on taku tuum koos rakutuumakestega
Na soola koostises (NaCl). Rakuväline element. K rakusisene element, leidub kapsas, rosinates. Mg kuulub luude koostisesse; tähtis klorofüllis; sõltub marjade küpsus. Ca luukoesse kuuluvad; vähesuse pärast luu hõreneb. Fe- kuulub vere punastes libledes (hemoglobiinis). I kilpnäärme hormoonis (türoksiin). Na ja K reguleerivad vee tasakaalu. Soodustavad närviimpulsside edasikannet. Kindlustavad raku laengu (pos/neg). Anorgaanilised ained I VESI vesi on universaalne lahusti. Hüdrofiilsed ained on need ained, mis lahustuvad vees (söögisööda, glükoos). Hüdrofoobsed ained on need, mis ei lahustu vees (rasvad, õlid). * Vesi tagab rakkude ainevahetuse e metabolismi. Mida rohkem on rakus vett, seda kiirem on ainevahetus. * Vesi tagab raku siserõhu e turgori. * Vesi kindlustab organismi ringeelundkondade töö (vereringe, lümfiringe). * Vesi kindlustab termoregulatsiooni. Vee auramine jahutab keha (higistamine, taimedel õhulõhede kaudu)
(DNA A&T;C&G, RNA A&U;C&G) 39 biheeliks DNA ruumiline mudel 1. Millised keemilised elemendid kuuluvad makroelementide hulka? Miks vajab organism neid suhteliselt suurtes kogustes? O, C, H, N, P, S O, C ja H kuuluvad kõigi orgaaniliste ühendite koostisse. N, P ja S on valkude ja nukleiinhapete ehituses. 2. Millist keemilist ühendit on organismides kõige rohkem? Vett (H²O) 3. Selgita 4 näitega, milles seisneb vee bioloogiline tähtsus. Rakus: Vesi on hea lahusti ja osaleb enamikus keemilistes reaktsioonides. Vesi aitab säilitada organismides püsivat temperatuuri. ... 4. Too 4 näidet katioonide ja anioonide tähtsusest organismis. Katioonid: Kaalium- ja naatriumioonid osalevad närviimpulsi moodustamises, neid leidub ka veres ja kõigi rakkude tsütoplasmas. Kaltsiumsoolad annavad luudele tugevuse. Raual oluline roll selgroogsete loomade hingamisel vajaliku hapniku sidumisel. Anioonid: Jood on vajalik kilpnäärmehormoonide sünteesiks
2H2O 2H2 + O2 * keemiline reaktsioon elektrivoolu toimel. 11 / 24 Tähtsamad ühendid Vesi (H2O) Kasutamine: ● H2 ja O2 tähtsaim ühend. ● põllumajanduses; ● Värvusetu vedelik. ● hügieenitoiminguteks; ● 3 agregaatolekut. ● tuumaelektrijaamades; ● Levinuim lahusti. ● joogiks; ● Levinuim aine Maal kui ● toidu valmistamiseks; ka universumis. ● jne... ● Leidub inimorganismides. 12 / 24 Tähtsamad ühendid Ammoniaak (NH3) Kasutamine: ● N2 ja H2 ühend. ● väetistes; ● Värvuseta. ● lõhkainete ja
Keemia aluste praktikumi KT küsimusi ja ülesandeid 1. Kippi aparaadi tööpõhimõte. Reaktsioonivõrrand CO2 saamiseks Kippi aparaadis. CO2 gaasi tekitamiseks (vesiniku) paigutatakse tahke aine (tsink) reaktori ülemisse ossa, hape (lahjendatud HCl) valatakse lehtrisse, kust ta valgub reaktori alumisse ossa. Pärast viimase täitumist satub hape tahke ainega kokkupuutesse. Keemilise reaktsiooni tulemusena tekkinud gaas väljub reaktorist kraani kaudu. 2. Milliseid gaase on võimalik saada Kippi aparaadi abil? Kippi aparaadi abil on võimalik saada gaase, mida võib saada tahkete ainete reageerimisel happega. Näiteks süsinikdioksiidi kaltsiumkarbonaadist soolhappe toimel. 3. Kuidas määratakse CO2 suhtelist tihedust õhu suhtes (töövahendid, töö käik, arvutused)? Kaalun kolvi, seejärel kolvi CO2-ga, seejärel täidan kolvi veega (vett 250 ml nagu gaasigi). Arvutan CO2 ja õhu mahu kolvis normaaltingimustel. Selleks vaatan ruumi temperatuuri ja rõhu ...
Etanool · Et C2H5OH keemistemperatuur on madalam kui veel, siis hakkab nende segu keemisel kõigepealt aurustuma etanool. · Saadud aurud kogutakse ja jahutatakse. Nii destilleerimise tulemusel on võimalik saada piiritust, milles on 95% etanooli ja 5% vett. Etanool · Veevaba 100% etanooli nimetatakse absoluutseks etanooliks, mille saamiseks seotakse piirituses olev vesi keemiliselt, näiteks veevaba vasksulfaadiga. · Etanool on hea lahusti, lahustab hästi orgaanilisi ühendeid (rasvu, vaike, bensiini jm.), kuid ka mõningaid anorgaanilisi aineid (joodi). Etanool · Etanool on hea sünteeside lähteaine (kummi tootmise, aga ka ravimite, värv- ja lõhnaainete valmistamisel ning alkohoolsete jookide koostisosa, meditsiinis konservandina ja antiseptilise vahendina). Etanool · Kasutatakse termomeetrites, sest külmumistemperatuur on 112 oC. Kõrge
Ökosüsteem Ühel territooriumil olev elusloodus ja eluta keskkond, mis on aineringe kaudu seotud. Rakkude koostises on orgaanilisi aineid 18% (suhkur) ja anorgaanilisi 82% (Vesi ja sool). Bioelemendid jagunevad: 1) Põhielemendid e makroelemendid C, H, O, P, N, S 2) Ioonsel kujul esinevad elemendid Na, K, Ca, Mg, Ce 3) Mikroelemendid Fe, Cu, Zn, I, F Anorgaanilised ained: Vesi, katioonid organismides. Vesi Miks nii palju: · Hea lahusti, seega ainus võimalik reaktsioonidetoimumise keskkond. · Osaleb ise reaktsioonides. · Suure soojusmahtuvusega hoiab organismide temperatuuri. Lisaks veega seotud: 1) Rakusisene rõhk 2) Mineraalainete allikas 3) Viljastumine 4) Vesi kui elukeskkond 5) Biosfääri kliimat kujundav tegur Katioonid organismis K ja Na ioonid: Närviimpulss sünapsis, rakurõhu regulaator Ca ioonid: Luudele tugevus
Peale käärimise saadava etanooli toodeteakse tööstuses suuretes kogustes etanooli süsivesinikest, mida omakorda saadakse naftast. Etanooli omadused Molekuraalvalem: C2H6O Molaarmass: 46.06844(232) g/mol Välimus: värvitu puhas vedelik Tihedus: 0.789 g/cm³ Sulamistemperatuur: -114.3 °C Keemistemperatuur: 78.4 °C Happelisus: 15.9 Etanooli kasutamine · Alkohoolsed joogid · Hea lahusti (lahustab rasvu, vaike, bensiini, aga ka näiteks joodi) · Värvi- ja lakitööstus · Parfümeeriatööstus ( odekolonnid, lõhnaõlid) · Ravimid ( tinktuurid, eeter) · Indikaatorlahused ( fenoolftaleiin) · Sünteetiline kautsuk (kummitööstus) · Lõhkeained (suitsuta püssirohi) · Keemiline süntees (dietüüleeter, kloroform, etaanhape, estrid jt) · Meditsiin ( antiseptiline toime, desinfitseerimisvahendid) · Piiritustermomeetrid
Ca- luukoe komponent, aktiveerib verehüübimist, mõjutab lihasrakkude talitlust, vahendab hormoonsignaale, tagab luukoe säilimise ja arengu Mg- osaleb luukoe moodustumises, on paljude ensüümide kofaktoriks, kindlustab ribosoomide terviklikkuse, on oluline replikatsioonil ja transkriptsioonil Fe- vajalik paljude valkude ja ensüümide ehituses ja talitluses (hemoglobiin, hingamisahela ensüümid jm.), seob ja transpordib organismis hapnikku 6. Vee ülesanded organismis? vesi on universaalne lahusti, on paljude reaktsioonide lähteaineks, loob stabiilse sisekeskkonna, kindlustab raku siserõhu ehk turgori, osaleb termoregulatsioonis, transpordib erinevaid aineid 7. Kuidas jaotatakse sahhariide? pentoosid (riboos, desoksüriboos) omavad viite süsinikku heksoosid (glükoos, fruktoos) omavad kuute süsinikku 8. Nimeta 4 erinevat monosahhariidi, nende valemid, kus neid leidub ja milles seisneb nende tähtsus. riboos, desoksüriboos, glükoos, fruktoos 9
Orgaanilised ained: valgud, lipiidid, sahhariidid, nukleiinhapped, madalmolekulaarsed orgaanilised ühendid. 17. Vee molekuli ehitus - üks vee molekul koosneb kahest vesiniku ja ühest hapniku aatomist. 18. Vee ülesanded organismides: Molekulaarsel tasandil - vesi on reaktsioonis lähteaineks (fotosünteesi reaktsioonis). Vesi kindlustab hüdrolüüs reaktsioonid (tärklise hüdrolüüs glükoosis). Vesi on väga hea lahusti. Kindlustab PH-tasakaalu. Raku tasandil kindlustab raku stabiilse sisekeskkonna. Organismi tasandil Kaitseb ülekuumenemise eest. Lahustunud kujul eraldub jääkaineid. Looteareng. Viljastumine. Ökosüsteemi tasandil - peamine kliimat kujundav faktor. On kolmes agregaatolekus.
V ekstrakti kogumaht, ml 3 d ekstrahendi tihedus, g/cm g uuritava proovi mass, g 3 10 tegur üleminekuks milligrammidele. LIPIIDIDE REAKTSIOONID Vajab parandamist 28.03. M.K. (1.3.) 01 Rasvapleki proov Teooria: kõigi lipiidide ühiseks omaduseks on lahustuvus orgaanilistes lahustites. Lahuse tilga kandmisel paberile ja lahusti aurustumisel moodustub lipiide sisaldava proovi korral paberile rasvaplekk, millest paberi läbipaistvus suureneb. Rasvaplekk on vastu valget vaadates muust paberist heledam ja pimeda poole vaadates tumedam. Töö käik: kahte katseklaasi pandi 1g kummastki tahke aine proovist. Mõlemasse katseklaasi valati umbes 1 ml orgaanilist lahustit (atsetooni). Loksutati ja lasti 5 min sesita. Mõlemast katseklaasist kanti pipetiga tilk tahke materjalikohal olevat lahust paberile ja kuivatati.
Nendest ainetest on mürgine metanool, kuid ülejäänud seda pole. Etanooli saadakse alkoholikäärimise teel. See on sarnane metanoolile, kuid pole nii mürgine. Etanool põhjustab joovet, suuremate koguste sissevõtmisel aga teadvusekaotust ja mürgitust, mis võib lõppeda ka surmaga. Etanoolist võib tekkida sõltuvus, kuna suur osa käärimisel saadavast etanoolist kulutatakse alkohoolsete jookide valmistamiseks. Kuid seda ei kasutata ainult sellel otstarbel. Etanool on hea lahusti ja seetõttu kasutatakse seda väga palju nii keemiatööstuses kui ka vedelate ravimite valmistamisel. Etanooli kasutatakse ka desinfitseerimisel, kölni vees ja lõhnaõlides. Osades troopikamaades, kasutatakse seda ka bensiinina. Peale käärimise toodetakse etanooli ka süsivesinikest. Etanooli kasutamisel alkohoolsetes jookides on aga väga suur tagajärg. Kuna see tekitab joovet võib see olla väga kahjulik inimese elule. Isegi kui inimene pole tihti joobes võib juba
Etanool on värvuseta, põletava, kõrvetava maitsega vedelik, mille sulamistemperatuur on -112 ºC ja keemistemperatuur 78 ºC. Etanool on veest kergem vedelik, sest tema tihedus on 0,794 g/cm³. (2) Ühendid: · Etanolaadid (naatriumetanolaat CH3-CH2ONa) · Etaani halogeenterivaadid (bromoeteen CH 2Br) · Eteen · Dietüüleeter · Etanaal (etüületanaat CH3-COO-CH2-CH3) (4) Kasutamine: · Alkohoolsed joogid · Hea lahusti (lahustab rasvu, valke, bensiini, aga ka näiteks joodi) · Värvi- ja lakitööstus 5 · Parfümeeriatööstus (odekolonnid, lõhnaõlid) · Ravimid (tinktuurid, eeter) · Indikaatorlahused (fenoolftaleiin) · Sünteetiline kautsuk (kummitööstus) · Lõhkeained (suitsuta püssirohi) · Keemiline süntees (dietüüleeter, kloroform, etaanhape , estrid jt) · Meditsiin (antiseptiline toime, desinfitseerimisvahendid) · Piiritustermomeetrid
· Polaarsed fosfaadi ,,pead" paigutuvad vee pinna äärde. · Mittepolaarsed rasvhapped jätavad ,,sabad" veest välja. Hüdrofiilne ,,pea" vettarmastav Hüdrofoobne ,,saba" vettkartev Lipiidide funktsioonid rakus: · On energiaallikas · Soojuse säilitamine · Varu toitumine · Ehituslik funktsioon · Ainevahetuslik funktsioon · Bioregulatoorne funktsioon · Lahusti funktsioon Valgud · Valgud koosnevad aminohapetest. · Valgud on kõrgmolekulaarsed ühendid. Valkudes on aminohapped seotud valkudega peptiidsidemetega. · Valgud on koostiselt lihtvalgud ehk proteiinid. · Aminohappejääkide arv võib ulatuda 100-st 1000-ni.
Metanooli kasutatakse keemiatööstuses suurtes kogustes, samuti ka lahustite koostisosana. Väliste omaduste poolest on metanool peaaegu eristamatult sarnane etanooliga ja see on põhjustanud hulganisti traagilisi eksitusi. Eluohtliku mürgituse võib saada 30 g joomisel. Sage tagajärg on pimedaks jäämine. 2)Etanool (C H OH ) ehk etüülalkohol jääb tööstusliku toodangu mahu poolest metanoolile alla, 2 5 kuid on samuti tähtis lahusti ja sünteeside lähteaine. Etanooli valmistatkse kahel viisil: 1)etüleeni katalüütilisel hüdraatimisel: 2)sahhariidide (taimsete materjalide) kääritamisel 3)Propanool (C H OH ) iseloomuliku lõhnaga narkootilise toimega mürgine värvuseta vedelik. 3 7 Seguneb igas vahekorras vee, etanooli ja etüüleetriga, sisaldub puskariõlis. Sünteetiliselt saadakse sedaeteenist oksosünteesi teel, seda tarvitatakse lahustina ja propaanhappe ja estrite sünteesis.
vedelik on poorse seinaga anumas teise vedeliku sees. Osmootne rõhk: p=RT/V RTM (R on universaalne gaasikonstant). Näit: looduses on osmoosseks anumaks rakk. Betoonid võivad osutuda poorseteks, et leiab aset osmoos. Mitmesugused läbivate pooridega ehitusmaterjalid. Keraamilised tooted st. põletatud savid. 11) Lahused kahe või enama puhta aine homogeensed segud (võivad olla vedelas, gaasilises või tahkes olekus) Lahusti üldjuhul see aine, mida on rohkem massi- või mahu%-des (erand: vesilahused olenemata vee kogusest, on lahustajaks vesi). Vahuks nimetatakse vedelikus lahustunud gaasi, suspensiooniks vedelikus lahustunud tahket ainet ja emulsiooniks vedelikus segunenud mitte lahustuva vedeliku segu. Vedelate lahuste klassifikats küllastamata: kui vedelasse lahusesse viidud väike kogus ainet selles veel lahustub
Vedelik tahke aine tasasel pinnal märgab:(adhesioon suurem kui kohesioon) tahke aine pind tõmbab vedeliku osakest tugevamalt, kui vedelik ise; 90; tõuseb mööda pragusid ja kapillaare üles (tõusu kõrgus on pöördvõrdeline kapillaari raadiusega h=2/gr), ei märga: vedelikuosakeste omavahelilsed jõud on tugevamad, kui vedeliku ja tahke aine vahelised jõud; 90; surub kapillaaridest välja. Valgub laiali täielik märgamine. Osmoos: lahusti molekulide ühesuunaline difusioon läbi poorse vaheseina. Looduses on osmoosseks anumaks rakk. Ehituses nt betoonist mahuti lahuses. Kohesiooni jõud on osakeste vahel vedelikus faasi ajal. Adhesiooni jõud on vedeliku osakeste ja pinna osakeste vahel erinevate faaside vahel. Muutes neid jõude, saab muuta märgavust. Näited: et vesi märgaks vähe puitu, siis puit värvitakse; vesi ja vesilahused pinda ei märga. 12
b) Kuidas muutub CO2 osarõhk, kui CO osarõhku vähendada? c) Kuidas muutub H2 kontsentratsioon, kui CO kontsentratsiooni suurendada? d) Kuidas muutub reaktsiooni tasakaalukonstant, kui H2O kontsentratsiooni vähendada? 25. Tasakaalulised protsessid (tuua näiteid). Aurustumine – küllastunud auru rõhk lahuse kohal on tasakaalu tingimustes konstantne suurus. Lahustumine – lahustunud aine jaotumine kahe omavahel mitteseguneva lahusti vahel vastavalt jaotuskoefitsendi väärtusele. Faaside tasakaal 26. Heterogeenne süsteem, faas, faasisiire. Faas - ühtlase koostisega ja konkreetses olekus olev süsteemi osa, mis on teistest faasidest eraldatud piirpinnaga. Faas võib koosneda mitmest ainest. Faasisiire e faasi üleminek, on aine üleminek ühest faasist teise. 27. Aururõhk, aurustumissoojus, sulamissoojus. Aurustumine on vedela faasi üleminek gaasiliseks, energia neeldub. Aine faasi
Kaltsiumi puudimisel tekkivad krambid. Reguleerib vee hulka organismis. Raud Kuulub selgroogsete punalibledes oleva valgu hemoglobiini koostisesse. (seob hapniku) HEEM(rauaühend-annab verele punase värvuse)* Jood On vaja kilpnäärme hormoonide sünteesiks. Kui inimese toidus joodididioone piisavalt pole siis kilpnääre haigestub ja tekkib struuma. 2.2 Anorgaanilised ained VESI -suurepärane lahusti Hüdrofiilsed ained- lahustuvad vees Hüdrofoobsed- ei lahustu vees(rasvad ja õlid) Vee ülesanded: · On suure soojusmahtuvusega( hoiab püsivat temperatuuri) · Hoiab ära ülekuumenemise · Kindustab organismide ringeelundkondade töö · Kaitsefunktsioon. Nt pisarad, liigesed, sülg jne. · Tagab raku siserõhu ehk turgori Osaleb paljudes keemilistes reaktsioonides 6CO2 + 12H2O C6H12O6 + 6H12O6 + 6H2O + 6O2 (fotosüntees)
-) Kaitsefunktsioon Nahaalune rasvkude juhib halvasti soojust ja see kaitseb organismi temperatuuride muutuste eest. -) Bioregulatoorne funktsioon Tsüklilised lipiidid on bioloogiliselt aktiivsed ained, mis reguleerivad ainevahetuslikke protsese. Seega ,,rasvad" reguleerivad ainevahetust. -) Ainevahetuslik funktsioon Rasvade oksüdatsioonil on lõpp-produktideks CO 2 ja H2O. Tekkinud vett kasutavad kõrveloomad veedefitsiidi tingimustes. -) Lahusti funktsioon Rasvlahustuvad vitamiinid (K, A, D, E, Q) lahustuvad vaid rasvas (vees ei lahustu). Teatud hüdrofoobsed ained talletuvad rasvkoes. Valgud * Valgud ehk proteiinid aminohapetest moodustunud biopolümeerid. -) Aminohapped valgumolekulis on ühendatud omavahel peptiidsidemetega. -) Valkude omadused tulenevad valgu molekuli koostises olevate aminohapete järjestusest ja hulgast. * Valgu molekulide struktuurid:
läheneda reaktsioonitsentrile haliidi vastasküljest. St steerilistel põhjustel ei saa Sn2 reaktsioon toimuda arüülhaliidides. Reaktsioon toimub seda kiiremini, mida tugevam on nukleofiil Lahkuv rühm on rühm, mida nukleofiil asendab, mida enam on laeng lahkuvas rühmas delokaliseeritud, seda stabiilsem ta on ja seda parem lahkuv rühm ta on. Soodustab karbkatiooni teket Sn1-s ja lahkub kergemini nukleofiili Sn2-s. Lahusti mõju reaktsioonidele: o Sn2 toimub kiiremini polaarsetes aprotoonsetes lahustites, kuna need ei solvateeru ei nukleofiili ega elektrofiiliga, samas soodustavad laengute eraldumist o Sn1 toimub kiiremini lahustites, mis stabiliseerivad karbkatiooni: polaarsed aprotoonsed lahustid ja protoonsed lahustid o Erinevus seisnebki protoonsete lahustite efektis Sn2 takistavad, Sn1 soodustavad.
klompuma alles ca 11000C juures. Seetõttu saab kivivilla kasutada väga kõrgete tulekaitsenõuetega kohtades.Kasutatakse seinte, katuste, põrandate, samuti torustiku isoleerimiseks. Tuntuimad tootjad Rockwool ning Paroc AS 58. Värvid - koostiskomponendid, sideaine kõvastumisprotsesside liigitus. Värvid jagunevad: õlivärvid, vesivedeldajaga mineraalvärvid alküüdvärvid, lateksvärvid, epoksüvärvid ja eriotstarbelisedvärvid Värvi koostiskomponentideks on: lahusti, pigment, täitematerjal, sideaine. Sideaine moodustab kelme, mis kinnitub alusele. Kelme koostisesse kuulub pigment ja muud värvi koostisosad. Sideaine määrab nakke alusega (adhesiooni) ja kelme osade omavahelise nakke (kohesiooni) ning värvi keemilised omadused. Sideaine oluliseks omaduseks on ka pigmenditerade fikseerimine kelmes. Värvides kasutatakse sideainena nii orgaanilisi (näiteks alküüdvaik) kui ka mineraalseid (näiteks lubi-, tsementvärvid) aineid
3) ainete kasutamine vastavalt organismi vajadustele 4) jääkproduktide väljutamine väliskeskkonda Toitainerühmad: süsivesikud, valgud, lipiidid (rasvad), vesi, vitamiinid, makro-ja mikromineraale. 2) Passiivne ainete transport Passiivselt liiguvad vesi, gaasid ja teised väikesed molekulid difusiooni, osmoosi teel või transportvalkude abil. Selleks pole vaja täiendavat energiat. Difusioon - CO2, O2 kõrgemalt madalama suunas. Osmoos (ka aktiivne)– H2O lahusti molekulid liiguvad madalamalt kontsentratsioonilt kõrgema kontsentratsiooni suunas. Aktiivne transport Aktiivtransport toimub ainult läbi transportvalkudes olevate kanalite. Erinevaid aineid transpordivad eri valgud. Energiat saadakse ATP-st. Hüpertooniline lahus on lahus, mille osmootne rõhk on kõrgem võrreldava lahuse (nt vereplasma) osmootsest rõhust. Hüpotooniline lahus, mille osmootne rõhk on madalam võrreldava lahuse (nt vereplasma) osmootsest rõhust.
[] Illustratsioon 3 Tsemendikotid (http://www.heidelbergcement.com/ee/et/kunda/tooted/Pakitult_turustatavad_tsemendid.htm ) AS Silbet-s toodetakse põlevkivituha baasil näiteks poorbetoonblokke [] Ehituskeemia Viru Keemia Grupp pakub erinevaid tooteid ehitustegevuseks. Esimeseks on mastiks ,,Esmol", mida toodetakse põlevkiviõli destilleerimisjäägi alusel ning millele on lisatud plastifikaator ja orgaaniline lahusti. Seda kasutatakse bituumen-rullmaterjalide liimimiseks katusekatte alusele ja valatud katuse paigaldamiseks. Lisaks saab seda kasutada vundamendi, raud-betoontarindite ja liivtsemendist põrandate hüdroisoleerimiseks. Kolmandaks kasutusalaks on torustike korrosioonitõrje. [] Ehituskrunt ,,Esmol"-it kasutatakse pehmekatuse remondiks ja paigaldamiseks ning vundamentide hüdroisoleerimiseks. Tegemist on tootega, mis põhineb põlevkiviõli
Etanool põleb, moodustades CO2 ja vee: CH3CH2OH + 3O2 -> 2CO2 + 3H2O Metanool ehk metüülalkohol ehk karbinool[viide?] (triviaalnimetusega puupiiritus) keemiline ühend valemiga CH3OH. Ta on lihtsaim alkohol. H | H -- C -- O -- H | H Füüsikalistelt omadustelt on metanool kergesti lenduv värvitu tuleohtlik mürgine nõrga alkoholilõhnaga vedelik. Metanool põleb praktiliselt nähtamatu leegiga: 2CH3OH+2O2=2CO2+2H2O Metanool on kasutusel antifriisi, lahusti ja kütusena. Samuti lisatakse teda etanoolile selle denatureerimiseks. Metanool tekib looduses mõningate anaeroobsete bakterite ainevahetuse tulemusena, päikesevalguse toimel oksüdeerub see aja jooksul taas süsihappegaasiks ja veeks. Mürgisus Et metanool on lõhnalt ja maitselt sarnane etüülalkoholile ehk etanoolile, juhtub tihti metanoolimürgistusi. Ensüüm alkoholi dehüdrogenaas lagundab metanooli mürgiseks sipelghappeks ja
Vere osmootne rõhk - kui palju erinevaid aineid on vereplasmas lahustunud. Vere onkootne rõhk - kui palju on vereplasmas valke. Hoitakse verd veresoonkonnas. o Isotooniline lahus selle osmootne rõhk on võrdne organismi sisese osmoose rõhuga, nt 0,93%line naatriumkloriidlahus o Hüpotooniline lahus selle osmootne rõhk on madalam organismi sisest osmoosest rõhust, nt vesi, seda süstida ei tohi, vesi hakkab minema punaliblede sisse, hakkab pihta osmoos lahusti ühesuunaline muutumine madalama rõhuga keskkonnas kõrgema suunas, punalibles kõrgem osm.rõhk. o Hüpertooniline lahus selle osmootne rõhk on kõrgen kui vereplasmas. Hakkab vedelik punalibledest minema välja vereplasmasse. Hemolüüs, nähtus kus punalibled purunevad ja nendes sisalduv hemoglobiin väljub. Punalibled ise on ümmargused vormelemendid, mis sisaldavad hemoglobiini, mis on punaka värvusega ja annab verele iseloomuliku värvuse
iooni) antud aine mass Homogeenne segu – selle koostis on sama ka väga väikestes segu kogustes. Nt siirup või soolvesi. Homogeenseid segusid nimetatakse lahusteks. Heterogeenne segu – selles segus on komponendid eristatavad kas palja silmaga (liiv ja vesi) või mikroskoobiga (piim). Lahusti – lahuse see komponent, mida on kõige rohkem, või mille tähtsust tahame rõhutada (nt vesi) Lahustunud aine – lahuse komponent, mis ei ole lahusti. Ühes lahuses võib olla mitu lahustunud ainet. Vesilahuses on lahustiks vesi. Mittevesilahuses on lahustiks muu aine kui vesi (nt piiritus, atsetoon, tolueen). On ka tahked lahused ja gaasilised lahused. Ruumalaprotsent = lahustatava aine ruumala/lahuse ruumala *100%. Kasutatakse nt alkohoolsete jookide puhul (vol) Molaarsus e molaarne kontsentratsioon – näitab lahustunud aine moolide arvu ühes liitris lahuses: molaarsus=lahustunud aine hulk/lahuse ruumala. Ühik mol/l ehk M
ületada. Enamiku lahuste lahustuvus paraneb kõrgemal temperatuuril. Lahustuvus küllastastanud lahuse kontsentratsioon. Küllastunud lahus on lahus, milles on lahustunud maksimaalne võimalik kogus lahustunud ainet. Üldreegelid lahustuvus: *Ioonvõrega ja polaarsed ühendid polaarsetes lahustites (soolad, alused, happed vees) *Mittepolaarsed ühendid mittepolaarsetes lahustites (orgaanika orgaanikas benseenis, süsiniktetrakloriidis CCl4) ·Kui nii lahusti kui lahustunud aine on vedelikud kasutatakse mõisteid segunevad ja mittesegunevad vedelikud. 35. Kuidas jagatakse lahuseid lahustunud aine sisalduse järgi? Iseloomusta lühidalt! Lahustunud aine sisalduse põhjal eristatakse: *küllastumata lahus lahus, milles antud ainet veel lahustub *küllastunud lahus lahus, mis sisaldab antud temperatuuril ja rõhul maksimaalse koguse lahustunud ainet (tasakaal) *üleküllastunud lahus aeglasel jahutamisel saadud ebapüsiv süsteem, mis
Ande Andekas Bioloogia Loomarakk Kuna valdav osa rakkudest on mikroskoopiliste mõõtmetega loetakse rakuteaduse e. tsütoloogia (uurib rakkude ehitust ja talitlust) alguseks XVII saj. keskpaika, mil leiutati valgusmikroskoop. Alles 1831. a. jõuti rakutuuma kirjeldamiseni. Kõik organismid on rakulise ehitusega. Iga uus rakk saab alguse üksnes olemasolevast rakust selle jagunemise teel. Rakuteooria on evolutsiooni- ja pärilikkusteooria kõrval üks bioloogia nurgakive. Rakkude ehitus ja talitlus on omavahel kooskõlas. Loomorganismide 4 põhilist koetüüpi on epiteel- (rakud paiknevad tihedalt üksteise kõrval, moodustab naha pindmise osa ja ümbritseb siseorganeid, kaitsefunktsioon), lihas- (rakud on pikliku kujuga ja sisaldavad valgulisi müofibrille, mis võimaldavad muut...