Kristallid Kristall on keemilise elemendi, ühendi või isomorfse segu korrapäraselt paigutunud aatomeist koosnev tahke homogeenne ja regulaarselt korduva ühikrakuga struktuur. Kristallide korrapärase siseehituse välispidiseks väljenduseks on siledate ja kindlate seaduspärasuste alusel moodustunud tahkudega kristallvormid. Kõik kristallid jagatakse kuue süngoonia vahel, mis omakorda koosnevad kolmekümne kahest punktigrupist. Füüsikalised omadused Esinemisvorm e. haabitus - kristallivorm või mineraalse agregaadi tüüp Värvus tuleneb mineraalilt peegeldunud valgusvoo spektraalsest koostisest, mis sõltub mineraali koostisest Kriipsu värvus on mineraali pulbri värvus, mis võib erineda kristalli värvusest Läige on mineraalide omadus peegeldada valgust. Erinev läige sõltub
Kristallid Kristallid on täiuslikud Maa energia kandjad. Oma füüsilise ja energeetilise kristallilise ülesehituse poolest on nad ka meie eluks vajaliku kosmilise elujõuenergia vahendajad. Oma erilise teadvusega suudavad nad muuta nii meie füüsilise, mentaalse, psüühilise kui spirituaalse keha vibratsioone ning neid harmoniseerida ja muuta. Praegusel Uuel Ajastul on meie maailma tunnetus, mõistmine ning teadvus oluliselt avardunud ning paljud meist otsivad loomulikumaid ning Loodusele lähemaid elamis- ja tervendusviise, et oma tõelist väge taastada. Seepärast on viimastel aastatel hüppeliselt kasvanud ka nende inimeste arv, kes tunnevad huvi kristallide ning kristalliteraapia vastu ning otsivad instinktiivselt kristallide ja nende tervendava väe lähedust. Nende juuresolekul toimub meis midagi maagilist ja seniseletamatut. Kristalle ja kive on kasutatud tervendamiseks iidsetest aegadest alates pea...
Alfalagunemine: aatomituuma radioaktiivne muundumine, mille korral kiirgub alfaosake(2p, 1n). Alfalagunemisel väheneb aatomituuma massiarv 4 ja laenguarv 2 võrra. Ioonside tekib kui üks aatom loovutab ja teine liidab elektrone, elektronegatiivsuste erinevus peab olema suur, esineb aktiivse met ja mmi vahel. Ruumvõre e. Kristallvõre kristallide aatomite ja ioonide kindel paiknemine, väga tihedalt. Aatomeid seob molekulideks ja kristallideks keemiline side. Kristallid: makroskoopilised hiidmolekulid, milles aatomite, ioonide või molekulide paiknemine on korrapärases kristallvõres. Kovalentside: tekib ainete ühiste elektronpaaride vahel, esineb aatomite vahel molekulides või kristallides, toimub nn elektronide jagamine. Keemiline side jaguneb: ioonsidemeks ja kovalentsidemeks. Võredefekt: kristallides esinev hälve võre ideaalses korrapärasuses. Elektron on ergastatud seisundis siis kui ta neelab footoni ning saades
Kvartsi perekonna kristallid Helena Tarum 10B Kvarts Kvarts (saksa quarz) on silikaatne kivimit moodustav mineraal. Esineb nii tard, moonde kui ka settekivimeis. Iseloomuliku kujuga: heksagonaalne prisma , mille tippudeks on püramiidid. Esieb paljude kivimite koostises. Liiva olulisim koostisosa(8090%) Kvartsikristalle kasvatatakse ka tehislikult Omadused Keemiline valem SiO2 Mineraaliklass karkasssilikaadid Molekulmass 60,08 Värvus puhtana värvitu Tihedus (g/cm³) 2,65 Kõvadus 7 Lõhenevus puudub Kriips valge Murdepind karpjas Läige klaasiläige (tahul), rasvaläige (murdepinnal) Kvartsi pere mineraale ahhaat mäekristall ametüst oonüks avanturiin plasma jaspis roosakvarts kaltsedon serdoolik karneoo...
sümmeetriaga olekutel erinev energia. Seotud seisund kovalentne side - saab tekkida ainult siis kui väliselektronide spinnid on antiparalleelsed (radiaalosa on sümmeetriline).Kovalentne side on spetsiifilise kvantmehaanilise päritoluga ja sellel klassikalist analoogi ei ole. (Ühinevate aatomite tuumade tõuge tasakaalustatakse nii,et elektronpilve tihedus on suurim tuumade vahelises alas ). 2. Kristallvõre: Kristallid on makroskoopilised hiidmolekulid, milles aatomid või ioonid on paigutunud korrapärasesse (perioodiliselt korduvate ühikrakkudega) ruumvõresse. Kristallides (tahkistes) muunduvad aatomite/ioonide väliselektronide energiatasemed mitme eV laiusteks energiatsoonideks, mille hõivamine elektronide poolt järgib tõrjutusprintsiipi ja mis on ühised kogu kristallile.Kristallvõre on igal juhul füüsikaline mudel idealiseering. 3
1.1. Aatomeid seob molekulideks ja kristallideks keemiline side, mille põhiliigid on ioon- ja kovalentside. 1.2. Ioonside tekib positiivsete ja negatiivsete ioonide vahel, kovalentside elektronpaaride ühistamisel 1.3. Kristallid on makroskoopilised hiidmolekulid, milles aatomid või ioonid on paigutunud korrapärasesse (perioodiliselt korduvate ühikrakkudega) ruumvõresse. 2.1. Kristallides (tahkistes) muunduvad aatomite/ioonide väliselektronide energiatasemed mitme eV laiusteks energiatsoonideks, mille hõivamine elektronide poolt järgib tõrjutusprintsiipi ja mis on ühised kogu kristallile. 2.2. Metallides on kõrgeim hõivatud energiatsoon ainult osaliselt elektronidega asustatud
Aatomikooslused Molekulid ja kristallid Klass: 12 Kuupäev: 9. aprill Tallinn 2009 Tõrjutusprintsiip Eri elemente eristab laenguarv Z:Z prootonit tuumas ja sama arv elektrone selle ümber elektronkattes parvlemas. Enamikus tuumades on olemas ka mingi kindel arv neutraalseid tuumaosakesi, neutroneid, kuid nendest ei sõltu, mis elemendile aatom kuulub ja aatomi omadusi mõjutavad nad nõrgalt. Positiivne tuum tõmbab neid kõiki endale võimalikult lähemale. Elektroni leiulaine on tema "koht" aatomis. Tuumale lähimale, põhiseisundile vastava leiulaine peakvantarv n = 1, edasi kihistuvad ergastatud kvantseisundid, mille n = 2, 3 jne. Elementide spektrite ning füüsikaliste ja keemiliste omaduste uurimine näitab, et laias laastus on selline alglähend mõistlik. Tuuma tõmbele alludes asuvad kõi Z elektronid tuumale lähimasse leiulainesse? Siis sarnaneks kõikide aatomite spektrid vesiniku spektrile. N...
Swarovski kristallid Koostas: Õppegrupp: Juhendaja: Mis on Swarovski ? · On kaubamärgi nimi varieeruvalt täpselt lõigatud kristallide ja luksus ehete tootjalt. · Kristall: kvaliteetse teemantlõikega ja tugeva sädelusvõimega, üks lummavamaid kristalle maailmas. · Kristallid: omapärased ja omavad maagilist võimet. · Meistrid räägivad , et need tooted hoiavad ruumides positiivset ja head energiat. Avastaja · Daniel Swarovski I (24.10.1862- 23.01.1956), sündis Põhja-Boheemias. · 1895.a. oli Daniel Swarovskil unistus luua ideaalne kristall, mis säraks kui teemant. · Ta rajas Swarovski aastal 1895 külas Wattens, koha küllaldase hüdroenergia pärast. Kristallwelten · Kristallwelten, kristaliseeritud fantaasia
TURMALIIN Füüsikalised omadused Keerulise koostisega alumiinium-boorsilikaat (Na,Ca)(Mg,Fe,Mn,Li,Al)3Al6[Si6O12](BO3)3*(OH)4 Mineraalide klass: silikaat Värvus: värvusetu,roosa,roheline,sinine,pruun,must jne. Süngoonia: trigonaalne Kuju: prismalised-tulpjad kristallid Läbipaistvus: läbipaistev või läbipaistmatu. Läige: klaasiläige Kõvadus: 7-7,5 Tihedus: 3,02-3,41 g/cm 3 Leidub graniitides ja pegmatiitides. Tunnused · Värvus oleneb selles leiduvatest lisanditest.Erinev värvus ei ole üksnes kristallidel vaid ühe eri kristalli osad võivad olla erivärvilised. · Kuumutamisel omandab elektrilaengu, millega on võimalik tuhka tõmmata. · Vastavalt värvusele on igal turmaliinil oma nimetused:
Füüsika Keemiline side - seob aatomeid molekulideks ja kristallideks Keemilise sideme liigid: · Kovalentne side ühtlustunud elektronpaaride vahendusel · Iooniline side positiivsete ja negatiivsete ioonide vahel Keemiliste sidemete tekkimine tekib aatomite ,,annetamise" või ,,ühistamise" teel Kristallvõre aatomid/ioonid on paigutatud korrapäraselt ruumvõresse Võredefekt: · Üksikud aatomid või ioonid paiknevad vales kohas · Mõned võresõlmed on vakantsed (tühjad) · Kristalli on lisatud teisi keemilisi elemente · Terasele lisati Cr ja Ni - roostevaba teras Keelutsoon on energiatsoon, millele vastav energiavahemik on elektronidele laineomaduste tõttu keelatud Lubatud tsoon- on kristallis valentselektronide energiatasemete jagunemisel tekkinud alatasemete kogum, millele vastavad energiad on elektronidele lubatud Valentstsoon - on viimane elektronidega täielikult täidetud lubatud tsoon Juhtivustsoon valentst...
Kristall. Vahendid: kuum vesi, sool/sooda, värv, lusikas, anum, kaas ja niit. Kirjeldus: Kõik vahendid panin valmis ning esimesene ma keetsin 200ml vett. Järgmisena panin vette ainet ja tegin küllastunud lahuse. Kui see kõik valmis sai, kinnitasin niidi kaane külge. Ja edasi, panin ma selle purgi külma kohta näiteks külmkappi. Kadri Lepiku 7k 29.11.11 Pildistasin ka mõned fotod kristalli kohta ...
Vaata tulemusi Laboritöö nr 6 Kasutaja ID: Katse: 1 / 3 Hulgast 100 Küsimus 1 (6 points) Kui vaadeldava sulami (näiteks 50% Cu ja 50% Ni) mikrostruktuuris on ühte liiki kristallid. Millise faasiga on tegemist? Student Response: Õppija Vastuse variandid vastus a. asendustüüpi tardlahusega b. sisendustüüpi tardlahusega c. keemilise ühendiga d. kahe komponendi kristallide mehaanilise seguga Score: 6/6 Küsimus 2 (5 points) Mis on eutektne mehaaniline segu?
Kristalli soojusjuhtivus ja tema optilised omadused sõltuvad samuti suunast. Sellist kristalli omaduste sõltuvust suunast anisotroopiaks. Kui aine omadused suunast ei sõltu, on tegemist isotroopiaga. Nagu vedelikuski on ka kristallides molekulid pakitud tihedalt, mis teeb kristalli raskesti kokkusurutavaks. Tahkises valitseb molekulide vahel vastastikmõju, mis määrab ka kristallile iseloomuliku struktuuri. Eristatakse nelja põhitüüpi vastastikmõju. Nende järgi jaotatakse ka kristallid nelja tüüpi: · Ioonkristallid · Aatomkristallid · Molekulkristallid · Metallilised kristallid Ioonkristallides on põhiliseks vastastikmõjuks positiivsete ja negatiivsete ioonide elektrostaatiline tõmbumine. Aatomkristallides seisavad aatomid koos naaberaatomite ühiste elektronpaaride abil. Molekulkristallis valitsevad elektrilised jõud, mis on tingitud sellest, et molekulid on polaarsed nende ühes otsas on positiivne, teises aga negatiivne
Tahke keha omadusi saab uurida, kui on teada Fermi nivoo asukohta. 1.1 Ioonilisesideme teke Iooniline side- üks aatom võtab teiselt elektroni ära, iooniline side moodustab kristalli, kuna struktuur võib jätkuda lõpmatuseni. Positiivsete ja negatiivsete ioonide vahel tekib tõmme, mis seostab ioonilise sideme. Kloor tõmbab naatriumi elektroni, et ma pilve aatom oleks ühtlasem ja energia väiksem. 1.1.1 Kristallid Aatomid/ioonid on paigutatud kindlas korras, moodustades ruumvõre . Võre konstandi saab määrata lainepikkuse kaudu. Kristallides on aatomid paigutatud väga tihedalt. Kristallide difraktsioon-uuringuiks tuleb asutada lühikesi laineid: röntgenkiirgust, elektornide või neutronite kimpe. 1.1.2 Metalliline side Metall koosneb positiivsetest aatomitest. Iga metalli aatom:ä 1. koosneb positiivsetest ioonidest 2. annab ära elektrone
NEW AGE'i MÕJU LÄÄNE-EUROOPLASTELE New Age on vaimne liikumine, mis hõlmab paljusid alternatiivseid maailmavaateid ja elulaade. Võetakse erinevatest religioonidest endale sobivaid komponente ja segatakse need kokku. Sellest hoolimata ei ole New Age religioon, see on mõtteviis, elulaad. Kuidas on New Age mõjutanud meid, lääne-eurooplasi? Esiteks tooksin ma välja ravimise kristallidega, mida New Age'i liikumise liikmed harrastavad. Alles hiljuti lugesin artiklit ühest Inglismaa spaast, kus on võimalik proovida kristallide ja muude vääriskividega keha eest hoolitsemist, ravimist. Teiseks, ka alternatiivne meditsiin on leidnud koha meie ühiskonnas. Näiteks minu ema, kellel on seljaga probleeme, käib valu ilmnemisel alati ühe mehe juures, kes tema selga masseerib, venitab, painutab, sellega ragistab ning raksutab ja valu kaob! New Age'i liikumise puhul kogunevad selle liikmed enesearendusgruppidesse või m...
kihtpilved (Stratus), kiudpilved (Cirrus) ning sajupilved (Nimbus); neist viimast enam eraldi klassiks ei loeta. Lumi Lumi on väikeste jääkristallide kogum. Lumi moodustub atmosfääris temperatuuril alla 0°C, kui veeaur sublimeerub otse kondensatsioonituumakesele või juba olemasolevale jääkristallile, moodustades heksagonaalse süngooniaga kristalle. Atmosfääris liikudes kasvavad jääkristallid suuremaks ning langevad lõpuks maapinnale. Kristallid võivad üksteisega seostuda, moodustades niiviisi lumehelbeid. Udu, sudu Udu on vahetult aluspinna kohal heljuvate veepiiskade, harvemini jääkristallide või mõlemate kogum, mis vähendab nähtavust väiksemaks kui 1 km. Udu tekib siis, kui õhu suhteline niiskus on 100%. Udupiisad moodustuvad, kui veeaur kondenseerub kondens atsioonituumakestele. Sudu on teatud tüüpi õhusaaste. Termin "sudu" on kokku pandud sõnadest 'suits' ja 'udu'. Eeskujuks sellise sõna
1. Kui vaadeldava sulami (näiteks 50% Cu ja 50% Ni) mikrostruktuuris on ühte liiki kristallid. Millise faasiga on tegemist? Student Response Feedback A. sisendustüüpi tardlahusega B. kahe komponendi kristallide mehaanilise seguga C. asendustüüpi tardlahusega D. keemilise ühendiga Score: 6/6 2. Mis on eutektne mehaaniline segu? Student Response Feedback
28. Millise kahe keemilise elemendi ühendid on Maakoores valdavad? Mis liiki mineraale need moodustavad? Maakoores on valdavad hapniku ja räni ühendid, mis moodustavad... 29. Mineraali mõiste ja selle tunnused. Mineraal on loodusliku tekkega, kindla koostise, kindla struktuuriga anorgaaniline tahke aine. See koosneb ühe või enama elemendi aatomitest. Mineraalid esinevad kristallilises olekus. Erinevatel mineraalidel on erikujulised kristallid. Maalt, meteoriitidest ja Kuu kivimeist käesolevaks ajaks leitud üle 3700 erineva mineraali. Mineraale uuriv teaduharu on mineraloogia. Mineraali koostise individuaalsus seisneb tema koostisosade aatomite, ioonide ja ioonrühmade seostumise kindlas vahekorras, mida väljendab mineraali keemiline valem. Mineraalide makroskoopilisel määramisel toetutakse nende mitmesugustele füüsikalistele omadustele. 30
Toidu külmutamine 10.kl Varstu Keskkool 2013 Üldiseloomustus Toidu külmutamine on levinud toidu säilitamise viis, mis aeglustab toidu hävinemist ja muudab vee jäätumisega bakterite arengu võimatuks ning aeglustab suuremat osa keemilisi reaktsioone Külmutamise protsess Külmutatud toitu peaks kvaliteedi nimel võimalikult kiiresti (värskena) külmutama Protsess algab toorainest, mis olgu kvaliteetne, sest õige külmutamine ei paranda toidu omadusi, vaid ainult säilitab seda Toitu tuleb hoida õhust eemal ja "mahlasid" tuleb säilitada. Vastasel juhul võib toit kuivada ja toidu kvaliteet langeda Külmutamiskiirus on oluline külmutada tuleb nii kiiresti kui saab. See vähendab jääkristallide suurust, vähendades jäätumisel toidule tekkinud kahju Külmutamise ajalugu Toidu kümutamise tehnoloogiat on näiteks palju kasutatud Arktika kommuunides Jäässe on kaevatud auk või ja sinna pannakse toiduai...
Aatom aineosake, mis koosneb aatomituumast ja elektronidest; molekuli koostisosa. Molekul molekulaarse aine väiksem osake, kovalentsete sidemetega seotud aatomite rühmitus Keemiline side aatomite- või ioonidevaheline vastasikmõju, mis seod nad molekuliks või kristalliks Kovalentne keemiline side aatomitevaheline keemiline side, mis tekib ühiste elektronipaaride moodustumisel Polaarne kovalentne side kovalentne side erineva elektronegatiivsusega aatomite vahel, sidet moodustavatel aatomitel tekivad seejuures erinimelised osalaengud. Mittepolaarne kovalentne side kovalentne side, mille ühine elektronipaar kuulub võrdselt mõlemale sidet moodustavale aatomile; esineb võrdse elektronegatiivsusega aatomite vahel Iooniline side ioonidevaheline keemiline side, mis tekib vastasmärgiliste laengutega ioonide tõmbumise tõttu. Vesinikside täiendav keemiline side, mille moodustab ühe molekuli negatiivse osalaenguga elektronegatiivse e...
Molekulid ja kristallid tekivad aatomite ühinemisel ühe aatomi elektron siirdub teisele,ioonide vahel tekib tõmme s.a ioonside Kristallid on makroskoopilised hiidmolekulid,milles aatomid või ioonid on paigutunud korrapärasesse ruumvõresse.Kristallides on aatomid/ioonid paigutatud kindla korra järgi(ruumvõre).Ruumvõres tuleb esile defekte,mida põhjustavad *lisandid,*irdunud aatomid või ioonid,*tühjad võresõlmed.Defektid mõjutavad elektrilisi,optilisi jm füüsikalisi keemilisi omadusi. Aatomeid seob molekulideks ja kristallideks keemiline side,mille põhiliigid on ioon-ja kovalentside. Ioonside tekib positiivsete ja negatiivsete ioonide vahel,kovalentside-elektronpaaride ühistamisel Ühinevate aatomite tuumade tõuge tasakaalustatakse nii,et elektronpilve tihedus on suurim tuumade vahelises alas.Sellist sidet nimet. kovalentseks e. homeopolaarseks. Metallis:väliselektronide tasemed saavutavad aatomite elektrilise vastasikmõju toimel laiad mõõ...
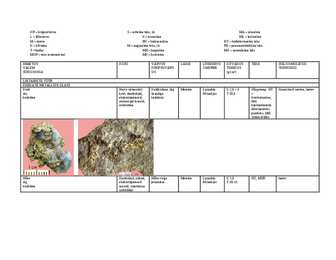
nende poolt võõrs keha sissetungimisele avaldatavat vastupanu. Mineraalide kirjeldamine Anorgaanilised mineraalid I rühmkond. Ehedad elemendid. Ehedas olekus on maakoores avastatud umbes 30 elementi, peamiselt metallid. Nende kaaluline osatähtsus on väga väike. Sellesse rühma kuuluvad kõik väärisgaasid, erirühma mood. väärismetallid. Väävel S. Mõnikord sisaldab S mehhaaniliste lisanditena kipsi, orgaanilisi aineid, gaase jms. Rombilise ja monokliinse süngoonia kristallid v. amorfsed kogumikud. Kõvadus (K) 1-2, erikaal (E) 2,1. Värvus iseloomulikult õlgkollane. Kristalli tahkudel teemandi-, murdepinnal rasvaläige. Tekib peam. biokeemilisel teel meredes, kus bakterite lagundava tegevusetagajärjel eraldub sulfaatidest H2S, mis oksüdeerudes annab eheda väävli. Samuti tekib S-i ka vulkaanide ümbruses vulkaanilistest gaasidest sublimeerulisel. S-i kasut. põllumaj.-ke kahjurite tõrjel, väävelhappe saamiseks, kummi vulkaniseerimisel jm. Teemant C
Teemant Oktaeedrilised, Värvitu, kollakas, Teemandi L selge K 10 MUA Murdumisnäitaja 2,42, 1 C kuubilised, punakas, sinakas, M ebatasane T 3,5 plahvatuslõõrid kraat = 0,2 g Kuubiline dodekaeedrilised must es, kristallid Grafiit Lehelised, Tumehall Metalne L täiuslik K 1, MO Teeb kriipsu paberile, C soomusjad agreg., katsumisel orgaanilise C määrib sõrmi heksagonaalne; strukt. kihiline muldjad massid; rasvane T 2,2 moondel; HT; heksagon
talk 1 ortoklass 6 kips 2 kvarts - 7 kaltsiit 3 topaas - 8 fluoriit 4 korund - 9 apatiit 5 teemant 10 Kõvadust määratakse mineraali kriimustamise teel kõvadus-skaalasse kuuluvate mineraalidega. Enamike mineraalide kõvadus ei ületa 7. 28.11.12 9 · Valem: CaCO3 · Kuju: rombilised kristallid · Kõvadus: 3,5 - 4 · Värvus: värvitu, valge, hall, kollakas, punakas · Läige: klaasi 28.11.12 10 · Valem: CaMg(CO3)2 · Kuju: teralised agregaadid, rombilised kristallid, mille tahud on kõverdunud · Kõvadus: 3,5 - 4 · Värvus: valge, kollakas, pruun, tumehall. · Läige: klaasi · Erikaal: 2,8 2,9. 28.11.12 11 Valem: MgCO3 Kuju: trigonaalsed kristallid. Kõvadus: 4 4,5
KRISTALLIDE KASVAMINE ERI KUU FAASIDEL Jevgeni Malešin 8B Aleksandra Ivask 8B Eesmäärgid 1.Kuidas kristalli kasvada? 1.Milles kuu faasidel kristall kasvab kiiremini? HÜPOTEES Kristallide kasvamine ei sõltub kuu faasidest. kristallid kristallid — on tahke aine ,milles on väikesed osakesed (aatomid,ionid või moleekulid) . ! Kristallid ei kanna nägu aksesuaar.et kristallid mõne aja pärast hakkavad katki saama, ja nad kahjustavad nahka! KRISTALLIDE LIIGID monokristall– õige kristall (õige kristalli polükristall– kristall millal on teiset kristallid kokku kuju). kasvanud. MEILE ON VAJA: 1.lehter 2.piirituslamp 3.kolb 4.keraamiline kruus 5.statiiv 6.mõõtetsilinder 7.filter Töö kaik Keeduklaasi valatakse u 50 ml – 100 ml keevat vett (mida rohkem
tükikesteks Esinemise vorm ja koht: Eestis leidub Alam-Siluri dolomiitides. Võhma ümbruses, kus polümetalne maagistumine on seotud tektoonste lõhedega. Püriit Kuju: kuubilised, pentagoondodekaeedrilised kristallid; massiivsed teralised kristallid Püriit Kõvadus: 6 – 6,5 Värvus: kollane, kriips must Läige: metalne Iseloomulikud tunnused: tahkudel viirutus, vasaraga löömisel annab sädemeid ja on tunda väävlilõhna Esinemise vorm ja koht: esineb terakestena või peeneteralise massina
Värvus muutub meekollasest mustani raua sisalduse suurenedes. Lõhenevus täiuslik Arseen normaaltingimustel stabiilne, hall, rabe tahke aine Kinaver punakat värvi, kristalliseerub heksagonaalse süngoonia kristallidena, kristallid on prismalised või nõeljad Väävel mittemetall, rombiline,värvuselt kollane,rohekas, punakas, kriips on valge, rabe, kristalliline, reljeefne aine, eristatav lõhn (tikud!!) Püriit - Õlgkollase värvusega, esineb sageli hästi väljakujunenud kuubilise kujuga kristallidena,
Põhjustab ka silma ja nahaärritusi. Kõrgetel temperatuuridel on süttiv. Etanool: kergesti süttiv, silma sattumisel ärritav. Meetodi olemus Ümberkristallimiseks on vaja saavutada kuumutamisel ja sobiva lahusti järkjärgulisel lisamisel küllastunud lahus. Seejärel lahus jahutatakse aeglaselt, kristallide tekkimist aitab tritureerimine, idustamine, lahuse külmutamine. Kristallide eraldamiseks lahus filtreeritakse, lisandid peaksid jääma lahusesse, kristallid koosnema vaid puhtast ainest. Katseseadme joonis (koos aparatuuri detailide nimetustega) Eksperimendi kirjeldus (tegevus punktide kaupa enne praktilist tööd ja töö käigus lisada detailsem kirjeldus koos omapoolsete tähelepanekutega) · Koostasin aparatuuri, kinnitasin statiivile muhvi abil kahe labaga käpa, muhv vastava avaga ülespool. · Käpaga kinnitasin ümarkolvi, kolvi mitte liiga tugevalt kinni pigistades, kuid ikkagi kindalt.
Metaanhüdraat - kas oht keskkonnale või tuleviku kütus? Metaanhüdraat ehk põlev jää on jääsarnane kristalliline aine, mida leidub ookeani sügavustes. See koosneb jääst ja kergestisüttivast gaasist metaanist. Metaan moodustub muda sees elavate mikroobide elutegevuse käigus. Need mikroobid lagundavad ookeani põhja vajunud orgaanilist ainet. Metaan ühineb peaaegu külmunud veega, misjärel moodustuvad metaanhüdraadi kristallid. Need kristallid on nagu imetilluksed jääpuurid, mis metaani enda sees hoiavad. Et kristallid saaksid moodustuda, peab vee temperatuur olema külmumispunktist veidi kõrgem ning mere sügavus peab olema vähemalt 500 meetrit. Kui need tingimused on täidetud, hakkavad metaanhüdraadi kristallid kasvama, moodustades kobrutavat lumetaolist ollust. Kui seda ainet tuua vee pinnale ning see põlema süüdata, põleb see punaka leegiga, järele jääb vaid veeloik
Alates 1980-ndate aastate lõpust pöördus taas Eesti publiku poole nii muusiku kui ka nt suuremate rockkontsertide ja -festivalide esinejana. Laulukonkurssid Rostockis (1972) Vilniuses (1974, kus anti talle kõik auhinnad, mis üldse ühel lauljal oli võimalik saada) Kahel aastal Sopotis (1975 zürii eripreemia ja 1979.a III preemia) Ansamblid Virmalised Kristallid Kustas Kikerpuu ansambel Radar Lainer Kristallid 1967. aastal alustas oma muusikukarjääri Olav Ehala popansamblis Kristallid. Koosseis: Olav Ehala (klahvpillid, saatevokaal) Jaak Joala (laul, flööt, basskitarr) Olev Künnap (soolokitarr, laul) Anton Lutt (löökriistad) Mati Tibar (saksofon) Vello Roomet (trompet) Evald Mölder (trompet) Boris Lehtlaan (laul) Virmalised Virmalised olid 19651977. aastal tegutsenud Eesti ansambel. Moodusati Tallinnas ajendiks mängida välismaa rockansamblite laule. Jaak Joala ühines bändiga 1968 sügisel.
b) katseklaasi pandi Zn graanul Zn pinnale vasekihti ei tekkinud, kuna kompleksühendi püsivuse tõttu ei suutnud Zn vaske ühendist välja tõrjuda 2.3 Kahte katseklaasi valati ~1 ml 0,2M NiSO4 lahust a) lisati tilkhaaval 0,2M NaOH lahust b) lisati tilkhaaval 6M NH3H2O vesilahust Atsiidokompleksid 3.1 0,5 ml 0,2M NaCl lahusele lisati 1 tilk AgNO3 lahust Lisati ~3 ml küllastunud NaCl lahust 3.2 a) katseklaasi pandi mõned Co(NO3)26H2O kristallid, 2-3 ml atsetooni tekkis lillakas lahus b) lisati NaCl kristalle NaCl kristallide ümber olev sade värvus siniseks 2 c) loksutati kuni NaCl lahustumiseni, lisati ~1 ml vett. Lahus värvus roosaks 3.3 0,5 ml 0,2M Bi(NO3)3 lahusele lisati tilkhaaval 0,25M KI lahust Lisati tahket KI 3.4 0,5 ml 0,25M KI lahusele lisati 1 ml vett ja 1-2 tilka 0,2M Pb(NO3)2 lahust Lisati tahket KI 3.5
kraadini ja suunatakse tankidesse seisma. Tekib sade ja puhas mahl, puhastatakse kaks korda. o Kuum puhastamine mahl kuumutatakse ja segatakse lubjapiimaga. Sade eemaldatakse. o Puhastamisele järgneb sulfiteerimine 5) Mahla paksendamine auruga o Kuivaine sisaldus 4050% suunatakse vaakumaparaati, jätkub aurustumine o Saadakse täitemass 6) Suhkru tsentrifuugimine eemaldatakse kristallid melassist 7) Suhkru rafineerimine toorsuhkur segatakse kokku suhkrusiirupiga (melassi jääkide lahustamine) o Tsentrifuugimine o Töötlemine auruga puhastamine o Lisatakse kemikaalid o Sade filtreeritakse o Kristalliseerimine o Tsentrifuugimine 8) Suhkru kuivatamine 2. Kirjeldada suhkrupeedist suhkru tootmise tehnoloogiat, mille poolest erineb see protsess suhkru tootmisest roosuhkrust.
NiSO4 + 2NaOH Ni(OH)2 + Na2SO4 - sade on heleroheline b) Lisati tilkhaaval 6M NH3·H2O vesilahust NiSO4 + 6NH3·H2O [Ni(NH3)6]SO4 + 6H2O - tekkis sinine kompleks Atsiidokompleksid 3.1 0,5 ml 0,2M NaCl lahusele lisasin 1-e tilga AgNO3 lahust NaCl + AgNO3 AgCl + NaNO3 - valge hõbekloriidi sade Ag+ + Cl AgCl Lisasin ~3 ml küllastunud NaCl lahust NaCl + AgCl Na[AgCl2] sade kadus, tekkis kompleksühend. 3.2 a) Panin katseklaasi mõned Co(NO3)2·6H2O kristallid, 2-3 ml atsetooni Tekkis punakas-lillakas lahus: Co(NO3)2*6H20 [Co(H2O)6]2+ b) Lisasin NaCl kristalle, NaCl kristallide ümber olev sade värvus siniseks, NaCl valged kristallid muutusid sinakaks. Co(NO3)2 + NaCl [CoCl4]2- + Na+ c) Loksutasin kuni NaCl lahustumiseni, lisasin ~1 ml vett. Lahus värvus roosaks [CoCl4]2-+6H2O[Co(H2O)6]2++HCl 3.3 0,5 ml 0,2M Bi(NO3)3 lahusele lisasin tilkhaaval 0,25M KI lahust Bi(NO3)3 + 3KI BiI3 + 3KNO3 tekkis must sade
SISUKORD Tunnused Tahked ained Difusioon Soojusjuhtivus Sisehõõrdumine Tahkiste liigid Kristallide struktuur Metallid TUNNUSED: Tahkete ainete kuju ja ruumala säilib Tõmbe- ja tõukejõud molekulide vahel on väga suured Molekulide paigutus tahkistes korrapärane Amorfsetes molekulide paigutus korrapäratu Korrastatus tahkistes- kaugkorrastus Korrastatus amorfsetes- lähikorrastus TAHKED AINED TAHKISED AMORFSED (kivi, kristallid jne) (plastiliin, pigi) Difusioon Difusioon Soojusjuhtivus Soojusjuhtivus Sisehõõrdumine Sisehõõrdumine DIFUSIOON Tahkistes esineb vähesel määral. Nt. Kulla ja plii kokkusurumine... Amorfsetes esineb suuremal määral. Nt. Plastiliini kokkusurumine... SOOJUSJUHTIVUS Tahkistes esineb regulaarselt. Nt. Kuumas tees metall- lusikas. Amorfsetes esineb vähem. Nt. Parafiini soojus. SISEHÕÕRDUMINE Tahkistes tinglik... Nt
samas soodustades teiste moodustumist. Aurustamine kahe solvendi segust · Meetodi puhul kasutatakse ära aine lahustuvuse erinevust erinevates solventides. Sageli valitakse solvendid nii, et aine on paremini lahustuv solvendis, mille aururõhk on suurem. Lahus aurustub, muutub lahuse komponentide koostis, sest solvendid lahustuvad erineva kiirusega ja lõpptulemus on, et aine kristalliseerub välja. · Kristallid saadakse kätte kui kuumutatakse ainet ühes lahustis ja siis valatakse lahust teise lahustisse või siis üle purustatud jää. Kristalliseerumine sulamist · Toimub vastavalt Oswaldi seadusele, mille järgi polümorfsete substantside sulami jahutamisel esimesena tekib vähim stabiilne modifikatsioon, mis järgnevalt muutub astmeliselt stabiilsemaks modifikatsiooniks. · Kuna metastabiilne vorm omab madalamat sulamistäppi, on tugev jahutamine vajalik
● Järgmisena paigutatakse mahl suurtesse anumatesse ja lastakse settida. See protsess kestab umbes kaks tundi ● Vedelik, mis jääb setetest ülespoole, kogutakse suurtesse anumatesse ning keedetakse läbi. Sellega tõuseb vedeliku suhkrusisaldus viieteist protsendilt kuuekümnele protsendile. Tekib paks suhrumass, kuna suhkur karamellistub ● Nüüd valatakse mikroskoopilised sahharoosi kristallid suhkrumassi (see kuivatab suhrumassi) ning asetatakse kuuma anuma sisse ● Järgmisena lastakse segul kuumas anumas seista ning selle protsessi käigus kuumutatakse vedelik välja. Seejärel hakkavad moodustuma suhrukristallid ● Kristaliseerunust massist eraldatakse mitte kristaliseerunud siirup ● Nüüd asetatakse suhkur keerlevasse anumasse, kust suurel kiirusel lendavad välja kuumad suhru kristallid.
13) Kas gaasid on head või halvad soojusjuhid? Kus seda ära kasutatakse? Gaasid on väga halvad soojusjuhid. Kasutatakse ära talvejopedes (sulejoped). 14) Mille poolest erineb mittemärguv aine märguvast ainest? Mittemärguv aine ei valgu siledal pinnal laiali, kuid märguv aine valgub. Mida suurem on märgumisteguri väärtus, seda paremini laoutub aine ruumis laiali. 15) Mille poolest erinevad monokristallid polükristallidest? · Monokristallid - monokristallilistes ainetes paiknevad kristallid kindla korra järgi. · Polükristallid - polükristallilistes ainetes paiknevad kristallid suvaliselt. Tehnikas kasutatavad kristallid ja sulamid on harilikult polükristallilised, sest nende omadusi saab muuta mehaanilise ja termilise töötlemisega.
vihmapiisad- tekib pilvedes, kui õhuvoolud moodustavad tillukeste veepiiskade omavahelise põrkumise. Need piisakesed liituvad suuremateks piiskateks, mis langevad vihmana alla. Õhk peab olema niiske, et vesi jõuaks aurustumata maapinnale, nii et selline sademete teke on iseloomulik põhiliselt troopilistele aladele. Enamik vihmast tekib kõigepealt jääkristallidena kõrgel atmosfääris madala temperatuuriga pilvedes. Jääkristallid kasvavad suuremaks, kui vesi nende peal külmub. Kas kristallid jõuavad maapinnale vihma või lumena, sõltub kõrgusest, millel nad külmuvad minimaalsest kõrgusest, millel temperatuurid ja rõhk üldse põhjustavad vee külmumise. Kui külmumine toimub madalamal kui 300 meetrit maapinnast, siis pole jääkristallidel aega enne maapinnale jõudmist sulada, nii et nad langevad lumena. Soojemates tingimustes toimub külmumine kõrgemal ja kristallid muutuvad enne maapinnale jõudmist vihmaks.( Õpilase teadus entsüklopeedia, The Concise Science
Tallinna Ülikool Matemaatik ja Loodusteaduste Instituut Loodusteaduste osakond Optilised nähtused atmosfääris Referaat Tallinn 2013 Sisukord SISSEJUHATUS.........................................................................................................................3 MIRAAŽID.................................................................................................................................4 Alumine miraaž.......................................................................................................................4 Ülemine miraaž.......................................................................................................................4 HALOD.......................................................................................................................................6 22° ja 46° halod....................
Selgendavad katted . Kasutatakse neid, et vähendada valguse tagasi peegeldumist pindadelt. Fotoaparaadid, teleskoobid, optilised süsteemid. Newtoni rõngad. Valgus peegeldub klaasplaadi ja läätse vahelt. Difraktsioonvõre. Klaasplaadil olevate paralleelsete pilude süsteem. Holograafia, Esemetest ruumilise kujutise fotografeerimine. Valguse polarisatsioonElektrivälja tugevuse vektor võngub ühes kindlas tasandis. See tekitab teatud kristallid, mis lasevad läbi kindlas tasandis. Need on POLAROIDID. Rakendused:Polaroid päikeseprillid.3D kino Max Plancki hüpotees. Footoni energia arvutamine. 1902. Osakestena ehk footonitena käitub valguskiirgamisel ja neeldmisel. Muutuv elektriväli tekitab muutuva magnetvälja muutuv magnetväli tekitab muutuva elektrivälja. Elektromagnetlaine on muutuvate elektri ja magnetväljade levimine lainena. Eml koosneb kahest komponendist : elektriväljast ja magnetväljast.
olid kunagi ammu kõrgem rõhk ja mereäärsetel aladel, vulkaaniliselt temperatuur). nt. Eesti). aktiivsed). 4. Miks nimetatakse tardkivimeid ka kristalseteks kivimiteks? Iseloomusta. Tardkivimite puhul on mineraalid kogunenud kristallideks neid on kivimit vaadates isegi näha (nt. graniit). Roosaks graniidiks nimetatakse graniiti, milles on roosakad kristallid, roheliseks graniidiks, millel on rohekad kristallid. Kristallideks on kogunuenud graniidis minerallid, kuna magma jahtumine sügaval maakoores on toimunud väga aeglaselt. 5. Mis on kivistised? Kivistised ehk fossiilid on veekogu põhjas setetesse vajunud organismide jäänused, millest on tekkinud kivimid. Kunagi ookeanis elanud loomade lubikojad. Taimede jäänused. 6. Nimeta 4-5 võimalust, milleks kasutatakse kivimeid?
Katse 4. NaCl + AgNO3 – tekib valge sade NaCl + AgNO3 + küllastatud NaOH – sade lahustub Hõbekloriidi sade lahustub, kuna tekib ühend [AgCl2]-, mis lahustub paremini kui AgCl. Sademe tekke reaktsioonivõrrand: NaCl + AgNO3 → NaNO3 + AgCl Sademe lahustumise reaktsioonivõrrand: AgCl + NaCl → [AgCl2]- + Na+ Katse 5. a) Co(NO3)2∙H2O + atsetoon – lahus muutub roosaks ja põhjas on Co(NO3)2∙H2O kristallid. b) eelmine lahus + NaCl – soola lisamisel muutub lahus lillaks. Soola pinnal olev lahus hakkab aegamööda minema siniseks. Umbes 4 minuti pärast on soola kristallide ümber märgatav tumesinise lahuse kiht ja NaCl ise on helesinine. Sinine värv tuleb Cl- ja Co+ reaktsioonil tekkinud [CoCl4]2- ioonidest. c) Eelmist lahust loksutasin kuni NaCl kristallid olid enam-vähem lahustunud. Loksutamisel muutus terve lahus tumesiniseks, seda samuti [CoCl4]2- ioonide mõjul
Valkude sadestamine sooladega Neutraalsete soolade suured sisaldused valgu lahuses põhjustavad valkude denaturatsiooni ja lahusest väljasadenemist, mida mõjutavad valgu mitmesugused tegurid( nt hüdrofiilsus, laeng jne.). Töö käik: 1 ml munavalgu lahusele lisati võrde hulk küllastunud (NH4)2SO4 lahust ja jäeti umbes 5 minutiks seisma. Globuliinide sade, mis tekkis eraldati filtrimisel. Filtraadile lisati küllastumiseni kristalset (NH4)2SO4 kuni kristallid enam ei lahustu, moodustub albumiinide sade. Järeldus: Kuna valkude sadestamist sooladega mõjutavad erinevad tegurid sadestusid globuliinid poolküllastunud lahuses, albumiinid sama soola küllastunud lahuses. Valkude termiline denatureerimine ja lahustuvuse sõltuvus pH-st Kõik valgud denatureeruvad kõrgel temperatuuril ja vastav temperatuur oleneb valgu loomusest ja keskkonna koostisest. Tavaliselt kaasneb valgu väljasadestumine.
Metallide ja sulamite mikrostruktuur Õppejõud Üliõpilased: Tallinn 2009 Töö eesmärk 1.Tutvuda metallide ja metallisulamite mikrostruktuuridega,nende struktuurides esinevate faaside ja mehaaniliste segudega. 2.Tutvuda survetöötluse mõjuga metallide ja metallisulamite struktuurile. Töö selgitav osa 1.Puhtad metallid. Metalli struktuur on polükristalliline(joon.3.1 a),kusjuures üksikud kristallid on üksteise suhtes orienteeritud erinevalt(joon 3.1 b).Survetöötlemise tulemusena võivad kõik kristallid saada ühesuunalise orientatsiooni-tekstruktuur.(joon.3.1 c) Survetöötlemise mõju metalli struktuurile Metallide ja sulamite survetöötlus liigitatakse lähtuvalt rekristallisatsioonitemperatuurist.: -külm(surve)töötlus.(rekristallisatsiooni-ja toatemperatuuri vahel) -kuum(surve)töötlus(rekristallisatsioonitemp kõrgemalt temp.)
koosneb pisikestest veepiiskadest, mis on nii väikesed, et ei lange maa peale, vaid hõljuvad õhus. Kaste (tekib temperatuuri suurest kõikumisest suvel) tekib, kui veeaur koguneb tilkadena jahedatele esemetele. Tavaliselt tekib kaste öösel, kui maapind jahtub. Jahtub ka maapinna kohal olev õhk. Jahtuvast õhust hakkab eralduma veeaur. See koguneb tilkadena jahedatele esemetele. Lumi - Maapinnalt aurunud vesi tõuseb üles külmadesse õhukihtidesse. Veeaur koguneb jääkristallideks. Kristallid ühinevad omavahel, tekivad lumehelbed. Lumehelbed on rasked ja liuglevad alla. Rahe- ( külmunud veepiisad, mis ühinevad teiste veepiiskadega) Raheterad tekivad, kui pilve ülemises osas vesi külmub ja pilve alumises osas jälle ära sulab. Suure paksu pilve ülemises osas on külm. Seal tekivad lumehelbed. Lumehelbed langevad allapoole. Pilve alumises osas on soojem. Lumehelbed sulavad. Igast lumehelbest jääb järele veepiisk. Veepiisk liigub pilves jälle ülespoole ning külmub uuesti
(segamisel) ning kirjutada vastavad reaktsioonivõrrandid. Nikli ammiinkompleksis on nikli koordinatsiooniarv 6. Atsiidokompleksid 3.1 Katseklaasi valada ~0,5 mL 0,2 M NaCl lahust ning lisada 1 tilk AgNO lahust. Loksutada ja lisada ~3 mL küllastatud NaCl lahust. Miks lahustub tekkinud hõbekloriidi sade? Kirjeldada reaktsioonivõrranditega sademe teket ja lahustumist. 3.2 a) Kuiva katseklaasi panna mõned Co(NO3)2·6H2O kristallid ja valada peale 2 3 mL atsetooni. Kirjeldada, mis toimub. b) eelmisesse lahusesse lisada NaCl kristalle nii palju, et katseklaasi põhjas oleks 2 3 mm paksune kiht. Kirjeldada 3 5 min jooksul, mis toimub NaCl kristallide ümber ja miks. c) eelmist lahust loksutada kuni NaCl kristallid on lahustunud ja lisada lahusesse pesupudelist ettevaatlikult mööda seina cá 1 mL vett. Kirjeldada, mis toimub ja miks. 3
Sadestumist mõjutavad hüdrofiilsus/hüdrofoobsus, laeng, molekulmass jt omadused. Globuliinid sadestuvad (NH4)2SO4 poolküllastunud lahuses, albumiinid küllastunud lahuses. Töö käik: lisasin 2 ml munavalgu lahusele võrdse mahu (NH4)2SO4 küllastunud lahust, loksutasin, jätsin viieks minutiks seisma. Eraldasin tekkinud globuliinide sademe filtrimise teel. Filtraadile lisasin kristalset (NH4)2SO4 kuni kristallid enam ei lahustu. Jälgisin albumiinide sademe moodustumist. Võrdlemisel segus, et globuliitset sadet tekkis rohkem. Järeldus: lahus sisaldas globuliine ja albumiine, kuna mõlemad sadestusid lahusest välja. Rohkem tekkis globuliinset sadet, seega oli globuliinide sisaldus lahuses suurem kui albumiinide oma. 7. Valkude termiline denatureerimine ja lahustuvuse sõltuvus pH-st Kõik valgud denatureeruvad kõrgel temperatuuril, kuna ruumilist struktuuri fikseerivad nõrgad sidemed katkevad
denaturatsiooni ja lahusest väljasadenemist, mida mõjutavad valgu mitmesugused tegurid( nt hüdrofiilsus, laeng jne.). Töö käik: 2ml munavalgu lahusele lisame 2ml (NH4)2SO4 küllastunud lahust, loksutame ja jääme 5 minutiks seisma. Tekkis globuliinide sade. Filtreerime sade filterpaberiga. Saadud filtraadile lisame kristelset (NH4)2SO4 kuni kontsentratsiooni saavutamiseni. (lisame väikeste portsjonitena soola ja loksutame katseklaasi hoolikalt. Toimingut korrame seni, kuni soola kristallid enam ei lahustu maksimaalse kontsentratsioonini(küllastunud lahus). Moodustus albumiinide sade. Võrreldes juhtus, et globuliinide sade on rohkem, kui albumiinide sade. Järeldus: Kuna valkude sadestamist sooladega mõjutavad erinevad tegurid sadestusid globuliinid poolküllastunud lahuses, albumiinid sama soola küllastunud lahuses. 1.1.7 Valkude termiline denatureerimine ja lahustuvuse sõltuvus pH-st
Sarnaneb nõelateraapiaga. Värvi vannid Sellise vanni tegemise jaoks sobib värviline vanni sool või toiduvärv. Vesi peab olema soe või külm. Kuum vesi segab värvi neeldumist. Sooja spektrivärvi vanni tuleb võtta esimese päeva poolel ja külma teisel poolel. Värviliste klaasidega prillid Valguskiired, mis tungivad läbi värviliste klaaside mõjutavad aju kutsudes esile erinevaid reaktsioone organismis. Teraapia kristallide, väärtus ja lihtikivide abil. Nagu on teada koosnevad kristallid molekulidest. Kui kristall allutada soojuse ja rõhu mõjule, siis tekib elektrivõngete voog. Selle pärast on kristallid energia saatjad ja neelajad. Neil on võime taastada balanssi selles keha piirkonnas, mis on haige või disharmoonias. Kristallid ja kivid on võimelised mõjutama inimeste organismi ka oma värviga. Nagu on teada, kivi valib ise oma peremehe. Arvatakse, et kividel on mõju meie mõtetele. Näiteks, kui minna kristallide ja
teole (sisekõrvas), kus asuvad heliretseptorid muundavad helivõnked närviimpulssideks. Närviimpulsid liiguvad mööda kuulmisnärvi peaaju oimusagara kuulmiskeskusse, kus tekib kuulmisaisting. (9) Kuulmislävi, kurtus. Väikseim helitugevus, mida inimene kuuleb, on kuulmislävi. Kurtuseks nimetatakse kuulmise täielikku puudumist. (10) Kuidas aitav sisekõrv tasakaalu hoida? Kuidas inimene veel oma keha asendit tajub? Kotikestes on sültjas aine ja kristallid, mis liiguvad vastavalt pea liikumisele. Keha tavalises asendis ärritava kristallid oma survega kindlaid meelerakkude karvakesi. Seetõttu tajume oma keha asendit ka siis, kui me pead ei liiguta. Pea liigutamisel paiknevad kristallid ümber ning ärritavad teisi närvirakke, need annavad peaajule informatsiooni pea uuest asendist. Poolringkanalid milles on vedelik, asuvad kolmel tasapinnal, üksteise suhtes täisnurga all. Sellise kanalite paigutuse korral pole tähtis, mis