Karboksüülhapped Screen clipping taken: 4.03.2011 9:06 Sisaldavad karboksüülrühma HCOOH -metaanhape(sipelghape) CH3COOH - etaanhape CH3CH3COOH - propaanhape · Neil on kõik hapetele iseloomulikud omadused o Hapu o Söövitav o Annavad lahusesse H+ ioone o Lakmus ->punaseks; MO->punaseks o Reageerivad leelistega, metallidega, endast nõrgemate sooladega · Keemilised omadused: o Reageerimine metallidega(mida aktiivsem metall, seda paremini reageerib) o Reageerimine metallioksiididega (aluselised oksiidid) o Reageerimine alustega o Nõrgemate hapete sooladega(karbonaadid, sulfaadid) o Vesinikuga -> aldehüüd + H2O (redutseerumine) Füüsikalised omadused · Molekulid moodustavad tugevaid vesiniksidemeid · Suhteliselt kõrge sulmas ja keemistemperatuuriga · Lühikese süsinikuahelaga (mida lühem ahel, seda paremi...
Tantaal Tantaali avastajaks on Anders Ekeberg. Ta nimetas selle Tantalose järgi tantaaliks. Legend räägib, et Zeusi poeg, rikas Väike-Aasia kuningas Tantalos oli jumalatega heas läbisaamises ja tal lubati nendega istuda ka pidulauas. Seal varastas ta nektarit ja reetis inimestele jumalate saladusi. Veendumaks jumalate kõiketeadmises tegi ta pöörase kuriteo tappes oma poja ning valmistades temast jumalatele toitu. Karistuseks panid jumalad ta igaveseks janu, nälga ja hirmu tundma. Nii pidi ta tundma piinu, mis tuntuks saanud Tantalose piinadena. Ka Ekeberg olevat tundnud uue elemendi avastamisel lausa Tantalose piinu. Tantaal ei reageerinud hapete ega isegi kuningveega ning ületas püsivuselt isegi väärismetalle. Tantaal on suure tihedusega(16,6g/cm³) rasksulav(3014 Celsiuse kraadi) hõbehall metall. Tantaal on erakordselt püsiv ja vastupidav keemilistele mõjutustele. See lahustu üheski happes ega kuningvees. Reageerib ainult vesinikfluor...
Broom Broom on keemiliste elementide perioodilisussüsteemi VII rühma element, mittemetall: järjenumber 35, aatommass on 79,904. Füüsikalistest omadustest on puhas broom terava ärritava lõhna ja sööbiva toimega punakaspruun mürgine vedelik. Broom aurustub toatemperatuuril kiiresti. Broomiaurud on oranzpruuni värvusega, terava lõhnaga, mis tugevalt ärritavad limaskesta. Lõhna tõttu sai broom ka oma nimetuse kreekakeelsest sõnast bromos, mis tähendab hais, lehk, lehkav. Broomiaurude tühine hulk õhus põhjustab inimesel rasket mürgitust. Broom keeb temperatuuril 58 kraadi Celsiust ja külmub temperatuuril 7 kraadi Celsiust.Tihedus 3,1 g/cm3. Broom sarnaneb keemilistelt omadustelt klooriga. Ta on halogeen. Broom erineb aga kloorist aktiivsuse poolest. Broom on keemiliselt väga aktiivne mittemetall, ühineb kõigi metallide (v.a. plaatina) ja paljude mittemetal...
Mittemetallid on suure elektronegatiivsusega elemendid, mis keemilistes reaktsioonides peamiselt liidavad elektrone. Perioodilisustabelis asuvad nad peaalarühmades ülal paremal, k.a. vesinik, mis asub tavaliselt kõige esimese elemendina ülal vasakul. Mittemetallide hulka kuuluvad ka väärisgaasid, kuigi need ei liida elektrone, sest nende väline elektronkiht on maksimaalselt täitunud. Võrreldes metallidega on mittemetallid oma ehituselt ja omadustelt palju vähem sarnased. Halogeenid on aga omavahel tunduvalt sarnasemad, kui teiste rühmade mittemetallid. Keemilistes reaktsioonides moodustavad nad teiste mittemetallidega tavaliselt kovalentse sideme, metallidega tavaliselt ioonilise sideme. Mittemetallide lihtainete omadused: · Ei juhi elektrit ning juhivad halvasti soojust · Neil puudub metalli iseloomulik läige · Esinevad nii gaasi (vesinik, fluor, hapnik, lämmastik, kloor, väärisgaasid), vedeliku (broom), kui ka tah...
METALLID ÜLDINE ISELOOMUSTUS ·Välisel elektronkihil on enamasti vähe elektrone(1-3) ·Metalliaatomite raadius suht suur. ·Aatomid hoiavad väliskihi elektrone nõrgalt kinni, seega on neil väike elektronegatiivsus. ·Ühendites alati pos. o.a FÜÜSIKALISED OMADUSED ·Elektrijuh., soojusjuh., plastilisus, metalne läige(peegeldusvõime). ·Metallid erinevad teineteisest: 1)tihedus(kerg-, raskemetallid):Li 0,5g/cm3 ; Os 22,6g/cm3 2)Sulamistemp.(kerg-, rasksulavad):Hg -39°C, W 3400°; 3)Kõvadus(kõvad Cr, pehmed leelismet.) 4)Värvus(kollane Au, punane Cu, teised valged,hallid) 5)Magnetiseerivus(Fe,Co,Ni) KEEMILISED OMADUSED ·Metallid on reaktsioonides alati redutseerijad(loovutavad elektrone) ·Reag. veega a)aktiivsed met.(K-Mg) reag. vedela veega; tekivad hüdroksiid ja H2 ( 2Na+2H2O®2NaOH + H2 ) b)keskm aktiivsed met.(Al-Fe) reag. auruga kõrgel temp; tekivad oksiidid ja H2 ( Zn+H2O®ZnO+H2 ) c)väh. akktiivsed met.(Ni-Au) ei reagereeri veega ·Reag. l...
Metallidel on kristalne struktuur.Erinevatel metallidel on erinev krisatllkuju. Metallidel on metalne läige. Metallide värvus. Enamik metalle on hõbevalged, vask on roosakaspunane, kuld on kollane.Mitmetel hõbevalgetel on iseloomulik helk.Nikkel helgib kollalkalt, kroom sinakalt. Metallide kõvasus. Mineraalide, metallide jt materjalide suhtelist kõvadust võrreldakse Moshi kõvadusastmikust.Kõige kõvem metall on kroom..Argielus ettetulevatest metallidest on kõige pehmem elavhõbe , väga pehme plii, kuld. Metallid on plastilised. Plastilisuse tõttu saab metalli valtsida õhukeseks leheks või tõmmata traadiks ja sepistada. Mõned metallid(antimon, mangaan) on haprad, sepistamisel purunevad nad kildudeks nagu klaas. Metallidon head soojus- ja elektrijuhid.Kõige paremad elektrijuhid on hõbe ja vask. Tehnikas rakendadtakse elektrijuhtidena ja elektrijuhtmete valmistamisel alumiiniumit ja vaske . Reeglina on head soojusjuhid ka head lektrijuhid. M...
FÜÜSIKALISED OMADUSED: *O2 väiksema aktiivsusega kui O3, sest O3 *Aatomiraadius metallide omadest laguneb: O2-ks ja O3-ks. väiksem,seetõttu hoiavad mitte-met. Elektrone *Tekib monohapnik, kõige aktiivsem.sa tugevamini kinni. *Hapnik reageerib liht-ja liit ainetega ja *Mit.metallid+ metall/vesinik = oksüdeerija. saaduseks on vastavate elementide oksiid. *Mitte-met. On molekulaarsed või aatomvõrega. 4FeS2+ 11O2=2Fe2O3 + 8SO2 *Mitte-met. Pole plastilised ja head elektri juhid. *Hapniku saamine: (v.a grafiit) *Mitte-met. Suurenevad V-lt , P-le 2HgO(temp)=2Hg+O2 Ja rühmas ülevalt alla. 2KNO3(temp)=2KNO3+O2 *Tahked: N2,O2,P,Br2,Cl2, Ar,Nl,He,F2. *Tööstuslikult: Vedela õhu traktrioneeriva KEEMILISED OMADUSED: destillatsioonil. Väärisgaasid reageeriv...
Alkeenid -Küllastumata CH'd, mol 1 kaksikside ja teised üksiksidemed. (1sigma ja 1 side) CnH2n CH2=CH-CH2-CH3 but-1-een Need on kaks 2 buteeni isomeeri( ained, millel on CH3-CH=CH-CH3 but-2-een ühesugune koostis, aga erinev ehitus.) 3. isomeer on tsüklobutaan Omadused: Eteen on värvusetu, vees lahustumatu, nark. toimega gaas. *Looduses esineb vähe, saadakse nafta töötl. *Lihtsaim ja keem.töö. toorainena enim kasutatav alkeen (CH). 1. Põleb - CO2 + H2O (redutseerija) 2. Liitumisreakts. -side katkeb ja liitumise tulemusena tekkib vastav küllast. ühend. a) Liitumine H2-ga CH2=CH2 - CH3-CH3 b) liitumine HG-dega CH2=CH2 + Br2 - CH2Br-CH2Br (1,2 di-bromoetaan) c) H HG-dega CH2=CH2 + HCl - CH2Cl -CH3 d) H2O-ga (OH rühm) CH2=CH2 + H2O - CH3 -CH2(OH) 3. Polümeriseerub(ühe sama või erinevate ainete palju X liitumine, mille tulemusena tek-pmeer) ! n- näitab lülide arv...
Alkaanide füüsikalised Omadused: *Metaani ja temaga sarnaste süsivesinike - alkaanide omadused muutuvad korrapäraselt süsiniku aatomite arvu suurenemisega molekulis *Metaan ja temale järgnevad alkaanid erinevad üksteisest aatomite rühma - CH 2 - võrra. Niisugust ühendite rida nimetatakse homoloogiliseks reaks. Rea üldvalem on CnH2n + 2. *Metaani homoloogilise rea 4 esimest ühendit on gaasid, viiendast kuni kuueteistkümnendani vedelikud ja kõrgemad on tahked ained. Molekulmassi kasvuga homoloogilises reas suureneb alkaanide tihedus ning kasvab sulamis- ja keemistemperatuur. *Alkaanid on vees peaaegu lahustumatud. Nad on hüdrofoobsed ehk vett-tõrjuvad *Homoloogilises reas muutuvad homoloogilise rea liikmete - homoloogide - füüsikalised omadused korrapäraselt. *alkaanide keemistemperatuur sõltub molekulmassist ehk süsinikahela Pikkusest-molekulmassi suurenemisega kasvab homoloogide tihedus, sulamis- ja keemistemperatuur ning agregaatolek ...
MITTEMETALLID Mittemetallideks loetakse elemente, mille välisel elektronkihil on neli kuni 8 elektroni ning mis reageerimisel metallidega käituvad redutseerijatena. Mittemetalli raadiused on väiksemad, kui metallidel ja nad hoiavad elektrone tugevamini kinni ehk nende elektronegatiivsused on suuremad. Üldised füüsikalised omadused: · halvad elektrijuhid (va. süsinik grafiidina) · toatemperatuuril valdavalt kas tahked või gaasilised (8A ehk vääris- inertgaasid 7A vesinik, kloor, fluor, 6A hapnik, 5A lämmastik) ainuke vedelmetall on broom, ülejäänud on tahked. · tihti molekulaarsed, kahe aatomolisi molekule moodustavad N, O, 7Arühm. · molekulaarsed on ka tahkena väävel ja fosfor, ülejäänud koosnevad ainult aatomitest (atomaarsed) · mittemetallid on reeglina halvad soojusjuhid va. teemant · kõik on tahkena rabedad · on kas molekul või aatomvõre Üldised keemilised omadused: kõi...
INDIUM Tartu 2008 Indium on keemiliste elementide perioodilisussüsteemi IIIA rühma element ning asub 5 perioodis. Järjenumber on 49, aatommass 114,82. Indiumis on 49 prootonit ja elektroni ning 66 neutronit. Indium on hõbevalge kergsulav pehme metall, st° 156,78 °C, kt° 2024 °C, tihedus 7,31 Mg/m3 . Keemilistelt omadustelt sarnaneb indium alumiiniumiga. Oksüdatsiooniaste ühendeis enamasti III, harvemini I või II. Looduses leidub indiumi hajusalt. Peamiselt lisandina tsingimaakides. Teda tarvitatakse aktseptorlisandi ja joodisena pooljuhtide tehnikas ning hermetiseeriva ja korrosioonikindla materjalina aparaaditööstuses. 1863. a. püüdis Freibergi Mäeakadeemia inspektor Ferdinand Reich avastada Saksamaa metallimaakidest talliumi, Et Reich oli värvipime, siis tegi spektraalanalüüsi tema assistent Hieronymos Theodor Richter, kes pidi otsima maakidest TI rohelise spektrijooni. Ootamatult avastas ta tsingima...
Liitium Üldine/aatomi ehitus Lühend: Li Elektronskeem: + 3| 2)1) Aatominumber: 3 Elektronide arv: 3 Aatommass: 6,941 Prootonite arv: 3 Kuuluvus: leelismetallid Neutronide arv: 4 Füüsikalised omadused Liitium see hõbevalge/hallika värvusega suhteliselt pehme leelismetall on kõige väiksema tihedusega metall üldse. Tema tihedus on 0,535 g/cm³, mis teeb liitiumist ka kõige väiksema tihedusega normaaltingimusel tahke aine. Olles erakordselt kerge metall on ta viis korda kergem kui alumiinium ning kaks korda kergem kui vesi. Sellepärast on liitium võimeline ujuma isegi petrooleumis. Tema sulamistemperatuur on 180,54 °C ning keemistemperatuur 1342 °C. Agregaatolek tavatingimustel on tahke. Võrreldes teiste leelismetallidega on liitium väiksema tihedusega ning kõrgema s...
CnH2·+1OH . Metanool(puupiiritus)- CH3OH üks lahustite koostisosi keemiatööstuses, etanoolist välimuselt eristamatu. Etanool (piiritus)C 2H5OH tähtis lahusti ja sünteeside lähteaine, valm eteeni katalüütilisel hüdraatimisel või sahhariidide kääritamisel. Glütseriin- Magus, viskoosne vedelik, seguneb hästi veega, pole mürgine, keemiliselt seotuna kuulub rasvade koostisse, kosmeetikas nahapehmendajana. Puskariõli on destillatsioonijääk etanooli eraldamisel käärimissegust, koosneb kahest pentanooli isomeerist. Põlemine- C2H5OH + 3O2 = 2CO2 + 3H2O. Oksüdeerumine(tekib aldehüüd: CHO)- 2C2H5OH + O2 = 2CH3CHO + 2H2O. Reag. Leelismetallidega(tekivad alkoholaadid)- 2C2H5OH + 2Na = 2C2H5ONa + H2. Alkoholaatide hüdrolüüs- C2H5ONa + H2O = C2H5OH + NaOH. Füüsilised omadused: Lihtsamad suht kõrgete keemistº ja vees hästi lahustuvad, molekulmassi kasvuga ...
VÄÄVEL 1)Leidumine looduses: nii ehedalt kui ka ühenditena (püriit, vaskläik) 2)Füüsikalised omadused: a) kollase värvusega b) tahke c) rabe d) vees ei lahustu e) halb soojus-ja elektrijuht. 3.Väävli allotroopsed teisendid: a) rombiline väävel: on looduslik ja püsiv vorm b) monokliinne väävel : Väävel sulatatakse ja jahutatakse aeglaselt. Tekivad nõeljad väävli kristallid. c) plastiline väävel: väävel sulatatakse ja jahutatakse kiiresti. Tekib pruun veniv mass. 4.Keemilised omadused: On aktiivne mittemetall. a) vesiniku ja metallidega käitub oksüdeerijana H2 + S = H2S Ca + S = CaS b) reaktsioonil hapnikuga käitub redutseerijana S +O2 = SO2 5. Kasutamine: tuletikutööstus, meditsiinis (salvid), musta püssirohu koostises, väävelhappe tootmiseks. ...
docstxt/132915447431159.txt
KT 7 1. Karboksüülhapped on orgaanilises keemias nõrgad happed, mis sisaldavad karboksüülrühma (COOH). Rasvhapped on looduslike rasvade koostises olevad monohapped, milles on üle kümne paarisarv süsiniku aatomi. Rasvhapped võivad olla küllastunud või küllastumata. Asendatud karboksüülhapped e. hüdroksühapped on puuviljades ja teistes looduslikes allikates esinevad orgaanilised karboksüülhapped. Aminohapped e. aminokarboksüülhapped on keemilised ühendid, mis sisaldavad funktsionaalsete rühmadena nii aminorühmi kui ka karboksüülrühmi. Aminohapped on karboksüülhapped, mille alküülradikaalis on üks või mitu vesiniku aatomit asendunud aminorühmaga. Kodeeritavad aminohapped on eluks vajalikud 20 aminohapet, millest loodus on ehitanud valgud. Asendamatud aminohapped on aminohapped, mida inimese organism ise kas üldse ei tooda või toodab vähesel määral, nii e...
Alumiinium Hanna Vahter 9.klass Muhu Põhikool Al ajaloolist, põnevat Avastas saksa keemik F. Wöhler 1827 a. Algselt oli Al väga kallis On mürgine Süüdistatakse Alzheimeri ja Parkinsoni tõve tekitamises Al leidumine looduses (lihtaine, ühendid) Ei leidu lihtainena Maakoores levikult metallilistest elementidest esimesel kohal (~8%) Esineb ühendite koostises - tähtsaim Al tooraine on mineraal boksiit Esineb veel poolvääriskividena - rubiini ja safiirina Al füüsikalised omadused Hõbevalge läikiv metall Kuulub kergmetallide hulka - tihedus on 2,7g/cm3 Sulamistemperatuur on 660 °C Keemistemperatuur on 2519 °C Aatommass on 26,98154 Hea elektrijuht Al keemilised omadused Kuulub aktiivsete metallide hulka Õhus olles püsib toatemperatuuril muutumatuna Reageerib hapetega ja leelistega (amfoteersus) Reageerib hapnikuga, halogeenidega, väävliga jt mittemetalli...
Väävel-kokkuvõte Väävel on mittemetalliline keemiline element järjenumbriga 16. VI A rühmas ehk kalkogeenid. Väävli stabiilsemad oksüdatsiooniastmed on −2, 0, 4 ja 6. Oksüdeerivas keskkonnas valdab oksüdatsiooniaste 6; redutseerivas keskkonnas on oksüdatsiooniastmed −2, 0 ja 4 võrreldava stabiilsusega ja lähevad kergesti üksteiseks üle. Aatomi väliskihil on 6 elektroni.Võib siduda kuni 2 elektroni saades miinimum oksüdatsiooni astmeks -II.Võib loovutada 6 elektroni saades maksimum oks.astmeks VI. Elektronskeem S:+16|2)8)6) Keemilised omadused Oksüdeerija Madalaima oks.astmega ühendid ei saa olla oksüdeerijad.kui oks.aste on 0,siis oksüdeerib metalle ja vesinikku.kui oks.aste on kõrgeim ehk VI,siis ta on tugev oksüdeerija. Süütab näiteks puupilpa C0 + 2 SVIO3 = CIVO2 + 2SIVO2 Redutseerija Oks.aste on -II siis ta põleb ja on redutseerija.oks.aste on 0 ,siis väävel põ...
Rakvere kool 9. klass Alumiinium Referaat Koostaja: Mihkel Juhendaja: õpetaja Õppeaasta 2004/2005 Avastamise lugu 1808. a. kinnitas Sir Humphry Davy alumiiniumi olemasolu ja nimetas selle. Algul eraldati metalli keemilisest ühendist halli pulbrina, mis peenestamisel omandas metallilise läike. Katsed saada metalli kangina või suurte teradena jäid tulemusteta. Enne kui neid katseid kroonis 1845.a. edu, kulus 18 aastat püsivaid otsinguid. Väliselt oli ta sarnane hõbedaga, kuid erinevalt viimasest erakordselt kerge, 4 korda kergem hõbedast, 3,5 korda kergem vasest ja peaaegu 5 korda kergem rauast. Kuna uue metalli saamise lähtaineks olid ammu tuntud maarjased (ladina keeles alumen ), siis hakati ka metalli nimetama alumiiniumiks. Alumiinium Alumiinium on tänapäeval üks tuntumaid ja enamkasutatavaid metalle(tähtsuselt teisel kohal raua järel...
Lämmastikhape Lämmastikhape Keemiline valem : HNO3 Lämmastikhape on söövitav värvuseta teravalõhnaline vedelik ning mürgine hape, mis võib põhjustada tõsiseid põletushaavu. Laialt levinud hapetest üks tugevamaid happeid. Iseloomulik terav lämmatav lõhn, mis pisut meenutab kloori lõhna. Füüsikalised omadused 99-protsendilise lämmastikhappe: Tihedus on umbes 1,52 g/cm³ Sulamistemperatuur on umbes -41,7 °C Keemistemperatuur on umbes 84 °C (lämmastikhape lagunemisel eraldub lämmastikdioksiid) Värvus- lämmastikhape ise on värvuseta, on tal enamasti punakaspruunikas või kollakas varjund, sest lagunemisel eraldub temast lämmastikdioksiidi, mis temas lahustub ja annab lahusele värvi. Lämmastikhappe aurud on õhust 3,2 korda raskemad. Keemilised omadused Lämmastikhapet võib vaadelda koosnevana lämmastikpentoksiidist (N2O5) ja veest (H2O). Lämmastikhape ei ole keemiliselt eriti stabiilne ja laguneb ka va...
Sten-Erik Ellermaa KOOBALT Referaat Õppeaines: ANORGAANILINE JA ANALÜÜTILINE KEEMIA Ringmajanduse ja tehnoloogia instituut Õpperühm: KT11/21 Juhendaja: Professor Viiu Sillaste Esitamiskuupäev:................ Üliõpilase allkiri:................. Õppejõu allkiri: .................. Tallinn 2018 SISUKORD 1.Sissejuhatus..............................................................................................................................3 2.Leidumine looduses.................................................................................................................4 3.Omadused..................................................................................................................
Tabasalu Ühisgümnaasium Etanool referaat Koostaja: Enelyn Vilk Juhendaja: Evelin Maalmeister Tabasalu, 2014 1. Saamine/ Leidumine 1.1 Saamine 1.2 Leidumine 2. Omadused 2.1 Füüsikalised omadused 2.2 Keemilised omadused 3. Kasutamine 4. Toime inimorganismile 5. Huvitavaid fakte 1.1 Saamine 1) Viinamarjade, puuviljade ja teiste suhkruid sisaldavate lahuste või tärklist sisaldavate produktide kääritamisel. Käärimisprotsess toimub pärmseente mõjul, mida leidub alati õhus, puuviljades, marjades, pinnases, vees, mistõttu on suhkruid sisaldavate vedelike alkoholkäärimine looduses väga levinud. Pärmseente elutegevuse mõjul toimub glükoosi muundumine etanooliks ja süsinikdioksiidiks. C6H12O6 2CH3CH2OH + 2CO2 Pärmseente mõjul käärib ka piimas olev ...
SISUKORD 2 SISUKORD..........................................................................................................................................2 SISSEJUHATUS..................................................................................................................................4 1.KULLALE ISELOOMULIKUD OMADUSED...............................................................................5 1.1. Füüsikalised omadused..............................................................................................................5 1.2.Keemilised omadused.................................................................................................................5 1.3.Kulla elektronskeem ja elektronvalem.......................................................................................6 1.4.Võimalikud oksüdatsiooniastmed..................................................................
Mittemetallid - erineva värvusega,tahkes või gaasilises olekus(-Br),juhivad soojust ja elektrit halvasti.Tahkes olekus olevad metallid on: aatomvõrega-teemant,räni,süsiniku-,räni- ja broomi ühendid;kõvad;vees mittelahustuvad;kõrge sulamis- ja keemistemp. Molekulvõrega-gaasid,väävel,fosfor;haprad;vees vähelahustuvad;madal sulamistemp. Paljud esinevad mitme allotroobina. Allotroopia on nähtus, kus üks ja sama keemiline element esineb mitme erineva lihtainena. Kõige levinum element:MAAL-hapnik,räni; KOSMOS-vesinik,heelium;ELUSORGANISMIS- süsinik,vesinik ja hapnik. Keemilised omadused:reaktsioonil metallidega käituvad oksüdeerijana_ O2+Ca=2CaO; S+Ca=2CaS.Reaktsioonil mittemetallidega võivad käituda nii oksüdeerijana kui ka redutseerijana (oleneb mittemetalli aktiivsusest) H2+S=H2S;S+O2=SO2 Vesinik-sobib kokku IA-rühmaga: üks elektron väliskihil, mille annavad elektroni ära; ei sobi IA-rühma-mittemetall ja teised metallid,vesinik gaas teised...
Materjalide füüsikalised, keemilised ja tehnoloogilised omadused Füüsikalised ja keemilised omadused Metalli füüsikalised omadused. · Värvuseks nimetatakse metalli võimet peegeldada kindla lainepikkusega valguskiirgust. · Tiheduseks nimetatakse metalli ühe mahuühiku massi. Tiheduse järgi jaotatakse metallid kerg- (kuni 4500 kg/m³) ja raskmetallideks. Nii näiteks käsutatakse lennuki- ja raketiehituses kergmetalle ja sulameid (alumiiniumi-, magneesiumi-, titaanisulamid). · Sulamistemperatuuriks nimetatakse temperatuuri, mille juures metall sulab. Selle järgi jaotatakse metallid rasksulavaiks (volfram 3416°C, titaan 1725°C jt.) ja kergsulavaiks (tina 232°C, tsink 419,5°C). Sulamistemperatuuril on suur tähtsus metalli valamisel, keevitamisel ja jootmisel. · Soojusjuhtivuseks nimetatakse metalli võimet soojust üle anda kõrgema temperatuuriga piirkonnalt madalama temperatuuriga piirkonnale. Head soojusjuhid on hõbe, vaskja alumiin...
Maikel Jätsa Raud Referaat Õpperühm: TÖ11 Juhendaja: V. Sillaste Tallinn 2011 Ferrum Raud asub perioodilisusüteemis VIII B rühmas ja neljandas reas. Aatommass on 55,847amü, raua aatomi tuumas on 26 prootonit, ja 56-26=30 neutronit,elektronide koguarv elektronkattes on võrdne prootonite arvuga ehk 26. Raud on neljanda perioodi element, järelikult asuvad tema elektronkatte 26 elektroni neljal elektronkihil Fe : +26/2)8)14)2) väliskihil asub 2 elektroni. Eleketronvalem: 1s22s22p63s23p64s23d6. Raual on muutuv oksüdatsiooniaste, II ja III. Raua massisisaldus maakoores on 6%,. Suurimad rauamaagivarud asuvad venemaal Kurskis magneetilise anomaalia piirkonnas. Tähtsamad ühendid: · Raudvitriol(FeSO4 x 7 H2O) on kristalliline raudsulfaat, mis on helerohelise värvusega suhteliselt püsiv ühend. Vaid vesilahuses oksüdeerub aeglaselt õhuhapniku toimel.Teda saadakse enam...
Gümnaasium GERMAANIUM Koostaja - Juhendaja - 2014 SISUKORD SISSEJUHATUS..................................................................................................................................3 FÜÜSIKALISED OMADUSED..........................................................................................................4 KEEMILISED OMADUSED..............................................................................................................5 ÜHENDID JA NENDE KASUTAMINE. ELEMENDI KASUTUSALAD........................................6 BIOTOIME...........................................................................................................................................7 HUVITAVAT!.......................................................................................................................................8 MIDA ANDIS MULLE REFERAADI TEGEMINE? ...........
SÜSIVESINIKUD Ained, mis koosnevad vaid süsinikust ja vesinikust. Süsivesinikud võivad moodustada alates 3ndast süsinikust isomeere. Isomeerid on ained, mille summaarne valem on sarnane, kuid struktuur on erinev C4H10 butaan CCCC 2metüülpropaan CCC C Süsivesinikud on võimelised moodustama ka homoloogilisi ridu. Homoloog aine, mille struktuur ja keemilised omadused on sarnased. Iga järgnev homoloog erineb eelmisest CH2 rühma võrra. 1. met 2. et 3. prop 4. but 5. pent 6. heks 7. hept 8. okt 9. non 10. dek Alkaanid CnH2n+2 Alkeenid CnH2n Alküünid CnH2n2 ALKAANID Alkaanid CnH2n+2 Alkaanid on küllastunud süsivesinikud, kus molekuli koostises süsinike vahel esinevad ainult ühekordsed kovalentsed sidemed. Nimetuse lõpp: aan Nt. Butaan C4H10 Metaan CH4 summaa...
Sisukord Sisukord...................................................................................................................................... 2 Sissejuhatus.................................................................................................................................3 Saamismeetodid.......................................................................................................................... 4 Füüsikalised omadused............................................................................................................... 5 Keemilised omadused................................................................................................................. 6 Kasutusalad.................................................................................................................................9 Ohutusnõuded............................
Raud Raud (ferrum) on keemiline element järjenumbriga 26. Raud asub perioodilisussüsteemi VIII B rühmas ja 4. perioodis. Tal on neli stabiilset isotoopi massiarvudega 54,56,57 ja 58. Omaduselt on raud metall. Raud on kõige levinum element Maa koostises ning levimuselt maakoores metallidest alumiiniumi järel teisel kohal. Raua füüsikalised omadused Raud on hõbevalge keskmise kõvadusega metall. Lisandid muudavad raua kõvemaks. Raua tihedus on 7874kg/m3 Raua sulamistemperatuu on 1535 kraadi. Raud muutub kuumutamisel palstiliseks, milletõttu seda on võimalik sepitseda ja valtsida. Ta on hea soojus- ja elektrijuht. Raud on magnetiseeritav. Raua keemilised omadused Raud on keemiliselt keskmise aktiivsusega metall. Raua kristallvõre muutub erinevatel tempareatuuridel. Kuivas õhus ta hapnikuga ei reageeri, kuid niiskuses kattub kergesti roostekihiga. Seejuures muudab ta oma värvi oraanzikas-pruun...
VESINIK ÜLDINE · Aatomiehituselt kõige lihtsam element. · Aatomi elektronkattes ainult 1 elekron. · Võimalikud oksüdatsiooniastmed ühendites on I ja l. · Erinevalt teistest puudub tal vesinikioonil elektronkate. · Vesinikioon on ainult aatomituum e. Prooton. · Positiivse osalaenguga vesiniku aatomid saavad moodustada elektronegatiivse elementide aatomitega ka täiendava sideme vesiniksideme. LIHTAINE · Koosneb H2 molekulidest, allotroope ta ei moodusta. · Tavatingimustes värvitu ja lõhnatu gaas. · Kõige madalama sulamis- ja keemistemperatuuriga. · Vesiniku molekulid on erakordselt väikesed ja mittepolaarsed. · Lahustub vees väga vähe. · Füüsikalised jõud nõrgad. · Tihedus on väiksem kui heeliumil. LEVIK LOODUSES · Vesinik on üks levinumaid mittemetallilisi elemente maakoores. · Maailmaruumis on vesinik aga kõige levinum keemiline element. · Moodustab põhiosa Päikese massist. · Looduses lihtainena vesinikk...
Süsinik Süsiniku ehitus, allotroopia Süsinik on mittemetalliline keemiline element järjenumbriga 6, asub perioodilisustabeli IV A rühmas. Süsiniku valentskihis on 4 elektroni ja tema elektronkate on kirjeldatav valemiga 1s2 2s2 2p2. Süsinikul on kalduvus moodustada 4 sidet või vastaval arvul mitmekordseid sidemeid. Et süsinik moodustab palju vähepolaarseid kovalentseid sidemeid, on oksüdatsiooniastme määramine Süsiniku 8 allotroopi: a) teemant, b) grafiit, c) sageli ...
Raud ehk Fe Aatomi ehitus: 26 Fe: 1s22s22p63s23p64s23d6 Fe oksuüdatsiooniaste ühendites on: II sel juhul loovutab raua aatom 2 elektroni väliskohi s-orbitaailt III-sel juhul loovutab raua aatom 2 elektroni väliskihi s-orbitaalilt ja 1 elektori 3d- orbitaalit Raua püsivam oksüdatsiooniaste on III, ebapüsivam II Levik looduses Kõigist melementidest on Fe levikult 4. Kohal, metallidest aga 2. Kohal Puhast (ehedat) rauda leidub looduses väga harva. Fe-aatom kuulub hemoglobiini koostisse. Hemoglobiin on valk, mis transpordib vere punalibledes hapnikku ja süsihappegaasi. Raua ühendid Fe2O3 raud(III)oksiid, pruun või punane rauamaak e. Hematiit. Hematiiti kasutatakse raua tootmiseks. Punase värvusega raud(III)oksiidi rauamennikut kasutataksekeedu- ehk rootsi värvides pigmendina (värvimullana). ...
Vill ja villane lõng Villa keemilised omadused Villa orgaanilise aine keemiline koostis sarnaneb naha ja lihaskoega. Villas leidub väga mitmesuguste omadustega valke keratiine, kollageeni, nukleiin ja aminohappeid. Villas on lipiide rasva ja rasvataoliste ainete steroole (kolesterooli, lanosteriooli), glükogeeni ehk loomset tärklist ning mitmesuguseid ainevahetusprodukte, nagu kusihapet, puriini, kabamiidi jt. Villa orgaaniline aine sisaldab süsinikku, hapnikku, lämmastikku, vesinikku, väävllit. Villa kuivaine sisaldab tuhka, mis sisaldab rohkesti kaltsiumi, seejärel naatriumi, magneesiumi, fosforit, tsinki, rauda, kaaliumi, mangaani, vaske. Villa keratiinide sünteesil on olulised tsink ja vask. Villa orgaanilise aine iseloomulikuks tunnuseks on fibrillaarsete valkude, eriti keratiinide kõrge sisaldus, milles leidub rohkesti väävlit sisaldavaid aminohappeid (tsüstiini, tsüsteiini jt). Väävlisisalduse järgi võib otsus...
Keemia (Amiinid,Aminohapped,Valgud) Amiinid Mõiste Amiinid kuuluvad lämmastiku sisaldavate orgaaniliste ainete hulka. Amiinis on funktsionaalseks rühmaks aminorühm NH2. Amiine leidub looduses. Nad tekivad nii loomsete kui ka taimsete organismide ainevahetus protsessides. Enamike amiine lõhnab ebameeldivalt, ka laibalõhna põhjuseks on valkude lagunemisel tekkivad amiinid. Fenoolidega sarnased ühendid on aromaatsed amiidid. Kui fefenoolid olid happeliste omadustega siis, aminorühma H2 olemasolust tingituna aluselised omadused. Molekuli ehitus. Tähtsaim aromaatne amiin on fenüülamiin ehk aniliin benseeni tuumas on asendatud üks vesinikuaatom aminorühmaga. Füüsikalised omadused Aniliin on värvitu, vees praktiliselt lahustumatu, õli taoline vedelik. Lahustub hästi orgaanilistes lahustites (etanool, eeter, benseen jne). Õhus oleva hapniku toimel oksüdeerub ta kergesti j...
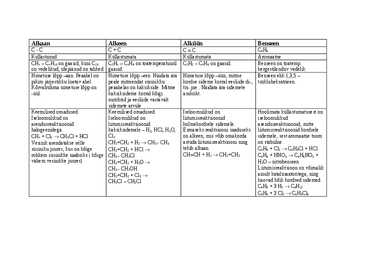
Alkaan Alkeen Alküün Benseen C-C C=C CC C6H6 Küllastunud Küllastumata Küllastumata Aromaatne CH4 C4H10 on gaasid, kuni C10 C2H4 C4H8 on toatemperatuuril C2H2 C4H6 on gaasid. Benseen on toatemp. on vedelikud, ülejäänud on tahked gaasid. kergestilenduv vedelik Nimetuse lõpp aan. Peaahel on Nimetuse lõpp een. Näidata ära Nimetuse lõpp üün, mitme Benseen ehk 1,3,5 pikim järjestikku loetav ahel. peale mitmendat süsinikku kordse sideme korral eesliide di-, tsükloheksatrieen. Kõrvalrühma nimetuse lõpp on peaahelas on kaksikside. Mitme tri- jne.. Näidata ära sidemete -üül. ...
METALLID ÕPPEMATERJAL 9. KLASSILE KOOSTAJA: KÜLLI PÄRTELSON © Külli Pärtelson, 2001 SISUKORD 1. METALLID ARGIELUS 2. ÜLDOMADUSED 3. AATOMI EHITUSE ERIPÄRA 4. KEEMILISED OMADUSED 5. KOKKUVÕTE I. METALLID ARGIELUS IGAPÄEVAELUS HEADE OMADUSTE ASENDAMATU TÕTTU MATERJAL KASUTATAKSE VÄGA LAIALDASELT SUHTELISELT HÄSTI TOODETAKSE JUBA TÖÖDELDAVAD 6000 - 7000 AASTAT ALUMIINIUM KÖÖGINÕUD, KONSERVIKARBID ELEKTRIJUHTMED PEEGLID VÄRVID AUTO- JA LENNUKI OSAD RAUD TÖÖRIISTAD KÖÖGINÕUD EHITUSMATERJALID (TRAAT, TORUD,VEDRUD JMS) MAGNETID VASK ELEKTRIJUHTMED EHTED, MÄRGID PEENRAHA TÖÖRIISTAD HÕBE KULD EHTED NÕU...
TALLINNA TEHNIKAÜLIKOOL Ärikorralduse instituut Töökeskkonna ja -ohutuse õppetool JOODI RISKIANALÜÜS Referaat Koostajad: Juhendaja: Tallinn 2009 1 SISUKORD SISUKORD.................................................................................................................................2 1.Sissejuhatus..............................................................................................................................3 2.Füüsikalis- keemilised omadused............................................................................................ 4 3.Kineetika ja metabolism...........................................................................................................5 4.Käitumine looduses........................................................................................
ALKÜÜNID Küllastumata süsivesinikud, kus süsinike vahel esineb kovalentne kolmikside. Nimetuse lõpp üün Üldvalem CnH2n2 Füüsikalised omadused sarnased alkeenidele. Füüsikalised omadused Homoloogilise rea 3 esimest liiget on gaasid(C 2C4), järgmised vedelikud(C5C17), alates 18ndast süsinikust on alkeenid tahked Süsiniku arvu kasvuga suureneb keemistemperatuur ja väheneb sulamistemperatuur. Sama süsinikuarvuga alkeenidel on võrreldes alkaanidega madalamad sulamis ja keemisto Hüdrofoobsed ained ja seetõttu ei lahustu vees Alkeenid on lõhnavad ühendid, narkootilise toimega Keemilised omadused Hüdrogeenimine CH#CH + H2 CH2=CH2 Halogeenimine CH#CCH3 + Br2 CHBr=CBrCH3 prop1üün reag. Broomiga Hüdraatimine tekib aldehüüd CH#CH + H2O CH3CHO (etanaal) Reageeri...
METALLID Metallid on : Berüllium, Magneesium, Alumiinium, Skandium, Titaan, Vanaadium, Kroom, Mangaan, Raud, Koobalt, Nikkel, Vask, Tsink, Gallium, Ütrium, Tsirkoonium, Nioobium, Molübdeen, Tehneetsium, Ruteenium, Roodium, Pallaadium, Hõbe, Kaadmium, Indium, Tina, Hafnium, Tantaal, Volfram, Reenium, Osmium, Iriidium, Plaatina, Kuld, Elavhõbe, Tallium, Plii, Vismut, Poloonium, Rutherfordium, Dubnium, Seaborgium, Bohrium, Hassium, Meitneerium, Darmstadtium ja Röntgeenium. Poolmetallid on : Germaanium, Arseen, Antimon, Telluur ja Astaat. Leelismetallid on : Liitium, Naatrium, Kaalium, Rubiidium, Tseesium ja Frantsium. Leelismuldmetallid on : Kaltsium, Strontsium, Baarium ja Raadium. Sulamistemperatuur metallidel on väga erinevad sulamis temperatuurid. Madalaima sulamistemperatuuriga metall on elavhõbe (-39ºC). Naatrium sulab 98ºC juures, tina sulamistemperatuur on 232ºC. Zn - 420ºC, Al - 660ºC,...
Sisukord SISUKORD.................................................................................................................................................. 2 SISSEJUHATUS......................................................................................................................................... 3 AMINOBENSEEN....................................................................................................................................... 4 MIS ON AMINOBENSEEN?........................................................................................................................... 4 EHITUS..................................................................................................................................................... 4 SAAMINE................................................................................................................................................... 4 FÜÜ...
Nimi MAGNEESIUM REFERAAT Õppeaines: Õpperühm: Juhendaja: professor nimi Esitamiskuupäev:................ Üliõpilase allkiri:................. Õppejõu allkiri: .................. Tallinn 2017 SISUKORD..........................................................................................................................................2 SISSEJUHATUS..................................................................................................................................3 1. MAGNEESIUM...............................................................................................................................4 1. Magneesiumi asend perioodilisustabelis......................................................................................5 2. Magneesiumi aatomi ehitus..................................................
KORDAMINE. 1. aldehüüdid - ained, mis tekivad kui karbonüülrühm asub molekuli otsas ketoonid - ained, mis tekivad kui karbonüülrühm asub molekuli keskel karboksüülhapped - orgaanilised ühendid, mis sisaldavad karboksüül rühma estrid - karboksüülhappe tuletised 2. Nomenklatuuria... 3. Karboksüülhapeid saadakse aldehüüdide oksüdeerumisel. a) "Hõbepeegli" reaktsioon: b) "Porgandimahla" reaktsioon: Tumesinine vedelik muutub kuumutamisel oranziks. Neid reaktsioone saab kasutada kõikide aldehüüdrühma sisaldavate ainetega. 4. Karboksüülhapete keemilised omadused: 1) Happed reageerivad aktiivsete metallidega. 2) Happed reageerivad metalli oksiididega. 3) Happed reageerivad alustega (leelistega, hüdroksiididega...) 4) Happed reageerivad nõrkade hapete sooladega. Saadused on alati soolad. 5) Karboksüülhapped reageerivad alkoholidega. Saadus kuulub estrite klassi. 5. Aldehüüdide esindajad: * Metanaal ehk formaldehüüd HCHO ...
Millise OA-ga on kõige enam a) Oksüdeerunud süsinik +4 (CO2) b) Redutseerunud süsinik -4 (CH4) Mis moodustub orgaanilise aine täielikul põlemisel? CO2+H2O Mis on pürolüüs? Aine lagunemine kõrge temperatuuri toimel Millal tekib põlemisel tahm? Kui põlemine on mittetäielik või pürolüüsiprotsessis Isomeeria On nähtus, kus ühenditel on ühesugune koostis kuid erinev struktuur ja sellest tulenevalt erinevad omadused Isomeerid On ühendid, millel on ühesugune koostis, kuid erinev struktuur ja erinevad omadused Ch3-Ch2-OH (C2H6O) Etanool, piiritus, vesilahuses viin, 78kraadi juures Ch3-O-Ch3 (C2H6O) eete...
Alkoholid on ühendid, mis sisaldavad OH-rühma süsinikuaatomi küljesehk süsiniku molekulis on üks või mitu vesinikku asendatud OH rühmaga Etanool CH3CH2OH füüsikalised omadused:*absoluutne alkohol on 100% etanool *piirituses on 96-98% etanooli *iseloomulik terav lõhn ja kõrvetav maitse *keemistemperatuur on 78°C*tahkumistemperatuur on -117°C*seguneb veega igas vahekorras*½ liitrit absoluutset alkoholi on harjutamata organismile tappev Glütserooli ehk propaan1,2,3triooli füüsikalised omadused:*Värvitu *siirupi taoline *magusa maitsega *vees väga hästi lahustuv *kuumutamisel laguneb aga ei kee *kõhtu lahtistava toimega *kuulub rasvade koostisesse *kasutatakse kreemides Kõik alkoholid põlevad CH3OH+1,5O2 ->CO2+2H2O ; CH3CH2OH+3O2->2CO2+3H2O Karboksüülhapped sisaldavad karboksüülrühma, mis määrab ära hapete füüsikalised ja keemilised omadused Metaanhape ehk sipelghape füüsikalised omadused*värvitu *terava lõhnaga *vees lahustuv *toatemperatu...
Raud Raud (Ferrum) on keemiline element järjenumbriga 26. Raud asub Perioodilisussüsteemi VIII B rühmas ja 4. perioodis. Tal on neli stabiilset isotoopi massiarvudega 54, 56, 57 ja 58. Omadustelt on raud metall. Normaaltingimustel on raud tahke aine tihedusega 7,87 g/cm3. Raua sulamistemperatuur on 1535 Celsiuse kraadi. Raud esineb madalal rõhul neljakristallmodifikatsioonina olenevalt temperatuurist. Raud on kõige levinum element Maa koostises ning levimuselt maakoores metallidest alumiiniumi järel teisel kohal. Raua asetus perioodilisussüsteemis ja aatomi ehitus Raud asub perioodilisusüteemis VIII rühma kõrvalalarühmas. Raua aatomi järjenumbrist (26) ja täisarvuni ümardatud aatomimassist (56) järeldub, et raua aatomi tuumas on 26 prootonit, ja 56-26=30 neutronit. Raud on neljanda perioodi element, järelikult asuvad tema elektronkatte 26 elektroni neljandal elektronkihil : Fe : ...
Referaat Kofeiin ja morfiin 2011 Kofeiin on puriinalkaloid, mida leidub kohvipuu ubades, teepõõsas, mates, guaraana-pauliinia marjades ning väheses koguses kakaos, koolapähklis ja okseiileksis. Taimedes töötab kofeiin pestitsiidina, tappes putukad, kes söövad seda taime. Guaraana-pauliiniast saadavat kofeiini nimetatakse vahel guaraniiniks, matest saadavat kofeiini mateiiniks ja teest saadavat kofeiini teiiniks. Valem: C8H10N4O2 Nomeklatuurnimetus: 1,3,7-trimetüül-1H-puriin- 2,6(3H,7H)-dioon Kofeiin on kesknärvisüsteemi stimulant, mis kõrvaldab uimasuse ning taastab erksuse. Kofeiini sisaldavate jookide populaarsuse tõttu on kofeiin kõige kasutatavam mõnuaine ja kõige kasutatavam psühhoaktiivne aine. Looduses leidub kofeiini koos teiste puriinalkaloididega (teofülliin ja teobromiin), mis on südamestimulandid. Kofeiini kasutatakse koos ravimitega, et nad tõhusamalt mõjuksid, näiteks koos ergotamiiniga mig...
Keemia. *P-METALLIDE ISELOOMUSTUS:Enamtuntud p-metallid on alumiinium, tina ja plii. Alumiinium on kõige levinuim metalliline element maakoores. Tina, pliid ja alumiiniumi lihtainena looduses ei leidu.Alumiiniumi tähtsaim mineraal on boksiit, tina leidub oksiidina(SnO2), plii peamine mineraal on PbS(pliiläik). P-metallide oksiididel ja hüdroksiididel võivad avalduda nii aluselised kui ka happelised omadused (amfoteersed ühendid). *AL, SN, PB KEEMILISED OMADUSED:P-metallid on vastupidavad õhu ja vee suhtes. Kolm mainitud metalli on suhteliselt pehmed. Al reageerib kergesti hapete lahustega ja ka leeliste lahustega. Konts.väävel(H2SO4)- või lämmasktikhappega(HNO3) alumiinium toatemperatuuril ei reageeri! Metall passiveerub! Tina ja plii on vähem aktiivsed metallid. Hapete lahustega praktiliselt ei reageeri. Al, Pb ja Sn kasutatakse sulamites: Al-termiitkeevitusel nt. raudteerööpad, Sn-konservikarbid, Pb- pliiakudes,elektrikaablite kaitset...
HALOGEENIÜHENDID ·Halogeeniühendites on süsiniku aatomid seotud halogeeni aatomi(te)ga CH4 => CH3Cl ·Füüsikalised omadused: Peamiselt vedelikud või tahked ained ·Madalamad halogeeniühendid aurustuvad kergesti, magusa lõhnaga Hüdrofoobsed => ei lahustu vees Suur tihedus (veest raskemad) Enamus on mürgised HALOGEENIÜHENDITE NOMENKLATUUR · Asendusnomenklatuur asendusrühmad + tüviühend fluoro-, kloro-, bromo-, jodo- · Funktsionaalnomenklatuur -süsivesinikrühm + aineklass fluoriid, -kloriid, -bromiid, -jodiid Halogeenühendite nomenklatuuri näited Elektrofiil tühja orbitaaliga osake · Elektrofiilsustsenter - elektrofiili koostisse kuuluv tühja või osaliselt tühja orbitaaliga aatom · Positiivne laeng või osalaeng + · Püüavad moodustada keemilist sidet, täites oma tühja orbitaali teise osakese vaba elektronipaariga · C, H Nukleofiil vaba elektronipaari...
KORDAMISKÜSIMUSED KT. NR.21 (ELEKTROLÜÜS, KEEMILINE VOOLUALLIKAS, METALLIDE KEEMILISED OMADUSED, KORROSIOON) Tuleb teada: 1. Mis on: oksüdatsiooniaste, redoksreaktsioon? Redoksreaktsioonid on reaktsioonid, mille käigus elemendi o.-a. Muutub. O.-a. On arvutuslik suurus, mis on arvuliselt võrdne iooni laenguga eeldusel, et kõik ained koosnevad ioonidest. 2. Mis on oksüdeerumine, redutseerumine, oksüdeerija, redutseerija lähtudes: a) oksüdatsiooniastme muutumisest, b) elektronide üleminekust? Oksüdeerumine on o.-a. suurenemine ta loovutab elektrone. Redutseerumine on o.-a vähenemine ta liidab elektrone. Oksüdeerija redutseerub, o.-a väheneb ja liidab elektrone. Redutseerija oksüdeerub, o.-a suureneb ja loovutab elektrone. 3. Kuidas määrata elementide maksimaalset ja minimaalset oksüdatsiooniastet? Max o.-a näitab rühma number. Metallide min o.-a on null ja mittemetallidel rühma number miinus kaheksa 4. Kui suur on oksüdatsiooniastmete s...