Soolhape MT113 Artur Kubja Soolhappest: Vesinikkloriidhape ehk soolhape (keemiline valem HCl) on gaasilise vesinikkloriidi vesilahus. Soolhape on tugev hape ja tema käsitsemisel tuleb olla ettevaatlik Omadused Hapnikuta hape Veest tihedam Keemistemperatuur 110 °C Üheprootoniline Kaitsevahendid Kanna kummikindaid Kanna kitlit Vajadusel kanna respiraatorit Pildid Click to edit Master text styles Second level Third level Fourth level Fifth level Videod http://www.youtube.com/watch?v=gUGBV8Pa9SM http://www.youtube.com/watch?v=YGjd7xxTuZw Seos erialaga Kasutatakse värvilahustis. Kasutatud Kirjandus http://www.rasketehnika
Hape on aine, mis annab vesilahusesse vesinikioone. Omadused: hapumaitse, reageerimine alustega, indikaatorite isel. Värvus hapete lahustes, reageerimine metallidega, reageerimine aluseliste oksiididega. Hapete liigitamine. * Hapnikuta hape hape, mis eisisalda hapnikku, nt HCl, HBr, HI, H2S. * Hapnikhape hape, mille koostisse kuulub ühe elemendina hapnik, nt H2SO4, H2SO3, HNO3, HNO2, H3PO4, H2CO3. * Üheprootonihape hape, mille molekul annab lahusesse ainult ühe vesinikiooni. Nt HCl, HBr, HI, HNO 3, HNO2, CH3COOH. * Mitmeprootonihape hape, mille molekul annab lahusesse kaks või enam vesinikiooni, nt H2SO4, H2SO3, H2CO3, H3PO4, H4SiO4.* Tugevad happed on tugevalt happeliste omadustgea. HCl, HBr, HI, HNO3, H2SO4. * Nõrgad happed on oluliselt nõrgemate happeliste omadustega nt
TTÜ keemiainstituut Anorgaanilise keemia õppetool YKI3030 Keemia ja materjaliõpetus Laboratoorne Töö pealkiri: Lahuse kontsentratsiooni määramine töö nr. 2 Õpperühm: Töö teostaja: Tuuli Viliberg EAEI 12 Õppejõud: Töö teostatud: Protokoll esitatud: Protokoll arvestatud: Jekaterina Gorohhova 22.09.2011 06.10.2011 1. Töö eesmärk Happe ja leelise lahuste kontsentratsiooni määramine tiitrimisega. 2. Kasutatavad ained Uuritava kontsentratsiooniga HCl lahus, täpse kontsentratsiooniga NaOH lahus, indikaatorid fenoolftaleiin ja metüülpunane. Katseseadmed: koonilised kolvid (250 cm 3), 2 büretti (25 cm3) , pipett (10 cm3). 3. Töö lühikirjeldus I KATSE Happe kontsentratsiooni kindlaksmääramiseks võtsime kindla kontsentratsi...
Töö eesmärk: Happe ja leelise lahuste kontsentratsiooni määramine tiitrimisega. Kasutatavad ained: Uuritava kontsentratsiooniga HCl lahus, täpse kontsentratsiooniga NaOH lahus, indikaatorid fenoolftaleiin (ff) ja metüülpunane (mp). Töövahendid: Koonilised kolvid (250 cm3), 2 büretti (25 cm3) , pipett (10 cm3). Töö käik A: Soolhappelahuse kontsentratsiooni määramine tiitrimisega: Kindla kontsentratsiooniga NaOH lahuse valan büretti, jälgin, et büreti väljalaskeavas ei oleks õhumulle, ning täidan mahuskaala 0- märgini. Pipeti abil mõõdan koonilisse kolbi 10 cm3 hapet ja lisan 2- 4 tilka ff. Järgnevalt tilgutan büretist leelise (NaOH) lahust happesse (HCl), kuni lahuse värv muutub ühe tilga leelise lisamisel punaseks. Loen büretis oleva leelise nivoo asukoha 0,05 cm3 täpsusega. Kordan katset kuni tiitrimiseks kulunud leelise lahuse mahtude vahe ei ületa 0,1 cm3. Katse tulemused: 1) katse 11,5 cm3 (üle tiitritud) 2) katse 11,1 cm3 3)...
CaO + H2O > Ca(OH)2 Veega reageerivad ainult I ja II A rühma, alates kaltsiumist, nende metallide oksiidid. 2) Reageerimine happega Saadused on sool ja vesi. + - + - Na2O + 2HCl > 2NaCl + H2O III -II + -2 3+ 2- Fe2O3 + 3H2SO4 > Fe2(SO4)3 + 3H2O 2+ - BaO + 2HI > BaI2 + H2O 3) Reageerimine happelise oksiidiga Saaduseks on sool. + 2- K2O + CO2 > K2CO3 Happeliste oksiidide keemilised omadused 1) Reageerimine veega Saaduseks on hape. + 2- CO2 + H2O > H2CO3 + 3- P4O10 + 6H2O > 4H3PO4 SiO2 + H2O Ei toimu, sest SiO2 on liiv. 2) Reageerimine alustega Saadused on sool ja vesi. + 2- SO2 + 2NaOH > Na2SO3 + H2O SO3 + Ba(OH)2 > BaSO4 + H2O 3) Reageerimine aluselise oksiidiga. Saadus on sool. Vaata aluseline oksiid reageerib happelise oksiidiga. K2O + CO2 > K2CO3 HAPPED 1) Reageerimine metallidega
Mõisted Aatom aineosake, mis koosneb tuumast ja elektronkattest Aatomituum aatomi osa, kuhu kuuluvad prootonid ja neutronid Elektronkate aatomi osa, mille moodustavad elektronid Aatommass (Ar) ühe aatomi mass aatommassiühikutes Isotoop elemendi teisend, mille tuumas on erinev arv neutrone Orbitaal ruumiosa, kus elektron viibib kõige sagedamini Keemiline element kindla tuumalaeguga aatomite liik Perioodilisusseadus elementide omadused on perioodilises sõltuvuses aatomite tuumalaegust Elektronegatiivsus elemendi võime elektrone enda poole tõmmata Molekul aine väiksem osake, mis koosneb aatomitest Keemiline side mõju, mis ühendab aatomid või ioonid molekuliks või kristalliks Osalaeng elektronegatiivsuse nihkumine polaarsel sidemel Hape aine, mis annab lahusesse vesinikioone Oksiid aine, mis koosneb kahest elemendist, milleks üks on hapnik Alus aine, mis annab lahusesse hüdroksiidioone Sool kristalne aine, mi...
docstxt/14760882859977.txt
Töö eesmärk: Happe ja leelise lahuste kontsentratsiooni määramine tiitrimisega Töövahendid: Koonilised kolvid (250 cm3), 2 büretti (25 cm3) , pipett (10 cm3) Kasutatud ained: Uuritava kontsentratsiooniga HCl lahus, täpse kontsentratsiooniga NaOH lahus, indikaatorid fenoolftaleiin ja metüülpunane Töö käik: Kõigepealt loputan pipetid ja büreti töölahusega. Seejärel valan kindla kontsentratsiooniga NaOH büretti. Pipeti abil mõõdan koonilisse kolbi 10 cm3 HCl-i ning lisan 4 tilka fenoolftaleiini. Järgnevalt tilgutan büretist leelise lahust tilkhaaval hapesse, kuni happe värv muutub. Fikseerin leelise nivoo asukoha ning kordan analoogset katset veel kolm korda. Tulemuste põhjal arvutan nende aritmeetilise keskmise. Kontroll-lahuse tiirimiseks loputan pipetid ja büreti vajaliku töölahusega ning valan HCl-i büretti. Siis mõõda kolbi 10 cm3 NaOH-i ja lisan 4 tilka metüülpunast. Seejärel tilgutan hapet leelise lahusesse, kuni leelise lahuse värv...
a) H2+O2=H2O 16. Halogeenid VII A rühma elemendid Cl2 17. Väärisgaasid VIII A rühma elemendid He 18. Iooniline side metalli ja mittemetalli vaheline side NaCl 19. Kovalentne side aatomite vaheline side Br ja Br mittepolaarne kovalentne side ühesuguste mittemetalli vaheline side Cl ja Cl polaarne side kahe erineva mittemetalli vaheline side H ja Cl 20. Oksiid koosneb kahest elemendist, millest üks on hapnik CaO 21. Hape aine mis annab lahuses vesinikioone (H+) H3PO4 22. Alus aine mis annab lahuses hüdroksiidioone (OH-) NaOH 23. Sool koosneb metallist ja happejäägist NaCl 24. Neutralisatsioonireaktsioon happe ja aluse vaheline reaktsioon H3PO4+3NaOH=Na3PO4+3H2O 25. Indikaator aine mis muudab värvust lahusele, happele või alusele lisamisel universaal- 26. Leelis vees lahustuv tugev lahus NaOH 27. Lahus ühtlane segu, mis koosneb lahusest ja lahustunud ainest 28
Võimaliku ärrituse ärahoidmiseks võiks enne ravi alustamist toodet proovida küünarlohus või otsmikul 3-5 päeva jooksul. Hüdrokinooni efektiivsus kõigub 64-88% vahel. Tõhususe tõstmiseks kombineeritakse seda enamasti tretinoiini, AHA-hapete või koji happega. Juhul, kui mingit toimet ei saabu 3 kuuga, valitakse agressiivsem raviskeem. Hüdrokinooni ei kasutata raseduse ja rinnaga toitmise ajal, kuna ohutus lootele pole tõestatud. Samuti ei kasutata seda aastaid järjest. Koji hape - eriti populaarne Jaapanis. Ta on Aspergillus seente ainevahetusprodukt, mis pärsib melaniini sünteesi. Koji hape on näidanud hüdrokinooniga sarnast efektiivsust, kuid omab kõrgemat nahka ärritavat ja sensibiliseerivat potentsiaali. Tavaliselt kasutatakse teda alternatiivselt hüdrokinoonile. Koji hapet võib kombineerida mitmete teiste ainetega, sealhulgas hüdrokinooniga. Feerulahape - taimne antioksüdant, mida leidub feerula taimedes ja rohelises murus.
Väävelhape Johannes Juhanson 11.A Valem H2SO4 Molekulmass 98,079 AMÜ Sulamistemperatuur 10oC Keemistemperatuur 337oC Tihedus 1,84 g/cm³ ● Väävelhape on anorgaaniline hape, tema anhüdriidiks on vääveltrioksiid. ● Väävelhape on tugev hape ja tema käsitsemisel tuleb olla ettevaatlik. ● Väävelhapet tuntakse ka lõngaõli ja akuhappena. ● Väävelhappe soolad kandsid Eesti rahva hulgas nimesid kübaramust ja sinine silmakivi. Ohutus Kuna väävelhape on väga tugev hape, siis peab seda käsitledes olema väga ettevaatlik: • Suukaudne manustamine võib vigastada seedeelundeid. • Nahale sattudes võib põhjustada tõsiseid söövitushaavu, arme. • Silma sattudes võib rikkuda nägemist.
o metüüloranzi lahus värvub kollasest punaseks. · reageerivad metallidega Hapete vesilahused on enamasti söövitavate omadustega läbipaistvad vedelikud. Kontsentreeritud hapete lahendamisel tuleb hapet valada peene joana vette. Kui hapet satub nahale, tuleb seda kohta pesta jooksva vee all ja neutraliseerida seejärel söögisooda (NaHCO3) lahusega ning siis uuesti jooksva vee all pesta. 3. HAPETE REAKTSIOONID 3.1 metall + hape à sool + vesinik Lahjendatud hapetega reageerivad kõik metallid, mis asuvad pingereas vesinikust vasakul. Seega näiteks Li, Na, K, Mg, Zn, Fe... Hapetega ei reageeri pingereas vesinikust paremal olevad metallid, näiteks Cu, Ag ja Au. Reaktsiooni tuum: metall tõrjub happest vesiniku välja ehk läheb nö tema asemel happeaniooni kõrvale. Niiviisi saadakse sool. Vesinik on sunnitud eralduma lihtainena. 0 I -II I -II 0
ENSÜÜMKATALÜÜSI KEEMILISED MEHHANISMID 1. Ensüümkatalüüsi kolm keemilist mehhanismi. Kovalentse katalüüsi põhimõte. Nukleofiilsed tsentrid ensüümides, side ensüümi ja substraadi vahel. 1. 1) Kolm mehhanismi: · kovalentne katalüüs · üldine happe-alus katalüüs · metalli-iooni katalüüs Kovalentse katalüüsi põhimõte: · Ensüüm ja substraat moodustuvad kovalentseid sidemeid ühes või mitmes reasktsiooniahela punktis. · Kovalentse sideme moodustumine E(ensüümi) ja S(substraadi) vahel tagab reaktsiooni kiiruse tõusu Näide : katalüüsita reaktsioon: BX+Y -> BY+X Kovalentne katalüüs: BX+Y+E -> E:B+Y+X-> E+BY+X Selle mõte on vähendada aktivatsiooni energiat reaktsioonil. Nukleofiilse katalüüsi puhul ensüümi mõni nukleofiilne tsenter (amiin, hüroksüül etc...) atakteerib substraadi elektrofiilset tsentrit. Tekib side substraadi ja ensüümi vahel. ...
Õige. e. Igale hüdroksiidile vastab happeline oksiid.—Õige. f. Leeliseid saadakse vastava aluse(Lihtaine) reageerimisel veega. g. Leeliseid saadakse vastava(I ja II A rühma metalli, alates Ca-st) metalli reageerimisel veega. h. Lahustumatuid aluseid saadakse soolalahuse (mittelahustuva elemendi) reageerimisel leelisega(Veega). i. Hapnikhappeid võib saada hapniku(happelise oksiidi) reageerimisel veega. j. Soolad reageerivad kõikide(siis) hapetega, kui tekib reageerinud happest nõrgem hape või sade. k. Amfoteersed hüdroksiidid reageerivad nii oksiidide(Hapete) kui ka sooladega(Alustega) 8. Kirjutage ja tasakaalustage kaks reaktsioonivõrrandit järgmiste ainete saamise kohta: a. tetrafosfordekaoksiid,-- P+O₂=> P₄O₁₀ / 4H₃PO₄=> P₄O₁₀ + 6H₂O b. kaaliumnitraat, 2K+ 2HNO₃ =>2KNO₃+ H₂ / KOH+ HNO₃=> KNO₃+H₂O c. magneesiumsulfaat. Mg+ H₂SO₄=> MgSO₄+ H₂ / MgO+ H₂SO₄=> MgSO₄+ H₂O 9
Kofeiin toimib ka diureetikuna ehk vee väljutajana. Tänu neile omadustele peletab kofeiin ajutiselt väsimuse ja suurendab nii vaimse kui füüsilise töö võimet. Rasedatel on kofeiini ainevahetus aeglustunud. Seetõttu peaksid rasedad olema kofeiini tarvitamisega eriti ettevaatlikud, sest liigtarbimist seostatakse raseduse katkemisega. Äärmuslikel juhtudel võib kofeiini liigtarbimine põhjustada surma. Mis on tauriin ? Tauriin on orgaaniline hape, mida leidub sapi koostises ja väiksemates kogustes ka loomade teistes kudedes. Inimeste seas on levinud arvamus, et tauriin vähendab ärevust ja tõstab meeleolu. Usaldusväärsed katsed inimestega siiani siiski puuduvad. Mõnedel andmetel vähendab tauriin lihaste väsimust ja tõstab sportlaste sportlikku vormi. Seetõttu on tauriini hakatud kasutama energiajookides. Mis on Guaraana ? Guaraana on Amazonase jõgikonnas kasvava ronipuu seemnetes sisalduv stimuleeriva toimega aine
CaO-kustutamata lubi,valge tahke aine,ehituses FeO raud(III)oksiid,rooste,tekib raual CO-süsinikdioksiid,tekib kütuse ja teiste süsinikku sisaldavate ainete põlemisel.süsihappegaas CO-süsinikoksiid, väga mürgine vingugaas,värvusetu,tekib hapniku mittetäielikul põlemisel NO ja NO lämmastikoksiid ja kämmastikdioksiid, mürgine keskkonna saastaja, punakaspruun SiO ränidioksiid ehk kvarts,kõva kristalne aine HAPPED: HCl- vesinikkloriid hape ehk soolhape H SO väävelhape HNO lämmastikhape H PO fosforhape H CO süsihape HCl-vesinikkloriidhape,lahustub hästi vees,aurud on mürgised,tugev hape, terava lõhnaga H S-divesiniksulfiidhape,väga mürgine,mädamuna lõhnaga,gaasiline hape H SO väävelhape,üks tugevamaid happeid,tugev oksüdeerija,õlitaoline vedelik,seob tugevalt õhuniiskust
Varstu Keskkool Plii Referaat Jevgenia Grigorovits 10. klass Juhendaja: Helen Oppar 2009 Sisukord 1. Aine......................................3 2. Ajalugu.................................4 - 5 3. Levimine..............................6 4. Omadused............................6 - 7 5. Ühendid................................8 - 9 6. Kasutamine..........................9 7. Biotoime..............................10 8. Kautatud kirjandus..............11 Plii. Plumbum. Pb Plii (seatina, sümbol Pb) ·IV A rühma metall ·järjekorranumbriga 82 ·oksüdatsiooniastmed ühendites II ja IV ·sisaldus maakoores 14 ppm ·metallide pingeras asub vagetult enne vesinikku · Aatom ·82 elektroni ·6 elektronkihti 1kihil 2 elektroni 2kihil 8 elektroni 3kihil 18 elektroni 4kihi...
Mis on alus? Aine, mis koosneb metallioonist ja hüdroksiidioonist Mis on hape? Aine, mis annab lahusesse vesinikioone Mis on oksiid? Aine, mis koosneb kahest elemendist, millest 1 on hapnik. Mis vahe on aluselistel oksiididel ja happelistel oksiididel? Aluselised on metallioksiidid ja happelised on mittemetallioksiidid. Mis on leelised? Leelised on tugevad alused. Lahuse pH. (näitab vesinikiooni sisaldust lahuses) 0-7 happeline ülekaalus H+ -ioonid 7 suurem aluseline ülekaalus OH- -ioonid 7 neutraalne H+ ja OH- -ioone lahuses võrdselt Hapete omadused
OKSIIDID keemilised omadused: ALUSED keemilised omadused: 1. al.oksiid+hape=sool+ves 1. alus+hape=sool+vesi 2. al.oksiid+hap.oksiid=sool 2. alus+hap.oksiid=sool+vesi 3. tugevalt al.oksiid+vesi=leelis 3. leelis+sool=uus sool+uus alus (üks neist 4. nõrgalt al.oksiid+vesi=? sade, esimesed lahustuvad vees) 5. hap.oksiid+alus=vesi+sool 4. lahustumatu alus (t)= oksiid+vesi 6. hap.oksiid+al.oksiid=sool ALUSED saamine: 7. hap.oksiid+vesi=hape 1. akt.metall+vesi=leelis+vesinik 8. amf.oksiid+hape=sool+vesi 2. akt.met.oksiid+vesi=leelis OKSIIDID saamine: 3. sool+leelis=alus+sool (esimesed vees 1. metall+hapnik=oksiid lahustuvad) 2. mit.metall+hapnik=oksiid SOOL...
aox+hape=sool+vesi aox+vesi=leelis(1,2arühm) aox+hox=sool hox+alus=sool+vesi hox+vesi=hape neut ox:NO,N2O,CO ei reag. aluse, hape, soolaga. Hape+metal=sool +H2 (vesinikust vasakul) Hape+ aox=sool+vesi Hape+alus=sool+vesi Hape+sool=hape+sool(kuitekib nõrgem hape v sade) Alus+hox=sool+vesi Alus+hape=sool+vesi Alus+sool=alus+sool(mõlem. Lah+lah=sade) Sool+met=sool+met(met aktiivsem) Sool+hape=sool+hape(kui tekib nõrgem hape v sade) Sool+alus=sool+alus (mõlem. Lah+lah=sade) Sool+sool=sool+sool(mõlem. Lah+lah=sade) Aox = aluseline oksiid Hox= happeline oksiid
oksiid siid oksiid Aluselin Sool+ vesi Hüdroksiid Sool e oksiid + vesi Hüdrok- Sool+ vesi Hüdroksiid+ LAHUS Sool+ vesi siid sool Hape Sool+ vesi Sool+ vesi Sool+ hape LAHUS Sool+ vesinik Sool Hüdrok Sool+ hape Sool+ sool LAHUS Sool+ metall siid+ sool Vesi Hüdroksiid + LAHUS LAHUS LAHUS Hape vesi Metall Sool+ vesinik Sool+ metall SULAM
1. aluseline oksiid + hape sool + vesi 2. aluseline oksiid + vesi leelis 3. happeline oksiid + alus sool + vesi 4. happeline oksiid + vesi hape 5. aluseline oksiid + happeline oksiid sool 6. lihtaine + hapnik oksiid 7. alus(veeslahustumatu temp. aluseline oksiid + vesi 8. vesinik + element vesinikühend 9. metal + hape sool + vesinik( lahjendatud hapetega reageerivad pingereas vasakul pool olevad metallid, paremal pool olevad mitte) 10. alus + hape sool + vesi 11. sool + hape sool + hape ( reaktsioon toimub kui tugevam hape tõrjub nõrgema happe soolast välja) 12. veeslahustumatu hüdroksiid temp. aluseline oksiid + vesi 13. leelis + sool veeslahustumatu alus + sool(ainult leelised reageerivad sooladega) 14. aktiivne metall + vesi leelis + vesinik 15. metall + sool metall + sool(aktiivsem metall tõrjub vähem aktiivsema soolast välja, vastupidi ei toimu) 16. sool + hape sool + hape 17
Aineklassid Happed Happed koosnevad vesinikust (H) ja happejäägist. Need jagunevad kaheks: 1) Tugevad happed: 2) Nõrgad happed: HCl, HSO, HNO HSiO, HS, HSO, HCO Happed tekivad: Happeline oksiid + vesi hape (SiO ei reageeri) Reaktsioonivõrrandid: Neutraliseerimise reaktsioon 1) Hape + alus sool + vesi HCl + NaOH NaCl + HO 2) Hape + aluseline oksiid sool + vesi Vaata pingerida! HSO + NaO NaSO + HO 3) Hape + metall sool + vesinik HNO + Na NaNO + H 4) Hape + sool hape + sool CaCO + HCl CaCl + HCO Tingimused: *Tekib nõrgem või lenduvam hape *Tekib sade Oksiidid Oksiidid koosnevad mittemetallist või metallist ja hapnikust (O). Jagunevad samuti kaheks:
HAPPELISED OKSIIDID HAPPED METALLID 1. Happeline oksiid + vesi = hape 1. Hape + alus = sool + vesi 1. Metall + hapnik = oksiid(v.a. väärismetallid Ag, Au, Pt) ( NB; SiO ei reageeri veega ) HCl + NaOH = NaCl + H2O (* Na, K peamiselt peroksiidid ja hüperoksiidid) 2 2
ULTIMATE KEEMIA REAKTSIOONIDE TABEL. (anorgaaniline) OKSIIDIDE REAKTSIOONID + vesi = leelis (reag. IA ja IIA metallidega) Aluseline oksiid + hape = sool + vesi (metallioksiidid) + happeline oksiid = sool + vesi = hape (reag. CO2, SO2, SO3, N2O3, P4O10) Happeline oksiid + alus = sool + vesi (mittemetallioksiid) + aluseline oksiid = sool HAPETE REAKTSIOONID + alus = sool + vesi HAPE + aluseline oksiid = sool + vesi + sool = uus hape + uus sool (uus hape peab olema nõrgem või uus sool mittelahustuv)
1. mida kõrgem temperatuur, seda suurem on dissotsatsioon (tegemist on endotermilise protsessiga) 2. mida lahjem lahus, seda suurem on dissotsatsioon (Ostwaldi lahjendusseadus – kontsentratsiooni vähenemisel dissotsatsioon kasvab, lõpmatul lahjendamisel saab α võrdseks ühega) 3. mida rohkem elektrolüüdi molekule, seda nõrgem dissotsatsioon (vastavalt Le Chatelier’i printsiibile) ALUSED HAPPED Arrheniuse teooria hape – aine, mis vesilahuses dissotsieerub vesinikioonideks ja anioonideks alus – aine, mis vesilahuses dissotsieerub katioonideks ja hüdroksiidioonideks. Brostedi-Lowry / protolüütiline teooria hape – aine, mille osakesed loovutavad prootoneid (H+) – PROOTONI DOONOR nt: H3O+; NH4^+; H2S; HNO2; CH3COOH alus – aine, mille osakesed seovad prootoneid (H+) – PROOTONI AKTSEPTOR nt: H2O; OH-; S^2-; NH3; F-; HS-
Metall+hapnik=metallioksiid Mittemetall+hapnik=mittemetallioksiid Metall+hape=sool+vesinik EI KEHTI HNO3 JA H2SO4, VESINIK NOOL ÜLESSE Alus+hape=sool+vesi Aluseline oksiid+vesi=alus OKSIID PEAB OLEMA TUGEVALT ALUSELINE Happeline oksiid+vesi=hape Aluseline(amfoteerne) oksiid+hape=sool+vesi Happeline oksiid+alus=sool+vesi Aluseline oksiid+happeline oksiid=sool Alus+sool=alus+sool LÄHTEAINED VEES LAHUSTUVAD, SAADUSTES ÜKS MITTELAHUSTUV(SADE) Hape+sool=hape+sool LÄHTEAINE TUGEV HAPE, SAADUS NÕRK HAPE VÕI TEKIB SOOLA SADE Sool+sool=sool+sool LÄHTEAINED VEES LAHUSTUVAD, SAADUSTES ÜKS MITTELAHUSTUV(SADE) Mittelahustuv alus=metallioksiid+vesi Vees lahustumatu karbonaat=metallioksiid+CO2 LAHUSE pH TASE pH iseloomustab vesinikioonide sisaldust lahuses. Happelistes lahustes pH<7, leidub vesinikioone. Aluselistes lahustes pH>7, leidub hüdroksiidioone. Neutraalsetes lahustes pH=7, vesinikioone ja hüdroksiidioone võrdselt.
Na2CO3 (naatriumkarbonaat) SiO3 2- -silikaat H2SiO3 (ränihape) metall-SiO3 näit. Al2(SiO3)3 (alumiiniumsilikaat) NO3 - -nitraat HNO3 (lämmastikhape) metall-NO3 näit. KNO3 (kaaliumnitraat) NO2 - -nitrit HNO2 (lämmastikushape) metall-NO2 näit. NaNO2 (naatriumnitrit) REAKTSIOONIVÕRRANDITE KOOSTAMINE HAPE + ALUS → SOOL + VESI H2SO4 + 2NaOH → Na2SO4 + 2H2O + ALUSELINE OKSIID → SOOL + VESI 2HCl + MgO → MgCl2 + H2O + SOOL → UUS SOOL + UUS HAPE H2SO4 + Na2S → Na2SO4 + H2S↑ + METALL → SOOL + VESINIK 2HCl + Zn → ZnCl2 + H2↑ Cu + 4k. HNO3→ Cu(NO3)2 + 2NO2↑ + 2H2O ALUS + HAPE vaata HAPE + ALUS + HAPPELINE OKSIID → SOOL + VESI 2NaOH + CO2→ Na2CO3 + H2O + SOOL → UUS ALUS + UUS SOOL CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl lagunemine (to) → ALUSELINE OSKIID + VESI Ca(OH)2→(to) CaO + H2O HAPPELINE OSKIID (mittemetalli oksiid) + VESI → HAPE SO3 + H2O → H2SO4 + ALUS vaata ALUS + HAPPELINE OKSIID
REAKTSIOONIVÕRRANDITE KOOSTAMINE HAPE + ALUS SOOL + VESI H2SO4 + 2NaOH Na2SO4 + 2H2O + ALUSELINE OKSIID SOOL + VESI HCl + MgO MgCl2 + H2O + SOOL UUS SOOL + UUS HAPE H2SO4 + Na2S Na2SO4 + H2S NB! Reaktsioon toimub siis, kui uus tekkiv happe on reageerivast happest nõrgem või lenduvam või kui uus tekkiv sool ei lahustu vees (sade). + METALL SOOL + VESINIK 2HCl + Zn ZnCl2 + H2
2( silikaat),H4SiO4-ränihape-SiO4-4( silikaat) 12. Millest on tingitud kõik a) hapete, b) aluste üldised omadused? a) Hapete üldised omadused tingitud vesinikioonide olemasolust lahuses . b)aluste omadused on tingitud hüdroksiidioonide esinemisest lahuses 13. Millised on oksiidide, hapete, aluste, soolade keemilised omadused (vajalikud tingimused reaktsioonide toimumiseks)? Oksiidid: 1) happeline oksiid+vesi hape 2) happeline oksiid+alussool + vesi 3) happeline oksiid +aluseline oksiid SOOL ! 4) aluseline oksiid+ vesi alus 5) aluseline oksiid +hape sool +vesi 6) aluseline oksiid+ happeline oksiid SOOL ! Happed: 1) hape+ aluseline oksiid sool +vesi 2) hape+ alus sool +vesi 3)hape +metall sool +vesinik 4) hape+ sool hape+ sool Alused: 1) alus+ sool alus +sool 2) aluse lagunemine kuumutamisel aluseline oksiid +vesi 3) alus happeline +oksiid sool
+ ALUS = SOOL + H2O +AL. OKSIID = SOOL + H2O = UUS SOOL + UUS HAPE + SOOL NB! Reaktsioon toimub siis, kui tekkiv hape on reageerivast HAPE happest nõrgem või kui uus tekkiv sool ei lahustu vees (sade). = SOOL + H2 NB! Reageerivad pingereas vesinikust vasakul paiknevad + METALL metallid. Erandiks on k. HNO3, lahj. HNO3 ja k. H2SO4 reageerimine metallidega (ei kehti metallide pingerida, ei eraldu
Alus+hape=sool+vesi aluseline o. +hape=sool+vesi happeline o. +alus=sool+vesi aluseline o. + happeline o.=sool REAGEERIVAD ALATI sool+sool=sool+sool LHTEAINED PEAVAD VEES LAHUSTAMA AGA VHEMALT 1 SAADUS PEAB OLEMA MITTELAHUSTUV sool+alus=alus+sool LHTEAINED PEAVAD VEES LAHUSTAMA AGA VHEMALT 1 SAADUS PEAB OLEMA MITTELAHUSTUV sool+hape=sool+hape PEAB TEKKIMA REAGEERINUD HAPPEST NRGEM HAPE VI SADE aluseline o. + vesi=alus+vesi AINULT 1A ja 2A RHMA METALLIDE OKSIIDID happeline o. + vesi=hape+vesi EI REAGEERI SIO3 metall+sool=sool+metall SOOL PEAB OLEMA LAHUSTUV JA METALL AKTIIVSEM KUI SOOLA KOOSTISES OLEV METALL metall+hape=sool+vesinik METALL PEAB OLEMA PINGEREAS VASAKUL VESINIKUST metall+vesi=alus+vesinik metall+mittemetall=sool REAKTSIOONI TOIMUMINE SLTUB M6LEMA AKTIIVSUSEST
+ vesi = alus (hüdroksiid) B rühma met. oks. met. oksiid + hap.oks = sool + alus + hape = sool + vesi + sool + vesi = hape + hap. oks hap. oksiid + alus.oks = sool + hape + alus = sool + vesi + sool + metall = sool + H2 pingerida! hape + met. oks = sool + vesi + alus = sool + vesi + sool = u. hape + u. sool + hap. oks = sool + vesi alus + hape = sool + vesi + sool = u. alus + u. sool
8) Inertsed oksiidid on oksiidid, mis ei reageeri happe ega alusega 9) Neutralisatsioonireaktsioon on happe ja aluse vaheline reaktsioon 10) Happe lahuse toimul muutub metüüloranž punaseks, lakmus punaseks 11) Aluse lahuse toimel muutub fenoolftaleiin punaseks, lakmus siniseks 12) Sool reageerib teise soolaga, kui lähteained on vees lahustuvad ja vähemalt üks saadustest mittelahustuv 13) Sool reageerib happega, kui lähtehape on tugevam kui saadud hape 14) Metall reageerib happega, kui üksikmetall asub pingereas enne H2 15) Sool reageerib alusega, kui lähteained on vees lahustuvad ja vähemalt üks saadustest mittelahustuv 16) Metall reageerib soola lahusega, kui üksikmetall on pingereas enne soola koostises olevat metalli 17) Alustelistest oksiididest reageerivad veega ainult IA ja IIA metallioksiidid 18) Happelistest oksiididest ei reageeri veega ainult SiO2 Keemilised omadused: 1. Happed
2Na + 2H2O = 2NaOH + H2 2. Aluseline oksiid + vesi = hüdroksiid Na2O + H2O = 2NaOH 3.Sool + leelis = hüdroksiid + sool CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4 HAPPED HCl vesinikkloriidhape 1.Happeline oksiid + vesi = hape H2CO3 süsihape SO2 + H2O = H2SO3 H2SO4 väävelhape 2.Hape + sool = sool + hape H2S + CuSO4 = CuS + H2SO4 SOOLAD CaSO4 kaltsiumsulfaat 1. Metall + mittemetall = sool FeCl2 raud(II)kloriid Ca + Cl = CaCl2
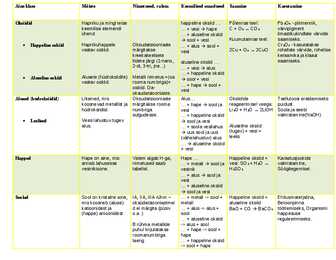
Aine klass Mõiste Nimetused, valem Keemilised omadused Saamine Kasutamine Oksiidid Hapniku ja mingi teise happeline oksiid ... Põlemise teel: PbO - pliimennik, keemilise elemendi ... + vesi hape C + O CO värvipigment ühend ... + aluseline oksiid ilmastikukindlate värvide sool + vesi Kuumutamise teel: saamiseks. · Happeline oskiid Hapnikuhappele Oksudatsiooniaste ... + alus sool + CrO - kasutatakse
KEEMIA REAAL Happelised oksiidid : Mittemetalli oksiidid Aluselised oksiidid: Metalli oksiidid 1. alus + hape sool + vesi NaOH + HCl NaCl + H2O 2. aluseline oksiid + hape sool + vesi CaO + 2HCl CaCl2 + H2O 3. happeline oksiid + alus sool + vesi Ca(OH)2 + CO2 CaCO3 + H2O 4. happeline oksiid + aluseline oksiid sool CaO + CO2 CaCO3 5. aluseline oksiid + vesi alus Na2O + H2O 2 NaOH CaO + H2O Ca(OH)2 CuO + H2O ei toimu 6. happeline oksiid + vesi hape CO2 + H2O H2CO3
SOOLADE HÜDROLÜÜS Soolad tekivad happe ja aluse vahelisel neutralisatsioonireaktsioonil. HCl + NaOH = NaCl (söögisool) + H2O Kõigi soolade lahused ei ole neutraalsed Soola hüdrolüüs Soola hüdrolüüs on neutralisatsioonireaktsiooni pöördreaktsioon. Sool reageerib veega, moodustades nõrga happe või nõrga aluse. Soola lahuse pH Soola lahuses tekkiva keskkonna määrab tugevam elektrolüüt. Tugev alus + nõrk hape aluseline kk Nõrk alus + tugev hape happeline kk Tugev alus + tugev hape neutraalne kk (Hüdrolüüsi ei toimu!) Mida nõrgem on hape, seda tugevamalt toimub tema soola hüdrolüüs. Mida nõrgema aluse sool, seda tugevam on soola hüdrolüüs lahuses. Na2CO3 aluseline (NaOH tugev alus ; H2CO3 nõrk hape). FeCl3 happeline ( Fe(OH)3 nõrk alus ; HCl tugev hape). Na2SO4 neutraalne
Keemia Mõisted: Hape Hape on keemiline aine, mis annab lahusesse vesinikioone. [HNO3, H2S, H2SO3] Alus Alus on keemiline aine, annab lahusesse hüdroksiidioone. [NaOH, Ca(OH)2] Oksiid Hapniku ja mingi teise keemilise elemendi ühend. [Li2O, SO3] Sool Soolad on kristalsed ained, mis koosnevad aluse katioonidest (näiteks Ca2+) ja happe anioonidest (näiteks SO42-). [K2S04, Na2CO3] Aluseline oksiid Alusele (hüdroksiidile) vastav oksiid. Aluselised oksiidid on oksiidid,
6. happeline oksiid + alus→ sool + vesi (vahetusreaktsioon) 7. aluseline oksiid + happeline oksiid→ sool (ühinemisreaktsioon) Teatud tingimustel toimuvad reaktsioonid: 1. sool + sool→ sool + sool (vahetusreaktsioon) lähteaine soolad peavad mõlemad vees lahustuma ja üks saadustes tekkinud sool peab olema sade. 2. sool+ alus→ uus sool + uus alus (vahetusreaktsioon) lähteained peavad vees lahustuma ja üks saadustest peab olema sade. 3. sool + hape→uus sool + uus hape (vahetusreaktsioon) saadustes peab tekkima kas lähteaine happest nõrgem hape või sade. 4. metall + sool→ uus sool + uus metall (asendusreaktsioon) lähteaine sool peab olema vees lahustuv ja metall peab olema aktiivsem kui soola koostises oleva metall (vt. Pingerida) – ehk lähteaines üksi olev metall peab pingereas olema vasakul pool soola koostises olevast metallist. 5. metall + hape→ sool + vesinik (asendusreaktsioon) lähteaine metall peab olema pingereas vasakul pool vesinikust
(reageeriv sool peab olema vees lahustuv) CuSO4 + Fe = FeSO4 + Cu (vt.pingerida) Erand: Kui metall on väga aktiivne(IA,IIA), siis eelistatult see reageerib soola vesilahuses oleva veega ja tekkiv leelis reag. soolaga. 2Na + 2H2O = 2NaOH + H2 2NaOH + ZnCl2 = Zn(OH)2 + 2NaCl 2Na+2H2O +ZnCl2 =Zn(OH)2 +2NaCl + H2 2)sool + LEELIS = uus sool + uus alus(üks) (reageeriv sool ja alus peavad olema vees lahustuvad) FeCl3 +3 KOH = 3KCl + Fe(OH)3 3)sool + HAPE = uus sool + nõrgem hape Na2S + 2HCl = 2NaCl + H2S Kui tekib sadenev sool, siis ei pea tekkiv hape olema nõrgem ega lenduvam. 4)sool + SOOL = uus sool + uus sool(üks ) (reageerivad soolad peavad olema vees lahustuvad) NaCl + AgNO3 = NaNO3 + AgCl 5) karbonaadid ja nitraadid lagunevad kuumutamisel CaCO3 = CaO + CO2 2NaNO3 = 2NaNO2 + O2 2Zn(NO3)2 = 2ZnO + 4NO2 + O2 2AgNO3 = 2Ag + 2NO2 + O2 Soolade saamine 1) Hape + metall =sool+H2 2) Hape+aluseline oksiid =sool+H2O
H I Cu I ja II F -I Sn II ja IV Pb II ja IV Hapete ja happeanioonide nimetused vastav hape happeline oksiid happeanioon happeaniooni nimi (saadakse veega reageerimisel) SO2 vääveldioksiid H2SO3 väävlishape SO32- -sulfit SO3 vääveltrioksiid H2SO4 väävelhape SO42- -sulfaat
1) metall + hapnik > al. Oksiid 2) mittemetall + hapnik > hap. oksiid 3) metall + vesi > leelis + vesinik 4) metall (aktiivsem) + sool (lahustub) > sool + metall (vähem aktiivsem) 5) al. oksiid + hap. oksiid (SO2 > H2SO3, SO3 > H2SO4, CO2 > H2CO3, P4O10 > H3PO4, N2O5 > HNO3) > sool 6) metall (H-st vasakul) + hape > sool + vesinik 7) al. oksiid + vesi > leelis 8) al. oksiid + hape > sool + vesi 9) hap. oksiid + vesi > hape 10) hap. oksiid + alus > sool + vesi 11)alus + sool (lahustuvad) > alus (sade) + sool 12) sool + leelis > sool + mittelahustuv alus 13) sool + sool (lahustuvad) > sool (sade) + sool 14) alus + hape > sool + vesi (neutralisatsiooni reaktsioon) 15) sool + hape (tugev H2SO4, HNO3, HI, HBr, HCl) > sool + hape (nõrk H2SO3, H3PO4, H2S, HNO2, H2CO3, H2SiO3) 16) hap. oksiid > mittemetall + hapnik 17) al. oksiid > metall + hapnik 18) alus >t al. oksiid + vesi 19) hapnikhape >t hap
ioonideks Vesiniksool -sool, mis sisaldab vesinikku http://www.abiks.pri.ee 2. ÜLESANDED hape + metall =>> sool + H2 -metall aktiivsem vesinikust hape + alus.oks =>> sool + H2O -alati hape + alus =>> sool + H2O -alati hape + sool =>> sool + hape -peab tekkima I happest nõrgem hape või sade alus + hap.oks =>> sool + H2O -alati alus + sool =>> sool + alus -I mõlemad lahustuvad, II üks lahutumatu sool + metall =>> metall + sool -sool lahutuv, I metall aktiivsem II metllist sool + sool =>> sool + sool -I mõlemad lahutuvad, II üks lahutumatu alus.oks + hap.oks =>> sool -alati
3. Aluste nimetused + valemid. Vaata vihiku tabelit ja näited. 4. Soolade nimetused + valemid. Vaata vihiku tabelit ja näited. 5. Oksiidide saamine. Metall / Mittemetall + hapnik -> OKSIID Näiteks: a) 4 Na + O2 -> 2 Na2O b) N2 + 2 O2 -> 2 NO2 Mittemetallid lihtainetena, millel on alati indeks 2: H2 O2 F2 N2 Cl2 Br2 I2 6. Hapete saamine. a) Happeline oksiid + vesi -> Hapnikhape Näiteks: SO2 + H2O -> H2SO3 Erand: SiO2 veega ei reageeri! b) Vesinik + vastav mittemetall -> hapnikuta hape Näiteks: H2 + Cl2 -> 2 HCl 7. Aluste saamine. a) Aluseline oksiid + vesi -> alus (leelis) Tingimus: Veega reageerivad vaid IA ja IIA rühma metallioksiidid, tekib leelis. Näiteks: Na2O + H2O -> 2 NaOH CaO + H2O -> Ca(OH)2 b) Leelis- ja leelismuldmetall + vesi -> leelis+ vesinik Tingimus: Veega reageerivad vaid IA ja IIA rühma metallid, tekib leelis ja vesinik. 2 Na + 2 H2O -> 2 NaOH + H2 Ca + 2 H2O -> Ca(OH)2 + H2 c) Vees lahustumatu aluse saamine (sool + leelis -> alus + sool)
3) Kui aine on toatemperatuuril gaasilises olekus, siis tuleb selle aine valemi taha märkida nool üles. Kui aine on toatemperatuuril tahkes olekus või vees mittelahustuv või veest raskem, siis tuleb märkida selle aine valemi taha nool alla. 4) Kõik toimuvad reaktsioonivõrrandid tuleb tasakaalustada. 5) Kui reaktsiooni ei toimu, siis tuleb sõnadega märkida põhjendus, miks antud reaktsioon ei toimu. Aluseliste oksiidide keemilised omadused 1) aluseline oksiid + hape sool + vesi II -II + - 2+ - III -II + 2- 3+ 2- CuO + 2HCl CuCl2 + H2O Al2O3 + 3H2SO4 Al2(SO4)3 + 3H2O 2) aluseline oksiid + vesi leelis Veega reageerivad ainult aktiivsete metallide oksiidid (I A rühma metalli oksiidid ja II A rühma alates kaltsiumist metallide oksiidid) II -II 2+ - I -II + - CaO + H2O Ca(OH)2 Na2O + H2O 2NaOH 3) aluseline oksiid + happeline oksiid sool II -II 2+ 2- I -II + 3- BaO + CO2 BaCO3 6Cs2O + P4O10 4Cs3PO4 Happeliste oksiidide keemilised omadused
ANORGAANILINE KEEMIA I: LABORATOORSE TÖÖ PROTOKOLL Robert Ginter - 142462MLGBII Praktikum IV Ühend pH FF Värv MP Värv Univ. ind. Aine Näit klass HCl; 0,01M 1,41 Värvusetu Roosa 4 Hape HNO3; 0,01M 1,97 Värvusetu Roosa 3 Hape H2SO4; 2,06 Värvusetu Roosa 3 Hape 0,01M H3PO4; 2,32 Värvusetu Kollane 4 Hape 0,01M NAOH; 0,01M 11,64 Roosa Kollane 8 Alus CH3COOH; 2,46 Värvusetu Roosa 4 Hape 1M CH3COOH; 3,22 Värvusetu Roosa 5 Hape 0,01M NH3*H2O; 9,05 Värvusetu Kollane 6 Alus 0,01M NH3*H20; 10,41 Roosa Kollane 10 Alus 1M
AINF.KLASSIDE VAHELISF.D REAKTSIOONID Aluselise ja l. alus hape sool NaOH HCI NaCl + HIC) happelise aine vesi 2 3 H2S04 6 E-120 reaktsioon: tekib 2. aluseline oksiid + hape Mgo + 2HCl MgC12 + alati sool. sool vesi Na20 + H2SOå* Na2S04 + 1-120 3. happcline oksiid + alus —i COZ CaC03 + H20 (Happelise oksiidi sool 4 vesi reageerimisel tekib 2 NaOH + — Nazso, + HIC) oksiidile happe 4. happelinc Okiid aluseline cao + c02 — CaC03 oksiid
SOOLAD Soolad on kristalsed ained, mis koosnevad katioonidest ja anioonidest. Keemilised omadused Vees lahustuvad soolad esinevad lahustes ioonidena: Na2SO4 2Na+ + SO42- 1. Reageerimine metalliga uus sool + uus metall (metall reageerib ves lahustuva soolaga, kui ta on aktiivsem kui soola koostises olev metall) Fe + CuSO4 FeSO4 + Cu 2. Reageerimine hapetega uus sool + uus hape (toimub vaid siis, kui tekib nõrgem hape) Na2S + H2SO4 Na2SO4 + H2S (kui tekib H2CO3, siis ta laguneb tekkemomendil veeks ja süsinikdioksiidik CaCO3 + 2HCl CaCl2 + H2O + CO2) 3. Reageerimine alustega uus alus + uus sool (lähteained peavad olema vees lahustuvad ja saadustest üks lahustumatu) CuCl2 +2NaOH Cu(OH)2 + 2NaCl 4. Reageerimine sooladega uus sool + uus sool (lähteained peavad olema vees
Happed Muud asjad HCl vesinikkloriidhape Cl- kloriid ehk soolhape SO3-2 sulfit H2SO3 väävlishape SO4-2 sulfaat H2SO4 väävelhape S-2 sulfiid H2S divesiniksulfiidhape CO3-2 H2CO3 süsihape karbonaat H3PO4 fosforhape PO4-3 fosfaat HNO3 lämmastikhape NO3- nitraat HNO2 lämmastikushape NO2- nitrit 4-tetra; 5-penta; 6-heksa; 7-hepta; 8-okta; 9-nona; 10-deka 1. aluseline oksiid + hape sool + vesi 2. CaO + 2HCl CaCl2 + H2O 3. 4. aluseline oksiid + vesi leelis 5. LiO + H2O 2LiOH 6. 7. happeline oksiid + alus sool + vesi 8. SO2 + 2NaOH Na2SO3 + H2O 9. 10. happeline oksiid + vesi hape 11. P4O10 + 6H2O 4H3PO4 12. 13. aluseline oksiid + happeline oksiid sool 14. CaO + CO2 CaCO3 15. 16. lihtaine + hapnik oksiid 17. C + O2 CO2 18. 19