+9| 2)7) +17| 2)8)7) +35| 2)8)18)7) +53| 2)8)18)18)7) 2 5 2 5 2 5 2s 2p 3s 3p 4s 4p 5s25p5 Max o.a. on VII Min o.a. on I · Cl keemilised omadused 1. Cl2 + 2NaBr = 2NaCl + Br2 2. 3Cl2 + 2Fe = 2FeCl3 3. Cl2 + 2Na = 2NaCl 4. Cl2 + H2 = 2HCl 5. Cl2 + H2O = Kloorivesi · HCl keemilised omadused 1. 2HCl + Fe = FeCl2 + H2 2. 2HCl + CaO = CaCl2 + H2O 3. HCl + NaOH = NaCl + H2O · Indikaatorid (H2 määramine) Happeline keskkond (pH<7; [H+]>[OH-]) mo= punane lakmus = punane ff
CaO- oksiid; SO3- vääveltrioksiid P4O10- tetrafosforheksaoksiid; Fe2O3-diraudtrioksiid H2SO3-väävlishape-hape; H3PO4-fosforhape CuSO4-vask(II)sulfaat- sool; BaCl2-baariumkloriid Ca(NO3)2-kaltsiumnitraat; Na2CO3-naatriumkarbonaat AgNO3-hõbenitraat; Al2(SO3)2-alumiiniumsulfiit Na2S-naatriumsulfiid; K2SiO3-kaaliumsilikaat Mg(OH)2- magneesiumhüdroksiid- alus KOH-kaaliumhüdroksiid ; Fe(OH)3- raud(III)hüdroksiid LiOH- liitiumhüdroksiid Baarium-baariumoksiid- baariumhüdroksiid- baariumnitraat 2Ba+O2->2BaO; BaO+H2O->Ba(OH)2 Ba(OH)2+2HNO3->Ba(NO3)2+2H2O Fosfor-fosfor(V)oksiid-fosforhape-kaltsiumfosfaat 4P+5O2->P4O10; P4O10+6H2O->4H3PO4 2H3PO4+3CaO->Ca3(PO4)2+3H2O Väävel-vääveldioksiid-väävlishape-naatriumsulfit S+O2->SO2; SO2+H2O->H2SO3 H2SO3+2Na->Na2SO3+H2 Vask(II)hüdroksiid-vask(II)oksiid- vask(II)sulfaat-vask Cu(OH)2->CuO+H2O; CuO+H2SO4->CuSO4+H2O CuSO4+Zn->Cu+ZnSO4 Raud(III)hüdroksiid-raud(III)oksiid- raud(III)kloriid- raud(III)hüdroksiid: ...
Mg(OH)2 OH + MgOH+ 2OH + Mg2+ 3) Happed HCl H+ + Cl H2SO4 H+ + HSO4 2H + SO42 METALLIDE KEEMILISED OMADUSED 1) REAGEERIMINE LIHTAINETEGA (mittemetallid) 4Al + 3O2 2Al2O3 3Fe + 2O2 Fe3O4 2) REAGEERIMINE VEEGA NB! Toimub pingerea alusel · Väga aktiivsed metallid reageerides veega, annavad saadustesse leelis + H2 2Na + 2H2O 2NaOH + H2 · Keskmise aktiivsusega metallid reageerivad kõrgel temperatuuril veeauruga oksiid + H2 Zn + H2O ZnO + H2 · Väheaktiivsed metallid ei reageeri veega 3) REAGEERIMINE HAPETEGA NB! Toimub pingerea alusel · Metallid mis asuvad pingereas vesinikust vasakul reageerivad lahjendatud hapetega ja tõrjuvad välja vesiniku(v.a. lämmastikhape HNO3)
LABORATOORNE TÖÖ Nr.3 Teema:Vee mööduva kareduse määramine Töö vahendid: HCl, triloon B lahus, puhverlahus (NH4Cl+NH4OH), indikaatorid metüüloranz, kroomgeenmust ET-00, bürett, pipett, koonilised kolvid, mõõtsilinder, statiiv. Neutralisatsioonimeetodi üheks tähtsamaks rakendusalaks on vee kareduse määramine. Loodusliku vee karedus on tingitud vees lahustunud kaltsiumi- ja magneesiumsooladest: Ca(HCO3)2; Mg(HCO3)2; CaSO4; MgSO4; CaCl2; MgCl2; CaSiO3. Peale soolade sisaldab looduslik vesi veel kolloidaalselt lahustunud ränihapet, orgaanilisi kolloide ja vees lahustunud gaase: CO2; O2 ja N2. Karedust väljendatakse katlakivi tekitajate Ca ja Mg soolade sisaldusega mg-ekvivalentides ühe liitri (cm3) kohta. Vee üldkaredus jaotub mööduvaks ja püsivaks kareduseks. Mööduva kareduse põhjustavad süsihappe happelised soolad Ca(HCO3)2 ja Mg(HCO3)2, mis on kõrvaldatavad vee keetmisega, sest vesinikkarbonaadid laguneva...
1. Metall + mittemetall sool NB! H2CO3 2Na + S Na2S H2O + CO2 2. Metall + hape sool + H2 Zn + 2HCl ZnCl2 + H2 3. Metall + sool uus metall + uus sool Fe + CuSO4 Cu + FeSO4 4. Alus + hape sool + vesi NaOH + HCl NaCl + H2O 5.Alus + happeline oksiid sool + vesi 2NaOH + SO2 Na2SO3 + H2O 6.Hape + aluseline oksiid sool + vesi 2HCl + CuO CuCl2 + H2O 7.Happeline oksiid + aluseline oksiid sool CaO + CO2 CaCO3 8. Alus(leelis) + sool uus alus + uus sool CuSO4 + NaOH Cu(OH)2 + Na2SO4 9. Hape + sool uus hape + uus sool H2SO4 + BaCl2 HCl + BaSO4 10. Sool + sool uus sool + uus sool K2SO4 + BaCl2 KCl + BaSO4
Alused ehk hüdroksiidid on liitained mis koosnevad 1, või mitmest OH rühmast. Saamine 1)Metallioksiid+Vesi Na2O+H20 -> 2NaOH 2)Aktiivne metall+Vesi 2Na+2H2O -> 2NaOH+H2 3)Soolade vesilahuste elektrolüüsil 2NaCl+2H2O -> 2NaOH +H2+Cl2 4)Vees lahustuv alus+sool CuSO4+2NaOH -> Na2SO4+Cu(OH) 2 Liigitus: Veeslahustuvad hüdroksiidid ehk leelised (LiOH;BaOH) ja vees lahustumatud(Cu(OH) 2;Zn(OH) 2). Keemilised omadused: Leelised 1)Reageerivad hapetega 2NaOH+H2SO4 -> Na2SO4+2H2O 2)Reageerivad vees lahustuvate sooladega CuSO4+NaOH -> Na2SO4+Cu(OH) 2 3)Reageerivad happeliste oksiididega Ca(OH) 2+CO2 -> CaCO3+H2O Lahustumatud 1) Reageerivad hapetega Cu(OH) 2+H2SO4 -> CuSO4+2H2O 2)Kuumutamisel lagunevad Cu(OH) 2 -> CuO+...
METALLIDE SAAMINE MAAKIDEST Maak→rikastatud maak→metallioksiid→metall Kogu protsess on väga energiamahukas. Ühendis sidemete lõhkumiseks tuleb kulutada Energiat. 1. Maagi rikastamine: maak vabastatakse kõrvalainetest kasutades füüsikaliste omaduste erinevust. 2. Särdamine: mitteoksiidsete maakide kuumutamine õhu juuresolekul, et saada oksiidne maak. 2PbS+3O2=2PbO+2SO2 3. Metalli redutseerimine metallioksiidist: Redutseerijana kasutatakse: a) koksi (C) (kõige odavam) Fe3O4+4C=3Fe+4CO b) süsinikmonooksiidi (CO), mis tekib ka koksi kasutamisel Fe2O3+3CO=2Fe+3CO2 c) vesinikku (väga puhaste metallide saamiseks) CuO+H2=Cu+H2O d) alumiiniumi (aluminotermia), kui on metalli vaja toota rasksulavast maagist Cr2O3+2Al=2Cr+Al2O3 Aktiivseid metalle saadakse sulandite elektrolüüsil: Sulatatud keedusoolast elektrivoolu läbijuhtimisel saadakse Na: 2NaCl=2Na+Cl2 Sulatatud boksiidist saadaks...
Keemia kordamine metallid Põhiklassid: Happed Soolad Alused e. Oksiidid metall+aniooni nim hüdroksiidid HCl- - + kloriid metall + OH- metall + O22- vesinikkloriidhape HBr- + bromiid -vesinikbromiidhape HI- - vesinikjodiidhape + jodiid Kui metall on B-rühmast, tuleb öelda nimetuses H2S2- - divesiniksulfiidhape + sulfiid tema o-a. Enamasti on see kas 2 või 3. Kui aine H2SO32- - väävlishape + sulfit on antud, tuleb leida metalli o-a ja siis anda H2SO42- - väävelhape + sulfaat nimetus. 3- H3PO4 - fosforhape + fosfaat Erand: Sn ja Pb on muidu A-rühmas, aga neil 2- H2CO3 - süsihape + karbonaat esinem mitu o-a'...
Oksiidideks nim liitaineid mis koosnevad 2-est elemendist millest üks on hapnik. Saamine: 1)Metall+HapnikOksiid 2Ca+ O2=2CaO 2)Alkoholi põletamine C2H5OH + O2 2CO2 + H2O 3)Lihtaine põletamine S + O2 SO2 4)Aluste lagunemine Cu(OH)2 CuO + H2O 5)Soolade lagunemin CaCO3 CO2 + CaO Liigitus: Aluselised oksiidid ehk metalli oksiidid ja Happelised oksiididel mittemetalli oksiidid. Keemilised omadused: Aluselised 1) Reageerivad H2O CaO+H2O -> Ca(OH) 2 2) Reageerivad hapetega CuO+H2SO4 -> CuSO4+H2O 3) Reageerivad oksiididega CaO+CO2 -> CaCO3 Happelised 1) Reageerivad H2O SO2+H2O -> H2SO3 2) Reag alustega Ca(OH) 2+CO2 -> CaCO3+H2O 3) Reageerivad oksiididega CaO+CO2 -> CaCO3 Amfoteersus on keemilise aine võime reag...
(hüdroksüül) rühma. (nomenklatuuris -nool lõpp) Üldvalem R OH Liigitus: 1) 1 hüdroksüülsed CH3OH 2) mitme hüdroksüülsed Propaan triool Alkohoolide keemilised omadused: 1) Põlemine 2CH3OH + 3O2 -> 2CO2 + 4H2O 2) Reageerivad metallidega moodustades alkoholaate 2CH3OH + 2Na -> 2CH3ONa + H2 3) Võivad dehüdraatuda tulemusena tekib alkeen C2H5OH -> H2C=CH2 + H2O 4) Alkoholid võivad oksüdeerida. NB! Cu katalüsaatori juuresolekul moodustade aldehüüde. 2CH3OH + O2 -> 2HCHO + H2O 5) Alkohol kui hape reageerib alustega (leelistega) C2H5OH + NaOH -> C2H5ONa + H2O Etanooli tootmine: a) Tärklisest (C6H10O5)n ->(ensüm) (C12H22O11)
Metallid reageerides hapnikuga tekivad oksiidid (NaO jne), reageerimisel väävliga tekivad sulfiidid(2Na + S Na2S), reageerimisel klooriga tekivad kloriidid (2Fe + 3Cl2 2FeCl3). Reageerimisel lahjendatud hapetega reageerivad ainult pingereas vesinikust vasakul olevad metallid, oksüdeerijaks on H2 ioon, leelistega reageerimisel on oksüdeerijaks OH (NaOH) ning tuleb vaadata aluste ja soolade lahustuvust vees(NaCl). Veega reageerivad aktiivsed metallid (K - Mg) tekivad hüdroksiid ja H2 - 2Na + 2H2O 2NaOH + H2; keskmised metallid (Al - Fe) reageerivad veeauruga (kõrgel to) - tekivad oksiid ja H2, Zn + H2O ZnO +H2; väheaktiivsed metallid (Ni-Au) ei reageeri veega. Hapnikuga reageerimisel tekivad oksiidid: 4Al+3O2=2Al2O3. Enamik metalle reageerib ka väävliga: Fe + S = FeS. Kloor on halogeen ( 7 A rühm) 2Na+Cl2=2NaCl. Lahjendatud hapetega reageerimine vastavalt elektrokeemilisele pingereale. Enne H2 tõrjub H2 välja ja peale vesinikku ei tõrju välja. Na + OH NaOH ???
NaCl naatriumkloriid Na2SO4 naatriumsulfaat Soolade liigitamine Lihtsoolad KCl NaCl keedusool Na2CO3 (pesu) sooda KNO3 kaaliumnitraat Vesiniksoolad NaHCO3 söögisooda KH2PO4 kaaliumdivesinikfosfaat Hüdroksiid soolad Cu2(OH)2CO3 Mg(OH)Cl Liitsoolad KAl(SO4)2 * 12H2O AlK(SO4)2*12H2O Soolade keemilised omadused 1. sool + metall = UUS SOOL + UUS METALL Ba + CuCl2 2Na + 2H2O = 2NaOH + H2 Li + FeCl3 2NaOH + CuSO4 = Cu(OH)2 + Na2SO4 CuSO4 + Ag CuSO4 + Fe = FeSO4 + Cu 2. sool + leelis = UUS SOOL + UUS ALUS FeCl3 + 3KOH = 3KCl + Fe(OH)3 3. sool + hape = UUS SOOL + UUS HAPE CaCO3 + 2HCl = CaCl + H2O + CO2 4. sool + sool = UUS SOOL + UUS SOOL Happed koosnevad vesiniku aatomi(te)st ja happejäägist. Happeid liigitatakse tugevuse järgi, vesinike arvu järgi, hapniku sisalduse järgi
N: CaO + 2HCl --) CaCl + H2O PH · PH > 7 aluseline NaOH · PH < 7 happeline HCl · PH = 7 neutraalne H2O Võrrandid · (tugevalt)Aluseline oksiid + vesi --) alus Na2O +H2O --) 2NaOH · (nõrga)aluse sool + leelis --) (tugevalt)aluse sool+ nõrk alus CuSO4 +2NaOH --) NaSO4 + Cu(OH)2 · Leelismetall + vesi --) leelis + vesinik Leelismuldmetall 2Na + 2H2O --) 2NaOH + H2 ALUSTE NIMETAMINE · Kui B-rühma metall siis sulgudesse tuleb öelda oksutatsiooni aste. Cr(OH)3 kroom(3)hüdrooksiid · Kui A-rühma metall siis ütled elemendi nime ja kohe järgi hüdrooksiid NaOH naatriumhüdrooksiid
a. metallid, mis reageerivad veega IA ja IIA alates Ca). Iga metall tõrjub pingereas temale järgnevad metallid soola lahusest välja, kuid ei tõrju talle pingereas eelnevaid metalle. Pingerida pole rakendatav aktiivsete metallide puhul (Li, K, Ba, Ca, Na, Mg), mis reageerivad esmalt veega vesiniku eraldumisega ja seejärel tekkiv hüdroksiid reageerib soola lahusega. Na + CuSO4 à 1. etapp: 2Na + 2H2O à 2NaOH + H2 2. etapp: 2NaOH + CuSO4 à Cu(OH)2 + 2Na2SO4 Summaarselt: 2Na + CuSO4 à Cu(OH)2 + 2Na2SO4 + H2 8) sool + sool à sool + sool vahetus Na2SO4 + BaCl2 à BaSO4 + 2NaCl 2KI + Pb(NO 3)2 à PbI2 + 2KNO3 Reaktsioon toimub siis, kui mõlemad lähteained lahustuvad vees ja vähemalt üks saadustest sadeneb.
3. Reaktsioonivõrrandid 1) Alkeenid alküünid Mida kõrgema energia side, seda lihtsam on neid lõhkuda. Markovnikovi reegel: vesinik läheb sinna, kus enne rohkem vesinikke on. Jälgida ainult neid, kus on kaksikside vahel. Alkeen + H2 > alkaan CH2=CH2 + H2> CH3CH3 CH2=CH-CH3 + HCl > CH3CHClCH3 CH2=CH-CH3 + Cl2> ClCH2CHClCH3 CH2=CH2 + H2O > CH3CH2OH CH2=CH-CH >(-H2) CH=-C-CH3 + H2 CH2=CH2 + 3O2 > 2CO2 + 2H2O 2) Karboksüülhapped reageerimine metalliga: 2RCOOH + 2Na > 2RCOONa + H2(up); 2RCOOH + Ca > (RCOO)2Ca +H2 (up) -''- metalliüksiidiga: 2RCOOH + ZnO > (RCOO)2Zn + H20 -''- hüdroksiidiga: 2RCOOH + Ca(OH)2 > (RCOO)2Ca + H2O; RCOOH + NaOH > RCOONa + H2O -''- soolaga: 2RCOOH + NaCO3 > RCOONa + H2CO3 H2Oja CO2(up) 3) Oksüdeerumine alkohol>aldehüüd/ketoon> karboksüülhape: CH3CH2OH >[O] CH3C=O ja H >[O] CH3C=O ja -OH 4) Redutseerumine eelmisele vastupidine järjekord 5) benseenide reaktsioonid
1. Karboksüülhapete (-COOH) moodustumine aldehüüdidest (-CHO): a)oksüdeerumine hapnikuga CH3-CHO + O2=CH3-COOH b)hõbepeegli reaktsioon. CH3-CHO + Ag2O=CH3-COOH + 2Ag c)oksüdeerumine vask(II)oksiidiga. CH3-CHO + 2CuO=CH3-COOH + Cu2O. 2.Estri(nagu COOH aga H asemel R) lagunemine veetoimel happelises keskkonnas karboksüülhappeks ja alkoholiks. HCOOC6H13 + HOH= HCOOH + C6H13OH. 3. Karboksüülhappe soola(nagu COOH aga H asemel Na, Li, Ca jne.) reageerimine tugevama happega. H2SO4 + CH3COONa=NaHSO4 + CH3COOH. 4. Karboksüülhapete omadused: a) Täielik põlemine CH3COOH + 2O2 = 2 CO2 + 2H2O b) Redutseerimine aldehüüdiks. C8H17COOH + H2=C8H17CHO + H2O c) Redutseerimine alkoholiks. C8H17COOH + 2H2=C9H19OH + H2O d) Anhüdriidi teke. CH3COOH + CH3COOH=(CH3CO)2O + H2O e) Metallidega reageerimine. 2CH3COOH + 2Na= 2CH3COONa + H2. 2CH3COOH + Ca =(CH3COO)2Ca + H2. f) Aluseliste oksiididega reageerimine(tekib sool). 2CH3COOH + Li2O =2CH3 COOLi + H2O g) Hüd...
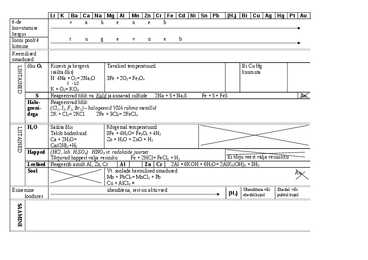
liitmine Keemilised omadused õhu O2 Kiiresti ja kergesti Tavalisel temperatuuril Bi Cu Hg LIHTAINED (säilta õlis) kuumuta N: 4Na + O2= 2Na2O 3Fe + 2O2= Fe3O4 I -1/2 K + O2= KO2 S Reageerivad kõik va. Kuld ja annavad sulfiide 2Na + S= Na2S Fe + S= FeS Au Halo- Reageerivad kõik geeni- (Cl2, I2, F2, Br2) halogeenid VIIA rühma metallid dega 2K + Cl2= 2KCl 2Fe + 3Cl2= 2FeCl3 H2O Säilita õlis Kõrgemal temperatuuril LIITAINED Tekib hüdroksiid 3Fe + 4H2O= Fe3O4 + 4H2 Ca + 2H2O= Zn + H2O = ZnO + H2 Ca(OH)2+H2
Tihedus normaaltingimustel on 8,9 g/cm3 Sulamistemperatuur on 1455 °C ja keemistemperatuur 2913 °C. 5 Kasutamine Rõhuv enamus nikli toodangust kasutatakse ära nii raua kui ka värviliste metallide sulamite koostises Mõni protsent nikli toodangust kasutatakse katalüsaatorite saamiseks, mida rakendatakse sünteesikeemias ja toiduainetööstuses 6 Võrrandid 2Ni + 2NaOH 2NiO + 2Na + H2 NiCl2 + 6H2O NiO + NiSO4 + 7H2O 7 Huvitavat Nikkel on Eesti rahvastiku hulgas kõige enam levinud kontaktallergeen. Põhilised niklitootjad maailmas on Venemaa, Kanada, Uus Kaledoonia ja Austraalia. Nikli aastane toodang jääb umbes miljoni tonnini. Nikkel võib palaval suvel põhjustada allergilist nahapõletikku. Üldvarusid maismaal hinnatakse 70 miljonile tonnile. 8 9 10 Küsimus Nikkel on.. a) Leelismetall
Elektrolüüdid Ained, mis jagunevad ioonideks, annavad lahusesse ioone. Tugevad elektrolüüdid: soolad, tugevad happed(HCl, HNO3, H2SO4), leelised(IA rühma, IIA rühma alataes Ca metallide hüdroksiidid) Nõrgad elektrolüüdid: nõrgad happed, nõrgad alused(rasklahustuvad) Dissotseeruminei ehk ioonideks jagunemine. 1) soolad dissotseeruvad esimeses astmes ja täielikult Na2CO3 --> 2Na+ + CO2-3 2) Alused mitme OH-rühmaga dissotseeruvad astmeliselt NaOH --> Na+ + OH- Ca(OH)2 --> CaOH+ + OH- --> <-- 2OH-+ Ca2+ 3) Happed. Mitmeprootonilised happed dissotseeruvad astmeliselt. Üheprootonilised nagu soolad HNO3 --> H++NO2- H2CO3 --> H++ HCO33- --> <-- 2H++ CO32- NB! H+ + H2O --> H3O+ hüdrooniumioon Lahustes on kõige rohkem I astme osakesi!!!!! Mitteelektrolüüdid Ei esine lahustes ioonidena, vaid lahuses on molekulid või aatomid. Oksiidid, lihtained, enamus orgaanilisi aineid. Hüdrolüüs ainet...
METALLID Metallid on : Berüllium, Magneesium, Alumiinium, Skandium, Titaan, Vanaadium, Kroom, Mangaan, Raud, Koobalt, Nikkel, Vask, Tsink, Gallium, Ütrium, Tsirkoonium, Nioobium, Molübdeen, Tehneetsium, Ruteenium, Roodium, Pallaadium, Hõbe, Kaadmium, Indium, Tina, Hafnium, Tantaal, Volfram, Reenium, Osmium, Iriidium, Plaatina, Kuld, Elavhõbe, Tallium, Plii, Vismut, Poloonium, Rutherfordium, Dubnium, Seaborgium, Bohrium, Hassium, Meitneerium, Darmstadtium ja Röntgeenium. Poolmetallid on : Germaanium, Arseen, Antimon, Telluur ja Astaat. Leelismetallid on : Liitium, Naatrium, Kaalium, Rubiidium, Tseesium ja Frantsium. Leelismuldmetallid on : Kaltsium, Strontsium, Baarium ja Raadium. Sulamistemperatuur metallidel on väga erinevad sulamis temperatuurid. Madalaima sulamistemperatuuriga metall on elavhõbe (-39ºC). Naatrium sulab 98ºC juures, tina sulamistemperatuur on 232ºC. Zn - 420ºC, Al - 660ºC,...
5.MITTEMETALLID 5.1 MITTEMETALLIDE MITMEKESISUS *Mittemetallid asuvad perioodilisussüsteemis perioodide lõpus ja suuremates rühmades. Mittemetallidel on viimasel kihil 4-8 elektroni. Lihtainena on nende seas 11 gaasilist: H2 , N2, O2, F2, Cl2 ; 6 väärisgaasi (He-Rn) 10 tahket: B, C, Si, P, As, S, Se, Te, I, At 1 vedel: Br2 *Mittemetallid on madala sulamistemperatuuriga, üsna pehmed ja kergesti peenestatavad. Mõned on väga kõrge sulamistemperatuuriga, kõvad kuid seejuures haprad. Väga erineva värvusega. Mittemetallide ühiseks omaduseks on see, et nad praktiliselt ei juhi elektrit, kuid süsinik allotroop grafiit on hea elektrijuht. Mittemetallide aatomid on metallide aatomitega võrreldes suhteliselt väiksemad. Välises elektronkihis on neil enamasti elektrone märgatavalt rohkem kui metallide aatomites. Tuumalaengu mõju väliskihi elektronidele on küllalt suur ja neid hoitakse aatomis suhteliselt tugevalt kinni, seega loovutavad väliskihi ...
Kloor on levikult maakoores 20. element. Seejuures sinna sisse ei ole arvestatud suuri kloorivarusid ookeanivetes. Levinumateks kloriidseteks mineraalideks on näiteks haliit ehk kivisool NaCl ja sülviin ehk sülviit KCl jt. Kivisoola tunti juba 40-50 tuhat aastat tagasi. Puhtalt sai kloori esmakordselt C.W. Scheele Uppsalas Rootsis 1774. aastal keedusoola ja väävelhappe segu kuumutamisel. Saadakse sulatatud kloriidide või nende vesilahuste elektolüüsil: 2NaCl à 2Na + Cl2 2NaCl + H2O à H2 + Cl2 + 2NaOH Laboratoorselt saadakse peamiselt vesinikkloriidhappest oksüdeerijate toimel: 4HCl + MnO2 à MnCl2 + Cl2 + 2H2O 2KMnO4 + 16HCl à 5Cl2 + 2MnCl2 + 2KCl + 8H2O Omadused: Kloor on kollakasroheline, terava lõhnaga, mürgine, õhust üle kahe korra raskem gaas. Kloori lahustub vees halvasti, kuid kloori osalisel lahustumisel vees moodustub kloorivesi. See kujutab endast kloori lahust vees, kus osaliselt toimuva reaktsiooni tulemusena tekib kaks hapet:
Keemia tunnikontroll 29.01 Alused Mõisted: Alus, hüdrooksiid, leelis, neutralisatsioon Saamine (3 viisi), Reeglid, võrrandid, keemilised omadused Alus – Aine mis annab lahusesse hüdroksiidioone(üaine mis seob vesinikioone ehk prootoneid) Hüdroksiid- Anorgaaniline ühend mille koostisse kuuluvad hüdroksiidioonid OH või hüdroksiidrühmad Leelis – Vees hästilahustuv tugev alus (ehk hüdroksiid) Neutralisatsioon – Aluse ja happe vaheline reaktsioon, milles tekivad sool ja vesi Aluste saamine – Leelise saamine metalli reageerimisel veega (Veega reageerivad ainult aktiivsed metallid. Se on redoksreaktsioon, mille käigus eraludb vesinik). 2Na + 2H2O 2NaOH + H2 (lendub) Leelise saamine tugevalt aluselise oksiidi reageerimisel veega. Siis saadakse leelis kui vesi reageerib metalliga, mis asub IA-s või IIA metallidega, mis on Ca,Sr,Ba BaO + H2O Ba(OH)2 Aluse(hüdroksiidi)kau...
CaCO3 = CaO + CO2 Hüdroksiid = Metallioksiid + vesi Cu(OH)2 = CuO + H2O (va leelismetallide hüdroksiidid) HÜDROKSIIDID NaOH naatriumhüdroksiid 1.Metall (aktiivne)+ vesi = hüdroksiid + vesinik Cu(OH)2 vask(II)hüdroksiid 2Na + 2H2O = 2NaOH + H2 2. Aluseline oksiid + vesi = hüdroksiid Na2O + H2O = 2NaOH 3.Sool + leelis = hüdroksiid + sool CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4 HAPPED HCl vesinikkloriidhape 1.Happeline oksiid + vesi = hape H2CO3 süsihape
1)Oksüdeerija aine mille osakesed liidavad elektrone ise redutseerides Oksüdeerumine el.loovutamine redoksreakts. sellele vastab o.a suurenemine Elektrolüüs elektroodidel kulgev redoksreakts. mis toimub elektrivoolu läbijuhtimisel lahusest või sulatatud elektrolüüdist Aluminotermia lihtainete enamasti met. Saamine ühenditest alumiiniumiga reutseerimise teel Akumulaator korduvalt kasutatav keemiline vooluallikas, mis on laetav Särdamine metalliühendi üleviimine oksiidiks kuumutamisel õhuhapniku juuresolekul 2)keemiline metalli vahetu keemiline reakts. keskkonnas leiduva oksüdeer. kuivade gaasidega kk. Elektrok metalli kokkupuude elektrolüüdilahusega. Rohkem levinud. 3)muudetakse keemilisel reakts vabanev energia elektrienergiaks. Et elekktri saada tuleb oksüdeerumine ja reduts läbi viia eraldi elektroodidel. Ioonide liikumiseks ühendatakse lahused u-kujulise klaastoru abil, milles on elektrolüüdilahus. Mõlemas lahuses on ...
Seebikivi KEEMILINE KOOSTIS Naatriumhüdroksiidi ehk seebikivi valem on NaOH, seega üks seebikivi molekul koosneb ühest naatriumi katioonist ja ühest hüdroksiidioonist. KEEMILISED OMADUSED Õhu käes seistes seob tugevasti õhuniiskust ning seetõttu tuleb säilitada teda õhukindlalt suletud anumas. Selle pH on leeliseline. Naatriumhüdroksiid ei põle ning on vees täielikult lahustuv ja anorgaaniline. FÜÜSIKALISED OMADUSED Naatriumhüdroksiid on valge tahke lõhnatu aine. See on väga kergesti lahustuv aine (lahustuvus 20°C juures on 111g/ 100g). See sulab 318°C juures ja selle keemistemperatuur on 1390°C. NaOH tihedus on 2,1 g/cm3 ning molaarmass 40 g/mol. TEKE 2Na+ + 2H2O + 2e- H2 + 2NaOH LEVIMUS Margariinid, kakaojahu, leivad (happesuse regulaatorid), seep, pinna-töötlemisained, E519, E520, E521, E522, E523, tehiskiudainetes jm. KASUTAMINE Naatriumhüdroksiid on väga tähtis tooraine keemiatööstus...
II kursususe teemad 1. Keemilised vooluallikad. Nimeta keemilisi vooluallikaid ja nende tööpõhimõtteid (ka reaktsioonid mis nendes toimuvad!). Kes oli esimese vooluallika leiutaja? 2. Leelis- ja leelismuldmetallid. Nende kasutamine igapäevaelus. Keemilised ja füüsikalised omadused (ka reaktsioonid!). Nende metallide ühendid ja nende kasutamine igapäevaelus. 3. p-metallid. Nende kasutamine igapäevaelus. Keemilised ja füüsikalised omadused (ka reaktsioonid!). Nende metallide ühendid ja nende kasutamine igapäevaelus. 4. Siirdemetallid. Nende kasutamine igapäevaelus. Keemilised ja füüsikalised omadused (ka reaktsioonid!). Nende metallide ühendid ja nende kasutamine igapäevaelus. 5. Mis metallide üldomadused, võrreldes mittemetallidega? 6. Mis on allotroop? 7. Halogeenid. Nende kasutamine igapäevaelus. Keemilised ja füüsikalised omadused (ka reaktsioonid!). Nende ühendid ja nende kasutamine igapäevaelus. 8. Kalkogeenid. Nende kasutamine iga...
Mittemetallid - erineva värvusega,tahkes või gaasilises olekus(-Br),juhivad soojust ja elektrit halvasti.Tahkes olekus olevad metallid on: aatomvõrega-teemant,räni,süsiniku-,räni- ja broomi ühendid;kõvad;vees mittelahustuvad;kõrge sulamis- ja keemistemp. Molekulvõrega-gaasid,väävel,fosfor;haprad;vees vähelahustuvad;madal sulamistemp. Paljud esinevad mitme allotroobina. Allotroopia on nähtus, kus üks ja sama keemiline element esineb mitme erineva lihtainena. Kõige levinum element:MAAL-hapnik,räni; KOSMOS-vesinik,heelium;ELUSORGANISMIS- süsinik,vesinik ja hapnik. Keemilised omadused:reaktsioonil metallidega käituvad oksüdeerijana_ O2+Ca=2CaO; S+Ca=2CaS.Reaktsioonil mittemetallidega võivad käituda nii oksüdeerijana kui ka redutseerijana (oleneb mittemetalli aktiivsusest) H2+S=H2S;S+O2=SO2 Vesinik-sobib kokku IA-rühmaga: üks elektron väliskihil, mille annavad elektroni ära; ei sobi IA-rühma-mittemetall ja teised metallid,vesinik gaas teised...
Leelismetallid on IA rühma metallid.reag veega tekivad leelised. Vees lahustuv hüdroksiid. Väga söövitav. 2Na+2H2O=2NaOH+H2.. leelismuldmetallid. Ca, Sr, Ba. Levikult maakoores. Al Fe Ca Na K Mg. Ühendid Na+O2=Na2O2.. naatriumperoksiid. K+O2=KO2 kaaliumhüperoksiid. CaO kustutamata lubi. CaCO3 lubjakivi, paekivi = Cao+CO2. CaO+H2O=Ca(OH)2. Lubja kustutamine. Vees vähelahustuv tekib lubjapiim veega segamisel, seismisel lubjavesi. NaOH seebikivi. NaHCO3 söögisooda kasutamine.. taignate kergitamine. Tugeva happe neutraliseerimiseks.Na2CO3 sooda kasutamine. tooraine klaasi valmistamisel, argielus. Na2CO3 pesusooda. NaCL keedusool. Tänu pinnale tekkivale õhukesele, kuid tihedale oksiidikihile on alumiinium väga vastupidav õhu ja vee toime suhtes. Al on raua järel üks enam kasutatavaid metalle. Temast valmistatakse mitmesuguseid tarbeesemeid, kerge metalline on ta hinnatud ehituses. Kasutatakse ka erinevates sulamites, vähemaktiivsete metallid...
Kontrolltöö 10.klass Vesinik ja halogeniidid l. Võrrelge metallide ja mittemetallide paiknemist perioodilisustabelis ning nende aatomi suurust. Metallidel on suured aatomid ja mittemetallidel on väiksed aatomid.Metallid paiknevad perioodilisustabelis vasakul pool ja katavad üle poole perioodilisustabelist.Mittemetallid paiknevad paremal pool perioodilisustabelit. 2. Selgitage, mis on allotroopia ja allotroobid. Tooge näiteid. Nähtust, kus üks ja sama keemiline element saab esineda mitme erineva lihtainena, nimetatakse allotroopiaks ja vastavaid lihtaineid allotroopideks. Nt. -Erinev aatomite arv molekulis: dihapnik O2 ja osoon O3 -Erinev kristallistruktuur: teemant ja grafiit 3. Kirjutage (ja tasakaalustage) kaks reaktsioonivõrrandit, milles vesinik oleks redutseerija. H2 + S = H2S H2+Cl2=2HCl 4. Mille poolest erinevad üksteistest halogeenid? Halogeenid erinevad üksteisest värvuse ja agregaatoleku poolest.Veel erinevad aatomite suuru...
- 1. - , () . . - , (, ) - , ; , . , 0 , ( ) . (Zn, Al, ). E 0 Al 3+ / Al = -1,66V . [ ] pH () E 0 ( Zn 2+ / Zn ) = -0,76V pH = - log H + . ( ) E 0 Fe 2+ / Fe = -0,44V . , . - , 1 ...
FÜÜSIKALISED OMADUSED: *O2 väiksema aktiivsusega kui O3, sest O3 *Aatomiraadius metallide omadest laguneb: O2-ks ja O3-ks. väiksem,seetõttu hoiavad mitte-met. Elektrone *Tekib monohapnik, kõige aktiivsem.sa tugevamini kinni. *Hapnik reageerib liht-ja liit ainetega ja *Mit.metallid+ metall/vesinik = oksüdeerija. saaduseks on vastavate elementide oksiid. *Mitte-met. On molekulaarsed või aatomvõrega. 4FeS2+ 11O2=2Fe2O3 + 8SO2 *Mitte-met. Pole plastilised ja head elektri juhid. *Hapniku saamine: (v.a grafiit) *Mitte-met. Suurenevad V-lt , P-le 2HgO(temp)=2Hg+O2 Ja rühmas ülevalt alla. 2KNO3(temp)=2KNO3+O2 *Tahked: N2,O2,P,Br2,Cl2, Ar,Nl,He,F2. *Tööstuslikult: Vedela õhu traktrioneeriva KEEMILISED OMADUSED: destillatsioonil. Väärisgaasid reageeriv...
KEEMIA EKSAM 2014 1. Kirjuta nimetused valemina välja: Dilämmastikoksiid – N2O Alimiiniumoksiid –Al2O3 Magneesiumhüdroksiid –Mg(OH)2 Raud (III)oksiid –Fe2O3 Naatriumnitraat –NaS 2. Anna nimetus: H2 S DiVesiniksulfiidhape H 2 C O3 Süsihappe 32−¿ Sulfit SO ¿ −¿ 2 Nitrit NO¿ −¿¿ Jodiid I 3. Määra keemiline side NaCl iooniline side F2 kovalentne mittepolaarne side NO2 kovalentne polaarne side −¿¿ Cl iooniline side Na iooniline side 4. Kirjuta välja, mis reegli alusel toimub a) Sool+alus=uus sool+uus alus reegel: lähteained peavad vees lahustuma ning 1 saadus peab olema lahustumatu b) Sool+hape=uus sool+uus hape reegel: üks saadustest peab olema r...
Распространенность металлов в природе Содержание некоторых металлов в земной коре: Алюминий 8,2% Железо 5,0% Кальций 4,1% Натрий 2,3% Магний 2,3% Калий 2,1% Al Fe Ca Na Mg K остальные В природе металлы могут встречаться Только в свободном (самородном) виде (благородные металлы - золото, платина); В самородном виде и в виде соединений (металлы малой активности – серебро, медь, ртуть, олово); Только в виде соединений (металлы, стоящие в ряду напряжений до олова). Распространенность металлов в природе Содержание некоторых металлов в морской воде: Na+...
a) Nimetus Naatriumhüdroksiid. b) Rahvapärane nimetus Seebikivi, vananenud nimetuselt ka sööbenaatrium, (varem ka kaustiline sooda) c) Kasutamine ja leidumine: Keetmisel rasvaga moodustab naatriumhüdroksiid seebi. 2Na+ + 2H2O + 2e H2 + 2NaOH Naatriumhüdroksiid on väga tähtis tooraine keemiatööstuses, sest lisaks keemialaborite, kasutatakse teda näiteks seebi valmistamiseks ja vedelkütuste töötlemisel, nafta- (nafta ja õlide puhastamisel), tselluloosi- ja paberitööstuses, tehiskiudainete valmistamisel, gaaside puhastamisel jm. Keedusoolast seebikivi tootmisel on kõrvalproduktiks kloor. Seebikivi vajatakse peamiselt paberi-, tselluloosi- ja klaasitööstuses, jääkaine kloor leiab aga tänuväärse paiga PVC tootmisel. PVC lähteainetest moodustab keedusool 57 %, ülejäänu toornafta. Leidumine: margariinid, kakaojahu, leivad (happesuse regulaatorid), seep, pinna-töötlemisained, E519, E520, E521, E522, E523, nafta-, tselluloosi- ja paberitööstu...
Mittemetallid Vesinik 1. Aatomi ehitus: 1 elektron ja 1 prooton, põhiliselt liidab ühe elektroni, väga harva loovutab. Deetrium raske vesinik, aatommass 2 (1 prooton + 1 neutorn) Triitium - Üliraske vesinik, aatommass 3 (1 prooton + 2 neutronit) 2. Leidumine looduses: leidub nii ehedalt kui ühenditena: ehedalt: päikeses, atmosfäri ülemistes kihtides ühenditena: vesi, taim- ja loomorganismid, looduslikud kütused 3. Füüsikalised omadused: Värvuseta, lõhnata, maitseta, õhust 14,5 korda kergem gaasiline aine. Vees praktiliselt ei lahustu, lahustub mitmetes metallides. 4. Keemilised omadused: Redutseerija, st loovutab elektrone. Reageerib aktiivsete mittemetallidega: 2H2 + O2 => 2H2O N2 + 3H2 => 2NH3 (amoniaak) H2 + S => H2S (divesiniksulfiid) H2 + Cl2 => 2HCl (vesinikkloriid) Reageerib hapnikku sisaldavate ainetega, võttes ära hapniku: CuO + H2 => Cu + H2O Reageerides väga aktiivsete ...
6.2 metallide reageerimine hapete lahustega 6.3 metallide reageerimine veega Metalli reageerimisel veega on redutseerijaks metall ja oksüdeerijals vesi. Metallid, mis asuvad pingereas vesinikust vasakul, tõrjuvad hapete lahustest välja vesiniku. Tavatingimustes reageerivad aktiivselt veega ainult leelis- ja leelismuldmetallid ( vähesel määral ka magneesium), tõrjudes veest välja vesiniku. Saadusena tekib metalli hüdroksiid (leelis). 2Na (t) + 2H2O (v) 2NaOH (l) + H2 (g) Ca (t) + 2H2O (v) Ca(OH)2 (l) + H2 (g) Keskmise aktiivsusega metallid (AL-Fe) reageerivad kuumutamisel veeauruga, tõrjudes välja vesinikku. Seejuures tekib metalli oksiid. Zn (t) + H2O (g) t° ZnO (t) + H2 (g) 3Fe (t) + 4H2O (g) t° Fe3O4 (t) + 4H2 (g) Rauast vähem aktiivsed metallid (pingereas rauast paremal) veega ei reageeri. Cu + H2O ei reag
Keemia aluste praktikum I Hüdrolüüs Juhendaja: Erika Jüriado Nimi: Henry Kaasik Kuupäev: 1. Soolalahuste pH Määran universaalindikaatorpaberiga erinevate soolalahuste pH Ammooniumkloriidi pH≈6,5 NH4Cl NH4+ + Cl- NH4+ + H2O NH3*H2O + H+ Alumiiniumsulfaadi pH≈1,0 Al2(SO4)3 2Al3+ + 3SO42- Al3+ + H2O Al(OH)2+ + H+ Naatriumkarbonaadi pH≈11 Na2CO3 2Na+ + CO32- CO32- + H2O HCO3- + OH- Kaaliumnitraadi pH≈7 Hüdrolüüsi ei toimu, kuna tegu on tugeva aluse ja happe soolaga, mis on tekkinud neutralisatsioonireaktsioonil, mis pole pöörduv. Alumiiniumsulfaadi ja ammooniumkloriidi hüdrolüüsil tekivad H+ ioonid, mis muudavad keskkonna happeliseks. Alumiiniumsulfaat võib mingil määral edasi hüdrolüüsuda, mis põhjendab ka tema madalama pH. Naatriumkarbonaadi puhul tekib hüdrolüüsil hüdroksiidioon...
KT elektrolüüdid 1. Ioonideks lagunemine e. dissotsiatsioon ainult vees lahustuvad ained! 1) Hapete jagunemine ioonideks: HCl -> H+ + Cl- (õigem: HCl + H2O -> H3O+ + Cl-) Happed, milles on rohkem vesinikke, jagunevad ioonideks astmeliselt: H2SO4 -> H+ + HSO4- = I aste HSO4- <-> H+ + SO42- = II aste 2) Soolade jagunemine ioonideks toimub ühes astmes: NaCl -> Na + + Cl- või Na2SO4 -> 2Na+ + SO42- või Na3PO4 -> 3Na+ + PO43- + 2- Cu2SO4 -> 2Cu + SO4 3) Aluste jagunemine ioonideks: NaOH -> Na+ + OH- Toimub astmeliselt, kui OH rühmi on rohkem: Ba(OH) 2 -> BaOH+ + OH- = I aste BaOH+ -> Ba2+ + OH- = II aste 2. Soolalahuse pH, keskkond, indikaatori värv Vees lahustuvad: tugevad alused: IA(Li alla) ja IIA(Ca alla) ja tugevad happed: HCl, HBr, HI, HNO 3, H2SO4 Tugevam aine määrab keskkonna: NaCl (mõlemad tugevad) => nautraalne keskkond pH=7 Na2SO3 (T(ugev) ja N(õrk)) => aluseline pH>7 ZnBr2...
1.Mittemetalliliste omaduste, aatomiraadiuse, elektronegatiivsuse muutumine perioodis ja rühmas. (Õ204) Mittemetallilised omadused tugevnevad perioodides vasakult paremale ja rühmaes alt üles, elektronegatiivsus kasvab ning aatomiraadius väheneb. 2. Mittemetallid kui oksüdeerijad või kui redutseerijad millega reageerivad, osata tuua ise näide või lõpetada reaktsioonivõrrandit. (Õ204) metalli ja endast vähem aktiivsemate mittemetallidega (on oksüdeerijad=oa. Väheneb) endast aktiivsemate metallidega (on redutseerijad=oa. Suureneb) 3. Maksimaalse ja minimaalse oksüdatsiooniastme määramine. (Õ205- 206) Maksimaalne on rühma nr Minimaalne on kui 8 lahutad maksimaalse oa. 4. Mittemetallide füüsikalised omadused. (Õ207) ei juhi elektrit, erineva värvusega, aatomite vahel kovalentsed sidemed. 5. Mis on molekulaarne ja mittemolekulaarne metall? Osata tuua näiteid. (Õ207) Molekulaarne metall- mida suuremad molekulide mõõtmed, seda tugevamad m...
MÕISTED: aluminotermia-lihtaine(enamasti metallide) saamine ühenditest alumiiniumiga redutseerimise teel elektrolüüs-elektsivoolu läbijuhtimisel lahustest või sulatatud elektrolüüdist elektroodidel kulgev redokreaktsioon karbotermia-metalli redutseerimine maagist süsiniku või süsinikoksiidi abil kõrgel temperatuuril keemiline vooluallikas-saade, milles keemilises reaktsioonis vabanev energia muudetakse vahetult elektrienergiaks. korrosioon- metalli hävimine(oksüdeerumine) keskkonna toimel oksüdeerija-aine, mille osakesed liidavad elektrone(ise redutseerudes) oksüdeerumine-elektronide loovutamine redoksreaktsioonis;sellele vastab elemendi oksüdatsiooniastme suurenemine redutseerija-aine, mille osakesed loovutavad elektrone(ise oksüdeerudes) redutseerumine-elektronide liitmine redoksreaktsioonis;sellele vastab elemendi oksüdatsiooniastme vähenemine sulam-mitmest metallist või metallist ja mittemetallist koosnev metalliliste omadustega ...
Oksiidid: Oksiidid koosnavad kahest elemendist, millest üks on hapnik. CaO- põletatud lubi, kustutamata lubi; CO2- süsihappegaas, CO- vingugaas 2 KNO3= 2 KNO2 + O2 2 Zn(NO3)2 = 2 ZnO+ 4 NO2 + O2 Alused: Alused koosnevad metallioonist ja hüdroksiidioonist. Alused on ained, mis liidavad prootoni (H +). Vees lahustuvad alused e. LEELISED: NaOH, KOH, Ba(OH)2 Amfoteersed alused: Al(OH)3, Zn(OH)2, Fe(OH)3, Cr(OH)3 Vees lahustumatud alused tabelis NaOH- seebikivi, sööbenaatrium; Ca(OH)2- kustutatud lubi Happed: Happed on ained, mis loovutavad prootoni (H+). Tugevad HNO3, H2SO4, HCl, HBr, HI Nõrgad H2S, H2CO3 2HCl + Mg(OH)2 = MgCl2 + 2H2O 2HCl + MgO = MgCl2 + H2O 2HCl + Mg = MgCl2 + H2 2HCl + Na2S = 2NaCl + H2S Soolad: Soolad koosnevad metallioonist ja happejääkioonist Vees lahustuvad: kõik N, Na- soola. Kõik nitraadid Vees lahustumatud tabelis 2Na + 2H2O = 2NaOH + H2 2NaOH + ZnCL2 = Zn(OH)2 + 2NaCl NaCl keedusool;CaCO3 lubjakivi, marmor...
C-C11 Vedelikud C12-C20 Tardunud rasvataolised C21-Cn Tahked Lahustuvus ·Sarnane lahustub sarnases Hüdrofoobsed ained lahustuvad hüdrofoobsetes lahustites (bensiin) Hüdrofiilsed ained lahustuvad hüdrofiilsetes lahustites (vesi) Alkoholide keemilised omadused · Täielik oksüdeerumine (põlemine) CH3CH2OH + 3O2 2CO2 + 3H2O · Osaline oksüdeerumine (Cu-katalüsaatoràaldehüüd) 2CH3CH2OH + O2 2CH3CHO + 2H2O · Reageerimine leelismetallidega (à alkoholaat) 2CH3CH2OH + 2Na 2CH3CH2ONa+H2 · Dehüdraatimine 2C2H5OH H2O + C2H5OC2H5 (eeter) CH3CH2OH H2O + CH2=CH2 (alkeen) Tähtsam esindajad CH3OH-metanaal->sipelghape C2H5OH-etanaal->äädikhape->CO2+H2O CH2- CH2 A| | Jahutusvedelik (tosool) OH OH CH2-CH-CH2 A| | | Propaantriool- glütserool (kreemid,lõhkeainete valmistamine) OH OH OH Puskariõli- etanooli käärimisel tekkinud destillatsiooni jääk EETRID Eetrid- orgaanilised ühendid, kus hapniku aatomiga on seotud süsivesinik rühmad
mittemetallidega kuumutamisel, sealjuures moodustuvad nn binaarsed ühendid, mille nime lõpus on alati -iid. Aktiivsemate mittemetallidega (Cl) reageerivad kõik metallid, hapniku ja väävliga ei reageeri mõned metallid (pingerea lõpus), neid nim väärismetallideks. Metallide reageerimisel mittemetallidega metall oksüdeerub ja mittemetall redutseerub. Mg+O2 => 2MgO Reageerimine veega: aktiivsed metallid (Li-Mg) reageerivad (vedela) veega; tekivad hüdroksiid ja H2: 2Na + 2H2O 2NaOH + H2 . keskmise aktiivsusega metallid (Al-Fe) reageerivad veeauruga (kõrgel temp.); tekivad oksiid ja H2: Zn + H2O ZnO +H2 . Väheaktiivsed metallid Ni-Au ei reageeri veega. Hapetega: Pingereas H2-st vasakul olevad metallid reageerivad lahj.hapetega oksüdeerijaks on H+-ioon eraldub H2 : Zn + 2HCl ZnCl2+ H2. Pingereas H2-st paremal olevad metallid ei reageeri lahj.hapetega. HNO3 ja konts. H2SO4 reageerimisel metallidega ei teki kunagi H2. Tekivad sool, vesi ja happeainioonid
Kordamisküsimused 1.Selgita mõisted. Redutseerija-loovutab elektrone. Oksüdeerija-redoksreaktsiooni käigus liidab endaga elektrone. Oksüdeerumine-aine loovutab elektrone ehk oksüdeerub. Redutseerimine-elektronide liitmisprotsess Korrosioon-metallide hävimine ümbritseva keskkonna toimel. Aluminotermia-oksiidist vaba metalli saamine alumiiniumi- ja oksiidipulbri segu süütamise teel. Akumulaator-aku, energia salvestamise seade Karbotermia-kõrgel temperatuuril metalli redutseerimine maagist süsiniku või süsinikoksiidi abil. Särdamine-metalliühendi üleviimine oksiidiks kuumutamisel õhuhapniku juuresolekul Keemiline vooluallikas-elektrokeemilises reaktsioonis vabanev energia muundub vahetult elektrienergiaks. Maagi rikastamine-maak vabastatakse kõrvalainetest kasutades füüsikaliste omaduste erinevust. 2.Võrrelge keemilise ja elektrokeemilise korrosiooni toimumise tingimusi. Keemiline- kuiva...
Vesinik Vesinik on keemiline element järjenumbriga 1. Ta on lihtsaima aatomiehitusega ning väikseima aatommassiga element. Keemiliste elementide perioodilisuse süsteemis kuulub ta 1. perioodi ja s-blokki. Kuigi vesinik paigutatakse tavaliselt I rühma, ei ole tema koht perioodilisussüsteemis üheselt määratav , sest ta on elementide seas erandlikul kohal. Mõnikord paigutatakse ta VII rühma, mõnikord mitte ühessegi rühma. Seega tema oksüdatsiooniaste võib olla -I, 0 või +I. Vesinik on kõige väiksema aatommassiga element; kõige sagedasema isotoobi prootiumi aatom koosneb ainult ühest prootonist ja ühest elektronist. Vesiniku aatommass on 1,00794±0,00007 g·mol-1. I rühma arvatakse vesinik sellepärast, et tal on üks valentselektron. Tal on leelismetallidega sarnane aatomispekter. Nagu leelismetallid, nii ka vesinik annab vesilahustes hüdrateeritud ühekordse positiivse elektrilaenguga iooni. Vesiniku vaba ioon on aga prooton, mi...
Karbonüülühendite liigitamine Aldehüüdide nomenklatuur ·Aldehüüdide nimetuse lõppliide on aal. ·Aldehüüdrühma süsinik võetakse tüviühendi süsinike nummerdamisel esimeseks. Ketoonide nomenklatuur ·Asendusnomenklatuuri korral on ketoonide nimetuse lõppliide oon, mille ette pannakse ketorühma süsiniku kohanumber. ·Funktsionaalnomenklatuuri korral kirjutatakse nimetusse mõlemad alküülrühmad ja lisatakse sõna ketoon. CH -CO-CH propanoon e. dimetüülketoon 3 3 CH CH CH COCH pentaan-2-oon e. metüülpropüülketoon 3 2 2 3 Ketoonide omadused · Kergesti lenduvad vedelikud · Vees lahustuvad · Narkootilise toimega · Kujundavad toiduainete lõhnabuketti Aldehüüdide redoksomadused ·Oksüdeerumine (ketoonidega ei toimu) CH CHO+Ag O®CH COOH+2Ag (hõbepeeglireaktsioon) 3 2 3 CH CHO+2CuO®CH COOH+Cu O (must à punane) 3 3 2 ·...
delivery of conscious yet raw lyrics. In his early days in the music business, Johnson worked as a hype man for underground rap and soul artists such as Slum Village, Steve Spacek, Platinum Pied Pipers, and Emanon. Some of the earliest tracks by Blu can be found on the 2003 mixtape Bruised Brothers, done with fellow L.A. emcee Blacc also known as Jac Spade. Spade is also a producer and has worked with the likes of Planet Asia and Chali 2na. Blu signed to L.A. independent label Sound in Color in 2004, choosing the label ahead of other big name companies such as Interscope Records and Death Row Records. After Blu was introduced to Los Angeles based producer Exile by Aloe Blacc, Blu released his debut album Below the Heavens in August 2007. New York weekly newspaper The Village Voice called the album "one of the most thoughtful indie-rap releases in some time". The rapper is currently working on several projects, one of
KLOOR - CL MIINA HÄRMA GÜMNAASIUM ÜLDISELOOMUSTUS · VIIA rühma element, 3. periood · Järjenumber 17, aatommass 35,453 · Prootonite ja elektronide arv 17, neutroneid 18 · O.a. ühendites I kuni VII · Aktiivne mittemetall ja keemilstelt omadustelt halogeen · Lihtainena koosneb 2 aatomilistest molekulidest (Cl2), kus on mittepolaarne kovalentne side · Elektronskeem Cl:+17I 2)8)7) OMADUSED · Raske rohekaskollane, terava, lämmatava lõhnaga gaas, mis on väga mürgine kõige elusa suhtes. · Õhust raskem (2,5 korda) · Sulamistemp. -100,98°C · Keemistemp. 34,6°C · Reageerib kergesti peaaegu kõikide keemiliste elementidega, v.a. väärisgaasidega. · Reageerimisel teiste ainetega eraldub soojust ja valgust. KEEMILISED OMADUSED 1) Lahustub vees vähe (Cl2 + H2O kloorivesi). Kloorivesi on baktereid hävitava toimega (kasut. vee puhastamisel) ja väga oksüdeerivate omadustega. 2) Vesinikug...
Alkoholid ja karboksüülhapped Alkoholid on sellised süsivesinikest tuletatud ühendid, milles üks või enam vesiniku aatomit on asendatud ühe või enam hüdroksüülrühmaga (-OH- rühmaga) Alkoholid ei muuda indikaatori värvi. R-alküülrühm (tuletatakse alkaani valemist lahustades ühe vesiniku aatomit) R-OH CH4 metaan ; CH3 metüül ; CH3OH metanool Metanool CH3Oh on suure süsinikuühendite rühm alkoholide kõige lihtsam esindaja. Metanooli võib saada metaani oksüdeerumisel: 2CH4 + O2 -> 2 CH3OH Metanool on värvitu, põletava maitsega mürgine vedelik, mis keeb temperatuuril 65C ja seguneb veega igasuguses vahekorras. Vähene kogus metanooli võib põhjustada raskeid tervisehädasid, sealhulgas pimedaks jäämist. Etanool CH3CH2OH on tähtsaim ja tuntuim alkohol. Etanooli saadakse glükoosi lagunemisel: C6H12O6 -> 2CH3CH2OH + 2CO2 Etanool on värvitu, põletava maitsega, lahustub hästi vees, keeb 78C juures, joomine te...