DDT diklorodifenüültrikloroetaan Ants Nokkur Metsandus I Sisukord Aine struktuur Ajalugu Paul Hermann Müller Omadused: keemilised/füüsikalised Kasutamine Kuidas tekib? Mõju inimestele Mõju keskkonnale DDT seos Eestiga Keelustamine Kasutamine tänapäeval Kasutatud materjalid Aine struktuur Ajalugu Sünteesiti esmakordselt 1874. Aastal 1939 avastas P.H.Müller insektitsiidse toime. Teise Maailmasõja ajal kasutati esimesena parasiitide tõrjeks. Paul Hermann Müller Sündis 1899 a. Klõpsake juhtslaidi teksti laadide redigee Sveitsi keemik. Teine tase Kolmas tase Neljas tase Õppis Baseli Ülikoolis. Viies tase Pälvis palju auhindu ja tunnustust. Suri 1...
Keemia Etanool ehk piiritus- CH3CH2OH Etanool on värvuseta, iseloomuliku lõhnaga, põletava, kõrvetava maitsega vedelik, mille sulamistemperatuur on -112 ºC ja keemistemperatuur 78 ºC. Etanool on veest kergem vedelik, sest tema tihedus on 0,794 g/cm³. Etanool lahustub veega igas vahekorras. Etanooli segunemisel veega esineb kontraktsioon. Kontraktsioon on nähtus, kus kahe aine segunemisel paigutuvad väiksemad aineosakesed suurematele vahele ära ning lõpptulemuseks on segu ruumala vähenemine ehk kokkutõmbumine. Näiteks 50 ml etanooli ja 50 ml vee segunemisel saadakse mitte 100 ml, aga 94 ml lahust. Etanool lahustab hästi orgaanilisi ühendeid. Metanool ehk puupiiritus- CH3OH on lihtsaim alkohol. Füüsikalistelt omadustelt on metanool kergesti lenduv värvitu tuleohtlik mürgine nõrga alkoholilõhnaga vedelik. Metanool põleb praktiliselt nähtamatu leegiga. Metanool on mürgine aine, võib põhjustada pimedus...
Keemia Etanool ehk piiritus- CH3CH2OH Etanool on värvuseta, iseloomuliku lõhnaga, põletava, kõrvetava maitsega vedelik, mille sulamistemperatuur on -112 ºC ja keemistemperatuur 78 ºC. Etanool on veest kergem vedelik, sest tema tihedus on 0,794 g/cm³. Etanool lahustub veega igas vahekorras. Etanooli segunemisel veega esineb kontraktsioon. Kontraktsioon on nähtus, kus kahe aine segunemisel paigutuvad väiksemad aineosakesed suurematele vahele ära ning lõpptulemuseks on segu ruumala vähenemine ehk kokkutõmbumine. Näiteks 50 ml etanooli ja 50 ml vee segunemisel saadakse mitte 100 ml, aga 94 ml lahust. Etanool lahustab hästi orgaanilisi ühendeid. Metanool ehk puupiiritus- CH3OH on lihtsaim alkohol. Füüsikalistelt omadustelt on metanool kergesti lenduv värvitu tuleohtlik mürgine nõrga alkoholilõhnaga vedelik. Metanool põleb praktiliselt nähtamatu leegiga. Metanool on mürgine aine, võib põhjustada pimedus...
II A RÜHMA METALLID: moodustavad veega reageerides leeliseid. loovutavad oma väliselektrone üsna kergelt ja on ühtlasi tugevateks redutseerijateks. Kusjuures, mida allpool metallid rühmas paikevad, seda kergemini nad neid loovutavad ja seda keemiliselt aktiivsemad nad on. Leekide värvused: Ca- telliskivi punane, Sr- punane, Ba- kollakasroheline Füüsikalised omadused: värvuselt hõbevalged või hallikasvalged. neil on kõrgemad sulamis- ja keemistemperatuurid, suurem tihedus ja kõvadus. pehmed, suhteliselt kergesti lõigatavad, hea elektri- ja soojusjuhtivusega. Keemilised omadused: keemiliselt aktiivsed, keemiline aktiivsus suureneb rühmas ülevalt alla. Hapnikuga reageerimisel süttivad metallid heleda leegiga põlema ja tekivad vastava metalli oksiidid. Reageerimisel happega tekib vastava metalli sool ja eraldub vesinik. Leelismuldmetallid reageerivad veega ning saadusteks on vastava metalli hüdroksiid ja vesinik BERÜLLIUM: on kergete, kor...
Tselluloos Referaat Koostaja: Juhendaja: Tselluloos Tselluloos on B ja D-glükopüranoosi jääkidest moodustunud polüsahhariid, elementaarlülide arv makromolekulis on 1000-6000. On kõige levinum orgaaniline aine maal üldse. Kõige puhtam looduslik tselluloos on puuvill (90%), okaspuu puidus (45%). Hüdrolüüsub väävelhappe juuresolekul ja moodustab glükoosi. Sellel reaktsioonil põhineb tselluloosi kasutamine lähteainena piirituse, alkoholi tootmisel. Erinevalt tärklisest reageerib tselluloos tugevate hapetega (näiteks lämmastikhappega) ja moodustab mono-, di-, trinitrotselluloosi. Tselluloos moodustab põhiosa taimsest biomassist, praktiliselt puhtal kujul siiski vaid puuvillakiududes. Tsellofaan saadakse looduslikust tselluloosist keemilise töötlemise tulemusena (lahustamine aluses ja saadud lahuse ekstrudeerimine läbi pilu happelisse keskkonda). Tselluloosi (vatt, paber) töötlemisel kontsentreeritud läm...
ETEEN ehk ETÜLEEN C2H4 Eteen on värvuseta, õhuga ligikaudu üheraskune, vees vähesel määral lahustuv, nõrgalt meeldiva lõhna ja narkootilise, uimastava toimega gaas. Looduslikult tekib eteeni vaid tühisel määral, näiteks puuviljades nende valmimisel. Tööstuslikult saadakse eteeni nafta töötlemisel (krakkimisel) moodustuvatest gaasidest ja teiste maavarade termilisel töötlemisel. Tänapäeval toodetakse eteeni kõrgel temperatuuril etaanist katalüsaatorite (Cr2O3) manulusel. Selle tulemusel moodustub etaanist eteen ja vesinik. Orgaanilise aine molekulidest vesiniku eraldamist nimetatakse dehüdrogeenimiseks. Cr2O3 CH3 - CH3 _ CH2=CH2 + H2 Laboratoorselt on võimalik eteeni saada etanooli soojendamisel kontsentreeritud väävelhappega. Konts. H2SO4 CH3CH2OH _ CH2=CH2 + H2O Eteen on tööstuslikult üks kõige rohkem toodetavam orgaa...
Süsinik Füüsikalised omadused: Süsinikul on kolm allotroopset(nähtus, kus samal keemilisel elemendil on mitu lihtainet) teisendit: teemant, grafiit, fullereen. Teemant: värvitu, lõhnatu, lahustumatu, halb elektrijuht, hea soojusjuht, kõige kõvem looduslik mineraal, sulamistemperatuur üle 4000kraadi Grafiit: hallikas-must, lõhnatu, poleeritav, rasvase pinnaga, sulamistemperatuur 3750kraadi, elektri pooljuht, halb soojusjuht, kihilise ehitusega Fullereen: C60 molekulaarteisend, must pulber mis leiti tahmas, ei juhi elektrit. Keemilised omadused: *Põleb C+O2 > CO2 süsihappegaas 2C+O2 > 2CO vingugaas *Reageerib metallioksiidiga CuO+C > Cu+CO *Reageerib vesinikuga C+2H2 > CH4 *H2O-aur C+H2O > CO+H2 Kasutamine: *Teemantit: ehtetööstuses ja tehnoloogias, lõiketeradel *Sütt: kütusena (kivisöe, koksina) *Grafiit: elektroodina, kirjutusvahendina *Aktiivsütt: söetablett=adsorbent, söefilter Adsorbent-seob pinnaga Absorbent-seob sisse CO ...
Aatomnumber: 19 Aatommass: 39,098 Klassifikatsioon: leelismetallid, s-elemendid Aatomi ehitus: · Elektronvalem: 1s2 2s2p6 3s2p6 4s1 · Elektronskeem: +19|2)8)8)1) · Elektronite arv: 19 · Neutronite arv: 20 · Prootonite arv: 19 · Oksüdatsiooniast(m)e(d) ühendites: 0, I · Kristalli struktuur: ruumikeskne kuubiline Füüsikalised omadused: · Aatommass: 39,098 · Sulamistemperatuur: 63,25 °C · Keemistemperatuur: 759,9 °C · Tihedus: 0,862 g/cm3 · Värvus: hõbevalge · Agregaatolek toatemperatuuril: tahke · Kõvadus Mohsi järgi: 0,4 · Isotoobid: Nukliid Levimus (%) Mass Poolestusaeg 39 K 93,22 38,9637 - 40 K 0,118 39,974 1,28 · 109 aastat 41 K 6,77 40,9618 ...
Karboksüülhapped- on orgaanilised ained KH keemilised omadused+võrrandid mis sisaldavad karboksüülrühma R-COOH 1.karboksüülhapped on happed sest Butlerovi struktuur 1. Neljavalentne eraldavad lahusesse vesinik ioone annab neli sidet CH3COOH--CH3COO+H 2. igal ainel on kindel koostis ja struktuur 2.Annavad reaktsiooni indikaatoriga (aine ehitus, sidemed ja aatomite paigutus) metüüloranz- punane, lakmus-roosa, a)kvalitatiivne koostis näitab, mis universaalindikaator- punane elementidest aine koosneb 3.CH3COOH+Zn=(CH#COO)2Zn+H2 b)kvantitatiivne koostis näitab aatomite HCOOH+Mg=(HCOO)2Mg+H2 arvu 4. aluselise oksiidiga 3.aine omadused sõltuvad aine koostisest CH3COOH+CaO=(CH3COO)2Ca+H2O ja struktuurist 5. alusega 4. aatomid avaldavad molekulis üksteisele CH3COOH+...
SOOLAD Soolad koosnevad metallioonist ja happejääkioonist Soolade liigitus lahustuvuse järgi · Vees lahustuvad soolad: Kõik K, Na- soolad, kõik nitraadid ( vt. lahustuvuse tabelit) · Vees lahustumatud soolad: BaSO4; AgCl jt.(vt. lahustuvuse tabelit) Soolade liigitus koostise järgi · Lihtsoolad: NaCl; Na2SO4 Na3PO4 = 3Na+ + PO4-3 · Vesiniksoolad NaHPO4 = 2Na+ + HPO4-2 NaH2PO4 = Na+ + H2PO4- Anna nimetus sooladele: · LiCl Al2(SO4)3 · Na2SO3 BaCl2 · FeSO4 Na2SiO3 · KBr Fe2(SO4)3 · Na3PO4 AgNO3 · CuSO4 CrCl3 · NaF Na2S · AlI3 CaCO3 · Ba(NO3)2 Mg3(PO4)2 · Ca(H2PO4)2 CaHPO4 Soolade keemilised omadused 1)sool+METALL =uus sool + vähemaktiivne metall (reageeriv sool peab olema vees lahustuv) CuSO4 + Fe = FeSO4 + Cu (vt.pin...
1. Millised väited on õiged, lähtudes joonisel toodud faasidiagra Possible Answers A. 4 % süsinikusisaldusega malmi faasiline koostis 1000 C B. 0.3 % teras on 1300 C juures sulanud C. 4 % süsinikusisaldusega malm on 1300 C juures tahkes D. 3 % süsiniku sisaldusega malmis on 1100C juures lahus 2. Milline on terase X12CrNi18-10 keemiline koostis? Possible Answers A. 0,12%C; 18%Cr; 10%Ni B. 1,2%C; 18%Cr; 10%Ni C. 0,12%C; 1,8%Cr; 1,0%Ni D. 1,2%C; 18%Cr; 1,0%Ni 3. Millised väited on õiged tööriistateraste kohta? Possible Answers A. Tööriistateraseid kasutatakse termotöödeldult õigele kõv B. Tööriistaterastest valmistatakse stantse ja survevaluvorm C. Tööriistateraseid kasutatakse ehituskonstruktsioonides D. Tööriistateraseid ei termotöödelda 4. Milli...
Ioonireaktsioonid (vesi)lahustes Põhireegel: Kokku lähevad ainult positiivne ioon negatiivsega. Reaktsioon kulgeb juhul, kui mõni ioonidest lahkub lahusest: Tekib nõrk elektrolüüt ja enamus tema koostisse kuuluvatest ioonidest lahkub lahusest molekulidena ( vesi, mõni nõrk hape) 1. Tekib gaasiline aine, mis lahusest minema lendab. 2. ( leeliste toimel: NH3 ja hapete toimel:CO2, SO2 , H2S). 3. Tekib vees lahustumatu aine (sade) ja vastavad ioonid lahkuvad lahusest. 4. Kui vähemalt üks tingimustest pole täidetud - reaktsioon ei kulge. 5. Tekib nõrk elektrolüüt ja enamus tema koostisse kuuluvatest ioonidest lahkub lahusest molekulidena ( vesi, mõni nõrk hape). Kontrolli, kas 1 lähteainetest on hape Jah - kirjuta võrrandi parem pool Ei - Kontrolli, kas mõlemad lähteained lahustuvad vees Ei , ...
NAATRIUMKLORIID LOODUSES, TOORAINE TÖÖSTUSEL, VAJALIK INIMESELE Naatriumkloriid ehk keedusool ehk sool on keemiline aine valemiga NaCl. Soola põhiliseks koostis osaks on naatriumkloriid, naatriumkloriidi sisaldus soolas oleneb puhtusastmest. Puhas sool sisaldab 40% naatriumi ja 60% kloori. Sool on maakeral väga laialt levinud, seda leidub kõikidel mandritel v.a. Antarktikas. Esimesed teada olevad andmed soola tootmisest on umbes 4000a. eKr kui egiptlased, roomlased ja kreeklased soola tootsid. Esimesena hakkasid soola merest korjama foiniiklased. Naatriumkloriidi leidub maakoores mineraal haliidina, soola leidub lahustunud kujul merevees, sooljärvedes ja iidsete veekogude põhjas. Soola toodetakse kaevandustes ning looduslikku vett külmutades ja aurutades. Kõige laiemalt tuntakse naatriumkloriidi kui söögisoola, mida kasutatakse toiduvalmistamisel maitseainena ning konserveerimisel säilitusainena. Keedusool on vees ...
1. Mittemetallid Mittemetallid on suure elektronegatiivsusega elemendid, mis keemilistes reaktsioonides peamiselt liidavad elektrone. Perioodilisustabelis asuvad need pea-alarühmades ülal paremal, nende hulgas ka vesinik, mis asub tavaliselt esimese elemendina ülal vasakul. Mittemetallide hulka kuuluvad ka väärisgaasid, kuigi need ei liida elektrone, sest nende väline elektronkiht on maksimaalselt täitunud. Keemilistes reaktsioonides moodustavad nad teiste mittemetallidega tavaliselt kovalentse sideme, metallidega tavaliselt ioonilise sideme. Väävel on üks esimesi mittemetalle, mida inimene kasutama ja tundma on õppinud. 2. Väävel 2.1 Väävli leidumine looduses Looduses esineb väävel nii ehedal kujul kui ka ühendites. Ühendites esineb väävel enamasti sulfiididena (FeS2, püriit) või sulfaatidena (CaSO4ˑ2H2O, kips). Lihtainena esineb väävel peamiselt kaheksa-aatomilise molekulina ehk rombilise väävlina- S8. Kuna väävlit l...
Glkoos ehk viinamarjasuhkur-on monosahhariid,mis kuulub disahhariidide sahharoosi ja laktoosi koostisse. Fruktoos-on ks monosahhariididest. Trklis-on taimedes olev polsahhariid. Tselluloos-polsahhariid. Anioon-neg. laenguga ioon. Katioon-pos. laenguga ioon. Elektron-neg. laenguga aatomi koostisosa. Prooton-pos. laenguga tuumaosake. Hape-aine,mille vesilahuses on lekaalus vesinikioonid vrreldes hdroksiidioonidega. Oksiid-elemendi hend laenguga. Eksotermiline reaktsioon-on keemiline reaktsioon,mille kigus eraldub soojust. Endotermiline reaktsioon-on keemiline reaktsioon,mille kigus neeldub soojust. Ensmid- on bioloogilised katalsaatorid. Katalsaator-on aine,mis muudab reaktsiooni kiirust,kuid vabaneb prast reaktsiooni lppu endises koguses. Indeks-on aine valemis esinev number,mis nitab antud elemendi aatomite arvu valemis. Sulam-on kahe vi enama metalli vi metalli ja mittemetalli kokku sulatamisel saadud aine. Korrosioon-metallide hvinemi...
Elektrolüüdid – ained mille vesilahused sisaldavad ioone autoakud – väävelhape NaCl Äädikas Orgaanilised ained vesi Tugevad Nõrgad Mitte Kõik soolad Nõrgad happed Tugevad happed – Hcl, HI, Hbr, Nõrgad alused HNO3, H2SO4 Tugevad alused, leelised ja Ca'st alla poole Aine lagunemist ioonideks nimetatakse elektrolüütiliseks dissotsiatsiooniks. HCl + H20 = H3O + Cl hüdrooninumioon Hcl – H + Cl 1. Sideme lõhkumine, jahtumine 2. Hüdraatumine (tekib uus side, energia eraldub), soojenemine Kui aineid lahustada vees siis lahus soojeneb või jahtub. CuSO4 x 5H2O kristallvesi – kuumutades lendab minema, õhu käes tuleb tagasi NaCl esineb ilma kristallveeta Dissotsiatsioonivõrrandid 1. Soolad +2 - Mg(NO3)2 Mg + 2NO3 Ühte pidi nool tule...
Plastiidid-membraanidest koosnev taimerakule omane organell(kloro,kromo,leuko) Vakuoolid-membraaniga ümbritsetud põiekesed,sisaldavad varu ja jääkaineid Lipiidid-org ühendite rühm,ei lahustu vees(rasv,õli,vaha) Rakukest-rakumembraanist väljapoole jääv ümbris,koosneb tselluloosist v kitiinist Tselluloos-taimne süsivesik,taimerakkude seinte kiudaine Poorid-nendest läbivad vesi,gaasid ja madalmolekulaarsed ühendid Biopolümeer-organismides moodustuv polümeer(valgud,nukleiinhapped) Ligniin-puidu põhistruktuuri kuuluv jäikust andev looduslik polümeer, puitaine Pektiin-taime rakukestades, eriti puuviljades ja marjades sisalduv polüsahhariid Difusioon-vahetus kokkupuutes olevate ainete aeglane segunemine aineosakeste soojusliikumise tõttu Osmoos-lahusti imbumine poolläbilaskva vaheseina kaudu lahusesse, kus lahustunud aine kontsentratsioon on suurem Kattekude-taime välispinda kattev ning sisemisi kudesid kaitsev kude Ksüleem- taime juhtkimbu pu...
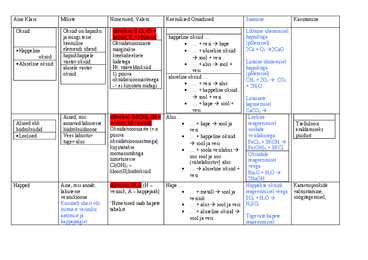
Aine Klass Mõiste Nimetused, Valem Keemilised Omadused Saamine Kasutamine Oksiid Oksiid on hapniku üldvalem: E2On (O = Lihtaine ühenemisel ja mingi teise hapnik, E = element) happeline oksiid ... hapnikuga keemilise Oksüdatsiooniaste · ... + vesi hape (põlemisel) · Happeline elemendi ühend märgitakse · ... + aluseline oksiid 2Ca + O2 2CaO oksiid hapnikhappele kreekakeelsete sool + vesi · Aluseline oksiid vastav oksiid liidetega Liitaine ühinemisel · ... + alus sool ...
Fruktoos Pamela Sageus LM14 Nimetatakse ka levuloos ehk ka puuviljasuhkur. See on üks monosahhariididest (lihtsuhkur) ning fruktoos on glükoosi isomeeriks. Fruktoos, nagu ka teised monosahhariidid, imendub seedimise käigus otse vereringesse. Kõige magusam suhkrutest ongi just fruktoos, selle avastas prantsuse keemik Augustin-Pierre Dubrunfaut 1847.aastal. Kuna Augustin avastas esimest korda fruktoosi puuviljadest, siis sellest on ka tekkinud nimetus „puuviljasuhkur”. Puhas, kuiv fruktoos on kristalne tahke aine, valge värvusega, magus ja lõhnatu. Ta on lisaks kõige magusamale suhkrule ka kõige paremini vees lahustuv. Seda sisaldub palju mees, puuviljades, õites, marjades ja enamikus juurviljades. Taimedes võib fruktoos esineda nii monosahhariidina kui ka disahhariidi koostises. Viimasel juhul on see sahharoosi (glükoosi...
1. I A RÜHMA METALLID 1.1 I A rühma metallide üldiseloomustus I A rühma metallideks on liitium, naatrium, kaalium, rubiidium, tseesium ja frantsium. I A rühma metalle nimetatakse ka leelismetallideks. Ajalooliselt tuleneb sõna leelismetall sellest, et nende metallide hüdroksiide tunti juba ammu ja neid nimetati leelisteks. Tänapäevane selgitus võiks olla lihtsalt selline, et nende metallide veega reageerimisel tekivad leelised. Leelismetallid on kõige metalsemad elemendid. Aatomi ehituselt kuuluvad nad s-elementide hulka, kuna nende aatomite välisel orbitaalil on üks elekt- 1 ron. Sellest tulenevalt on kõikide leelismetallide aatomite väliskihi elektronvalemiks ns ja oksüdatsiooniastmeks ühendis +I. Kuna leelismetallidel on väliskihis ainult üks elektron, siis seetõttu nad loovutavad selle ...
Sisukord 1 Mis on halogeenid? ............................................................................................................................... 3 2 Halogeenide omadused ........................................................................................................................ 4 3 Halogeenide kasutamise valdkonnad ................................................................................................... 5 4 Halogeenid looduses sealhulgas elusorganismis ehk BIOTOIME ........................................................ 6 1 Mis on halogeenid? Fluor, kloor, broom, jood ja astaat on halogeenid, mis on VII A rühma elemendid. Halogeenid kuuluvad kõige aktiivsemate mittemetallide hulka, kusjuures nende keemiline aktiivsus suureneb rühmas alt üles. Suure keemilise aktiivsuse tõttu leidub neid looduses vad ühenditena. Sõna halogeen tuleneb kreeka keelsest (`hals' meresool; `gen' tekitama...
TALLINNA TEENINDUSKOOL T11HT Kohv Referaat Tallinn 2010 Sisukord Sissejuhatus 3 Kohvi ajalugu 4 Taimest 5 Kohvi kasvatuspiirkonnad 6 Kohvi liigid 7 Kohvi valmistamisviisid 8- 9 Kokkuvõte 10 Kasutatud kirjandus 11 Sissejuhatus Kohvi tähtsust maailma majanduses ei saa üle hinnata. See on üks väärtuslikumaid esmatarbekaupu maailmakaubanduses, jäädes paljude aastate vältel arengumaade kaubavahetusartiklina alla ainult naftale. Selle kasvatamine, töötlemine, turusta...
Akrüülmaal Referaat Sisukord Sissejuhatus 1. Akrüülvärvid 1.2 Akrüülvärvi omadused 2. Akrüülmaali aluspind 2.2 Pindade ettevalmistamine 2.3 Haakuvuse kontrollimine 3. Akrüülmaali kuivamistingimused 3.2 Vahendite puhastamine ja värvi eemaldamine Kokkuvõte Kasutatud allikad 1. Akrüülvärvid Vesivärvide perekonna kõige noorem võsu on akrüülvärv. Kuna jutt on vesivärvist, siis loomulikult on akrüül vees lahustuv. Kuna jutt on noorimast vesivärvide seas, siis on akrüül oma loomuselt igati tänapäevane ja moodne. Nimelt on akrüül sünteetiline plastvärv ning tema eluiga sai alguse alles eelmise sajandi 60-ndail aastail. Akrüülvärvi toonid on eredad ja silmatorkavad ning tänu oma keemilisele koostisele on akrüül ka elastne, heade katteomadustega ning mittepleekiv. Akrüüli saab veega lahjendada, kuid ainult enne maalimist. Kui...
Pärnu Täiskasvanute Gümnaasium Vitamiin A Referaat Oliver Nahksep 11 AÕ 18 Jaanuar 2010 Sisukord Avastuslugu............................................................................................................................. 6 Saamine ja depood................................................................................................................. 7 Defitsiit.................................................................................................................................... 9 Kokkuvõte............................................................................................................................. 10 Kasutatud kirjandus............................................................................................................... 11 Kasutatud pildimaterjal...................
Halogeenid 1. Halogeenide üldiseloomustus ja keemilised omadused Halogeenid on VII A rühma elemendid ja nendeks on fluor, kloor, broom, jood ja astaat. Halogeenid kuuluvad kõige aktiivsemate mittemetallide hulka, kusjuures nende keemiline aktiivsus suureneb rühmas alt ülesse. Seda on võimalik tõestada ka katseliselt, kus aktiivsem halogeen tõrjub vähemaktiivsema halogeeni tema soolast välja. F2 + CaBr2 _ CaF2 + Br2 Cl2 + 2NaI _ 2NaCl + I2 Suure keemilise aktiivsuse tõttu leidub neid looduses vaid ühendite koosseisus. Halogeenid lihtainena koosnevad kaheaatomilistest molekulidest, mistõttu reaktsoonivõrrandites neid kirjutatakse alljärgnevalt: F2, Cl2, Br2 ja I2. Kuna nende molekulide vahel on suhteliselt nõrgad molekulidevahelised jõud, siis on halogeenidel suhteliselt madalad keemistemperatuurid. Fluor ja kloor on toatemperatuuril gaasid, broom on ainukene toatemperatuuril vedelas olekus olev m...
Mittemetallid Mittemetallide füüsikalised omadused: · Rabedad · Halvad elektrijuhid(v.a. grafiit) · Aatomvõre või molekulvõre · Vees lahustumatud · Agregootolek toatemp: 1. gaasiline(02,N2,H2,Cl2,F2+väärisgaasid) 2. vedelad( Br2) 3. tahked(C;P;S;J2;Si) Üldised keemilised omadused: · kõik mittemet. Reageerivad met-ga · Reageerivad O2 (S+O2SO2) · Reageerivad H2 (H2+F22HF) Vesinik H:+1|1) Füs omadused: · Värvitu · Lõhnatu · Õhust 14,5 korda kergem · Keemis temp. On -253C · Vees väga vähe lahustuv · Kõige kergem (väiksema tihedusega) gaas Keemilised omadused: · H2 põleb e. Reageerib O2-ga( 2H2+O22H2O) · H2 reageerib teiste mittemet.( H2+F22HF) · H2 reageerib vähe aktiivsete met. Oksiididega. Saamine: 1. elektrolüüs (2H2O2H2+O2) 2. met+hape (2HCl+MgMgCl2+H2) 3. tööstuses saadakse Metaani abil [CH4C(tahm)+2H2] Kasutamine: · kasutati õhupa...
S Ü S I V E S I K U MONOSAHHARIIDID e. MINOOSID SAHHARIIDI NIMETUS Glükoos/fruktoos Riboos VALEM C6H12O6 C5H10O5 LEIDUMINE 1)mesi 1)koeensüümid 2)veri, koed, rakkud 2)vitamiinid 3)viinamarjad, marjad 3)kõik organismid 4)maisisiirup 5)puuviljad, juurviljad 6)õienektar SAAMINE Glükoosi saadakse tärklise hüdrolüüsil mineraalhapete manulusel. Fruktoosi saa- dakse sahharoosi hüdro- lüüsil. KASUTAMINE Glükoosi kasutatakse ravi- mina, energiaallikana mitme- suguste haiguste ravil, ...
Lämmastik Lämmastik looduses,füüsikalised,füsioloogilised ja keemilised omadused Füüsikalised omadused Füüsikalised omadused: Ilma lõhna maitse ja värvuseta gaas. vees lahustub minimaalselt ja pole mürgine Õhus on teda 78% mahu järgi ja sealt teda ka toodetakse.Kuulub valkude, nukleiinhapete jmt koostisse. Mineraale eriti ei teata, ainus oluline on nn Chile salpeeter - NaNO 3 Laboris võib lämmastikku saada ammooniumnitriti lagundamisel. NH 4NO2 = N2 + 2H2O Oksüdatsiooniastmed, aatomi ja molekuli ehitus Oksüdatsiooniastmed: minimaalne -III ja maksimaalne V Aatomi ja molekuli ehitus: +7/ 2) 5) 1s22s22p3 seega on tal 3 paardumata elektroni ja molekulis seetõttu kolmikside : N ::: N : Tavatemperatuuril on lämmastik inertne,kuid kuumutamisel kolmikside (osaliselt)laguneb, tekivad . N :: N. ja lõpuks tekivad ka üksikud aatomid Paardumata elekt...
Anti-friis · Nimetus: Anti-friis · 1,2-etaandiool ehk etüleenglükool CAS number: 107-21-1, dinaartiumfosfaat CASnumber: 7558-79-4 · Koostis: Vesi, Etüleenglükool, korrosioonitõrjeaine: tolüültriasool, dinaatriumfosfaat · Omadused: Etüleenglükool- Ta on värvuseta ja lõhnatu magus siirupitaoline mürgine hügroskoopne (niiskustimav) vedelik. Kõrge keemispunkt, madal külmumispunkt, stabiilsus laial temperatuuride vahemikul ning kõrge erisoojus ja soojusjuhtivus. Lisaks on etüleenglükoolil ka madal viskoossus. Tolüültriasool- Tööstuses kasutatava tolüültriasooli ebameeldiv lõhn tuleneb tootmisel tekkivate kõrvalproduktide toluidiini isomeeride (orto-, meta- ja para-toluidiin) ja meta- diaminotolueeni ebapuhtusest. Need kõrvalproduktid on väga aktiivsed ja eritavad lenduvaid aromaatseid amiine, millest tulenebki ebameeldiv lõhn. Dinaatriumfosfaat- Valge, niiskustimav, v...
AINETE PÕHIKLASSID JA NENDE VAHELISE SEOSED . Oksiidid. *Oksiid-aine, mis koosneb kahest elemendist, millest üks on hapnik(o/a-II). -aluselised oksiidid (metall + hapnik) reageerivad hapetega. Tugevalt aluseliste oksiidide reageerimisel veega tekivad leelised ehk lahustuvad alused(tugevad alused). Nt. NaOH -happelised oksiidid(mittemetall + hapnik) reageerivad alustega. Happeliste oksiidide reageerimisel veega tekib enamasti hape. Nt. H2SO4. -amfoteersed oksiidid (Al2O3;Cr2O3;Fe2O3;ZnO) reageerivad nii aluste kui hapetega alustega reageerimisel tekivad kompleksühendid. Nt Na[Al(OH)4]. Amfoteersed oksiidid veega ei reageeri. -Neutraalsed oksiidid(CO;NO;N2O) on mittemetallioksiidid, mis veega reageerides hapet ei anna. Oksiidide peamised saamisvõimalused a) Vastavate lihtainete reageerimine hapnikuga = C + O2 = CO2 b) Suhteliselt ebapüsivate hapnikku sisaldavate ühendite lagundamine(kuumutamine). Alus=Oks...
Kohvipuu Liisi Palu 10B Kohvipuu välimus Kohvipuud on igihaljad lehtpuud või lehtpõõsad. Kohvipuul on rootsuga lihtlehed. Lehelaba on läikiv. Leheseis on vastak. Abilehed võivad olla suured kuni väikesed. Vili on algul roheline, küpsedes muutub kollaseks ja siis kui vili on täielikult valmis on ta tumepunane. Kasvutingimused kasvumaad asuvad troopilises keskmäestikus 1000- 2000 meetri kõrgusel. Kasvutingimuste suhtes on kohvipuu nõudlik. Vajab aastas sademeid 2200-2300 mm ning pidevaid plusskraade. Alla + 40C temperatuuri juure kohvipuud hukkuvad. Kohvipuu on üks varaseima viljakandvusega puid maailmas. Juba 1,5-aastaselt võivad nad esimest korda vilju kanda. Kohvipuu elab kuni 50-60 aastaseks. Aastas võib ta anda kuni kolm saaki, mis ühe täiskasvanud puu kohta on keskmiselt 3 kilogrammi toorube. Millistes riikides kasvatatakse? Kohvipuid kasvatatakse 50-60 riigis üle maailma, kus s...
Pelgulinna Gümnaasium Stella Altmets 8.ak. KAALIUM Referaat Tallinn 2016 1 Sisukord: 1. Kaalium ja selle elemendi avastamise ajalugu . . . . . . . . . . . . . . . . . . . . . . . . . . . .3 2. Levinumad ühendid . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 4 3. Elemendi kasutusalad ja toime inimkehas . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 4 4. Kasutatud kirjandus . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 6 2 Kaalium ja selle elemendi avastamis ajalugu Kaalium ehk ladinakeeles kalium ja tähisega K on keemiline element perioodilussüsteemi 1 rühmas ja järjekorranumbriga 19. Kaaliumi mass on 39,0983. Kaaliumi leidub looduslikul kujul vähe, valmistatakse teda tehislikult. Üks suuremaid leiukohti...
VÄÄVEL 2017 Väävel on aktiivne mittemetall 16 Keemiline sümbol: S (Sulfur) Järjenumber/aatomnumber: 16 Asub 3. perioodis (elektronkattes 3 kihti) S 32,064 6 8 2 VÄÄVEL Asub VIA rühmas (väliselektrone 6) Elektronskeem: S: +16|2)8)6) Pilt 1: Vääveli paiknemine perioodilidudtsbelis KEEMILISED OMADUSED Väävel lihtainena S on nii oksüdeerija, kui redutseerija Väävli kõige madalam oksüdatsiooniaste on II. See esineb metalliühendites (sulfiidid) ja vesinikühendis (divesiniksulfiid) Väävli kõige kõrgem oksüdatsiooniaste on + VI (sulfaadid, väävelhape...
Raud Robert Põldoja 6. B Tartu 2012 Raud ja omadused Raud (Ferrum) on keemiline element järjenumbriga 26. Raud asub Perioodilisussüsteemi VIII B rühmas ja 4. perioodis. Tal on neli stabiilset isotoopi massiarvudega 54, 56, 57 ja 58. Omadustelt on raud metall. Normaaltingimustel on raud tahke aine tihedusega 7,87 g/cm3. Raua sulamistemperatuur on 1539 Celsiuse kraadi. Raud esineb madalal rõhul nelja kristallmodifikatsioonina olenevalt temperatuurist. Raud looduses Raud on looduses laialt levinud element , olles sisalduselt maakoores neljandal kohal. Raud on ka kosmoses levinud element. Meie Päikesesüsteemi planeetidest on rauarikkamad Merkuur ja Marss. Lihtainena esineb rauda maailmaruumist Maale langenud meteoriitides, kuid ka mõningates magmakivimeis. Maa tuum koosneb metal...
Alused ehk hüdroksiidid On ühendid, mis koosnevad metalli ioonist ja hüdroksiid ioonist. Annab vesilahuses hüdroksiide. Üldised omadused *sööbiv toime *indikaatorite iseloomulik värvus aluselistes lahustes *reageerimine hapetega *reageerimine happeliste oksiididega. Hüdroksiid-mittemolekulaarne kristalne aine, mis annab dissotsieerumisel lahesesse metalli katioone ja hüdroksiiniioone. Leelis- vees lahustuv tugev aine nt NaOH. Vähemaktiivsete metallide hüdroksiid-nõrgad alused ja nad lahustuvad vees halvasti nt Cu[OH](2). Hüdroksiidide nimetused on analoogsed vastavate metallioksiidide nimedega. Nimi antakse nagu metallioksiididele. Nime lõpp on hüdroksiid. NaOH - naatriumhüdroksiid Fe(OH)3 - raud(III)hüdroksiid Fr(OH)2 - raud(II)hürdoksiid Alused jagunevad kahte gruppi vees lahustuvad ja vees lahustumatud. Vees lahustavaid nim. leelisteks. Leelise lahuseid saab kindlaks teha indikaatorite abil. Mitte lahustuvad hüdr. indikaatori värvust...
Lämmastik 1)Aatomi ja molekuli ehitus: N: +7| 2) 5) Lämmastiku järje- ehk aatomnumber on 7, ta kuulub perioodilisustabeli VA rühma elementide hulka, asudes 2. perioodis. Lämmastiku aatomis on 7 prootonit, 7 elektroni ja 7 neutronit. Lämmastiku aatomi väliskihis on viis elektroni ning lämmastiku aatomid võivad elektrone nii liita kui ka loovutada. Seetõttu on lämmastiku oksüdatsiooniaste ühendites 3 kuni +5. 2)Lihtaine omadused 2.1)Füüsikalised omadused: · terava lõhnaga · värvuseta · gaas · õhust ~2 korda kergem · vees väga hästi lahustuv · veeldub 33oC juures NB! 25% line lahus võib põhjustada hingamislihaste krampi ja silma sattudes pimedaks jäämise. 2.2)Keemilised omadused: Lämmastik on väga püsiv, sest molekulis on tal aatomite vahel tugev kolmikside NºN , mistõttu ta onkeemiliselt väheaktiivne.Lämmastik reageerib kõrgel temperatuuril, mil side ...
Vesinik Vesinik on keemiline element järjenumbriga 1. Ta on lihtsaima aatomiehitusega ning väikseima aatommassiga element. Keemiliste elementide perioodilisuse süsteemis kuulub ta 1. perioodi ja s-blokki. Kuigi vesinik paigutatakse tavaliselt I rühma, ei ole tema koht perioodilisussüsteemis üheselt määratav , sest ta on elementide seas erandlikul kohal. Mõnikord paigutatakse ta VII rühma, mõnikord mitte ühessegi rühma. Seega tema oksüdatsiooniaste võib olla -I, 0 või +I. Vesinik on kõige väiksema aatommassiga element; kõige sagedasema isotoobi prootiumi aatom koosneb ainult ühest prootonist ja ühest elektronist. Vesiniku aatommass on 1,00794±0,00007 g·mol-1. I rühma arvatakse vesinik sellepärast, et tal on üks valentselektron. Tal on leelismetallidega sarnane aatomispekter. Nagu leelismetallid, nii ka vesinik annab vesilahustes hüdrateeritud ühekordse positiivse elektrilaenguga iooni. Vesiniku vaba ioon on aga prooton, mi...
1. Mis on glükoosi lagundamise eesmärgiks? Energia saamine 2. Millest koosneb DNA nukleotiid(joonis)? Fosfaatrühm,desoksüriboos ja lämmastikalus 3. Selgitage mõisteid:nukleotiid,biheeliks,komplementaarsusprintsiip,biopolümeer nukleotiid-nukleiinhappe monomeer,mis on moodustunud lämmistikaluse,5-süsinikulise suhkru ja fosfaatrühma liitumisel. biheeliks-DNA molekul sekundaarstruktuur,mis moodustub vesiniksidemetega ühindatud kahe ahela keerdumisel. komplementaarsusprintsiip-kindlate lämmastikaluste paardumine nukleiinhapete(DNA&RNA)molekulidega,mis põhineb vesiniksidemete moodustumisel. biopolümeer-organismides moodustuv polümeer(valgud,nukleiinhapped jt.). 4. On teada üks lõik DNA-st,leidke selle vastas oleva teise DNA ahela nukleotiidiline järjestus A-T & C-G 5. Selgitage tärklise ja tselluloosi funktsioonide erinevust Tärklis on taimedes energeetilisel otstarbel,aga tselluloos on ehituslikul...
Vask (Cu) on keemiline element järjenumbriga 29. Tal on kaks stabiilset isotoopi massiarvudega 63 ja 65. Aatommass on 64. Omaduste poolest on vask metall. Normaaltingimustes on vase tihedus 8,9 g/cm³. Vask asub IB rühmas ning 4. perioodis. Tema sulamistemperatuur on 1083 °C. Vaske leidub looduses sülfiidsete ühenditena Cu 2S (vaskläik), CuFeS2 (malahhiit). Punaka värvusega, hästi sepistatav metall, hea soojus- ja elektrijuht. Kuivas õhus püsiv, niiskes kattub roheka paatinakihiga [Cu 2CO3(OH)2]. Suured vasemaagi maardlad asuvad Tðiilis, sh maailma suurim lahtine vasekaevandus – Chuquicamata karjäär. Vask ja tema ühendid on mürgised ! Vaske saadakse ja puhastatakse elektrolüütiliste meetoditega Kasutamine: energeetikaseadmed, elektrijuhtmed, soojusvahetid, müntide metall, Sulamid (pronksid): Cu – Sn tinapronks Cu – Si ränipronks Cu – Zn valgevask Lihtainete omadused Vask reageerib õhuga kõrgemal t°-l (~800°C) Vase ala...
Sahhariidid Sahhariidid e. süsivesikud elusorganismide tähtsad ehitusplokid: · RNA, DNA koostises · rakumembraanide koostises · rakukestade koostises · rakkudes energiavaruained Monosahhariidid · Monosahhariidid e. suhkrud koosnevad mitmest liitunud · C ja H aatomist · Lisaks OH rühmad ja karbonüülrühm · riboos ja desoksüriboos pentoos · glükoos ja galaktoos heksoosid Monosahhariidide mitmekesisus · lineaarsed ja tsüklilised vormid · optilised isomeerid · OH rühmade erinevad paigutused · erinev C aatomite arv · erinev karbonüülrühma paigutus · Saame väga palju erinevaid molekule: igaühel unikaalne struktuur ja funktsioon Polüsahhariidide tekkimine · Elusrakkudes toimub suhkrute polümeriseerumine ainult sp...
Vask (Cu) on keemiline element järjenumbriga 29. Tal on kaks stabiilset isotoopi massiarvudega 63 ja 65. Aatommass on 64. Omaduste poolest on vask metall. Normaaltingimustes on vase tihedus 8,9 g/cm³. Vask asub IB rühmas ning 4. perioodis. Tema sulamistemperatuur on 1083 °C. Vaske leidub looduses sülfiidsete ühenditena Cu2S (vaskläik), CuFeS2 (malahhiit). Punaka värvusega, hästi sepistatav metall, hea soojus- ja elektrijuht. Kuivas õhus püsiv, niiskes kattub roheka paatinakihiga [Cu2CO3(OH)2]. Suured vasemaagi maardlad asuvad Tiilis, sh maailma suurim lahtine vasekaevandus Chuquicamata karjäär. Vask ja tema ühendid on mürgised ! Vaske saadakse ja puhastatakse elektrolüütiliste meetoditega Kasutamine: energeetikaseadmed, elektrijuhtmed, soojusvahetid, müntide metall, Sulamid (pronksid): Cu Sn tinapronks Cu Si ränipronks Cu Zn valgevask Lihtainete omadused Vask reageerib õhuga kõrgemal t°-l (~800°C) Vase alarüh...
Minu keskkonnakaitsealased harjumused OSTMINE 1. Minu tarbimine päeva jooksul. Toit: kohuke, lahustuv kohv, kohupiim, mustikad, riis, lillkapsas, sampinjonid, oad Kodukeemia: Fairy, Cif Hügeenivahendid: deodorant, dussigeel, Transport: jalgratas Meelelahutus: teleka vaatamine 2. Asjadest mida tarbisin olid Eesti päritolu kohuke, kohupiim ja mustikad. 3. Kõige kaugemalt oli pärit riis. 4. Uuringupäeval ei pidanud toitu prügikasti viskama. VESI 1. Minu joogivesi tuled AS Tartu Veevärk ettevõttest. Kasutatava vee 1 m3 hind on 0,739 eurot. 2. Tartus juhitakse reovesi tarbija juurest läbi kanalisatsiooni ja tunnelkollektori reoveepuhastisse. Tartu reovett puhastab Ihaste puhastusjaam. Seal tõstetakse reovesi pumpadega maa peale ning algab reovee mehhaaniline puhastus. Puhastuse käigus eemaldatakse suuremad jää...
Aldoosid Mis on aldoos? Aldooson monosahhariid ehk lihtsuhkur, mis koosneb ainult ühest aldehüüdrühmast molekuli kohta. Aldoosi nimetatakse ka veel Karbonüül aldehüüdiks Aldoosi keemiline valem on Cn(H2O)n Aldooseon olemas 16 tükki, mis omakorda jagunevad veel erinevatesse monosahhariidide rühmadesse. Glükoaldehüüd Kõige väikseim olemasolev molekul, mis kuulub nii aldehüüdrühma kui ka hüdroksüülrühma. Süsiniku arvu tõttu kuulub ainukesena dioosi alla. Siiskiei ole see aine päris aldoos, kuna ainel puuduvad enamik suhkru omadusi, kuid siiski kuulub ta aldoosi perekonda. Glütseeraldehüüd On trioosne monosahhariid, valemiga C3H6O3 Kõige levinum ja lihtsaim aldoos. Magus, värvitu, kristalne aine. Mängib tähtsat rolli meie metabolismis, sünteesis ja biokeemias. Erütroos Tetroosne sahhariid, valemiga C4H8O4 Samuti on oluline metabolismis. Värvitu või kollane siirupi taolin...
Keemia: SÜSINIK, LIHTSAD SÜSINIKUÜHENDID SÜSINIK LIHTAINENA: Süsinik esineb lihtainena mitmes erinevas vormis: allotroobid (koosnevad mõlemad süsiniku aatomitest, erinevad on struktuur ja omadused) TEEMANT · iga süsinik seotud nelja naabersüsinikuga · elektrit ei juhi · kõrge sulamistemperatuuriga · väga kõva (klaasinoad, puuriotsad) · hea peegeldumisvõime (ehete valmistamine: briljandid) GRAFIIT · iga süsinik seotud kolme naabersüsinikuga; kihiline (pliiatsisüdamikud) · kõrge sulamistemperatuuriga (sulatustiiglite valmistamine) · metalse läikega, pehme (määrdeainete valmistamine) juhib elektrit (elektroodid) SÜSINIKU OKSÜDATSIOONIASTE Süsiniku aatomi elektronskeem: C: +6| 2)4) Süsinik võib reaktsioonides liita või loovutada elektrone: tema oksüdatsiooniaste võib olla vahemikus IV... IV SÜSIN...
ANILIIN Merilin Talimaa Aravete Keskkool Sissejuhatuseks Esmakordselt aminobenseen ehk aniliin oli saadud 1826. aastal indigost Otto Unverdorbeni poolt, kes andis talle nimetuse kristaliin Tööstuses hakati kasutama esmakordselt aniliini 1865. aastal Läks violetse värviaine koostisesse Mis on aminobenseen? Aniliin ehk aminobenseen (C6H5NH2) on tähtis keemiatööstuse tooraine Aniliini nimetus tuleneb kreeka keelest sõnast anil, millega tähistati tumesinist taimset värvi, mida teatakse indigona tänapäeval. Indigo kuivdestillatsioonil saadigi värvusetust õlist vedelikku aniliini Aniliini omakorda toodetakse klorobenseenist või nitrobenseenist On aromaatne amiin, mille molekul kujutab endast benseeni, kus üks vesiniku aatom on asendatud amiinorühmaga Ehitus Aniliin koosneb benseeni rõngast ja aminorühmast Joonistel on näha...
Alkoholid ja karboksüülhapped Alkoholid on sellised süsivesinikest tuletatud ühendid, milles üks või enam vesiniku aatomit on asendatud ühe või enam hüdroksüülrühmaga (-OH- rühmaga) Alkoholid ei muuda indikaatori värvi. R-alküülrühm (tuletatakse alkaani valemist lahustades ühe vesiniku aatomit) R-OH CH4 metaan ; CH3 metüül ; CH3OH metanool Metanool CH3Oh on suure süsinikuühendite rühm alkoholide kõige lihtsam esindaja. Metanooli võib saada metaani oksüdeerumisel: 2CH4 + O2 -> 2 CH3OH Metanool on värvitu, põletava maitsega mürgine vedelik, mis keeb temperatuuril 65C ja seguneb veega igasuguses vahekorras. Vähene kogus metanooli võib põhjustada raskeid tervisehädasid, sealhulgas pimedaks jäämist. Etanool CH3CH2OH on tähtsaim ja tuntuim alkohol. Etanooli saadakse glükoosi lagunemisel: C6H12O6 -> 2CH3CH2OH + 2CO2 Etanool on värvitu, põletava maitsega, lahustub hästi vees, keeb 78C juures, joomine te...
Tarbeplastid Tarbeplastid on massiliselt toodetavad, odavad ning ei oma erilisi mehaanilisi ja termilisi omadusi. PS - polüstüreen Puhas polüstüreen on jäik ja rabe, klaasjas ja läbipaistev polümeer. Ta on kergesti töödeldav ning tal on hea mõõtmete püsivus. Seevastu on tal väga madal kemikaalikindlus ja ta on tundlik UV-kiirgusele ning töötemperatuurivahemik vaid -10...70 °C. PS on veel omadustelt lahustuv süsivesinikes ja õlides, omab häid elektriisolatsiooniomadusi. Vahtpolüstüreen (EPS, PS-E) on levinud polüstüreen, mis saadakse, kui puhtale PS-ile lisatakse tootmisel vahustavaid lisandeid, näiteks CO2. Vahtpolüstüreen (EPS) saadakse stüreeni polümerisatsioonil koos madalal temperatuuril keeva süsivesinikuga massis või suspensioonis. EPS on väikese tihedusega ja heade soojusisolatsiooniomadustega, teda võib kombineerida survevalu ja ekstrusiooniga. Graanulite töötlemisel vormides auruga toimub eelpaisumine...
Võistluse ajal keelatud glükokortikoidid Aine struktuur https://upload.wikimedia.org/wikipedia/commons/thumb/0/0d/Co rtisol2.svg/250px-Cortisol2.svg.png Toime inimorganismile, kõrvalmõjud Farmakoloogilistes doosides manustatuna võivad sünteetilised glükokortikoidid põhjustada mitmeid kõrvaltoimeid, ebamugavustundest eluohtlike seisundite ja surmani. Kõrvalmõjud võivad olla järgmised: immuunpuudulikkus, hüperglükeemia, insuliini resistentsus, glükokortikoidide indutseeritud osteoporoos, kaalutõus, hypercortisolemia, mäluhäired ja tähelepanupuudulikkus, primaarne neerupealiste koorolluse puudulikkus, lihaste lõhustumine, lipomatoos, kesknärvisüsteemi ülierutuvus (eufooria, psühhoos), ovulatsioonipuudus, kasvupeetus, rohekae, kaed jpt. Glükokortikoididega seotud Glükokortikoidid takistavad haigused: ...
Puurmani Gümnaasium Lämmastik Uurimustöö keemias Koosjata: Marju Perova Juhendaja: Aleksandr Kirpu Puurmani/ Pikknurme 2009 Lämmastiku ladinakeelne nimetus on nitrogenium, mille võttis teaduses kasutusele Chaptal ning tähendab "salpeetri tekitaja" ja elemendi sümbol on N. Lämmastiku avastas Daniel Rutherford 1772 aastal Edinburgis. Põlemist mittesoodustava gaasina nimetati teda algul "mürgiseks õhuks". Aatomi ja molekuli ehitus: N: +7| 2) 5) Lämmastiku järje- ehk aatomnumber on 7, ta kuulub perioodilisustabeli VA rühma elementide hulka, asudes 2. perioodis. Lämmastiku aatomis on 7 prootonit, 7 elektroni ja 7 neutronit. Lämmastiku aatomi väliskihis on viis elektroni ning lämmastiku aatomid võivad elektrone nii liita kui ka loovutada. Seetõttu on lämmastiku oksüdatsiooniaste ühendites 3 kuni +5. Näiteks oksüdatsiooniaste -III : NH...
FOSFOR (nimi tuleneb kreekakeelsest sõnast phosphoros- "valguskandja") Fosfor on kergesti süttiv mittemetall, mis asub VA rühmas 2.perioodis ja järjenumber on 15. Fosfori ainus looduslik isotoop on massiarvuga 31. Fosfori stabiilseim oksüdatsiooniaste on +5. Teised olulisemad oksüdatsiooniastmed on +3 ja 3. Fosfori sulamistemperatuur on 44,1 °C, keemistemperatuur 277 °C ja agregaatolek toatemperatuuril on tahke. 1669. aastal kui Hennig Brand hakkas uurima uriin, avastas ta katse käigus fosfori. Brand kogus tünnitäie uriini, aurutas seda siirupi konsistensini ning sai pruunika vedeliku, mille nimetas uriiniõliks. Viimase segas ta liiva ja söega ning kuumutas siis tugevasti õhu juurdepääsuta. Äraarvamatu oli alkeemiku rõõm, kui ta avastas anumas omalaadse, nõrgalt küüslaugulõhnalise vahataolise aine, mis pimedas helendab. Tõenäoliselt sai aga fosforit juba 12.saj aarabia alkeemik Alhid Behil. Leidumine Fosforit ehedalt looduses...